Сборник ответов на ваши вопросы. Работа хром
Работа - Хром - Химия
/>/>/>/>
Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил:Гуляева Т.А.
КАРАГАНДА2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
/> /> Введение.К металлам побочных подгрупппериодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома,марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общиехарактеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы —хром Cr, молибден Мо и вольфрам W. Хром возглавляет побочную подгруппу 4группы. Его электронная формула +24Cr 1s2|2s22p6|3s23p63d5|4s1
На внешнем энергетическомуровне атомов хрома и молибдена содержится по одному электрону, вольфрама — дваэлектрона, что обусловливает металлический характер этих элементов и отлично отэлементов главной подгруппы. В соответствии с числом валентных электронов онипроявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общейформулы h3RO4.Сила кислот закономерноснижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо,хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хромапроявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединениявысшей степени окисления, которые во многом весьма похожи на соответствующиесоединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера вподгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390°С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитейв электрических лампочках накаливания.
Металлы подгруппы хрома вобычных условиях весьма устойчивы к воздействию воздуха и воды. При нагреваниивзаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием идр. Известны их многочисленные сплавы с другими металлами. Сплавы и самиметаллы — весьма ценные материалы современной техники.
По физическим и химическимсвойствам молибден и вольфрам сходны между собой и несколько отличаются отхрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметнопонижается.
/>/>Нахождение в природе.Хром встречается ввидесоединений в различных минералах. Наиболее распространен минерал хромит, илихромистый железняк FeCr204,богатые месторождениякоторого имеются на Урале и в Казахстане. Массовая доля хрома в земной коресоставляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г.Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень солянойкислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся беломосадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудникиописал академик П. С. Паллас. «Березовские копи, — писал он, — состоят изчетырех рудников, которые разрабатываются с 1752 года. В них наряду с золотомдобываются серебро и свинцовые руды, а также находят замечательный красныйсвинцовый минерал, который не был обнаружен больше ни в одном другом рудникеРоссии. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари),тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минералабывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошокона дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, былинайдены огромные залежи хромита — основного промышленного сырья дляпроизводства феррохрома. В годы войны на базе этого месторождения был построенАктюбинский ферросплавный завод, который впоследствии стал крупнейшимпредприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположенобольшое число месторождений этого металла: Сарановское, Верблюжьегорское,Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистыхруд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии,на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такиепромышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия,совершенно лишены хромового сырья, а США и Канада располагают лишь оченьбедными рудами, практически не пригодными для производства феррохрома. Всего жена долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским краснымсвинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этогоминерала был в конце XVIII века привезен Палласом в Париж. Крокоитомзаинтересовался известный французский химик Луи Никола Воклен. В 1796 году онподверг минерал химическому анализу. «Все образцы этого вещества, которыеимеются в нескольких минералогических кабинетах Европы, — писал Воклен в своемотчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника.Раньше рудник был очень богат этим минералом, однако говорят, что несколько летназад запасы минерала в руднике истощились и теперь этот минерал покупают навес золота, в особенности, если он желтый. Образцы минерала, не имеющиеправильных очертаний или расколотые на кусочки, годятся для использования их вживописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся навоздухе… Красивый красный цвет, прозрачность и кристаллическая формасибирского красного минерала заставила минералогов заинтересоваться егоприродой и местом, где он был найден; большой удельный вес и сопутствующая емусвинцовая руда, естественно, заставляли предполагать о наличии свинца в этомминерале...».
Один из друзей Воклена предложил емуназвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразногоцвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входитво многие термины, не связанные с элементом хромом: слово «хромосома»,например, в переводе с греческого означает «тело, которое окрашивается»; дляполучения цветного, изображения пользуются прибором хромоскопом; фотолюбителямхорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования ватмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилосьпредложенное название, поскольку открытый им металл имел скромную серую окраскуи как будто не оправдывал своего имени. Но друзья все же сумели уговоритьВоклена и, после того как французская Академия наук по всей формезарегистрировала его открытие, химики всего мира внесли слово «хром» в спискиизвестных науке элементов.
Свое название хром получил от греческогослова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Металлический хром получаютвосстановлением оксида хрома (III) принагревании с алюминием:
Сr2О3+ 2Аl = Аl2О3 +2Сr
Металлический хром получаюттакже электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ.Растертый в порошок крокоит он поместил в раствор углекислого калия ипрокипятил. В результате опыта ученый получил углекислый свинец и желтыйраствор, в котором содержалась калиевая соль неизвестной тогда кислоты. Придобавлении к раствору ртутной соли образовывался красный осадок, после реакциисо свинцовой солью появлялся желтый осадок, а введение хлористого оловаокрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинцаВоклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовыйангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокойтемпературы. Когда опыт был закончен, ученый обнаружил в тигле множество серыхсросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество.Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой рудыпоступает сегодня на ферросплавные заводы, где выплавляются различные сортаферрохрома и металлического хрома.
Впервые феррохром был получен в 1820 годувосстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854году удалось получить чистый металлический хром электролизом водных растворовхлорида хрома. К этому же времени относятся и первые попытки выплавитьуглеродистый феррохром в доменной печи. В 1865 году был выдан первый патент нахромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыгралэлектрический ток, точнее электротермический способ получения металлов исплавов. В 1893 году французский ученый Муассан выплавил в электропечиуглеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производстворазвивалось черепашьими темпами. Мизерные количества ферросилиция иферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегуреки Сатки (Южный Урал) был построен маленький электрометаллургический завод«Пороги», который стал производить феррохром, а затем и ферросилиций. Но обудовлетворении нужд своей промышленности не могло быть и речи: потребностьРоссии в ферросплавах приходилось почти полностью покрывать ввозом их из другихстран.
Хром — серовато-белыйблестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый,его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит изсмеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56.Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов —хорошо проводит тепло, почти не оказывает сопротивления электрическому току,имеет присущий большинству металлов блеск. Любопытна одна особенность хрома:при температуре около 37°С он ведет себя явно «вызывающе» — многие его физическиесвойства резко, скачкообразно меняются. В этой температурной точке внутреннеетрение хрома достигает максимума, а модуль упругости падает до минимальныхзначений. Так же внезапно изменяются электропроводность, коэффициент линейногорасширения, термоэлектродвижущая сила. Пока ученые не могут объяснить этуаномалию.
Даже незначительные примеси делают хром очень хрупким,поэтому в качестве конструкционного материала его практически не применяют,зато как легирующий элемент он издавна пользуется у металлургов почетом.Небольшие добавки его придают стали твердость и износостойкость. Такие свойстваприсущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%),входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаютсяисключительной твердостью — они-то и позволяют металлу уверенно сопротивлятьсяодному из опаснейших врагов — износу.
В качестве представителяметаллов, относящихся к побочным подгруппам периодической системы, рассмотримхром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранеерассмотренных металлов он, как и все металлы с достраивающимся предпоследнимэлектронным слоем атома, отличается тугоплавкостью и твердостью. По твердостихром превосходит все металлы, он царапает стекло.
/>/>Химические свойства./> /> Расположение электронов на 3d- и4s-орбиталях атома хрома можно представитьсхемой:Отсюда видно, что хром можетпроявлять в соединениях различные степени окисления — от +1 до +6; из нихнаиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Такимобразом, в образовании химических связей участвует не только электрон внешнегоуровня, но и пять электронов d-подуровнявторого снаружи уровня.
Как и у алюминия, наповерхности хрома образуется оксидная пленка Сr2О3.Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться несразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированнойсерной кислотах хром не растворяется, так как его оксидная пленка упрочняется,т. е. хром переходит в пассивное состояние. По этой же причине невзаимодействуют с хромом разбавленные серная и соляная кислоты, содержащиерастворенный кислород. Пассивацию хрома можно устранить очисткой поверхностиметалла.
При высокой температуре хромгорит в кислороде, образуя оксид Cr2О3. Раскаленный хромреагирует с парами воды:
2Cr + ЗН2О= Cr2О3 + ЗН2
Металлический хром принагревании реагирует также с галогенами, галогеноводородами, серой, азотом,фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3; 2Cr + N2 = 2CrN
2Cr +3S = Cr2S3; Cr + Si = CrSi
На воздухе хром совершенно неизменяется. Поэтому хромом с помощью электролиза его соединений покрывают —хромируют — стальные изделия для предохранения их от ржавления и механическогоизноса. Эти же качества хром придает своим сплавам с железом — хромистымсталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошлав виде вилок, ножей и других предметов домашнего обихода. Блестящие,серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская»Московского метрополитена.
При химических реакциях атомхрома может отдавать, кроме единственного электрона наружного слоя, до 5электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6).Но, как и все элементы с достраивающимся предпоследним слоем атома, хромпроявляет несколько значений степеней окисления, т. е. кроме высшего и низшиезначения, а именно + 2 и + 3. У металлов с переменной валентностью, как и уэлементов одного и того же периода, например III, с возрастанием степениокисления уменьшается радиус иона. Так, у хрома:
/>
Радиус иона
При этом соблюдается та жесамая закономерность в изменении химических свойств соединений металла свозрастанием его степени окисления, как у элементов одного и того же периода, аименно:
1. С возрастанием степениокисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значенияхстепени окисления и близких значениях ионного радиуса химические свойствагидроксидов элементов оказываются сходными.
Это мы и наблюдаем нагидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2и Mg2; Сг3 и А13; С г6и S6*:
/>
Гидроксиды хрома
Гидроксидыэлементов III периода
Хром образует три рядасоединений:
/>
Познакомимся с важнейшими изэтих соединений. При растворении хрома в кислотах получаются соли, в которыххром двухвалентен, например:
/>
Соединения двухвалентногохрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, вкоторых содержится хром в степени окисления +6: оксид
/>/>Применение.Хром широко используется, как добавочный материал кметаллам, для получения высококачественной стали, подшипников и др. данныйпроцесс называется хромированием.
Молодое Советское государство не могло зависеть откапиталистических стран в такой важнейшей отрасли промышленности, какпроизводство качественных сталей, являющейся основным потребителем ферросплавов.Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны,требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая,автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование истроительство ферросплавных заводов. В 1931 году вошел в строй Челябинскийзавод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Одиниз создателей советской качественной металлургии член-корреспондент Академиинаук СССР В. С. Емельянов в эти годы находился в Германии, куда он былнаправлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась нетолько в Германию, но и в Швецию, Италию, США. И у них же нам приходилосьпокупать феррохром.
Но когда вслед заЧелябинским в 1933 году были построены еще два ферросплавных завода—в Запорожьеи Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, втом числе и феррохром, но и получила возможность экспортировать их за границу.Качественная металлургия страны была практически полностью обеспеченанеобходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии иокислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углеродвреден: карбидообразующие «наклонности» хрома приводят к тому, что большиеколичества этого элемента связываются в карбиды, выделяющиеся на границах зеренстали, а сами зерна оказываются бедны хромом и не могут стойко оборонятьсяпротив натиска кислот и кислорода. Поэтому содержание углерода в нержавеющейстали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться«чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов.Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием,в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служатсплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта имолибдена придает металлу способность переносить большие нагрузки при t = 650—900°С. Из этих сплавов делают, например, лопатки газовых турбин.<sup/>Сплав кобальта,молибдена и хрома («комохром») безвреден для человеческого организма и поэтомуиспользуется в восстановительной хирургии.
Одна из американских фирм недавно создала новыематериалы, магнитные свойства которых изменяются под влиянием температуры. Этиматериалы, основу которых составляют соединения марганца, хрома исурьмы,по мнению ученых, найдут применение в различных автоматических устройствах,чувствительных к колебаниям температуры, и смогут заменить более дорогиетермоэлементы.
Хромиты широко используют и в огнеупорнойпромышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал дляфутеровки мартеновских печей и других металлургических агрегатов. Этот материалобладает высокой термостойкостью, ему не страшны многократные резкие изменениятемпературы.
Химики используют хромиты для получения бихроматовкалия и натрия, а также хромовых квасцов, которые применяются для дублениякожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», асапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимаетдеятельное участие в производстве красителей для стекольной, керамической,текстильной промышленности.
Окись хрома позволила тракторостроителям значительносократить сроки обкатки двигателей. Обычно эта операция, во время которой всетрущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго иэто, конечно, не очень устраивало работников тракторных заводов. Выход изположения был найден, когда удалось разработать новую топливную присадку, в составкоторой вошла окись хрома. Секрет действия присадки прост: при сгорании топливаобразуются мельчайшие абразивные частицы окиси хрома, которые, оседая навнутренних стенках цилиндров и других подвергающихся трению поверхностях,быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Этаприсадка в сочетании с новым сортом масла позволила в 30 раз сократитьпродолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную«специальность»: в США изготовлена экспериментальная магнитофонная пленка,рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицыокиси хрома. Замена оказалась удачной — качество звучания резко улучшилось,пленка стала надежнее в работе. Новинкой в первую очередь предполагаетсяобеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемойхромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причинанеудач заключалась в том, что используемый при этом электролит содержалтрехвалентный хром, который не мог создать нужное покрытие. А вот егошестивалентному «собрату» такая задача оказалась по плечу. С этого времени вкачестве электролита начали применять хромовую кислоту — в ней валентностьхрома равна 6. Толщина защитных покрытий (например, на некоторыхнаружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1миллиметра. Но иногда хромовое покрытие используют в декоративных целях — дляотделки часов, дверных ручек и других предметов, не подвергающихся серьезнойопасности. В таких случаях на изделие наносят тончайший слой хрома(0,0002—0,0005 миллиметра).
Существует и другой способ хромирования —диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначальностальную деталь помещали в порошок хрома и нагревали в восстановительнойатмосфере до высоких температур. При этом на поверхности детали появлялсяобогащенный хромом слой, по твердости и коррозионной стойкости значительнопревосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но»)при температуре примерно 1000°С хромовый порошок спекается и, кроме того, наповерхности покрываемого металла образуются карбиды, препятствующие диффузиихрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка дляэтой цели начали использовать летучие галоидные соли хрома — хлорид или иодид,что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно вустановке для хромирования, пропуская пары соответствующей галоидоводороднойкислоты через порошкообразный хром или феррохром. Образующийся газообразныйхлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом.Такое покрытие гораздо прочнее связано с основным материалом, чемгальваническое.
До последнего времени хромировали только металлическиедетали. А недавно советские ученые научились наносить хромовую «броню» наизделия из пластмасс. Подвергнутый испытаниям широко известныйполимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менеестрашными такие известные «враги» конструкционных материалов, как истирание,изгиб, удар. Само собой разумеется, возрос срок службы деталей.
/>/>Резюме.… Прежде чем закончить рассказ о хроме, мы вновь обратимсяк воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, —я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! —незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда быладля нас символом технического прогресса. И вот теперь Англия покупает нашферрохром! Англичане понимают толк в том, что покупают».
/>/>Список Литературы:1. «Химия за 11 класс».Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химияза 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия дляподготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Не работает Гугл - причины и полезные советы, фото и видео уроки по исправлению ошибки.
Краткое содержание статьи:
Монополия Mozilla Firefox на рынке браузеров серьёзно пошатнулась, после выхода программного обеспечения от Google. Но периодически пользователи сталкиваются с тем, что не работает Гугл и браузер Google Chrome. И без посторонней помощи справится с возникающими проблемами очень сложно.

Почему не работает Гугл Хром на компьютере?
Самый простой путь решения любой проблемы, связанной с современной техникой – перезапустить компьютер. Это помогает в 9 из 10 случаев, пара нажатий клавиш исправит проблему, над которой можно было бы биться часами. Ещё есть переустановка программы, но это уже самый кардинальный способ. Он редко когда подходит, ведь в браузере сохраняется наша история посещений, закладки, информация по скачанным файлам и сохранённые пароли.
Мало кто держит в уме все логины и пароли, а с годами их становится только больше.
Использовать один для каждой учётной записи – не слишком безопасно, записывать в отдельный блокнот все данные – тоже сомнительный вариант. Поэтому для восстановления работоспособности любимого браузера придётся попотеть.
Для начала обратитесь за помощью к службе поддержки, возможно на официальном сайте уже выложили свежее обновление, которое исправляет возникшую ошибку. Большая часть пользователей сталкивается с типичными, а не какими-то уникальными неполадками. Вбив в поисковую строку название ошибки, вы получите перечень ссылок:
- На одну из служб Google, где описана проблема и пути её устранения.
- На тематический форум, на котором один из пользователей поднимает интересующий вас вопрос.
- На блог или статейный сайт, где автор в доступной форме объясняет, с чем может быть связана проблема.

Не работает Google поиск.
Чаще всего проблема возникает с использованием поиска, и пусть это тавтология, но чаще всего проблема связана с вирусами. Гугл Хром многие любят за возможность «вычленить» любой процесс и отделить его от всех остальных. Чисто теоретически, это новшество должно было позволить защитить пользователей от хакерских атак, сделать невозможным самопроизвольный запуск вредоносного обеспечения.
Но как только начала развиваться защита, вслед за ней стали эволюционировать и вирусы.
Ваш брандмауэр или антивирус смог вовремя обнаружить вирус, поместил его в карантин или сразу удалил заражённые файлы? Считайте, что вам повезло. Но если базы слишком давно не обновлялись или вы используете взломанную версию, ваша зашита никак не отреагирует на атаку. Что делать в таком случае?
Скачайте бесплатную утилиту по поиску и устранению вирусных угроз. Например ЭТУ.
Почти у любой серьёзной компании есть такая, от вас потребуют только возможность отправки отчёта разработчикам. После сканирования, которое может продлиться и несколько часов, программа предоставит вам данные о всех найденных угрозах и уязвимостях, с возможностью бесплатно излечить ваш компьютер или ноутбук.
В дальнейшем лучше установите себе нормальный антивирус, пусть даже и платный. Не посещать сомнительные сайты – первый шаг к безопасности в сети, но ещё не полная гарантия вашей защищённости:
- Могут быть точечные атаки конкретно на ваш IP.
- Вирусы могут быть прикреплены к абсолютно безобидным файлам.
- Атака может идти с взломанного сайта, хозяин которого ничего не подозревает о текущем положении дел.
Не работает голосовой поиск Гугл.
За последние лет пять все успели обзавестись мобильными устройствами. С развитием технологий, появлением планшетов и смартфонов, ваш карманный девайс перестал быть просто средством связи. С его помощью можно получить доступ к сети и воспользоваться всеми её преимуществами. А тысячи полезных приложений помогут превратить устройство в слаженно работающий на ваше благо механизм.
Но иногда мы теряем возможность пользоваться всеми его возможностями. В пример можно поставить голосовой набор, ещё вчера с его помощью мы за пару секунд находили всё необходимое. А сегодня он перестал работать и приходится вручную вбивать целые предложения в строку поиска. Долго и неудобно, особенно в холодное время года или при неисправном дисплее. Проблема не самая страшная, но решить её лучше быстро и кардинально.

Восстанавливаем работоспособность поиска от Google.
Как исправить положение?
- Сбросить всё до заводских настроек.
- Обновить версию Android.
- Скачать новую клавиатуру.
- Установить правильные настройки.
Первый вариант можно отнести к действительно кардинальным способам, вы потеряете всю имеющуюся информацию. Но при этом гарантированно исправите текущую проблему. А если ваше устройство синхронизировано с одним из «облачных» сервисов, потери информации могут быть не такими уж и значительными. После подключения к сети, сможете восстановить основной массив данных и получить обратно все свои приложения. Зато голосовой поиск снова будет работать.
Но чаще люди не готовы рисковать всем имеющимся на телефоне или планшете. В таком случае стоит убедиться, что ваша версия программного обеспечения в принципе поддерживает голосовой набор. Только Android 2.2 и более свежие версии могут похвастаться такой функцией. Может быть, у вас был значок набора на клавиатуре даже при более старой версии. Но это было особенностью вашей версии клавиатуры, на устройстве такая функция не поддерживалась.
Посмотрите пошаговый видео урок, что делать если Гугл Хром не открывает страницы:
Обнаружив проблему, либо делайте upgrade для своей операционной системы, либо скачивайте новую клавиатуру. Если значок есть, но не активен – зайдите в настройки и поставьте галочку рядом с пунктом «голосовой ввод». В зависимости от модели устройства и версии системы, комбинация действий может немного отличаться.
Работа «Хрома» в тяжёлых условиях.
Уровень оптимизации Гугл Хрома оставляет желать лучшего, на старых и слабых машинах он может потреблять слишком много оперативной памяти. С этим могут быть связаны частые вылеты и аварийные закрытия страниц.
На помощь к нам придёт диспетчер задач, запустив который можно увидеть, какой именно процесс потребляет основные ресурсы машины. Для ускорения работы браузера лучше позакрывать все другие процессы.
Внимательно следите за количеством открытых вкладок, даже бездействуя, они будут потреблять оперативку. Чем дольше не закрываете страницу, тем больше затрат уходит на поддержание её работоспособности. Если у вас мощное устройство, но вы столкнулись с такой проблемой – проверьте систему на вирусы. Ещё одной причиной могут быть проблемы во время сборки компьютера, может часть «железа» была неправильно установлена или на него просто нет драйверов. Займитесь оптимизацией своего устройства.

Когда не работает Google Chrome, приходится временно пользоваться другими браузерами. Всегда стоит держать «про запас» Mozilla, Opera, или ЯндексБраузер, как три актуальные альтернативы. Остаётся надеяться, что корпорация Google не будет заставлять нас прибегать к этим заменам слишком часто.
Видео-урок: как исправить ошибку
Далее в коротком пошаговом видео уроке будет показано, как избавиться от ошибки, когда «Гугл не работает»:
1-vopros.ru
Дипломная работа - Хром - Химия

Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил: Гуляева Т.А.
КАРАГАНДА 2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
 |
К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W.Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24 Cr 1s2 |2s2 2p6 |3s2 3p6 3d5 |4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3 RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современнойтехники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается.
Хром встречается ввиде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr2 04, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе… Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2 О3 + 2Аl = Аl2 О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
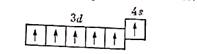 |
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2 О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2 О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2 О = Cr2 О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3 ; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2 S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
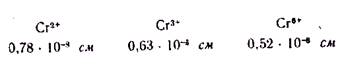
Радиусиона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2; Сг3 и А13; С г6 и S6 *:

Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:
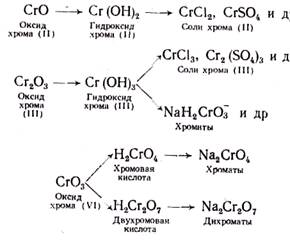
Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:
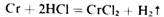
Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид
Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием .
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома исурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
… Прежде чем закончить рассказ о хроме, мы вновь обратимся к воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, — я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! — незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда была для нас символом технического прогресса. И вот теперь Англия покупает наш феррохром! Англичане понимают толк в том, что покупают».
1. «Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия для подготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Браузер Google Chrome - основные приемы работы с браузером
Chrome делает просмотр страниц простым и быстрым. На этом уроке мы поговорим о навигации между сайтами в Chrome. Вы также узнаете, как использовать вкладки, получить доступ к истории просмотров, а также как просмотреть загрузки.
Если у вас нет опыта работы с браузером, то мы рекомендуем к изучению Что такое браузер?.
Омнибокс
Некоторые браузеры используют адресную строку для перехода между сайтами и строку поиска для выполнения поиска в интернете. Google Chrome объединяет эти два элемента в один элемент, который называется Омнибокс. За счет интеграции технологии Google поиска, Омнибокс предлагает подсказки во время набора в нем адреса или запроса, которые делают навигацию в интернете быстрее и проще.
Чтобы использовать Omnibox:
- Введите адрес или поисковый запрос в Omnibox.

- Под Omnibox будут появляться подсказки. Подсказки, выделенные зеленым цветом – это сайты. Подсказки черного цвета – это поисковые запросы.

- Кликните по подсказке, чтобы перейти на сайт или выполнить запрос. Вы также можете полностью набрать адрес и нажать Enter, чтобы перейти на сайт, как и в обычной адресной строке.
Иконки в подсказках в Omnibox
Слева от каждой подсказки в Omnibox располагается серая иконка, определяющая тип подсказки.
 Страница, которую вы посещали ранее, или сайт, связанный с тем, что вы набираете.
Страница, которую вы посещали ранее, или сайт, связанный с тем, что вы набираете. Подсказка – поисковый запрос.
Подсказка – поисковый запрос. Этот сайт находится у вас в закладках.
Этот сайт находится у вас в закладках.
Навигация в Chrome
В Chrome для навигации используется три кнопки, находящиеся сверху на панели навигации: кнопки Назад, Вперед и Обновить.
- Кнопки Назад и Вперед позволяют перемещаться между недавно просмотренными страницами. Если кликнуть по одной из этих кнопок и удерживать ее нажатой, можно просмотреть недавнюю историю.

- Кнопка Обновить перезагружает текущую страницу. Если сайт перестает работать, попробуйте воспользоваться этой кнопкой. Если сайт нормально не загружается, то на месте кнопки Обновить временно появляется кнопка Стоп. Нажмите на нее, чтобы остановить загрузку страницы.

Окна и вкладки
Как и все браузеры, Chrome позволяет открывать новые окна для просмотра разных сайтов. Более того, с помощью вкладок Chrome позволяет открывать несколько сайтов в одном окне. Использовать вкладки обычно более удобно, чем открывать несколько окон одновременно.
Чтобы открыть новое окно:
- Кликните по меню Chrome в правом верхнем углу браузера и выберите Новое окно, либо нажмите сочетание клавиш Ctrl+N.

- Появится новое окно.

Чтобы открыть новую вкладку:
- Кликните по кнопке Новая вкладка справа от открытых вкладок, либо нажмите сочетание Ctrl+T.

- Появится новая вкладка. Введите адрес и нажмите Enter, чтобы перейти на новую страницу.

- Страница откроется на новой вкладке.

Чтобы переключиться между вкладками:
- Кликните по любой, не выбранной в данный момент вкладке.
- Эта вкладка станет выбранной.
Вы также можете использовать сочетание Ctrl+Tab для переключения между вкладками.
Чтобы закрыть вкладку:
- Чтобы закрыть вкладку, наведите курсор мыши на вкладку и кликните по кнопке Закрыть вкладку, либо воспользуйтесь сочетанием Ctrl+W для закрытия текущей вкладки.
Чтобы открыть ссылку в новой вкладке:
Вкладки могут сделать просмотр сайтов проще. Ведь если вы находите ссылку на сайт, то можете открыть ее в новой вкладке, не покидая текущую страницу.
- Кликните правой кнопкой по открываемой ссылке и выберите Открыть ссылку в новой вкладке, либо наведите курсор мыши на эту ссылку и нажмите на колесико мыши.

- Страница откроется в новой вкладке.

- Перейдите на новую вкладку, чтобы просмотреть страницу.

Управление вкладками
Вкладки можно перемещать, вытаскивать на отдельное окно и помещать обратно и даже закреплять на одном месте.
Чтобы переместить вкладку:
- Кликните по вкладке и не отпуская копку мыши, перетащите ее в нужное место.
- Отпустите кнопку мыши.
Чтобы вытащить вкладку из окна:
Если вы хотите просматривать две вкладки одновременно, проще всего вытащить вкладку в отдельное окно.
- Кликните по вкладке и, не отпуская копку мыши, потащите ее вниз. Появится прозрачное окно предварительного просмотра.
- Отпустите кнопку мыши. Вкладка появится в новом окне.
- Чтобы поместить вкладку обратно в окно, кликните по вкладке и, удерживая кнопку мыши, перетащите вкладку в нужное окно. Отпустите кнопку мыши, когда вкладка появится в панели вкладок.
Чтобы закрепить вкладку:
Если у вас есть сайты, которые вы открываете постоянно, например, электронная почта, календарь, то вы можете закрепить вкладки с ними. Закрепленные вкладки будут автоматически открываться вместе с Chrome.
- Кликните правой кнопкой по нужной вкладке и выберите Закрепить вкладку.
- Закрепленная вкладка будет показываться в виде уменьшенной вкладки в верхнем левом углу браузера.
- Чтобы открепить вкладку, кликните по ней правой кнопкой мыши и выберите Открепить вкладку.
Страница Новая вкладка
Когда вы открываете новую вкладку, на ней отображается страница Новая вкладка. Эта страница содержит ярлыки на наиболее часто посещаемые сайты, установленные приложения и недавно закрытые вкладки. Разобравшись с интерфейсом этой страницы, вы станете работать в интернете намного быстрее.

Просмотр истории
Как и все браузеры Chrome сохраняет информацию и Куки-файлы со всех посещенных сайтов. Все это вы можете посмотреть на вкладке История. Chrome использует часть этой информации для уменьшения времени загрузки сайтов, которые вы посещаете регулярно. Chrome также позволяет проводить поиск в истории и удалять историю для сохранения конфиденциальности.
Чтобы просмотреть вашу историю:
- Кликните по меню Chrome в правом верхнем углу браузера и выберите История.

- Появится вкладка История с полной историей просмотра сайтов. В историю попадает каждый просмотренный за последние несколько недель сайт. Список отсортирован по дате посещения, причем недавно посещенные сайты будут наверху.

- Если вы не помните точный адрес или название сайта, то можете выполнить поиск по истории. Введите поисковый запрос в панели поиска и нажмите Искать в истории.

- Появится список результатов поиска. Если вы хотите открыть найденный сайт, просто кликните по ссылке.
Ознакомьтесь с нашим уроком Chrome: безопасность и конфиденциальность, чтобы узнать, как удалить историю браузера.
Загрузка файлов
Chrome может отображать много разных типов файлов, таких как PDF и MP3 файлы. Но иногда доступ к файлам нужен вне браузера. Чтобы его получить, нужно скачать файл на компьютер.
Например, вам нужно заполнить и распечатать форму, найденную в интернете. Вы можете скачать эту форму, открыть ее в подходящей программе (например, Microsoft Word), заполнить, а потом распечатать.
Чтобы скачать файл с помощью Сохранить ссылку как:
Если вы кликните по ссылке ведущую на файл, то скачивание может начаться автоматически. Однако, в зависимости от типа файла, файл может открыться в браузере. Чтобы файл не открылся в Chrome, вы можете использовать функцию Сохранить ссылку как, тогда файл загрузится на компьютер.
- Кликните правой кнопкой по ссылке на файл и выберите Сохранить ссылку как.
- Появится диалоговое окно. Выберите папку сохранения файла, введите имя файла и нажмите Сохранить.
- Файл начнет скачиваться и ход загрузки будет показываться в левом нижнем углу браузера. После завершения загрузки просто кликните по файлу, чтобы открыть его.
По разным причинам некоторые сайты не позволяют скачивать их контент. Например, YouTube не разрешает скачивать видео.
Чтобы просмотреть Загрузки:
Вкладка Загрузки позволяет просматривать загрузки и управлять ими.
- Кликните по меню Chrome в правом верхнем углу браузера и выберите Загрузки.
- Появится вкладка Загрузки. Здесь вы сможете открыть ранее загруженные файлы, найти нужную загрузку или очистить список загрузок.
composs.ru
Работаем в браузере Google Chrome - Ячайник
На страницах нашего сайта мы не раз рассказывали о популярнейших веб-браузерах: Internet Explorer, Mozilla Firefox, Opera. Сегодня настала очередь Google Chrome – быстрого и удобного браузера от всемирно известной компании Google.
{mosloadposition debug}
Когда-то сайты представляли собой статические страницы, но которых мы с вами могли лишь получить интересующую нас информацию. С годами интернет развивался, появлялись новые технологии разработки веб-страниц и языки программирования, позволившие создавать динамические сайты, содержимое которых изменялось бы в зависимости от действий посетителей. Это привело к тому, что мы сейчас наблюдаем в глобальной сети: вездесущее проникновение социальных сетей, online игр и сервисов. С точки зрения Google сайты стали представлять собой не просто набор страниц, а набор самодостаточных приложений. Поэтому всемирно известная корпорация задумала создать новый браузер с удобным интерфейсом и отсутствием ненужных элементов, позволяющий пользователям быстро и безопасно работать с любимыми сайтами, и не требующий от нас с вами больших усилий по установке и настройке. Так в декабре 2008 года увидела свет первая стабильная версия бесплатного браузера Google Chrome.
Google Chrome разработан на основе программного обеспечения с открытым исходным кодом. Свежую версию браузера всегда можно загрузить с официального сайта разработчика: http://www.google.com/chrome/?hl=ru&brand=CHMB. Прочитав условия соглашения, щелкните кнопочку «Принять условия и установить». Если вы хотите, чтобы Chrome автоматически отправлял в Google информацию об ошибках браузера, отметьте галочкой соответствующую опцию.
Сохраните скаченный файл на компьютере и запустите его. Несколько секунд вам придется просто наблюдать за установкой Google Chrome.

По окончании установки нажмите кнопочку «Запустить Google Chrome». Если вы хотите, чтобы Windows использовала Google Chrome как браузер по умолчанию, отметьте галочкой соответствующий пункт.

Интерфейс Google Chrome минималистичен, но очень удобен и понятен даже начинающим пользователям. Как и планировали разработчики, на глаза не попадается ничего лишнего, что помешало бы вам серфить в глобальной паутине. Сразу после запуска Google Chrome вы увидите список наиболее посещаемых вами сайтов, недавно добавленные закладки и закрытые вкладки, а также поле для поиска сайтов в истории посещений. Нажмите ссылку «Показать всю историю» для просмотра полного списка ранее посещенных вами веб-страниц. Все сайты будут сгруппированы по дням. Для удаления списка посещенных в определенный день сайтов щелкните «Удалить историю за этот день». Открыть историю также можно через меню «Настройка и управление Google Chrome» - «История». Если требуется отыскать в истории какой-либо сайт, введите его название или часть адреса в поле поиска и нажмите кнопочку «История поиска».

Новая вкладка в Google Chrome открывается щелчком по кнопке со значком «+», а в адресной строке браузера можно вводить не только названия сайтов, но и поисковые запросы. По умолчанию поиск будет осуществляться в системе Google. При этом Google Chrome автоматически предложит вам и варианты поисковых запросов, и адреса подходящих сайтов.
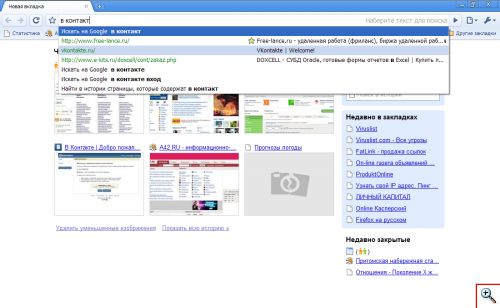
Для добавления любимого сайта в закладки щелкните значок звездочки рядом с адресом сайта и выберите, куда сохранить закладку.

Введите имя закладки, выберите подходящую для неё папку и нажмите «ОК».
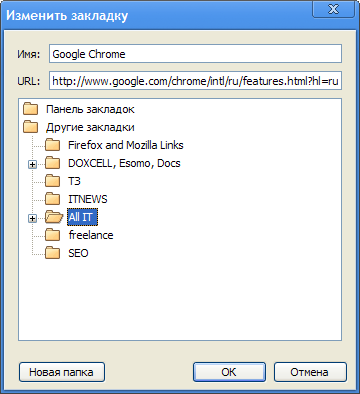
Просмотреть свои закладки вы можете, нажав кнопочку «Другие закладки» в правой части окошка Google Chrome.

Google Chrome также умеет экспортировать и импортировать закладки. Данные опции доступны в меню «Настройка и управление Google Chrome» - «Диспетчер закладок».

Контекстное меню закладки позволяет производить с ней различные действия, в частности переименовать или удалить.

Вы можете импортировать в Google Chrome закладки из html-файла (например, закладки Mozilla Firefox) или, наоборот, сохранить где-нибудь на компьютере все закладки из Google Chrome в виде html-файла (экспортировать закладки). Для этого служат соответствующие пункты меню «Инструменты». Вам придется выбрать нужную операцию и место сохранения файла на компьютере (при экспорте) либо уже готовый html-файл с закладками (при импорте).

Помимо импорта закладок в Google Chrome можно импортировать настройки из браузеров Mozilla Firefox и Internet Explorer. Для этого в меню «Настройка и управление Google Chrome» щелкните по пункту «Импорт закладок и настроек», затем выберите браузер, отметьте галочками элементы для импорта и нажмите кнопочку «Импорт». Имейте в виду, что первоначальный импорт всех настроек и закладок Google Chrome производит автоматически еще на этапе установки.

Загрузка файлов в Google Chrome не требует особых усилий. Все загружаемые из интернета объекты будут отображаться на отдельной панели в нижней части окошка браузера.

Для просмотра списка загруженных файлов и управления загрузками нажмите ссылку «Показать все загрузки…» либо выберите в меню «Настройка и управление Google Chrome» пункт «Загрузки». Вы увидите список загрузок, в том числе активные загрузки с указанием скорости закачки (кБ/сек). Их можно приостановить («Пауза») либо отменить («Отмена»). Чтобы найти какой-либо файл в загрузках достаточно ввести его имя в поле поиска и нажать кнопочку «Поиск в загрузках».
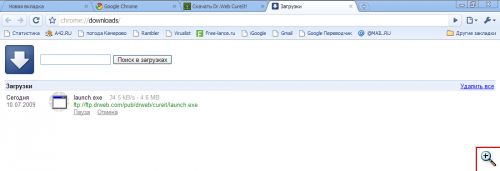
Все основные действия с загруженной в браузер веб-страницей выполняются при помощи контекстного меню и пунктов меню «Управление текущей страницей».

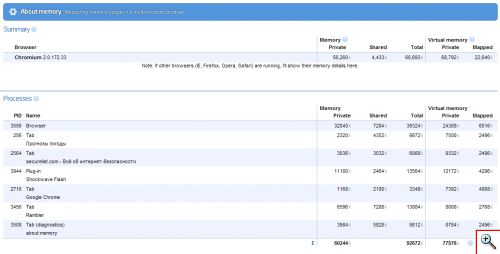
Для изменения масштаба страницы воспользуйтесь пунктом «Размер текста», а для просмотра исходного кода веб-страницы выберите «Разработчикам» - «Просмотреть исходный код». Кстати, программисты при помощи раздела «Разработчикам» Google Chrome могут также работать с JavaScript на своих сайтах, используя инструменты «Отладка JavaScript» и «Консоль JavaScript». Создав Google Chrome, разработчики сделали огромный шаг в сторону безопасности пользователей, снабдив браузер не только инструментами предупреждения об опасных сайтах, но и заставив каждую вкладку, т.е. каждую открытую веб-страницу, или плагин действовать как независимый процесс. При этом зависание одного сайта на отдельной вкладке никак не влияет на работу браузера в целом и на работу других сайтов, открытых на оставшихся в живых вкладках. Зависший сайт можно закрыть, выбрав «Управление текущей страницей» - «Разработчикам» - «Диспетчер задач». Здесь вы увидите все открытые вкладки, запущенные плагины и соответствующие им процессы, а также информацию о потребляемых каждым процессом ресурсах компьютера (загрузка процессора, сети и оперативной памяти). Выделите зависший сайт и нажмите кнопочку «Завершить процесс».

На месте зависшего сайта вы увидите вот такое веселое сообщение.
Вам останется лишь закрыть данную вкладку либо нажать на клавиатуре клавишу «F5», чтобы обновить веб-страницу. Диспетчер задач Google Chrome помогает не только пользователям, но и системным администраторам, предоставляя детальную информацию об используемой программой, закладками и плагинами оперативной памяти компьютера. Просмотреть её можно, нажав ссылку «Статистика для сисадминов» в окошке Диспетчера задач браузера.
Рассмотрим еще одно из полезных нововведений Google Chrome – возможность создания ярлыков веб-приложений. Например, вы часто пользуетесь online переводчиком ПРОМТ или играете в игры на Rambler, а запускать браузер каждый раз, чтобы перевести текст или поиграть, не очень то и хочется. Да и вообще идеально было бы видеть переводчик в виде отдельного окна, похожего на обычную программу. В Google Chrome не ничего проще! Откройте нужную веб-страницу и в меню «Управление текущей страницей» выберите «Создать ярлыки приложения…». Определитесь, куда поместить ярлык: на Рабочий стол или в меню Пуск Windows. Для некоторых сайтов можно поместить ярлык и на Панель быстрого запуска браузера Google Chrome. Нажмите кнопочку «ОК».

Щелкнув по свежесозданному ярлыку, вы запустите веб-приложение или откроете сайт в окошке, по внешнему виду абсолютно не напоминающему окно обычного браузера. При этом совсем необязательно запускать сам Google Chrome. При помощи контекстного меню вы можете совершать в окне с приложением различные действия: перемещаться по сайту (пункты «Вперед», «Назад»), обновить страницу (пункт «Перезагрузить»), сохранить и распечатать её, просмотреть исходный код и подробные сведения о странице.

Веб разработчикам понравится функция Google Chrome, касающаяся просмотра кода выделенного на веб-странице объекта. Для этого достаточно выделить какой-либо элемент, например, ссылку, нажать правую кнопку мышки и выбрать «Просмотр кода элемента». Вы попадете в окошко Инспектора Google Chrome, который подсветит код выделенного элемента особым цветом. В правой части окна будет показан список стилей и свойств элемента и сайта в целом.

Если вы не хотите, чтобы просмотренные вами сайты остались в истории посещений Google Chrome, воспользуйтесь режимом инкогнито, который доступен в меню «Настройка и управление Google Chrome» - «Новое окно в режиме инкогнито».

Для удаления истории посещений, кэша и других элементов в меню «Настройка и управление Google Chrome» выберите «Удаление данных о просмотренных страницах». Выбрав подлежащие удалению объекты и временной период, нажмите кнопочку «Очистить данные просмотров».
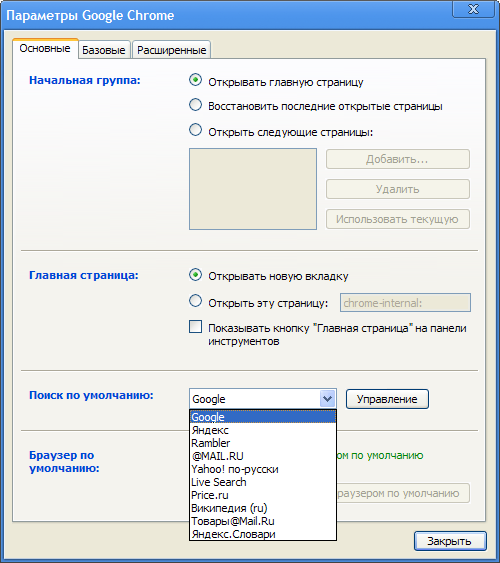
Основные настройки браузера Google Chrome содержатся в меню «Настройка и управление Google Chrome» - «Параметры». На вкладке «Основные» вы можете задать стартовую страницу браузера (раздел «Начальная группа»), главную страницу и выбрать поисковую систему по умолчанию.
На вкладке «Базовые» укажите папку для сохранения загружаемых файлов и разрешите браузеру запоминать введенные пароли (раздел «Пароли»). Впоследствии все сохраненные логины и пароли можно просмотреть, нажав кнопочку «Показать сохраненные пароли».
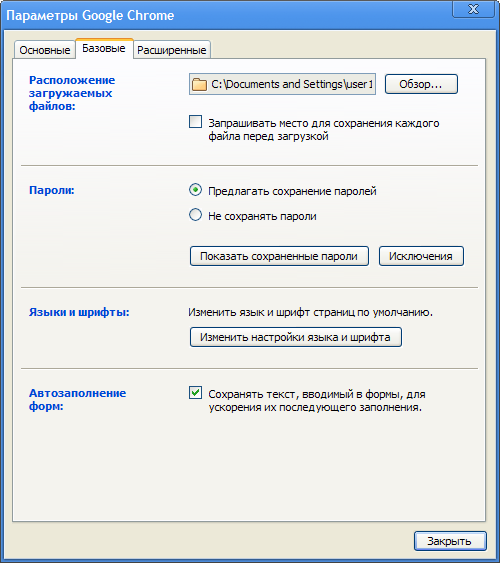
По умолчанию Google Chrome показывает только имя сайта и логин для входа. Чтобы увидеть пароль выделите сайт в списке и нажмите кнопочку «Показать пароль». Для скрытия пароля нажмите «Скрыть пароль».
В настройках Google Chrome вы не найдете опций для отключения скриптов, анимации или картинок на сайтах. Браузер предоставляет минимум настраиваемых параметров, достаточный для комфортной работы в интернете. На этом позвольте завершить наш рассказ и пожелать приятного веб серфинга. Надеемся, Google Chrome станет верным и преданным другом в вашем путешествии по глобальной сети.
Специально для Ячайник, Елена Карлтон
{mosloadposition cpanel}
{mosloadposition debug}
yachaynik.ru