Начало работы с Google Chrome. Хром работа
Как работать в браузере Google Chrome
 В самом начале развития интернета, сайты были статическими, и на них можно было только просматривать необходимую информацию. Но в процессе развития стали появляться новые технологии создания страниц и языки программирования, с помощью чего интернет-ресурсы стали динамическими, в которых информация изменяется в зависимости от поведения посетителя.
В самом начале развития интернета, сайты были статическими, и на них можно было только просматривать необходимую информацию. Но в процессе развития стали появляться новые технологии создания страниц и языки программирования, с помощью чего интернет-ресурсы стали динамическими, в которых информация изменяется в зависимости от поведения посетителя.
Благодаря этому получилось то, что сейчас можно увидеть во Всемирной паутине. Появились соцсети, онлайн-игр и сервисы. Google представляет это все не как простой набор страниц, а пакет самостоятельных приложений. Это способствовало тому, что компания решилась на создание собственного веб-обозревателя, обладающего удобным меню и без лишних элементов.
Такое сочетание позволяет юзерам безопасно и быстро работать с необходимыми интернет-ресурсами, при этом не требующее прилагать какие-то усилия по инсталляции и настройке. Итак, зимой 2008 года в свет вышла первая редакция веб-обозревателя.
Данный браузер основывается на ПО с открытым кодом. Актуальную редакцию можно скачать с ресурса разработчика. Ознакомившись с условиями соглашения, необходимо кликнуть на «Принять условия и инсталлировать». Если есть необходимость в том, чтобы браузер пересылал в автоматическом режиме данные об ошибках в Google, нужно поставить соответствующие отметки.
После этого необходимо сохранить загруженный файл на ПК и открыть его. Затем нужно немного подождать, пока произойдет инсталляция веб-обозревателя. После завершения инсталляции нужно нажать на «Запустить браузер». если нужно, чтобы этот интернет-проводник использовался по умолчанию, необходимо выделить соответствующий пункт.
Меню обозревателя можно назвать минималистичным, но при этом он довольно комфортный и понятный даже неопытным юзерам. Создателям удалось, и юзерам ничего не мешает выполнять серфинг по просторам интернета.
Запустив обозреватель, отобразится перечень наиболее популярных ресурсов, недавно добавленных закладок и закрытых вкладок. Кроме того, отображается строка для поиска интернет-ресурсов в истории посещений. Если кликнуть на «Показать всю историю», можно увидеть полный перечень просмотренных страниц.
Все интернет-ресурсы сгруппированы по числам. Для очистки перечня посещенных ресурсов за какой-то день «Удалить историю за этот день». Перейти в историю можно с помощью «Настройка и управление браузером», где необходимо выбрать «История». Если нужно найти в истории какой-нибудь сайт,надо ввести его название в строке поиска и кликнуть клавишу «История поиска».
Чтобы открыть новую вкладку, необходимо кликнуть на значок «+». Адресная строка может выполнять функции поисковой. В данном случае в качестве поисковика будет использоваться Google. Кроме того, веб-обозреватель в автоматическом режиме будет предлагать возможные варианты запросов и адреса интернет-ресурсов.
Чтобы добавить ресурс в закладки, необходимо кликнуть на звездочку возле адреса и указать, куда ее сохранить. Затем необходимо прописать название закладки, указать нужную директорию и нажать OK. Ознакомиться со своими закладками можно через клик на клавишу «Другие закладки» справа в окне Google Chrome. Кроме того, этот веб-обозреватель позволяет обмениваться закладками. Эту функцию можно отыскать в меню «Настройка и управление браузером», а потом нужно выбрать «Диспетчер закладок».
В контекстном меню закладки можно найти различные действия, которые с ней можно выполнять. Можно переименовать закладку или удалить. Кроме того, можно переносить в веб-обозреватель закладки из html-файла. Также можно сохранять на ПК закладки из Google Chrome в html-файл. Для этого необходимо использовать соответствующие пункты в «Инструментах». Нужно указать действие и место хранения файла на компьютере или имеющийся html-файл с закладками.
Кроме переноса закладок, этот веб-обозреватель позволяет переносить настройки издругих интернет-проводников. В данном случае необходимо перейти в «Настройки и управление Google Chrome» и выбрать пункт «Импорт закладок и настроек». После этого требуется указать веб-обозреватель и выделить элементы, которые будут переноситься. После этого нужно нажать «Импорт». Стоит помнить, что Chrome импортирует все настройки и закладки в автоматическом режиме при инсталляции.
Скачивание файлов в этом веб-обозревателе не составляет труда. Все скачанные из сети элементы будут располагаться в отдельной панели внизу окна браузера. Чтобы просматривать перечень скачанных файлов и управлять закачкой, необходимо кликнуть на «Показать все загрузки». Также можно перейти в меню «Настройка и управление браузером» и выбрать «Загрузки».
После этого откроется перечень закачек. Здесь же будут отображаться действующие загрузки с указанием скорости. Их можно поставить на паузу или отменить. Для поиска необходимой загрузки, требуется написать ее имя в строке поиска и кликнуть на клавишу «Поиск в загрузках».
Все важные манипуляции со скачанной в веб-проводник страницей проводятся через контекстное меню или меню «Управление текущей страницей». Чтобы изменить масштаб страницы, необходимо использовать пункт «Размер текста». Чтобы ознакомиться с кодом страницы требуется указать «Разработчиками» и кликнуть «Посмотреть исходный код».
Стоит отметить, что программисты могут использовать раздел «Разработчикам браузера» для работы на своих веб-сайтах с JavaScript. Для этого в этом разделе имеются средства «Отладка JavaScript» и «Консоль JavaScript».
Создатели веб-обозревателя Chrome особое внимание уделили безопасности юзеров в сети. Для этого интернет-проводник получил средств, предназначенные для предупреждения о заходе на небезопасные сайты. Кроме того, каждая запущенная вкладка работает, как независимый процесс. Этим удалось добиться того, что зависание одного ресурса в отдельной вкладке никоим образом не влияет на работу веб-обозревателя и остальных ресурсов, открытых в других вкладках.
Подвисший ресурс можно закрыть с помощью «Управление текущей страницей», где необходимо выбрать «Разработчикам», а потом нажать на «Диспетчер задач». Здесь отображаются все запущенные вкладки, активные плагины и их процессы. Также здесь можно ознакомиться с данными о потребляемых системных ресурсах всеми процессами. Необходимо отметить зависший ресурс и кликнуть «Завершить процесс». После этого нужно просто закрыть вкладку или нажать F5 для обновления страницы.
Диспетчер задач обозревателя может пригодиться не только юзерами, но и сисадминам, предоставляя полные данные о применяемой утилите, закладками и плагинами оперативки ПК. Чтобы их посмотреть, необходимо кликнуть на «Статистика для сисадминов» вразделе «Диспетчер задач обозревателя».
Кроме того, веб-обозреватель Chrome обладает еще один новшеством, которое позволяет создавать ярлыки веб-приложений. К примеру, если довольно часто используется какое-то приложение, а каждый раз его запускать не хочется, тогда эта функция может пригодиться. К тому же пользоваться такими сервисами удобней в виде отдельной программы.
Для этого требуется запустить необходимый сайт и указать «Управление текущей страницей». Здесь необходимо указать пункт «Создать ярлыки приложения…». После этого нужно только выбрать место его расположения. Некоторые интернет-ресурсы можно размещать в Панели быстрого запуска обозревателя. После этого нужно только нажать OK.
Кликнув по такому ярлыку, запустится веб-программа или ресурс в отдельном окне. При этом ничего не будет напоминать окно стандартного веб-обозревателя, причем запускать браузер не нужно.
Используя контекстное меню, можно выполнять в окне приложения всевозможные манипуляции. Можно передвигаться по ресурсу, обновлять страницу, сохранять ее и распечатывать. Также есть возможность посмотреть исходный код и информацию о странице.
Создателям веб-приложений может пригодиться функция, которая относится к просмотру кода, отмеченного на странице объекта. В данном случае требуется отметить какой-то элемент, щелкнуть ПКМ и указать «Просмотр кода элемента». Вследствие этого откроется Инспектор браузера, который отметить код выбранного элемента каким-то цветом. Справа будет отображаться перечень стилей и свойств элемента и ресурса.
Если нет желания оставлять просмотренные ресурсы в истории посещений, тогда можно применять анонимный режим, в который можно попасть через «Настройка и управление браузером», где необходимо выбрать «Новое окно в режиме инкогнито».
Чтобы удалить историю посещений, кэш и какие-то элементы, надо перейти в «Настройка и управление браузером» и указать «Удаление информации о посещенных страницах». Указав необходимые элементы и период времени, нужно кликнут «Очистить данные просмотров».
Все важные настройки находятся в меню «Настройка и управление браузером», где надо перейти в «Параметры». В разделе «Основные» можно указывать домашнюю страницу, стартовую страницу и задавать поисковик.
В разделе «Базовые» можно задавать директории для хранения скачанных данных и предоставить веб-обозревателю возможность запоминать прописанные данные. Вследствие этого все сохраненные логины и пароли можно просматривать, путем нажатия клавиши «Показать сохраненные пароли».
Веб-обозреватель отображает только название ресурса и логин для входа. Для просмотра пароля необходимо выделить ресурс в перечне и кликнуть на клавишу «Показать пароль». Чтобы скрыть пароль, нужно нажать «Скрыть пароль».
computerologia.ru
Помощь гугл хром

Как сделать Google Chrome по умолчанию
Если вы на своем компьютере используете браузер Оперу, Mozilla Firefox, Internet Explorer браузером по умолчанию, но вдруг захотели сделать браузер Google Chrome по умолчанию, то тогда вам сюда, из этого урока вы узнаете, как на своем компьютере сделать браузер Google Chrome по умолчанию.
Подробнее...
Как посмотреть историю Google Chrome
Если вы хотите посмотреть историю посещенных web-сайтов в браузере Google Chrome, но не знаете, как просмотреть историю в хроме, то тогда вам сюда, в этом уроке вы узнаете, как просмотреть историю браузера Google Chrome.
Подробнее...
Как изменить поиск в Google Chrome
В этом уроке я подробно и пошагово расскажу вам, как сделать браузер Google Chrome с поиском Яндекса. Урок нетрудный и рассчитан на каждого пользователя ПК.
Подробнее...
Как очистить кэш в Google Chrome
В этом уроке мы с вами рассмотрим очень удобный способ удаления истории посещения сайтов, очистки кэша, удаления cookie, очистки истории загрузок в браузере Google Chrome.
Подробнее...
Как узнать версию Google Chrome
Если вы хотите узнать версию браузера Google Chrome, но не знаете, как узнать версию своего браузера, то тогда вам сюда, из этой инструкции вы узнаете, как посмотреть версию Google Chrome.
Подробнее...
Как скачать музыку с одноклассников через гугл хром
Если вы на своем компьютере используете браузер Google chrome и хотите знать, как загрузить музыку с сайта одноклассники себе на компьютер, то вам тогда сюда, из этой простой и доступной инструкции вы узнаете, как скачать музыку с одноклассников через гугл хром.

Как изменить папку загрузок в хроме
Если вы на своем компьютере пользуетесь браузером google chrome и вам необходимо поменять папку загрузок, то вам тогда сюда, из этой подробной и пошаговой инструкции, вы узнаете, как изменить папку загрузок в хроме.
Подробнее...
Как полностью удалить гугл хром
Если вам нужно удалить браузер Google Chrome с компьютера, но вы не знаете, как полностью удалить браузер гугл хром то вам тогда сюда, из этой подробной инструкции вы узнаете, как полностью удалить браузер гугл хром с компьютера.
Подробнее...
Горячие клавиши Google Chrome
В этой статье мы с вами рассмотрим основные сочетание клавиш Google chrome, которые помогут вам быстро и легко работать с браузером Google chrome.

Как заблокировать сайт в Google
Если вы не знаете, как закрыть доступ к определённому сайту в браузере Google Chrome, то тогда вам сюда, в этом уроке я подробно и пошагово расскажу вам, как заблокировать сайт в Google.
Подробнее...www.computerhom.ru
Работа - Хром - Химия

Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил: Гуляева Т.А.
КАРАГАНДА 2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
 |
К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W.Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24 Cr 1s2 |2s2 2p6 |3s2 3p6 3d5 |4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3 RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современнойтехники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается.
Хром встречается ввиде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr2 04, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе… Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2 О3 + 2Аl = Аl2 О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
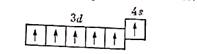 |
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2 О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2 О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2 О = Cr2 О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3 ; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2 S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
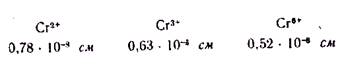
Радиусиона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2; Сг3 и А13; С г6 и S6 *:

Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:
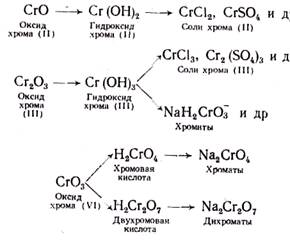
Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:
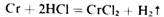
Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид
Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием .
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома исурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
… Прежде чем закончить рассказ о хроме, мы вновь обратимся к воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, — я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! — незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда была для нас символом технического прогресса. И вот теперь Англия покупает наш феррохром! Англичане понимают толк в том, что покупают».
1. «Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия для подготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Как работать с браузером Google Chrome?
Что научитесь делать, посмотрев это видео?
В этом уроке вы научитесь изменять поисковую систему браузера, настраивать стартовую страницу, изменять папку для загрузки фалов, работать с панелью закладок и историей просмотра.
Описание видео:
Из предыдущего урока вы уже знаете, как настроить браузер Google Chrome? В этом уроке вы научитесь работать с Google Chrome.
Браузер – это программа, которая позволяет просматривать Интернет-страницы. Одним из быстрых и простых браузеров является Google Chrome.
На примере автор показывает, что поисковый запрос вы можете вводить прямо в адресную строку. А результаты поиска будут выводиться той системой, которая выбрана по умолчанию. Чтобы изменить поисковую систему, зайдите в параметры. Кликните по гаечному ключу в правом верхнем углу экрана и перейдите в раздел Параметры. В открывшейся вкладке нужно в пункте Поиск выбрать желаемую поисковую систему из выпадающего списка (Google, Yandex, Mail, Rambler, Bing). Теперь при вводе запроса в адресную строку, поиск будет осуществляться в выбранной системе.
Если у вас изначально не настроена стартовая страница, то при запуске браузера будет открываться Панель быстрого доступа, где отображаются миниатюры тех сайтов, которые вы посещали в последнее время.
Для того чтобы настроить стартовую страницу, нужно опять зайти в Параметры и в разделе Главная страница прописать адрес той страницы, которая будет загружаться при старте браузера. Если вы поставите галочку Открывать страницу быстрого доступа, то при запуске браузера будет открываться страница с миниатюрами недавно посещенных сайтов. Тут же в параметрах в разделе Начальная группа можно настроить восстановление последних открытых страниц. Это очень удобно.
Если браузер Google Chrome не назначен браузером по умолчанию, то с помощью кнопки Назначить Google Chrоme браузером по умолчанию это можно быстро исправить.
Во вкладке Расширенные можно настроить папку загрузок, куда будут сохраняться все скачиваемые из Интернета файлы. В разделе Загрузки нажмите кнопку Изменить и укажите путь к папке для автоматического сохранения файлов. Теперь все, что будет скачано с помощью браузера Google Chrome, будет сохраняться в указанной папке.
Нажмите на гаечный ключ, наведите мышь на раздел Закладки и выберите пункт Показывать панель закладок. Под адресной строкой появится строка, где будут отображаться закладки. Чтобы поместить в эту строку закладку, откройте нужный сайт и перетащите его прямо с адресной строки в панель закладок. После этого для быстрого перехода на любимые сайты достаточно будет просто кликнуть мышкой по значку сайта в панели закладок. Если по значку сайта в панели закладок кликнуть правой кнопкой мыши и выбрать пункт Изменить, то откроется окно редактирования ссылки, где вы можете изменить имя закладки и отредактировать ссылку. Если Имя закладки полностью убрать, то в панели закладок будет отображаться только значок сайта, без подписи. Это удобно для компактного размещения закладок.
В панель закладок обычно удобно выводить ссылки на конкретные сайты, а понравившуюся страницу или статью можно поместить просто в закладки. Для этого нужно кликать по звездочке, которая расположена справа в адресной строке. По умолчанию обычно Google Chrome предлагает сохранить ссылку в Панель закладок, однако вы можете в выпадающем списке выбрать Другие закладки. После этого в правом углу появится папка Другие закладки, где будут размещаться ссылки на интересные статьи, блоги и страницы.
Очень полезно уметь пользоваться Историей. Кликните по гаечному ключу и выберите раздел История. Тут вы увидите все ссылки, по которым вы переходили за все время пользования браузером.
В следующем уроке вы узнаете, как установить Google Chrome? Как настроить браузер для комфортной работы?
 Loading ...
Loading ... www.kak-v.com
Начало работы с Google Chrome
 Google Chrome – это бесплатный веб-браузер от компании Google. Для установки нужно зайти на сайт Google. В открывшемся окне сначала устанавливаем язык (если сразу не открылась страница на русском языке), для этого нажимаем на треугольник «Select a language» и выбираем «Русский». После этого нажимаем кнопку «Загрузить Google Chrome».
Google Chrome – это бесплатный веб-браузер от компании Google. Для установки нужно зайти на сайт Google. В открывшемся окне сначала устанавливаем язык (если сразу не открылась страница на русском языке), для этого нажимаем на треугольник «Select a language» и выбираем «Русский». После этого нажимаем кнопку «Загрузить Google Chrome».
 Читаем условия предоставления услуг, при необходимости сделать браузер по умолчанию – проставляем галочку в чекбоксе, и нажимаем кнопку «Принять условия и установить».
Читаем условия предоставления услуг, при необходимости сделать браузер по умолчанию – проставляем галочку в чекбоксе, и нажимаем кнопку «Принять условия и установить».
Открывается окно установщика, в котором виден процесс установки. После установки запускается веб-браузер и открывается его окно.
После установки нужно произвести необходимые настройки. В правом верхнем углу нажимаем иконку с изображением гаечного ключа — открывается меню настроек.
Хром обновился и теперь вместо гаечного ключа -три палки.
Назначение элементов:
- Новая вкладка – при нажатии откроется новая вкладка;
- Новое окно — при нажатии откроется новое окно Хрома;
- Новое окно в режиме инкогнито – позволяет просматривать страницы интернета без оставления следов на компьютере. Т.е. не будет истории просмотра, «куки», но всё что скачано останется;
- Изменить – при выделении мышью текста в адресной строке на веб-странице его можно, скопировать, вырезать или вставить в нужное место;
- Масштаб – изменяет масштаб отображения веб-страницы;
- Сохранить страницу как… — сохраняет страницу;
- Найти… — поиск информации на открытой веб-странице.
- Печать – печать страницы;
- Инструменты – при нажатии откроется подменю
— Создать ярлыки приложения…
— Расширения
— Диспетчер задач
-удаление данных о просмотренных страницах
И т.д.
- Закладки – можно смотреть все закладки;
- История – история просмотра страниц;
- Загрузки – видно какие, загрузки были, а в случае продолжения загрузки – сам процесс;
- Параметры – откроется целое окно с дополнительными настройками;
- О Google Chrome – краткие сведения о программе;
- Просмотреть фоновые страницы – видно, что происходит в фоне;
- Справка – справка о Хроме;
- Выход – выход из программы.
delajblog.ru
Курсовая работа - Хром - Химия

Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил: Гуляева Т.А.
КАРАГАНДА 2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
 |
К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W.Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24 Cr 1s2 |2s2 2p6 |3s2 3p6 3d5 |4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3 RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современнойтехники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается.
Хром встречается ввиде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr2 04, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе… Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2 О3 + 2Аl = Аl2 О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
 |
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2 О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2 О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2 О = Cr2 О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3 ; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2 S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
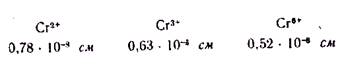
Радиусиона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2; Сг3 и А13; С г6 и S6 *:

Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:

Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:
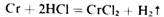
Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид
Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием .
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома исурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
… Прежде чем закончить рассказ о хроме, мы вновь обратимся к воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, — я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! — незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда была для нас символом технического прогресса. И вот теперь Англия покупает наш феррохром! Англичане понимают толк в том, что покупают».
1. «Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия для подготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Реферат : Хром (работа 1)


Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил: Гуляева Т.А.
КАРАГАНДА 2001г.
Оглавление:
Введение. 3
Нахождение в природе. 3
Происхождение. 4
Получение. 5
Физические свойства. 5
Химические свойства. 6
Применение. 8
Резюме. 10
Список Литературы: 11
В ведение.
ведение.
К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W. Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24Cr 1s2|2s22p6|3s23p63d5|4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современной техники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается.
Нахождение в природе.
Хром встречается в виде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr204, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
...Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная... Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры.
Происхождение.
Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе... Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Получение.
Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2О3 + 2Аl = Аl2О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран.
Физические свойства.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
Химические свойства.
Р асположение электронов на 3d- и 4s-орбиталях атома хрома можно представить схемой:
асположение электронов на 3d- и 4s-орбиталях атома хрома можно представить схемой:
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h4
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2О = Cr2О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3 ; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:

Радиус иона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2 ; Сг3 и А13; С г6 и S6*:

Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:

Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:

Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид
Применение.
Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием.
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома и сурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
Резюме.
...Прежде чем закончить рассказ о хроме, мы вновь обратимся к воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, — я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! — незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда была для нас символом технического прогресса. И вот теперь Англия покупает наш феррохром! Англичане понимают толк в том, что покупают».
Список Литературы:
«Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
«Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
«Химия для подготовительных отделений». Г.П. Хомченко.
Интернет.
topref.ru