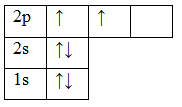
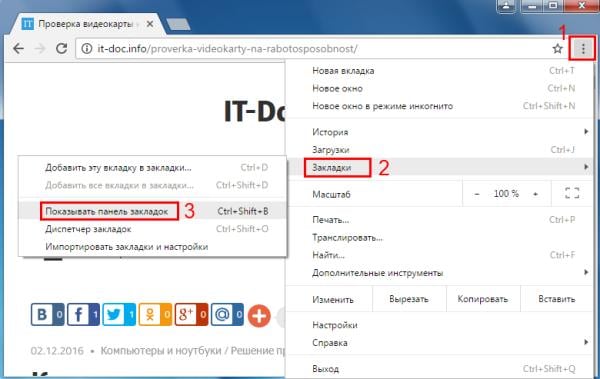
Графическое заполнение валентных энергетических слоев | Электронные конфигурации атомов. Энергетические уровни хрома
особенности строения и их роль во взаимодействиях между атомами
Что происходит с атомами элементов во время химических реакций? От чего зависят свойства элементов? На оба эти вопроса можно дать один ответ: причина лежит в строении внешнего энергетического уровня атома. В нашей статье мы рассмотрим электронное строение атомов металлов и неметаллов и выясним зависимость между структурой внешнего уровня и свойствами элементов.
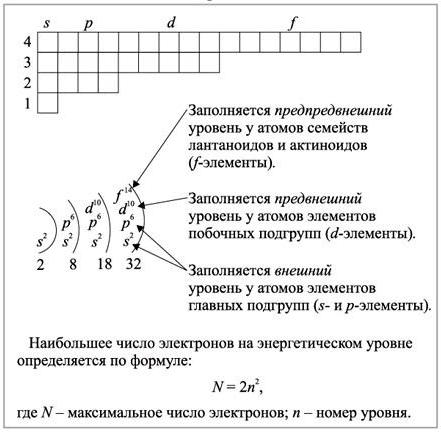
Особые свойства электронов
При прохождении химической реакции между молекулами двух или более реагентов происходят изменения в строении электронных оболочек атомов, тогда как их ядра остаются неизменными. Сначала ознакомимся с характеристиками электронов, находящихся на наиболее удаленных от ядра уровнях атома. Отрицательно заряженные частицы располагаются слоями на определенном расстоянии от ядра и друг от друга. Пространство вокруг ядра, где нахождение электронов наиболее возможно, называется электронной орбиталью. В ней сконденсировано около 90 % отрицательно заряженного электронного облака. Сам электрон в атоме проявляет свойство дуальности, он одновременно может вести себя и как частица, и как волна.
Правила заполнения электронной оболочки атома
Количество энергетических уровней, на которых находятся частицы, равно номеру периода, где располагается элемент. На что же указывает электронный состав? Оказалось, что количество электронов на внешнем энергетическом уровне для s- и p-элементов главных подгрупп малых и больших периодов соответствует номеру группы. Например, у атомов лития первой группы, имеющих два слоя, на внешней оболочке находится один электрон. Атомы серы содержат на последнем энергетическом уровне шесть электронов, так как элемент расположен в главной подгруппе шестой группы и т. д. Если же речь идет о d-элементах, то для них существует следующее правило: количество внешних отрицательных частиц равно 1 (у хрома и меди) или 2. Объясняется это тем, что по мере увеличения заряда ядра атомов вначале происходит заполнение внутреннего d- подуровня и внешние энергетические уровни остаются без изменений.
Почему изменяются свойства элементов малых периодов?
В периодической системе малыми считаются 1, 2, 3 и 7 периоды. Плавное изменение свойств элементов по мере возрастания ядерных зарядов, начиная от активных металлов и заканчивая инертными газами, объясняется постепенным увеличением количества электронов на внешнем уровне. Первыми элементами в таких периодах являются те, чьи атомы имеют всего один или два электрона, способные легко отрываться от ядра. В этом случае образуется положительно заряженный ион металла.
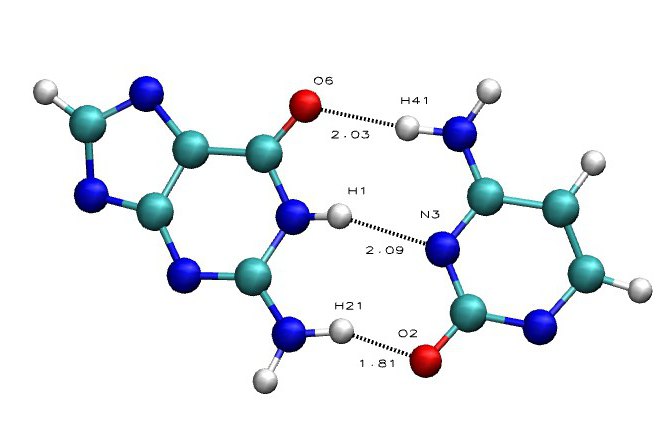
Амфотерные элементы, например, алюминий или цинк, свои внешние энергетические уровни заполняют небольшим количеством электронов (1- у цинка, 3 – у алюминия). В зависимости от условий протекания химической реакции они могут проявлять как свойства металлов, так и неметаллов. Неметаллические элементы малых периодов содержат от 4 до 7 отрицательных частиц на внешних оболочках своих атомов и завершают ее до октета, притягивая электроны других атомов. Например, неметалл с наибольшим показателем электроотрицательности – фтор, имеет на последнем слое 7 электронов и всегда забирает один электрон не только у металлов, но и у активных неметаллических элементов: кислорода, хлора, азота. Заканчиваются малые периоды, как и большие, инертными газами, чьи одноатомные молекулы имеют полностью завершенные до 8 электронов внешние энергетические уровни.
Особенности строения атомов больших периодов
Четные ряды 4, 5, и 6 периодов состоят из элементов, внешние оболочки которых вмещают всего один или два электрона. Как мы говорили ранее, у них происходит заполнение электронами d- или f- подуровней предпоследнего слоя. Обычно это - типичные металлы. Физические и химические свойства у них изменяются очень медленно. Нечетные ряды вмещают такие элементы, у которых заполняются электронами внешние энергетические уровни по следующей схеме: металлы - амфотерный элемент – неметаллы – инертный газ. Мы уже наблюдали ее проявление во всех малых периодах. Например, в нечетном ряду 4 периода медь является металлом, цинк – амфотерен, затем от галлия и до брома происходит усиление неметаллических свойств. Заканчивается период криптоном, атомы которого имеют полностью завершенную электронную оболочку.

Как объяснить деление элементов на группы?
Каждая группа – а их в короткой форме таблицы восемь, делится еще и на подгруппы, называемые главными и побочными. Такая классификация отражает различное положение электронов на внешнем энергетическом уровне атомов элементов. Оказалось, что у элементов главных подгрупп, например, лития, натрия, калия, рубидия и цезия последний электрон расположен на s-подуровне. Элементы 7 группы главной подгруппы (галогены) заполняют отрицательными частицами свой p-подуровень.
Для представителей побочных подгрупп, таких, как хром, молибден, вольфрам типичным будет наполнение электронами d-подуровня. А у элементов, входящих в семейства лантаноидов и актиноидов, накопление отрицательных зарядов происходит на f-подуровне предпоследнего энергетического уровня. Более того, номер группы, как правило, совпадает с количеством электронов, способных к образованию химических связей.
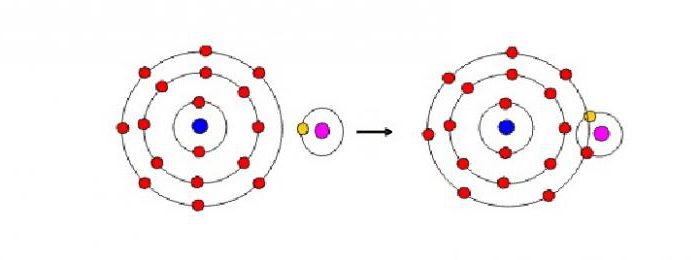
В нашей статье мы выяснили, какое строение имеют внешние энергетические уровни атомов химических элементов, и определили их роль в межатомных взаимодействиях.
fb.ru
Твердотельные квантовые генераторы
Твердотельные квантовые генераторы в зависимости от используемого активного вещества разделяются на кристаллические и стеклянные (аморфные).
Наиболее изучены следующие активные вещества: синтетический рубин, фтористый кальций, активированный трехвалентным ураном, и стекло с примесью неодимия. Лазеры, в которых в качестве активного вещества используются твердые тела, позволяют получить большие мощности излучения. Излучение таких лазеров лежит в широком диапазоне длин волн (6943—27 000 Å) и может быть как импульсным, так и непрерывным.
Кристаллические лазеры
К группе кристаллических лазеров относится хорошо изученный лазер на синтетическом рубине. В рубиновом лазере в качестве активного вещества использован монокристалл рубина, представляющий собой окись алюминия, в которой часть атомов алюминия замещена атомами хрома. Так называемый розовый рубин содержит 0,05—0,07% окиси хрома, а красный — 0,5—0,7%.
При освещении кристалла рубина светом ионы хрома возбуждаются и переходят на высший уровень, поглощая ультрафиолетовое излучение и широкую полосу зеленого и синего цвета. Высший уровень — это совокупность нескольких неустойчивых энергетических уровней (на рис. 1 показан только один). В основное состояние ионы хрома могут возвращаться либо непосредственно, либо через промежуточные, метастабильные уровни. При этом вероятность перехода возбужденных ионов хрома на промежуточные уровни больше, чем вероятность перехода на основной уровень.
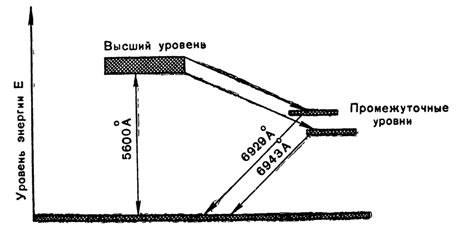 Рис.1 Диаграмма энергетических уровней ионов хрома в рубине
Рис.1 Диаграмма энергетических уровней ионов хрома в рубине
Ионы на промежуточные уровни переходят без излучения энергии, передавая часть своей энергии кристаллической решетке рубина. При отсутствии внешних причин, вызывающих вынужденное излучение, атомы хрома пребывают на промежуточных уровнях около 0,003—0,05 сек, что значительно больше времени нахождения ионов на верхнем энергетическом уровне. По- этому промежуточные уровни будут более заселенными, чем основной.
Если энергия возбуждения недостаточна, ионы хрома с промежуточных уровней спонтанно возвращаются на основной. Излучение в этом случае некогерентно и происходит на длинах волн 6943 и 6929 Å. При выполнении условий генерации лазер излучает поток фотонов длиной волны 6943 Å, причем интенсивность данного индуцированного излучения на несколько порядков выше спонтанного.
В лазере на рубине резонансной системой служит сам рубиновый стержень, торцы которого отполированы и представляют собой зеркала, причем один торец покрыт плотным непрозрачным слоем серебра, а другой полупрозрачный (также посеребренный) имеет коэффициент пропускания около 10%. Благодаря резонансной системе происходит усиление колебаний, распространяющихся параллельно продольной оси рубинового стержня. В результате многократного отражения от передней и задней зеркальных граней рубинового стержня фотоны через полупрозрачную грань выходят наружу в виде лавинного потока.
Колебания с длиной волны 6929 Å, а также все колебания, имеющие иное направление распространения, ввиду малого времени взаимодействия их с активным веществом подавляются, так как условия самовозбуждения на этих частотах не выполняются — усиление колебаний активной средой не компенсирует потери.
Стеклянные лазеры
В оптических квантовых генераторах наряду с кристаллическими широко используются стеклянные активные среды с примесью различных редкоземельных элементов. Преимущество таких лазеров в том, что стеклянные активные среды можно изготовить больших размеров и любой формы. Такие генераторы имеют более низкий порог самовозбуждения, чем генераторы на рубиновых лазерах. Стеклянные лазеры позволяют получить очень мощные выходные импульсы и обладают высокой оптической однородностью.
В настоящее время широко применяется лазер, в котором в качестве активного материала используется бариевый кронгласс (59% SiO2, 25% ВаО, 15% К2O, 1% Sb2O3) с примесью трехвалентного неодимия. Структура энергетических уровней трехвалентных ионов неодимия в стекле примерно та же, что и в кристаллах, однако отсутствие кристаллической структуры приводит к уширению линий поглощения и излучения.
Ширина спектра индуцированного излучения на волне 1,06 мкм (микрон) составляет около 100 Å. Стеклянные лазеры могут быть изготовлены в виде волокон малого диаметра (порядка длины волны). В такой системе будут отсутствовать высшие типы волн, и ее можно использовать как усилитель бегущей волны.
www.teh-lib.ru
Электронные конфигурации атомов | Задачи 183
Задача 183. Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации: а) 1р3 б) 3p6 в) 3s2; г) 2s2; д) 2d5; е) 5d2; ж) 3f12; з) 2р4 и) 3p7.Решение:а) Электронная конфигурация 1p3 не реализуется, потому что первый энергетический уровень (n = 1 ) содержит только s-подуровень. Максимальное число электронов на каждом энергетическом уровне равно 2n2, где n - главное квантовое число. Так на первом энергетическом уровне (n = 1) может находиться максимальное число электронов 2(2 .12 = 2). Следовательно, не только неправильно указан подуровень, но общее число электронов.
б) 3p6 – электронная конфигурация возможна, потому что на третьем энергетическом уровне содержатся s-, p- и d-подуровни. На p-подуровне содержится три атомные орбитали, а в каждой орбитали, согласно правилу Хунда, может находиться максимальное число электронов равное двум. Поэтому на 3p-подуровне может максимально находиться шесть электронов (3 . 2 = 6).
в) Электронная конфигурация 3s2 верна, потому что на третьем энергетическом уровне (n = 3) находятся s-, p- и d-подуровни. Согласно правилу Хунда, на s-подуровне, состоящем из одной атомной орбитали, может находиться максимальное число электронов равное двум.
г) Электронная конфигурация 2s2 реализуется, потому что на втором энергетическом уровне (n = 2) содержатся s- и p-подуровни, и на s-подуровне, в его единственной атомной орбитали, может содержаться максимальное число электронов равное двум.
д) Электронная конфигурация 2d5 не реализуется, потому что во втором энергетическом уровне (n = 2) d-подуровень не содержится, в этом слое расположены только s- и p-подуровни.
е) Электронная конфигурация 5d2 реализуется, потому что на пятом энергетическом уровне (n = 5) содержатся s-, p- d- и f-подуровни. Подуровень d содержит пять атомных орбиталей, в которых может находиться максимальное число электронов равное десяти (5 . 2 = 10). Запись 5d2 означает, что на 5d-подуровне содержится два неспаренных электрона.
ж) Электронная конфигурация 3f12 не реализуется, потому что на третьем энергетическом уровне (n = 3) могут находиться только s-, p- и d-подуровни.
з) Электронная конфигурация 2p4 реализуется, потому что на втором энергетическом уровне (n = 2) могут находиться только s- и p-подуровни. Подуровень p состоит из трёх атомных орбиталей, на которых, согласно правилу Хунда, может находиться до шести электронов.
и) Электронная конфигурация 3p7 не реализуется, потому что на p-подуровне, состоящем из трёх атомных орбиталей, согласно правилу Хунда, максимальное число электронов равно 6.
Задача 184. Сколько вакантных Зd-орбиталей имеют возбужденные атомы: а) С1; б) V; в) Мn?Решение:а) электронная конфигурация атома хлора имеет вид: …3s23p53d0. Графическое заполнение валентного энергетического слоя атома хлора можно представить следующей схемой:
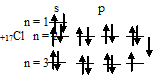
Таким образом, внешний энергетический уровень атома хлора имеет свободные орбитали на 3d-подуровне, что позволяет электронам переходить в возбуждённое состояние (перемещаться на более высокие свободные орбитали). У атома хлора возможно три состояния перемещения электронов на более высокие свободные орбитали, электроны с s- и p-подуровней переходят на 3d-подуровень:
1) При затрате некоторой энергии один из 3p-электронов атома хлора может быть переведён на вакантную 3d-орбиталь, при этом энергия атома возрастает, так что возникающая электронная конфигурация (1s22s22p63s23p43d1) соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
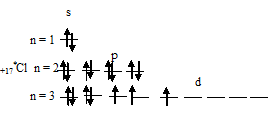
В данном случае 3d-подуровень содержит четыре вакантные орбитали возбуждённого атома хлора.
2) При затрате некоторой энергии два из 3p-электронов атома хлора могут быть переведены на вакантные 3d-орбитали, при этом энергия атома возрастает, так что возникает электронная конфигурация (1s22s22p63s23p33d2), которая соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
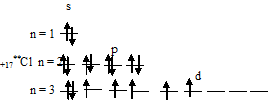
В таком возбуждённом состоянии атом хлора содержит три вакантные 3d-орбитали.
3) При затрате некоторой энергии один из 3s- и два 3p-электронов могут быть переведены на свободные 3d-орбитали, при этом энергия атома возрастает, так что возникающая конфигурация (1s22s22p63s13p33d3) также соответствует одному из возможных состояний хлора:
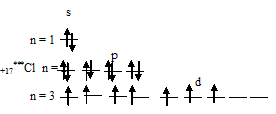
б) Электронная конфигурация валентного энергетического уровня атома ванадия имеет вид: …3d34s2. Графическая схема заполнения электронами имеет вид:
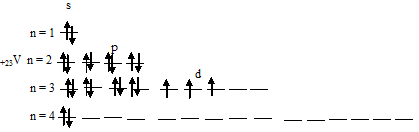
В возбуждённом состоянии атома ванадия один 4s-электрон может быть переведён на свободную 3d-орбиталь, так что возникающая электронная конфигурация валентного уровня (3d44s1) соответствует возбуждённому состоянию атома ванадия, что можно представить в виде схемы:
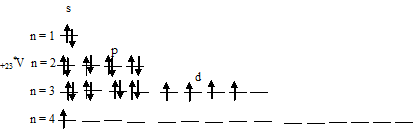
При возбуждении атома ванадия остаётся вакантной одна 3d-орбиталь.
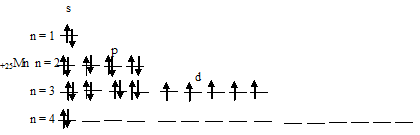
в) Электронная конфигурация валентного энергетического уровня атома марганца имеет вид: …3d54s2. Графическая схема заполнения электронами имеет вид:
При возбуждении атома марганца один s-электрон переходит на 3d-орбиталь, при этом получается электронная конфигурация валентного уровня (3d64s1) соответствует возбуждённому состоянию атома марганца, что можно представить в виде схемы:
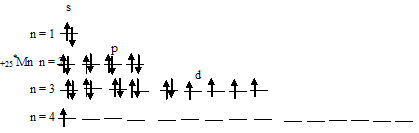
Из схемы вытекает, что при возбуждении атома марганца свободных d-орбиталей нет, так как на 3d-подуровне распределяются два спаренных электрона и четыре неспаренных. Таким образом, атом марганца ни в основном, ни в возбуждённом состоянии не имеет свободных d-орбиталей.
Задача 185. Сколько неспаренных электронов содержат невозбужденные атомы: а) В; б) S; в) Аs; г) Сг; д) Нg; е) Еu?Решение:а) Электронная формула атома бора 1s22s22p1. Валентность орбитали в этом атоме являются орбитали внешнего (второго) электронного, т.е. 2s-, 2p-орбитали. Графическая схема заполнения электронами этих орбиталей имеет следующий вид:
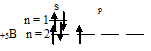
Следовательно, атом бора содержит один неспаренный 2p-электрон.
б) Электронная конфигурация валентного электронного слоя атома серы имеет вид: …2s22p4. Графическая схема заполнения электронами этого слоя имеет следующий вид:
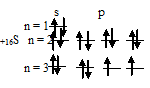
Следовательно, атом серы в стационарном состоянии содержит два неспаренных электрона -, 2p-подуровне.
в) Электронная конфигурация валентного электронного слоя атома мышьяка имеет вид: …4s24p3. Графическая схема распределения валентных электронов имеет следующий вид:

Таким образом, атом мышьяка имеет три неспаренных электрона на 4p-подуровне.
г) Электронная конфигурация валентного электронного слоя атома хрома имеет вид: …3d5 4s1. Графическая схема заполнения электронами этого слоя имеет следующий вид:
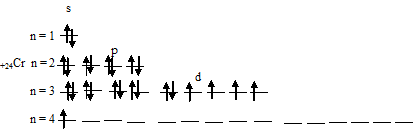
Следовательно, атом хрома в стационарном состоянии содержит шесть неспаренных электронов, из которых пять на 3d-подуровне и один на 4s-подуровне.
д) Электронная конфигурация валентного электронного слоя атома ртути имеет вид: … 6s26p0. Графическая схема заполнения электронами этого слоя имеет следующий вид:

Атом ртути не содержит ни одного неспаренного электрона.
е) Электронная конфигурация валентного электронного слоя атома европия имеет вид: …4f7 6s2. Графическая схема заполнения электронами этого слоя имеет следующий вид:
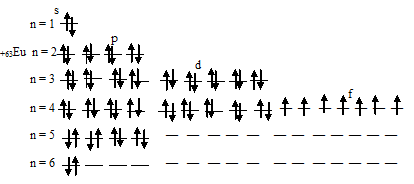
Таким образом, атом европия содержит семь неспаренных 4f-электронов.
Ответ: а) 1; б) 2; в) 3; г) 6; д) 0; е) 7.
Задача 186. Составить электронно-графические схемы ионов Ее2+ и Ее3+. Чем можно объяснить особую устойчивость электронной конфигурации иона Ее3+?Решение:Электронная формула атома железа имеет вид: 1s22s22p63s23p63d64s2. Графическая схема размещения электронов в квантовых ячейках атома железа будет иметь следующий вид:
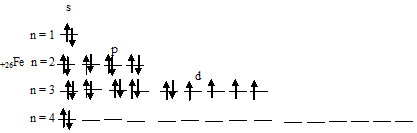
При отдаче двух 4s-электронов атомом железа образуется ион Ее2+, графическая схема размещения электронов в котором будет иметь вид:
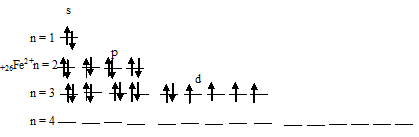
При отдаче трёх электронов (двух 4s- и одного 3d) атомом железа образуется ион Ее3+, графическая схема размещения электронов в котором будет иметь вид:
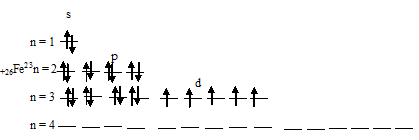
Таким образом, на внешнем энергетическом уровне иона Ее2+ содержится два 3s-, шесть 3p- и шесть 3d-электронов. Причём на 3d-подуровне содержатся четыре неспаренных и два спаренных электрона. Ион Ее3+ отличается от Ее2+ тем, что содержит на 3d-подуровне на один электрон меньше, и все они неспаренные, такая система 3d-подуровня является энергетически более устойчивой. Электростатическое взаимодействие между ядром и электронной плотностью у иона Ее3+ больше, чем у иона Ее2+.
Задача 187. Указать особенности электронных конфигураций меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?Решение:Так как число электронов в атоме элемента равно его порядковому номеру, то общее число электронов в атоме меди и хрома соответственно равно 29 и 24.
Последовательность заполнения энергетических уровней и подуровней в атоме элемента определяется правилами Клечковского, согласно которым электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией (меньшая сумма n + l). Порядок заполнения подуровней определяется правилом Хунда. Согласно правилу Хунда, минимальной энергии атома соответствует такое распределение электронов по атомным орбиталям данного подуровня, при котором абсолютное значение суммарного спина атома максимально.
Электронные формулы атомов хрома и меди можно выразить следующим образом:
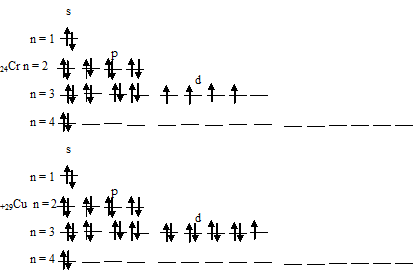
Экспериментально установлено, что на внешнем энергетическом уровне у хрома и меди находится по одному электрону. Объясняется это тем, что произошёл «провал» одного 4s-электрона у атомов хрома и меди на 3d-подуровень. Происходит это потому, что энергетически выгодным состоянием является состояние атома, когда при четырёх неспаренных электронах на 3d-подуровне происходит заполнение пятой свободной атомной орбитали. Поэтому электронная формула атома хрома имеет следующий вид: 1s22s22p63s23p63d54s1.
У атома меди все атомные орбитали 3d-подуровня заполнены, причём четыре полностью, а на пятой находится один неспаренный электрон. Такая система 3d-подуровня, состоящая из девяти электронов является энергетически неустойчивой, и поэтому происходит «провал электрона с 4s-орбитали на 3d-орбиталь. Электронную формулу атома меди можно теперь представить следующим образом: 1s22s22p63s23p63d104s1.
Таким образом, атомы хрома и меди на внешних энергетических уровнях содержат по одному 4-электрону. Графические схемы распределения электронов по квантовым ячейкам у атомов хрома и меди в стационарном состоянии будут иметь следующий вид:
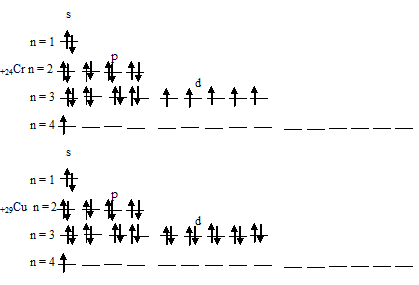
buzani.ru