Справочник химика 21. Темно синий хром
Трилонометрия
Комплексонометрия (трилонометрия)
Обоснование Метод основан на свойстве ионов металлов (1+ до 4+) образовывать с трилоном Б бесцветные, прочные, растворимые внутрикомплексные соединения в мольном отношении 1:1.
Титрант – трилон Б
(динатриевая соль этилендиаминтетрауксусной кислоты – ЭДТА)

Трилон Б имеет в структуре карбоксильные группы и 2 атома азота с неподвижной парой атомов. Ионы металлов образуют соли, замещая атомы водорода карбоксильных групп и одновременно связываясь координационно с атомами азота.

Прочность комплексов характеризуется величиной константы нестойкости (Кнест), которая указывает на способность комплекса к диссоциации. Чем больше значение Кнест, тем менее прочен комплекс, тем больше он диссоциирует с образованием исходных катиона и аниона.
Прочность комплекса Ме-ТрБ возрастает в ряду:
Mg→ Ba→ Ca→ Zn→ Al→ Cu→ Pb→ Bi
Значение констант нестойкости следует учитывать при выборе индикатора: комплекс иона металла с индикатором должен быть менее прочным, чем комплекс того же иона с трилоном Б.
Определяемые вещества
Лекарственные вещества, содержащие ионы двух- или трехвалентных металлов: цинка сульфат, цинка оксид, кальция хлорид, висмута нитрат основной, магния оксид, кальция лактат, кальция глюконат, меди сульфат…
Реакция сопровождается выделением и накоплением ионов водорода. Связанные Н+ будут смещать реакцию в сторону образования комплекса, поэтому д.б. pH=9,5-10.
Условия определения
создание рН среды с помощью буферных растворов (например, аммиачного буферного раствора), растворов оснований (натрия гидроксида, аммония гидроксида, гексаметилентетрамина), кислот (например, кислоты азотной).
Индикаторы – металлохромные органические красители:
эриохром черный Т,
хромовый темно-синий,
ксиленоловый оранжевый,
кальконкарбоновая кислота, пирокатехиновый фиолетовый и др.
Индикация основана на свойстве ионов металлов образовывать с индикатором интенсивно окрашенные комплексы, но в другой, по сравнению с самим индикатором, цвет и по устойчивости уступающие комплексам ионов металлов с трилоном Б.
1.эриохром черный Т (кислотный хром черный специальный), Определяемые катионы Zn2+,Mg2+ (ФС) , Ca2+.
Изменение окраски при рН=9,5-10 раствора от красно-фиолетовой (комплекс) до синей (свободный индикатор)

2.Хромовый темно-синий (кислотный хром темно-синий).
Определяемые катионы Ca2+ (ФС), Mg2+, Zn2+.
Изменение окраски при рН=9,5-10 раствора от красной (комплекс) до сине-фиолетовой (свободный индикатор)

3.пирокатехиновый фиолетовый.
Определяемые катионы Zn2+,Bi3+ (ФС), Al3+, Pb2+
Изменение окраски при рН=2-3 раствора от синей (комплекс) до желтой (свободный индикатор)

4. Ксиленоловый-оранжевый. Изменение окраски при рН=2-3 раствора (красная – желтая), при рН=5-6 от красной до фиолетово-желтой. Определяемые катионы Bi3+Al3+ (ФС) Pb2+, Zn2+
5. Кальконкарбоновая кислота. Изменение окраски при рН =12 от красновато-сиреневой до голубой. Определяемые катионы Ca2+ Zn2+ (МФ).

Этапы титрования
На первом этапе добавляют индикатор к р-ру, содержащему определяемый катион. Р-р должен иметь определенное значение рН, добавляют аммиачного буфера, кислоты или щелочи. Образуется хорошо растворимое в воде не устойчивое окрашенное соединение 1% металла с индикатором.
На втором этапе – титруют трилоном Б, он связывает свободные ионы Ме в устойчивый комплекс, как правило бесцветный
На третьем этапе – вблизи т.э. когда свободных ионов в р-ре нет, разрушается менее прочный комплекс Ме – индикатор и р-р окрашивается в цвет свободного индикатора. 1)
2)
3)
Для четкого установления т.э. необходимо:
1) комплекс Ме+n – индикатор д.б. достаточно прочным, но его устойчивость д.б. в 10 раз меньше чем устойчивость комплекса Ме+n - ЭДТА. Иначе титрование будет закончено либо преждевременно, либо поздно.
2) концентрация индикатора д.б. малой, инд. должен связывать менее 1% ионов определяемого металла Ме+n
3) изменение окраски индикатора д.б. четким, контрастным, быстрым.
Различают способы прямого, обратного и косвенного титрования.
В большинстве случаев применяется прямое комплексонометрическое титрование.
Прямым титрованием определяют растворимые в воде или кислотах лекарственные вещества, способные легко и быстро реагировать с трилоном Б.
При определении оксидов металлов их предварительно растворяют в кислотах:
MgO + 2НСl → MgCl2 + h3O
ZnO + 2HCl → ZnCl2 + h3O
Bi2O3 + 6 HNO3 → 2Bi(NO3)3 + 3 h3O


Обратное титрование применяют
для лекарственных веществ, нерастворимых в воде и кислотах, например бария сульфат
когда образование комплекса с титрантом идет медленно во времени и при нагревании, например алюминия гидроксид,
когда катионы осаждаются аммиаком аммиачного буфера.
Обратный вариант основан на растворении определяемых веществ в избытке титрованного раствора трилона Б, остаток которого титруют вторым титрантом – магния сульфатом или свинца нитратом.
В т.э. р-р приобретает окраску свободного индикатора.

Особенности расчетов при комплексонометрическом титровании:
1) в независимости от заряда Ме+n (II или III) ЭДТА реагирует в соотношении 1:1 М.э = М.м
Na2h3Tp (трилон Б) → 2Na+ + h3Tp2-
Mg+2 + Na2h3Tp → Na2MgTp +2H+
Аl+3 + Na2h3Tp → NaАlTp +2H+ + Na+
Кстех=1/1=1
Титрант приготовлен с учетом реальных частиц (РЧ) по ГФ ХI ОФС "Титрованные растворы" (РЧ Tpилон Б - РЧ принимаем за 1)
fэкв= Кстех· (РЧ или УЧ) = Кстех· 1
М.э = fэкв · М.м = 1· М.м
При расчете М.э эквивалента всегда берем М.э =М.м (кроме висмута нитрата основного)
2) титрант – динатриевая соль – двухосновной ЭДТУ кислоты. Для приготовления 1л 0,1н титрованного раствора учитывается основность кислоты и берут навеску выраженную в граммах
а =0,1 • М.м (Трилона Б) : 2.
Поэтому 0,1н = 0,05 М.
Однако в химической реакции, лежащей в основе комплексонометрического определения, Трилон Б всегда вступает в реакцию 1 моль с 1 моль соли Меn+, т.е. основность здесь не имеет значения, поэтому при расчете титра соответствия в формулу подставляют не нормальную концентрацию в N, а молярную концентрацию (М, моль/л):
Т = М.э · Ст-та= М.э · 0,05М (г/мл)
1000 1000
Расчет концентрации:
С% = V · K· T · Vколбы · 100%
a · Vал.пробы
Висмута нитрат основной – расчет ведут по висмута оксиду (Bi2О3), при растворении его в HNO3 образуется 2 Bi(NО3)3
Bi2О3+ 6 HNO3→ 2 Bi(NО3)3+3 h3O
2 Bi3++ 2Na2h3Tp →2NaBiTp +4H+ + 2Na+
Кстех=1/2
fэкв=1/2 ·1
М.э =1/2 · М.м = М.м/2
1)
 +Zn+2→
+Zn+2→
Красно-фиолетовый
2)

 + 2H+
+ 2H+
3)
 +
+ →
→
 синий +
синий +
studfiles.net
Металлиндикаторы кислотный хром темно-синий - Справочник химика 21
Комплексонометрическое определение иона магния основано на свойстве комплексона III (трилон Б) извлекать магний пз его окрашенного комплекса с некоторыми металлиндикаторами, как хромоген черный ЕТ-00, кислотный хром темно-синий и другие. Чаще всего определение проводят по хромогену черному, или хром темно-сине.му. [c.233]При малой величине суммы ионов кальция и магния лучше пользоваться металлиндикаторами хром темно-синим или кислотным хром синим (стр. 72). Эти индикаторы входят в набор реактивов для определения жесткости воды Союзреактива . [c.235]
При комплексометрическом титровании кальция и магния используют ряд металлиндикаторов для кальция— мурексид, флуорексон, а для кальция и магния — хромоген черный ЕТ-00 (эриохром черный Т), кислотный хром синий К, кислотный хром темно-синий. Предпочтение следует отдавать кислотному хром темно-синему, так как чувствительность его к ионам кальция в четыре раза больше, чем мурексида (1,4переход окраски более резко выражен, чем у хромоген черного. Применяя кислотный хром темно-синий, можно оттитровать кальций и магний в одной пробе с одним и тем же индикатором, но при разных значениях pH. Содержание кальция и магния может быть найдено и фотометрическим титрованием (см. главу I, п. 3) на титраторе ФЭТ-УНИИЗ или ТФЛ-46-2. [c.39]
Из большого числа металлиндикаторов при определении двухвалентных металлов чаще всего используют мурексид, хромоген черный, кислотный хром темно-синий, кислотный хром синий К и флуорексон. В случае маскировки полуторных окислов триэтано-ламином для определения магния пользуются особыми индикаторами— метилтимоловым синим и тимолфталексоном (взамен хромогена черного). Все металлиндикаторы образуют комплексные соединения лишь при определенном значении pH раствора, поэтому перед прибавлением индикатора в анализируемый раствор в него вносят буферный раствор с соответствующим значением pH. [c.71]
chem21.info
Кислотный хром темно-синий - Справочник химика 21
Кислотный хром синий К(П) и кислотный хром темно-синий (III) были предложены для комплексонометрического определения жесткости воды. [c.288]Определение Са +. К исследуемому раствору прибавляют 10 см аммиачного буферного раствора, доводят общий объем раствора до 100 м прибавляют ложечку индикатора — кислотный хром темно-синий. [c.705]
Кислотный хром темно-синий [c.265]
Проведите количественное определение препарата фармакопейным методом около 0,1 г (точная навеска) кальция глюконата поместите в мерную колбу вместимостью 100 мл, растворите в горячей воде, доведите водой до метки, охладите тщательно перемешайте Затем 10 мл разведения поместите в колбу для титрования, добавьте 5 мл аммиачного буфера и 3 капли индикатора (раствор кислотного хром темно-синего) и титруйте 0,05 М раствором трилона Б до сиие-фиолетового окрашивания [c.377]Концентрацию железа определяют по каталитически ускоряемой железом реакции окисления кислотного хром темно-синего перекисью водорода. При содержании железа 0,01 0,02 и 0,03 мкг/мл оптические плотности растворов за 8 мин уменьшились от [c.237]
Для определения жесткости деминерализованной воды титрование ведут 0,01 yV раствором комплексона III в присутствии кислотного хром-темно-синего. [c.317]
В щелочной среде (pH 10) эти индикаторы образуют с магнием и кальцием комплексные соединения красного цвета. Молярное отношение катиона к реагенту в комплексах с кислотным хром темно-синим равно 1 2 [562]. рК магниевого комплекса равно 8,51, кальциевого —9,28. В отсутствие ионов магния и кальция при pH 10 кислотный хром темно-синий окрашен в сине-сирене-вый цвет, а кислотный хром синий К — в сиреневый. При титровании этих ионов кислотный хром темно-синий дает лучший переход окрасок (из ярко-розовой — в сине-сиреневую), поэтому из этих двух индикаторов пользуются предпочтительно им [1156]. Методики титрования в присутствии кислотного хром темно-синего и приготовления его растворов аналогичны таковым для эриохром черного Т. Преимуществом кислотного хром темно-синего перед эриохром черным Т является более высокая чувствительность взаимодействия с ионами магния (2,0-10 г мл) и особенно кальция (1,4-10 г мл) [380, 534]. [c.41]
Карбоксиарсеназо Кислотный хром темно-синий Кислотный хром фиолетовый К Крахмал растворимый [c.636]
Хлор-2-оксифенил) -азо]-1,8-диоксинафталин--3,6-дисульфокислоты динатриевая соль см. Кислотный хром темно-синий [c.524]
Смесь комплексонатов оттитровывают в щелочной среде в ари-сутствии одного из индикаторов кислотного хрома темно-синего или хромогена черного Т. [c.372]
Для определения жесткости деминерализованной воды титрование ведут 0,01 н. раствором комплексона III с добавлением индикатора кислотного хром темно-синего (сухая смесь с хлоридом натрия 1 100). К 100 мл воды до- бавляют 5 мл аммиачного буферного раствора с pH 10 (см. выше), 0,1—0,2 г индикатора и титруют до изменения окраски от красной до сине-сиреневой. [c.343]
Фотометрический метод определения кальцпя с кислотным хром темно-синим применяется при анализе цементных сырьевых смесей и клинкеров [50, 51]. Метод предложен для определения больших количеств кальция (40—45% СаО). При этом большую часть кальция связывают в бесцветный комплекс с комплексоном III, а оставшийся кальций ( 6%) определяют по цветной реакции с кислотным хром темно-синим. [c.100]
Преимущество кислотного хром темно-синего — возможность использования для последовательного определения Са и Mg в одной порции раствора [388, 422, 532, 533, 535]. Определение индивидуальных элементов в одной порции раствора возможно по методике, предложенной для анализа продуктов металлургического производства [388]. [c.60]
Предложен [533] метод комплексонометрического определения кальциевой (и магниевой) жесткости воды с индикатором кислотным хром темно-синим. [c.190]
В отличие от эриохром черного Т кислотный хром темно-синий позволяет отчетливо фиксировать точку эквивалентности (pH 10) при определении кальция в отсутствие магния [394, 488] или при низких содержаниях последнего. К тому же кислотный хром темно-синий устойчив по отношению к окислителям и восстановителям. Однако, если индикаторный переход в случае применения эриохром черного Т заканчивается возникновением чисто-синей окраски, то кислотный хром темно-синий и кислотный хром синий К дают переходы к оттенкам, менее удобным для определения конца титрования (сиренево-синий, сиреневый). Кислотный хром темно-синий, так же как и эриохром черный Т, не отличается специфичностью, и характер влияния посторонних ионов на эти индикаторы аналогичен [534]. [c.41]Гидрон I реагирует с кальцием с большей чувствительностью (0,012 мкг С 1мл), чем эриохром черный Т и кислотный хром темно-синий, что позволяет успешно титровать кальций в отсутствие магния, с которым индикатор реагирует с такой же высокой чувствительностью. По специфичности гидрон I мало отличается от эриохром черного Т и кислотного хром темно-синего. Недостаток этого индикатора —наличие существенной солевой ошибки. Свойства гидрона I свидетельствуют о том, что его целесообразно применять для определения жесткости слабоминерализованных вод. [c.42]
Четкость перехода окраски оптимальна в довольно узком интервале значений pH (10,5—11,2) [511]. С другой стороны, преимуществом бериллона II сравнительно с эриохром черным Т, кислотным хром темно-синим и другими индикаторами является его более высокая специфичность [369, 516]. Бериллон II не образует окрашенных комплексов с Ге +, АР+, Т1 +. Поэтому присутствие небольших количеств этих ионов, а также не мешает титрованию кальция и магния [521]. Определению с бериллоном II не мешают высокие содержания хлоридов, сульфатов, а также присутствие некоторых органических веществ солевая ошибка этого индикатора невелика. [c.43]
По сравнению с мурексидом, эриохром черным Т, метилтимоловым синим, кислотным хром темно-синим и кислотным хром синим к при спектрофотометрическом титровании кальция и магния [168], кислотный хром синий К дает наибольшую величину Де при X = 590—630 нм, что позволяет повысить чувствительность определения (типичный вид кривой титрования показан на рис. 5). [c.48]
При высоком содержании магния наблюдается адсорбция кальция и кислотного хром темно-синего гидроокисью магния, что ухудшает индикаторный переход окраски [309, 532, 533]. Для уменьшения соосаждения кальция при pH 13 к анализируемому раствору прибавляют 1—2 мл 2%-ного раствора сахара, связывающего кальций в растворимый сахарат. Во избежание адсорбции индикатора его добавляют непосредственно перед титрованием и титруют до первого отчетливого изменения окраски, не обращая внимания на возможность последующего появления розового оттенка. [c.60]
Кислотный хром темно-синий применяется при анализе шлаков, агломератов, руд [387, 500], кальцита, флюорита [468, 470] и др. [c.61]
Кислотный хром темно-синий применен также для фотометрического определения кальция в биологических объектах [655, 748, 1657], чугуне [1316], металлическом титане [987]. Используется также для косвенного фотометрического определения кальция эриохром черный Т [1351, 1546, 1663]. [c.100]
Применение кислотного хром темно-синего предпочтительно также при определении малых жесткостей. [c.189]
КИСЛОТНЫЙ ХРОМ ТЕМНО-СИНИЙ (кислотный хром синий Т, эриохромсиний ЗЕ), черные крист. раств. в воде. [c.258]
Селективное определение гидрохлорида папаверина в лекарственных формах возмолсно при использовании в качестве реагента-красителя кислотного хром темно-синего (КХТС). Этот краситель образует с гидрохлоридом папаверина комплекс фиолетового цвета в соотношении 1 2, который количественно экстрагируется хлороформом (теоретические и экспериментальные основы экстракции описаны в работе 10). [c.138]
Для установления точки эквивалентности применяются спе циальные индикаторы, которые по своей природе являются ор ганическими красителями. К ним относятся кислотный хром темно-синий, кислотный хром черный специальный, называемый эриохром черный Т или хром черный специальный ЕТ-00, мурек-сид и др. [c.27]
Количественное определение водного раствора препарата производят с помощью 0,05 М раствора трилона Б в присутствии аммиачного буферного раствора и индикатора кислотного хром-темно-синего (1,8-диокси-2- (2-оксифенилазо)-нафталин-3,6-дисульфоната натрия) до сине-фиолетового окрашивания. [c.531]
Эриохром яерный (специальный ЕТ-00) замена — кислотный хром синий К, кислотный хром темно-синий ИНД. 4 г [c.84]
Определение Са2+ и Мд2+. Наиболее быстрым и точным методом определения Са + и является при меняемый сейчас повсеместно трилонометрический метод, основанный на способности трилона-Б (двузаме-щенной натриевой соли этилендиаминтетрауксусной кислоты) образовывать с ионами Са + и Mg2+ малодис-социированные комплексы. В ходе анализа к пробе воды добавляют индикатор, дающий цветные реакции со щелочноземельными металлами. Такими индикаторами могут служить хромоген черный, специальный ЕТ-00,. кислотный хром синий К, кислотный хром темно-синий. Эти индикаторы, растворенные в воде, не содержащей ионов Са + и М 2+, окращивают ее соответственно в голубой, сиреневый и сиренево-синий цвет. Вода, содержащая Са + и Mg2+, в присутствии хромогена черного окращивается в винно-красный цвет, в присутствии кис-, лотного хрома синего К и кислотного хрома темно--синего —в розово-красный цвет. Вследствие этого при титровании воды трилоном-Б в конечной точке титрования происходит резкое изменение цвета воды из виннокрасного в голубой (хромоген черный) или из розовокрасного в сиреневый или сиренево-голубой (кислотный хром синий К и кислотный хром темно-синий). [c.169]
В качестве буферных растворов используют аммиачно-хлорид-ный [1121, 1525], аммиачно-фторидный [1525], аммиачно-тарт-ратный [976, 978], аммиачно-ацетатный [535, 759, 1518], аммиачно-боратный [760] и другие. Для удержания Мп(И) в растворе при pH 10 рекомендуют применять триэтаноламин, а во избежание окисления Мп(П) кислородом воздуха необходимо вводить восстановитель — аскорбиновую кислоту или солянокислый гидро-ксиламин [ИЗ, 532, 538, 740, 741, 752, 976, 1309, 1345]. Однако в присутствии кислотного хром темно-синего и кислотного однохром бодро С титрование можно вести и в отсутствие восстановителя [538]. Необходимо избегать введения восстановителя также в присутствии Fe(III). [c.46]
Количественное содержание вещества в препарате определяется комплексометрически с индикатором кислотным хром темно-синим (ГФ X). Индикатор реагирует с в щелочной среде с образованием вишнево-красного комплекса. При титровании трилоном Б в эквивалентной точке происходит переход цвета раствора в синевато-сиреневый. Чистого кальция хлорида в препарате должно быть не менее 98,0%. [c.119]
Количественное содержание кальция лактата в препарате определяется методом комплексометрии (фармакопейный метод). Раствор препарата титруется трилоном В в присутствии аммиачного буферного раствора по индикатору кислотному хром темно-синему до сине-фиолетового окрашивания (см. Комплексометрический метод титрования ). [c.186]
Точку эквивалентности отмечают по изменению ойраски введенного в раствор индикатора. В качестве последнего применяют эриохром черный Т [532, 740, 741, 972, 976—978, 1121, 1413], эриохром красный В [1525], кислотный хром темно-синий [116, 301, 538, 612], тимолфталексон [752, 876, 1148, 1343], пирокате-хиновый фиолетовый [1200, 1413], метилтимоловый синий [1141, 1148], ксиленоловый оранжевый [ИЗ], 1-[2-пиридилазо]-2-нафтол [977, 1148], кислотный хром бордо И [538], фталеиновый фиолетовый [1309], пиридилазорезорцин [1148], метиленовый голубой [1394], дифенилкарбазон [1394], о,о -диоксиазокрасители, мурек-сид [760], флюоресцеинкомплексон [1518], а также гематоксилин [c.44]
В силу различных причин были получены отрицательные результаты при использовании следующих индикаторов (pH 0,5— 1,5) пирокатехинового, фиолетового, 2,4-дисульфобензаурин-3,3-дикарбоновой кислоты нитрозо-Н-соли эриохром черного Т 1,8-диокси-2-(2 -карбоксибензолазо) - нафталин-3,6-дисульфокис-лоты кислотного хром темно-синего 2,4-диоксибензол--2-оксинафталин-4-сульфокислоты и дифениламин-2-сульфо-кислота--диоксинафталин-3,6-дисульфокислоты. Последние два индикатора просто разрушались азотной кислотой. [c.209]
Для фиксирования точки эквивалентности в качестве индикаторов используют органические красители кислотный хром темно-синий, кислотный хромоген черный специальный (называемый эриохром черный Т, или хромоген специальный ЕТ-00 — С2оН1з07Кз8), мурексид gHeNeOe и др. Наиболее часто применяют хромоген черный специальный ЕТ-00 и мурексид. [c.314]
Железо и алюминий при концентрации выше 10 мг1л затрудняют титрование в присутствии кислотного хрома темно-синего [531, 534]. Для их маскировки используют триэтаноламин [549]. Мешающее действие меди, цинка и марганца проявляется при очень малой концентрации и устраняется осаждением сульфидом натрия [517, 534]. Для предупреждения окисления марганца в раствор вводят солянокислый гидрокспламин [356, 477] или реже — сернокислый гидразин [324]. [c.42]
Для ускоренного определения кальция и магния в мартеновских шлаках с высоким содержанием фосфора (J>10%) рекомендуется обратное титрование избытка комплексона III раствором Mg lj или ZnS04 [324]. Описан вариант экспрессного полумикро-определения кальция и магния с индикатором кислотным хром темно-синим [501] методом капельного титрования. [c.42]
Описано последовательное определение кальция и магния в одной порции раствора фотометрическим титрованием раствором комплексона III с индикатором кислотным хром темно-синим [523]. Кальций и магний предварительно отделяют от Ре, А1, Mg, окиси кремния и щелочных металлов осаждением. в виде СаСОз и Mg (ОН), при pH 13 в присутствии триэтаноламина. [c.48]
Чтобы определить, сколько щелочи нужно добавить к титруемому раствору (на 100 мл) при анализе сложных материалов, используют кислотно-основные индикаторы малахитовый зеленый (добавляют 5 N КОН до обесцвечивания раствора и еше 4 мл этого же раствора КОН [360, 415, 518, 579] и аурамин (добавляют 30%-ный КОН до перехода желтой окраски в серую и еще 1 лл этого же раствора КОН) [1432]. Реакция чувствительнее, чем с мурексидом, эриохром черным Т, кислотным хром темно-синим, кислотным хром синим К, кальционом, кальцоном, метилтимоловым синим, глиоксаль-б с-(2-оксианилом), крезолфталексоном [142]. [c.55]
Азоиндикаторы. Кислотный хром темно-синий используют при определении суммы магния и кальция, а такжо при определении кальция в присутствии магния при высоком значении pH [531, 533]. Индикаторный переход характеризуется изменением красной окраски в сиренево-синюю. По точности результатов титрования кислотный хром темно-синий превосходит мурексид, по индикатор не дает четкого перехода окраски в точке эквивалентности [142]. [c.59]
Раздельному комплексонометрическому титрованию кальция и магния мешают большие количества хлорида аммония. Рекомендуют удалять аммонийные соли кипячением анализируемого раствора с 8N раствором NaOH в присутствии малахитового зеленого до исчезновения окраски. Затем раствор выпаривают досуха и осадок растворяют в соляной кислоте [309]. После нейтрализации раствора кальцпй и магний последовательно определяют с кислотным хром темно-синим. Лучшим методом удаления аммонийных солей авторы считают окисление их смесью азотной кислоты и нитрита натрия (или царской водкой). [c.60]
Для косвенного фотометрического определения кальция используют кислотный хром темно-синий [50, 51, 655, 748, 987, 1109, 1316, 1379, 1657]. Реагент хорошо растворим в воде. Водные растворы кислотного хром темно-синего окрашены в вишневокрасный цвет, в щелочной среде — в синевато-сиреневый. [c.99]
Как видно из рис. 20, наибольшая разность в поглощении комплекса наблюдается при 600 нм [50]. Фотометрируют при 595 нм [50, 51] по уменьшению интенсивности окраски кислотного хром темно-синего. Окраска развивается сразу же после сливания растворов и устойчива в течение 90 мин. 655, 1316]. Чувствительность реакции 1,4-10" г мл раствора [50]. Закон Бера для растворов комплексного соединения кальция с кислотным хром темно-синим не соблюдается (оптическая плотность уменьшается с увеличением концентрации кальция) [50]. Повышение pH приводит к уменьшению чувствительности (рис. 21). Оптимальное количество щелочи —5-мл 10%-ного раствора Ка0н/100.Л4Л [50]. При фотометрическом определении кальция используют 0,02%-ный водный раствор кислотного хром темно-синего [50, 51]. Водные растворы реагента устойчивы несколько недель [50]. Определению [c.99]
Широко используется для определения общей жесткости воды индикатор кислотный хром темно-синий [531, 533], который, в отличие от эрихром черного Т, позволяет титровать при низком содержании магния и даже в его отсутствие без добавления комплексоната магния. [c.189]
Пробу анализируемой воды доводят дистиллированной водой до объема 100 мл, добавляют 5 мл аммиачного буферного раствора (100 мл 20%-ного раствора Nh5 I смешивают со 100 мл 20%-ного Nh5OH и разбавляют до 1 дистиллированной водой). Добавляют 5—7 капель 0,5%-ного раствора кислотного хром темно-синего и медленно титруют 0,05 М раствором комплексона П1, интенсивно перемешивая до изменения окраски жидкости [233]. [c.189]
Аналитическая химия (1994) -- [ c.314 ]Аналитическая химия кадмия (1973) -- [ c.3 , c.84 , c.91 ]
Основы аналитической химии Часть 2 (1965) -- [ c.257 ]
Справочник по аналитической химии (1979) -- [ c.288 ]
Производство органических красителей (1962) -- [ c.145 ]
Основы аналитической химии Книга 2 (1961) -- [ c.316 ]
Курс аналитической химии Издание 5 (1982) -- [ c.240 , c.243 ]
Руководство по химическому анализу почв (1970) -- [ c.72 ]
Комплексонометрическое титрование (1970) -- [ c.57 , c.81 ]
Курс аналитической химии Кн 2 Издание 4 (1975) -- [ c.243 ]
Основы аналитической химии Кн 2 (1965) -- [ c.257 ]
Государственная фармакопея союза социалистических республик Издание 10 (1968) -- [ c.822 ]
chem21.info
Хром прочный темно-синий - Справочник химика 21
Комплексообразов ние обычно сопровождается изменением окраски раствора, так в первой реакции голубой цвет (Си 04) переходит в темно-синий (окраска комплекса), во второй реакции окраска изменяется из зеленой в светло-фиолетовую. Наиболее прочные комплексы с NHз образуют хром и кобальт в степени окисления +3. Это объясняется тем, что в комплексах данных ионов, имеющих конфигурацию соответственно е/ и -электроны заполняют слабо экранирующие ядро орбитали с низкой энергией (см. разд. 2.7). [c.402] Комплексонат бария отличается малой прочностью (рК 7,8) (табл. 6). Поэтому титрование его комплексоном III по хромогену черному и хром темно-синему возможно лишь в присутствии ионов магния, который образует с комплексоном III более прочный комплексонат (рК 8,7). Изменение окраски раствора происходит в тот момент, когда комплексон III извлечет магний из его соединения с металлиндикатором. [c.244]Более точные результаты получаются при титровании раствора трилона Б анализируемым раствором. Перед титрованием раствор трилона Б смешивают с определенным количеством щелочного буфера (см. ниже), добавляют индикатор хром темно-синий и разбавляют смесь водой. Разбавленную смесь медленно титруют анализируемым раствором. При этом каждая капля анализируемого раствора реагирует с избытком комплексона в условиях (по значению pH), наиболее благоприятных для образования комплекса, с молекулярным отношением лиганда и центрального иона (металла-комплексообразователя). Медленное приливание по каплям к титруемой смеси анализируемого раствора приводит к образованию прочного комплекса, но осаждения кальция не происходит, несмотря на присутствие щелочного буферного раствора. [c.159]
Крашение ацетилцеллюлозных этролов производится теплостойкими, светостойкими немигрирующими органическими и неорганическими красителями. К числу таких органических красителей и пигментов относятся пигмент желтый прочный, пигмент ярко-оранжевый антрахиноновый, пигмент бордо антрахиноновый, лак алый С, лак красный 2СМ, лак бордо СМ, пигмент синий антрахиноновый, пигменты голубой и зеленый фталоцианиновые, глубоко черный и др. Из минеральных пигментов применяются кадмий лимонный, кадмий оранжевый, кадмий красный темный, охра красная, кобальт синий, ультрамарин, окись хрома, изумрудная зелень, английская красная, сиена жженая и др. [c.213]
Кадмий красный темный Лак красный СМ Диоксид титана Кадмий лимонный Голубой фталоцианиновый Диоксид титана Синий антрахиноновый Диоксид титана Желтый прочный 23 Голубой фталоцианиновый Диоксид титана Технический углерод ламповый Оксид хрома [c.132]
Сущность метода. ЭДТА образует с кальцием более прочно е комплексное соединение, чем с магнием (р/( устойчивости комплексов соответственно равны 10,57 и 8,68). Поэтому при добавлений ЭДТА к раствору, содержащему Са + и М +, в первую очередь реагирует кальций и только тогда, когда весь кальций будет свя зан в комплекс, начинает титроваться магний. Это рааделение облегчается еще и тем, что титрование кальция проводят прй pH 12—13, когда магний выпадает в осадок в виде гидроксида. После титрования кальция раствор подкисляют, добавлением буферного раствора приводят pH к 10 0,1 и титруют магний. Если в качестве индикатора при определении кальция служил кислотный хром темно-синий, то этот же индикатор будет служить и для определения магния, Если при определении кальция применили мурексид, то при подкислении раствора он разрушится. Разрушение ускоряют нагреванием или добавлением 1 капли бромной воды. Затем для определения магния вводят новый индикатор— кислотный хром черный специальный (эриохром черный Т). Если содержание кальция в пробе известно заранее, то можно, пользуясь этим индикатором, оттитровать при pH = 10 0,1 сумму кальция и магния и, зная содержание кальция, рассчитать содержание магния. [c.119]
Калькой, кислотный хром сине-черный В, мордант черный 17, палатнн хром черный 6BN, понтахром сине-черный R, солохром темно-синий В, суперхром си-не-черный, хромовый прочный цианин В, хромовый прочный цианин G, хромовый синий, эриохром сине-черный R, 2-гидрокси-1-(2 -гидроксинафталин-Г-азо)-4-сульфонафталин [c.215]
На водяной бане нагревают при 50° 1 часть галламинового синего с 6 частями раствора бисульфита натрия, содержащего 25% SO2, до прекращения выделения сернистой кислоты. Это происходит примерно через 1 час, затем нагревают при 85° в течение 1—3 дней до тех пор, пока смесь не станет серо-зеленой. Полученный таким образом краситель является сульфокислотой лейкосоединения (вероятно, комплексной сульфосолью ) он /окрашивает шерсть с уксуснокислым хромом в красивые и npoiinbie темно-синие (флотские синие) цвета. Он может использоваться и в ситцепечатании, однако другие красители этой группы его превосходят. Так, восстановлением галламинового синего сероводородом получают лейкосоединение — модерн фиолетовый (фирмы Дюран и Гюгенен ), образующий на хлопке чрезвычайно чистый и прочный хромовый лак. [c.277]
Хромовый прочный зеленый О, см. Кислотный хром темно-зеленый. Хромовый прочный синий 2С, см. Бриллиантовый прочный синий РВ. Хромовый прочный синий ФБ, 2-(2 -гидрокси-3, 5, б -трихлорбензолазо) кислота [c.430]
chem21.info
Хромовый темно-синий - Справочник химика 21
Доводят объем раствора водой до 50 мл, прибавляют 10 мл буферного раствора с pH 9,5—10,0 0,1 г индикаторной смеси или 7 капель раствора индикатора хромового темно синего и титруют раствором трилона Б (0,05 моль/л) до сине-фиолетового окрашивания. [c.187]Хромовый темно-синий Кислотный хромовый темно-синий ТУ 6-09-3870-84 [c.99]
Реактивы и растворы. 1) Кислота соляная, р=1,19 г/см , и разбавленная 1 1 2) аммиак, р = 0,91 г/см и разбавленный 1 1 3) индикатор метиловый красный 4) индикатор кислотный хромовый темно-синий [c.237]
Кислотный хромовый темно-синий [c.635]Хромовый темно-синий Протравной синий 13 Эриохромовый синий 5Е(Су) [c.725]
Смесь хромового темно-синего (202), хромового темнозеленого С (101) и хромового желтого К (75) [c.730]
Хромовый темно-синий Хромовый черный О Хромовый черный С Хромовый ярко-красный [c.534]
Хромовый темно-синий (кислотный хром темно-синий) — однородный порошок черного цвета. [c.226]
Скорость восстановления красителей зависит от их структуры и обратно пропорциональна требуемому количеству водорода. Так, на восстановление хромового темно-синего красителя, протекающее аналогично уравнению (2.4) по схеме [c.37]
Хромовый темно-синий [c.89]
Хромовый темно-синий образуется [c.197]
Хромовый желтый 3 Хромовый желтый 2К Хромовый желтый К Хромовый оранжевый Хромовый оранжевый 5К Хромовый красный ализариновый Хромовый ярко-красный Хромовый ярко-красный 2С Хромовый рубиновый Ж Хромовый рубиновый С Хромовый бордо С Хромовый фиолетовый К Хромовый синий К Хромовый синий 2К Хромовый темно-синий Хромовый зеленый антрахиноновый Хромовый зеленый антрахиноновый [c.232]
Хромовый темно-синий 4 3 5 4 6 5 5/5/5 5/5/5 5/4-5/5 4 5 [c.234]
Хлор-2-оксифенил) азо -1,8-диокси-нафталин-3,6-дисульфокислоты динатриевая соль см. Хромовый темно-синий [c.495]
Хромовый сине-черный см. 1-[(2-Окси-1-нафтил) азо] -2-нафтол-4-сульфокислота Хромовый темно-синий, индикатор Кислотный хром темно-синий 2- [ (5-Хлор- [c.502]
ТУ 6—09—07—202—74 чда 230-00 Хромовый темно-синий [c.548]
Хромовый темно-синий 9,5-10,0 синевато-сиреневая розово-красная МП2-1-Мд -ь, Са2+ [c.691]
Хромовый темно-синий Са титриметрический [c.699]
Хромовый темно-синий (красный) [c.271]
Хромовый темно-синий для Пыль взрывоопасна [c.371]
Дифенилкарбазид, иод 0,01 н. раствор (фиксанал), кЖтия бихромат, натрия гидрокарбонат, натрия гидроксид, натрия хлорид, серебра нитрат Активный ярко-голубой КХ (МРТУ 6-14-16—68), аммония хлорид (ос, ч.), гидроксиламин гидрохлорид, ионообменная смола КУ-2-8Ч С в Н-форме, кислотный ярко-красный, магния сульфат, натрия диэтилдитиокар-бамат, натрия сульфат, трилон Б, хромовый темно-синий, цинка сульфат, эриохром черный Т Аммония хлорид, железа (III) хлорид, калия бихромат (0,1 н. стандарт-титр), калия гидроксид, калия гидрофосфат, калия дигидрофосфат, калия иодид, кальция хлорид, магния сульфат, марганца хлорид, натрия гидрофосфат, натрия тиосульфат (0,1 н. стандарт-титр), крахмал растворимый для иодометрии, мочевина [c.380]
Хромовый темно-синий образуется при сочетании диазотированного 4-хлор-2-аминофенола с хромотроповой кислотой [c.221]
Сущность метода заключается в комплексонометрическом титровании кальция и магния трилоном Б при pH 10. В качестве индикатора используют эриохром черный Т (хромовый темно-синий) или протравной черный II. [c.97]Хромовый темно-синий получают из той же диазосоставляющей и хромотроповой кислоты. До хромирования он окрашивает шерсть в красный цвет, после хромирования в темно-синий. Более глубокий цвет по сравнению с предыдущим красителем объясняется тем, что Хромовый темно-синий участвует в комплексообразовании в хинонгидразонной форме. [c.89]
Для определения цинка в органических силикатах предложен весовой метод (в виде 2п2Рг07) или комплексометрическое титрование трилоном Б с индикатором хромовым темно-синим [322, 331]. Другие элементы И группы рекомендуют определять в виде соответствующих окислов с предварительным использованием методики мокрого сожжения (обработки вещества смесью концентрированных серной и азотной кислот) [331, 847]. [c.135]
Хромовый темно-синий (получается сочетанием диазотированного 4-хлор-2-аминофенола с хромотроповой кислотой) [c.142]
Сульфофеннл (1 -азо-2 ) -Г,8 -диоксинафталин-3, 6 -дисульфокислота Тимолфталексон Хромовый темно-синий 1.5—2,5 12,0—12,2 9.5—10,0 Красная Светло-серая Синевато-си- Пурпурно-ро- зовая Синяя Розово-крас- 2п" +, ТН[c.605]
Хромовый синий 2К (из 4-хлор-2-аминофенола и Аш-кислоты) — в кра-сновато-фиолетовый, Хромовый темно-синий (из той же диазосоставляющей и хромотроповой кислоты) — в красный. Более глубокий цвет последнего красителя после хромирования, по сравнению с Хромовым синий 2К, является, по-видимому, следствием участия в комплексообразовании красителя в хинонгидразонной форме [c.271]
Хромовый темно-синий для меха Хромрвый зеленый для меха [c.346]
К числу о,о -диоксиазокрасителей относятся Хромовый синий 2К и Хромовый темно-синий — из 4-хлор-2-аминофенола и соответственно Ы-ацетил-Аш-кислоты и хромотроповой кислоты [c.298]
chem21.info
Реактивы и их приготовление. — МегаЛекции
· Дистиллированная вода и проверка ее качества. Рекомендуется пользоваться водой, полученной в стеклянном дистилляторе, или Н-катионированной. Качество дистиллированной воды испытывают следующим образом: к 100 мл дистиллята добавляют 1 мл аммиачного буферного, раствора и 5-7 капель индикатора кислотного хром темно-синего (хромоген черного). Голубая с сиреневым оттенком окраска раствора указывает на частицу воды.
· Раствор трилона Е. Для приготовления его берут следующие количества: для 0,1н. - 18,6 г; для 0,5 н. - 9,3 г; для 0,01 н. -1,86 г. Отведенное количество трилона Б растворяют в дистиллированной воде и фильтруют, если раствор мутный. Объем раствора доводят до 1 л.
Точную нормальность 0,1 н. (децинормального) раствора трилона Б устанавливают с помощью 0,01 н. (сантинормального) раствора сернокислого магния. Отвешивают на аналитических весах 1,232 г перекристаллизованного химически чистого MgSO4 × 7h3O и растворяют, в мерной колбе на 1 л дистиллята. В коническую колбу отмеривают пипеткой 100 мл 0,01 н. раствора сульфита магния, добавляют 5 мл аммиачного буферного раствора, 5-7 капель индикатора кислотного хром темно-синего и медленно титруют при интенсивном перемешивании 0,1 н. раствором трилона Б до перехода красной окраски в синюю.
При установке титров раствора трилона Б 0,05; 0,01 нормальности берут соответственно 50 и 10 мл 0,01 н. раствора сульфата магния и доводят дистиллированной водой до 100 мл.
Поправочный коэффициент раствора трилона Б к данной нормальности вычисляют по формуле:
Kтр=10КМg/g,
где КМg - поправочный коэффициент 0,01 н. раствора сульфата магния (коэффициент сантинормальности) при точно 0,01 н. Раствора KМg=1;
g- расход трилона Б на титрование, мл.
· Буферный раствор: 20 г хлористого аммония (химически чистого) растворяют в дистиллированной воде, добавляют 100 мл 20%-го раствора аммиака и объем раствора доводят до 1 л дистиллированной водой.
· Растворы индикаторов (хромоген черный, кислотный хром темно-синий): 0,5 г одного из индикаторов растворяют в 20 мл аммиачнoго буферного раствора. Объем раствора доводят до 100 мл этиловым спиртом. Раствор хромоген чёрного ЕТ-00 следует готовить на срок, не превышающий 10 суток.
Подготовка пробы воды. При анализе воды с жесткостью 0,5 мг×экв/кг и менее объем пробы составляет 100 мл. При жесткости воды 0,5 мг×экв/кг и более объем пробы берут не 100 мл, а 50 или 25 мл, разбавляют дистиллированной водой до 100 мл, обеспечивая содержание солей жесткости в пробе менее 0,5 мг×экв/кг. Воду, имеющую температуру ниже 10-12оС, перед титрованием следует подогревать.
Порядок анализа. К 100 мл соответственно подготовленной для титрования воды добавляют 5 мл аммиачного буферного раствора и 5-7 капель индикатора эриохрома черного или кислотного хром темно-" синего. После этого медленно титруют воду из бюретки раствором трилона Б требуемой концентрации в зависимости от предполагаемой жесткости. При титровании необходимо обеспечить интенсивное перемешивание раствора. Титрование проводят до перехода окраски раствора от розово-красного до синевато-сиреневого цвета, что соответствует эквивалентной точке связывания всех катионов кальция и магния. Окраска раствора от избытка трилона Б остается неизменной, поэтому в конце титрования рабочий раствор трилона Б следует прибавлять по каплям.
Расчет результатов анализа. Расчет результатов анализа основан на том, что каждый 1 мл нормального раствора трилона Б оттитровывает 1 мг×экв жесткости. Соответственно этому 1 мл децинормального (0,1 н.) раствора трилона Б оттитровывают 0,1 мг×экв жесткости, а 1 мл сантинормального (0.1 н.) раствора оттитровывают 0,01 мг×экв жесткости.
Следовательно, общая жесткость определяется по формуле
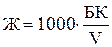 , (3)
, (3)
где Ж - общая жесткость воды, мг×экв/кг;
Б - расход трилона Б на титрование, мл;
К - коэффициент нормальности раствора трилона Б;
V - объем пробы воды, взятый для анализа без учета конденсата для разбавления пробы, мл;
1000 - для пересчета миллилитров в литры.
При Ж = 100 мл и К = 0,01 Ж =0,1 Б мг×экв/кг. Для воды с общей жесткостью менее 0,5 мг×экв/кг её величину принято выражать в микрограмм-эквивалентах на литр (килограмм). В этом случае при К - 0,01 Ж - 100 Б мкг×экв/кг.
Определение некарбонатной жесткости
Некарбонатную жесткость определяют по разности между общей и карбонатной жесткостью:
Жн = Ж - Жк. (4)
Определение окисляемости
Данные, получаемые при определении окисляемости воды, позволяют судить о количестве кислорода, необходимого для окисления органических соединений, находящихся в воде, способных окисляться марганцовокислым калием; полнота окисления зависит от состава органических соединений, концентрации KMnO4 и условий испытания. Поэтому для получения сравнимых результатов, характеризующих относительную степень загрязнения воды органическими веществами, необходимо соблюдение постоянных условий определения.
Пробу исследуемой воды в количестве 100 мл с помощью пипетки помещают в коническую колбу. Прибавляют 5 мл серной кислоты (1:3) и 10 мл 0,01 н. раствора перманганата калия и кипятят в течение 10 мин.
По окончании кипячения к горячему раствору приливают 10 мл 0,01 н. раствора щавелевой кислоты, избыток которой оттитровывают 0,01 н. раствором перманганата калия до появления слабо-розового окрашивания.
Для расчета окисляемости, выражаемой в миллиграммах кислорода на 1 л воды, пользуются формулой:
Х = (а + в) – С × 0,08 × 10, (5)
где Х - количество кислорода, мг/л;
а - количество 0,01 н. раствора перманганата, прилитое к воде для окисления органических примесей, мл,
в - количество 0,01 н. раствора перманганата, пошедшее на титрование избытка щавелевой кислоты, мл;
С - количество 0,01 н. раствора щавелевой кислоты, мл;
0,08 количество кислорода, соответствующее 1 мл 0,01 н, раствора перманганата калия, мг;
10 - коэффициент для выражения полученных результатов в миллиграммах на литр.
megalektsii.ru
Фотометрическое определения кальция кислотным хром темно-синим
Фотометрический метод определения кальцпя с кислотным хром темно-синим применяется при анализе цементных сырьевых смесей и клинкеров [50, 51]. Метод предложен для определения больших количеств кальция (40—45% СаО). При этом большую часть кальция связывают в бесцветный комплекс с комплексоном III, а оставшийся кальций ( 6%) определяют по цветной реакции с кислотным хром темно-синим. [c.100] Кислотный хром темно-синий применен также для фотометрического определения кальция в биологических объектах [655, 748, 1657], чугуне [1316], металлическом титане [987]. Используется также для косвенного фотометрического определения кальция эриохром черный Т [1351, 1546, 1663]. [c.100]Реактивы, используемые в качестве индикаторов при комплексонометрическом титровании кальция, находят все большее применение при прямом фотометрическом определении последнего. Часто для этого применяют мурексид [86, 101—103], кислотный хром синий К [104], кислотный хром темно-синий [105] и др. [c.148]
Описано последовательное определение кальция и магния в одной порции раствора фотометрическим титрованием раствором комплексона III с индикатором кислотным хром темно-синим [523]. Кальций и магний предварительно отделяют от Ре, А1, Mg, окиси кремния и щелочных металлов осаждением. в виде СаСОз и Mg (ОН), при pH 13 в присутствии триэтаноламина. [c.48]
Для косвенного фотометрического определения кальция используют кислотный хром темно-синий [50, 51, 655, 748, 987, 1109, 1316, 1379, 1657]. Реагент хорошо растворим в воде. Водные растворы кислотного хром темно-синего окрашены в вишневокрасный цвет, в щелочной среде — в синевато-сиреневый. [c.99]
Как видно из рис. 20, наибольшая разность в поглощении комплекса наблюдается при 600 нм [50]. Фотометрируют при 595 нм [50, 51] по уменьшению интенсивности окраски кислотного хром темно-синего. Окраска развивается сразу же после сливания растворов и устойчива в течение 90 мин. 655, 1316]. Чувствительность реакции 1,4-10" г мл раствора [50]. Закон Бера для растворов комплексного соединения кальция с кислотным хром темно-синим не соблюдается (оптическая плотность уменьшается с увеличением концентрации кальция) [50]. Повышение pH приводит к уменьшению чувствительности (рис. 21). Оптимальное количество щелочи —5-мл 10%-ного раствора Ка0н/100.Л4Л [50]. При фотометрическом определении кальция используют 0,02%-ный водный раствор кислотного хром темно-синего [50, 51]. Водные растворы реагента устойчивы несколько недель [50]. Определению [c.99]
chem21.info