Большая Энциклопедия Нефти и Газа. Хрома кристаллическая решетка
Типы кристаллических решёток — урок. Химия, 8–9 класс.
Большинство твёрдых веществ имеет кристаллическое строение, которое характеризуется строго определённым расположением частиц. Если соединить частицы условными линиями, то получится пространственный каркас, называемый кристаллической решёткой. Точки, в которых размещены частицы кристалла, называют узлами решётки. В узлах воображаемой решётки могут находиться атомы, ионы или молекулы.
В зависимости от природы частиц, расположенных в узлах, и характера связи между ними различают четыре типа кристаллических решёток: ионную, металлическую, атомную и молекулярную.
Ионными называют решётки, в узлах которых находятся ионы.
Их образуют вещества с ионной связью. В узлах такой решётки располагаются положительные и отрицательные ионы, связанные между собой электростатическим взаимодействием.
Ионные кристаллические решётки имеют соли, щёлочи, оксиды активных металлов. Ионы могут быть простые или сложные. Например, в узлах кристаллической решётки хлорида натрия находятся простые ионы натрия Na+ и хлора Cl−, а в узлах решётки сульфата калия чередуются простые ионы калия K+ и сложные сульфат-ионы SO42−.
Связи между ионами в таких кристаллах прочные. Поэтому ионные вещества твёрдые, тугоплавкие, нелетучие. Такие вещества хорошо растворяются в воде.

Кристаллическая решётка хлорида натрия

Кристалл хлорида натрия
Металлическими называют решётки, которые состоят из положительных ионов и атомов металла и свободных электронов.
Их образуют вещества с металлической связью. В узлах металлической решётки находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы, отдавая свои внешние электроны в общее пользование).
Такие кристаллические решётки характерны для простых веществ металлов и сплавов.
Температуры плавления металлов могут быть разными (от \(–37\) °С у ртути до двух-трёх тысяч градусов). Но все металлы имеют характерный металлический блеск, ковкость, пластичность, хорошо проводят электрический ток и тепло.

Металлическая кристаллическая решётка

Металлические изделия
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, соединённые ковалентными связями.
Такой тип решётки имеет алмаз — одно из аллотропных видоизменений углерода. К веществам с атомной кристаллической решёткой относятся графит, кремний, бор и германий, а также сложные вещества, например, карборунд SiC и кремнезём, кварц, горный хрусталь, песок, в состав которых входит оксид кремния(\(IV\)) SiO2.
Таким веществам характерны высокая прочность и твёрдость. Так, алмаз является самым твёрдым природным веществом. У веществ с атомной кристаллической решёткой очень высокие температуры плавления и кипения. Например, температура плавления кремнезёма — \(1728\) °С, а у графита она выше — \(4000\) °С. Атомные кристаллы практически нерастворимы.

Кристаллическая решётка алмаза

Алмаз
Молекулярными называют решётки, в узлах которых находятся молекулы, связанные слабым межмолекулярным взаимодействием.
Несмотря на то, что внутри молекул атомы соединены очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому молекулярные кристаллы имеют небольшую прочность и твёрдость, низкие температуры плавления и кипения. Многие молекулярные вещества при комнатной температуре представляют собой жидкости и газы. Такие вещества летучи. Например, кристаллические иод и твёрдый оксид углерода(\(IV\)) («сухой лёд») испаряются, не переходя в жидкое состояние. Некоторые молекулярные вещества имеют запах.
Такой тип решётки имеют простые вещества в твёрдом агрегатном состоянии: благородные газы с одноатомными молекулами (He,Ne,Ar,Kr,Xe,Rn), а также неметаллы с двух- и многоатомными молекулами (h3,O2,N2,Cl2,I2,O3,P4,S8).
Молекулярную кристаллическую решётку имеют также вещества с ковалентными полярными связями: вода — лёд, твёрдые аммиак, кислоты, оксиды неметаллов. Большинство органических соединений тоже представляют собой молекулярные кристаллы (нафталин, сахар, глюкоза).

Кристаллическая решётка углекислого газа

«Сухой лёд»

Кристаллики иода
Если известно строение вещества, то можно предсказать его свойства.
Попробуем определить, каковы примерно температуры плавления у фторида натрия, фтороводорода и фтора.
У фторида натрия — ионная кристаллическая решётка. Значит, его температура плавления будет высокой. Фтороводород и фтор имеют молекулярные кристаллические решётки. Поэтому их температуры плавления будут невысокими. Молекулы фтороводорода полярные, а фтора — неполярные. Значит, межмолекулярное взаимодействие у фтороводорода будет сильнее, и его температура плавления будет выше по сравнению со фтором.
Экспериментальные данные подтверждают эти предположения: температуры плавления NaF, HF и F2 составляют соответственно \(995\) °С, \(–83\) °С, \(–220\) °С.
Источники:
Габриелян О. С. Химия. 8 класс. Учебник для общеобразовательных учреждений. М.: Дрофа, 2013. — 133 с.
www.yaklass.ru
Кристаллическое строение металлов. Кристаллическая решетка металлов
Одним из самых распространенных материалов, с которым всегда предпочитали работать люди, был металл. В каждую эпоху предпочтение отдавалось разным видам этих удивительных веществ. Так, IV-III тысячелетия до нашей эры считаются веком хальколита, или медным. Позже его сменяет бронзовый, а затем в силу вступает тот, что и по сей день является актуальным - железный.
Сегодня вообще сложно представить, что когда-то можно было обходиться без металлических изделий, ведь практически все, начиная от предметов быта, медицинских инструментов и заканчивая тяжелой и легкой техникой, состоит из этого материала или включает в свой состав отдельные части из него. Почему же металлы сумели завоевать такую популярность? В чем проявляются особенности и как это заложено в их строении, попробуем разобраться далее.
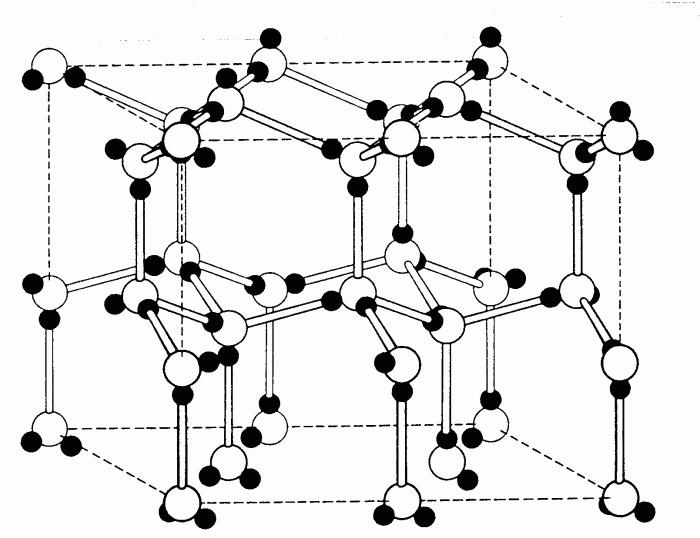
Общее понятие о металлах
"Химия. 9 класс" - это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
- кальций;
- натрий;
- титан;
- железо;
- магний;
- алюминий;
- калий.
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.

Свойства металлов
К специфическим свойствам рассматриваемых веществ относят следующие.
- Металлический блеск. Все представители простых веществ им обладают, причем большинство одинаковым серебристо-белым цветом. Лишь некоторые (золото, медь, сплавы) отличаются.
- Ковкость и пластичность - способность деформироваться и восстанавливаться достаточно легко. У разных представителей выражена в неодинаковой мере.
- Электропроводность и теплопроводность - одно из основных свойств, которое определяет области применения металла и его сплавов.
Кристаллическое строение металлов и сплавов объясняет причину каждого из обозначенных свойств и говорит о выраженности их у каждого конкретного представителя. Если знать особенности такого строения, то можно влиять на свойства образца и подстраивать его под нужные параметры, что и делают люди уже многие десятилетия.

Атомно-кристаллическое строение металлов
В чем же заключается такое строение, чем характеризуется? Само название говорит о том, что все металлы представляют собой кристаллы в твердом состоянии, то есть при обычных условиях (кроме ртути, которая является жидкостью). А что такое кристалл?
Это условное графическое изображение, построенное путем пересечения воображаемых линий через атомы, которые выстраивают тело. Другими словами, каждый металл состоит из атомов. Они располагаются в нем не хаотично, а очень правильно и последовательно. Так вот, если мысленно соединить все эти частицы в одну структуру, то получится красивое изображение в виде правильного геометрического тела какой-либо формы.
Это и принято называть кристаллической решеткой металла. Она очень сложная и пространственно объемная, поэтому для упрощения показывают не всю ее, а лишь часть, элементарную ячейку. Совокупность таких ячеек, собранная вместе и отраженная в трехмерном пространстве, и образует кристаллические решетки. Химия, физика и металловедение - это науки, которые занимаются изучением особенностей строения таких структур.
Сама элементарная ячейка - это набор атомов, которые располагаются на определенном расстоянии друг от друга и координируют вокруг себя строго фиксированное число других частиц. Она характеризуется плотностью упаковки, расстоянием между составными структурами, координационным числом. В целом все эти параметры являются характеристикой и всего кристалла, а значит, отражают и проявляемые металлом свойства.
Существует несколько разновидностей кристаллических решеток. Объединяет их все одна особенность - в узлах находятся атомы, а внутри располагается облако электронного газа, которое формируется путем свободного передвижения электронов внутри кристалла.
Типы кристаллических решеток
Четырнадцать вариантов строения решетки принято объединять в три основных типа. Они следующие:
- Объемно-центрированная кубическая.
- Гексагональная плотноупакованная.
- Гранецентрированная кубическая.
Кристаллическое строение металлов было изучено только благодаря электронной микроскопии, когда стало возможным получать большие увеличения изображений. А классификацию типов решеток впервые привел французский ученый Браве, по фамилии которого их иногда называют.

Объемно-центрированная решетка
Строение кристаллической решетки металлов данного типа представляет собой следующую структуру. Это куб, в узлах которого находится восемь атомов. Еще один располагается в центре свободного внутреннего пространства ячейки, что и объясняет название "объемно-центрированная".
Это один из вариантов наиболее простого строения элементарной ячейки, а значит, и всей решетки в целом. Такой тип имеют следующие металлы:
- молибден;
- ванадий;
- хром;
- марганец;
- альфа-железо;
- бетта-железо и другие.
Основные свойства таких представителей - высокая степень ковкости и пластичности, твердость и прочность.
Гранецентрированная решетка
Кристаллическое строение металлов, имеющих гранецентрированную кубическую решетку, представляет собой следующую структуру. Это куб, который включает в свой состав четырнадцать атомов. Восемь из них формируют узлы решетки, а еще шесть расположены по одному на каждой грани.
Подобную структуру имеют:
- алюминий;
- никель;
- свинец;
- гамма-железо;
- медь.
Основные отличительные свойства - блеск разного цвета, легкость, прочность, ковкость, повышенная устойчивость к коррозии.

Гексагональная решетка
Кристаллическое строение металлов, обладающих данным типом решетки, следующее. В основе элементарной ячейки лежит шестигранная призма. В ее узлах располагается 12 атомов, еще два по основаниям и три атома свободно лежат внутри пространства в центре структуры. Всего семнадцать атомов.
Подобную сложную конфигурацию имеют такие металлы, как:
- альфа-титан;
- магний;
- альфа-кобальт;
- цинк.
Основные свойства - высокая степень прочности, сильный серебристый блеск.
Дефекты кристаллического строения металлов
Однако все рассмотренные типы ячеек могут иметь и естественные недостатки, или так называемые дефекты. Это может быть связано с разными причинами: посторонними атомами и примесями в металлах, внешними воздействиями и прочим.
Поэтому существует классификация, отражающая дефекты, которые могут иметь кристаллические решетки. Химия как наука изучает каждый из них с целью выявления причины и способа устранения, чтобы свойства материала не были изменены. Итак, дефекты следующие.
- Точечные. Они бывают трех основных видов: вакансии, примеси или дислоцированные атомы. Приводят к ухудшению магнитных свойств металла, электро- и теплопроводности его.
- Линейные, или дислокационные. Выделяют краевые и винтовые. Ухудшают прочность и качество материала.
- Поверхностные дефекты. Влияют на внешний вид и структуру металлов.
В настоящее время разработаны методики устранения дефектов и получения чистых кристаллов. Однако совсем искоренить их не удается, идеальной кристаллической решетки не существует.

Значение знаний о кристаллическом строении металлов
Из вышеизложенного материала очевидно, что знания о тонкой структуре и строении позволяют спрогнозировать свойства материала и повлиять на них. И это позволяет делать наука химия. 9 класс общеобразовательной школы делает в процессе обучения упор на то, чтобы сформировать у учащихся четкое понятие о важном значении основополагающей логической цепочки: состав - строение - свойства - применение.
Сведения о кристаллическом строении металлов очень четко иллюстрирует эту зависимость и позволяет учителю наглядно объяснить и показать детям, насколько важно знать тонкую структуру, чтобы правильно и грамотно использовать все свойства.
fb.ru
Кристаллический хромом - Справочник химика 21
Подобную же группу составляют, например, гексафториды серы, молибдена и урана. В каждой из этих групп увеличение молекулярного веса соединения связано с возрастанием энтропии. На рис. П1,5 подобное же сопоставление дано для энтропии (Sr) некоторых групп окислов металлов в кристаллическом состоянии. Здесь наблюдаются такие же закономерности, как и для энтропии газов. Отчетливо выделяется группа, линий моноокисей магния, кальция и бария,группа линий полуторных окислов алюминия, хрома и лантана и группа пятиокисей ниобия и тантала. В каждую из таких групп входят также не показанные на рисунке линии других однотипных с ними соединений. [c.101] Карбиды представляют собой кристаллические тугоплавкие вещества очень большой твердости. Так, карбиды вольфрама почти не уступают по твердости алмазу. Свойства карбидов хрома, молибдена и вольфрама приведены в табл. 23. [c.287]Некоторые из предложенных объяснений склонности ферритных нержавеющих сталей к межкристаллитной коррозии основаны на разнице скоростей растворения различных образующихся карбидов или на предполагаемой большей реакционной способности напряженной кристаллической решетки металла. Однако наиболее убедительное объяснение получено с помощью теории, широко используемой для объяснения этих явлений в аустенитных нержавеющих сталях. Согласно этой теории, разрушения происходят вследствие обеднения границ зерен хромом [36—38]. Различия в температурах и времени, необходимых для сенсибилизации этих сталей, объясняются более высокими скоростями диффузии углерода, азота и хрома в ферритной объемно-центрированной кубической решетке по сравнению с аустенитной гранецентрированной. В соответствии с этим, карбиды и нитриды хрома, которые растворены при высокой температуре, ниже [c.310]
Блестящие, твердые осадки хрома, получаемые в этих условиях, очень пористы и имеют сетку трещин. Растрескивание осадка происходит за счет больших внутренних напряжений, которые возникают при уменьшении объема осадка (сжатие) вследствие перехода неустойчивой гексагональной кристаллической решетки металла в более устойчивую кубическую объемно-центрированную решетку. [c.420]
В сплавах внедрения атомы растворенного вещества образуют дополнительные связи с соседними атомами по сравнению с чистым растворителем, а это приводит к тому, что кристаллическая решетка сплава становится тверже, прочнее и менее пластичной. Например, железо, содержащее менее 3% углерода, намного тверже чистого железа и приобретает значительно большую прочность на растяжение, а также другие ценные физические свойства. Так называемые мягкие (малоуглеродистые) стали содержат менее 0,2% углерода они обладают высокой пластичностью и ковкостью и используются для изготовления кабелей, гвоздей и цепей. Средние (углеродистые) стали содержат 0,2-0,6% углерода, они жестче мягких сталей и используются для изготовления балок и рельсов. Высокоуглеродистые стали, применяемые для изготовления нож-нгщ, режущих инструментов и пружин, содержат 0,6-1,5% углерода. При введении в стали других элементов получают различные легированные стали. Одним из наиболее известных сплавов такого типа является нержавеющая сталь, содержащая 0,4% углерода, 18% хрома и 1% никеля. Сплавы типа твердых растворов отличаются от обычных химических соединений тем, что имеют произвольный, а не постоянный состав. Отношение содержания неметаллических элементов к металлическим может варьировать в них в широких пределах, что позволяет придавать этим материалам самые разнообразные физические и химические свойства. [c.364]
Лиганды, находящиеся в левой части спектрохимического ряда, называются лигандами слабого поля или просто слабыми лигандами. Те лиганды, которые находятся в правой части спектрохимического ряда, называются лигандами сильного поля или сильными лигандами. На рис. 23.27 схематически показано, что происходит с энергией расщепления кристаллическим полем при изменении лигандов в ряду нескольких комплексов хрома(Ш). (Здесь уместно напомнить, что при последовательной ионизации атома переходного металла первыми отрываются валентные -электроны. Поэтому атом хрома имеет электронную конфигурацию [Аг] 45 3 , а ион Сг имеет конфигурацию [Аг] 3 .) Отметим, что с усилением поля, действующего на ион металла со стороны шести окружающих лигандов, расщепление энергетических уровней -орбита-лей металла усиливается. Поскольку спектр поглощения связан с этим энергетическим расщеплением, окраска комплексов неодинакова. [c.394]
Приборы и реактивы. Водяная баня. Штатив. Стеклянные палочки. Платиновая проволочка. Фарфоровая палочка. Борная кислота. Бура. Магний (лента или порошок). Нитрат кобальта кристаллический, порошок. Сульфат хрома. Лакмус (нейтральный раствор). Универсальный индикатор. Бумага лакмусовая синяя. Метиловый спирт. Глицерин. Растворы серной кислоты (плотность 1,84 г/см ), нитрата серебра (0,1 н.), сульфата меди (0,5 н.), сульфата алюминия (0,5 н.), [c.182]
Координационное число металла при образовании ОЦК решетки равно восьми. Такая решетка, как уже говорилось, свойственна, например, металлическому натрию, железу при температуре до 911 °С. Атом натрия имеет один электрон на внешней электронной оболочке, с помощью которого он образует металлическую связь с другими атомами. В то же время остальные его валентные орбитали являются вакантными. Избыток числа орбиталей над числом электронов приводит к образованию такой структуры, когда каждый атом натрия создает у себя устойчивую восьми-электронную оболочку благородных газов, отстоящих как слева (N6), так и справа (Аг) от натрия в периодической системе. Это достигается при количестве ближайших атомов в кристаллической решетке (координационном числе) равном восьми. Аналогично, атом хрома в основном [c.320]
Ионы хрома и алюминия не мешает реакции. Другие ионы, например Си + и Со +, способны образовывать с белым кристаллическим соединением Zп[Hg(S N)4] смешанные кристаллы, придавая последним характерную окраску. Способность к образованию окрашенных смешанных кристаллов может быть использована для обнаружения как ионов цинка, так и ионов меди и кобальта. [c.268]
Продвижение анионов через пленку менее вероятно, чем продвижение катионов, обладающих значительно меньшими размерами. Для прохождения ионов через кристаллическую решетку оксидов при комнатной температуре необходим градиент потенциала порядка 10 В/см. В то же время скачок потенциала при пассивации многих металлов обычно составляет 0,5—1,5 В. Следовательно, толщина пленки не должна превышать 5—15 10" см. При этом металлы, например железо, никель, хром, в пассивном состоянии продолжают медленно растворяться, а толщина пленки стабилизируется. По мере утолщения пленки все в большей степени затрудняется продвижение через нее ионов. Соответственно, если сохранить неизменной плотность тока, произойдет сдвиг анодного потенциала в [c.368]
Оксид хрома (VI) СгОз — твердое кристаллическое вещество темно-красного цвета, хорошо растворимое в воде. Путем непосредственного взаимодействия элементов его получить нельзя. [c.276]
Установлено, что при прокаливании цинкхромового катализатора в токе водорода и токе воздуха изменяется его химический и фазовый состав. Окись хрома при повышении температуры имеет тенденцию соединяться с окисью цинка, образуя при этом сначала аморфные, а затем кристаллические соединения ZnO-СгЮз и Zn raOa. При более высокой температуре 2пО-СггОз, по-видимому, переходит в кристаллический хромит цинка (шпинель). [c.173]
Металлический хром получен Девиллем (вероятно, с содержанием углерода) при восстановлении углем окиси хрома при температуре, близкой к плавлению платины имеет стальной цвет, уд. вес 5,9 и весьма большую твердость (хорошо полируется), растворяется в соляной кислоте, но холодная разведенная серная и азотная кислоты на него не действуют. Бунзен получил металлический хром, разлагая раствор Сг2С1 гальваническим током, в виде чешуек серого цвета (уд. вес 7,3). Вёлер получил кристаллический хром, накаливая смесь безводного Сг С с измельченным цинком и хлористым калием до температуры кипения цинка. После охлаждения цинк растворяется в разбавленной азотной кислоте, причем остается серый кристаллический хром (уд. вес 6,81). Фреми приготовил также кристаллический хром, действуя парами натрия на безводный Сг С1 в струе водорода кристаллы металлического хрома имели черный цвет, кубическую форму, значительную твердость и сопротивлялись действию кислот. Глат-цель (1890) получил кристаллический порошок Сг при накаливании двойной соли КСгС1 с магнием, уд. веса 6,7 такой хром в кислотах легко растворялся с выделением водорода. Таким образом, повидимому, является явное разноречие между показаниями разных исследователей, что объяснилось, как указано далее, только в недавнее время. Муассан (1893), при [c.238]
Оксид хрома (И ) СГ2О3 — темно-зеленый порошок, а в кристаллическом состоянии — черный с металлическим блеском. Структура СГ2О3 соответствует октаэдро-тетраэдрической координации атомов (структура типа a-A Oj, см. рис. 72). Оксид хрома (HI) тугоплавок (т. пл. 2265 С), химически инертен. В воде, кислотах и щелочах не растворяется. Его амфотерная природа проявляется при сплавлении с соответствующими соединениями. Так, при сплавлении СГ2О3 с дисульфатом калия образуется сульфат хрома (HI) [c.558]
Схема импульсного рубинового лазера показана на рис. 5.2, а. Лазер состоит из рубинового стержня 1, импульсной лампы-вспышки 2, электрода поджигав и двух источников питания системы поджига и лампы вспыщки 5. Уровни энергии встроенных в решетку оксида алюминия (А12О3) примесных атомов хрома (Сг +) с концентрацией 0,05% показаны на рис. 5.2, б. При активации импульсом света лампы-вспышки (накачке) электроны переходят из основного состояния 1 на полосу 2, а с этой полосы за очень короткое время в результате взаимодействия с кристаллической решеткой переходят на узкий нижележащий уровень 3. [c.98]
Особый интерес представляют условия образования твердых растворов замещения, в которых железо играет роль растворителя. И. И. Корнилов установил связь между растворимостью элементов в железе и их ионными диаметрами атомный диаметр растворимого элемента должен отличаться от атомного диамет)ра железа не более чем на 8—15%. Только при этих условиях не происходит значительной деформации кристаллической решетки растворителя и изменения характера связи. Если это ра.зличие не превышает 8%, то образуются непрерывные твердые растворы если различие составляет 8—15%, то образуются ограниченные твердые растворы. Так, например, хром, с атомным диаметром, отличающимся от железа не более чем на 1,5%, дает с ним непрерывный ряд твердых растворов молибден, отличающийся от железа по атомному диаметру на 10%, ограниченно растворяется в железе еще меньше растворяется вольфрам и т. д. Отмеченные закономерности в отношении растворимости элементов в железе распространяются и на некоторые другие элементы. [c.123]
Железо м хром образуют непрерывный ряд твердых раствором. а-железо п хром имеют одинаковый тип кристаллической решетки оот.емноцеитрированного куба с близкими параметрами решетки, 0,26 и 0,278 нм. Хром стабилизирует -область и сужает область существования у-железа. [c.208]
Графиты широко используются в смазках в качестве наполнителей и антифрикционных присадок. Естественный графит представляет собой минерал, состоящий из самородного углерода встречается он в В1ще пластинок и сплошных масс. Содержание графита й промышленных рудах колеблется в больших пределах. В числе примесей могут содержаться пирит, слюда, хромит. Выпускаются графиты карандашный, кристаллический (серебристый), графит П, элементный и скрытокристаллический (аморфный). При изготовлении смазок применяется только графит П — порошок серо-стального цвета (ГОСТ 8295—57), концентрат, полученный обогащением графитовой руды. Выпускается двух марок А и Б. В зависимости от месторождений установлены следующие обозначения выпускаемых марок ПБ-А — бото-гольский марки А ПБ-Б ботогольский марки Б ПЗ-А — завальевский марки А и ПЗ-Б завальевский марки Б ПТ-А и ПТ-Б — тайгинский марок А и Б. В продукте должны содержаться (в мае. %) [c.688]
Сульфида. Известны многочисленные сульфиды хрома, молибдена и вольфрама. Практически наиболее важным из них является дисульфид молибдена Мо5о. Его кристаллическая решетка гексагональной структуры кристаллы легко скалываются по плоскостям спайности. Дисульфид молибдена применяется как смазочный материал для поверхностей скольжения, работающих с большой нагрузкой при высоких температурах. При нагревании в отсутствие воздуха разлагается, а иа воздухе горит разлагается кислотами с выделением сероводорода. [c.286]
Карбид вольфрама С, почти не уступаюпщй по твер,дости алмазу, используется для получения металлоксра.мических пластинок для режущего инструмента—резцов, фрез, сверл, способных обрабатывать самые твердые материалы. Для 1зготовления этих пластинок служит материал, состоящий из карбида вольфрама в виде тонкого кристаллического порошка, распределенного в кобальте. Твердосплавный инструмент изготовляют также электро-дуговой наплавкой, используя карбиды вольфрама, молибдена и хрома. [c.289]
Окисная железохромовая система представляет в исходном (невосстановленном) состоянии непрерывный ряд твердых растворов СгаОз в а-РбаОз [144]. Активность железохромовых катализаторов связана с образованием твердого раствора Рез04—СгаОд шпинельного типа замечет замещения трехвалентных ионов железа в кристаллической решетке Гед04 трехвалентными ионами хрома. Избыток окиси хрома, присутствующей в катализаторе в виде свободной фазы, снижает активность катализатора. [c.191]
Предполагают, что окислы образуют твердые растворы СггОз в Рез04 шпинельного типа. Ионы Ре + в кристаллической решетке Рез04 замещаются на Сг +. При этом избыток окиси хрома присутствует в виде свободной фазы и снижает активность катализатора [68]. Активной частью катализатора является магнетит РезО . В первоначальный же состав массы.входит а-РегОз — кристаллическая окись железа ромбоэдрической структуры. Для превращения а-РеаОз в активный магнетит катализатор восстанавливают газовой смесью, содержащей СО и На- Восстаийвление обычно производят в цехах-потребителях катализатора, Процесс идет при [c.121]
Следует отметить некоторые физические особенности водорода, оппеде-ляющие дополнительные, специфические требования к конструкционным материалам. Водород обладает способностью проникать через толщу материала, в частности металлов, и с повышением давления и температуры диффузия водорода в металлы возрастает. Глубина проникания молекул водорода в кристаллическую решетку металла в большинстве случаев не превышает 4—6 мм, а при нагартовке материала может быть снижена до 2,0—1,5 мм. Для алюминия она достигает 15—30 мм, а при нагартовке снижается до 4—6 мм. Водородная диффузия в сталях практически полностью устраняется путем легирования с помощью хрома, молибдена, вольфрама и других элементов. [c.181]
Соли серной кислоты — сульфаты — находят разнообразное применение. Особенно интересны двойные сульфаты — квасцы (например, K[A1(S04)2]). Кристаллы квасцов построены так, что один из металлов (трехвалентные хром, алюминий, железо) образует вместе с кислотным отстатком комплексный анион [Me(S04)2] , занимающий определенное место в кристаллической решетке. При растворении в воде квасцы диссоциируют на одно- и трехвалентные катионы и суль-фат-анионы, т. е. ведут себя как растворы смеси сульфатов [c.117]
Необходимы механически свойства металлов и сплавов достигаются введением в расплав легирующих добавок. Добавки стабилизируют кристаллическую фазу зерна, образуют твердые растворы с основным компонентом расплава и способствуют образованию новой дисперсной фазы. Появление твердых растворов между зернами структуры может увеличить ее пластические свойства. Упрочняющее действие возникающих дисперсных фаз при введении легирующих добавок можно проиллюстрировать образованием в хромоникелевых сплавах при добавлении титана и алюминия кристалликов NisTi и NisAl, которые сильно взаимодействуют с твердым раствором сплава. Высокое содержание никеля и хрома в стали обеспечивает получение устойчивой аустенитной кристаллической структуры зерен (у-фаза), обладающей наибольшей жаропрочностью. [c.387]
Соответствующий перекрытый комплекс порфирии—Ре(1П) затем восстанавливался бисацетилацетонатом двухвалентного хрома в бензоле до кристаллического ферропорфирина, который обратимо связывается с кислородом в растворе при комнатной [c.362]
После охлаждения реакционной смеси в нее вливают 120 мл воды и вновь охлаждают. Выделившуюся нитробензойную кислоту отфильтровывают на воронке Бюхнера, промьшают водой. Для удаления солей хрома сырую нитробензойную кислоту растворяют в 5%-ном растворе едкого натра осадок гидроокиси хрома отфильтровывают и к фильтрату, содержащему натриевую соль п-нитробензой-ной кислоты, добавляют при перемешивании концентрированную серную кислоту до кислой реакции по конго. При этом выпадает желтый кристаллический осадок п-нитробензойной кислоты, который отфильтровывают и тщательно промывают водой. [c.143]
В раствор, полученный растворением 100 г нитрата хрома(1П) Сг(Ы0з)з-9Н20 в 100 смЗ НгО, приливают 100 см 38%-ной НС1 и пропускают при охлаждении льдом сильную струю НС1 до прекращения выделения [Сг(Н20)б]С1з. Кристаллическую ка-щицеобразную массу быстра отсасывают на больщом нутч-фильтре с пластинкой из пористого стекла, промывают небольшим количеством дымящей НС1, растворяют в 100 см воды и снова при охлаждении льдом осаждают газообразным HG1. По окончании осаждения находящийся над кристаллами зеленоватый раствор сливают и путем трехкратного смешивания с ацетоном отмывают серо-синий осадок от основного количества захваченной им H I и зеленого хлорида, которые затем окончательно удаляют на нутч-фильтре с пластинкой из пористого стекла промыванием небольшими количествами ацетона. Промывание заканчивают после того, как фильтрат становится бесцветным. Ацетон удаляют промыванием абсолютным эфиром. В эксикаторе над h3SO4 соль освобождают от эфира и следов влаги. [c.529]
Опыт 6. Окислителыше свойства соединений хрома (VI). Внести в пробирку" 3—4 капли раствора бихромата калия, 4—5 капель разбавленной серной кислоты, кристаллический сульфит натрия на кончике микрошпателя. Встряхнуть содержимое пробирки до растворения соли. Наблюдать изменение окраски раствора от оранжевой до зеленой. Составить уравнение реакции [c.98]
Положение переходной области на оси потенциалов зависит от многих факторов и, в частности, от ориентации кристаллических граней на поверхности электрода. Поэтому при заданном потенциале могут достигаться условия пассивации одних граней, тогда как другие продолжают активно растворяться. Это играет важную роль в истолковании природы некоторых видов коррозии. Аналогично этому каждая структурная составляющая сплава также характеризуется своей парциальной потенциостатической кривой. На рис. 195 представлены парциальные потенциостатические кривые компонентов нержавеющей стали, содержащей 18% хрома, 8% никеля и не большую примесь углерода. При застывании этой стали по границам зерен выпадают карбиды хрома СгазСя и Сг,Сз, далее следует узкая зона обедненного углеродом раствора и, наконец, среднюю часть зерна образует твердый раствор, в котором содержание компонентов отвечает среднему составу сплава. Если потенциал электрода поддерживается в переходной области, то, как видно из рис. 195, наиболее быстрому растворению подвергается зона обедненного углеродом металла. При потенциалах в области перепассивации происходит более интенсивное растворение карбидов хрома. При этом сталь подвергается межкристаллитной коррозии. [c.366]
Гидратная изомерия комплексов хрома. Хлорид хрома СгС1з-6Н20 в кристаллическом состоянии образует несколько изомеров, различающихся числом молекул воды и хлорид-ионов, расположенных во внешней и внутренней сферах комплексной частицы. Свойства изомеров, в том числе и окраска, заметно различаются [c.409]
chem21.info
Элементарная кристаллическая решетка - Большая Энциклопедия Нефти и Газа, статья, страница 2
Элементарная кристаллическая решетка
Cтраница 2
Центрами кристаллизации могут быть группы элементарных кристаллических решеток, неметаллические включения и тугоплавкие примеси. [16]
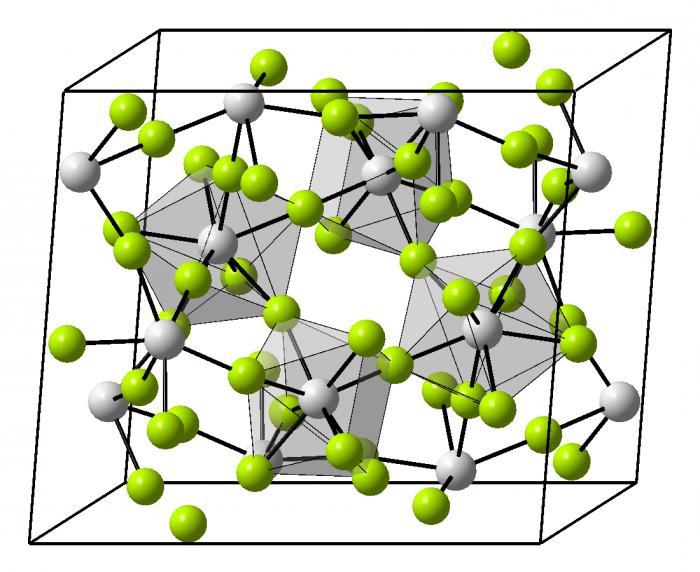
На рис. 22, а показана элементарная кристаллическая решетка твердого раствора замещения хрома в железе. Отдельные узлы в кристаллической решетке а-железа заняты ионами хрома. Ионы обоих металлов располагаются в узлах кристаллической решетки произвольно. [18]
На рис. 20, а показана элементарная кристаллическая решетка твердого раствора замещения хрома в железе. Отдельные узлы в кристаллической решетке а-железа заняты ионами хрома. Ионы обоих металлов располагаются в узлах кристаллической решетки в произвольном порядке. [20]
На рис. 31 изображены основные типы элементарных кристаллических решеток. [21]
На рис. 1 - 8 а показана элементарная кристаллическая решетка твердого раствора замещения хрома в железе. Отдельные узлы решетки железа замещены ионами хрома. Ионы обоих металлов располагаются в узлах кристаллической решетки в произвольном порядке, со средней статистической равномерностью. [23]
Образование полных кристаллов, которые состоят из одинаково ориентированных элементарных кристаллических решеток, происходит редко. [24]
Атомы ( ионы, молекулы), составляющие элементарную кристаллическую решетку, находятся в состоянии химического взаимодействия, образуя тот или иной тип связи. [25]
Моноарсенид гафния имеет гексагональную структуру типа TiP с параметрами элементарной кристаллической решетки: а 3 764, с 12 680 А, наименьшие расстояния между атомами в элементарной ячейке: Hf - Hf 3 40, Hf - As 2 62 и As - As 3 76 А. [26]
На рис. 1.1 показано расположение атомов ( ионов) в элементарных кристаллических решетках трех типов: кубической объемно-центрированной, кубической гранецентрированной и гексагональной. [27]
Концентрация, отвечающая нижней границе смешиваемости, может быть различной для разных систем, так как она зависит от степени сложности элементарной кристаллической решетки, от соотношения адсорбционных сил различных ионов и их концентраций в растворе. Увеличение концентрации сопряженного иона ( например, SOi - в системе КМпО4 - BaSO4 - Н2О) понижает нижнюю границу смешиваемости. Как показали качественные опыты по сокристаллизации BaSO4 с КМпО4, добавление посторонних ионов ( А13, Fe3, K и Н) повышает нижнюю границу смешиваемости. [28]
Во втором случае в связи с весьма незначительной взаимной растворимостью обеих фаз скррость комплексообразования близка к нулю и образование комплекса ограничивается зарождением на поверхности раздела фаз элементарной кристаллической решетки. Происходящая в это время на поверхности раздела фаз адсорбция молекул ингибиторов комплексообразования сокращает и без того чрезвычайно малую поверхность контакта двух фаз, величина которой во многом определяет скорость комплексообразования. И только в случае контакта без перемешивания углеводородной фазы и спиртового ( или спирто-водного с большой концентрацией спирта) раствора карбамида образуется комплекс, что объясняется относительно высокой взаимной растворимостью этих двух фаз и нейтрализующим действием спирта по отношению к ингибиторам комплексообразования. [29]
Образование реальных кристаллических структур не происходит без дефектов и отклонений от идеализированных структур, показанных на рис. 1.5 и 1.6. Дефекты носят точечный и линейный характер. Точечные дефекты присущи элементарным кристаллическим решеткам и весьма разнообразны. Наиболее часто встречающиеся точечные дефекты показаны на рис. 1.7 [1.2]: а - пустой узел или вакансия; б - междоузельный атом; в - вакансия и междо-узельный атом; г - примесный атом. Имеют место искажения и геометрической формы кристаллической решетки, вызванные спецификой технологии производства металлов. [30]
Страницы: 1 2 3
www.ngpedia.ru
Хром, окись структура - Справочник химика 21
Дегидроциклизацией изооктана при 550° С над молибден-хромовым катализатором получают ксилолы [289], но над окисью хрома получаются олефины [264]. Необходимо отметить протекающую здесь промежуточную изомеризацию [291]. При дегидроциклизации диизобутил- и диизоамил- [279, 284, 285] -декана, пентакозана [276] и керосина [286] образуются ароматические углеводороды. Бутилбензол дает нафталин [279] смесь 1- и 2-ок-тена превращается в о-ксилол ароматические углеводороды получаются при дегидроциклизации компактных олефиновых структур, таких как 2-этил-1-бутен и З-метил-2-пентен. Во всех вышеприведенных превращениях углеводороды, кипящие ниже исходного сырья, не образуются до тех нор, пока преобладают мягкие условия процесса [279]. [c.103] Метод дифференциального термического анализа (д. т. а.) уже более трех десятилетий широко применяется для выяснения структуры глины и других минералов. Д. т. а. как метод систематического изучения твердых катализаторов не получил широкого распространения. Можно указать всего лишь несколько работ по данному вопросу [1—6]. В настоящей работе сообщается о результатах дифференциального термического анализа ряда твердых катализаторов, а именно окиси хрома, окиси железа и бинарной системы окись хрома — окись железа. Была сделана попытка согласовать данные д. т. а. с рентгенографическими данными и величинами удельной поверхности, а также с некоторыми литературными данными по активности изученных в этой работе катализаторов. [c.135]Дисперсная структура катализатора окись хрома —окись цинка. Магнитная восприимчивость кат-ров различного способа приготовления. [c.202]
Формирование дисперсной структуры активного компонента на поверхности носителя описывается эмпирическим уравнением, справедливым для некоторых систем активный компонент — носитель [1, 2] (сюда относятся платина на окиси алюминия, окись хрома на окиси алюминия и алюмосиликата и некоторые другие системы) [c.116]
Брегг [51] установил, что плотная упаковка встречается редко. Вещества с одинаковым типом структурной решетки отличаются, главным образом, плотностью упаковки. Например, окись цинка и окись бериллия одинаковы по структуре, т. е. имеют кристаллы типа вурцита, но имеют резкие различия в упаковке. Именно, окись цинка имеет плотность упаковки 44%, а окись бериллия 64%,. Одинаковая плотность упаковки (58%) была найдена у окисей магния, никеля, кобальта, железа, марганца, кадмия, кальция, стронция и бария (все с типом решетки хлористого натри-я), и у окисей церия, празеодима, урана и лития (с типом решетки флюорита) 55%. Самая высокая плотность упаковки окисям алюминия, хрома, ванадия, бериллия и родия, а также полуторной окиси железа и титана. [c.58]
Соединения вольфрама, хрома, молибдена и ванадия, псевдоморфные с соединениями, применяемыми для приготовления катализаторов, например моноклинные иглы пара-вольфрамата аммония, обрабатывают сероводородом в течение 48 часов при 300 в течение 24 часов при 350 48 часов при 410° получающийся дисульфид вольфрама серого цвета с металлическим блеском имеет ту же игольчатую кристаллическую структуру, что и вольфрамат аммония последний после обработки аналогичным образом дает кристаллическую окись в виде сине-черных игл обработка окиси молибдена водородом в течение 15 часов при 230° дает псевдоморфную окись молибдена все эти катализаторы пригодны для процессов крекинга [c.319]
Очень широко, как уже указывалось ранее, используются в данном случае сложные катализаторы, в состав которых входит окись хрома. При этом многочисленными исследованиями, главным образом Баландина с сотрудниками, установлено, что кроме алюмо-хромовых катализаторов высокими дегидрирующими свойствами обладают также медно-хромовые контакты, предварительно восстановленные водородом. Согласно данным рентгеноструктурного анализа, медно-хромовый катализатор обладает кристаллической структурой и линии его рентгеновского спектра принадлежат решеткам металлической меди и окиси хрома при этом грань (111) решетки меди полностью укладывается на слой кислородных атомов окиси хрома [137]. Дегидрирующее влияние медно-хромового катализатора исследовалось в широком ряду алкилбензолов и алкилфенолов. Найдено, что при нормальном давлении и температуре 650° С выход стирола в присутствии медно-хромового контакта доходит до 40% на пропущенный и около 60% на разложенный этилбензол (скорость пропускания этилбензола 450 г на 1 л катализатора в час). В качестве побочных продуктов получалось 7% толуола и 4% бензола имело место также некоторое разложение на газы (метан, этан, этилен) и углеотложение [1381. При снижении парциального давления этилбензола разбавлением углекислым газом (этилбензол С02 =1 2 (мол.)) выход стирола на пропущенный этилбензол и селективность [c.166]
Поскольку среди названных катализаторов большей активностью обладали содержащие окись хрома, исследования велись в направлении разработки методики приготовления их наиболее активных структур. В результате был разработан катализатор Н-2, который и применялся в опытах по синтезу 2-метилтиофена. [c.29]
Образующаяся окись хрома способствует развитию внутренней поверхности активного компонента и повышению термической устойчивости катализатора. Пористая структура полученного по хроматному методу никель-хромового катализатора, по данным работы / 7, характеризуется величиной внутренней поверхности , равной 160 м /г, общей пористостью 11% и средним радиусом пор 90 А. [c.23]
В самое последнее время было опубликовано обширное исследование Шваба и Блока [115] относительно окисления СО на NiO и ZnO. Эти авторы также варьировали дефектную структуру окислов, но для NiO их данные противоречат результатам, полученным Парравано [113], поскольку они нашли, что увеличение концентрации положительных дырок (добавкой лития) снижает энергию активации, в то время как уменьшение п (добавлением хрома) увеличивает энергию активации. Шваб и Блок исследовали реакцию в другом температурном интервале (250—400° С), чем Парравано (100—280° С), но есть основания считать, что в обоих случаях лимитирующей стадией было поглощение СО. Согласно описанному выше механизму, подобный парадокс может быть обусловлен тем, что на окислах р-типа окись углерода способна хемосорбироваться как обратимо, так и необратимо (рис. 15). В опытах Парра- [c.530]
В системе окись цинка — окись хрома, так же как и в системе окись цинка — кремнезем , в которой не образуется никаких промежуточных аморфных фаз, Яндер наблюдал эти различные стадии реакции. Образование виллемита, с его характерной кристаллической структурой, было установлено с помощью рентгеновского анализа. Сначала кремнезем существует в очень неупорядоченном состоянии и служит сильным катализатором реакции N2O 4-Нг = N2-1-HjO (фиг. 744), Механически от- [c.706]
Ответ. Окись углерода имеет электронную структуру С = 0 , поэтому каждая молекула окиси углерода может служить двухэлектронным донором по отношению к атому Ре или N1. Никель имеет 28 электронов — на восемь меньше, чем у криптона, имеющего 36 электронов. Железо имеет 26 электронов, т. е. на 10 меньше, чем у криптона. Таким образом, никель имеет набор из четырех свободных орбиталей и образует N (00)4, а железо имеет пять свободных орбиталей и образует Ре (СО) 5. Отметим, что для хрома с 24 электронами можно было бы ожидать образования карбонила Сг(СО)е. Это и наблюдается в действительности. Аналогично марганец (25 электронов) образует Мп(СО)5. Почему [c.259]
Он обнаружил, что некоторые изученные полимеры, полученные полимеризацией мономера под действием продуктов реакции триалкилалюминия с хлоридом титана (катализатора Циглера, названного по имени открывшего его К. Циглера) или под действием трехокиси хрома, нанесенной на окись алюминия, имеют значительно более регулярную структуру, чем другие полимеры полипропилена. Дальнейшие исследования [c.86]
Помимо сплошности первоначально образующегося слоя окислов на защитные свойства окисных пленок оказывают влияние и другие факторы. Большое значение имеет соответствие между кристаллическими структурами образующихся окислов и металла. Чем больше различия между этими структурами, тем большие напряжения возникают в соприкасающихся кристаллических решетках металла и окисла. Накопление в растущей пленке остаточных внутренних напряжений приводит к механическому ее разрушению (вспучиванию, отслаиванию, растрескиванию). Когда объем окислов намного больше объема окислившегося металла (Уок> ме), в окисной пленке возникают напряжения сжатия. У вольфрама, имеющего соотношение ок Уме=3,35, условие получения сплошной пленки окислов выполняется. Однако большая разница в объемах окисла Оз и металла обусловливает возникновение значительных внутренних напряжений. В результате окисная пленка на вольфраме получается очень хрупкой, со слабыми защитными свойствами. Предпосылкой высоких защитных свойств пленки является малая электропроводность образующихся окислов. Большая стойкость алюминия к окислению кислородом объясняется низким значением электропроводности АЬОз, которая при 1000°С равна 10 " Ом Х Хсм- . При относительно высокой электропроводности окислов возможно образование пленок с хорошими защитными свойствами в связи с решающим влиянием других факторов. Например, удельная электропроводность СггОз больше, чем у N 0, почти в 10 раз, в то же время защитные свойства у окислов хрома выше, чем у окислов никеля. [c.28]
Окись хрома, окись олова (вместо сернокислого хрома следует употреблять нитрат хрома) 23102 СГаОд-N320 + Н О (цеолитовая структура) 180 см силиката натрия (щелочность 0,3955 ЛГ), содержащего 0,03 г двуокиси кремния в 1 сл , нагревают с 60 см 4,8085 N едкого натра до 70°, к которым постепенно [c.166]
Механическое полирование представляет собой процесс, принципиально мало отличающийся от шлифования и, по существу, является дальнейшим сглаживанием неровностей на поверхности металла более тонким абразивным материалом.. Полирование производят на сукне, фетре или бархате до полного удаления рисок, остающихся от шлифования. Во время полирования на полировальный материал непрерывно или периодически наносят суспензию воды с тонкоразмельченными абразивными веществами (окись алюминия, окись железа, окись хрома, окись магния и др.). При полировании мягких металлов (алюминий, магний, олово и их сплавы) на тонкую шлифовальную бумагу наносят слой парафина или раствор парафина в керосине. Механический способ полирования достаточно прост, поэтому широко распространен, однако имеет свои недостатки [46] трудность и длительность, значительный расход полировочного сукна, появление на шлифовальной поверхности (так же как и при шлифовании) деформированного наклепанного слоя, искажающего истинную структуру металла. Последнее нежелательно при микроэлектрохимических исследованиях, при испытании металлов на устойчивость к коррозионному растрескиванию и коррозионноусталостную прочность, при которых увеличение внутренних напряжений в поверхностных слоях металла может отразиться на результатах испытаний. Для удаления внутренних напряжений, связанных с шлифованием и механическим полированием, применяют термообработку, например отпуск при определенной температуре [49], ° С [c.53]
Важным этапом в развитии синтеза спиртов из СО и На была разработка Ъп—Си- и Ъп—Сг-катализаторов, в присутствии которых селективно образуется метанол [200—221]. До недавнего времени синтез метанола в промышленности в основном осуществляли на гп-Сг-катализаторах при 350—400° С, давлении 250— 320 атм и объемной скорости 10 ООО—60 ООО час циркулирующего газа, содержащего 10—20% СО (СО На от 1 5 до 1 10). Часто синтез метанола совмещают с процессами деструктивной гидрогенизации и синтезом аммиака, что улучшает его технико-экономические показатели [203, 211—213]. Активность Zn—Сг-катализатора зависит от способа приготовления [214, 215], атомного отношения г/Zn [214], а также от способа предварительной обработки, в процессе которой происходит формирование активной структуры. Свежеприготовленный гп—Сг-катализатор содержит в основном фазу цинкгидроксихромата lpZn2(0H)2 r04 [214, 216, 217]. В начале восстановления синтез-газом, водородом или азот-водородной смесью при низкой температуре кристаллическая решетка хромата цинка разрушается и образуются окись хрома, окись цинка и хромит цинка частично в виде аморфной, а частично в виде высоко дисперсной кристаллической фазы [218— [c.23]
Анализ этих данных обнаруживает некоторые неожиданные различия по сравнению со структурой, установле11Ной для системы окись хрома — окись алюминия. Закон Кюри — Вейса описывает эти данные должным образом только примерно до 6% никеля, а выше этой концентрации отклонения столь существенны, что становится бесполезной всякая попытка рассчитать момент или константу Вейса. [c.426]
Сравнение значений й для наблюденных линий с соответствующими значениями для гидроокиси хрома со структурой байерита, алюминиевого байерита и бемита показало, что байе-ритная фаза в геле, содержащем 28,4 мол. % СтоОг, является почти чистым гидратом окиси алюминия, тогда как бемитная фаза в образце с 18,4 мол. % СггОз содержит окись хрома в виде твердого раствора. [c.185]
Рассмотрим окись хрома, СГ2О3. В объеме твердой СГ2О3 катионы Сг " , октаэдрически окруженные шестью анионами (структура алунда), физически идентичны центральным катионам октаэдрических Сг " -комплексов в растворе. Но на поверхности кристалла могут появляться ионы хрома с различными зарядами и координационным числом, образующиеся путем следующего механизма. [c.25]
Примером зеркальных изомеров являются комплексы хрома (П1), содержащие две молекулы этиленднамина. Координацион ное число Сг+ равно 6 лиганды располагаются по верщинам ок- таэдра, в центре которого находится ион Сг+ Молекула этилеН диамина, имеющая изогнутую форму, присоединяется к Сг+ двумя группами ЫНа (как уже указывалось, она занимает дйа координационных места). При наличии в октаэдрическом комплексе двух молекул этиленднамина возможны два варианта структуры, показанные на рис. 1.58 эти формы относятся друг к другу, как предмет к своему зеркальному изображению. [c.119]
Предполагают, что окислы образуют твердые растворы СггОз в Рез04 шпинельного типа. Ионы Ре + в кристаллической решетке Рез04 замещаются на Сг +. При этом избыток окиси хрома присутствует в виде свободной фазы и снижает активность катализатора [68]. Активной частью катализатора является магнетит РезО . В первоначальный же состав массы.входит а-РегОз — кристаллическая окись железа ромбоэдрической структуры. Для превращения а-РеаОз в активный магнетит катализатор восстанавливают газовой смесью, содержащей СО и На- Восстаийвление обычно производят в цехах-потребителях катализатора, Процесс идет при [c.121]
Для нейтрализации кислотных центров поверхности, а следовательно, для предотвращения нежелательных побочных реакций, в алюмохромовые катализаторы вводят соли щелочных и щелочноземельных металлов. В промышленных катализаторах наиболее часто используют окиси калия, натрия, бериллия. Наиболее подробно изучено влияние добавок калия, действие которого сводится к стабилизации структуры хрома в катализаторе. Предполагают [3, с. 35), что калий в структуре алюмохромового катализатора находится в виде или алюмината АЮОК (восстановительная среда) или хромата К2СГО4 (окислительная среда). Ион К , связанный в форме — ОК, мигрирует от иона Сг к иону находясь в динамическом равновесии, зависящем от окислительно-восстановительных условий среды [c.136]
Рентгенографическим анализом установлено, что образцы однофазны, предс,тавляют собой твердые растворы хромита магния с магнетитом и имеют структуру шпинели. Хромит магния имеет параметр кристаллической решетки а=8.317 кх, а образцы, полученные из шихт, содержащих окись железа, имели более высокие значения параметра (табл. 1). Зависимость параметра кристаллической решетки твердых растворов от содержания магнетита показывает, что в исследуемой области выполняется закон Вегарда, что согласуется с данными работы. [c.102]
Удельная поверхность окиси хрома снижается с увеличением температуры термообработки. Начальная удельная поверхность дегидратированной, например при 370 К, окиси сильно зависит от условий приготовления и обычно колеблется в интервале 80—300 м /г. Данные Дерена и др. [61] и Каррозерса и др. [58] показывают, что удельная поверхность гелей, дегидратированных нагреванием на воздухе, относительно слабо зависит от температуры, если она превышает приблизительно 770 К, и составляет 10—30 м2/г. Однако, если дегидратация ведется в инертном газе, заметная зависимость удельной поверхности от температуры наблюдается вплоть до примерно 970 К. Окись хрома с высокой удельной поверхностью, более 200 м2/г, конечно, имеет микропористую структуру с порами эквивалентным диаметром менее 2 нм после рекристаллизации до а-СггОз микропоры исчезают. По данным [62], гель окиси хрома, полученный с использованием гидролиза мочевины и обезгаженный при температуре ниже 470 К, характеризуется однородными порами весьма малого диаметра и проявляет мо-лекулярно-ситовые свойства. [c.65]
Сохранение неравновесности структуры наблюдается и для КИСЛ0В. Так, окись цинка — активный катализатор синтеза метанола — быстро теряет активность в результате рекристаллиза-дии. Промотором может быть окись хрома (2пО СггОз = 2 1). При совместном осаждении гидратов окисей или карбонатов динка и хрома и последующем прогреве при 400° полученный катализатор является аморфным. В результате нагревания до 600° на рентгенограммах катализатора появляются диффракци-онные линии окиси данка и каталитическая активность исчезает. Даже небольшое добавление окиси хрома (2пО СггОз = 20 1) препятствует росту кристаллов окиси цинка при 400°. Нагревание окиси цинка при этой температуре в течение 15 часов дает увеличение среднего размера кристаллов от 250 до 350 А, тогда как в присутствии окиси хрома размер кристаллов окиси цинка увеличивается со 130 до 170 А. [c.221]
Однако в 1932 г. Лазиер и Воген нашли, что окись хрома такя е способна дегидрировать циклогексан, хотя ее кристаллическая решетка не имеет требуемой для секстетной модели структуры. А. А. Баландин и И. И. Брусов подробно исследовали дегидрогенизацию циклогексана на окиси хрома и при-П1ЛИ к заключению, что в данном случае дегидрогенизация про- [c.139]
Процесс приготовления катализаторов обычно состоит из нескольких стадий. Сначала получают основное вещество, которое можно превратить в катализатор. Например, окись Х1рома, применяющаяся для детндрирования углеводородов, может быть приготовлена разлггчными способами. По одному из рецептов к раствору азотнокислого хрома (Сг(КОз)) добавляют аммиак. Выпадающая гидроокись хрома (Сг(ОН)з) разлагается с образованием окиси СггОз. Большое значение при получении активного катализатора имеют условия, в которых образуются исходные вещества, в данном случае гидроокись хрома. Физико-химические факторы (температура, концентрация растворов, степень кислотности среды и т. д.) также могут оказывать сильное влияние на свойства и структуру образующихся соединений. Например, гидроокиси металлов осаждают из растворов солей, добавляя в них щелочь. Не безразлично, какой катион содержится в щелочи ведь следы его могут остаться в гидроокиси и засорить катализатор. Повтому чаще всего используют аммиак, который образует в растворах легко удаляющийся ион аммония. [c.61]
Попытаемся оценить все материалы с хорошо развитой пористой поверхностью для разделения перманентных газов вне зависимости от их природы и происхождения. Так, активированный уголь или графитированная сажа [10—14], силикагель [11, 15, 16], алюмосиликагель [17], окись алюминия [18], природные или синтетические цеолиты [18—25], различные активированные окислы, подобные трехвалентному окислу хрома или трехвалентной окиси железа [26], могут служить примером неорганических адсорбентов. В настоящее время с большим успехом используются для этих целей синтетические макропористые органические полимеры типа иорапаков и полисорбов [25, 27—32]. Было также описано разделение перманентных газов методом газо-жидкостной хроматографии 33—35]. Без сомнения, любые другие материалы с хорошо развитой пористой структурой должны давать прекрасные результаты нри разделении перманентных и подобных газов. [c.269]
Примеров структурообразующего промотирования, изученных так же хорошо, как только что рассмотренный, мало. Однако та же окись алюминия является промотором по отношению к никелю, кремнезему, окиси тория, окиси хрома СГ2О3. Можно сказать, что вообще трудновосстановимые окислы, вводимые, в восстанавливаемую окись, стабилизируют структуру образующегося металла. [c.179]
Окись хрома(П1). n Og— вещество зеленого цвета со структурой корунда (стр. 286, ч. 2). Оно образуется при горении металла з кислороде, при термическом разложении окислов Сг - или бихромата аммония, а также при обжиге водной окиси r.jOg-nHjO. Последняя (часто называемая гидроокисью хрома, хотя содержание воды в сй не постоянно) выделяется в виде осадка при добавлении щелочи к растворам солей Сг . Сильно прокаленная окись хрома инертна по отношению к кислотам и основаниям, но в обычных условиях она, так же как ее гидратированная форма, представляет собой амфотерное соединение, легко растворимое в кислотах с образованием акво-понов [Сг(Н20) 1"+ и в концентрированных щелочах с образованием хромитов. Вещества, присутствующие в раство-)ах хромитов, точно не идентифицированы, но, вероятно, это Сг(0Н)с1 и [Сг (ОН)з (Н 0)1 . Из таких растворов можно выделить кристаллические соединения состава М Сг(ОН)з+,Дгг=3—5), а также аналогичные соли щелочноземельных металлов. [c.233]
Из рисунка видно, что введение в сталь 5—8% Сг повышает ока-линостойкость до 700 —750° С, 15—17% Сг — до 950—ЮС0° С, а 25% Сг — до 1100° С. При этом следует иметь в виду, что окали-ностойкость зависит только от состава стали и не зависит от ее структуры. Окалиностойкость аустенитной и ферритной стали при равном содержании хрома практически одинакова (см. рис. 41). [c.93]
По данным [88], в алюмо-хромовых катализаторах, получаемых пропиткой у-А120з, окись хрома находится в виде а-Сг Оз, имеющей корундовую структуру, которая образуется при нагревании СгОз в присутствии кислорода воздуха. При прокаливании в токе воздуха при 500° С а-СгаОд может образовать с 7 А1.Рз твердый раствор, если общее содержание окиси хрома в катализаторе поряд- [c.34]
chem21.info