Таблица валентностей химических элементов. Валентность хрома
Валентность хрома (Cr), формулы и примеры
Общие сведения о валентности хрома
Хром в виде простого вещества – серовато-белый блестящий металл. Имеет структуру объемно-центрированной кубической решетки.Плотность – 7,2 г/см3. Температуры плавления и кипения равны 1890oС и 2680oС, соответственно.
Валентность хрома в соединениях
Хром находится в четвертом периоде в VIB группе Периодической таблицы Д.И. Менделеева. Порядковый номер равен 24. В ядре атома хрома содержится 24 протона и 28 нейтронов (массовое число равно 52). В атоме хрома есть четыре энергетических уровня, на которых находятся 24 электрона (рис. 1).
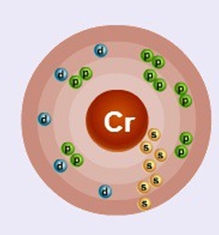
Рис. 1. Строения атома хрома.
Электронная формула атома хрома в основном состоянии имеет следующий вид:
1s22s22p63s23p63d54s1.
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
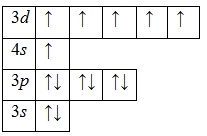
Наличие шести неспаренных электронов свидетельствует о том, что хром в своих соединениях может проявлять валентность IV (CrVIO3, CrVICl6, CrIVO2Cl6, K2CrVI2O7 и т.д.).
Известно, что для хрома также характерны валентности II (CrIIO, CrII(OH)2, CrIICl2) и III(CrIII2O3, CrIII(OH)3, KCrIIIO2, CrIIICl3).
Примеры решения задач

| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Валентность - хром - Большая Энциклопедия Нефти и Газа, статья, страница 1
Валентность - хром
Cтраница 1
Валентность хрома изменяется при этой реакции от шести до трех, значит, каждый его атом приобретает 3 электрона. Но в молекуле бихромата содержится 2 атома хрома и превращение К2Сг2О7 в Сг2 ( 5О4) з связано с приобретением 6 электронов. [1]
Валентность хрома изменяется при этой реакции от шести до трех, значит каждый его атом приобретает 3 электрона. Но в молекуле бихромата содержится 2 атома хрома и превращение К2Сг2О7 в Cr2 ( SO4) 3 связано с приобретением б электронов. [2]
Валентность хрома изменяется при этой реакции от шести до трех, значит, каждый его атом приобретает 3 электрона. Но в молекуле бихромата содержится 2 атома хрома и превращение К2Сг3О7 в Cr2 ( SO4) 3 связано с приобретением 6 электронов. [3]
Валентность хрома изменяется при этой реакции от шести до трех, значит, каждый его атом приобретает 3 электрона. Но в молекуле бихромата содержится 2 атома хрома и превращение К2Сг2О, в Cr2 ( SO4) 3 связано с приобретением 6 электронов. [4]
Определим валентность хрома в соединении состава: 68 вес. [5]
Так как валентность хрома изменяется при этой реакции от шести до трех, значит каждый его атом приобретает 3 электрона. Но в молекуле бихромата содержится 2 атома хрома и превращение КаСг2О7 в Cr2 ( SO4) 3 связано с приобретением 6 электронов. [6]
Таким образом, валентность хрома в обеих надкислотах различна. Соли первой из них обычно окрашены в синий, соли второй - в красный цвет. [7]
Таким образом, валентность хрома в обеих надкислотах оказывается различной. [8]
Таким образом, валентность хрома в обеих надкнслотах различна. Соли первой из них обычно имеют сипи, соли второй - красный цвет. [9]
В процессе работы и регенерации валентность хрома может изменяться. Часть хрома после регенерации присутствует в форме СЮ, и ее можно экстрагировать водой. Хотя вероятность контакта воды с регенерированным катализатором крайне мала, возможность такого изменения валентности следует все же иметь в виду. [10]
Рассмотрим теперь реакции, при которых валентность хрома изменяется. [11]
Если не принимать во внимание изменение валентности хрома, гидроксилированная поверхность его окиси, по крайней мере формально, сходна с рассмотренной в предыдущем разделе поверхностью окиси алюминия. Процессы дегидроксилиро-вания и гидроксилирования, образования и разрушения кислотных и основных поверхностных центров различных типов для этих двух систем аналогичны. [12]
Третий путь состоит 8 изыскании возможности применения растворов с изкой валентностью хрома, обеспечивающих к тому же высокий выход по току. В работах зарубежных исследователей ( Япония) описаны опыты, проведенные на полузаводской ванне по декоративному хромированию из растворов солей трехвалентного хрома и мочевины, облегчающей восстановление храма на катоде. [13]
Так как заряды комплекса, построенного в соотношениях 1: 2, являются анионными валентностями хрома и сульфогрупп, то комплекс и волокно, повидимому, связываются друг с другом солевыми связями хрома и сульфогрупп с аминогруппами волокна. [14]
Существенное отличие окиси хрома как катализатора полимеризации олефинов от других окислов металлов заключается в том, что валентность хрома должна быть максимальной. В процессе полимеризации хром полностью восстанавливается до трехвалентного. Катализаторы в виде окиси хрома, также как и катализаторы на основе окиси молибдена и вольфрама, промотируются добавками металлорга-нических соединений. [15]
Страницы: 1 2
www.ngpedia.ru
Валентность - хром - Большая Энциклопедия Нефти и Газа, статья, страница 2
Валентность - хром
Cтраница 2
Эта реакция имеет место, если кислород расходуется на окисление какого-либо вещества; происходящее при этом изменение валентности хрома обусловливает переход оранжевой окраски раствора в зеленую. Промежуточными продуктами при этом, по-видимому, являются кислые сложные эфиры хромовой кислоты. [16]
Эта реакция имеет место, если кислород расходуется на окисление какого-либо вещества; происходящее при этом изменение валентности хрома обусловливает переход оранжевой окраски раствора в зеленую. [17]
У хрома как элемента побочной подгруппы в образовании химических связей принимают участие d - электроны предвнеш-него слоя, и предсказать заранее валентность хрома, как это делалось, например, для алюминия или для других элементов главных подгрупп, в данном случае нельзя. [18]
При изучении возможности электрохимического осаждения хрома из жидких шлаков и определении растворимости его окислов, нами были получены данные, позволяющие оценивать валентность хрома непосредственно в расплавах. [19]
Один из окислов хрома содержит 30 38 % кислорода. Соответствует ли валентность хрома в этом соединении его положению в периодической системе. [20]
По своим свойствам все полученные соединения вполне сходны с подобными соединениями алюминия. Это сходство выражается и в валентности хрома. [21]
Существенное отличие окиси хрома как катализатора полимеризации олефинов от других окислов металлов заключается в том, что валентность хрома в исходном катализаторе должна быть максимальной. Было показано [60, 61], что в этих системах ограничение роста молекулярной цепи происходит путем передачи цепи на мономер и спонтанного переноса. [22]
У атомов хрома и молибдена происходит провал одного s - электрона с внешнего электронного слоя в предвнешний. Однако соединения, в которых Сг и Мо были бы одновалентны, неизвестны. Минимальная валентность хрома, молибдена и вольфрама отвечает возбуждению внешних s - электронов и равна двум, как и у всех d - элементов. [23]
У атомов хрома и молибдена происходит провал одного s - электрона с внешнего слоя на предвнешний. Однако соединения, в которых Сг и Мо были бы одновалентны, неизвестны. Минимальная валентность хрома, молибдена и вольфрама отвечает возбуждению внешних s - электронов и равна двум. [24]
Ионы свинца, бария и серебра образуют малорастворимые хроматы, и содержащийся в них хром ( VI) не определяется. Хром ( III) и другие мешающие ионы осаждают сульфатом аммония с фосфатным буферным раствором и удаляют фильтрованием. Окислители, которые могут изменить валентность хрома, удаляют путем добавления сульфита натрия. Избыток сульфита затем окисляют гипохлоритом натрия. Гипохлорит и любые образующиеся хлорами-ны разрушают кислым раствором хлорида натрия, а образующийся хлор удаляют воздухом. Несмотря на такую предварительную подготовку, в пробах некоторых городских и промышленных сточных вод наблюдаются потери хрома ( VI) через несколько часов. Поэтому такие пробы следует анализировать как можно быстрее после отбора. [25]
Данные по распределению хрома, вязкости, рентгеноструктурному н петрографическому анализам застывших шлаков позволили ряду авторов предположить существование и шлаках двухвалентного хрома. Кербер и Эльсен [1], а также Хнтрик [2] сделали попытку подтвердить это химическим анализом кислых шлаков. Наоборот, в отношении основных шлаков оценки валентности хрома с помощью идеального закона действующих масс приводят к противоречивым результатам. Однако Времер [9] показал, что его экспериментальные результаты хороню описываются константой равновесия с образованием двухвалентного хрома. Ольшанский [10], определяя вес и бруттосостав фаз, установил, что даже в системе О - СаО - СгЮз возникают расплавы, богатые низшими окислами хрома. По-видимому, при оценке соотношения двух - и трехвалентного хрома недостаточно учитывать только основность шлака. В значительно мере соотношение Сг И и Сг11 определяется степенью окисленности шлака и составом контактирующего с ним металла. Последнее подтверждается рядом работ [ И, 12 ] по изучению продуктов окисления желозохромистых сплавов. К сожалению, перечисленные выводы сделаны на основании химического анализа застывших шлаков, в которых соотношение Сг11 и Сг111 может изменяться в процессе затвердевания. [26]
Другой метод регулирования времени гелеобразования, а отсюда и глубины проникновения геля в пласт заключается в двухступенчатое реакции сшивки. Наибольшее развитие получила система, содержащая полимер - сшивающий поливалентный катион и окислительно-восстановительный агент. Образование геля задерживается до тех пор, пок окислительно-восстановительная реакция не снизит в пласте валентность хрома до трех, далее медленно протекающий лигандный обмен приводит к сшивке полимера. [27]
Уэллер ( S. W. Weller, Houdry Process Corporation): Предварительная обработка часто существенна не только с точки зрения каталитической активности, но и для изменения действительного химического состава поверхности, а следовательно, и электронной конфигурации, приписываемой металлическим ионам. Например, в случае Сг2О3 предварительная обработка кислородом при повышенных температурах приводит к прочному покрытию поверхности адсорбированным 02, и в действительности валентность поверхностных ионов хрома превышает три. Предварительная обработка водородом аналогично приводит к значительному покрытию поверхности адсорбированным Н2 и к эффективному снижению валентности хрома, вероятно до двух. [28]
Страницы: 1 2
www.ngpedia.ru
Таблица валентностей химических элементов. Таблица валентности. Стандартные, редкие, исключения. Версия для печати.Считается, что валентность химических элементов определяется группой (колонкой) Периодической таблицы . Действительно, теоретически, это самая распространенная валентность для элемента, но на практике поведение химических элементов значительно сложнее. Причина множественности значений валентности заключается в том, что существуют различные способы (или варианты) заполнения, при которых электронные оболочки стабилизируются. Поэтому, предлагаем Вашему вниманию таблицу валентностей химических элементов. Числовое значение положительной валентности элемента равно числу отданных атомом электронов, а отрицательной валентности – числу электронов, которые атом должен присоединить для завершения внешнего энергетического уровня. В неорганической химии обычно применяется понятие степень окисления, а в органической химии — валентность, так как многие из неорганических веществ имеют немолекулярное строение, а органических — молекулярное..
|
www.dpva.ru
| ПОЛЕЗНЫЕ ССЫЛКИ: БОНУСЫ ИНЖЕНЕРАМ!: МЫ В СОЦ.СЕТЯХ: | Навигация по справочнику TehTab.ru:  главная страница / / Техническая информация / / Химический справочник / / Таблица валентностей химических элементов. главная страница / / Техническая информация / / Химический справочник / / Таблица валентностей химических элементов.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
tehtab.ru
Шестивалентный хром - это... Что такое Шестивалентный хром?

Шестивалентный хром — химический элемент хром в степени окисления +6. Практически вся хромовая руда обрабатывается через преобразование в дихромат натрия. В 1985 году было произведено примерно 136 000 т. шестивалентного хрома.[1] Другими источниками шестивалентного хрома являются триоксид хрома и различные соли — хроматы и дихроматы. Шестивалентный хром используется при производстве нержавеющих сталей, текстильных красок, консервантов дерева, для хромирования и пр.
Шестивалентный хром является признанным канцерогеном при вдыхании.[2] На многих рабочих местах сотрудники подвержены воздействию шестивалентного хрома, например, при гальваническом хромировании или сварке нержавеющих сталей.[2] В Европейском союзе использование шестивалентного хрома существенно ограничено директивой RoHS.
Токсичность
Шестивалентный хром транспортируется в клетки человеческого организма с помощью сульфатного транспортного механизма благодаря своей близости к сульфатам и хроматам по структуре и заряду.
Трёхвалентный хром, более часто встречающийся, не транспортируется в клетки.Внутри клетки Cr(VI) разлагается к метастабильному пятивалентному хрому (Cr(V)), затем к трехвалентному хрому (Cr(III)). Трехвалентный хром, присоединяясь к протеинам, создает гаптены, которые включают иммунную реакцию. После их появления, чувствительность к хрому не пропадает. В этом случае даже контакт с текстильными изделиями, окрашенными хромсодержащими красками или с кожей, обработанной хромом, может вызвать раздражение кожи. Витамин C и другие агенты реагируют с хроматами и создают Cr(III) внутри клетки.[3]
Продукты шестивалентного хрома являются генотоксичными канцерогенами. Хроническое вдыхание соединений шестивалентного хрома увеличивает риск заболеваний носоглотки, риск рака лёгких. (Лёгкие особенно уязвимы из-за большого количества тонких капилляров). Видимо, механизм генотоксичности вызывается пятивалентным и трехвалентным хромом.
В США предельно допустимая концентрация шестивалентного хрома в воздухе составляет 5 мкг/м³ (0.005 мг/м³).[4][5] В России предельно допустимая концентрация хрома (VI) существенно ниже 1,5 мкг/м³ (0,0015 мг/м3).[6]
Одним из общепризнанных методов избежания шестивалентного хрома является переход от технологий гальванического хромирования к газотермическому напылению.
Примечания
- ↑ Gerd Anger, Jost Halstenberg, Klaus Hochgeschwender, Christoph Scherhag, Ulrich Korallus, Herbert Knopf, Peter Schmidt, Manfred Ohlinger, «Chromium Compounds» in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.
- ↑ 1 2 IARC Volume 49: Chromium, Nickel, and Welding. — Lyon: International Agency for Research on Cancer. — ISBN 92-832-1249-5
- ↑ Salnikow, K. and Zhitkovich, A., «Genetic and Epigenetic Mechanisms in Metal Carcinogenesis and Cocarcinogenesis: Nickel, Arsenic, and Chromium», Chem. Res. Toxicol., 2008, 21, 28-44. DOI:10.1021/tx700198a
- ↑ OSHA: Small Entity Compliance Guide for the Hexavalent Chromium Standards
- ↑ David Blowes (2002). «Tracking Hexavalent Cr in Groundwater». Science 295: 2024–25. DOI:10.1126/science.1070031. PMID 11896259.
- ↑ ПДК воздуха населенных мест
Ссылки
dic.academic.ru
Хром высшей валентности - Справочник химика 21
Если процесс восстановления протекает на катоде с малым перенапряжением выделения водорода, первая стадия процесса не должна определять кинетику суммарного процесса, а потенциал катода можно считать близким к равновесному. В этом случае строение двойного электрического слоя и адсорбция поверхностноактивных веществ не будут сказываться на кинетике процесса, и определять закономерности последней будет замедленность химической стадии восстановления органического вещества атомарным водородом. Если же процесс протекает на катоде с высоким перенапряжением выделения водорода, определять кинетику восстановления будет замедленность первой электрохимической стадии, и кинетические закономерности восстановления не будут отличаться от наблюдаемых для перенапряжения выделения водорода на этом металле. Плотность тока в этом случае не будет существенно зависеть от концентрации органического вещества в электролите. Подобные кинетические закономерности наблюдаются также при использовании, так называемых, переносчиков водорода, каталитических добавок ионов металлов переменной валентности, таких как титан, ванадий, хром, церий и т. д. Подобные добавки применяют в тех случаях, когда электродный процесс восстановления органического соединения требует значительно большего перенапряжения, чем восстановление иона металла переменной валентности, например в то время как восстановление органического вещества происходит без затруднений в растворе под действием который окисляется до Естественно, что кинетика суммарного процесса восстановления органического соединения в этом случае будет определяться замедленностью процесса восстановления ионов металла переменной валентности. [c.445] Низкий выход хрома по току и высокая валентность соединений хрома, из которых производится выделение его на катоде, определяют медленность наращивания хрома на детали. [c.14]Изучен процесс озонирования в присутствии добавок, служащих донорами электронов (солей мета.ллов переменной валентности, галоидных соединений, аммиака и др.). Применение добавок дает возможность получать ароматические оксипроизводные, хиноны, карбоновые кислоты, перекисные соединения, нитрилы и другие соединения с высокой избирательностью. Показано, что получение того или иного продукта зависит от скорости взаимодействия озона с добавкой. Приведены константы скорости. Описан синергетический эффект, наблюдаемый при использовании в качестве катализатора смеси солей хрома и марганца. Предложена схема процессов, объясняющая полученные результаты, согласно которой озонолиз ароматических соединений предотвращается быстрыми реакциями озона с добавками. [c.330]
Обработка катализатора водородом приводит к восстановлению ионов хрома высокой валентности в ионы Сг +, которые, как хорошо известно, не являются активными центрами полимеризации. Поэтому (Сг +04) — промежуточный продукт восстановления — по-видимому, не образуется и увеличение каталитической активности не наблюдается. [c.183]
Если активацию проводить при высоких температурах (600—700°С), то за счет разложения хрома высших валентностей до трехокиси хрома получается малоактивный катализатор. [c.86]
Часто транспассивное состояние связывается с гем, что пленка фазового окисла, пассивирующего электрод, окисляется до соединений, хорошо растворимых в воде и отвечающих более высокой валентности металла. Например, СггОз или СгОг, на хроме окисляется до СгОз, образующей СггО в кислых растворах или СгО " в щелочных [69]. Подобное же объяснение дается для железа (образование РеО ), никеля (образование КЮа) и других металлов. [c.249]
NO r ПОН способствует первичной пассивации ЭП-220, по при более положительных значениях потенциала анодное растворение происходит через поры пленки вследствие растворения оксидов никеля и хрома более высокой валентности. [c.65]
Феррохром — сплав железа с большим содержанием хрома — получают восстановлением хромита углеродом в электропечах. Его используют при производстве легированных сталей. Сплавы хрома имеют очень важное значение, (причем особое место занимают его сплавы с железом специальные стали). Хромовые стали отличаются высокой твердостью, вяз(костью и прочностью. Их свойства -можно связать с высокой металлической валентностью хрома (VI) и взаимодействием между разнородными атомами, что, как правило, приводит к получению сплавов, отличающихся более высокой твердостью и вязкостью, чем исходные металлы. Хромовые стали идут на изготовление брони, ра(кет, сейфов и пр. Обычная нержавеющая сталь содержит 14—18% хрома и, как правило, 8 /о никеля. [c.576]
Полимеризация этилена при высоком давлении (100—350 МПа,, или 1000—3500 кгс/см ) протекает при 200—300°С в расплаве в присутствии инициаторов (кислорода, органических перекисей). Полиэтилен низкого давления получают полимеризацией этилена под давлением 0,2—0,5 МПа (2—5 кгс/см ) и температуре 50— 80 °С в присутствии комплексных металлоорганических катализаторов (триэтилалюминия, диэтилалюминийхлорида и триизобутил-алюминия). Полиэтилен среднего давления получают полимеризацией этилена в растворителе при давлении 3,5—4,0 МПа (35— 40 кгс/см ) и температуре 130—170 °С в присутствии окислов металлов переменной валентности, являющихся катализаторами (окислы хрома, молибдена, ванадия). В качестве растворителей применяют бензин, ксилол, циклогексан и др. [c.104]
Следует отметить, как это было указано ранее в гл. IV, что при высоких концентрациях азотной кислоты хромоиикелевые стали подвержены так называемому явлению перепассивации , прн котором пассивные пленки теряют свои защитные свойства вследствие иерехода хрома в окислы высшей валентности, неустойчивые в высококонцентрированной кислоте. [c.227]
Интересно отметить, что хром в металлическом состоянии имеет металлическую валентность 6, соответствующую степени окисления + 6, характерной для хроматов и бихроматов, а не более низкой степени окисления -ЬЗ, характерной для солей хрома металлы марганец,, железо, кобальт и никель тоже имеют металлическую валентность 6, хотя почти все эти элементы образуют соединения со степенями окисления + 2 и -ЬЗ. Ценные физические свойства переходных металлов обусловлены высокой металлической валентностью этих элементов. [c.494]
Окислительный потенциал системы Се Се + в серной кислоте равняется 1,44 в. Такой высокий окислительный потенциал позволяет применять соли церия в качестве окислителя так же широко, как применяют растворы бихромата, ванадата и перманганата. Четырехвалентный церий в окислительных реакциях имеет ряд преимуществ по сравнению с перманганатом и бихроматом. При восстановлении перманганата и бихромата образуются нестойкие вещества, в которых ионы марганца и хрома имеют промежуточные состояния валентности и косвенно могут изменять направление реакции. [c.43]
В присутствии неорганических анионов, обладающих окислительными свойствами, появляются иногда в растворах, а также в защитных пленках, ионы низшей валентности (например, Сг ). Последнее как будто противоречит тому, что было сказано выше о невозможности восстановления на железе в нейтральных средах ионов хромата или бихромата на самом же деле здесь никакого противоречия нет. В начальный момент соприкосновения железа с электролитом происходит восстановление некоторого количества анионов хромата (реакция идет с очень малой скоростью) однако как только на поверхности железа образуется пленка из гидратов окиси хрома и железа, дальнейшее восстановление ионов хромата прекращается из-за высокого перенапряжения процесса. [c.57]
Изучение катализаторов в нестационарном состоянии позволило установить прямую связь между валентностью катионов окислов и селективностью в окислении углеводородов. Это открывает возможности предсказания поведения химических соединений определенного состава в качестве катализаторов окисления углеводородов. Так, например, повышение содержания ионов хрома высокой валентности в СГ2О3 приводит к увеличению каталитической активности в реакции полного горения пропилена. Если допустить, что характер зависимости каталитических свойств от изменения валент- [c.264]
Направления дальнейших исследований. Обширный класс интерметаллических соединений, особенно очень стабильных Бруеровских соединений, представляет интерес для широкого применения в катализе, особенно в области получения синтетического топлива. Так, появляется возможность приготовления нанесенных интерметаллов, которые имеют необычно высокую термическую и химическую стойкость, комбинацией металлов группы УП1 с титаном, стронцием, гафнием, ванадием, ниобием, таллием, хромом, молибденом и вольфрамом. Из-за очень сильных взаимодействий, возникающих при образовании данных соединений, ожидается, что спекание будет существенно уменьшено. Такие сильные взаимодействия, по-видимому, модифицируют электронные и каталитические свойства металла группы УП1. В некоторых случаях это может приводить к ухудшению каталитических свойств. Например, для 2гР1з интенсивное изъятие электронов атомами циркония делает платину заметно истощенной по электронам, а поэтому менее металлической, чем платина нулевой валентности. Такое чрезмерное взаимодействие можно уменьшить или регулировать использованием в качестве второго элемента металла, расположенного -справа или слева от циркония (например, молибдена). [c.139]
Подобно хрому, молибден и вольфрам проявляют переменную валентность, но, в отличие от хрома, устойчивыми у ннх являются соединения, отвечающие их высшей валентности +6. Их окислы МоОз и ШОз вследствие высокой валентности металла являются ангидридами. Им отвечают в качестве гидратов кислоты Н2М0О4 — молибденовая и НгШО — вольфрамовая. [c.153]
Весовой метод основан на отделении осадка молибдена с а-бен-зоиноксимом Комплекс осаждают из холодного раствора серной кислоты (1 20), но допускаются и большие концентрации кислоты (1 4). Для предотвращения восстановления пятивалентного молибдена в раствор добавляют небольшой избыток брома. Для полного перевода хрома и ванадия соответственно в трех- и четырехвалентное состояние в раствор добавляют также соль Мора, так как эти элементы в более высоких валентных состояниях мешают анализу. [c.64]
Некоторые минералы, включающие металлы, которые окисляются до более высокого валентного состояния, можно разложить сплавлением со щелочными окислительными расплавами (смесь Na2 03+ KNO3 или более агрессивно действующая Na202). Таковы, например, некоторые минералы из хрома, ванадия, молибдена, которые в этих условиях переходят соответственно в хроматы, ванадаты, молибдаты. Сплавление в этом случае также проводят в железных или никелевых тиглях. [c.448]
Молибден и вольфрам относятся к шестой группе периодической системы и входят в подгруппу хрома. Атомньш вес молибдена 95,95, заряд ядра 42. Атомный вес вольфрама 183,82, заряд ядра 74 находясь в пятом периоде, т. е. во втором большом периоде, молибден и вольфрам имеют следующее расположение электронов 2, 8, 18 13, 1 и 2, 8, 18, 32,12, 2 соответственно. Вследствие такого расположения электронов молибден и вольфрам обладают переменной валентностью, причем наиболее устойчивой оказывается валентность 4 и 6 при валентности 6 атомы обоих элементов освобождаются от одного электрона с наружной оболочки и пяти электронов со второй, приобретая вследствие этого структуру атома инертного газа криптона. Благодаря высокой валентности молибден и вольфрам входят в большинство соединений в виде кислородсодержащего аниона ШоОГ и [c.48]
В пассивном состоянии окисление самого металла протекает с очень малой скоростью, если ее отнести к общей поверхности электрода, но не прекращается совершенно. Ни фазовый окисел, ни адсорбционный слой кислорода не изолируют полностью поверхность металла от раствора. Поэтому в отдельных местах поверхности, не фиксированных точно, а, вероятно, перемежающихся, может продолжаться растворение металла при высоком положительном потенциале. Если металл может существовать в нескольких степенях окисления, то более высокому положительному потенциалу часто отвечает образование ионов более высокой валентности. Так, например, железо может переходить в раствор не в виде двухвалентных ионов (как обычно), а в виде трехвалентных хром может образовывать анионы Сг04 или СГ2О7, в зависимости от pH раствора, и т. д. [c.586]
Исследование А. Т. Ваграмяна и Д. Н. Усачева и показало, что в случае злектроосаждения хрома процесс осложняется наличием пленки на поверхности электрода. Согласно развитому в работе представлению [39], восстановление ионов хрома происходит не из ионов раствора, а непосредственно из продуктов пленки, образующейся в процессе электролиза на поверхности катода. В состав этой пленки входят хромат-ионы и продукты их неполного восстановления, кроме того,— некоторое количество чужеродных анионов, без которых выделения металла не происходит. Д. Н. Усачевым и А. Т. Ваграмяном было предположено, что металлы, которые входят в пленку в виде сложных анионов и являются ее составной частью, могут разряжаться наряду с ионами хрома. Исследование показало, что действительно при введении в раствор хромовой кислоты марганца в виде КМПО4 на катоде осаждается сплав марганец —хром, содержащий при определенных условиях электролиза (температура, плотность тока, концентрация) 15% Мп и 85% Сг. При изменении условий электролиза состав сплава меняется. Следует отметить, что при введении в хромовый электролит марганца не в виде аниона, а в виде катиона М.п + на катоде осаждается лишь хром, а марганец в осадке не обнаруживается. Это совершенно необычное, аномальное явление для электрохимии, когда в одинаковых условиях электролиза ион более высокой валентности восстанавливается до металла, а более низкой — не восстанавливается. [c.194]
Все известные до сих пор катализаторы для дегидрирования н-бутана и других парафиновых углеводородов состоят в основном из окислов хрома на окиси алюминия. Характерным свойством алю-мохромовых катализаторов является их высокая чувствительность к отравляющему действию воды. Активность алюмохромовых катализаторов связана с содержанием в них окислов хрома высшей валентности (например, СгОз). [c.118]
У металлов, которые образуют несколько окислов, пассивирующим свойством обладает, как правило, только один из них. Например, у хрома и железа пленка, состоящая из МеаОд, малорастворима, неактивна и очень компактна. В случае анодного окисления при потенциале выше Е образуются соединения с более высокой валентностью, которые могут быть значительно более растворимы. У хрома окисление хромистых соединений пассивной пленки до растворимых хромовокислых происходит уже при потенциале 1,2 в, тогда как выделение кислорода в кислых растворах начинается при 1,6 в. У железа Е выше Ео , так что кислород выделяется, не нарушая пассивной пленки. Она разрушается при более высоких потенциалах. Подобно хрому ведет себя и молибден. Оба эти металла содержатся в нержавеющих сталях как составные элементы снлава и являются причиной усиления их коррозии в транспассивном состоянии [52]. [c.15]
О происходяш,ем восстановлении катализатора под действием этилена свидетельствует резкое уменьшение в нем содержания Ст в начале полимеризации, на что указывают данные анализа и изменение окраски катализатора. Так, например, в активированном воздухом катализаторе иодометрически определенное содержание Сг составляло 1,96 вес. %, а через 3 мин. после начала реакции полимеризации оно равнялось 0,22 вес.%. По-ви-димому, для проявления катализатором полимеризуюш ей способности необходимо, чтобы это восстановление остановилось на промежуточном валентном состоянии, а не шло глубоко, до образования окисла трехвалентного хрома, который, как известно, не ведет полимеризацию [4, 5, 18, 26]. Поэтому суш ествование температурного предела, до которого катализатор активен (—180°), по-видимому, связано с тем, что при более высоких температурах происходит глубокое восстановление хрома (до Сг ). В литературе имеются высказывания о том, что каталитическая активность в реакции полимеризации связана с окислами хрома промежуточных валентностей [17—19]. Косси и Ван-Рейн [24] восстанавливали в мягких условиях образцы окиснохромового катализатора и снимали их спектры электронного парамагнитного резонанса (ЭПР). Наблюдаемые узкую и широкую линии они приписывают соединениям Сг и. Эти авторы высказывают предположение, что такие ионы хрома и являются активными центрами в реакции полимеризации. Подтверждение в пользу образования иона пятивалентного хрома дается в работе В. Б. Казанского и Ю. И. Печерской [25]. Авторы работы показали, что узкая линия поглош,ения в спектрах электронного парамагнитного резонанса, снятых на неполностью восстановленных алюмохромовых катализаторах (СгОз на А12О3), обусловлена поверхностной фазой соединения Сг . Полученные нами предварительные результаты исследования наших катализаторов методом электронного парамагнитного резонанса сводятся к следующему. [c.162]
Оксиды лантана и калия усиливают гетероциклизующие, дегидрирующие и ослабляют крекирующие, коксообразующие свойства алюмохромового катализатора. Введение оксида калия также приводит к повышению стабильности катализатора. Стационарно работающий катализатор содержит ионы хрома низшей валентности [58, 61]. Но и в присутствии модифицированного алюмохромокалиевого катализатора выход тиофена из бутана и Н28 невелик - не превышает 30-40 %. Гетероциклизацию -бутана ведут при большой концентрации сероводорода, который обладает высокой коррозионной активностью. Уменьшение этого нежелательного воздействия достигается [62] проведением каталшического процесса с небольшой концентрацией сероводорода, но в присутствии элементарной серы. При взаимодействии вьщеляющегося в процессе водорода с серой образуется сероводород, вступающий в реакцию гетероциклизации -бутана в тиофен. [c.177]
По мере накопления экспериментального материала выяснилось, что высокие давления вызывают зачастую уникальные изменения в веществах, которые никаким другими способами достигнуты быть не могут. Это может проявляться в переходе электрона с одной орбитали на другую (церий, цезий), переходе вещества из диэлектрика в состояние с металлической проводимостью (фосфор, оксиды железа, никеля, хрома), переходе вещества из. модификации с малой плотностью в модификацию с большой, в изменении валентности, получении совершенно новых соединений и т. д. Все эти явления крайне интересны, и далеко не всем им в настоящее время дано убедительное объяснение. Давление существенно влияет и на кинетику различных процессов. Многочисленные примеры показывают, как действует давленпе на с.чорость реакций различных порядков и какие выводы можно сделать па основании исследования таких процессов. Действие давления на сложные химические реакции редко удается объяснить до конца, ибо очень трудно выделить в суммарном эффекте, где давление проявило себя как действующее на равновесие процесса, а где — на его кинетику. Особо следует указать на давление, влияющее на скорость пространственно-затруд-ненных реакций. [c.6]
Если общее содержание хрома в катализаторе высоко, то доля Сг + будет низкой. Однако активной является лишь та часть Сг +, которая взаимодействует с поверхностью носителя именно этот Сг + участвует i образовании АЦ. Остальная часть 6-валентного хроыг при активации с удалением влаги (при высоких температурах в токе сухого воздуха) превращается в неактивную фазу СГ2О3. [c.42]
Все три элемента близки по химическим свойствам. Это относится, в частности, к поливалентности, способности образовывать изополи-и гетерополисоединения, проявлению как металлических, так и неметаллических свойств.Основные свойства окислов усиливаются от хрома к вольфраму. Хромовая кислота Н2СГО4 более сильная, чем вольфрамовая. Устойчивость соединений с низшей валентностью растет от вольфрама к хрому. Соединения Мо(У) более устойчивы, чем (V). Соединения Сг(П1) — ярко выраженные ионные соединения. Соединения (У) и Мо(У) почти не имеют ионного характера. Об этом, в частности, говорит их высокая летучесть. Молибден и вольфрам намного более способны образовывать изополи- и гетерополисоединения, чем хром. [c.159]
Хром находится в 6-й группе, в его электронной оболочке на два электрона больше, чем у титана. В основном состоянии атом хрома содержит две полузаполненные оболочки [Аг]3( 4з с шестью неспаренными электронами. Благодаря наличию шести валентных электронов и не очень высокой электроотрицательности хрома (1,6) химия его очень богата и разнообразна он проявляет все степени окисления от -2 до -Ьб. Как и в случае титана, самые низкие степени окисления (-2, -1,0 и -Ы) проявляются только в комплексных соединениях с л-акцепторными лигандами, например в карбониле Сг(СО)в. Наиболее характерна для хрома степень окисления -ЬЗ и, соответственно, электронная конфигурация иона В природе хром встречается в основном в виде соединений Сг(Ш), например хромистого железняка ГеО СГ2О3, правда на Урале встречается красная свинцовая руда РЬСгО , в которой хром находится в степени окисления -Ьб, характеризуюш ейся выраженными окислительными свойствами. [c.347]
При адсорбции этана и пропана на молибдате хрома при 200-300 °С образуются поверхностные формы, характеризующиеся полосами поглощения 1390, 1450 и 1550 см . Их интерпретируют как валентные колебания групп формиатных и кар-боксилатных поверхностных структур [97]. Они на молибдате хрома имеют достаточно высокую термостабильность, и полная их десорбция наблюдается лищь при температуре вьшхе 400 °С. [c.90]
НИЗШИМ валентным состояниям данного элемента. Однако в тех случаях, когда имеет место внутренняя конверсия у-лучей захвата, следствием ее может - явиться возникновение у атомов высокого положительного заряда, что соответствует процессу окисления. Так, при облучении гидратированных солей трехвалентного хрома до 10% радиоактивного хрома находится в шестивалентном состоянии, а при облучении хлорида четырехвалентного рения наблюдается образование иона перрената КеОГ [39]. [c.26]
Сила адсорбции представляет собой электростатическое притяжение между положительно заряженной внутренней частью иона и электронами металла или его окисла. Имеются основания считать, что в анионах типа МО " валентные электроны распределяются между центральным атомом и атомами кислорода по-разному. В хромат-ионе, например, некоторые из электронов хрома, по всей вероятности, оттянуты от него и перешли к кислороду (электровалентная связь). Поэтому центр иона должен обнаруживать высокий положительный заряд. Благодаря этому заряду хромат-ион, адсорбированный поверхностью металла или окисной пленкой, может вытягивать свободные электроны с поверхности металла. Это будет до некоторой степени ограничивать подвижность электронов и задерживать коррозию. Следует, однако, заметить, что выполненные нами совместно с Ларькиным квантовохимические расчеты показали, что связь хромат-ионов с железом осуществляется не центральным атомом хрома, а посредством кислородных атомов (подробно см. ниже). [c.68]
chem21.info