Теплопроводность цветных металлов, теплоемкость и плотность сплавов. Теплопроводность хрома
Коэффициент теплопроводности металлов (Таблица)
Теплопроводность многих металлов следует соотношению k = 2,5·10-8σT, где Т обозначает температуру в °К, а σ — электропроводность в единицах (ом·см)-1. Это соотношение, которое лучше всего оправдывается для хороших проводников электричества и при высоких температурах, можно применять и для определения коэффициентов теплопроводности.
Соотношение kpcp=const, где р обозначает плотность, а ср — удельную теплоемкость при постоянном давлении, было предложено Стормом для того, чтобы объяснить температурные изменения этих величин для некоторых металлов и сплавов.
Таблица коэффициент теплопроводности металлов
Элементы с металлической электропроводностью (числа, набранные курсивом, относятся к жидкой фазе)
| Металл | Коэффициент теплопроводности металлов при температура, °С | ||||
| - 100 | 0 | 100 | 300 | 700 | |
| Алюминий | 2,45 | 2,38 | 2,30 | 2,26 | 0,9 |
| Бериллий | 4,1 | 2,3 | 1,7 | 1,25 | 0,9 |
| Ванадий | — | — | 0,31 | 0,34 | — |
| Висмут | 0,11 | 0,08 | 0,07 | 0,11 | 0,15 |
| Вольфрам | 2,05 | 1,90 | 1,65 | 1,45 | 1,2 |
| Гафний | — | — | 0,22 | 0,21 | — |
| Железо | 0,94 | 0,76 | 0,69 | 0,55 | 0,34 |
| Золото | 3,3 | 3,1 | 3,1 | — | — |
| Индий | — | 0,25 | — | — | — |
| Иридий | 1,51 | 1,48 | 1,43 | — | — |
| Кадмий | 0,96 | 0,92 | 0,90 | 0,95 | 0,44 (400°) |
| Калий | — | 0,99 | — | 0,42 | 0,34 |
| Кальций | — | 0,98 | — | — | — |
| Кобальт | — | 0,69 | — | — | — |
| Литий | — | 0,71 | 0,73 | — | — |
| Магний | 1,6 | 1,5 | 1,5 | 1,45 | — |
| Медь | 4,05 | 3,85 | 3,82 | 3,76 | 3,50 |
| Молибден | 1,4 | 1,43 | — | — | 1,04 (1000°) |
| Натрий | 1,35 | 1,35 | 0,85 | 0,76 | 0,60 |
| Никель | 0,97 | 0,91 | 0,83 | 0,64 | 0,66 |
| Ниобий | 0,49 | 0,49 | 0,51 | 0,56 | — |
| Олово | 0,74 | 0,64 | 0,60 | 0,33 | — |
| Палладий | 0,69 | 0,67 | 0,74 | — | — |
| Платина | 0,68 | 0,69 | 0,72 | 0,76 | 0,84 |
| Рений | — | 0,71 | — | — | — |
| Родий | 1,54 | 1,52 | 1,47 | — | — |
| Ртуть | 0,33 | 0,09 | 0.1 | 0,115 | — |
| Свинец | 0,37 | 0,35 | 0,335 | 0,315 | 0,19 |
| Серебро | 4,22 | 4,18 | 4,17 | 3,62 | — |
| Сурьма | 0,23 | 0,18 | 0,17 | 0,17 | 0,21 |
| Таллий |
| 0,41 | 0,43 | 0,49 | 0,25 (400 0) |
| Тантал | 0,54 | 0,54 | — | — | — |
| Титан | — | — | 0,16 | 0,15 | — |
| Торий | — | 0,41 | 0,39 | 0,40 | 0,45 |
| Уран | — | 0,24 | 0,26 | 0,31 | 0,40 |
| Хром | — | 0,86 | 0,85 | 0,80 | 0,63 |
| Цинк | 1,14 | 1,13 | 1,09 | 1,00 | 0,56 |
| Цирконий | — | 0,21 | 0,20 | 0,19 | — |
Таблица коэффициент теплопроводности полупроводники и изоляторы
| Вещество | Коэффициент теплопроводности при температура, °С | ||||
| - 100 | 0 | 100 | 500 | 700 | |
| Германий | 1,05 | 0,63 | — | — | — |
| Графит | — | 0,5—4,0 | 0,5—3,0 | 0,4-1,7 | 0,4-0,9 |
| Йод | — | 0,004 | — | — | — |
| Углерод | — | 0,016 | 0,017 | 0,019 | 0,023 |
| Селен | — | 0,0024 | — | — | — |
| Кремний | — | 0,84 | — | — | — |
| Сера | — | 0,0029 | 0,0023 | — | — |
| Теллур | — | 0,015 | — | — | — |
infotables.ru
Хрома теплопроводность - Справочник химика 21
Как самый тугоплавкий металл вольфрам входит в состав ряда жаропрочных сплавов. В частности, его сплавы с кобальтом и хромом — стеллиты — обладают высокими твердостью, износоустойчивостью, жаростойкостью. Сплавы вольфрама с медью и с серебром сочетают в себе высокие электрическую проводимость, теплопроводность и износоустойчивость. Они применяются для изготовления рабочих частей рубильников, выключателей, электродов для точечной сварки. [c.517] По мере повышения температуры теплопроводность уменьшается. Теплопроводность зависит главным образом от состава чугуна и в меньшей степени от его структурных составляющих. Кремний, никель, марганец и ванадий уменьшают теплопроводность, а хром и вольфрам увеличивают се. [c.128]Если основным материалом являются пластмассы, то вначале необходимо применить электролиз медного или никелевого осадка. Для того чтобы основной слой стал электропроводным, часто приходится использовать плотные пластичные грунтовые покрытия с целью сохранения адгезии между пластмассой и слоями хрома и никеля. В противном случае из-за разной удельной теплопроводности этих материалов может возникнуть внутреннее напряжение на межфазных границах. [c.126]
В электропечах сопротивления косвенного действия теплота выделяется в специальных нагревательных элементах, по которым проходит электрический ток. При этом нагреваемой среде теплота передается как лучеиспусканием и теплопроводностью, так и конвекцией. В таких печах возможно осуществлять нагревание до температур на уровне 1000-1400 °С. Принципиальная схема обогрева электропечи показана на рис. 12-8. Теплота выделяется при прохождении электрического тока через спиральные нагревательные элементы 2, уложенные в футеровке печи вокруг аппарата. Проволочные или ленточные нагревательные спирали изготовляют чаще всего из нихрома - сплава, содержащего 20% хрома, 30-80% никеля и 0,5-50% железа. [c.328]
Каталитическое окисление сернистого газа Платина (0,015—0,02%) Алюминиевая проволока (2 мм диаметром, 3 мм длиной), а также другие металлические носители, например хром, никель (с обычными носителями платины, такими как силикагель, достижение идеального температурного режима невозможно вследствие их малой теплопроводности) 12 [c.454]
Дегидрогенизация алифатических вторичных спиртов (изопропилового спирта, вторичных гексиловых спиртов) в кетоны Окись церия, цинка, магния, марганца, хрома и т. д. на носителе с теплопроводностью по меньшей мере 0,2 для приготовления катализатора из окиси и воды делают пасту, которую наносят на опилки или маленькие кусочки меди, алюминия, латуни, стали или карборунда 1 3178 [c.357]
Для поглощения излучения применяют ребра ряда специфических форм. Хотя при кипении воды температура стенки гладкой трубы остается достаточно низкой, существуют причины, препятствующие использованию ребер в таких системах. Основания ребер значительно холоднее, чем их вершины. Для того чтобы вершины ребер выдерживали высокие температуры, их необходимо изготавливать из стали с повышенным содержанием хрома, что увеличивает допустимые температуры их эксплуатации. Для повышения допустимой температуры до 870— 925°С требуется сталь, содержащая 27% хрома. Для того чтобы допустимая температура составляла около 1000°С, требуется нержавеющая сталь с содержанием 18% хрома и 8% никеля. При этом не только возрастает стоимость материала, но, что, пожалуй, самое существенное, вследствие увеличения содержания хрома и никеля происходит значительное уменьшение теплопроводности. В табл. 1.1 приведены данные [c.46]
Электролитические хромовые покрытия отличаются высокой твердостью, лрочностью сцепления с основным металлом, коррозионной стойкостью, хорошей теплопроводностью и теплостойкостью. В технике нашли применение блестящие, молочные и переходные между ними дымчатые покрытия хрома (рис. И). [c.112]
С повышением температуры термообработки теплопроводность электролитического хрома увеличивается от 0,064 при температуре 60° С и 0,082 при температуре 200° С до 0,13 кал/(с-см-°С) при температуре 400° С. [c.116]
Многие легирующие элементы (титан, ванадий, алюминий, вольфрам, медь, молибден, хром, олово, марганец, никель) повышают твердость Б. ч., кремний и сера уменьшают ее. Увеличение содержания цементита снижает теплопроводность чугунов, вследствие чего они склонны к образованию холодных трещин. Б. ч. отличаются хорошей жидкотекучестью, повышающейся с увеличением содержания углерода и кремния. Однако значительная линейная усадка и грубая первичная структура обусловливают повышенную склонность Б. ч. к образованию горячих трещин.Наибольшей износостойкостью характеризуются Б. ч., содержащие 12—24% Сг (рис., г). Чугуны, содержащие 34% Сг и [c.126]
Их мех. св-ва улучшают нормализацией, закалкой и отпуском. Из таких чугунов изготовляют блоки цилиндров, станины, поршневые кольца, гильзы, поршни, коленчатые и распределительные валы, головки различных двигателей, корпуса, штампы. К износостойким (табл. 1 иа с. 687) относятся средне- и высоколегированные (хромом, никелем, молибденом) чугуны, характеризующиеся мартенситной структурой и твердыми карбидами. Эти чугуны идут на изготовление деталей, эксплуатируемых при интенсивном абразивном изнашивании. Для получения необходимой структуры и св-в чугуны иногда подвергают закалке, обработке холодом (см. Холодом обработка металлов). Распространен износостойкий чугун нихард (см. также Износостойкий чугун). Антифрикционные чугуны относятся к низколегированным. Кроме высокой износостойкости, они отличаются небольшим коэфф. трения, высокой теплопроводностью, хорошей обрабатываемостью, прирабатывае-мостью, сопротивлением задирам. Такие св-ва обусловливаются наличием в структуре мягкой основы (перлита, феррита) и сфероидальных карбидов или фосфидной эвтектика. Различают серые (марки АЧС), ковкие (марки АЧК) и высокопрочные (марки АЧВ) антифрикционные чугуны (табл. 2). Их легируют хромом (до 0,4%), никелем (до 0,4%), титаном (до 0,1%), медью (0,3—1,5%), сурь- [c.688]
МЕДИ СПЛАВЫ — сплавы на ото ве меди. В виде бронзы применялись за 3000 лет до н. э. В жидком состоянии медь сплавляется со многими элементами, с большинством из них — в любом соотношении. Лишь вольфрам, молибден, осмий, рутений и тантал практически не сплавляются с нер. В твердом состоянии макс. растворимость элементов (в альфа-твердом растворе меди) изменяется в очень широких пределах от сотых и десятых долей процента (хром, ниобий, свинец, ванадий, цирконий) до процентов (серебро, алюминий, мышьяк, бериллий, кадмий, кобальт, железо, магний, кремний, титан и др.) и десятков процентов (индий, олово, цинк). Неограниченно растворяются никель, золото, марганец, палладий и платина. Однако с золотом, марганцем, палладием и платиной М. с. в твердом состоянии претерпевают превращения. С увеличением концентрации легирующего элемента в альфа-твердом растворе меди повышается мех. прочность сплавов их теплопроводность и электропроводность уменьшаются (менее всего при легировании серебром). К вредным примесям относятся висмут, сурьма, свинец и углерод (в медноникелевых сплавах), к-рые приводят к хрупкости. Стойкость против коррозии М. с. зависит от природы легирующего элемента и окружающей среды. Повышают стойкость никель, олово и алюминий. С понижением т-ры раст [c.780]
Электронная теплоемкость хрома "=[1,4 мДж/(моль-К )] / . Теплопроводность X в зависимости от температуры [c.371]
Все вышесказанное в сочетании с чрезвычайно высокой твердостью и хорошей теплопроводностью (табл. 1) делает карбиды хрома перспективными материалами, особенно в условиях, предъявляющих к материалу жесткие износостойкие и жаростойкие требования. Ценность карбидов хрома как конструкционных материалов со временем, очевидно, значительно возрастет благодаря возможности изменять путем легирования в широких пределах их коррозионные, физические, механические и другие свойства. Так, имеется указание[161] О разработке карбидов на основе хрома, содержащих никель [c.55]
Некоторыми исследователями изучалось влияние обработки кристалла на свойства рубина [136—142]. Разработаны методы определения хрома в рубине [143—144]. Берман, Фостер и Зай-ман [145] исследовали теплопроводность искусственных кристаллов сапфира при низких температурах. Мекке [404] при помощи инфракрасных спектров обнаружил в сапфире присутствие радикала ОН. [c.300]
Толщина слоев футеровки рассчитывается по теплопроводности материалов и допустимым температурам на границе слоев. При этом принимается, что максимальная температура минеральной шлаковой ваты не должна превышать 780 °С, а каолиновой обычной — 1260 °С, а с добавкой оксида хрома — 1450 °С. [c.723]
Согласно недавнему предложению [7], 2—3 г стальной стружки прессуют при давлении около 12 т/см в медном цилиндре весом 40 г, диаметром 20 мм и толщиной 15 мм. Медь является связующим веществом с хорошей теплопроводностью, и поэтому таблетки из стали получаются компактными и легко затачиваются. Кремний и хром могут определяться по аналитической кривой, построенной с помощью литых стальных образцов, в то время как для других компонентов (N1, Мп) аналитические кривые должны строиться по стандартным образцам, спрессованным тем же способом, что и пробы. [c.18]
Теплоемкость хрома с повышением температуры непрерывно возрастает (табл. 134), а теплопроводность уменьшается (табл. 135). Коэффициент термического линейного расширения хрома, карбида и дисилицида хрома с ростом температуры увеличивается (табл. 136). Особенностью хрома является высокая упругость его паров [c.85]
Процесс сварки труб из центробежнолитых трубных заготовок отличается рядом особенностей вследствие специфических свойств аустенитных хромоникелевых сталей. Аустенитная сталь типа НК-40 характеризуется электрическим сопротивлением, примерно в 5 раз большим, чем обычных углеродистых сталей, и низкой теплопроводностью металла, что определяет выбор методов и режимов сварки. Химический состав хромоиикелевых сталей также оказывает влияние на происходящие металлургические процессы сварки. Высокое содержание хрома в сплаве делает его взаимодействие с кислородом и рядом оксидов (МпО п 5102) достаточно активным, что вызывает интенсивные марган-цево-кремневосстановительные процессы, сопровождающиеся окислением значительных количеств хрома. Другие элементы, входящие в жаропрочный сплав (Ре, N1, Мп, 51, 5, Р, N и др.), при сварке могут образовывать различные эвтектики, карбиды, нитриды, интерметаллиды. Образование в металле новых фаз вызывает появление структурных напряжений, особенно металлов центробежнолитых трубных заготовок с характерной анизотропной дендритной структурой. Наконец, при сварке в результате воздействия высоких температур происходит укрупнение зерен в структуре металла и его разупрочнение при комнатной температуре, что ухудшает эксплуатационные свойства труб. [c.33]
Условия опыта. Длина колонки 1 м, внутренний диаметр 4 мм. Скорость потока газа-носителя (аяот) 30 мл/мин. Температура комнатная (20° С). Количество образца для анализа 0,5 мл. Твердый носитель — ИНЗ-600 или сферо-хром-1, или сферохром-2, зернение 0,25—0,5 мм. Неподвижная фаза для распределительной колонки — вазелиновое масло (30% от массы носителя). Сорбент для адсорбционной колонки — силикагель МСК- Токовая нагрузка на плечи детектора по теплопроводности (катарометра) 100 ма. [c.101]
Свойства сплавов. Сплавы сохраняют хорошую электрическую проводимость, теплопроводность и другие присущие металлам свойства. Однако их свойства не складываются как среднее арифметическое из свойств сплавляемых компонентов. Наоборот, температуры плавления сплавов ниже, чем у исходных металлов. Например, сплав Вуда плавится пр11 75 "С, а температура плавления самого легкоплавкого его компонента — олова 232 С. Сплав Деварда [50% (мае.) меди, 45% (мае.) алюминия и 5% (мае.) цинка] легко растирается в порошок и вытесняет водород из воды, хотя ни один из исходных металлов этим свойством не обладает. Очевидно, у сплавов появляются новые свойства, возникают новые качества. Как правило, сплавы более тверды, чем исходные металлы. Например, твердость латуни составляет 150 условных единиц, а исходных компонентов — меди и цинка — соответственно 40 и 50. Удельное электрическое сопротивление сплавов обычно выше, чем у исходных чистых металлов. Например, у нихрома [20% (мае.) хрома + 80% (мае.) никеля] сопротивление 110-10 , у хрома 15-Ю , а у никеля только 7 10" Ом-см. [c.267]
N1) сильно повышает прочность и понижает вязкость. Стали аустенитиого класса характеризуются высокой вязкостью и низкой прочностью и твердостью. в сочетании с хромом повышает прочность и пластические свойства конструкционных сталей. Снижает теплопроводность. Повышает сопротивление коррозии на воздухе, в морской воде и некоторых кислотах. Увеличивает прокаливаемость. Способствует появлению отпускной хрупкости [c.17]
Монокристаллические материалы составляют основу современной полупроводниковой и вычислительной техники, оптических квантовых генераторов, методов голографии. Искусственные монокристаллы получают различными способами из расплавов, рас-,1 . парообразной или твердой фазы. В первом твердотельном х /ооре, построенном в 1960 г., в качестве рабочего элемента использован монокристалл рубина. Рубин — это кристалл корунда (а-АЬОз), содержащий примеси ионов хрома, Сг+ . Присутствие ионов хрома придает кристаллам корунда красную окраску. В оптических квантовых генераторах (ОКГ) чаще всего применяют бледно-розовый рубин с содержанием хрома около 0,05%. При повышении количества хрома окраска становится уже ярко-красной, а в дальнейшем переходит в зеленую. Кристаллы рубина по своим физико-химическим свойствам в определенной степени уникальны и отвечают всем требованиям, предъявляемым к материалам для ОКГ. Они обладают высокой теплопроводностью, что позволяет избежать их саморазогрева во время работы, имеют высокую оптическую и механическую однородность, исключающую паразитное поглощение и рассеяние энергии, обладают высокой термической, механической и химической стойкостью. Монокристалл рубина для ОКГ должен быть длиной от 50 до 300 мм и диаметром 5—25 мм. Кристаллы такого размера получают синтетическим путем. Одним из наиболее распространенных методов синтеза монокристаллов рубина остается способ, предложенный в 1891 г. Вернейлем. Ультрадисперсный порошкообразный оксид алюминия, легированный оксидом хрома (1П), попадает в пламя кислородно-водородной горелки, где температура достигает 2000 °С, плавится и опускаете) на расплавленную верхнюю часть [c.158]
Хорошие клеевые композиции получают [142], сочетая АФС с 2гОг и порошком титана (Осж после 600 °С — 250 МПа) или хрома. Порошки металлов в этом случае не являются инертным наполнителем и образуют аморфные кислые фосфаты. В высокотемпературные клеи и массы на основе АФС вводят иногда и графит. Это позволяет регулировать теплопроводность шва или композиционного материала. Так, известно использование смеси наполнителей АЬОз и графита. Клеи на основе АФС + корунд (размер зерна После обжига склеенной конструкции прочность при сдвиге составляла около 2,7 МПа. При склеивании стали с корундом клеем на основе АФС + корунд прочность на сдвиг растет в интервале 500—1300°С, достигает максимума при 1100 °С (6—14 МПа), причем более высокая прочность наблюдается при использовании АФС с 50 %-ной условной степенью нейтрализации Л/[Л/ = 0% — соответствует Н3РО4, Л/= 100 % — получению А1 (РО4) ], Специфический термостойкий клей получают, сочетая АФС с оксидом алюминия, высокоглиноземистым цементом, оксидом хрома (III). Такой клей отвердевает при 120 °С и работает до 2000 °С, Использование фосфатных связок в качестве клеев рассмотрено в работе [143]. [c.119]
Пример 25. Определить уменьшение величины коэффициента теплопередачи в теплообменнике, у иоторого поверхность теплообмена из легированной стали заменена стеклянной. Коэффициенты теплоотдачи следующие со сто роны греющей среды С] = 3000 ккал м час °С, со стороны налреваемой среды вг = = 2000 ккал л час С. Толщина (металлической стенки б мм, стеклявной 7 мм. Коэффициент теплопроводности хром оникелевой стали, согласно табличным данным. равен X = 24 ккал/м час С, а стекла X = 0,64 ккал/м час °С. [c.157]
ХРОМИСТАЯБРОНЗ А-брон-за, легированная хромом. Наиболее распространена X. б. марки БрХ0,5 (0,4—1,0% Сг, остальное — медь). Ее плотность 8,9 г см , т-ра плавления 1080° С, удельное электрическое сопротивление (в отожженном состоянии) 0,02 ом-мм /м, коэфф. теплопроводности 0,8 кал/см-сек-град, модуль норм, упругости 13 800 кгс/мм , предел текучести (после старения и холодного деформирования) 40 кгс/мм" , относительное удлинение 10—12%, относительное сужение 40—45% Я.В = 130 ч- 150. X. б. отличается хорошими мех. св-вами, повышенной т-рой рекристаллизации, высокой электропроводностью, жаропрочностью, легко поддается обработке в горячем и холодном состоянии. Хром ограниченно растворим в [c.701]Среди металлов серебро % == 1,0 кал/см-сек-град при 20°) и медь (0,94) отличаются особо высокой теплопроводностью [15]. Если требуется металл с возможно меньшей теплопроводностью и достаточной, прочностью, то применяют такие сплавы, как нейзильбер (0,06) или контрацид (0,03) и хромай. Очень незначительной теплопроводностью обладают также В1, 5Ь и Hg (0,02). С составом и прочими свойствами сплавов можно ознакомиться в приведенной литературе. Данные о свойствах и методах обработки щелочных и щелочноземельных металлов приведены в разд. 1.9. [c.12]
Предъявляемым требованиям для осуществления пиролизных процессов при разных температурах удовлетворяют металлические материалы. Они являются компактными, плотными, теплопроводными, термически устойчивыми с удовлетворительными данными по механическим свойствам. Металургическим путем из них можно получать трубы и использовать их в качестве реакторов для пиролиза углеводородов при температурах, при которых эти реакторы обеспечивают ведение процесса пиролиза, не разрушаясь сами от действия газовой коррозии. Металлические материалы удовлетворяют многим техническим требованиям и условиям эксплуатации их в пирогенных установках. Однако в высокотемпературных пиролизных процессах могут быть применимы только высокохимически стойкие металлические материалы. Нержавеющие стали с содержанием 8, 10—12, 14% N1 и 18% Сг, с 25% N1 и 20% Сг, остальное железо, применяемые для пиролиза углеводородов при температурах 750° и выше, легко окисляются, они взаимодействуют с серой и разрушаются, науглероживаются и охрупчива-ются сталь содержит в своем составе дорогостоящий никель, более нужный в других отраслях техники. По стоимости нержавеющая сталь дороже в Р/г—2 раза железо-хромо-алюминиевого сплава № 2. [c.327]
Частичная замена линоксина В1 линолеумном цементе может быть достигнута в)ведением некоторых коллоидных металлических солей, как, например, еафтен тов алюминия, железа, хрома и т. д. Ф Для расширения линолеумиого производства, помимо исходных органических материалов, необходимых для образования органического связующего — линоксина и смол, громадное зяачение имеет органический наполнитель — пробковая мука. Применяя древесную муку или целлюлозные наполнители, нельзя получить слоистый материал, по своим свойствам отвечающий линолеуму с Цробков ой мукой, в особенности в отношении веса, теплопроводности и т. д. [c.301]
Электроды дуговых плазмотронов — единственная их расходуемая часть. Электроды могут быть выполнены из меди и медных сплавов, вольфрама, циркония, графита и других материалов в зависимости от конструкции плазмотрона, его назначения и пр. Стержневой (фронтальный) электрод (нри прямой полярности — катод) выполнен чаш е всего из торированного или лантанированного вольфрама (для уменьшения работы выхода электрона). Выходной электрод такого плазмотрона (анод при прямой полярности) имеет трубчатую форму и изготавливается из меди, имеющей высокую теплопроводность. Если оба электрода имеют трубчатую форму, то они обычно выполнены из меди. Легирование меди серебром приводит к уменьшению потерь металла за счет окисления это особенно эффективно при работе в кислороде или кислородсодержащих средах. Легирование меди цирконием или хромом увеличивает ее твердость и устойчивость к окислению. Электроды плазмотронов охлаждаются очищенной от растворимых солей водой при повышенном давлении (4 15 атм). Для некоторых приложений применяют деионизованную воду. Расход охлаждающей воды — 40 1000 л/мин в зависимости от параметров плазмотрона. [c.71]
chem21.info
Теплопроводность цветных металлов, теплоемкость и плотность сплавов: таблицы при различных температурах

Теплопроводность цветных металлов и технических сплавов
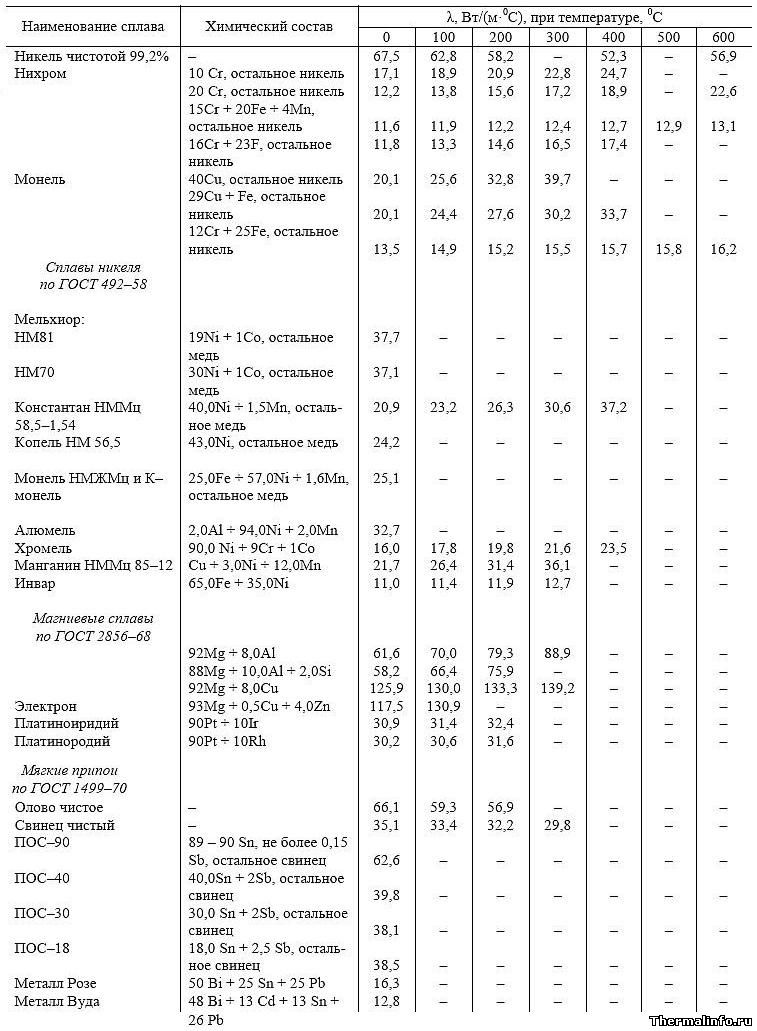
В таблице представлены значения теплопроводности металлов (цветных), а также химический состав металлов и технических сплавов в интервале температуры от 0 до 600°С.
Цветные металлы и сплавы: никель Ni, монель, нихром; сплавы никеля (по ГОСТ 492-58): мельхиор НМ81, НМ70, константан НММц 58,5-1,54, копель НМ 56,5, монель НМЖМц и К-монель, алюмель, хромель, манганин НММц 85-12, инвар; магниевые сплавы (по ГОСТ 2856-68), электрон, платинородий; мягкие припои (по ГОСТ 1499-70): олово чистое, свинец, ПОС-90, ПОС-40, ПОС-30, сплав Розе, сплав Вуда.
По данным таблицы видно, что высокую теплопроводность (при комнатной температуре) имеют магниевые сплавы и никель. Низкая же теплопроводность свойственна нихрому, инвару и сплаву Вуда.
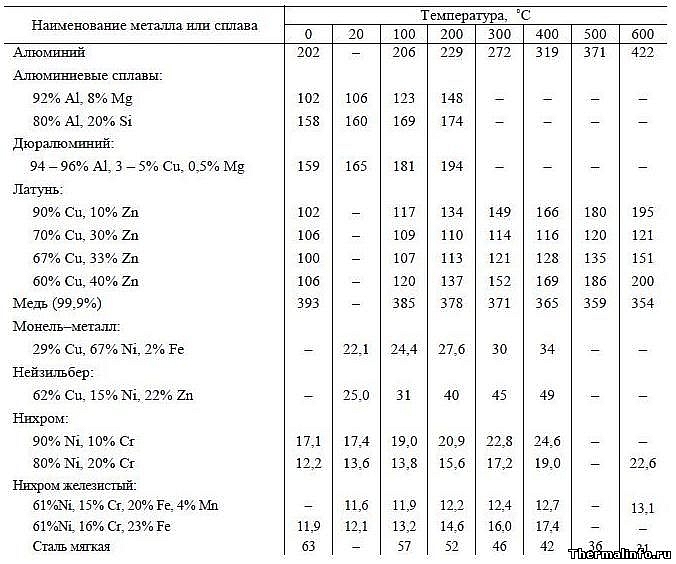
Коэффициенты теплопроводности алюминиевых, медных и никелевых сплавов
Теплопроводность металлов, алюминиевых, медных и никелевых сплавов в таблице дана в интервале температуры от 0 до 600°С в размерности Вт/(м·град).Металлы и сплавы: алюминий, алюминиевые сплавы, дюралюминий, латунь, медь, монель, нейзильбер, нихром, нихром железистый, сталь мягкая. Алюминиевые сплавы имеют большую теплопроводность, чем латунь и сплавы никеля.
Коэффициенты теплопроводности сплавов
В таблице даны значения теплопроводности сплавов в интервале температуры от 20 до 200ºС.Сплавы: алюминиевая бронза, бронза, бронза фосфористая, инвар, константан, манганин, магниевые сплавы, медные сплавы, сплав Розе, сплав Вуда, никелевые сплавы, никелевое серебро, платиноиридий, сплав электрон, платинородий.
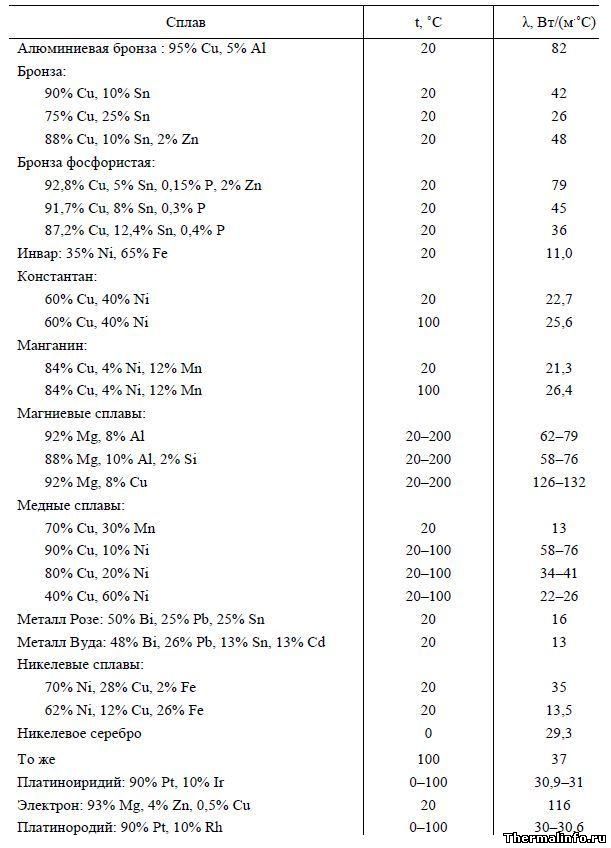
Удельное сопротивление и температурный коэффициент расширения (КТР) металлической проволоки (при 18ºС)
В таблице указаны значения удельного электрического сопротивления и КТР металлической проволоки, выполненной из различных металлов и сплавов.Материал проволоки: алюминий, вольфрам, железо, золото, латунь, манганин, медь, никель, константан, нихром, олово, платина, свинец, серебро, цинк.Как видно из таблицы, нихромовая проволока имеет высокое удельное электрическое сопротивление и успешно применяется в качестве спиралей накаливания нагревательных элементов множества бытовых и промышленных устройств.
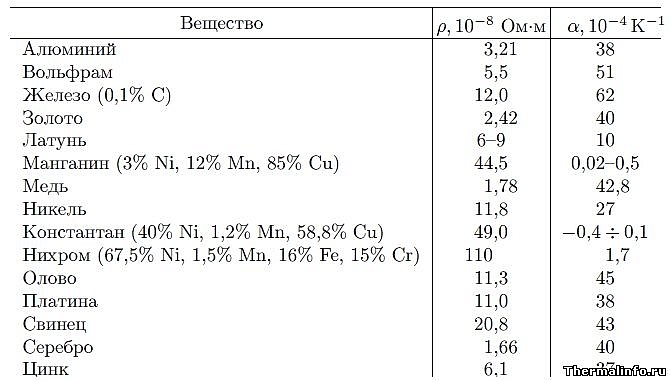
Удельная теплоемкость цветных сплавов
В таблице приведены величины удельной (массовой) теплоемкости двухкомпонентных и многокомпонентных цветных сплавов, не содержащих железа, при температуре от 123 до 1000К. Теплоемкость указана в размерности кДж/(кг·град).Дана теплоемкость следующих сплавов: сплавы, содержащие алюминий, медь, магний, ванадий, цинк, висмут, золото, свинец, олово, кадмий, никель, иридий, платина, калий, натрий, марганец, титан, сплав висмут — свинец — олово, сплав висмут-свинец, висмут — свинец — кадмий, алюмель, сплав липовица, нихром, сплав розе.
Также существует отдельная таблица, где представлена удельная теплоемкость металлов при различных температурах.

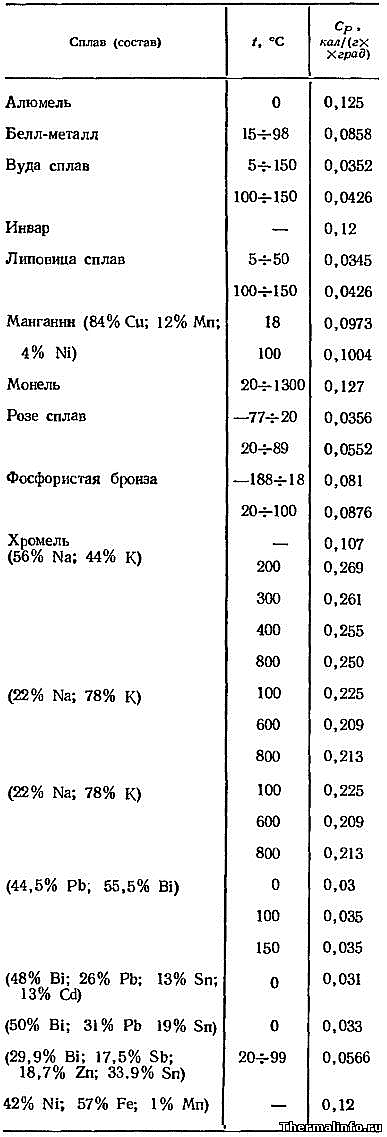
Удельная теплоемкость многокомпонентных специальных сплавов
Удельная (массовая) теплоемкость многокомпонентных специальных сплавов приведена в таблице при температуре от 0 до 1300ºС.Размерность теплоемкости кал/(г·град).Теплоемкость специальных сплавов: алюмель, белл-металл, сплав Вуда, инвар, липовица сплав, манганин, монель, сплав Розе, фосфористая бронза, хромель, сплав Na-K, сплав Pb — Bi, Pb — Bi — Sn, Zn — Sn — Ni — Fe — Mn.
Плотность сплавов
Представлена таблица значений плотности сплавов при комнатной температуре.Приведены следующие сплавы: бронза, оловянистая, фосфористая, дюралюминий, инвар, константан, латунь, магналиум, манганин, монель — металл, платино — иридиевый сплав, сплав Вуда, сталь катаная, литая.

ПРИМЕЧАНИЕ: Будьте внимательны! Плотность сплавов в таблице указана в степени 10-3. Не забудьте умножить на 1000!Например, плотность катанной стали изменяется в пределах от 7850 до 8000 кг/м3.
Источники:
- Михеев М.А., Михеева И.М. Основы теплопередачи.
- Физические величины. Справочник. А.П. Бабичев, Н.А. Бабушкина, А.М. Братковский и др.; Под ред. И.С. Григорьева, Е.З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
- Таблицы физических величин. Справочник. Под ред. акад. И.К. Кикоина. М.: Атомиздат, 1976. — 1008 с.
- Шелудяк Ю.Е., Кашпоров Л.Я. и др. Теплофизические свойства компонентов горючих систем. М. 1992. — 184 с.
- Промышленные печи. Справочное руководство для расчетов и проектирования. 2–е издание, дополненное и переработанное, Казанцев Е.И. М.: «Металлургия», 1975.- 368 с.
thermalinfo.ru
Плотность хрома (Cr), значение и примеры
Плотность хрома и другие его физические свойства
Парамагнитен, хорошо проводит электрический ток, отличается высокой твердостью, царапает стекло.

Рис. 1. Хром. Внешний вид.
На механические свойства титана сильно влияет наличие примесей. Чистый хром пластичный, а содержащий даже небольшую долю примесей азота и кислорода – хрупкий и ломкий. Хром технической чистоты легко раскалывается и истирается в порошок.
Основные константы хрома приведены в таблице ниже.
Таблица 1. Физические свойства и плотность хрома.
|
Плотность, г/см3 |
7,23 |
|
Температура плавления, oС |
1860 |
|
Температура кипения, oС |
2680 |
|
Тип кристаллической решетки |
объемно-центрированная кубическая |
Распространенность хрома в природе
Содержание хрома в земной коре составляет 0,012% (масс.) и сравнимо с содержанием хлора (0,013% (мас.)). Важнейший промышленный минерал хрома – хромистый железняк FeCr2O4. Реже встречаются другие минералы – крокоит – PbCrO4, хромовая охра Cr2O3.
Краткая характеристика химических свойств и плотность хрома
При умеренных температурах хром устойчив на воздухе: хромированные изделия не тускнеют, так как тонкая и прозрачная пленка оксида надежно защищает их от окисления.
Хром легко растворяется в соляной кислоте (без доступа воздуха) с образование сине-голубых растворов солей хрома (II):
Cr + 2HCl = CrCl2 + h3.
С кислотами-окислителями – концентрированной серной и азотной – при комнатной температуре хром не взаимодействует. Не растворяется он и в царской водке. Интересно, что очень чистый хром не реагирует даже с разбавленной серной кислотой, хотя причина этого до сих пор не установлена. При выдерживании в концентрированной азотной кислоте хром пассивируется, т.е. утрачивает способность взаимодействовать с разбавленными кислотами.
Примеры решения задач

| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Свойства оксидов металлов

Теплофизические свойства оксидов металлов
В таблице представлены теплофизические свойства оксидов (спеченных окислов) металлов при различной температуре. Даны значения свойств следующих плотных спеченных окислов: оксиды алюминия и магния Al2O3, MgO, оксид кальция CaO, оксид кремния SiO2, оксид никеля NiO, оксид титана TiO, оксид циркония ZrO2, оксид урана UO2, оксид тория ThO2, оксид плутония PuO2
Теплопроводность спеченных окислов в таблице указана при температуре от 127 до 1727 °С в зависимости от пористости. Коэффициент линейного теплового расширения (КТР) указан при температуре от 300 до 400 К. Плотность оксидов металлов дана при комнатной температуре.
Теплопроводность спеченных оксидов металлов зависит от чистоты и кристаллической структуры исходных порошков, метода и степени прессования и режимов спекания. Теплопроводность порошкообразных окислов зависит от плотности, размера зерен и влажности; для любых порошкообразных оксидов металлов (не спеченных) теплопроводность лежит в пределах 0,1…1,1 Вт/(м·град).
В таблице даны следующие свойства оксидов металлов:
- температура плавления, К;
- коэффициент линейного теплового расширения (КТР), 1/град;
- плотность, кг/м3;
- пористость, %;
- коэффициент теплопроводности, Вт/(м·град).
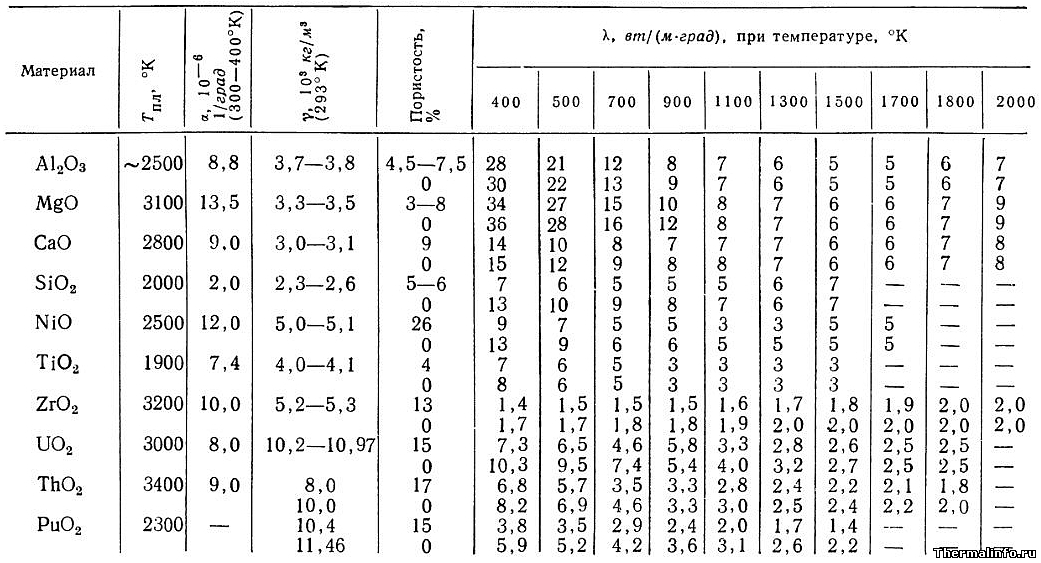
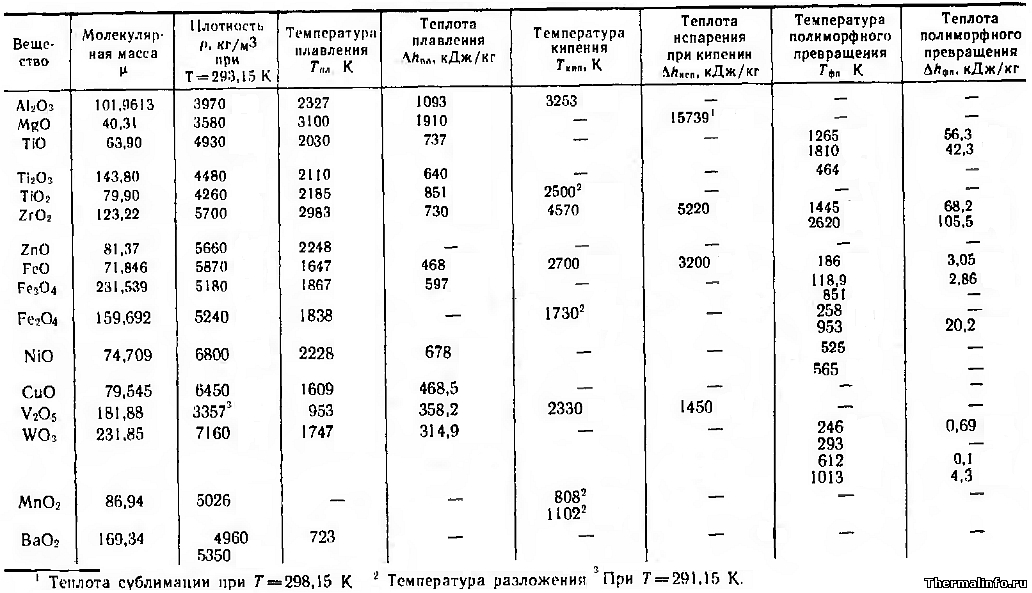
Основные свойства оксидов металлов
В таблице приведены основные свойства оксидов металлов при комнатной температуре.Свойства указаны для следующих оксидов металлов: Al2O3, MgO, TiO, Ti2O3, TiO2, ZrO2, оксид цинка ZnO, оксиды железа FeO, Fe3O4, Fe2O3, NiO, оксид меди CuO, оксид ванадия V2O5, оксид вольфрама WO3, оксид марганца MnO2, оксид бария BaO2.
Даны следующие свойства оксидов металлов:
- молекулярная масса оксида;
- плотность, кг/м3;
- температура плавления, К;
- теплота плавления, кДж/кг;
- температура кипения, К;
- теплота испарения при кипении, кДж/кг;
- температура полиморфного превращения, К;
- теплота полиморфного превращения, кДж/кг.
Теплопроводность плотных спеченных оксидов металлов
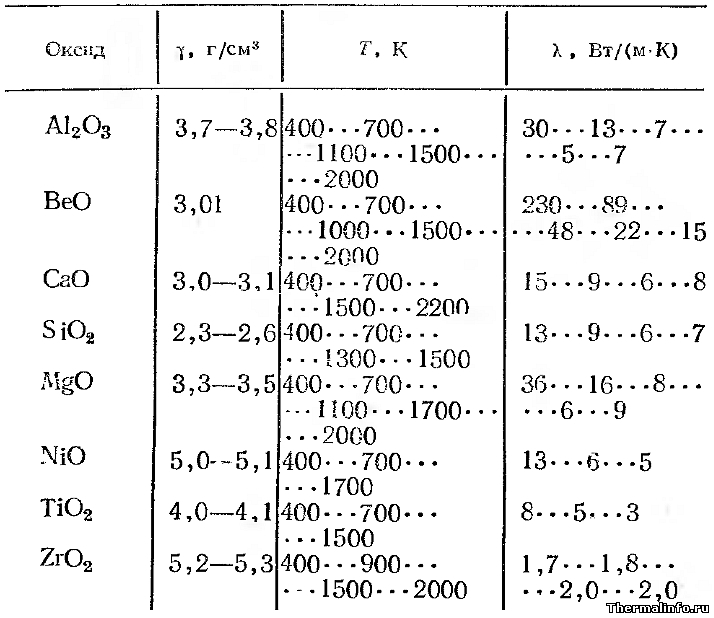
В таблице представлены значения теплопроводности плотных спеченных оксидов металлов (пористость равна нулю) в зависимости от температуры.Теплопроводность дана для следующих оксидов металлов: оксид алюминия Al2O3, оксид бериллия BeO, оксид кальция CaO, оксид кремния SiO2, оксид магния MgO, оксид никеля NiO, оксид титана TiO2, оксид циркония ZrO2. Теплопроводность окислов металлов приведена при температуре от 100 до 2000 К.
Видно, что в основном, теплопроводность оксидов снижается при росте температуры. В таблице также указана плотность оксидов металлов (оксидная керамика) при комнатной температуре.
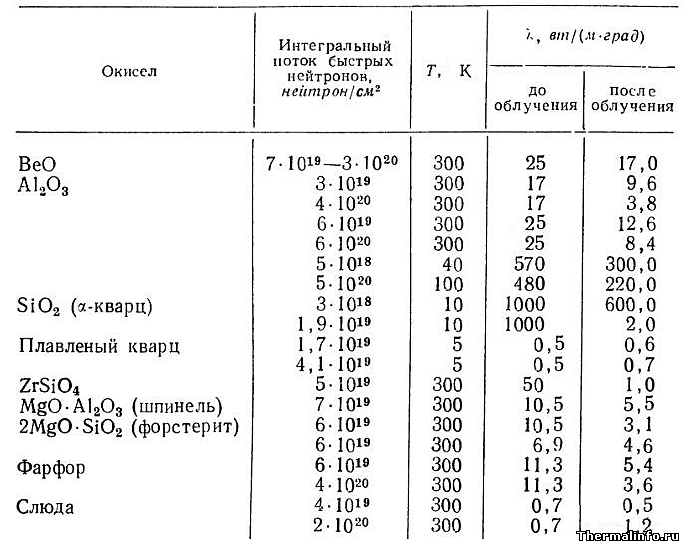
Влияние нейтронного облучения на теплопроводность спеченных оксидов металлов
В таблице представлены значения теплопроводности плотных спеченных оксидов металлов до и после облучения потоком быстрых нейтронов.Теплопроводность оксидов дана при комнатной температуре и при сверхнизких температурах (5…100 К).
Значения указаны для следующих оксидов металлов: BeO, Al2O3, SiO2 (α-кварц), плавленый кварц, ZrSiO4, шпинель, форстерит, фарфор, слюда.Как видно из таблицы, значение коэффициента теплопроводности оксидов металлов при их облучении потоком быстрых нейтронов, в основном снижается.
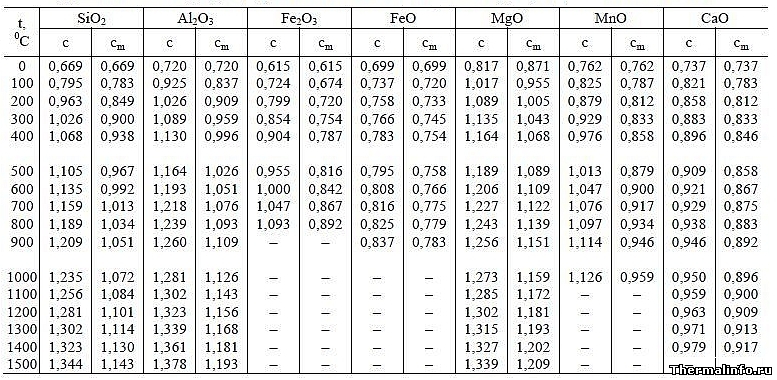
Теплоемкость оксидов металлов
В таблице указаны значения истинной и средней удельных теплоемкостей оксидов металлов в зависимости от температуры.Теплоемкости (размерность кДж/(кг·град)) даны при температуре от 0 до 1500°С.Значения представлены для следующих оксидов металлов (компонентов огнеупорных материалов и шлаков): SiO2, Al2O3, Fe2O3, FeO, MgO, MnO, CaO.
Примечание: Истинная теплоемкость соответствует указанной температуре, а значение средней теплоемкости Cm приведено для интервала температуры от 0°С до указанной в таблице. По данным таблицы видно, что удельная (массовая) теплоемкость оксидов металлов при увеличении их температуры также увеличивается.
Источники:
- Физические величины. Справочник. А.П. Бабичев, Н.А. Бабушкина, А.М. Братковский и др.; Под ред. И.С. Григорьева, Е.З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
- Чиркин В.С. Теплофизические свойства материалов ядерной техники. М.: Атомиздат, 1967 — 474 с.
- Шелудяк Ю.Е., Кашпоров Л.Я. и др. Теплофизические свойства компонентов горючих систем. М. 1992. — 184 с.
- Промышленные печи. Справочное руководство для расчетов и проектирования. 2–е издание, дополненное и переработанное, Казанцев Е.И. М.: «Металлургия», 1975. — 368 с.
thermalinfo.ru
Физические свойства
Хром – серебристый металл с плотностью 7200 кг/м3. В свободном виде — голубовато-белый металл с кубической объемно-центрированной решеткой, а = 0,28845 нм, z = 2, пространств. При температуре 39 °C (312 К) переходит из парамагнитного состояния в антиферромагнитное (точка Нееля).
Хром является самым твердым металлом (твердость по шкале Мооса 8.5).
При обычных температурах существует в виде -модификации и имеет кубическую объемно-центрированную решетку[10].
Атомный объем хрома численно равен 7,23 см, плотность – 7,19 г/см3. Ионизационный потенциал – 652,83 кДж/моль, удельная теплоемкость – 22,550 Дж/г•моль•К, энтропия кристаллического состояния – 23,56, а газообразного 174,33 при температуре 298 К. Некоторые свойства элемента приведены в виде таблиц с указанием на различные источники [5].
Таблица 1. [2].
| Элемент | Атомный номер | Температура плавления, К | Температура кипения, К | ||||||
| [3] | [16] | [7] | Рекомендованная | [3] | [16] | [7] | Рекомендованная | ||
| Cr | 24 | 2148 | 2130 | 2130 | 2130 | 2472 | 2945 | 2958 | 2950 |
Таблица 2.
Радиусы элемента, 10-10м
| Элемент | Атомные | Металлические | Ковалентные | Ионные | ||||
| [16] | [11] | [16] | заряд | Ri | заряд | Ri | ||
| Cr | 1,85 | 1,27 | 1,28 | 1,18 | +3 | 0,69 | +6 | 0,52 |
Таблица 3. [2].
| Элемент | Коэффициент теплопроводности [3] | Электроотрицательность элемента, эВ | Электропроводность | ||
| Т,К | Коэффициент, Вт/(м•К) | [6] | [16] | 0,0774 | |
| Cr | 293 | 67 | 1,6 | 1,66 | |
Вывод. Хром – серебристый металл с плотностью 7200 кг/м3. В свободном виде — голубовато-белый металл с кубической объемно-центрированной решеткой, а = 0,28845 нм, z = 2, пространств. При температуре 39 °C (312 К) переходит из парамагнитного состояния в антиферромагнитное.
Химические свойства элемента и его соединений
Электронная конфигурация [Ar] 3d5 4s1. Как известно, в природе мало элементов с атомными массами, которые совпадают с атомными массами, указанными в периодической системе. Чаще эти численные значения складываются как средняя масса всех изотопов. И хром не исключение. Средняя атомная масса 24Cr 51,99616, во всей массе хрома на его изотоп 50Crприходится 4,31% массы, на 52Cr– 83,76%, 53Cr– 9,55%, 54Cr– 2,38% [5].
Изотоп 51Cr радиоактивен, распадается с захватом орбитальных электронов (с выделением -квантов), а период его полураспада 27,7 суток.
Таблица 4. Масса и энергия образования изотопов.
| Изотоп | Масса, 1/12 m 12C | Погрешность | Энергия образования, кэВ | Погрешность | Коэффициент захвата тепловых нейтронов |
| 48Cr | 47,953760 | 210 | 411710 | 200 | - |
| 49Cr | 48,951271 | 12 | 422101 | 16 | - |
| 50Cr | 49,9460507 | 45 | 435035 | 12 | 16,3 |
| 51Cr | 50,9447859 | 45 | 444284 | 12 | 3,1 |
| 52Cr | 51,9405137 | 36 | 456335 | 12 | 0,73 |
| 53Cr | 52,9406511 | 37 | 464278 | 13 | 17,5 |
| 54Cr | 53,9388794 | 48 | 474000 | 13 | 0,3 |
| 55Cr | 54,941080 | 150 | 480020 | 140 | - |
| 56Cr | 55,940640 | 160 | 488500 | 150 | - |
Таблица 5. [16]
| Атом | Потенциалы ионизации атома, эВ | Сродство к электрону | ||||||||
| 1 эВ | 2 эВ | 3 эВ | 4 эВ | 5 эВ | 6 эВ | 7 эВ | 8 эВ | эВ | кДж | |
| 24Cr | 6,7653 | 16,498 | 32,12 | 50,9 | 72,4 | 96,0 | 167,6 | 193,9 | 0,98 0,35 | 95 34 |
Химически хром довольно инертен вследствие образования на его поверхности прочной тонкой пленки оксида. Он не окисляется на воздухе даже в присутствии влаги, а при нагревании окисление проходит только на поверхности. Хром пассивируется разбавленной и концентрированной азотной кислотой, царской водкой, и даже при кипячении металла с этими реагентами растворяется лишь незначительно. Пассивированный азотной кислотой хром, в отличие от металла без защитного слоя, не растворяется в разбавленных серной и соляной кислотах даже при длительном кипячении в растворах этих кислот. Тем не менее, в определенный момент начинается быстрое растворение, сопровождающееся вспениванием от выделяющегося водорода – из пассивной формы хром переходит в активированную, не защищенную пленкой оксида:
Cr + 2HCl → CrCl2 + h3↑
Если в процессе растворения добавить азотной кислоты, то реакция сразу прекращается – хром снова пассивируется.
При нагревании металлический хром соединяется с галогенами, серой, кремнием, бором, углеродом и некоторыми другими элементами:
Cr + 2F2 → CrF4 (с примесью CrF5)
2Cr + 3Cl2 → 2CrCl3
2Cr + 3S → Cr2S3
Cr + C → смесь Cr23C6 + Cr7C3.
При нагревании хрома с расплавленной содой на воздухе, нитратами или хлоратами щелочных металлов получаются соответствующие хроматы(VI):
2Cr + 2Na2CO3 + 3O2 → 2Na2CrO4 + 2CO2.
Хром устойчив на воздухе (однако тонкоизмельченный пирофорен) и к действию воды. Нагретый в кислороде до ~ 300°С сгорает с образованием Сr2О3. Растворы щелочей на хром не действуют, расплавленные щелочи в отсутствие воздуха очень медленно реагируют с выделением Н2. Фтор действует на хром выше 350°С. Сухой хлор начинает реагировать при температуре выше 300° С, влажный хлор начинает действовать уже с 80°С. Бром и йод действуют на хром при температуре красного каления, также как HF и HCl.
При 2000°C сгорает с образованием зелёного оксида хрома(III) Cr2O3, обладающего амфотерными свойствами. Сплавляя Cr2O3 со щелочами получают хромиты:
Cr2O3 + 2NaOH → 2NaCrO2 + h3O. Хром в соединениях проявляет степени окисления: +2, +3, +4, +6. У хрома наиболее стабильной является степень окисления +3.
Растворы солей хрома (II) можно получить взаимодействием металлического хрома кислот–неокислителей:
Cr + 2H+ → Cr2+ + h3↑,
или восстановлением соединений хрома (III) цинком:
2CrCl3 + Zn → ZnCl2 + 2CrCl2
Растворы солей хрома (II) окрашены в синий цвет аквакомплекса [Cr(h3O)6]2+ . При термическом разложении карбонила хрома Cr(СО)6 получают красный основной оксид хрома(II) CrO. Коричневый или желтый гидроксид Cr(OH)2 со слабоосновными свойствами осаждается при добавлении щелочей к растворам солей хрома(II).
Для того чтобы избежать окисления Cr2+ в Cr3+, эксперимент чаще всего проводят в сосуде, закрытом пробкой, снабженной клапаном Бунзена (это резиновая трубка, закрытая с одного конца, с прорезью, через которую выходят пары, если в сосуде повышается давление, что препятствует прониканию атмосферного кислорода внутрь сосуда) или под слоем бензола.
Безводные соли Сr(П) бесцветны. Водные растворы имеют небесно-голубой цвет; из них выделяют кристаллы различных гидратированных солей — CrS04•5h30, CrС12•4Н20, CrВr2•6Н20, Cr(С104)2•6НгО и [Cr(ОСОСН3)2]•2Н20. Соединения Cr(П) — сильные восстановители. Наиболее распространенный среди них K4[Cr(CN)3] — кристаллическое соединение синего цвета; водные растворы его окрашены в красно-оранжевый цвет и устойчивы только в течение ~ 3 часов. Они быстро восстанавливают до металлов соединения Ag(I), Pb(II), Hg(II), T1(I), Bi(III), As(V), Sb(V), Sn(IV), Te(IV), медленно - Cu(I), Cu(II), Cd(II). Наиболее устойчивым соединением является ацетат хрома (II). Он имеет структуру димера, в котором два атома хрома непосредственно связаны между собой (Cr—Cr). Такие связи характерны для переходных элементов.
Ацетат хрома представляет собой одно из самых распространенных, самых устойчивых и легкодоступных соединений Cr(П). Он выпадает в виде трудно растворимого красного кристаллического вещества при приливании раствора хлорида Cr(П) к очень концентрированному раствору ацетата натрия [9].
H 3C
3C
C Ch4
C
O O
O O
h3O Cr Cr Oh3
O O
O O
C
C
h4C Ch5
Рисунок 1. [9].
studfiles.net
|
Материал |
Коэффициент линейного теплового расширения |
|
|
(10-6 м/(мK)) / ( 10-6 м/(мoС)) |
(10-6 дюйм/(дюйм oF)) |
|
| ABS (акрилонитрил-бутадиен-стирол) термопласт | 73.8 | 41 |
| ABS - стекло, армированное волокнами | 30.4 | 17 |
| Акриловый материал, прессованный | 234 | 130 |
| Алмаз | 1.1 | 0.6 |
| Алмаз технический | 1.2 | 0.67 |
| Алюминий | 22.2 | 12.3 |
| Ацеталь | 106.5 | 59.2 |
| Ацеталь , армированный стекловолокном | 39.4 | 22 |
| Ацетат целлюлозы (CA) | 130 | 72.2 |
| Ацетат бутират целлюлозы (CAB) | 25.2 | 14 |
| Барий | 20.6 | 11.4 |
| Бериллий | 11.5 | 6.4 |
| Бериллиево-медный сплав (Cu 75, Be 25) | 16.7 | 9.3 |
| Бетон | 14.5 | 8.0 |
| Бетонные структуры | 9.8 | 5.5 |
| Бронза | 18.0 | 10.0 |
| Ванадий | 8 | 4.5 |
| Висмут | 13 | 7.3 |
| Вольфрам | 4.3 | 2.4 |
| Гадолиний | 9 | 5 |
| Гафний | 5.9 | 3.3 |
| Германий | 6.1 | 3.4 |
| Гольмий | 11.2 | 6.2 |
| Гранит | 7.9 | 4.4 |
| Графит, чистый | 7.9 | 4.4 |
| Диспрозий | 9.9 | 5.5 |
| Древесина, пихта, ель | 3.7 | 2.1 |
| Древесина дуба, параллельно волокнам | 4.9 | 2.7 |
| Древесина дуба , перпендикулярно волокнам | 5.4 | 3.0 |
| Древесина, сосна | 5 | 2.8 |
| Европий | 35 | 19.4 |
| Железо, чистое | 12.0 | 6.7 |
| Железо, литое | 10.4 | 5.9 |
| Железо, кованое | 11.3 | 6.3 |
| Золото | 14.2 | 8.2 |
| Известняк | 8 | 4.4 |
| Инвар (сплав железа с никелем) | 1.5 | 0.8 |
| Инконель (сплав) | 12.6 | 7.0 |
| Иридий | 6.4 | 3.6 |
| Иттербий | 26.3 | 14.6 |
| Иттрий | 10.6 | 5.9 |
| Кадмий | 30 | 16.8 |
| Калий | 83 | 46.1 - 46.4 |
| Кальций | 22.3 | 12.4 |
| Каменная кладка | 4.7 - 9.0 | 2.6 - 5.0 |
| Каучук, твердый | 77 | 42.8 |
| Кварц | 0.77 - 1.4 | 0.43 - 0.79 |
| Керамическая плитка (черепица) | 5.9 | 3.3 |
| Кирпич | 5.5 | 3.1 |
| Кобальт | 12 | 6.7 |
| Констанан (сплав) | 18.8 | 10.4 |
| Корунд, спеченный | 6.5 | 3.6 |
| Кремний | 5.1 | 2.8 |
| Лантан | 12.1 | 6.7 |
| Латунь | 18.7 | 10.4 |
| Лед | 51 | 28.3 |
| Литий | 46 | 25.6 |
| Литая стальная решетка | 10.8 | 6.0 |
| Лютеций | 9.9 | 5.5 |
| Литой лист из акрилового пластика | 81 | 45 |
| Магний | 25 | 14 |
| Марганец | 22 | 12.3 |
| Медноникелевый сплав 30% | 16.2 | 9 |
| Медь | 16.6 | 9.3 |
| Молибден | 5 | 2.8 |
| Монель-металл (никелево-медный сплав) | 13.5 | 7.5 |
| Мрамор | 5.5 - 14.1 | 3.1 - 7.9 |
| Мыльный камень (стеатит) | 8.5 | 4.7 |
| Мышьяк | 4.7 | 2.6 |
| Натрий | 70 | 39.1 |
| Нейлон, универсальный | 72 | 40 |
| Нейлон, Тип 11 (Type 11) | 100 | 55.6 |
| Нейлон, Тип 12 (Type 12) | 80.5 | 44.7 |
| Нейлон литой , Тип 6 (Type 6) | 85 | 47.2 |
| Нейлон, Тип 6/6 (Type 6/6), формовочный состав | 80 | 44.4 |
| Неодим | 9.6 | 5.3 |
| Никель | 13.0 | 7.2 |
| Ниобий (Columbium) | 7 | 3.9 |
| Нитрат целлюлозы (CN) | 100 | 55.6 |
| Окись алюминия | 5.4 | 3.0 |
| Олово | 23.4 | 13.0 |
| Осмий | 5 | 2.8 |
| Палладий | 11.8 | 6.6 |
| Песчаник | 11.6 | 6.5 |
| Платина | 9.0 | 5.0 |
| Плутоний | 54 | 30.2 |
| Полиалломер | 91.5 | 50.8 |
| Полиамид (PA) | 110 | 61.1 |
| Поливинилхлорид (PVC) | 50.4 | 28 |
| Поливинилденфторид (PVDF) | 127.8 | 71 |
| Поликарбонат (PC) | 70.2 | 39 |
| Поликарбонат - армированный стекловолокном | 21.5 | 12 |
| Полипропилен - армированный стекловолокном | 32 | 18 |
| Полистирол (PS) | 70 | 38.9 |
| Полисульфон (PSO) | 55.8 | 31 |
| Полиуретан (PUR), жесткий | 57.6 | 32 |
| Полифенилен - армированный стекловолокном | 35.8 | 20 |
| Полифенилен (PP), ненасыщенный | 90.5 | 50.3 |
| Полиэстер | 123.5 | 69 |
| Полиэстер, армированный стекловолокном | 25 | 14 |
| Полиэтилен (PE) | 200 | 111 |
| Полиэтилен - терефталий (PET) | 59.4 | 33 |
| Празеодимий | 6.7 | 3.7 |
| Припой 50 - 50 | 24.0 | 13.4 |
| Прометий | 11 | 6.1 |
| Рений | 6.7 | 3.7 |
| Родий | 8 | 4.5 |
| Рутений | 9.1 | 5.1 |
| Самарий | 12.7 | 7.1 |
| Свинец | 28.0 | 15.1 |
| Свинцово-оловянный сплав | 11.6 | 6.5 |
| Селен | 3.8 | 2.1 |
| Серебро | 19.5 | 10.7 |
| Скандий | 10.2 | 5.7 |
| Слюда | 3 | 1.7 |
| Сплав твердый (Hard alloy) K20 | 6 | 3.3 |
| Сплав хастелой (Hastelloy) C | 11.3 | 6.3 |
| Сталь | 13.0 | 7.3 |
| Сталь нержавеющая аустенитная (304) | 17.3 | 9.6 |
| Сталь нержавеющая аустенитная (310) | 14.4 | 8.0 |
| Сталь нержавеющая аустенитная (316) | 16.0 | 8.9 |
| Сталь нержавеющая ферритная (410) | 9.9 | 5.5 |
| Стекло витринное (зеркальное, листовое) | 9.0 | 5.0 |
| Стекло пирекс, пирекс | 4.0 | 2.2 |
| Стекло тугоплавкое | 5.9 | 3.3 |
| Строительный (известковый) раствор | 7.3 - 13.5 | 4.1-7.5 |
| Стронций | 22.5 | 12.5 |
| Сурьма | 10.4 | 5.8 |
| Таллий | 29.9 | 16.6 |
| Тантал | 6.5 | 3.6 |
| Теллур | 36.9 | 20.5 |
| Тербий | 10.3 | 5.7 |
| Титан | 8.6 | 4.8 |
| Торий | 12 | 6.7 |
| Тулий | 13.3 | 7.4 |
| Уран | 13.9 | 7.7 |
| Фарфор | 3.6-4.5 | 2.0-2.5 |
| Фенольно-альдегидный полимер без добавок | 80 | 44.4 |
| Фторэтилен пропилен (FEP) | 135 | 75 |
| Хлорированный поливинилхлорид (CPVC) | 66.6 | 37 |
| Хром | 6.2 | 3.4 |
| Цемент | 10.0 | 6.0 |
| Церий | 5.2 | 2.9 |
| Цинк | 29.7 | 16.5 |
| Цирконий | 5.7 | 3.2 |
| Шифер | 10.4 | 5.8 |
| Штукатурка | 16.4 | 9.2 |
| Эбонит | 76.6 | 42.8 |
| Эпоксидная смола , литая резина и незаполненные продукты из них | 55 | 31 |
| Эрбий | 12.2 | 6.8 |
| Этилен винилацетат (EVA) | 180 | 100 |
| Этилен и этилакрилат (EEA) | 205 | 113.9 |
|
Эфир виниловый |
16 - 22 | 8.7 - 12 |
tehtab.ru