Диоксид-дихлорид хрома. Хрома диоксид
диоксид хрома - это... Что такое диоксид хрома?
диоксид хромаchromium dioxide
Англо-русский словарь технических терминов. 2005.
- диоксид хлора
- диоксид церия
Смотреть что такое "диоксид хрома" в других словарях:
Диоксид-дихлорид хрома — Диоксид дихлорид хрома … Википедия
ХРОМА ОКСИДЫ — ХРОМА ОКСИДЫ: оксид CrO секстиоксид Cr2O3, диоксид CrO2 и триоксид (хромовый ангидрид) CrO3. Cr2O3 темно зеленые кристаллы; компонент футеровок металлургических печей, шлифовальных и притирочных паст; пигмент для стекла и керамики; катализатор… … Большой Энциклопедический словарь
хрома оксиды — хрома оксиды: оксид CrO, сесквиоксид Cr2O3, диоксид CrO2 и триоксид CrO3. Cr2O3 тёмно зелёные кристаллы; компонент футеровок металлургических печей, шлифовальных и притирочных паст; пигмент для стекла и керамики; катализатор многих процессов.… … Энциклопедический словарь
Бромид хрома(II) — Общие Систематическое наименование Бромид хрома (II) Химическая формула CrBr2 Физические свойства Состояние (ст. усл.) твёрдое вещество желтовато белого цве … Википедия
Бромид хрома(III) — Общие Систематическое наименование Бромид хрома(III) Традиционные названия Бромистый хром Химическая формула CrBr3 Физические свойства … Википедия
Карбид хрома(II) — Карбид хрома(II) … Википедия
Оксид хрома(VI) — Общие … Википедия
Хлорид хрома(III) — Хлорид хрома(III) … Википедия
Оксид хрома(III) — Оксид хрома(III) … Википедия
Гидроксид хрома(III) — Гидроксид хрома (III) сложное неорганическое вещество с химической формулой Cr(OH)3. Описание Гидроксид хрома (III) амфотерный гидроксид. Серо зеленого цвета, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид CrO(OH). Не… … Википедия
Сульфат хрома(III) — Эта статья или раздел нуждается в переработке. Пожалуйста, улучшите статью в соответствии с правилами написания статей. Сульфат хро … Википедия
Диоксид-дихлорид хрома - Gpedia, Your Encyclopedia
Диокси́д-дихлори́д хро́ма (хло́ристый хроми́л) — жидкость тёмно-красного цвета, дымится во влажном воздухе вследствие гидролиза, растворим в неполярных растворителях (четыреххлористый углерод, дихлорметан, сероуглегод). Сильный окислитель, при контакте воспламеняет фосфор, серу, скипидар и др., используется в органическом синтезе для получения альдегидов окислением метиларенов и терминальных алкенов.
Синтез
Хромилхлорид впервые был синтезирован Берцелиусом взаимодействием концентрированной серной кислоты со смесью хлорида натрия и бихромата калия с последующей отгонкой продукта:
K2Cr2O7+4NaCl+6h3SO4→2CrO2Cl2+2KHSO4+4NaHSO4+3h3O{\displaystyle {\mathsf {K_{2}Cr_{2}O_{7}+4NaCl+6H_{2}SO_{4}\rightarrow 2CrO_{2}Cl_{2}+2KHSO_{4}+4NaHSO_{4}+3H_{2}O}}}Он также может быть получен реакцией К2СrО4 (или других хроматов или бихроматов) с концентрированной соляной кислотой (или хлоридами щелочных металлов) и серной кислоты в качестве обезвоживающего агента, CrO2Cl2 в этих случаях отделяется с помощью простой дистилляции, однако, поскольку при нагревании в присутствии серной кислоты хромилхлорид разлагается с образованием сульфата хрома (III) и выделением хлора, выходы в этих методах не превышают 50%. Хлористый хромил может быть получен действием серной кислоты на хлорохромат калия.
Максимальные выходы хлористого хромила получаются при реакции сухого хлороводорода с хромовым ангидридом CrO3) в присутствии серной кислоты на холоду[2].
Свойства
Диоксид-дихлорид хрома является молекулярным соединением. Это означает, что в жидких и твердых агрегатных состояниях молекулы данного соединения будут взаимодействовать исключительно с помощью сил Ван-дер-Ваальса. Такая слабая связь приводит к низким температурам плавления и кипения.
Реакционная способность
Хлористый хромил формально являющийся хлорангидридом хромовой кислоты CrO2Cl2 - сильный электрофил с подвижными атомами хлора, легко замещающимися под действием различных нуклеофилов.
Полный гидролиз ведет к образованию хромовой и соляная кислоты:
CrO2Cl2+2h3O⟶ h3CrO4+2HCl{\displaystyle {\mathsf {CrO_{2}Cl_{2}+2H_{2}O\longrightarrow \ H_{2}CrO_{4}+2HCl}}}Гидролиз идет через промежуточное образование хлорхромовой кислоты (формально - монохлорангидрида хромовой кислоты):
CrO2Cl2 + h3O →{\displaystyle \to } HOCrO2Cl + HCl ,избыток хлорид-иона в растворе способствует сдвигу равновесия в сторону хлорхромата: так, гидролиз хромилхлорида в насыщенным водном растворе хлорида калия ведет к образованию хлорохромата калия (соли Пелиго):
CrO2Cl2 + h3O + KCl →{\displaystyle \to }Хлористый хромил в четыреххлористом углероде реагирует с изоцианатом серебра с образованием темно-красного раствора хромилизоцианата:
CrO2Cl2 + 2 AgOCN →{\displaystyle \to } CrO2(OCN)2 + 2 AgCl ,образующийся хромилизоцианат нестабилен и разлагается со взрывом при упаривании раствора при пониженном давлении:
CrO2(OCN)2→{\displaystyle \to } CrO2 + 2 CO + N2С азотным ангидридом хлористый хромил образует хромилнитрат и нитронилхлорида:
CrO2Cl2 + 2 N2O5→{\displaystyle \to } CrO2(NO3)2 + 2 NO2ClРеакция с нитратом хлора также ведет к хромилнитрату[3]:
CrO2Cl2 + 2 ClNO3→{\displaystyle \to }Хромилхлорид с алкилароматическими соединениями образует аддукты (комплексы Этара) в отношении 2:1, дальнейшее разложение этих аддуктов ведет к образованию ароматических альдегидов (реакция Этара):
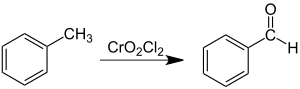
С алкенами хромилхлорид образует комплексы Этара в отношении 1:1, пути их разложения зависят от строения алкенов, терминальные алкены таким образом могут быть окислены взаимодействием с хромилхлоридом и последующим восстановлением реакционной смеси цинковой пылью до альдегидов с препаративными выходами:
R1R2C=Ch3→{\displaystyle \to } R1R2CH-CHOОпасность применения
Дихлорид-диоксид хрома является очень агрессивным реагентом. Активно реагирует с водой, спиртами и другими сильно электрофильными веществами, такими как VOCl3, TiCl4 и SO2Cl2.
При гидролизе дихлорид-диоксида хрома образуются агрессивные вещества: хлористый водород и соединения шестивалентного хрома (CrVI). CrVI может приводить к хромосомным аберрациям. Частые воздействия на кожу веществом могут привести к её изъязвлениям. Хлористый водород может привести к поражению органов дыхания, вплоть до летального исхода. Воздействие паров диоксида-дихлорида хрома может привести к раздражению дыхательных путей, сильному раздражению глаз и ожогам кожи и глаз. При попадании внутрь может вызвать серьёзные отравления и повреждения внутренних органов.
См. также
Примечания
Литература
- Реми Г. т.II // Курс неорганической химии. — М.: Мир, 1966. — 836 с.
www.gpedia.com
диоксид хрома - это... Что такое диоксид хрома?
1) Engineering: chromium dioxide
2) Telecommunications: chrome dioxide
Универсальный русско-английский словарь. Академик.ру. 2011.
- диоксид хлора
- диоксид церия
Смотреть что такое "диоксид хрома" в других словарях:
Диоксид-дихлорид хрома — Диоксид дихлорид хрома … Википедия
ХРОМА ОКСИДЫ — ХРОМА ОКСИДЫ: оксид CrO секстиоксид Cr2O3, диоксид CrO2 и триоксид (хромовый ангидрид) CrO3. Cr2O3 темно зеленые кристаллы; компонент футеровок металлургических печей, шлифовальных и притирочных паст; пигмент для стекла и керамики; катализатор… … Большой Энциклопедический словарь
хрома оксиды — хрома оксиды: оксид CrO, сесквиоксид Cr2O3, диоксид CrO2 и триоксид CrO3. Cr2O3 тёмно зелёные кристаллы; компонент футеровок металлургических печей, шлифовальных и притирочных паст; пигмент для стекла и керамики; катализатор многих процессов.… … Энциклопедический словарь
Бромид хрома(II) — Общие Систематическое наименование Бромид хрома (II) Химическая формула CrBr2 Физические свойства Состояние (ст. усл.) твёрдое вещество желтовато белого цве … Википедия
Бромид хрома(III) — Общие Систематическое наименование Бромид хрома(III) Традиционные названия Бромистый хром Химическая формула CrBr3 Физические свойства … Википедия
Карбид хрома(II) — Карбид хрома(II) … Википедия
Оксид хрома(VI) — Общие … Википедия
Хлорид хрома(III) — Хлорид хрома(III) … Википедия
Оксид хрома(III) — Оксид хрома(III) … Википедия
Гидроксид хрома(III) — Гидроксид хрома (III) сложное неорганическое вещество с химической формулой Cr(OH)3. Описание Гидроксид хрома (III) амфотерный гидроксид. Серо зеленого цвета, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид CrO(OH). Не… … Википедия
Сульфат хрома(III) — Эта статья или раздел нуждается в переработке. Пожалуйста, улучшите статью в соответствии с правилами написания статей. Сульфат хро … Википедия
universal_ru_en.academic.ru
|
РЫНОК ХРОМА НЕОБРАБОТАННОГО, ДИОКСИДА ХРОМА, ТРИОКСИДА ХРОМА, ДИХРОМАТА НАТРИЯ 2011 ПОЛНОЕ ОГЛАВЛЕНИЕСПИСОК ТАБЛИЦСЕГМЕНТАЦИЯ ПО ТНВЭД
МИРОВАЯ ТОРГОВЛЯ Мировая торговля хромом необработанным
РОССИЙСКАЯ ТОРГОВЛЯ Российская торговля хромовыми соединениями по обощенным видам продукции
СПИСОК ИСТОЧНИКОВ
СПИСОК ТАБЛИЦ Таблица 1 – Номенклатура внешней торговли хромом необработаннымТаблица 2 – Номенклатура внешней торговли диоксидами и триоксидами хромаТаблица 3 – Номенклатура внешней торговли дихроматом натрияТаблица 4 – Мировой импорт хрома необработанного по странам получателям в 2009-2010 гг., тТаблица 5 – Цены мирового импорта хрома необработанного по странам получателям в 2009-2010 гг., $/тТаблица 6 – Мировой экспорт хрома необработанного по странам отправителям в 2009-2010 гг., тТаблица 7 – Цены мирового экспорта хрома необработанного по странам отправителям в 2009-2010 гг., $/тТаблица 8 – Мировой импорт оксидов и гидроксидов хрома по странам получателям в 2009-2010 гг., тТаблица 9 – Цены мирового импорта оксидов и гидроксидов хрома по странам получателям в 2009-2010 гг., $/тТаблица 10 – Мировой экспорт оксидов и гидроксидов хрома по странам отправителям в 2009-2010 гг., тТаблица 11 – Цены мирового экспорта оксидов и гидроксидов хрома по странам отправителям в 2009-2010 гг., $/тТаблица 12 – Мировой импорт триоксидов хрома по странам получателям в 2009-2010 гг., тТаблица 13 – Цены мирового импорта оксидов и гидроксидов хрома по странам получателям в 2009-2010 гг., $/тТаблица 14 – Мировой экспорт триоксидов хрома по странам отправителям в 2009-2010 гг., тТаблица 15 – Цены мирового экспорта триоксидов хрома по странам отправителям в 2009-2010 гг., $/тТаблица 16 – Мировой импорт дихромата натрия по странам получателям в 2009-2010 гг., тТаблица 17 – Цены мирового импорта дихромата натрия по странам получателям в 2009-2010 гг., $/тТаблица 18 – Мировой экспорт дихромата натрия по странам отправителям в 2009-2010 гг., тТаблица 19 – Цены мирового экспорта дихромата натрия по странам отправителям в 2009-2010 гг., $/тТаблица 20 – Российский импорт хромовых соединений по укрупненным видам продукции в 2009-2010 гг., тТаблица 21 – Российский экспорт хромовых соединений по укрупненным видам продукции в 2009-2010 гг., тТаблица 22 – Российский импорт хромовых соединений по уточненным видам продукции в 2009-2010 гг., тТаблица 23 – Российский экспорт хромовых соединений по уточненным видам продукции в 2009-2010 гг., тТаблица 24 – Российский импорт хромовых соединений по видам продукции и странам отправления в 2009-2010 гг., тТаблица 25 – Российский экспорт хромовых соединений по видам продукции и странам назначения в 2009-2010 гг., тТаблица 26 – Российский импорт хромовых соединений по видам продукции и регионам получения в 2009-2010 гг., тТаблица 27 – Российский экспорт хромовых соединений по видам продукции и регионам отправления в 2009-2010 гг., тТаблица 28 – Адресный справочник Российских импортеров хромовых соединенийТаблица 29 – Адресный справочник Российских экспортеров хромовых соединений |
www.metalresearch.ru
Способ получения порошка двуокиси хрома для носителей магнитной записи
Изобретение относится к магнитной записи информации. Целью изобретения является обеспечение высокоплотной, высокочастотной записи путем получения частиц двуокиси хрома со средним объемом (2-10).10-4 мкм3. Исходную пасту, содержащую, мас.%: хромовый ангидрид 65,35-70,5 окись хрома 25,95-34,97 модифицирующие добавки 0,28-4,0 вода остальное, предварительно разогревают в автоклаве со средней скоростью 15-30 град/ч и ведут разложение при 330-350°С и давлении 350-450 атм. 1 табл.
СОЮЗ СОВЕТСКИХ
СОЦИАЛ ИСТИЧЕСНИХ
РЕСПУБЛИК
„,SU„„5 0996
А1 (ц) з С 01 G 37/027 Н Ol F 1/06
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н А BTOPCHOMY СВИДЕТЕЛЬСТВУ
Цель изобретения — синтез порошка для изготовления но ителей высокоплот ной, высокочастотной записи путем снижения объема частиц порошка двуокиси хрома до 2-10 ° 10 мкм
-4 3
Пример 1. Гидротермальный синтез двуокиси хрома производится из смеси хромового ангидрида (СгОз) и окиси хрома (Cr Oз), К 274,4 г хромового ангидрида добавляется 1,3816 r окиси железа и 0,7256. г окиси сурьмы и вода (118 г). Далее к смеси постепенно добавляется окись хрома Сг Оз (137,2 r) при непрерывном перемешивании, причем температура смеси доо стигает 70 С.
После этого пасту переливают в пробирку из кварцевого стекла, которую устанавливают в автоклаве, в ко— торый предварительно налито 17 г воды»
ГОСУДАРСТВЕННЫЙ КОМИТЕТ
f10 ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР
1 (21) 4317712/23-26 (22) 20,!)7,87 (46) 15.06.90. Бюл. Р 22 (71) Шосткинский филиал Всесоюзного государственного научно-исследовательского и проектного института химикофотографической промышленности и Ленинградский государственный универси тет (72) !1, Г. Осмоловский, Л. Ю. Иванова, С. М., Козьмина, А. А. Соломко и Э. А. Кужелева (53) 661.876(088,8) (56) 1!атент США !» - 4524008, кл. С 01 G 37/027, опублик. 18.06.85. (54) СПОСОБ 1!ОЛУЧЕНИЯ ПОРОШКА ДБУОКИИзобретение относится к магнитной записи информации, в частности к получению магнитного порошка двуокиси хрома для изготовления носителей магнитной записи.
Одной иэ основных характеристик магнитного порошка является размер магнитных частиц, так как частотные и шумовые характеристики носителя магнитной записи связаны с размером частиц.
Как известно длина частиц не долж1 на превышать половину длины волны записываемого сигнала, и объем частиц . должен лежать в однодоменной области.
Кроме того, для получения высокой отдачи при записи высоких частот тре-, буется повышение числа частиц в единице объема носителя, что может быть обеспечено только за счет уменьшения среднего объема частиц.2
GÈ ХРОМА ДЛЯ НОСИТЕЛЕЙ ИАГ11ИТНОЙ ЗАПИСИИ (57) Изобретение относится к магнитной з апис и информации. 11елью из о бретения является обеспечение высокоплотной, высокочастотной записи путем получения частиц двуокиси хрома со средним. объемом (2-10) 10 "мкм . Исходную пасту, содержащую, мас,/: хромовый ангидрид 63,35-70,5; окись хрома 25,95-34,97; модифицирующие добавки 0,28-4,0; вода остальное, предварительно разогревают в автоклаве со средней скоростьи 15-30 град/ч и ведут разложение при 330-350 С и давлени 350-450 атм. I табл.
1570996
Синтез проводится путем разогрева пасты до 330 С, причем давление достигает 350 атм.
Разогрев смеси ведется со средней скоростью .! 1 0 град/ч .. Далее образец
5 ибвлекают, перетирают, сушат при 110120 С 2 ч, Полученный порошок имеет
: коэрцитивную силу 502 Э, состоит из кристаллов средней длины 0,60 мкм и толщиной 0,044 мкм (средний объем
11,6,10 мкмжд) .
Ч р и,м е р 2. Синтез двуокиси хрома проводится также, как в примере 1, но скорость разогрева до 330 С составляет 15 ч, т.е. она равна
22 град/ч. В результате получается порошок, имеющий коэрцитивную силу
514 Э и состоящий из кристаллов со средней длиной 0,25 мкм и тол ниной 20
0,041:мкм (средний объем 4,2 ° 10 мкм), пригодный для высокочастотной высокоплотной записи.
Из сравнения примеров 1 и 2 ясно, что использование одного отличитель- 25 ного признака- — присутствия н пласте окиси хрома, недостаточно для того, чтобы достичь желаемой величины кристаллов и он достигается .только за счет одновремейного использования 30 обоих отличительных признаков (как в примере 2).
Пример 3. В бочку. вводится хромовый ангидрид 114,4 кг, окись железа 4,31 кг, окись сурьмы 274 г, и к ним приливается вода 43,5 л. Смесь перемешивается и далее к ней добавляется окись хрома (43,5 кг), смесь .перемешивается мешалкой до достижения о температуры 70 С, далее смесь перели- 40 нается в одну из четырех бочек для синтеза. Аналогичным образом подготавливаются остальные- бочки. Бочки ставятся друг на друга в автоклав емкостью 800 л, н который предваритель- 45 но налито 28 л воды и начинается нагрев исходной смеси. Нагрев ведут до тех пор, пока..температура смеси достигнет 350 С, а давление 450 атм скорость разогрева смеси составляет
20,6 град/ч, время разогрева 17 ч.
После охлаждения прореагиранавшую смесь сушат при 160 С, далее иэнлека-, о ют из бочек, прокаливают н токе воздуха при 320 С, стабилизируют раство ром Ма 80 > (267 кг Ма ВО >/м з раствора), дистиллируют, промывают дистиллированной водой, сушат в распылительной сушилке. Полученный. продукт имеет коэрцитивную силу 642 Э, обладает частицами со средйей длиной 0,390 мкм и толщиной 0,026 мкм (средний объем
2,6:10 MKM) и пригоден для применения в носителях высокоплотной высокочастотной записи.
Пример 4, Синтез двуокиси хрома проводят также, как в примере 3, но cMecb разогревают до 350 С со скоростью 15 град/ч, Обработку порошка проводят также, как в примере 3. Полученный продукт имеет коэрцитивную силу 613 Э, обладает частицами со средней длиной 0,240 мкм и средней толщиной О, 025 мкм и средним объемом 2,02», rl0 4 мкм и пригоден для применения в носителях высокоплотной высокочастотной записи, П,р и м е р 5. Синтез двуокиси хрома проводят также, как в примере
3, но смесь разогревают до 350 С .со скоростью 30 град/ч. Обработку порошка проводят также,, как в примере 3, Полученный продукт имеет козрцитивную силу 610 Э обладает частицами со средней длиной 0,580 мкм и средней толщиной 0,041 мкм (средний объем
-4
9,8 l0 мкм) и пригоден в качестве носителя высокочастотной высокоплотной записи.
П р .и м е р 6. Исходную пасту для синтеза готовят так же, как в примере 1, но с иными количествами исходных компонентов, г: хромовый ангидрид
274,4; окись хрома 146,8; окись сурьмы 0,6718; окись железа 0,8958, вода
1!8, что отвечает составу, мас,X:
Хромовый ангидрид 65,3
Окись хрома 34,9
Окись сурьмы 0,12
Окись железа 0,16
Пасту, помещенную в пробирку кварцевого стекла, устанавливают в автоклав, в которьп предварительно залито 17 мл воды. Содержимое автоклава нагревают со скоростью 22 град/ч до
350 С. При этом давление достигает
310 атм.
В .результате синтеза после сушки при 110-120 C в течение 2 ч, получен порошок со следующими характеристиками H, Э, 520; длина, мкм 0,342; толщина мкм 0,038; объем, мкм 4,94 » . 10
Пример 7. Исходную пасту для синтеза готонят так же, как в примере 1, но с иным количеством исходных компойен тон, г:
5 157099
Хромоный ангицрид 274 4
Окись хрома 101 О
Э
Окись сурьмы О, 8063
Окись железа, 13,011
Вода 118 5 что отвечает составу, мас,X
Хромовый ангидрид 70,5
Окись хрома 25,95
Окись .сурьмы О 207
У 1О
Окись железа 3,343
Нагрев пасты ведется в пробирке кварцевого стекла, н автоклаве предварительно вливается 17 мл воды. Íàгрев проводится до 320 С, причем давление увеличивается до 360 атм, В результате синтеза после сушки при 110-120 С в течение 2 ч, полученный матeриал имеет следующие характе— ристики:
Н, Э 720; Длина, мкм 0,351;
Толщина, мкм 010271 Объем, м 3
2,56 10
1 !
Пример 8, Способ подготовки добавки окиси сурьмы и состав исходной пасты был осуществлен по патенту
С!ЯА В 4524008.
Окись сурьмы 30 r, хромовый ангидрид 200 r и нода 120 г были нагреты о до температуры 120 С при интенсивном перемешивании механической мешалкой и выдержаны при этой температуре
30 мин. 8,22 r смеси были введены в пасту, содержащую 269,7 г хромового ангидрида, 137,0 r окиси хрома, 101,4 r воды, 1,562 r окиси железа.
Таким образом, состав пасты по относительному содержанию всех компонентов отвечал составу пасты по примеру 1 патента СИА N - 4524008. Синтез бып проведен в гидротермальных условиях примера 2: в автоклав емкостью
0 5 л воды влита дополнительно вода в количестве 17 мл, паста находилась в пробирке иэ кварцевого стекла, разогрев пасты до температуры 330ОС проведен за 15 ч, т.е. скорость разогрева с;>ставляла 22 град/ч, причем давление достчгло 335 атм, т.е, 4786 фунтов/дюйм 2. В результате синтеза после сушки при 110-120 С 2 ч был получен порошок, имеющий удельную поверхность 41 м /г. Коэрцитивная си2 ла и размер .кристаллов определены следующие: Н, 3. 503:! длина, мкм, 0,252; толщина, мкм 0,021; объем, мкм 1111-10, Относительная длину/толщина составила 12,0.
6 6
Пример 9 (прототип ). Синтез порошка проведен из пасты, приготовленной такж же образом, как и в примере 8, т.е. с предварительной подгоТоВКоА добанки - окиси сурьмы, путем ее нагрева н водном растворе хромового ангидрида.
Загрузка всех компонентов н автоклав была та же, что н примере 8, отличие от проведения синтеза по примеру 8 заключалось в увеличении скорости разогрева пасты. Конечная температура синтеза и давление, как и в примере 8,составили 330 С и 335 атм,разогрев проведен за 10 ч 30 мин, т,е, скорость разогрева составила
31,4 град/ч. В результате синтеза после извлечения продукта и сушки при о
20 110-120 С за 2 ч был получен порошок с удельной поверхностью 36,3 м /r u со следующими коэрцитивной силой и размерами кристаллов: Н, Э 560; длина, мкм О, 268; толщина, мкм О, 0227;
25 объем, мкм 1,38 10 . При соотношении длина — толщина 11,8.
Таким образом, характеристики порошка черезвычайно близки к свойствам, приведенным в примере 1 предлагаемого
30 зспертизой прототипа (уд.понерхность
36 м /г, Н 575 Э).
Существует предпочтительное содержание окиси хрома н исходной смеси: при соотношении массы хромового ангидрида к массе окиси хрома менее
1,9, часть окиси хрома остается не переработанной н двуокись хрома и, следовательно, происходит-ухудшение эксплуатадионных качеств магнитного порошка — снижается концентрация магнитных частиц в рабочем слое носителя записи за счет присутствия второй твердой фазы и качество распределения частиц по рабочему слою, кроме того, появляется повышенная абразивность магнитной ленты, приводящая к повышенному истиранню магнитной головки. При массоном соотношении хромового ангидрида и окиси хрома равно 2,7 по сравнению с соотношением, равным 2, на
257 возрастает парциальное давление кислорода в автоклаве, что янляется нежелательным фактором при проведении
55, синтеза и приводит к необходимости снижения суммарной загрузки. Поэтому оптимальным соотношением масс хромового ангидрида и. окиси хрома является область 1,9-2,7 (см. табл). Ука1570996
Объем час з тип, мкм
Годе рж. окиси жеСодерж. окиси сурь > мас, X
При Содермамер, ние Сто
II> ма с, X
Годер>к.
Cl О ° . мас Л
Козрцитивная сила, Э
Г.реди яя скорость разогрева, град/ч
Пригоден или нет для высокоплотной записи леза, мас.7.! 66,327
33,1636 0,1754 0,3346 110
Пе пригоден, поскольку большая скорость разогрева
Пригоден
66,327
70,4069
70,4069
65,35
70;5
54,62
54 62
22 514
1 5 613.
30 610
22 520 .
22 720
22 503
3t,4 560
4>2 IO
2,02 1О
9,8 10
4,94 10
2,56 10
1,11 ° 1О
1,38 ° IO
33,1636
26>7719
26,7719 34, 97
25,95
15, 91
15,91
О, 1754
О,! 686 . 0,1686
0,12
0,20
3,49
3,49
0,3340
2, 6526
2,6526
0,16
3,8
I 82
I,82
Не пригоден
Пример II 9 проведен в условиях прототипа.
Составитель Н.Наумова
Редактор В,Ковтун Техред Л.Сердюкова
Корректор М,Пожо
Заказ 1483 .. Тираж 405 Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., д..4/5
Производственно-издательский комбинат "Патент, r.Óæãoðîä, ул. Гагарина,101 занная область соотношения масс хро- . мового ангидрида и окису хрома, выраженная в 1 мас.Х, отвечает составам
Хромовый ангидрид 65,35-70,50
Окись хрома 25195 "34ю 37 при суммарном количестве. модифицирующих добавок от О, 28 до 4; 0 мас, X.
Ограничение максимальной скорости равогрева смеси 30 град/ч связано с тем, что при более высокой скорости разогрева снижается число зЫ ективно работающих микрокристаллов смешанных оксидов, на которых кристаллизуется двуокись хрома, так как кристаллиэа- !5 ция двуокиси хрома начинается и продолжает идти на ограниченном числе микрокристаллов-зародышей. В результате образуются более крупные крис-, таллы двуокиси хрома, ймеющие размеры, не обеспечивающие их применение в высокоплотной записи из-за большого объема.
Ограничение минимальной скорости разогрева 15 град/ч связано с тем, 25 что образуются слишком малые по объему кристаллы двуокиси хрома и по размеру кристаллов двуокись хрома переходит. в область, близкую к суперпарамагнитной, что препятствует осуществ- 30 лению магнитной записи.
Указанная область. размеров кристаллов 2-10 10 мкм з двуокиси хрома одновременно обеспечивает достижение максимума козрцитивной силы порошка, причем дальнейшее уменьшение размеров кристаллов приводит к уменьшению коэрцитивной силы эа счет начала перехода магнитного материала в суперпарамагнитное состояние.
Таким образом, изобретение позволяет синтезировать носители магнитной записи со средним размером частиц
2-10 10 мкмз, обеспечивающие высокоплотную, высокочастотную запись, Формулаизобретения
Способ получения поро1вка двуокиси хрома для носителей магнитной записи, включающий предварительный разогрев исходной пасты, содержащей хромовый ангидрид, окись хрома, модифицирующие добавки, и ее разложение при 330350 С и 350-450 ат, о т л и ч а ю— шийся тем, что, с целью обеспечения высокоплотной, высокочастотной записи путем получения частиц со средним объемом (2-1 0) 1 О 4 мкм, используют исходную пасту, содержащую, мас.Х:
Хромовый ангидрид 65,35-70,5
Окись хрома 25, 95-34, 37
Модифицирующие добавки 0,28-4,0 и разогрев исходной пасты до температуры разложения ведут со средней скоростью !5-30 град/ч, !




www.findpatent.ru
Диоксид-дихлорид хрома - Википедия
Материал из Википедии — свободной энциклопедии
Диокси́д-дихлори́д хро́ма (хло́ристый хроми́л) — жидкость тёмно-красного цвета, дымится во влажном воздухе вследствие гидролиза, растворим в неполярных растворителях (четыреххлористый углерод, дихлорметан, сероуглегод). Сильный окислитель, при контакте воспламеняет фосфор, серу, скипидар и др., используется в органическом синтезе для получения альдегидов окислением метиларенов и терминальных алкенов.
Синтез[ | ]
Хромилхлорид впервые был синтезирован Берцелиусом взаимодействием концентрированной серной кислоты со смесью хлорида натрия и бихромата калия с последующей отгонкой продукта:
K2Cr2O7+4NaCl+6h3SO4→2CrO2Cl2+2KHSO4+4NaHSO4+3h3O{\displaystyle {\mathsf {K_{2}Cr_{2}O_{7}+4NaCl+6H_{2}SO_{4}\rightarrow 2CrO_{2}Cl_{2}+2KHSO_{4}+4NaHSO_{4}+3H_{2}O}}}Он также может быть получен реакцией К2СrО4 (или других хроматов или бихроматов) с концентрированной соляной кислотой (или хлоридами щелочных металлов) и серной кислоты в качестве обезвоживающего агента, CrO2Cl2 в этих случаях отделяется с помощью простой дистилляции, однако, поскольку при нагревании в присутствии серной кислоты хромилхлорид разлагается с образованием сульфата хрома (III) и выделением хлора, выходы в этих методах не превышают 50%. Хлористый хромил может быть получен действием серной кислоты на хлорохромат калия.
Максимальные выходы хлористого хромила получаются при реакции сухого хлороводорода с хромовым ангидридом CrO3) в присутствии серной кислоты на холоду[2].
Свойства[ | ]
Диоксид-дихлорид хрома является молекулярным соединением. Это означает, что в жидких и твердых агрегатных состояниях молекулы данного соединения будут взаимодействовать исключительно с помощью сил Ван-дер-Ваальса. Такая слабая связь приводит к низким температурам плавления и кипения.
Реакционная способность[ | ]
Хлористый хромил формально являющийся хлорангидридом хромовой кислоты CrO2Cl2 - сильный электрофил с подвижными атомами хлора, легко замещающимися под действием различных нуклеофилов.
Полный гидролиз ведет к образованию хромовой и соляная кислоты:
CrO2Cl2+2h3O⟶ h3CrO4+2HCl{\displaystyle {\mathsf {CrO_{2}Cl_{2}+2H_{2}O\longrightarrow \ H_{2}CrO_{4}+2HCl}}}Гидролиз идет через промежуточное образование хлорхромовой кислоты (формально - монохлорангидрида хромовой кислоты):
CrO2Cl2 + h3O →{\displaystyle \to } HOCrO2Cl + HCl ,избыток хлорид-иона в растворе способствует сдвигу равновесия в сторону хлорхромата: так, гидролиз хромилхлорида в насыщенным водном растворе хлорида калия ведет к образованию хлорохромата калия (соли Пелиго):
CrO2Cl2 + h3O + KCl →{\displaystyle \to } KCrO3Cl + 3 HClХлористый хромил в четыреххлористом углероде реагирует с изоцианатом серебра с образованием темно-красного раствора хромилизоцианата:
CrO2Cl2 + 2 AgOCN →{\displaystyle \to } CrO2(OCN)2 + 2 AgCl ,образующийся хромилизоцианат нестабилен и разлагается со взрывом при упаривании раствора при пониженном давлении:
CrO2(OCN)2→{\displaystyle \to } CrO2 + 2 CO + N2С азотным ангидридом хлористый хромил образует и нитронилхлорида:
CrO2Cl2 + 2 N2O5→{\displaystyle \to } CrO2(NO3)2 + 2 NO2ClРеакция с также ведет к хромилнитрату[3]:
CrO2Cl2 + 2 ClNO3→{\displaystyle \to } CrO2(NO3)2 + 2 Cl2Хромилхлорид с алкилароматическими соединениями образует аддукты (комплексы Этара) в отношении 2:1, дальнейшее разложение этих аддуктов ведет к образованию ароматических альдегидов (реакция Этара):
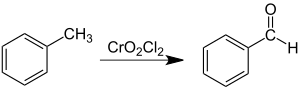
С алкенами хромилхлорид образует комплексы Этара в отношении 1:1, пути их разложения зависят от строения алкенов, терминальные алкены таким образом могут быть окислены взаимодействием с хромилхлоридом и последующим восстановлением реакционной смеси цинковой пылью до альдегидов с препаративными выходами:
R1R2C=Ch3→{\displaystyle \to } R1R2CH-CHOОпасность применения[ | ]
Дихлорид-диоксид хрома является очень агрессивным реагентом. Активно реагирует с водой, спиртами и другими сильно электрофильными веществами, такими как VOCl3, TiCl4 и SO2Cl2.
При гидролизе дихлорид-диоксида хрома образуются агрессивные вещества: хлористый водород и соединения шестивалентного хрома (CrVI). CrVI может приводить к хромосомным аберрациям. Частые воздействия на кожу веществом могут привести к её изъязвлениям. Хлористый водород может привести к поражению органов дыхания, вплоть до летального исхода. Воздействие паров диоксида-дихлорида хрома может привести к раздражению дыхательных путей, сильному раздражению глаз и ожогам кожи и глаз. При попадании внутрь может вызвать серьёзные отравления и повреждения внутренних органов.
См. также[ | ]
Примечания[ | ]
Литература[ | ]
- Реми Г. т.II // Курс неорганической химии. — М.: Мир, 1966. — 836 с.
encyclopaedia.bid
диоксид хрома - это... Что такое диоксид хрома?
диоксид хромаchromium dioxide
Русско-английский политехнический словарь. Академик.ру. 2011.
- диоксид хлора
- диоксид церия
Смотреть что такое "диоксид хрома" в других словарях:
Диоксид-дихлорид хрома — Диоксид дихлорид хрома … Википедия
ХРОМА ОКСИДЫ — ХРОМА ОКСИДЫ: оксид CrO секстиоксид Cr2O3, диоксид CrO2 и триоксид (хромовый ангидрид) CrO3. Cr2O3 темно зеленые кристаллы; компонент футеровок металлургических печей, шлифовальных и притирочных паст; пигмент для стекла и керамики; катализатор… … Большой Энциклопедический словарь
хрома оксиды — хрома оксиды: оксид CrO, сесквиоксид Cr2O3, диоксид CrO2 и триоксид CrO3. Cr2O3 тёмно зелёные кристаллы; компонент футеровок металлургических печей, шлифовальных и притирочных паст; пигмент для стекла и керамики; катализатор многих процессов.… … Энциклопедический словарь
Бромид хрома(II) — Общие Систематическое наименование Бромид хрома (II) Химическая формула CrBr2 Физические свойства Состояние (ст. усл.) твёрдое вещество желтовато белого цве … Википедия
Бромид хрома(III) — Общие Систематическое наименование Бромид хрома(III) Традиционные названия Бромистый хром Химическая формула CrBr3 Физические свойства … Википедия
Карбид хрома(II) — Карбид хрома(II) … Википедия
Оксид хрома(VI) — Общие … Википедия
Хлорид хрома(III) — Хлорид хрома(III) … Википедия
Оксид хрома(III) — Оксид хрома(III) … Википедия
Гидроксид хрома(III) — Гидроксид хрома (III) сложное неорганическое вещество с химической формулой Cr(OH)3. Описание Гидроксид хрома (III) амфотерный гидроксид. Серо зеленого цвета, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид CrO(OH). Не… … Википедия
Сульфат хрома(III) — Эта статья или раздел нуждается в переработке. Пожалуйста, улучшите статью в соответствии с правилами написания статей. Сульфат хро … Википедия
polytechnic_ru_en.academic.ru



 HOCrO2Cl + HCl ,
HOCrO2Cl + HCl ,

 HOCrO2Cl + HCl ,
HOCrO2Cl + HCl ,