Электронные конфигурации атомов. Возбужденное состояние хрома
Электронные конфигурации атомов - Общая и неорганическая химия
Заполнение орбиталей в не возбужденном атоме осуществляется таким образом, чтобы энергия атома была минимальной (принцип минимума энергии). Сначала заполняются орбитали первого энергетического уровня, затем второго, причем сначала заполняется орбиталь s-подуровня и лишь затем орбитали p-подуровня. В 1925 г. швейцарский физик В. Паули установил фундаментальный квантово-механический принцип естествознания (принцип Паули, называемый также принципом запрета или принципом исключения). В соответствии с принципом Паули:в атоме не может быть двух электронов, имеющих одинаковый набор всех четырех квантовых чисел.
Электронную конфигурацию атома передают формулой, в которой указывают заполненные орбитали комбинацией цифры, равной главному квантовому числу, и буквы, соответствующей орбитальному квантовому числу. Верхним индексом указывают число электронов на Данных орбиталях.Водород и гелий
Литий
Три электрона в атоме лития распределяются следующим образом: 1s21s1. В образовании химической связи участвуют электроны только внешнего энергетического уровня, называемые валентными. У атома лития валентным является электрон 2s-подуровня, а два электрона 1s-подуровня - внутренние электроны. Атом лития достаточно легко теряет свой валентный электрон, переходя в ион Li+, имеющий конфигурацию 1s22s0. Обратите внимание, что гидрид-ион, атом гелия и катион лития имеют одинаковое число электронов. Такие частицы называются изоэлектронными. Они имеют сходную электронную конфигурацию, но разный заряд ядра. Атом гелия весьма инертен в химическом отношении, что связано с особой устойчивостью электронной конфигурации 1s2. Незаполненные электронами орбитали называют вакантными. В атоме лития три орбитали 2p-подуровня вакантные.
Бериллий
Электронная конфигурация атома бериллия - 1s22s2. При возбуждении атома электроны с более низкого энергетического подуровня переходят на вакантные орбитали более высокого энергетического подуровня. Процесс возбуждения атома бериллия можно передать следующей схемой: 1s22s2 (основное состояние) + hν → 1s22s12p1 (возбужденное состояние).
Сравнение основного и возбужденного состояний атома бериллия показывает, что они различаются числом неспаренных электронов. В основном состоянии атома бериллия неспаренных электронов нет, в возбужденном их два. Несмотря на то что при возбуждении атома в принципе любые электроны с более низких по энергии орбиталей могут переходить на более высокие орбитали, для рассмотрения химических процессов существенными являются только переходы между энергетическими подуровнями с близкой энергией.Это объясняется следующим. При образовании химической связи всегда выделяется энергия, т. е. совокупность двух атомов переходит в энергетически более выгодное состояние. Процесс возбуждения требует затрат энергии. При распаривании электронов в пределах одного энергетического уровня затраты на возбуждение компенсируются за счет образования химической связи. При распаривании электронов в пределах разных уровней затраты на возбуждение столь велики, что не могут быть компенсированы образованием химической связи. В отсутствие партнера по возможной химической реакции возбужденный атом выделяет квант энергии и возвращается в основное состояние - такой процесс называется релаксацией.
Бор
Пять электронов в атоме бора распределяются по орбиталям следующим образом: 1s22s22p1. Как следует из приведенной электронной конфигурации, атом бора имеет в основном состоянии один неспаренный электрон (на p-подуровне). При возбуждении один из электронов с 2s-подуровня переходит на вакантную орбиталь 2p-подуровня, в результате чего в атоме появляются три неспаренных электрона. Бор - пример электронодефицитного атома: число электронов в нем меньше числа орбиталей заполняемого энергетического подуровня.
Правило Гунда
Заполнение в невозбужденных атомах p, d- и f-подуровней осуществляется таким образом, чтобы мультиплетность атома была максимальной (правило Гунда).
Энергетические ячейки
Электронную конфигурацию атомов часто представляют в форме энергетических ячеек. В этом случае чертой (или квадратом) обозначают каждую орбиталь. Чаще всего так обозначают только те орбитали, на которых находятся или могут находиться валентные электроны. Электроны обозначают с помощью стрелок, направленных вверх (s = +½) или вниз (s = -½)- Неспаренный электрон и спаренные электроны изображают так:
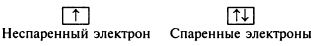
Без учета правила Гунда для основного состояния атома углерода можно предложить два варианта электронной конфигурации, отвечающих и принципу минимума энергии, и принципу Паули:
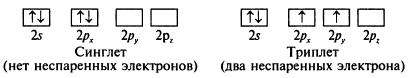 В соответствии с правилом Гунда основному состоянию атома углерода отвечает триплет. Таким образом, спаривание электронов возникает только после того, как на каждой орбитали данного подуровня уже находится по одному электрону.
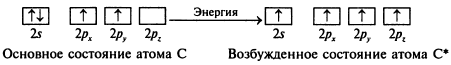
В соответствии с правилом Гунда основному состоянию атома углерода отвечает триплет. Таким образом, спаривание электронов возникает только после того, как на каждой орбитали данного подуровня уже находится по одному электрону.При возбуждении атома углерода электрон с 2s-подуровня переходит на 2p-подуровень:
Атом фтора имеет электронную конфигурацию [He]2s22p5. Имея только один неспаренный электрон, фтор может быть только одновалентным. Атом фтора легко присоединяет один электрон, превращаясь во фторид-ион с конфигурацией [He]2s22p6. Такую электронную конфигурацию имеет атом неона - благородного газа. Восьмиэлектронная оболочка 2s22p6 отвечает очень устойчивому состоянию. До настоящего времени не получено ни одного соединения неона.
Электронные конфигурации атомов элементов 3-го периода Периодической системы элементов будут в определенной степени аналогичны приведенным выше (нижним индексом указан атомный номер):
11Na [Ne]3s112Mg [Ne]3s213Al [Ne]3s23p114Si [Ne]2s22p215P [Ne]2s23p3
Максимальное число неспаренных электронов в атоме фосфора может достигать пяти:
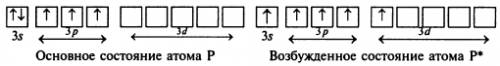 Этим объясняется возможность существования соединений, в которых валентность фосфора равна 5. Атом азота, имеющий конфигурацию валентных электронов в основном состоянии такую же, как и атом фосфора, образовать пять ковалентных связей не может.
Этим объясняется возможность существования соединений, в которых валентность фосфора равна 5. Атом азота, имеющий конфигурацию валентных электронов в основном состоянии такую же, как и атом фосфора, образовать пять ковалентных связей не может.Аналогичная ситуация возникает при сравнении валентных возможностей кислорода и серы, фтора и хлора. Распаривание электронов в атоме серы приводит к появлению шести неспаренных электронов:
[Ne]3s23p4 (основное состояние) → [Ne]3s13p33d2 (возбужденное состояние).
Это отвечает шести валентному состоянию, которое для кислорода недостижимо. Максимальная валентность азота (4) и кислорода (3) требует более детального объяснения, которое будет приведено позднее.Наличие вакантных Зd-орбиталей у всех элементов третьего периода объясняется тем, что, начиная с 3-го энергетического уровня, происходит частичное перекрывание подуровней разных уровней при заполнении электронами. Так, 3d-подуровень начинает заполняться только после того, как будет заполнен 4s-подуровень. Запас энергии электронов на атомных орбиталях разных подуровней и, следовательно, порядок их заполнения, возрастает в следующем порядке:
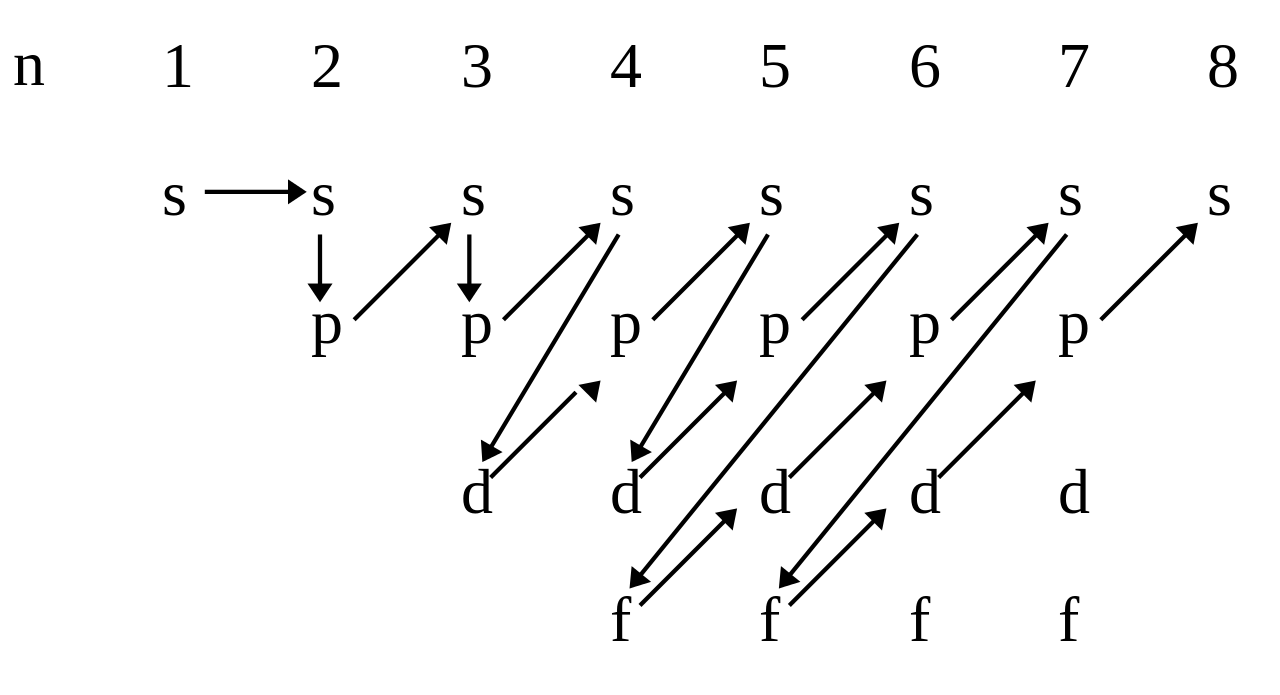
Раньше заполняются орбитали, для которых сумма первых двух квантовых чисел (n + l) меньше; при равенстве этих сумм сначала заполняются орбитали с меньшим главным квантовым числом.
Эту закономерность сформулировал В. М. Клечковский в 1951 г.Элементы, в атомах которых происходит заполнение электронами s-подуровня, называются s-элементами. К ним относятся по два первых элемента каждого периода: водород, гелий, все элементы IА (щелочные металлы) и IIА (бериллий, магний и щелочноземельные металлы) групп.
Первый d-элемент - скандий - имеет электронную конфигурацию [Ar]4s23d1. Электронные конфигурации следующих двух d-элементов не выходят за рамки общих представлений о строении электронных оболочек: 22Ti [Ar]4s23d2 и 23V[Ar]4s23d3. Максимальная валентность титана, равная 4, объясняется переходом в возбужденное состояние за счет распаривания электронов: [Ar]4s23d2 → [Ar]4s13d3. Аналогично для ванадия: [Ar]4s23d3 → [Ar]4s13d4 (максимальная валентность 5).
Однако уже у следующего d-элемента - хрома - наблюдается некоторое «отклонение» в расположении электронов по энергетическим уровням в основном состоянии: вместо ожидаемых четырех неспаренных электронов на 3d-подуровне в атоме хрома имеются пять неспаренных электронов на 3d-подуровне и один неспаренный электрон на s-подуровне: 24Cr [Ar]4s13d5.
Явление перехода одного s-электрона на d-подуровень часто называют «проскоком» электрона. Это можно объяснить тем, что орбитали заполняемого электронами d-подуровня становятся ближе к ядру вследствие усиления электростатического притяжения между электронами и ядром. Вследствие этого состояние [Ar]4s13d5 становится энергетически более выгодным, чем [Ar]4s23d4. Таким образом, наполовину заполненный d-подуровень (d5) обладает повышенной стабильностью по сравнению с иными возможными вариантами распределения электронов. Электронная конфигурация, отвечающая существованию максимально возможного числа распаренных электронов, достижимая у предшествующих d-элементов только в результате возбуждения, характерна для основного состояния атома хрома. Электронная конфигурация d5 характерна и для атома марганца: [Ar] 4s23d5. У следующих d-элементов происходит заполнение каждой энергетической ячейки d-подуровня вторым электроном: 26Fe [Ar]4s23d6; 27Co [Ar]4s23d7; 28Ni [Ar]4s23d8.
У атома меди достижимым становится состояние полностью заполненного d-подуровня (d10) за счет перехода одного электрона с 4s-под-уровня на 3d-подуровень: 29Cu [Ar]4s13d10. Последний элемент первого ряда d-элементов имеет электронную конфигурацию 30Zn [Ar]4s23d10.
Общая тенденция, проявляющаяся в устойчивости d5 и d10 конфигурации, наблюдается и у элементов ниже лежащих периодов. Молибден имеет электронную конфигурацию, аналогичную хрому: 42Mo [Kr]5s14d5, а серебро - меди: 47Ag[Kr]5s0d10. Более того, конфигурация d10 достигается уже у палладия за счет перехода обоих электронов с 5s-орбитали на 4d-орбиталь: 46Pd [Kr]5s0d10. Существуют и другие отклонения от монотонного заполнения d-, а также f-орбиталей.
chemiday.com
Возбужденный атом - хром - Большая Энциклопедия Нефти и Газа, статья, страница 1
Возбужденный атом - хром
Cтраница 1
Возбужденный атом хрома при переходе в основное состояние испускает фотон света. Все направления для спонтанного излучения фотонов равновероятны, и поэтому сначала большинство излученных фотонов покидает кристалл, вылетая из него по различным направлениям. [1]
Все возбужденные атомы хрома могут существовать в состоянии возбуждения только миллиардные доли секунды, после чего сваливаются на более низкие промежуточные уровни возбуждения красного света. [2]
Пролетая вблизи возбужденных атомов хрома, эти фотоны вызывают вынужденное излучение таких же фотонов, летящих в том же направлении. [3]
Пусть какой-нибудь из возбужденных атомов хрома самопроизвольно испускает фотон, летящий вдоль оси стержня. Этот фотон вызывает индуцированное излучение других атомов хрома, и образуется лавина фотонов. Поскольку волны, соответствующие этим фотонам, точно совпадают по фазе, возникает электромагнитная волна с непрерывно увеличивающейся амплитудой. [4]
Пусть какой-нибудь из возбужденных атомов хрома самопроизвольно испускает фотон, летящий вдоль оси стержня. Этот фотон вызывает индуцированное излучение других атомов хрома, и образуется лавина фотонов. Поскольку волны, соответствующие этим фотонам, точно совпадают по фазе, возникает электромагнитная волна с непрерывно увеличивающейся амплитудой. Дойдя до зеркального торца, она отражается и проходит вдоль стержня в обратном направлении. В результате многократного отражения возникает стоячая волна с быстро увеличивающейся амплитудой. При этом расстояние между зеркальными торцами стержня содержит целое число полуволн, и рубиновый стержень, таким образом, представляет собой объемный резонатор. [5]
После прекращения светового импульса возбужденные атомы хрома, стремясь вернуться к равновесному состоянию, переходят на энергетически более низкий уровень ( рис. VII. [7]
За время порядка долей миллисекунды все возбужденные атомы хрома переходят в нормальное состояние, и излучение лазера прекращается. Рубиновый лазер испускает короткие, но очень мощные вспышки красного света. [8]
За время порядка долей миллисекунды все возбужденные атомы хрома переходят в нормальное состояние, и излучение лазера прекращается. Рубиновый лазер испускает короткие, но очень мощные вспышки красного света. При работе лазера выделяется много тепла, и необходимо его охлаждение. [9]
Эти фотоны с Я6943 А, сталкиваясь при своем движении с другими возбужденными атомами хрома, находящимися в неустойчивом состоянии, лавинообразно вызовут индуцированное излучение. [10]
Благодаря значительной ширине этих полос примерно 10 - 15 % лучистой энергии лампы-вспышки передается возбужденным атомам хрома. [11]
Возвращаясь в основное состояние, атом хрома спонтанно излучает фотон, который сталкивается с возбужденным атомом хрома, выбивая из него другой фотон. Эти фотоны, встречаясь, в свою очередь, с другими возбужденными атомами хрома, опять выбивают фотоны, и этог процесс лавинно нарастает. [12]
Упрощенная схема действия такого генератора состоит в следующем. Некоторые из возбужденных атомов хрома спонтанно излучают фотоны, переходя на более низкий энергетический уровень. [13]
На своем пути они вызывают вынужденное излучение у новых атомов хрома, и процесс продолжается. Процесс высвечивания всех возбужденных атомов хрома завершается за 10 - 8 - 10 - 10 с. [14]
Возвращаясь в основное состояние, атом хрома спонтанно излучает фотон, который сталкивается с возбужденным атомом хрома, выбивая из него другой фотон. Эти фотоны, встречаясь, в свою очередь, с другими возбужденными атомами хрома, опять выбивают фотоны, и этог процесс лавинно нарастает. [15]
Страницы: 1 2
www.ngpedia.ru
Возбужденное состояние атома - Электрон. Электронные слои - Строение атома - ОБЩАЯ ХИМИЯ - ХИМИЯ
РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
2. Строение атома
2.4. Электрон. Электронные слои
2.4.2. Возбужденное состояние атома
При возбуждении атомов электроны приобретают большую энергии, происходит переход электронов с нижних энергетических подуровней на высшие. Так, у атома Серы имеются свободные d-орбитали, поэтому возможен переход одного из спаренных электронов с 3p-орбитали (гх) на вакантную 3и-орбиталь (первый возбужденное состояние - S*):
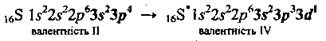
А при дальнейшем возбуждении - переход одного из 3s-электронов на другую вакантную d-орбиталь (второй возбужденное состояние - S**):
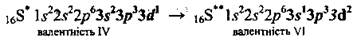
Электронное строение некоторых атомов больших периодов имеет определенные особенности. Так, у Калия 19-й электрон размещается не на 3d-подуровне, а на 4s-подуровне, оказывается энергетически более выгодным: 19К...3s23p63d04s1. В атома Кальция 4s-подуровень завершается: 4s2. Поскольку энергия 3d-электронов ниже энергию 4р-елекгронів, заполнение 3d-подуровня начинается только со Скандия: 21Sс...3s23p63d14s2. В следующих за Скандием элементов - Титана, Ванадия (V), Хрома (Сr), Марганца (Мn), Железа (Fe), Кобальта (Co), Никеля (Nи), Купруму (Cu), Цинка (Zn) - происходит заполнение только 3d-орбиталей.
Элементы с порядковыми номерами от 21 до 36 называют переходными. К ним также относятся другие элементы (соответствующих групп) 5, 6 и 7-го периодов, в которых происходит заполнение d-или f-орбиталей второго или третьего снаружи электронного слоя.
Как только 3d-подуровень завершается i на третьем энергетическом уровне разместятся 18 электронов (на трех подуровням: s, p и d)1, начинает формироваться 4р-орбиталь до завершения четвертого периода Криптоном Кr. Аналогично происходит заполнение подуровней электронами в атомах других крупных периодов.
Заметим, что атомы Купруму [Ar]3d104s1, Аргентуму [Kr]4d105s1, Ауруму [Xe]4f145d106s1, а также Хрома [Ar]3d54s1 и Молибдена [Kr]4d65s1 имеют на внешнем Энергетическом уровне по Одному s-электрону. Это объясняется особой устойчивостью электронных структур, в которых на d-орбиталях размещается 5 или 10 электронов (d5 и d10). Вследствие этого один из двух спаренных электроне», внешнего s-слоя «проваливается» на d-подуровень предыдущего энергетического уровня. Такое явление называют провалом электрона.
_____________________________________________________
1 Здесь есть еще одна особенность, связанная с энергетической стабильностью атомов: при переходе от Никеля к Купруму, от Родия до Рутения, от Иридия к Платине происходит переход s-электрона внешнего слоя на d-орбиталь предыдущего.
na-uroke.in.ua