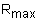Категория:Оксиды хрома. Хрома vi оксид
Оксид хрома(VI) - Material DB - RoHS
Окси́д хро́ма(VI) (триоксид хрома, трёхокись хрома, хромовый ангидрид), CrO3 — соединение хрома с кислородом, тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.
Свойства
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
CrO3+h3O→h3CrO4{\displaystyle {\mathsf {CrO_{3}+H_{2}O\rightarrow H_{2}CrO_{4}}}}или дихромовая кислота (при избытке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
CrO3+2KOH→K2CrO4+h3O{\displaystyle {\mathsf {CrO_{3}+2KOH\rightarrow K_{2}CrO_{4}+H_{2}O}}}При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
4CrO3→2Cr2O3+3O2{\displaystyle {\mathsf {4CrO_{3}\rightarrow 2Cr_{2}O_{3}+3O_{2}}}}Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет иод, серу, фосфор, уголь, например:
Комплекс триоксида хрома с пиридином используется для окисления спиртов в соответствующие карбонильные соединения (реакция Саретта).
Получение
Получают действием h3SO4 на дихромат натрия Na2Cr2O7 (реже дихромат калия K2Cr2O7).
Na2Cr2O7+h3SO4→2CrO3+Na2SO4+h3O{\displaystyle {\mathsf {Na_{2}Cr_{2}O_{7}+H_{2}SO_{4}\rightarrow 2CrO_{3}+Na_{2}SO_{4}+H_{2}O}}}Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность
Оксид хрома(VI) очень ядовит, как и многие другие соединения шестивалентного хрома. Летальная доза для человека при попадании внутрь 0,08 г/кг.
Техника безопасности
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или фарфоровая герметичная посуда, необходимо исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
b2b.partcommunity.com
Steam Community :: Cro3 Какой Оксид
Скачать:
http://sylusueastc.ru/?f=cro3-kakoy-oksid&r=steamХромовый ангидрид Распределите оксиды на основные и кислот - Школьные Хром образует три оксида: CrO, Cr2O3, CrO3. CrO получают разложением в вакууме карбонила хрома Cr(СО)6 при 300С. Оксид хрома (III) Cr2O3 тугоплавкий порошок зеленого цвета. CrO- оксид хрома (2) - основный оксид CrO3- оксид хрома (6) - кислотный оксид. Оксид хрома(VI) - это Что такое Оксид хрома(VI)? CrO3 - Оксид хрома(VI) Химия соединений Оксиды хрома (II), (III) и (VI) Оксид хрома (VI) CrO3 темно-красное кристаллическое CrO3 кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3) При взаимодействии CrO3 со щелочами образуются хроматы: CrO3 2KOH K2CrO4 h3O. ОтветыMail.Ru: Дана формула CrO3. Какой это оксид? а) основной б) кислотный в) амфотерный г) щелочной. cro3 какой оксид смотрите картинки Химические свойства. CrO3 кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3) При взаимодействии CrO3 со щелочами образуются хроматы: CrO3 2KOH K2CrO4 h3O. Кислотный оксид, соответствующая ему кислота - h3CrO4. Подскажите, пожалуйста, CrO CrO3. Al2O3 амфотерный оксид, K2O основной оксид, Mn2O7 кислотный оксид, FeO основной оксид, CuO основной оксид, SO3 кислотный оксид, P2O5 кислотный оксид, Na2O основной оксид, SO2 кислотный оксид, CrO Оксид хрома(VI) (триоксид хрома, трхокись хрома, хромовый ангидрид), CrO3 соединение хрома с кислородом, тмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот. Оксид хрома(VI) Википедия 10.9. Соединения хрома (VI). Оксид хрома (VI) CrO3 темно-красное кристаллическое вещество, имеет цепочечную структуру. Оксид хрома(VI) WiKi Оксид хрома(VI) (триоксид хрома, трхокись хрома, хромовый ангидрид), CrO3 соединение хрома с кислородом, тмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот. Править. Править. Другие названия: триоксид хрома, трехокись хрома, хромовый ангидрид. Оксид хрома(VI) - неорганическое соединение с химической формулой CrO3. Физические свойства. Молярная масса. 99,994 гмоль. Температура плавления, tпл. nonemazda premacy трейлер прибытие опережая выстрел
steamcommunity.com
Оксид хрома(VI)
Окси́д хро́ма(VI) (триоксид хрома, трёхокись хрома, хромовый ангидрид), CrO3 — соединение хрома с кислородом, тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.Содержание
- 1 Свойства
- 1.1 Физические свойства
- 1.2 Химические свойства
- 2 Получение
- 3 Применение
- 4 Токсичность
- 4.1 Техника безопасности
Свойства
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
или дихромовая кислота (при избытке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет иод, серу, фосфор, уголь, например:
Комплекс триоксида хрома с пиридином используется для окисления спиртов в соответствующие карбонильные соединения (реакция Саретта).
Получение
Получают действием h3SO4 на дихромат натрия Na2Cr2O7 (реже дихромат калия K2Cr2O7).
Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность
Оксид хрома(VI) очень ядовит, как и многие другие соединения шестивалентного хрома. Летальная доза для человека при попадании внутрь 0,08 г/кг.
Техника безопасности
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или пластиковая герметичная посуда, необходимо исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
Оксид хрома(VI) Информация о
 Оксид хрома(VI)Оксид хрома(VI)
Оксид хрома(VI)Оксид хрома(VI) Оксид хрома(VI) Информация Видео
Оксид хрома(VI) Просмотр темы.Оксид хрома(VI) что, Оксид хрома(VI) кто, Оксид хрома(VI) объяснение
There are excerpts from wikipedia on this article and video
www.turkaramamotoru.com
Категория:Оксиды хрома - WikiVisually
1. Диоксид-дихлорид хрома – Chromyl chloride is a chemical compound with the formula CrO2Cl2. This compound is an opaque dark blood-red liquid at room temperature and pressure and it is tetrahedral, somewhat like SO2Cl2. CrO2Cl2 is similar to the most commonly encountered chromium derivative chromate, 2−, however, they differ in both oxidizing power and in physical properties, one is a liquid and the other forms salts. CrO2Cl2 is a molecular species. This means that in the liquid and solid forms, the individual CrO2Cl2 entities interact predominantly via van der Waals bonding, such weak bonding leads to low melting and boiling points, which is related to the fact that it is a distillable liquid. The diminished oxidizing power of 2− vs. CrO2Cl2 can be ascribed to its anionic nature, also, chloride is a poorer pi-donor ligand than is oxide. Chromyl chloride can be prepared by mixing potassium chromate or potassium dichromate with sodium chloride and treating this mix with concentrated sulfuric acid, the chromyl chloride test entails heating a sample suspected of containing chloride with potassium dichromate and concentrated sulfuric acid. If chloride is present, chromyl chloride is formed and red fumes of CrO2Cl2 are evident, if there is no chloride present, no red fumes are produced. No analogous compounds are formed with fluorides, bromides, iodides and cyanides, the test is related to the synthesis shown above, exposure of CrO42− to HCl. Depending on solvent, CrO2Cl2 oxidizes terminal alkenes to aldehydes, internal alkenes give alpha-chloroketones or related derivatives. It will also attack benzylic methyl groups to give aldehydes via the Étard reaction, apart from this it can also be used for testing the absence of nitrate ions. CrO2Cl2 is such a reagent that solvents must be chosen judiciously. Typical for other electrophilic chlorides, chlorocarbons are excellent solvents, especially dichloromethane As a further practical complication, CrO2Cl2 reacts with water to release hydrochloric acid and hexavalent chromium Acute, HCl can be acutely lethal. Exposure to chromyl chloride vapour irritates the respiratory system and severely irritates the eyes, ingestion would cause severe internal damage. Chronic, CrVI can produce chromosomal aberrations and is a human carcinogen via inhalation, frequent exposure of the skin to chromyl chloride may result in ulceration. Thus, CrO2Cl2 should be handled in a well ventilated area. CrO2Cl2 is so aggressive that its storage can be problematic as it attacks rubber, F. Freeman Chromyl Chloride in Encyclopedia of Reagents for Organic Synthesis 2004, J. Wiley & Sons, New York. CDC - NIOSH Pocket Guide to Chemical Hazards - Chromyl Chloride
2. Оксид хрома(IV) – Chromium dioxide or chromium oxide is an inorganic compound with the formula CrO2. It is a synthetic magnetic solid. It once was used in magnetic tape emulsion. With the increasing popularity of CDs and DVDs, the use of chromium oxide has declined, however, it is still used in data tape applications for enterprise-class storage systems. It is still considered by many oxide and tape manufacturers to have one of the best magnetic recording particulates ever invented. CrO2 was first prepared by Friedrich Wöhler by decomposition of chromyl chloride, acicular chromium dioxide was first synthesized in 1956 by Norman L. Cox, a chemist at E. I. DuPont, by decomposing chromium trioxide in the presence of water at a temperature of 800 K, when commercialized in the late 1960s as a recording medium, DuPont assigned it the tradename of Magtrieve. As such each Cr center has octahedral geometry and each oxide is trigonal planar. Chrome tapes did, however, require a new generation of audiocassette recorders equipped with a bias current capability than that used by iron oxide to properly magnetize the tape particles. These bias and EQ settings were later carried over to chrome-equivalent cobalt-modified tapes introduced in the mid 1970s by TDK, Maxell, the resulting product was potentially a competitor to metallic iron pigments but apparently achieved little market penetration. Until manufacturers developed new ways to mill the oxide, the crystals could easily be broken in the process. Output from a tape could drop about 1 dB or so in a years time, the chrome coating was harder than competitive coatings, and that led to accusations of excessive head wear. DuPont licensed the product to Sony in Japan and BASF in Germany in the early 1970s for regional production and distribution, Japanese competitors developed cobalt-adsorbed and cobalt ferrite chrome equivalent Type II audio cassettes and various videotape formats as substitutes. Added to that was the problem that the production of CrO2 yielded toxic by-products of which Japanese manufacturers had great difficulty properly disposing. BASF eventually became the largest producer of both the chromium dioxide pigment and chrome tapes, basing its VHS & S-VHS video tape, audio cassettes, dupont discontinued its production of chromium dioxide particles in the 1990s. Jaleel, V. Abdul, Kannan T. S. Hydrothermal synthesis of chromium dioxide powders, a survey of recent advances in magnetic recording materials. The Technical Argument for Chromium Dioxide, the BASF Inventors Notebook Number 6, http, //www. ant-audio. co. uk/Tape_Recording/Library/Chrome. pdf
3. Оксид хрома(VI) – Chromium trioxide is an inorganic compound with the formula CrO3. It is the anhydride of chromic acid, and is sometimes marketed under the same name. This compound is a solid under anhydrous conditions, bright orange when wet. Millions of kilograms are produced annually, mainly for electroplating, Chromium trioxide is a powerful oxidiser and a suspected carcinogen. The solid consists of chains of tetrahedrally coordinated chromium atoms that share vertices, each chromium center, therefore, shares two oxygen centers with neighbors. Two oxygen atoms are not shared, giving an overall stoichiometry of 1,3, the structure of monomeric CrO3 has been calculated using density functional theory, and is predicted to be pyramidal rather than planar. In these oxidations, the Cr converts primary alcohols to the carboxylic acids. It is typically employed with additives that affect the plating process, the trioxide reacts with cadmium, zinc, and other metals to generate passivating chromate films that resist corrosion. It is also used in the production of synthetic rubies, Chromic acid solution is also used in applying types of anodic coating to aluminium, which are primarily used in aerospace applications. A Chromic Acid/ Phosphoric Acid solution is also the preferred stripping agent of anodic coatings of all types, Chromium trioxide is highly toxic, corrosive, and carcinogenic. It is the example of hexavalent chromium, an environmental hazard. The related chromium derivatives are not particularly dangerous, thus, reductants are used to destroy chromium samples, Chromium trioxide, being a powerful oxidizer, will ignite organic materials such as alcohols on contact. ATSDR Case Studies in Environmental Medicine, Chromium Toxicity U. S. Department of Health and Human Services Chromium Trioxide at The Periodic Table of Videos
4. Пероксид хрома(VI) – The generally yellow chromates or orange dichromates turn to dark blue as chromium peroxide is formed. Chromate or dichromate reacts with hydrogen peroxide and an acid to give chromium peroxide, crO42− +2 h3O2 +2 H+ → CrO5 +3 h3O After a few seconds, the chromium peroxide decomposes to turn green as chromium compounds are formed. In this way, the peroxide is dissolved in the immiscible organic solvent. In this condition it can be observed over a longer period. 2 CrO5 +7 h3O2 +6 H+ →2 Cr3+ +10 h3O +7 O2 This compound contains one oxo ligand, the etherate, bipyridyl and pyridyl complexes of this compound have been found to be effective oxidants in organic chemistry. The structure of the complex has been determined crystallographically
5. Оксид хрома(III) – Chromium oxide is the inorganic compound of the formula Cr 2O3. It is one of the oxides of chromium and is used as a pigment. In nature, it occurs as the rare mineral eskolaite, Cr 2O3 adopts the corundum structure, consisting of a hexagonal close packed array of oxide anions with ⅔ of the octahedral holes occupied by chromium. Similar to corundum, Cr 2O3 is a hard, brittle material and it is antiferromagnetic up to 307 K, the Néel temperature. It is not readily attacked by acids or bases, although molten alkali gives chromate salts with the CrO−4 anion and it turns brown when heated, but reverts to its dark green color when cooled. Cr 2O3 occurs naturally in mineral eskolaite, which is found in chromium-rich tremolite skarns, metaquartzites, eskolaite is also a rare component of chondrite meteorites. The mineral is named after Finnish geologist Pentti Eskola, the Parisians Pannetier and Binet first prepared the transparent hydrated form of Cr 2O3 in 1838 via a secret process, sold as a pigment. It is derived from the mineral chromite, Cr 2O4, 2Cr 2O7 → Cr 2O3 + N2 +4 H 2O The reaction has a low ignition temperature of less than 200 °C and is frequently used in “volcano” demonstrations. Because of its stability, chromia is a commonly used pigment and was originally called viridian. It is used in paints, inks, and glasses and it is the colourant in chrome green and institutional green. On a piece of leather, balsa, cloth or other material, in this context it is alternatively known as green compound. Although insoluble in water, it dissolves in acid to produce hydrated chromium ions and it dissolves in concentrated alkali to yield chromite ions. When heated with finely divided carbon it can be reduced to metal with release of carbon dioxide. Because of the high melting point of chromium, chromium thermite casting is impractical
wikivisually.com
Оксид хрома(VI)
Окси́д хро́ма(VI) (триоксид хрома, трёхокись хрома, хромовый ангидрид), CrO3 — соединение хрома с кислородом, тёмно-красные кристаллы, хорошо растворимые в воде. Ангидрид хромовой и дихромовой кислот.Содержание
- 1 Свойства
- 1.1 Физические свойства
- 1.2 Химические свойства
- 2 Получение
- 3 Применение
- 4 Токсичность
- 4.1 Техника безопасности
Свойства
Физические свойства
Чёрно-красные с фиолетовым оттенком кристаллы — пластины или иголки. Гигроскопичен, расплывается на воздухе.
tпл=196 °C, при атмосферном давлении разлагается ниже температуры кипения.
Плотность 2,8 г/см³; Растворимость в воде — 166 г/100 г (15 °C), 199 г/100 г (100 °C).
Химические свойства
CrO3 — кислотный оксид. При его растворении в воде образуется хромовая кислота (при недостатке CrO3):
или дихромовая кислота (при избытке CrO3):
При взаимодействии CrO3 со щелочами образуются хроматы:
При нагревании выше 250 °C разлагается с образованием оксида хрома(III) и кислорода:
Как и все соединения Cr(VI), CrO3 является сильным окислителем (восстанавливается до Cr2O3). Например этанол, ацетон и многие другие органические вещества самовоспламеняются или даже взрываются при контакте с ним (хотя некоторые справочники указывают «растворим в спирте и эфире»). Окисляет иод, серу, фосфор, уголь, например:
Комплекс триоксида хрома с пиридином используется для окисления спиртов в соответствующие карбонильные соединения (реакция Саретта).
Получение
Получают действием h3SO4 на дихромат натрия Na2Cr2O7 (реже дихромат калия K2Cr2O7).
Применение
Используется для получения хрома электролизом, электролитического хромирования; хроматирования оцинкованных деталей, в качестве сильного окислителя, изредка в пиросоставах.
Применяют также, как окислитель в органической химии (в производстве изатина, индиго и т. д.).
В смеси с кизельгуром применяется для очистки ацетилена под названием «эпурит».
Растворы хромового ангидрида (или, чаще, дихромата калия) в серной кислоте широко используются в лабораторной практике для очистки посуды от органических загрязнений (хромовая смесь).
Токсичность
Оксид хрома(VI) очень ядовит, как и многие другие соединения шестивалентного хрома. Летальная доза для человека при попадании внутрь 0,08 г/кг.
Техника безопасности
Хромовый ангидрид — весьма химически активное вещество, способен вызвать при соприкосновении с органическими веществами возгорания и взрывы. Воспламеняет бензин при комнатной температуре и используется в качестве воспламенителя топлива в ракетной технике. При попадании на кожу вызывает сильные раздражения, экземы и дерматиты, а также может спровоцировать развитие рака кожи. Даже при своевременном удалении с кожных покровов оставляет пятна коричневого цвета. Весьма опасно вдыхание паров хромового ангидрида, хотя он и малолетуч.
Для хранения его применяется стеклянная или пластиковая герметичная посуда, необходимо исключение контакта с органическими веществами. Работа с ним требует применения спецодежды и средств индивидуальной защиты.
Оксид хрома(VI) Информация о
 Оксид хрома(VI)Оксид хрома(VI)
Оксид хрома(VI)Оксид хрома(VI) Оксид хрома(VI) Информация Видео
Оксид хрома(VI) Просмотр темы.Оксид хрома(VI) что, Оксид хрома(VI) кто, Оксид хрома(VI) объяснение
There are excerpts from wikipedia on this article and video
www.turkaramamotoru.com
15. Определение оксида хрома (VI)
15.1. Ошибка повторяемости и расхождение между результатами параллельных определений не должны превышать значений, указанных в табл. 15.
Таблица 15
%
| Массовая доля оксида хрома
|
|
|
|
До 0,3 включ.
|
±0,02 |
0,03 |
| Св. 0,3 до 1,0 "
| ±0,07 | 0,10 |
| " 1,0 " 3,0 "
| ±0,18 | 0,25 |
| " 3,0 " 8,0 "
| ±0,40 | 0,50 |
15.2. Фотоколориметрический метод
Метод основан на взаимодействии дифенилкарбазида с ионами шестивалентного хрома с образованием в кислой среде соединения, окрашенного в красно-фиолетовый цвет.
Реакция протекает в течение нескольких секунд.
Мешающее влияние трехвалентного железа устраняют переводом его в бесцветный фосфатный комплекс.
15.2.1. Средства анализа
Весы лабораторные общего назначения.
Фотоэлектроколориметр концентрационный.
Кислота соляная по ГОСТ 3118 и раствор 1:5.
Кислота ортофосфорная по ГОСТ 6552, раствор 1:2.
Спирт этиловый ректификованный технический по ГОСТ 18300.
Дифенилкарбазид: 0,25 г дифенилкарбазида растворяют при слабом нагревании в 100 куб.см раствора этилового спирта 1:1. Дифенилкарбазид нестоек и его раствор готовят непосредственно перед определением.
Калий двухромовокислый по ГОСТ 4220, перекристаллизованный и высушенный до постоянной массы при температуре 130 град.С.
Смесь для сплавления по п. 6.4.1.
15.2.2. Подготовка к анализу
15.2.2.1. Приготовление стандартного раствора
Навеску двухромовокислого калия массой 0,0484 г растворяют в 100 куб.см воды; раствор переводят в мерную колбу вместимостью 250 куб.см, разбавляют до метки водой и тщательно перемешивают.
Аликвотную часть этого раствора объемом 50 куб.см разбавляют водой до метки в мерной колбе вместимостью 250 куб.см. Массовая концентрация оксида хрома в стандартном растворе - 0,02 мг/куб.см.
15.2.2.2. Построение градуировочного графика
В пять мерных колб вместимостью 100 куб.см наливают соответственно 0,4; 0,8; 1,2; 1,6; 2,0 куб.см стандартного раствора, что соответствует 0,008; 0,016; 0,024; 0,032; 0,040 г оксида хрома, разбавляют примерно до 70 куб.см водой, добавляют в каждую колбу по 1,5 куб.см соляной кислоты, 4 куб.см ортофосфорной кислоты, тщательно перемешивают, затем прибавляют по 1,5 куб.см дифенилкарбазида, разбавляют до метки водой, вновь перемешивают и через 5 - 7 мин фотометрируют полученные градуировочные растворы относительно дистиллированной воды, используя зеленый светофильтр с максимумом светопропускания при длине волны 530 - 536 нм и кювету с толщиной поголощающего свет слоя 30 мм.
По полученным результатам определений оптической плотности и известной концентрации оксида хрома в фотометрируемых объемах строят градуировочный график или составляют калибровочное уравнение.
15.2.3. Проведение анализа
Навеску пробы массой 0,2 - 0,5 г (в зависимости от предполагаемой массовой доли оксида хрома) сплавляют с 2 г смеси для сплавления. После охлаждения плав растворяют в 40 - 50 куб.см раствора соляной кислоты, переводят раствор в мерную колбу вместимостью 100 куб.см, разбавляют до метки водой и тщательно перемешивают.
Для определения массовой доли оксида хрома отбирают аликвотную часть объемом 10 - 25 куб.см полученного раствора (в зависимости от предполагаемой массовой доли элемента) в мерную колбу вместимостью 100 куб.см, добавляют 50 - 60 куб.см воды, 4 куб.см раствора ортофосфорной кислоты и перемешивают. Далее прибавляют 1,5 куб.см дифенилкарбазида, разбавляют до метки водой, перемешивают и через 5 - 7 мин фотометрируют по п. 15.2.2.2.
15.2.4. Обработка результатов
Массу оксида хрома в миллиграммах находят по градуировочному графику и вычисляют искомую массовую долю элемента по формуле (7).
Непосредственно массовую долю оксида хрома в процентах определяют по градуировочному графику, построенному в координатах "оптическая плотность - массовая доля элемента в процентах" или находят по калибровочному уравнению.
studfiles.net