Большая Энциклопедия Нефти и Газа. Плотность хрома
Хрома плотность - Справочник химика 21
Обеднение не исключает однако значения напряжений для ускорения межкристаллитной коррозии. Обеднение хромом нельзя предотвратить даже более высоким содержанием хрома в стали, хотя интенсивность процесса при этом падает [54]. Электрохимическое исследование снятием поляризационных кривых показывает, что со снижением содержания хрома, плотности критического тока пассивации и тока в пассивном состоянии возрастают, а потенциал пассивации сдвигается в сторону более положительных величин [15, 52, [c.49] Хром представляет собой твердый блестящий металл, плавящийся при 1890 °С плотность его 7,19 г/см1 При комнатной температуре хром стоек к воде н к воздуху. Разбавленные серная и соляная кислоты растворяют хром с выделением вс дорода. В холодной концентрированной азотной кислоте хром нерастворим и после обработки ею становится пассивным. [c.654]Коррозионный процесс разрушения стали при высоких температурах замедляется, так как образуются стойкие поверхностные пленки. Наружный слой пленок, состоящий из Ре5 и РеЗг, не содержит хрома, имеет рыхлое строение и способен отслаиваться. Внутренний же слой, обладая повышенной адгезионной способностью, соединен с основным металлом, имеет шпинельную структуру, состоит из смешанных сульфидов хрома и железа и часто содержит больше хрома, чем основной металл. Такой слой надежно защищает металл от коррозии, интенсивность которой обратно пропорциональна толщине пленки и особенно велика в начальный период эксплуатации труб. Затем скорость коррозии уменьшается. Прочность и плотность пленок на металле зависит от цикличности процессов. Теплосмены — нагревы и охлаждения — приводят к разрыхлению и отслаиванию пленок под влиянием термических напряжений, что прежде всего заметно при частых процессах регенерации, проводимых на установках. [c.149]
Основу покрытия почти все> современных электродов составляют мрамор и плавиковый шпат, обеспечивающие комбинированную газошлаковую защиту зоны сварки от воздуха, что предотвращает окисление хрома стали жаропрочной трубы. Вследствие большого электрического сопротивления аустенитных сталей применяют короткие электроды и сварочный ток небольшой плотности. Сварку аустенитными электродами ведут короткой дугой для уменьшения степени азотирования и окисления наплавленного металла и образования горячих трещин, а также для лучшей защиты плавильного пространства и предотвращения разбрызгивания. Отмечается, что брызги металла, прилипшие к поверхности, могут привести к образованию горячих трещин и очагов коррозионного разрушения [39—40]. [c.236]
Плотность Легкие металлы (р Тяжелые металлы (р > 5 г/см ) Хром (р = 7,19 г/см ) Железо (р = 7,86 Г/ м ) [c.13]
Потенциал металла покрытия измеряют на цельном электроде, считая, что диффузионные и кинетические ограничения, а также площадь электрода из-за пор практически не меняются. Затем строят поляризационную кривую для иокрытия, на нее наносят потенциал системы основа — металлическое покрытие и по нему определяют плотность тока коррозионного элемента. На рис. П.10 приведены коррозионные диаграммы двухэлектродных систем. Из приведенных графиков следует, что в электрохимическом отношении при одинаковых толщинах покрытий наиболее активна система железо-медь, а наименее активна железо—хром, чем объясняются высокие во многих случаях защитные свойства хромовых покрытий. Таким образом, возможность определения коррозионного тока, возникающего между основой и покрытием, позволяет оценить защитную способность покрытия и является объективным показателем пористости покрытия. [c.75]
Согласно второй точке зрения, металлы, пассивные по определению 1, покрыты хемосорбционной пленкой, например, кислородной. Такой слой вытесняет адсорбированные молекулы НаО и уменьшает скорость анодного растворения, затрудняя гидратацию ионов металла. Другими словами-, адсорбированный кислород снижает плотность тока обмена (повышает анодное перенапряжение), соответствующую суммарной реакции М гё. Даже доли монослоя на поверхности обладают пассивирующим действием [16, 17]. Отсюда следует предположение, что на начальных этапах пассивации пленка не является диффузионно-барьерным слоем. Эту вторую точку зрения называют адсорбционной теорией пассивности. Вне всякого сомнения, образованием диффузионно-барьерной пленки объясняется пассивность многих металлов, пассивных по определению 2. Визуально наблюдаемая пленка сульфата свинца на свинце, погруженном в НаЗО , или пленка фторида железа на стали в растворе НР являются примерами защитных пленок, эффективно изолирующих металл от среды. Но на металлах, подчиняющихся определению 1, основанному на анодной поляризации, пленки обычно невидимы, а иногда настолько тонки (например, на хроме или нержавеющей стали), что не обнаруживаются методом дифракции быстрых электронов . Природа пассивности металлов и сплавов этой группы служит предметом споров и дискуссий вот уже 125 лет. Представление, что причиной пассивности всегда является пленка продуктов реакции, основано на результатах опытов по отделению и исследованию тонких оксидных пленок с пассивного железа путем его обработки в водном растворе К1 + или в ме-танольных растворах иода [18, 19]. Анализ электроно рамм пле- [c.80]
Некоторые металлы, например хром, на воздухе пассивны и остаются блестящими годами, в отличие от железа или меди, которые быстро корродируют и тускнеют в короткое время. Показано, что пассивные свойства хрома присущи и железохромистым сплавам при содержании Сг — 12 % и более (такие сплавы известны как нержавеющие стали). Типичные зависимости скорости коррозии, коррозионного потенциала и критической плотности тока от содержания хрома показаны на рис. 5.9—5.11. Заметим, что на рис. 5.11 /крит пассивации Сг — Ее-сплавов при pH = 7 достигает минимального значения (около 2 мкА/см ) при содержании Сг 12 % . Это значение так мало, что коррозионные токи [c.88]
Экономически целесообразна электрохимическая регенерация хромовой кислоты, используемой в качестве окислителя в органическом синтезе. Регенерация производится из стоков, содержащих трехвалентный хром. Электролизу подвергают сернокислые растворы, содержащие трехвалентный хром. На аноде из двуокиси свинца при 30—50°С и плотности тока 300 А/м происходит окисление трехвалентного хрома [c.213]
Более существенное влияние на выход металла по току и свойства осадков оказывает концентрация в растворе посторонних анионов. Максимальный выход по току, наибольшая твердость и блеск осадков достигаются при определенном соотношении концентраций хромовой кислоты и посторонних анионов, которое зависит, в свою очередь, от природы аниона, температуры и плотности тока. Так, при концентрации СгОз 250 г/л, / = 55°С и = 50 А/дм2 наиболее высокий выход хрома по току при получении твердых и блестящих осадков, по данным Бильфингера [43], был получен при содержании анионов ЗО , и 51Р , равном 1—2,57о от количества растворенного СгОз (рис. Х11-17), [c.417]
При большом содержании нитрат-ионов хром вообще не выделяется на катоде. Примесь в электролите солей железа уменьшает рабочий интервал плотностей тока и увеличивает сопротивление электролита. [c.418]
Так как с повышением плотности тока при выделении хрома катодный потенциал изменяется мало, а выход металла по току увеличивается, электролит имеет очень низкую рассеивающую [c.419]
Как видно из рис. XII-19, зависимость поверхностной твердости осадков хрома от температуры и плотности тока проходит через максимум, причем при повышении плотности тока максимум твердости смещается в сторону более высоких температур. Износостойкость хромовых покрытий возрастает при [c.419]В противоположность блестящим осадкам молочные оСадки хрома, получаемые главным образом при высокой температуре (60—70 °С) и сравнительно небольшой плотности тока ( к = = 20—30 A/дм ), не имеют трещин и значительно менее пористы. Такие осадку при достаточной толщине ( 20 мкм) могут быть использованы для защиты стальных изделий от коррозионного разрушения в атмосферных условиях при повышенных влажности и температуре. Для этой цели В. И. Лайнером и О. А. Петровой был предложен процесс комбинированного двухслойного покрытия сначала молочным, а затем блестящим хромом (тонкий слой) взамен многослойного покрытия медь — никель — хром. [c.420]
Решение. Заменим в выражении (84) 7 и т/ на / = 5б [из формулы (85)] и т = 5ф , В которых 5 — площадь (м ) хромируемой поверхности, —толщина (м) получаемого слоя хрома, р —плотность (кг/м ) хрома. После преобразования получаем [c.192]
Для хрома плотность тока, требуемая для пассивации, имеет еще меньшее значение. По данным Хойманна и Розенера , [c.827]
Режим анодйого окисления трехвалентного хрома плотность тока на аноде 4—5 а дм , на катоде 8—10 а/дм температура электролита 20—40° С, напряжение на ванне 10—12 в. Ванну для проработки следует включать на [c.142]
Цвет пигмента зеленого имеет тусклый оттенок, однако более чистый, чем у окиси хрома. Плотность 1500 кг/м насыпная плотность 300—350 кг/м маслоемкость 54. Стоек к действию льняного масла, уайт-спирита, ксилола, нерастворим в воде, стоек к слабым щелочам на холоду, кислотами разлагается. Светостойкость при разбавлении с Т102 очень хорошая (7) при слабом разбавлении (1 1), хорошая (5—6) при большем разбавлении (1 15) и удовлетворительная (5) при сильном разбавлении (1 100). Атмосферостойкость удовлетворительная (3) при слабом (1 1) и плохая (1) при сильном разбавлении (1 100), стойкость к нагреву хорошая. [c.590]
Точки 1 а 2 отвечают саморастворяющемуся хрому. Плотность тока i выражена в а сж. [c.106]
Кроме хромовой и серной кислот в электролите в начале процесса присутствует некоторое количество трехвалентных ионов хрома (1,2—2,5 г/л), который затем образуется при восстановлении шестивалентных соединений хрома на катоде в процессе электролиза. В случае чрезмерного накопления трехвалентного хрома его окисляют проработкой электролита при пониженной анодной плотности тока. Вместо СггОд используется краситель метиленовый голубой (концентрацией 2—5 г/л), который позволяет увеличить выход хрома по току и повысить качество покрытия. [c.94]
Высокие защитные свойства двойных окислов со шпинельной структурой В. И. Архаров связывает с плотностью упаковки этих структур, защитные свойства которых тем выше, чем меньше параметр решетки. Высокие защитные свойства шпинели Ы1Сг204, образующейся при окислении Ы1-сплавов с высоким (>10%) содержанием хрома, Хауффе объясняет практическим отсутствием [c.102]
После первого цеолитсодержашего промышленного шарикового катализатора крекинга — дюрабед-5 фирма Сокони мобил ойл корпорейшн с 1965 г. начала применять дюрабед-6, который обладал более высокой прочностью и повышенной насыпной плотностью. Эти два катализатора содержали 2,5% редкоземельных элементов и 0,15% окиси хрома [30]. В последнее время фирмой созданы более активные и стабильные цеолитсодержащие катализаторы, в частности катализатор дюрабед-8 [25]. [c.22]
Из мерной колбы вместимостью 100 мл, содержащей раствор титана в 1 М НС1 (элюат 1), отбирают пипеткой 5 мл раствора, переносят в мерную колбу вместимостью 25 мл, прибавляют по каплям концентрированный раствор аммиака до слабокислой реакции (рН = 2—3), 1 мл 2,5%-ного раствора хромо-гроповой кислоты, доводят объем до метки дистиллированной водой и тщательно перемещивают. Измеряют оптическую плотность на фотоэлектроколориметре с синим светофильтром (Я акс = 470 нм), толщина слоя кюветы /=10 мм. Раствором сравнення служит дистиллированная вода. Пользуясь градуировочным графиком, определяют содержание ионов Ti в анализируемом растворе. [c.234]
Появление питтинга приводит к образованию активно-пассивного элемента с разностью потенциалов 0,5—0,6 В. Большая плотность тока в этом элементе отвечает высокой скорости коррозии в питтинге, являющемся анодом. В то же время участки сплава, непосредственно прилегающие к питтингу, находятся при потенциалах ниже критического значения. При протекании тока ионы С1" поступают в питтинг, образуя концентрированные растворы хлоридов железа (П), никеля и хрома (III). В результате их гидролиза раствор в питтинге подкисляется (рис, 18.4). В области накопления анодных продуктов коррозии нержавеющей стали 18-8 в 5 % растворе Na l при плотности тока 200 А/м (0,02 А/см ) измеренное значение pH = 1,5 [43]. [c.313]
При введении в никель хрома он приобретает стойкость в окислителях (в частности, НЫОз и Н2СГО4). Определенное по измерениям критической плотности тока минимальное массовое содержание хрома, необходимое для анодной пассивации сплава в серной кислоте, составляет 14 % [3]. Однако сплавы с хромом более чувствительны к воздействию С1 и НС1. В неподвижной морской воде на них образуются более глубокие питтинги. Хром повышает также стойкость никеля к окислению при повышенных температурах. Широкое применение нашел сплав, содержащий 20 % Сг и 80 % N1 (см. разд. Ю.11.3). [c.361]
Кобальт можно анодно запассивировать в 0,5 т растворе h3SO4. Для этого необходима минимальная плотность тока 5000 А/м , что в 14 раз больше соответствующей плотности тока для никеля [1 ]. Легирование кобальта хромом приводит к уменьшению плотности тока для пассивации сплава с 10 % Сг требуется плотность тока лишь в Ю А/м (1 мА/см ). Сплав, содержащий 10—12 % Сг, почти не подвергается коррозии в горячем и холодном 10 % растворе HNO3, однако в 10 % растворе h3SO4 ИЛИ НС пассивации не происходит, и скорость коррозии достигает очень высоких значений. Легирование сплавов Со—Сг молибденом или вольфрамом ослабляет воздействие на них серной или соляной кислоты, но не азотной. i [c.369]
Важное значение для повышения показателей работы действующих установок 43-102 имеет повышение нахьшнои—плотности, износостойкости, улучшение регенерационных свойств катализаторов типа Цеокар. Например, катализатор Цеокар-4 с добавкой 0,15% (масс.) хрома [21, 22], который прошел опытно-промышленные испытания, позволяет увеличить на 20—30 % коксовую яагрузку на регенератор установки типа 43-102 и обеспечивает значительный рост производительности установки. [c.230]
Состав электролита по 15 г/л Сг + и Сг +, 200—270 г/л (Nh5)2S04, концентрация свободной серной кислоты в анолите 250—280 г/л, что отвечает извлечению из 1 л питающего электролита около 100 г хрома. Процесс ведут при катодной плотности тока до 1000 А/м , температуре 50 °С и напряжении до 4,5 В, расход электроэнергии достигает 18 000—20 000 кВт-ч/т. [c.286]
Температура электролита и плотность тока оказывают большое влияние на выход по току и свойства катодных осадков хрома. Выход металла по току при повышении температуры уменьшается, а при повышении плотности тока увеличивается (рис. ХП-18). Предполтгают [42], что первое связано с удалением от поверхности катода продуктов восстановления хромат-ионов и [c.418]
В процессе электролиза свинцовые аноды покрываются слоем двуокиси свинца PbOj, которая катализирует окисление трехва-лентного ipoMa и защищает свинец от дальнейшего разрушения. При поддержании определенного соотношения анодной и катодной плотностей тока можно установить равновесие, при котором на аноде будет окисляться такое же количество трехвалентного хрома, которое попадет в электролит из катодной зоны. Чем больше анодная поверхность и, следовательно, чем меньше анодная плотность тока, тем с ббльшим выходом по току окисляется трехвалентный хром. В нормально работающих ваннах рекомендуется поддерживать отношение анодной поверхности к катодной в пределах от 1 2 до 2 3. [c.421]
В. Определение хрома(У1). Основной стандартный раствор хрома готовят растворением 0,050 г металлического хрома марки X. ч. в концентрированной азотной кислоте. После охлаждения раствор количественно переносят в мерную колбу вместимостью 250 мл и разбавляют бидистиллированной водой до метки. Для приготовления стандартных растворов отмеряют 0,1 0,2 0,3 0,4 0,5 мл основного раствора и добавляют биди-стиллированную воду до 5 мл. В каждый раствор вводят 0,1 мл 0,5 %-го раствора дифенилкарбазида в ацетоне и измеряют оптическую плотность окрашенных в малиновый цвет растворов в кювете с толщиной слоя 1 см при X = 670 нм. [c.336]
Пример 4. Электрохромирование стальных изделий проводится в сернокислотных растворах СгОз при плотности тока 3000 А/м . Вычислите выход по току, если покрытие изделий в указанных условиях слоем хрома толщиной 400 мкм длится 520 мин. Плотность хрома принять равной 7140 кг/м [c.192]
Для повышения износоустойчивости гильзы поршневых цилиндров и поршневые кольца покрывают слоем хрома толщиной до 150 мкм. Определите расход электроэнергии на покрытие 1 м поверхиости указанных изделий электролизом из раствора хромовой кислоты (Н2СГО4), если выход по току равен 0,25, Плотность хрома принять равной 7140 кг/м [c.197]
Определите расход электроэнергии на восстановление изношенных распределительных и коленчатых валов электрохро-мнрованием, если процесс проводится при напряжении 6,5 В, суммарная поверхность изделий составляет 0,50 м , толшнна слоя хрома достигает 100 мкм, а выход по току равен 0,30. Плотность хрома принять равной 7140 кг/м . [c.197]
Как известно из практики хромирования, а процесс осаждения хрома существенно влияет ггрисутствие НгЗО в растворе. В отсутствии серной кислоты катод покрывается коричневой пленкой, на нем выделяется только водород. По мере увеличения содержания серной кислоты в растворе возрастает плотность тока, отвечающая площадке предельного тока, причем потенциал выделения металлического хрома и водорода на катоде смещается к более электроотрицательным значениям (рис. 241). [c.522]
chem21.info
Плотность хлоридов хрома - Справочник химика 21
Приборы н реактивы. Пипетка капельная. Приборы для получения оксида углерода и диоксида углерода. Фильтровальная бумага. Уголь активированный. Уголь древесный (порошок). Фуксии. Оксид меди. Мрамор. Мел (кусковой). Основной карбонат меди. Известковая вода. Бром. Лакмус (нейтральный раствор). Муравьиная кислота. Растворы нитрата свинца (0,01 н.), иодида калия (0,1 и.), перманганата калия (0,05 н.), нитрата серебра (0,1 н.), карбоната натрия (0,5 н.), карбоната калия (0,5 н.), гидрокарбоната калия (0,5 н.), хлорида железа (III) (0,5 н.), хлорида хрома (0,5 и.), серной кислоты (плотность 1,84 г/см ), хлороводородной кислоты (плотность 1,19 г/см , 2 н.), едкого натра (2 н.), аммиака (25 й-ный). [c.164] Приборы и реактивы. Пробирки. Штатив для пробирок. Ступка фарфоровая с пестиком. Стеклянные пластинки. Фарфоровые пластинки. Центрифуга. Пипетка капельная. Приборы для получения окиси углерода, ацетилена, метана и двуокиси углерода. Прибор для сухой перегонки дерева. Фильтровальная бумага. Уголь активированный. Уголь древесный (порошок). Окись меди. Мрамор, Мел (кусковой). Основной карбонат меди. Натронная известь. Ацетат натрия. Лучина (сухая тонкая). Вода дистиллированная. Известковая вода. Бром. Бромная вода. Лакмус (нейтральный раствор). Растворы нитрата свинца (0,0] н.) иодида калия (0,1 н.) перманганата калия (0,05 н.) нитрата серебра (0,1 н,) карбоната натрия (0,5 и.) карбоната калия (0,5 н.) бикарбоната калия (0,5 н.) хлорида трехвалентного железа (0,5 н.) хлорида хрома (0,5 н,) серной кислоты (плотность 1,84 г/сж ) соляной кислоты (плотность 1.19 г/с, ) едкого натра (2 п.) аммиака (25%-ный). [c.201]Приборы и реактивы. Весы техно-химические с разновесами. Колба емкостью 100 мл. Конические колбы емкостью 100 мл. Мерные колбы емкостью 100 мл. Бюретка емкостью 50 мл. Пипетка на 15 мл. Мензурка на 50 мл. Часовое стекло. Термометр. Эксикатор с серной кислотой (плотность 1,84 г/см ). Колба Вюрца с капельной воронкой. Фильтровальная бумага. Лед. Хлорид хрома(1П). Хлорид натрия. Ацетон. Растворы нитрат серебра (0,1 н.). Бихромат калия (0,5 и.). Кислота соляная (плотность 1,19 г/см ). [c.164]
Приборы и реактивы. Тигелек. Капиллярная трубка. Лупа (х5). Предметное стекло. Фильтровальная бумага. Водяная баня. Паяльная трубка. Ступка фарфоровая с пестиком. Фарфоровая пластинка. Фарфоровая чашечка. Кисточка. Вазелин. Хром. Бихромат аммония. Бихромат калия. Хлорид хрома(III). Оксид хро-ма(1И). Хромовый ангидрид. Феррохром. Сера (порошок). Нитрат калия. Карбонат калия. Пиросульфат калия. Едкий натр. Диэтиловый эфир. Крахмальный клейстер. Сероводородная вода. Лакмус (нейтральный). Растворы сульфата хрома (III) или хромовых квасцов (0,5 н.) хромата калия (0,5 и.) бихромата калия (0,5 н.) серной кислоты (2 н.) азотной кислоты (2 н. плотность 1,2 г/см ) соляной кислоты (6 н. плотность 1,19 г/см ) уксусной кислоты (2 н.) едкого натра (2 н.) карбоната натрия (0,5 н.) сульфида аммония (0,5 и.) нитрата свин-ца(П) (0,5 н.) нитрата серебра (0,1 н.) хлорида бария (0,5 н.) нодида калия (0,5 н.) пероксида водорода (3%-ный). [c.288]
Известны попытки электролитического выделения металлов подгруппы хрома из неводных растворов. Например, в работе [1961 хромовые покрытия были получены путем электролиза растворов хлорида хрома в формамиде, ацетамиде, в смеси мочевины и аце-тамида. Оптимальная плотность тока составляет 5 А/дм , Описано также вы-.целение хрома при электролизе растворов его солей в ацетамиде, анилине, ацетоне, пиридине, этаноламине, хлористом бензиле и уксусной кислоте. [c.107]
В отсутствие хлорид-анионов при ионном легировании железа хромом получается легированный металл, для которого плотность критического тока пассивации в 30 раз меньше, плотность тока в пассивном состоянии примерно в 10 раз меньше, чем для нелегированного железа, что, естественно, ведет к увеличению стойкости первого к общей коррозии. Аналогичное действие на железо и сталь оказывает имплантация фосфора. [c.131]
Хром — твердый металл блестящего серого цвета, плотность 6,92 г/м , способен корродировать. Гидроокись хрома и карбонаты в воде не растворяются, но соединения трехвалентного хрома (хлориды, нитраты и сульфаты) и шестивалентного (хроматы и бихроматы натрия, калия и аммония) в воде растворяются легко. [c.26]
Казалось, что по анодному поведению в растворах хлоридов сплавы никель — хром, железо — хром должны сильно различаться, так как известно, что никель в растворах хлоридов более стоек, чем железо. Но из сравнения кривых 5 (рис. 144) и 3 (рис. 146) видно, что при малых плотностях тока различие между ними очень небольшое, т. е. железо и никель в бинарных сплавах с хромом обладают близкими свойствами. [c.301]
Авторы [64] исследовали в качестве анодного материала силициды титана и молибдена, бориды титана, хрома и циркония, карбиды титана, циркония, ниобия в растворах хлорида натрия и установили, что при малых плотностях тока идет выделение хлора и начинается окисление поверхности. При повышении плотности тока на этих анодах образуется запорный слой, потенциал резко возрастает, ток падает до нуля. При анодной поляризации все эти соединения неустойчивы. [c.37]
Сущность работы. Для определения хрома и марганца при совместном присутствии их окисляют соответственно до бихромата и перманганата. Оптическая плотность исследуемого раствора пропорциональна содержанию марганца и хрома. В растворе должны отсутствовать восстановители (в том числе и хлорид-ионы). [c.90]
Приборы и реактивы. Прибор для получения газа с отводными трубками (вертикальной и изогнутой). Ложечка железная. Проволока мягкая. Лучина, Фильтровальная бумага. Пинцет. Ланцет и нож. Вата. Эфир. Иодокрахмальная бумага. Пероксид натрия. Оксид ртути(П). Перманганат калия. Хлорат калия. Диоксид марганца. Сера. Натрий (металлический). Древесный уголь. Персульфат аммония. Цинк (гранулированный). Алюминий (жесть). Оксид меди. Индикаторы лакмус (нейтральный), фенолфталеин, индиго. Растворы азотной кислоты (плотность 1,4 г/см ) серной кислоты (2 н. 4 н. 75%-ный плотность 1,84 г/см ) соляной кислоты (2 п.) едкого кали (2 н.) сульфата марганца (0,5 н.) иодида калия (0,5 и.) перманганата калия (0,5 и.) хлорида железа(1П) (0,5 н.) нитрата ртути(П) (0,5 и.) роданида аммония (0,01 н.) пероксида водорода (3%-ный, 30%-ный) сульфата хрома (0,5 к.) бихромата калия (0,5 и. 0,01 н. и насыщенный). [c.167]
В качестве основных расчетных параметров приняты концентрация органических примесей по ХПК, а также концентрация остаточного активного хлора после электролиза. В расчетах учитывали влияние следующих параметров очистки начальной концентрации загрязнений по ХПК (Со), плотности тока а, начальной концентрации хлоридов и 6-валентного хрома д, продолжительности обработки tэ, pH среды, температуры Т. [c.177]
Приборы и реактивы. Тигелек. Асбестовая сетка. Железная проволока. Водяная баня. Фарфоровые тигли. Хром. Дихромат аммония. Дихромат калия. Хлорид хрома ( II). Феррохром. Нитрат калия. Карбонат калия. Пиросульфат калия. Диэтиловый эфир. Сероводородная вода. Лакмус (нейтральный). Рас-твмы сульфата хрома (111) или хромовых квасцов (0,5 и.) хромата калия (0,5 н.) дихромата калия (0,5 и.) серной кислоты (2н.) азотной кислоты (плотность 1,2 г/см ) хлороводородной кислоты (6 п. плотность 1,19 г/см ) едкого натра (2 н.) карбоната натрия (0,5 н.) сульфида аммония (0.5 и.) нитрата свинца (II) (0,5 н.) нитрата серебра (0,1 н.) хлорида бария (0,5 н.у, иодида калия (0,5 н.) пероксида водорода (3%-ный). [c.229]
Гексагональные кристаллы безводного трихлорида хрома СгС1з имеют окраску цветов персикового дерева они парамагнитны, расплываются на воздухе, имеют плотность 2,87 г см . сублимируются при 1047°, плавятся при 1152°, трудно растворимы в воде, спирте, эфире, ацетальдегиде, ацетоне, хлорокиси фосфора восстанавливаются при высокой температуре до металлического хрома кальцием, цинком, магнием, водородом, железом, превращаются в хлорид хромила при нагревании в атмосфере влажного хлора, а прп нагревании с h3S — в СггЗз. Соединение СгС1з используется в качестве катализатора в многочисленных реакциях органической химии. [c.247]
Появление питтинга приводит к образованию активно-пассивного элемента с разностью потенциалов 0,5—0,6 В. Большая плотность тока в этом элементе отвечает высокой скорости коррозии в питтинге, являющемся анодом. В то же время участки сплава, непосредственно прилегающие к питтингу, находятся при потенциалах ниже критического значения. При протекании тока ионы С1" поступают в питтинг, образуя концентрированные растворы хлоридов железа (П), никеля и хрома (III). В результате их гидролиза раствор в питтинге подкисляется (рис, 18.4). В области накопления анодных продуктов коррозии нержавеющей стали 18-8 в 5 % растворе Na l при плотности тока 200 А/м (0,02 А/см ) измеренное значение pH = 1,5 [43]. [c.313]
Рассмотрим назначение компокентов электролитов. Хлорид аммония участвует в токообразующей реакции, обеспечивает электропроводность электролита, а также вследствие буферных свойств растворов Nh5 I стабилизирует pH электролита при невысоких плотностях тока. Хлорид кальция снижает температуру замерзания электролита. Он обязательно используется в рецептурах для ХИТ, работающих при низких температурах до —40°С хлорид цинка ускоряет загустевание электролита и предохраняет пасту от гниения. Сулема Hg b является ингибитором коррозии цинка. Контактно восстанавливаясь на нем до металлической ртути, она амальгамирует поверхность цинка, в результате увеличивается перенапряжение водорода и снижается скорость саморазряда. Следует отметить, что ввиду токсичности соединений ртути ведутся поиски других способов защиты цинка от коррозии. Рекомендованы органические ингибиторы коррозии, а также использование более стойких сплавов цинка со свинцом и кадмием. Сульфат хрома является дубителем и способствует упрочнению пасты. Бк хромат калия служит ингибитором коррозии цннка. Крахмал (250 г/л) является загустителем. [c.70]
П = —100, где /ол и г ф — плотности тока электролиза соотв. в присут. вспомогат. реактива и без него при одном и том же значении Е. Варьируя параметры элект лиза (концентрацию вспомогат. реактива, кислотность электролита, т-ру и т. п.), находят условия, при к-рых ц достигает 100%. Момент завершения хим. р-ции определяют с помощью цветных индикаторов или применяемыми в титримет-рии физ.-хим. методами. Обычно О определяют по произведению /,Тэ. Кулонометрич. титранты можно получать также анодным растворением металлов электрохимически активных электродов (напр., хрома, ванадия, меди, ртути) или амальгам либо катодной р-цией из нанесенных на электрод труднорастворимых осадков (напр., хлорида серебра или ргути, ферри- или ферроцианида серебра). [c.292]
Ионы висмута, тория, арсената, хлорида и фторида замедляют развитие окраски. Если они присутствуют в заметных количествах, то для развития максимальной окраски требуется больше времени, например 30 мин. Концентрация ионов арсената не должна превышать 100 мкг1мл, а концентрация ионов хлорида и фторида — 50 мкг1мл. Висмут допустим в концентрации до 400 мкг/мл. Концентрация двухвалентного кобальта не должна превышать 100 мкг/мл, трехвалентного хрома — 10 мкг/мл. Ионы йодида, бихромата и перманганата должны отсутствовать. Четырехвалентный церий, четырехвалентное олово и серебро мешают определению вследствие образования осадка или мути. Когда в анализируемом растворе присутствуют большие количества силиката, хлорида или трехвалентного железа, то рекомендуется предварительное выпаривание с хлорной кислотой до получения почти сухого остатка. При этом удаляются ионы хлорида и происходит дегидратация кремневой кислоты, после чего она может быть отфильтрована. Трехвалентное железо в хлорнокислых растворах поглощает свет при 460 ммк не так сильно, как в солянокислых растворах. Следует также отметить воз-. можность компенсации помех от больших количеств трех-валентного железа путем измерения оптической плотности относительно соответственно разбавленного анализируемого раствора. [c.18]
Фосфорномолибденовая кислота экстрагируется селективно, и ионы силиката, арсената и германата не мешают, в то время как при обычном методе определения по образованию фосфорномолибденовой кислоты названные ионы мешают определению. Уэйдлин и Меллон [26] исследовали зкстрагируемость гетерополикислот и установили, что 20%-ный по объему раствор бутанола-1 в хлороформе селективно извлекает фосфорномолибденовую кислоту в присутствии ионов арсената, силиката и германата. Предложенный ими метод позволяет определить 25 мкг фосфора в присутствии 4 мг мышьяка, 5 мг кремния и 1 мг германия. Более того, при экстракции удаляется избыток молибдата, поглощающего в ультрафиолетовой области. Измерение оптической плотности экстракта при 310 ммк обеспечивает увеличение чувствительности метода. Для получения надежных результатов необходимо строго контролировать концентрацию реагентов. Определению не мешают ионы ацетата, аммония, бария, бериллия, бората, бромида, кадмия, кальция, хлорида, трехвалентного хрома, кобальта, двухвалентной меди, йодата, йодида, лития, магния, двухвалентного марганца, двухвалентной ртути, никеля, нитрата, калия, четырехвалентного селена, натрия, стронция и тартрата. Должны отсутствовать ионы трехвалентного золота, трехвалентного висмута, бихромата, свинца, нитрита, роданида, тиосульфата, тория, уранила и цирконила. Допустимо присутствие до 1 мг фторида, перйодата, перманганата, ванадата и цинка. Количество алюминия, трехвалентного железа и вольфрамата не должно превышать 10 мг. [c.20]
Покрытие никель—хром с микротрещинами получают следующим образом. На слой блестящего никелевого покрытия толщиной 20. .. 25 мкм осаждают слой матового никеля толщиной 2. .. 2,5 мкм из раствора, г/л сульфата никеля 240. .. 250, хлорида никеля 40. .. 50, борной кислоты 40. .. 50, триметиламинобората 1. .. 2 при pH = = 3. .. 4 температуре 50. .. 60 °С и плотности тока 4. .. 5 А/дм , а затем слой хрома толщиной 0,5. .. 1 мкм из универсального раствора с добавкой 0,005. .. 0,01 г/л селената натрия. Двухслойные покрытия никель—хром рекомендуются для защиты от коррозии деталей сложной конфигурации в машиностроении. [c.689]
Серый металл плотность 7,19 т. пл. 1890 °С т. кип. 2680 °С растворимы хлорид, н-итрат, сульфат хрома (III), хроматы и бихроматы натрия, калия, аммония. Соединения хрома (VI) в водоемах очень стабильны в анаэробных условиях xpoM(VI) переходит в хром(П1), соединения которого выпадают в осадок. При щелочной реакции осаждение происходит быстрее и эта особенность используется при очистке сточных вод от хрома. При низкой температуре осаждение соединений хрома (III) замедляется, поэтому отстойники должны устраиваться в отапливаемых помещениях, иначе зимой осаждение происходить не будет. [c.134]
Оксихлорид хрома СгОгСЬ, или хлористый хромил, —темнокрасная жидкость с плотностью 1,911 г см при 20°, плавится при —96,5°. Давление пара в (ммрт.ст.) 10 при 13,8°, 100 при 58°, 400 при 95,2°, 760 при 117,1° (4)- Водой, а также на свету и при нагревании разлагается. Образуется при взаимодействии газообразного НС1 и СгОз или при обработке концентрированной серной кислотой смеси бихромата и хлорида. > [c.567]
После Бунзена (1854) Борхерс (1898), Коупер-Коулс (1900), а затем Нейман и Глазер (1901) изучали электролиз растворов хлорида и сульфата хрома. Последние авторы нашли, что хорошие, но тонкие катодные осадки хрома могут быть получены при высоких плотностях тока — 900— 1800 а м , прц температурах не выше 50° и при высокой концентрации хрома в электролите с выходом по току 38—56%. Большое исследование электролиза водных растворов солей хрома с диафрагмой провел Памфилов с сотрудниками они нашли, что повышение плотности тока до 7500 а м позволяет несколько увеличить выход хрома по току. [c.314]
Гольц и Израилевич разработали условия эл ктроосаждения хрома из водных растворов хлорного хрома r lg при длительной работе ванны с получением толстых осадков хрома значительной чистоты. Авторы предлагают такие условия электролиза состав католита — 35—100 г л хрома (в виде хлорида), 1,4 мол/л NH l, анолит — 1—3 н НС1, температура комнатная, плотность тока — 800—400 а/м напряжение — 4,5 в, выход хрома по току — 30—40%. Основное влияние на выход хрома по току имеет кислотность католита при слишком большой кислотности облегчен разряд ионов водорода на хроме, при слишком малой — образуются основные соли типа r(0H) l2, гидраты и окислы хрома. На аноде, если допускать хлористый аммоний реагировать с хлором, очевидно, также, как и при электролизе растворов хлористого марганца (см. 70), получается не хлор, а азот и хлористый водород. Несмотря на то, что электролиз растворов хлористого хрома представляет значительный интерес с точки зрения применения графитового анода вместо свинцового, а также потому, что выделение хлора позволяет отказаться от циркуляции анолита все же, до сих пор хлористый электролиз не вышел из стадии лабораторного исследования. [c.314]
Мешают определению (без экстракции комплексной кислоты) следующие ионы кремний в больших концентрациях, железо(III) в присутствии хлорида или сульфата, восстановители, хром (VI), мышьяк(V) и цитрат. Висмут(III), торий(IV), хлорид н фторид влияют на развитие окраски. Кремний можно удалить при кипячении раствора с концентрированной H IO4. Железо(III) можно связать в комплекс с фторидом, избыток которого удаляют введением борной кислоты. Борную кислоту можно использовать и для связывания фторидов, присутствующих в исходном анализируемом растворе. С использованием экстракции комплексной гетерополикислоты был разработан метод определения фосфора. Метод был применен для анализа практически всех фосфорсодержащих материалов стали [139, 140J, железных руд [141], алюминиевых, медных и никелевых сплавов с белыми металлами [142], воды [143, 144] и удобрений [145—147]. Работы по анализу удобрений [145—147] посвящены автоматизации очень точного метода определения фосфора с применением автоматических анализаторов. В анализаторы был заложен метод прямого измерения светопоглощения, а не дифференциальный вариант, который обычно используют для повышения точности определения. Полученные результаты позволяют заключить, что абсолютная ошибка измерения оптической плотности в интервале О—1,2 единицы не выше ошибки самого измерительного прибора (0,001 единицы поглощения). Следует отметить, что описанный метод по точности превосходит метод с применением молибдофосфата хинолина и, кро.ме того, обладает еще одним преимуществом — простотой выполнения определения. В биохимии метод применяли для определения фосфата в присутствии неустойчивых органических фосфатов [148] и неорганического фосфата в аденозинтрифосфате [149]. Метод был использован для анализа фосфатных горных пород [150]. В органическом микроанализе метод применяют после сожжения органических соединений в колбе с кислородом [151, 131]. [c.461]
Кроль [11] получил хром в виде губки из электролита, составленного на основе хлоридов калия и натрия, с графитовым анодом. Вследствие взаимодействия кислорода с верхним слоем электролита в электролитическом осадке находилось до 3,6% СгОз. Институт черной металлургии предложил следующий состав электролита 1 мольн. доля Na l, 0,45 K l, 0,3 NaF. Катодная плотность тока составляет 50—200 а/дм , температура электролита 750—850° С, выход по току 85 %. [c.7]
Для построения градуировочных графико в в ряд мерных колб объемом 100 мл помещают различные количества рабочего стандартного раствора бихромата калия так, чтобы. содержание Сг + составляло 0 0,00025 0,0005 0,001 0,002 0,004 мг и т. д. в зависимости от предполагаемого количества хрома в вытяжках. В каждую колбу доливают до 100 мл дистиллированную воду или физиологический раствор (0,8%-ный раствор хлорида натрия) и тщательно перемешивают. Из каждой колбы отбирают в пробирки две параллельные пробы по 5 мл, вносят по 0,5 мл свежеприготовленного раствора дифенилкарбазида, перемешивают и через 30 мин замеряют оптическую плотность на фотоэлектроколориметре в кювете с. толщиной слоя 10 мм при использовании зеленого светофильтра № 6 (Я, = 540 нм) по отношению к контрольной пробе (первая колба). [c.34]
Электрохимическая регенерация хлорида двухвалентного хрома происходит в результате восстановления на катоде трехвалентного хрома в электролизере с диафрагмой при одновременном выделении на графитовом аноде хлора. При катодной плотности тока 800—1000 А/м и температуре раствора 20—25 °С выход СгС1а на графитовом катоде составляет около 90% [560]. [c.186]
Навеску стали переводят в раствор, удаляют хроц в виде хлористого хромила при выпаривании с хлорной кислотой, вольфрам отделяют в виде вольфрамовой кислоты, мышьяк — выпариванием с бромистоводородной кислотой, титан связывают аскорбиновой кислотой и после получения желтой фосфорномолибденовой кислоты экстрагируют ее изобутанолом. Затем в неводном растворе восстанавливают желтый комплекс до синего с помощью хлорида олова(II) и измеряют оптическую плотность неводного слоя. [c.97]
chem21.info
Свойства атома Хрома | |
| Название | Хром / Chromium |
| Символ | Cr |
| Номер | 24 |
| Атомная масса (молярная масса) | 51,9961 (6) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d5 4s1 |
| Радиус атома | 130 пм |
Химические свойства Хрома | |
| Ковалентный радиус | 118 пм |
| Радиус иона | (+6e)52 (+3e)63 пм |
| Электроотрицательность | 1,66 (шкала Полинга) |
| Электродный потенциал | -0,74 |
| Степени окисления | 6, 3, 2, 0 |
| Энергия ионизации (первый электрон) | 652,4 (6,76) кДж/моль (эВ) |
Термодинамические свойства простого вещества Хрома | |
| Плотность (при н. у.) | 7,19 г/см3 |
| Температура плавления | 2130 K |
| Температура кипения | 2945 K |
| Уд. теплота плавления | 21 кДж/моль |
| Уд. теплота испарения | 342 кДж/моль |
| Молярная теплоёмкость | 23,3 Дж/(K·моль) |
| Молярный объём | 7,23 см3/моль |
Кристаллическая решётка простого вещества Хрома | |
| Структура решётки | кубическая |
| объёмноцентрированая | |
| Параметры решётки | 2,885 Å |
| Температура Дебая | 460 K |
Прочие характеристики Хрома | |
| Теплопроводность | (300 K) 93,9 Вт/(м·К) |
| Номер CAS | 7440-47-3 |
infotables.ru
Температура плавления хрома - Справочник химика 21
Металлы, температура плавления которых превышает температуру плавления хрома (1890°С), условно относят к тугоплавким. Понятие тугоплавкости [c.322]Заметное взаимодействие металлов с кислородом начинается при температурах около 400° С при более высоких температурах окисление идет весьма энергично. С водородом хром, молибден и вольфрам химически не взаимодействуют вплоть до температур плавления. Хром в больших количествах, молибден в значительно меньших поглощают водород с образованием твердых растворов, вольфрам адсорбирует водород незначительно. [c.571]
Температура плавления алюминия ниже температуры плавления хрома на 1272°, а железа — на 872°. [c.168]В свободном состоянии ванадий, ниобий и тантал весьма стойки к химическим воздействиям и обладают высокими температурами плавления. Эти металлы, вместе с хромом, молибденом, вольфрамом, рением (см. 228—232), а также рутением, родием, осмием и иридием (см. табл. 40, стр. 676), относятся к тугоплавким металлам. Под последними условно понимают металлы, температура плавления которых превышает температуру плавления хрома (1890°С). [c.631]
Учитывая указанные обстоятельства, а также результаты нового определения температуры плавления хрома [500], на рис. 81 приведена скорректированная диаграмма состояния системы Сг—Si, не требующая специальных пояснений. Свойства силицидов хрома приведены в табл. 2. [c.154]
Температура плавления хрома зависит от его чистоты. Многие исследователи пытались ее определить и получили значения от 1513 до 1920°С. Такой большой разброс [c.350]
Следует внести также поправку и в отношении такой важной физической константы, как температура плавления хрома. [c.61]
В ряде справочников, в частности в известном капитальном труде Справочник по электролитическому хромированию Бильфингера [2] температура плавления хрома характеризуется интервалом 1513—1553°, в то время как многие исследования последнего времени оценивают ее в 1920° [3]. [c.61]
Наиболее вероятна температура плавления хрома 1800 . [c.437]
Вода, ртуть, платина, спирт, сахар, бензойная кисло га, криптон и многие другие индивидуальные вещества строго контролируемого качества издавна играют роль эталонных веществ в измерительной технике. По мере увеличения точности и стабильности приборов и образцов растут и требования к чистоте исходных веществ. Ведь примеси в той или иной мере искажают значения всех констант. Так, долгое время устанавливали разные значения температуры плавления хрома (от 1513 до 1920°). Причина столь большого разброса — характер и количество примесей в [c.29]
Условно жаропрочными металлами называют металлы, температура плавления которых равна или превышает температуру плавления хрома (1875° С). Все эти металлы представляют собой элементы переменной валентности, входящие в подгруппы от IV левой до VIII правой периодической системы и включают (в последовательности снижения температуры плавления) вольфрам, рений, осмий, тантал, молибден, иридий, ниобий, рутений, гафний, родий, ванадий и хром. [c.311]
Поры в диффузионном слое могут возникать из-за эффекта Киркендолла, как это для пары медь — цинк показал Бюкл [920], довольно обстоятельно проанализировавший возможности защиты тугоплавких сплавов от окисления в результате образования диффузионных зон. Следующие параметры процесса нужно подбирать с такил расчетом, чтобы добиться создания наиболее благоприятных условий для нанесения покрытия из новой фазы на матрицу продолжительность и температура процесса состав донорной фазы, ее толщина, природа сцепления покрытия с подложкой. Хром и молибден, например, взаимно растворимы и характеризуются минимальной температурой ликвидуса. Выбрав температуру спекания выше этого минимума, но ниже температуры плавления хрома, порошок хрома удается спечь на молибденовой сердцевине с временным образованием промежуточного жидкого слоя, который впоследствии обеспечивает сцепление покрытия с подложкой. [c.397]
Для изготовления аналогичных материалов можно использовать сплав, содержащий 80 о никеля и 20% хрома. В качестве армирующего материала могут быть применены волокнистые монокристаллы окиси алюминия. Эти волокна или усы можно нама-тывать на стержень радиусом в доли сантиметра, при этом они не растрескиваются. Кроме того, около 50% прочности при растяжении сохраняется при температуре плавления хромо-никелевого сплава . [c.192]
При измерении установившейся температуры пирометром с исчезающей нитью целесообразно подобрать ток таким образом, чтобы нить казалась раскаленной вначале несколько ярче, а затем несколько темнее источника излу чения, и соотв етствен-но сделать два отсчета. При постоянной температуре, например в точке плавления никеля, установлена возможность производить измерения в течение 10 мин., причем разброс замеров составляет не более 5°, тогда как при температуре плавления хрома (1860°) разброс не превышает 7°. При измерении изме- [c.116]
chem21.info
Концентрация - хром - Большая Энциклопедия Нефти и Газа, статья, страница 1
Концентрация - хром
Cтраница 1
Концентрация хрома в испытуемом растворе соответствует оптической плотности ЛСгЛобщ - Лха. [1]
Концентрация хрома в верхней зоне легированного слоя образца стали 25Л достигает 40 - 45 %, а на некоторых других таких же образцах приближается к концентрации хрома в легирующей поверхности литейной формы. На границе с легированным слоем в структуре стали имеется ферритная полоса, обедненная перлитом. В отожженных образцах эта полоса по размерам гораздо больше, чем в неотожженных, что, по-видимому, связано с диффузией углерода из стали в легированный слой к области, сильно насыщенной хромом. [3]
Концентрация хрома, которую до сих пор не удавалось объяснить, может быть легко объяснена, если учесть, что в случае роста двухмерного дендрита вектор диффузии должен содержаться в самой плоскости межповерхностной границы между зернами, а не перпендикулярно к ней, как это следует из схемы Бейна ( рис. 5), лежащей в основе теории. Схема Бейна объясняет межкристаллитную коррозию уменьшением концентрации хрома в результате диффузии из внутренней части кристалла в направлении между зернами. При температурах около 700 С скорость диффузии обеднения границ зерен хромом по границам зерен на несколько порядков величин превышает скорость диффузии внутри кристаллита. [5]
Концентрация хрома, молибдена, ванадия и марганца снижается по направлению к борированному слою, а никеля и кобальта - возрастает. [6]
Концентрации хрома менее 0 01 мг / мл не удается определять количественно, поскольку при столь низких концентрациях наблюдается быстрое нелинейное уменьшение чувствительности. [7]
Концентрация хрома может быть различной, изменяясь от сотых долей до нескольких процентов по массе. При увеличении концентрации Сг2О3 выше 8 % цвет смешанного кристалла изменяется от красного к зеленому, что объясняется появлением связей между ионами хрома. [8]
Концентрация хрома в тканях новорожденных, как правило, значительно выше, чем у взрослых, и быстро снижается в течение первых месяцев жизни. Исключение составляют печень и почки, в которых концентрация этого МЭ сохраняется на одном уровне от рождения до 10-летиего возраста [ Schroeder H. При сахарном диабете содержание хрома в тканях, как правило, понижено. [9]
Концентрацию хрома определяют химически. [10]
Концентрацию хрома находят методом сравнения или по градуиро-вочному графику. [11]
Определить концентрации хрома и марганца в растворе, если оптическая плотность исследуемого раствора в кювете 1 см при 550 нм и при 430 нм составляет DXI и Dx2 соответственно. [12]
При концентрации хрома 1 мг / л вода имеет горький вкус без запаха. Соединения хрома при соприкосновении с кожей оказывают общетоксическое воздействие на человека, вызывая дерматиты, экземы, а также аллергию. [13]
При концентрации хрома от 1 до 5 % ( табл. 1) большая его часть в катализаторе, активированном при 540 С, имеет степень окисления VL Однако при более высоких содержании хрома и температуре активации доля Cr ( VI) резко снижается. Это происходит даже при 540 С, если для активации используют влажный воздух. [14]
При концентрации хрома от 30 до 65 % из а-твердого раствора медленно охлажденных железохромистых сплавов выделяется хрупкая немагнитная - фаза. Основой этой фазы является металлическое соединение FeCr. Подробные свойства его сплавов изложены в гл. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Исследование свойств хрома и его соединений
План.
- Краткая характеристика.
- Физические свойства хрома.
- Химические свойства хрома.
- История открытия.
- Нахождение в природе.
- Виды соединений хрома.
- Лабораторные исследования.
- Область применения.
- Влияние на окружающую среду.
- Заключение.
1. Краткая характеристика.
Общие сведения.
Область применения хрома достаточно широка.
Хром и его соединения активно используются в промышленном производстве, в частности, в металлургии, химической и огнеупорной промышленности.
Хром Cr - химический элемент VI группы периодической системы Менделеева, атомный номер 24, атомная масса 51,996, радиус атома 0,0125, радиусы ионов Cr2+ - 0,0084; Cr3+ - 0,0064; Cr4+ - 6,0056.
Хром проявляет степени окисления +2, +3, +6, соответственно имеет валентности II, III, VI.
Имеет четыре стабильных изотопа с атомными массами 50, 52, 53, 54 . Самым распространенным из них, конечно, является хром с атомной массой 52 – 83,79% в природе.
Структура атома хрома изображена на рисунке:

2. Физические свойства хрома.
Хром представляет собой твердый, пластичный, довольно тяжелый, ковкий металл серо-стального цвета.
Кипит при 24690С, плавится при 1878± 220С. Обладает всеми характерными свойствами металлов - хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет блеск, присущий большинству металлов. И в то же время, устойчив к коррозии на воздухе и в воде.
Примеси кислорода, азота и углерода, даже в самых малых количествах, резко изменяют физические свойства хрома, например, делая его очень хрупким. Но, к сожалению, получить хром без этих примесей очень трудно.
Структура кристаллической решетки - объемноцентрированная кубическая. Особенностью хрома является резкое изменение его физических свойств при температуре около 37°С. Это аномальное явление ученым не удалось объяснить достоверно до сих пор. Дело в том, что в этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила.
Ниже приведена сводная таблица основных физических свойств хрома:
Параметр | Значение |
Температура кипения | 2469-2480 0C |
Температура плавления | 1878± 220С |
Теплота парообразования | 344,4 кДж/Моль |
Плотность при 200C | 7,19 г/см3 |
Теплопроводность | 93,7 Вт/(мґ К) |
Температурный коэффициент линейного расширения | 6,2ґ 10-6 |
Удельное электрическое сопротивление | 12,7ґ 10-8Омґ м |
Твердость по Бринеллю | 687 МПа |
Удельная магнитная восприимчивость | +4,45ґ 10-8м/кг3 |
3. Химические свойства хрома.
В зависимости от температур меняется и химическая активность хрома.
Так при небольших температурах хром мало активен и взаимодействует только со фтором.
С увеличением температуры от 6000C, начинает взаимодействовать с галогенами, серой, азотом, кремнием, бором, углеродом, кислородом.
Реакция с кислородом протекает сначала довольно активно, но через некоторое время резко замедляется, так как поверхность покрывается тонкой чрезвычайно устойчивой пленкой, препятствующему дальнейшему окислению.
Это явление получило название – пассивирование.
Хром пассивируется холодными концентрированными h3SO4 и HNO3, однако при сильном нагревании он растворяется в этих кислотах:
2Cr + 6h3SO4(конц.) = Cr2(SO4)3 + 3SO2 + 6h3O
Cr + 6HNO3(конц.) = Cr(NO3)3 + 3NO2 + 3h3O
Дальше, уже при 1200 0C пленка начинает разрушаться и окисление снова идет быстро.
При 20000C хром воспламеняется в кислороде с образованием темно-зеленого оксида Cr2O3.
В сильных разбавленных кислотах - HCl и h3SO4, хром имеет свойство растворяться.
В отсутствии воздуха при этом образуются соли Cr2+, а на воздухе - соли Cr3+:
Cr + 2HCl = CrCl2+ h3
4Cr + 12HCl +3O2 = 4CrCl3 + 6h3O
Благодаря защитной пленке, хром не растворим кислотах в h4PO4, HClO4.
Приведем основные химические реакции чистого хрома:
1.При температурах 0…600 0С:
- реакция со фтором 2Cr0 + 3F20 = 2Cr+3F3-
- При температурах 600…1200 0С:
- При температурах 1200…2000 0С:
- История открытия хрома.
- с кислородом 4Cr + 3O2 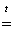 2Cr2O3
2Cr2O3
Хром был обнаружен в конце XVIII века.
В 1766 году петербургский профессор химии И.Г.Леман описал новый минерал,
найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга. Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец.
Спустя несколько лет, в 1770 году, Березовские рудники описал академик П.С.Паллас.
Вот как он описывал хром в своих работах:
“Березовские копи, состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная... Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...”.
Сначала обнаруженный минерал был назван “сибирским красным свинцом”. Впоследствии за ним закрепилось название “крокоит”.
В конце XVIII века образец крокоита был привезен Палласом в Париж.
Этим минералом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу.
Он проводит анализ минерала в своем отчете: “Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, были получены из Березовского золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились, и теперь этот минерал покупают на вес золота, в особенности, если он желтый.
Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе...
Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден. Большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...”
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был оксид шестивалентного хрома) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество.
Так впервые был выделен новый элемент. Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески “хрома” - окраска) из-за яркого разнообразного цвета его соединений. Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово “хром” в списки известных науке элементов.
В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. В металлургии, где расход хрома для легирования сталей очень велик, используют не сам хром, а его сплав с железом - феррохром.
Впервые феррохром был получен в 1820 году восстановлением смеси оксидов железа и хрома древесным углем в тигле. В 1865 году был выдан первый патент на хромистую сталь.
5. Нахождение в природе.
Среднее содержание хрома в земной коре 83 г/т, по массе содержание хрома в земной коре составляет 0,035%, в воде морей и океанов 2 x10-5 мг/л. Мировые подтвержденные запасы хромовых руд составляют 1,8 млрд. т. Более 60% cосредоточено в ЮАР. Крупными запасами обладают Зимбабве, Казахстан Турция, Индия, Бразилия. Руды хрома имеются в Новой Каледонии, на Кубе, в Греции, Югославии. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами.
Запасы хромовых руд России сосредоточены, главным образом, в группе Сарановских месторождений (Верблюжьегорское, Алапаевское, Халиловское и др.) на Урале (Пермская область) и составляют 6,4 млн. т. (0,36%от мировых запасов).
Добыча хромовых руд в мире составляет около 12 млн. т. в год, в том числе 108 тыс. т. в России. Главные производители товарной хромовой руды - ЮАР, Казахстан, на долю которых приходится более 60% добычи сырья ежегодно. В Красноярском крае месторождения хрома отсутствуют. Но на правом берегу р.Енисей, в устье р.Березовой (к югу от устья р. Подкаменная Тунгуска) есть рудопроявление с выходом пород 1,5´ 4 м, возраст пород оценивается в 500 млн. лет. Содержание чистого хрома в руде порядка 42% .
По содержанию Cr2O3 хромовые руды подразделяются на очень богатые (более 65%), богатые (65-52%), средние (52-45%), бедные (45-30%), убогие (30-10%). Руды, содержащие более 45% Cr2O3 не требуют обогащения.
- Виды соединений хрома.
- Лабораторные исследования.
1.Оксиды
Оксид хрома (II) CrO (основной) - сильный восстановитель, чрезвычайно неустойчив в присутствии влаги и кислорода. Практического значения не имеет.
Оксид хрома (III) Cr2O3 (амфотерный) устойчив на воздухе и в растворах.
Cr2O3 + h3SO4 = Cr2(SO4)3 + h3O
Cr2O3 + 2NaOH = Na2CrO4 + h3O
Образуется при нагревании некоторых соединений хрома (VI), например:
4CrO3 2Cr2O3 + 3О2
(Nh5)2Cr2O7 Cr2O3 + N2 + 4h3O
4Cr + 3O2 2Cr2O3
Оксид хрома (III) используется для восстановления металлического хрома невысокой чистоты с помощью алюминия (алюминотермия) или кремния (силикотермия):
Cr2O3 +2Al = Al2O3 +2Cr
2Cr2O3 + 3Si = 3SiO3 + 4Cr
Оксид хрома (VI) CrO3 (кислотный) - темно малиновые игольчатые кристаллы.
Получают действием избытка концентрированной h3SO4 на насыщенный водный раствор бихромата калия:
K2Cr2O7 + 2h3SO4 = 2CrO3 + 2KHSO4 + h3O
Оксид хрома (VI) - сильный окислитель, одно из самых токсичных соединений хрома.
При растворении CrO3 в воде образуется хромовая кислота h3CrO4
CrO3 + h3O = h3CrO4
Кислотный оксид хрома, реагируя со щелочами, образует желтые хроматы CrO42
CrO3 + 2KOH = K2CrO4 + h3O
2.Гидроксиды
Гидроксид хрома (III) обладает амфотерными свойствами, растворяясь как в
кислотах (ведет себя как основание),так и в щелочах (ведет себя как кислота):
2Cr(OH)3 + 3h3SO4 = Cr2(SO4)3 + 6h3O
Cr(OH)3 + KOH = K[Cr(OH)4]
Cr(OH)3 + NaOH = NaCrO2 + 2h3O
При прокаливании гидроксида хрома (III) образуется оксид хрома (III) Cr2O3.
Нерастворим в воде.
2Cr(OH)3 = Cr2O3 + 3h3O
3.Кислоты
Кислоты хрома, отвечающие его степени окисления +6 и различающиеся соотношением числа молекул CrO3 и h3O, существуют только в виде растворов. При растворении кислотного оксида CrO3, образуется монохромовая кислота (просто хромовая) h3CrO4.
CrO3 + h3O = h3CrO4
Подкисление раствора или увеличение в нем CrO3 приводит к кислотам общей формулы nCrO3 h3O
при n=2, 3, 4 это, соответственно, ди, три, тетрохромовые кислоты.
Самая сильная из них - дихромовая, то есть h3Cr2O7. Хромовые кислоты и их соли- сильные окислители и ядовиты.
4.Соли
Различают два вида солей: хромиты и хроматы.
Хромитами с общей формулой RCrO2 называются соли хромистой кислоты HCrO2.
Cr(OH)3 + NaOH = NaCrO2 + 2h3O
Хромиты обладают различной окраской - от темно коричневой до совершенно черной и обычно встречаются в виде сплошных массивов. Хромит мягче многих других минералов, температура плавления хромита зависит от его состава 1545-1730 0С.
Хромит имеет металлический блеск и почти нерастворим в кислотах.
Хроматы - соли хромовых кислот.
Соли монохромовой кислоты h3CrO4 называют монохроматами (хроматы) R2CrO4, соли дихромовой кислоты h3Cr2O7 дихроматы (бихроматы) - R2Cr2O7. Монохроматы обычно окрашены в желтый цвет. Они устойчивы только в щелочной среде, а при подкислении превращаются в оранжево-красные бихроматы:
2Na2CrO4 + h3SO4 = Na2Cr2O7 + Na2SO4 + h3O
1.Получение оксида хрома (III)
Приборы и реактивы: асбестированная сетка; спички; бихромат аммония (Nh5)2Cr2O7 (измельченный).
Выполнение опыта.
Расстилаю большой лист бумаги, на который кладу
асбестированную сетку. Тонко измельченный бихромат аммония насыпаю в виде горки. До бихромата аммония дотрагиваюсь зажженной спичкой.
Начинается разложение бихромата, которое протекает с выделением тепла и
постепенно захватывает все большие и большие количества соли. В конце реакция идет все более бурно - появляются искры, пламя, летит рыхлый и легкий пепел - типичное извержение вулкана в миниатюре. Образовалось большое количество рыхлого темно-зеленого вещества.
Вывод: оксид хрома (III) Cr2O3 получается путем нагревания бихромата аммония:
(Nh5)2Cr2O7Cr2O3+N2+4h3O
2.Получение гидроксида хрома.
Приборы и реактивы: раствор соли хрома (III) CrCl3, едкий натр (гидроксид
натрия) NaOH.
Выполнение опыта. В пробирку с раствором хлорида хрома (III) по каплям добавляю раствор едкого натра до образования серо-зеленого осадка.
Вывод: Гидроксид хрома Cr(OH)3 получается при действии на соль трехвалентного хрома щелочью:
CrCl3 + 3NaOH = Cr(OH)3Ї + 3NaCl
3.Исследование свойств оксида хрома (III)
Приборы и реактивы: колба, вода h3O, оксид хрома (III) Cr2O3, серная кислота.
Выполнение опыта.
Добавляю полученный зеленый порошок оксида хрома (III) сначала в колбу с водой Cr2O3 + 3h3O = 2Cr(OH)3,
затем в колбу с серной кислотой Cr2O3 + 3h3SO4 = Cr2(SO4)3 + 3h3O.
Наблюдаю растворение оксида в обоих колбах.
Вывод: Оксид хрома растворяется в воде и в кислотах.
4.Переход хромата в бихромат и обратно.
Приборы и реактивы: раствор хромата калия K2CrO4, раствор бихромата калия
K2Cr2O7, серная кислота, гидроксид натрия.
Выполнение опыта.
К раствору хромата калия добавляю серную кислоту, в результате
происходит изменение окраски раствора из желтого в оранжевый.
2K2CrO4 + h3SO4 = K2Cr2O7 + K2SO4 + h3O
К раствору бихромата калия добавляю щелочь, в результате происходит изменение окраски раствора из оранжевого в желтый.
K2Cr2O7 + 4NaOH = 2Na2CrO4 + 2KOH + h3O
Вывод: В кислой среде хроматы неустойчивы, ион CrO42- желтого цвета превращается в ион Cr2O72- оранжевого цвета, а в щелочной среде эта реакция протекает в обратном направлении
2CrO42- + 2H+ ® ¬ Cr2O72- + h3O.
® - кислая среда,
¬ - щелочная среда.
5.Исследование свойств солей хрома (VI)
Приборы и реактивы:концентрированная соляная кислота HCl, концентрированный раствор бихромата калия K2Cr2O7.
Выполнение опыта. Концентрированная соляная кислота HCl добавляется к концентрированному раствору бихромата калия K2Cr2O7.
Наблюдаем при нагревании выделение резкого хлорного запаха, от которого жжет нос и горло.
Вывод: Так как все соединения хрома (VI) являются сильными окислителями, то при реакции с соляной кислотой:
K2Cr2O7 + 14HCl = 3Cl2 + 2CrCl3 + 2KCl + 7h3O
происходит восстановление хлора:
2Cl-2е = Cl20
6.Получение малорастворимых солей хромовых кислот.
Приборы и реактивы: раствор бихромата калия K2Cr2O7, раствор нитрата серебра AgNO3, раствор хромата калия K2CrO4.
Выполнение опыта.
Наливаю в одну пробирку раствор хромата калия, в другую - раствор бихромата калия, и добавляю в обе пробирки раствор нитрата серебра, в обоих случаях наблюдаю образование красно-бурого осадка.
K2CrO4 + 2AgNO3= Ag2CrO4¯ + 2KNO3
K2Cr2O7 + AgNO3 ® Ag2CrO4¯ + KNO3
Вывод: Растворимые соли хрома при взаимодействии с нитратом серебра образуют нерастворимый осадок.
7.Окислительные свойства солей хрома (VI)
Приборы и реактивы: раствор сульфита натрия Na2SO3, серная кислота h3SO4,раствор бихромата калия K2Cr2O7.
Выполнение опыта.
К раствору K2Cr2O7, подкисленному серной кислотой, добавляю раствор Na2SO4. Происходит изменение окраски.
Оранжевый раствор стал зелено- фиолетовым.
Вывод: В кислой среде хром восстанавливается сульфитом натрия от хрома (VI) до хрома (III):
K2Cr2O7 + 3Na2SO3 + 4h3SO4 = K2SO4 + Cr2(SO4)3 + 3Na2SO4 + 4h3O
8. Область применения.
Основная часть добываемой в мире хромистой руды поступает сегодня на
ферросплавные заводы, где выплавляются различные сорта феррохрома и
металлического хрома.
В химической промышленности используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют “хромом”, а сапоги из нее “хромовыми”.
Хромиты широко используют в огнеупорной промышленности для изготовления
огнеупорного хромитового и хромомагнезитового кирпича. Такой кирпич химически пассивен, устойчив при температурах выше 22000С, хорошо выдерживает резкие колебания температур.
Магнезитохромитовый кирпич - отличный огнеупорный материал для футеровки (защитной внутренней облицовки) мартеновских печей и других металлургических агрегатов. Своды из хромомагнезитового кирпича выдерживают вдвое больше плавок, чем своды из упорного кварцевого материала.
Химики используют хромиты для получения бихроматов калия и натрия, а также
хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют “хромом”, а сапоги из нее “хромовыми”.
Растворимые в воде хроматы натрия и калия применяются в текстильном и кожевенном производстве, как консерванты древесины (они уничтожают древесные грибки).
Хромовая смесь - сернокислый раствор бихромата калия или натрия используется для мытья химической посуды в лабораториях. Наиболее часто применяется раствор содержащей по массе приблизительно 12 частей K2Cr2O7, 70 частей воды и 22 части h3SO4.
Как бы оправдывая свое название, хром принимает деятельное участие в
производстве красителей для стекольной, керамической, текстильной
промышленности.
Нерастворимые хроматы некоторых металлов (PbCrO4, ZnCrO4, SrCrO4) - прекрасные художественные краски. Богатством оттенков – от розово-красного до фиолетового славится SnCrO4, используемый в живописи по фарфору.
В мире драгоценных камней рубину принадлежит второе место после алмаза.
Технология получения искусственного рубина заключается в следующем: в оксид
алюминия Al2O3 вводят дозированную добавку оксида хрома (III), - ему-то и
обязаны рубиновые кристаллы своим чарующим цветом. Но искусственные рубины
ценятся не только за свои “внешние данные”: рожденный с их помощью лазерный луч способен буквально творить чудеса.
Оксид хрома (III) позволил тракторостроителям значительно сократить сроки
обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны “привыкнуть” друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошел оксид хрома (III). Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы оксида хрома (III), которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Замена в рабочем слое магнитофонной пленки оксида железа на частицы оксида хрома (III) позволила резко улучшить качество звучания, пленка стала надежнее в работе.
Фотоматериалы и лекарства, катализаторы для химических процессов и металлические покрытия - всюду хром оказывается “при деле”.
Особое внимание следует уделить хромовым покрытиям. Коснемся их более подробно.
Хромирование.
Известно, что хорошо сопротивляется окислению на воздухе, не взаимодействует с кислотами, и самое главное, не имеет конукурентов по степени твердости среди металлов.
Сначала, тонкий слой этого металла попробовали электролитически осаждать на поверхность изделий из других материалов, чтобы предохранить их от коррозии, царапин и различных повреждений.
Но хромовые покрытия оказались пористыми и легко отслаивались.
И лишь в начале XIX века проблема была решена. Дело в том, что использовавшийся трехвалентный хром, содержащийся в электоролите, не мог создать нужного покрытия. Опыт удался, когда стали использовать электролит, содержащий хром – шестивалентный.
В качестве электролита начали применять хромовую кислоту - в ней валентность хрома равна 6.
Иногда хромовое покрытие используют в декоративных целях - для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002-0,0005 миллиметра).
Толщина защитных покрытий на некоторых наружных деталях автомобилей, мотоциклов, велосипедов составляет до 0,1 миллиметра.
Литовскими химиками был разработан способ многослойного покрытия, для особо
ответственных деталей.
Верхний слой этого покрытия состоит из хрома и по внешнему виду напоминает кольчугу. В процессе эксплуатации на этот слой приходится вся нагрузка, но пройдут многие годы, прежде чем он начнет окисляться.
Изделия из пластмасс так же подвергаются хромированию. Так полистирол, широко известный полимер, заключенный в хромовую оболочку, стал намного прочнее, для него оказались менее страшными истирание, удары и изгибы.
Следующий способ хромирования – диффузионный.
Принципиальное его отличие в том, что он протекает не в гальванических ваннах, а в печах.
Первоначально стальную деталь помещали в
порошок хрома и нагревали в восстановительной атмосфере до высоких температур.
На поверхности детали при таком способе появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь.
Недостатком такого способа являлось то, что при температуре примерно 1000°С хромовый порошок на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь.
Потому для этой цели начали использовать летучие галоидные соли хрома, вместо порошка. Соли хрома, так называемый хлорид или иодид, позволяют снизить температуру процесса.
Получают хлорид (йодид) хрома непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром.
При этом образуется газообразный хлорид, который обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. С основным материалом такое покрытие гораздо прочнее связано, чем гальваническое.
Еще одна область применения хрома, которую следует рассмотреть более подробно - это сплавы.
Хромовые сплавы весьма многочисленны.
Приведем основные из них в виде таблицы:
Название | Хром Cr | Никель Ni | Кобальт Co | Алюминий Al | Железо Fe | Вольфрам W |
Феррохром | 65% | 35 % | ||||
Хромаль | 17-30% | 4-6% | 64-79% | |||
Стеллит | 20-25% | 45-60% | 1-3% | 5-29% | ||
Нихром | 15-30% | 70-85% |
Феррохром в идеале – это чистый сплав хрома с железом.
Хром в таком сплаве вводится в жидкую сталь для ее легирования. Однако, температура плавления хрома выше, чем у стали и вводить его в сталь в чистом виде весьма затруднительно.
У феррохрома же температура плавления такая же, как у стали, или ниже.
Стеллит – сплав хрома и кобальта. Применяется в металлообрабатывающей промышленности. Его хорошо использовать для изготовления режущих инструментов. Это очень твердый сплав.
Стоек против износа и коррозии.
Хромали и нихромы используются в основном в приборостроении, в частности, для изготовления нагревателей в электрических печах сопротивления, т.к. весьма устойчивы в температурном интервале 1000-13000C и обладают высоким электросопротивлением.
Комохром - сплав хрома, кобальта и молибдена. Используется в медицине, в восстановительной хирургии. Этот сплав безвреден для человеческого организма.
Вообще, добавка к хромоникелевым сплавам кобальта и молибдена позволяет металлу переносить большие нагрузки при 650-900° С.
Всем известна сталь с добавлением хрома и никеля – “нержавейка”. Эта сталь, отлично противостоящая коррозии и окислению, содержит примерно 17-19% хрома и 8-13% никеля. Содержание углерода в такой стали допускается не более 0,1%.
Чтобы при высоких температурах сталь ложилась гладко и не покрывалась “чешуей”, когда детали нагреваются до сотен градусов, в нее вводят 25-30% хрома. Такой прием позволяет стали выдерживает температуры до 1000°С.
9. Влияние на окружающую среду.
Здесь я хочу рассмотреть вредное влияние геологоразведочных работ, добычи и переработки сырья на состояние окружающей среды и живые организмы.
Хром – очень токсичный элемент, но не всегда это учитывается при проведении геологоразведочных работ. А меры защиты окружающей среды при этом процессе необходимы.
Для исключения попадания рудной пыли в воздух населенных пунктов, при добыче хромовых руд, следует выполнять ряд условий:
- соблюдение определенного расстояния от населенных пунктов,
- орошение дорог в карьерах и в складах добытой руды.
Как уже было отмечено выше, хром относится к высоко токсичным веществам. Действие на живой организм солей хрома сопровождается раздражением кожи или слизистой оболочки, иногда с образованием язв.
Главным образом соли хрома опасны тем, что поражают верхние дыхательные пути, легкие и глаза.
Оксиды хрома менее токсичны, чем чистый металл.
Значительное нарушение окружающей среды связано с переработкой хромового сырья.
В процессе переработки сырья, при сухом долблении и сортировке, в воздух попадает большое количество пыли.
А в процессе переработки сырья, при мокром обогащении, хром и его оксиды попадают в сточные воды. При этом сброс сточных вод в водоемы не возможен без очистки.
Для хранения отходов предусматривается строительство экранированных шламохранилищ.
10.Заключение
В данной работе проведен анализ хрома и его соединений по всем направлениям.
Дана общая характеристика хрома, как металла, подробно изложена информация о физических и химических свойствах данного металла. Отмечены малая химическая активность хрома, сильные окислительные свойства и высокая токсичность его соединений.
Приведен ряд экспериментов, с указанием реагентов и реакций образования.
Большое внимание уделено исследованию различных соединений хрома - оксидов, гидроксидов и солей.
Отдельным пунктом приведены интересные факты из истории открытия хрома, от его открытия до присвоения настоящего названия.
Указаны основные месторождения хрома.
А так же рассмотрен важный, на мой взгляд вопрос, об экологическом загрязнении окружающей среды, при добыче и переработке хромовых руд.
Список литературы.
1. Салли А., Брендз Э. Хром.- Изд. 2-е переработ. и доп. Перев. с англ. М.: Металлургия, 1971.- 360 с.
2. Лисицын А.Е., Остапенко П.Е. Минеральное сырье. Хром // Справочник. - М :ЗАО Геоинформмарк, 1999. - 25 с.
3. Энциклопедический словарь юного химика/ Сост. В.А.Крицман, В.В.Станцо.- М.: Педагогика, 1982.- 368 с.
4. Химия. Решение задач: учеб. пособие для уч. сред. и ст. шк. возраста/ Авт.- сост. А.Е.Хасанов. - Мн.: Современный литератор, 1999. -448 с.
5. Неорганическая химия. Энциклопедия школьника/ Гл. ред. И.П.Алимарин.- М.: Советская Энциклопедия, 1975.- 384 с.
studyport.ru