Подгруппа хрома. Подгруппа хрома
Подгруппа хрома
Подгруппа хрома - побочная подгруппа VI группы Свойства элементов подгруппы хрома
|
Атомный номер |
Название |
Электронная конфигурация |
r г/см3 |
t°пл.°C |
t°кип.°C |
ЭО |
Атомный радиус, нм |
Степень окисления |
|
24 |
Хром Cr | [Ar] 3d54s1 |
7,2 |
1857 |
2672 |
1,56 |
0,125 |
+1,+2,+3,+4,+5,+6 |
|
42 |
Молибден Mo | [Kr] 4d55s1 |
10,2 |
2610 |
2560 |
1,3 |
0,135 |
+1,+2,+3,+4,+5,+6 |
|
74 |
Вольфрам W | [Xe] 4f145d46s2 |
19,3 |
3410 |
5660 |
1,4 |
0,141 |
+1,+2,+3,+4,+5,+6 |
Физические свойства Блестящие, сероватого цвета металлы. С увеличением атомного номера растут температуры плавления и кипения.Вольфрам - самый тугоплавкий из известных металлов. Химические свойства В ряду Cr – Mo – W химическая активность падает.С увеличением степени окисления элементов у их оксидов и гидроксидов законо-мерно происходит ослабление основных свойств и усиление кислотных. Высшим оксидам RO3 соответствуют кислоты h3RO4.В том же направлении происходит усиление окислительных свойств соединений. Хром и его соединения Получение
1. Алюминотермия: Cr2O3 + 2Al ® Al2O3 + 2Cr 2. Восстановлением оксидов оксидом углерода (II). 3. Электролизом водных растворов соединений хрома.
При обычных условиях хром реагирует только со фтором. При высоких температурах (выше 600°C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором. 4Cr + 3O2 –t°® 2Cr2O32Cr + 3Cl2 –t°® 2CrCl32Cr + N2 –t°® 2CrN2Cr + 3S –t°® Cr2S3 В раскалённом состоянии реагирует с парами воды: 2Cr + 3h3O « Cr2O3 + 3h3 Хром растворяется в разбавленных сильных кислотах (HCl, h3SO4)В отсутствии воздуха образуются соли Cr2+, а на воздухе – соли Cr3+. Cr + 2HCl ® CrCl2 + h32Cr + 6HCl + O2 ® 2CrCl3 + 2h3O + h3 Наличие защитной окисной плёнки на поверхности металла объясняет его пассив-ность по отношению к концентрированным растворам кислот – окислителей. Соединения хрома Соединения двухвалентного хрома Оксид хрома (II) и гидроксид хрома (II) имеют основной характер. Cr(OH)2 + 2HCl ® CrCl2 + 2h3O Соединения хрома (II) - сильные восстановители; переходят в соединения хрома (III) под действием кислорода воздуха. 2CrCl2 + 2HCl ® 2CrCl3 + h34Cr(OH)2 + O2 + 2h3O ® 4Cr(OH)3 Соединения трёхвалентного хрома Оксид хрома (III) Cr2O3 – зелёный, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома (III) или дихроматов калия и аммония: 2Cr(OH)3 –t°® Cr2O3 + 3h3O4K2Cr2O7 –t°® 2Cr2O3 + 4K2CrO4 + 3O2(Nh5)2Cr2O7 –t°® Cr2O3 + N2+ 4h3O Амфотерный оксид. При сплавлении Cr2O3 со щелочами, содой и кислыми солями получаются соединения хрома со степенью окисления (+3): Cr2O3 + 2NaOH ® 2NaCrO2 + h3OCr2O3 + Na2CO3 ® 2NaCrO2 + CO2Cr2O3 + 6KHSO4 ® Cr2(SO4)3 + 3K2SO4 + 3h3O При сплавлении со смесью щёлочи и окислителя получают соединения хрома в степени окисления (+6): 2Cr2O3 + 4KOH + KClO3 ® 2K2Cr2O7(дихромат калия) + KCl + 2h3O Гидроксид хрома (III) Cr(OH)3 - нерастворимое в воде вещество зелёного цвета. Cr2(SO4)3 + 6NaOH ® 2Cr(OH)3¯ + 3Na2SO4 Обладает амфотерными свойствами - растворяется как в кислотах, так и в щелочах: 2Cr(OH)3 + 3h3SO4 ® Cr2(SO4)3 + 6h3OCr(OH)3 + KOH ® K[Cr(OH)4](или, упрощая, Cr(OH)3 + KOH ® KCrO2(хромат калия) + 2h3O) Соли хрома (III) имеют фиолетовую или тёмно-зелёную окраску. По химическим свойствам напоминают бесцветные соли алюминия.Соединения Cr (III) могут проявлять и окислительные, и восстановительные свойства: Zn + 2Cr+3Cl3 ® 2Cr+2Cl2 + ZnCl22Cr+3Cl3 + 16NaOH + 3Br2 ® 6NaBr + 6NaCl + 8h3O + 2Na2Cr+6O4 Соединения шестивалентного хрома Оксид хрома (VI) CrO3 - ярко-красные кристаллы, растворимые в воде.Получают из хромата (или дихромата) калия и h3SO4(конц.). K2CrO4 + h3SO4 ® CrO3 + K2SO4 + h3OK2Cr2O7 + h3SO4 ® 2CrO3 + K2SO4 + h3O CrO3 - кислотный оксид, со щелочами образует жёлтые хроматы CrO42-: CrO3 + 2KOH ® K2CrO4 + h3O В кислой среде хроматы превращаются в оранжевые дихроматы Cr2O72-: 2K2CrO4 + h3SO4 ® K2Cr2O7 + K2SO4 + h3O В щелочной среде эта реакция протекает в обратном направлении: K2Cr2O7 + 2KOH ® 2K2CrO4 + h3O кислая среда 2CrO42- + 2H+ ¬––––––––––––––––––––––––® Cr2O72- + h3O щелочная среда
Все соединения хрома (VI) - сильные окислители. 4CrO3 + 3S ® 3SO2 + 2Cr2O3
www.examen.ru
ПОДГРУППА ХРОМА. Общая химия
ПОДГРУППА ХРОМА
Подгруппу хрома образуют металлы побочной подгруппы шестой группы — хром, молибден и вольфрам.
Наружный электронный слой атомов элементов подгруппы хрома содержит один или два электрона, что обусловливает металлический характер этих элементов и их отличие от элементой главной подгруппы. Вместе с тем их максимальная степень окисленности равна +6, так как, помимо наружных электронов, в образовании связей может участвовать еще соответствующее число электронов из недостроенного предпоследнего слоя.
Для хрома и его аналогов наиболее типичны производные высшей степени окисленности, во многом сходные с соответствующими соединениями серы. 228. Хром (Chromium).
Хром содержится в земной коре в количестве 0,02% (масс.). В природе он встречается главным образом в виде хромистого железняка FeO·Cr2O3, богатые месторождения которого имеются в Казахстане и на Урале.
При восстановлении хромистого железняка углем получается сплав хрома с железом — феррохром, который непосредственно используется в металлургической промышленности при производстве хромистых сталей. Для получения чистого хрома сначала получают оксид хрома(III), а затем восстанавливают его алюмино-термическим способом.
- 634 -
Хром представляет собой твердый блестящий металл, плавящийся при 1890°C плотность его 7,19 г/см3. При комнатной температуре хром стоек и к воде и к воздуху. Разбавленные серная и соляная кислоты растворяют хром с выделением водорода. В холодной концентрированной азотной кислоте хром нерастворим и после обработки ею становится пассивным.
Металлический хром используется для хромирования, а также в качестве одного из важнейших компонентов легированных сталей. Введение хрома в сталь повышает ее устойчивость против коррозии как в водных средах при обычных температурах, так и в газах при повышенных температурах. Кроме того, хромистые стали обладают повышенной твердостью. Хром входит в состав нержавеющих кислотоупорных, жаропрочных сталей (см. также стр. 537, 665).
Хром образует три оксида: оксид хрома(II), или закись хрома, CrO, имеющий основной характер, оксид хрома (III), или окись хрома, Cr2O3, проявляющий амфотерные свойства, и оксид хрома (VI), или хромовый ангидрид, CrO3 — кислотный оксид. Соответственно этим трем оксидам известны и три ряда соединений хрома.
Соединения хрома(II).
Соединения хрома(III).
Оксид хрома(III) Cr2O3 представляет собой тугоплавкое вещество зеленого цвета, применяемое род названием зеленого крона для приготовления клеевой и масляной красок. При сплавлении с силикатами оксид хрома (III) окрашивает их в зеленый цвет и поэтому служит для окраски стекла и фарфора, Cr2O3 входит также в состав полирующих средств.
Гидроксид хрома(III) Cr(OH)3 выпадает в виде синевато-серого осадка при действии щелочей на соли хрома(III):
Подобно гидроксидам алюминия и цинка, он имеет амфотерный характер и растворяется в кислотах с образованием солей хрома (III), а в щелочах — с образованием изумрудно-зеленых растворов хромитов, например:
или
Хромиты, полученные сплавлением Cr2O3 с оксидами других металлов и известные главным образом для двухвалентных металлов, имеют состав, отвечающий формуле M(CrO2)2, и представляют собой соли метахромистой кислоты HCrO2.
- 635 -
К ним относится и природный хромистый железняк Fe(CrO2O)2.
Из солей хрома(III) самой распространенной является двойная соль хрома и калия — хромокалиевые квасцы KCr(SO4)2·12h3O, образующие сине-фиолетовые кристаллы. Хромокалиевые квасцы применяются в кожевенной промышленности для дубления кож и в текстильной промышленности в качестве протравы при крашении.
Соли хрома(III) во многом похожи на соли алюминия. В водных растворах они сильно гидролизованы и легко превращаются в основные соли. Со слабыми кислотами хром(III), подобно алюминию, солей не образует.
Растворы солей хрома (III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. В некоторых случаях такие гидраты удалось выделить в твердом виде. Так, кристаллогидрат хлорида хрома (III) CrCl3·6h3O известен в трех изомерных формах: в виде сине-фиолетовых, темнозеленых и светло-зеленых кристаллов одинакового состава. Строение этих изомеров можно установить на основании различного отношения их свежеприготовленных растворов к нитрату серебра. При действии последнего на раствор сине-фиолетового гидрата осаждается весь хлор; из раствора темнозеленого гидрата осаждается 2/3 хлора, а из раствора светло-зеленого гидрата — только 1/3 хлора. Принимая во внимание эти данные, а также координационное число хрома, равное шести, строение рассматриваемых кристаллогидратов можно выразить следующими формулами:
сине-фиолетовый темно-зеленый светло-зеленый
Таким образом, изомерия гидратов хлорида хрома (III) обусловлена различным распределением одних и тех же групп (h3O и Cl-) между внутренней и внешней координационными сферами и может служить примером гидратной изомерии (стр. 574).
Соединения хрома(VI).
Важнейшими соединениями хрома (VI) являются триоксид хрома, или хромовый ангидрид, CrO3 и соли отвечающих ему кислот — хромовой h3CrO4 и двухромовой h3Cr2O7. Обе кислоты существуют только в водном растворе и при попытках выделить их из раствора распадаются на хромовый ангидрид и воду; но соли их достаточно стойки. Соли хромовой кислоты называются хроматами, а двухромовой — бихроматами или дихроматами.
Почти все хроматы имеют желтую окраску. Некоторые из них применяются в качестве красок. Например, нерастворимый в воде хромат свинца PbCrO4, под названием желтый крон, служит для приготовления желтой масляной краски.
При подкислении раствора какого-нибудь хромата, например хромата калия K2CrO4, чисто-желтая окраска раствора сменяется на оранжевую вследствие перехода ионов CrO42- в ионы Cr2O72-.
- 636 -
Из полученного раствора может быть выделена соль двухромовой кислоты — дихромат калия K2Cr2O7 — в виде оранжево-красных кристаллов. Реакция превращения хромата в дихромат выражается уравнением:
Реакция обратима. Это значит, что при растворении дихромата в воде всегда образуется некоторое, хотя и незначительное, количество ионов H+ и CrO42- поэтому раствор дихромата имеет кислую реакцию. Если к раствору дихромата прибавлять щелочь, то гидроксид-ионы будут связывать находящиеся в растворе ионы водорода, равновесие смещается влево и в результате дихромат превращается в хромат. Таким образом, в присутствии избытка гидроксид-ионов в растворе практически существуют только ионы CrO42-, т. е. хромат, а при избытке ионов водорода — ионы Cr2O72-, т. е. дихромат.
Хроматы щелочных металлов получаются путем окисления соединений хрома(III) в присутствии щелочи. Так, при действии брома на раствор хромита калия образуется хромат калия:
О происходящем окислении можно судить по тому, что изумрудно-зеленая окраска раствора хромита переходит в ярко-желтую.
Хроматы могут быть получены также сплавлением Cr2O3 со щелочью в присутствии какого-нибудь окислителя, например хлората калия:
Хроматы и дихроматы — сильные окислители. Поэтому ими широко пользуются для окисления различных веществ. Окисление производится в кислом растворе и обычно сопровождается резким изменением окраски (дихроматы окрашены в оранжевый цвет, а соли хрома(III) зеленый или зеленовато-фиолетовый).
Мы видели, что в кислых и в щелочных растворах соединения хрома (III) и хрома (VI) существуют в разных формах: в кислой среде в виде ионов Cr3+ или Cr2O72-, а в щелочной — в виде ионов [Cr(OH)6]3- или CrO42-. Поэтому взаимопревращение соединений хрома (III) и хрома (VI) протекает по-разному в зависимости от реакции раствора. В кислой среде устанавливается равновесие
а в щелочной
Однако и в кислой, и в щелочной среде окисление хрома (III) приводит к уменьшению pH раствора; обратный же процесс — восстановление хрома(VI) - сопровождается увеличением pH.
- 637 -
Поэтому, в соответствии с принципом Ле Шателье, при повышении кислотности среды равновесие смещается в направлении восстановления хрома (VI), а при уменьшении кислотности — в направлении окисления хрома (III). Иначе говоря, окислительные свойства соединений хрома (VI) наиболее сильно выражены в кислой среде, а восстановительные свойства соединений хрома(III) - в щелочной. Именно поэтому, как указывалось выше, окисление хромитов в хроматы осуществляют в присутствии щелочи, а соединения хрома (VI) применяют в качестве окислителей в кислых растворах.
Приведем несколько примеров окислительно-восстановительных реакций, протекающих при участии дихроматов.
1. При пропускании сероводорода через подкисленный серной кислотой раствор дихромата оранжевая окраска раствора переходит в зеленую и одновременно жидкость становится мутной вследствие выделения серы:
2. При действии концентрированной соляной кислоты на дихромат калия выделяется хлор и получается зеленый раствор, содержащий хлорид хрома (III):
3. Если пропускать диоксид серы через концентрированный раствор дихромата калия, содержащий достаточное количество серной кислоты, то образуются эквимолекулярные количества сульфатов калия и хрома (III):
При выпаривании раствора из него выделяются хромокалиевые квасцы KCr(S)4)2·12h3O. Этой реакцией пользуются для получения хромокалиевых квасцов в промышленности.
Наиболее важными из дихроматов являются дихромат калия K2Cr2O7 и дихромат натрия Na2Cr2O7·2h3O, образующие оранжево-красные кристаллы. Обе соли, известные также под названием хромпиков, широко применяются в качестве окислителей при производстве многих органических соединений, в кожевенной промышленности при дублении кож, в спичечной и текстильной промышленности. Смесь концентрированной серной кислоты с водным раствором дихромата калия или натрия под названием «хромовой смеси» часто применяется для энергичного окисления и для очистки химической посуды.
Все соли хромовых кислот ядовиты.
Триоксид хрома, или хромовый ангидрид, CrO3 выпадает в виде темно-красных игольчатых кристаллов при действии концентрированной серной кислоты на насыщенный раствор дихромата калия или натрия:
- 638 -
Хромовый ангидрид принадлежит к числу наиболее сильных окислителей. Например, этиловый спирт при соприкосновении с ним воспламеняется. Производя окисление, хромовый ангидрид превращается в оксид хрома (III) Cr2O3.
Хромовый ангидрид легко растворяется в воде с образованием хромовой и двухромовой кислот.
229. Молибден (Mollbdenium).
Главным природным соединением молибдена является молибденит, или молибденовый блеск, MoS2 — минерал, очень похожий по внешнему виду на графит и долгое время считавшийся таковым. В 1778 г. Шееле, показал, что при обработке молибденового блеска азотной кислотой получается белый остаток, обладающий свойствами кислоты. Шееле назвал его молибденовой кислотой и сделал заключение, что сам минерал представляет собой сульфид нового элемента. Пять лет спустя этот элемент был получен в свободном состоянии путем прокаливания молибденовой кислоты с древесным углем.
Общее содержание молибдена в земной коре составляет 0,001% (масс.). Залежи молибденовых руд имеются в СССР, Чили, Мексике, Норвегии и Марокко. Большие запасы молибдена содержатся в сульфидных медных рудах.
Для получения металлического молибдена из молибденового блеска последний переводят обжигом в MoO3, из которого металл восстанавливают водородом. При этом молибден получается в виде порошка.
Компактный молибден получают главным образом методом порошковой металлургии. Этот способ состоит из прессования порошка в заготовку и спекания заготовки.
При прессовании порошка из него получают заготовки — тела определенной формы, обычно — бруски (штабики). Штабики молибдена получают в стальных пресс-формах при давлении до 300 МПа. Спекание штабиков в атмосфере водорода проводят в две стадии. Первая из них — предварительное спекание — проводится при 1100-1200°C и имеет целью повысить прочность и электрическую проводимость штабиков. Вторая стадия — высокотемпературное спекание — осуществляется пропусканием электрического тока, постепенно нагревающего штабики до 2200-2400°C. При этом получается компактный металл. Спеченные штабики поступают на механическую обработку — ковку, протяжку.
Для получения крупных заготовок молибдена применяют дуговую плавку, позволяющую получать слитки массой до 2000 кг. Плавку в дуговых печах ведут в вакууме. Между катодом (пакет спеченных штабиков молибдена) и анодом (охлаждаемый медный тигель) зажигают дугу. Металл катода плавится и собирается в тигле. Вследствие высокой теплопроводности меди и быстрого отвода теплоты молибден затвердевает.
Для получения особо чистого молибдена и других тугоплавких металлов применяется плавка в электронном пучке (электронно-лучевая плавка).
- 639 -
Нагревание металла электронным пучком основано на превращении в теплоту большей части кинетической энергии электронов при их столкновении с поверхностью металла. Установка для электронно-лучевой плавки состоит из электронной пушки, создающей управляемый поток электронов, и плавильной камеры. Плавку ведут в высоком вакууме, что обеспечивает удаление примесей, испаряющихся при температуре плавки (O, N, P, As, Fe, Cu, Ni и др.). Кроме того, высокое разрежение необходимо для предотвращения столкновений электронов с молекулами воздуха, что приводило бы к потере электронами энергии. После электронно-лучевой плавки чистота молибдена повышается до 99,9%.
Кроме компактных тугоплавких металлов методами порошковой металлургии получают ряд других материалов. Важнейшими из них являются карбидные твердые сплавы, ферриты, пористые материалы, керметы.
О карбидных твердых сплавах рассказывается в § 230, о ферритах — в § 242. К изделиям из пористых материалов относятся пористые подшипники и металлические фильтры. Пористые подшипники изготовляют спеканием порошков бронзы и графита. Поры таких подшипников пропитывают смазочным материалом, что дает возможность использовать их в условиях затрудненной смазки и при опасности загрязнения продукции (например, в пищевой или текстильной промышленности). Металлические фильтры изготовляют спеканием порошков меди, никеля, нержавеющей стали. Они служат для очистки различных жидкостей, масел, жидкого топлива, обладают длительным сроком службы, устойчивы при повышенных температурах и могут быть изготовлены в широком диапазоне пористости.
Керметы, или керамикометаллические материалы, получают спеканием смесей порошков металлов и неметаллических компонентов — тугоплавких оксидов, карбидов, боридов и др. В качестве металлической составляющей используют, главным образом, металлы подгрупп хрома и железа. Эти материалы сочетают в себе тугоплавкость, твердость и жаростойкость керамики с проводимостью, пластичностью и другими свойствами металлов.
Молибден — серебристо-белый металл плотностью 10,2 г/см3, плавящийся при 2620°C. При комнатной температуре он не изменяется на воздухе, но при накаливании окисляется в белый триоксид MoO3. Соляная и разбавленная серная кислоты при комнатной температуре не действуют на молибден; он растворяется в азотной кислоте или горячей концентрированной серной кислоте.
Около 80% всего добываемого молибдена расходуется на производство специальных сортов стали. Он входит в состав многих нержавеющих сталей; кроме того, его введение способствует увеличению их жаропрочности.
Из сплава молибдена с танталом изготовляют лабораторную посуду, применяемую в химических лабораториях вместо платиновой. Из чистого молибдена изготовляют детали электронных ламп и ламп накаливания — аноды, сетки, катоды, вводы тока, держатели нитей накала.
В своих соединениях молибден проявляет положительные степени окисленности: шесть, пять, четыре, три и два. Наиболее стойкими являются соединения молибдена (VI). Важнейшие из них - соли молибденовой кислоты h3MoO4 (молибдаты), часто имеющие сложный состав.
- 640 -
Молибдат аммония (Nh5)6Mo7O24·4h3O применяется в анализе для открытия и количественного определения фосфорной кислоты, с которой он образует характерный желтый осадок состава (Nh5)3PO4·12MoO3·6h3O. Последний представляет собою аммонийную соль комплексной фосфорномолибденовой кислоты, относящейся к классу гетерополикислот (см. § 204).
230. Вольфрам (Wolfram).
По распространенности в земной коре [0,007% (масс.)] вольфрам уступает хрому, но превосходит молибден. Природные соединения вольфрама в большинстве случаев представляют собой вольфраматы — соли вольфрамовой кислоты h3WO4. Так, важнейшая вольфрамовая руда — вольфрамит— состоит из вольфраматов железа и марганца. Часто встречается также минерал шеелит CaWO4.
Для выделения вольфрама из вольфрамита последний сплавляют в присутствии воздуха с содой. Вольфрам переходит в вольфрамат натрия Na2WO2, который извлекают из полученного сплава водой, а железо и марганец превращаются в нерастворимые в воде соединения Fe2O3 и Mn3O4.
Из водного раствора действием соляной кислоты выделяют свободную вольфрамовую кислоту в виде аморфного желтого осадка:
При прокаливании вольфрамовая кислота переходит в триоксид вольфрама WO3. Восстанавливая его водородом или углеродом (для чего используют чистые сорта сажи), получают порошок металлического вольфрама, подвергаемый в дальнейшем для получения компактного металла такой же обработке, как и порошок молибдена.
Вольфрам — тяжелый белый металл плотностью 19,3 г/см3. Его температура плавления (около 3400°C) выше, чем температура плавления всех других металлов. Вольфрам можно сваривать и вытягивать в тонкие нити.
На воздухе вольфрам окисляется только при температуре красного каления. Он очень стоек по отношению к кислотам, даже к царской водке, но растворяется в смеси азотной кислоты и фторо-водорода.
Большая часть добываемого вольфрама расходуется в металлургии для приготовления специальных сталей и сплавов. Быстрорежущая инструментальная сталь содержит до 20% вольфрама и обладает способностью самозакаливаться. Такая сталь не теряет Своей твердости даже при нагревании докрасна. Поэтому применение резцов, сделанных из вольфрамовой стали, позволяет значительно увеличить скорость резания металлов.
Кроме быстрорежущих широко применяются другие вольфрамовые и хромовольфрамовые стали. Например, сталь, содержащая от 1 до 6% вольфрама и до 2% хрома, применяется для изготовления пил, фрез, штампов.
- 641 -
Как самый тугоплавкий металл вольфрам входит в состав ряда жаропрочных сплавов. В частности, его сплавы с кобальтом и хромом — стеллиты — обладают высокими твердостью, износоустойчивостью, жаростойкостью. Сплавы вольфрама с медью и с серебром сочетают в себе высокие электрическую проводимость, теплопроводность и износоустойчивость.
Они применяются для изготовления рабочих частей рубильников, выключателей, электродов для точечной сварки.
Чистый вольфрам в виде проволоки, ленты и различных деталей применяют в производстве электрических ламп, в радиоэлектронике, в рентгенотехнике. Вольфрам — лучший материал для нитей ламп накаливания: высокая рабочая температура (2200-2500°C) обеспечивает большую светоотдачу, а очень малое испарение — длительный срок службы нитей из вольфрама. Вольфрамовую проволоку и прутки применяют также в качестве нагревательных элементов высокотемпературных печей (до 3000°C).
Карбид вольфрама WC обладает очень высокой твердостью (близкой к твердости алмаза), износоустойчивостью и тугоплавкостью. На основе этого вещества созданы самые производительные инструментальные твердые сплавы. В их состав входит 85—95% WC и 5-15% кобальта, придающего сплаву необходимую прочность. Некоторые сорта таких сплавов содержат кроме карбида вольфрама карбиды титана, тантала и ниобия. Все эти сплавы получают методами порошковой металлургии и применяют главным образом для изготовления рабочих частей режущих и буровых инструментов.
Соединения вольфрама очень сходны с соединениями молибдена. Из них наибольшее значение имеют вольфрамовая кислота h3WO4 и ее соли.
librolife.ru
Тема 24. Подгруппа хрома — Мегаобучалка
К элементам VIB-группы Периодической системы относятся хром, молибден и вольфрам. В силу стабильности конфигурации (Р у атомов первых двух элементов подгруппы наблюдается проскок одного электрона с оболочки ns на оболочку (n — \)d. У вольфрама валентной электронной конфигурации предшествует завершенная 4f14-оболочка. Поэтому на его свойствах сказывается влияние лантаноидной контракции. Ниже сопоставлены некоторые характеристики элементов и простых веществ VIB-группы:

Обращает на себя внимание тот факт, что первые потенциалы ионизации в отличиe от последующих (и их сумм) возрастают в ряду Сг — Mo — W. Увеличение 1-го потенциала ионизации обусловливает возрастание химической благородности простых веществ при переходе от хрома к вольфраму. Вторые потенциалы ионизации у хрома и молибдена различаются незначительно, в то время как I2 для вольфрама заметно меньше. Это обусловлено проскоком электрона у первых двух элементов, вследствие чего 1% у них характеризует энергию, необходимую для отрыва d-электрона с предвнешнего уровня. У вольфрама 2-й потенциал ионизации соответствует отрыву 6s-электрона. Подобная же закономерность наблюдается и в отношении четвертых потенциалов ионизации. Напротив, шестые потенциалы ионизации и сумма шести потенциалов более близки для молибдена и вольфрама, вследствие чего следует ожидать большого сходства этих элементов в высшей степени окисления.
Значения ОЭО этих элементов свидетельствуют о том, что они являются сравнительно малоактивными металлами. Поэтому для химии хрома и его аналогов не характерно образование преимущественно ионных соединений даже при взаимодействии с сильноэлектроотрицательными элементами. Напротив, следует ожидать большого разнообразия интерметаллических соединений. Ионные радиусы в высшей степени окисления у молибдена и вольфрама практически одинаковы и резко отличаются от радиуса иона Сг6+. Это хорошо коррелирует с отмеченной выше закономерностью изменения I6 и их суммы и объясняет подобие свойств Мо и W в характеристической степени окисления.
Природные соединения и получение металлов V I В-г р у п п ы. Самым распространенным минералом хрома является хромистый железняк (хромит) FeO-Сг2Оз. Вторая по значимости руда хрома — крокоит — представляет собой хромат свинца РЬСгО4 . Наиболее распространенный минерал молибдена — молибденит (молибденовый блеск) МоS2. Вольфрам представлен в природе главным образом в виде вольфраматов двухвалентных металлов. К ним относятся, например, вольфрамит — изоморфная смесь вольфраматов железа и марганца переменного состава FexMn1-xWO4, шеелит CaWO4, штольцит PbWO4 и т.д. Помимо того, встречается вольфрамовый блеск WS2 в смеси с молибденитом.
В чистом виде эти металлы получают с помощью алюмотермии для хрома и водородного восстановления для молибдена и вольфрама:

При водородном или металлотермическом восстановлении получаются либо порошкообразные, либо губчатые металлы. Для получения компактных металлов и их дополнительной очистки используют обычно вакуумную плавку с применением электронно-лучевого нагрева или плавку в электродуговых печах с расходуемым электродом из чернового металла в водоохлаждаемых медных тиглях.
Для нужд черной металлургии обычно нет необходимости получать очень чистый легирующий металл. Поэтому при карботермическом восстановлении совместно с железными рудами получают обычно феррометаллы (феррохром, ферромолибден, ферровольфрам).
Простые вещества. Физические и химические свойства. В компактном состоянии Сг, Мо и W представляют собой плотные серебристо-белые металлы. Все три металла обладают высокими температурами плавления и являются самыми тугоплавкими в своих d-рядах. Вольфрам вообще является самым тугоплавким из всех металлов. Для всех трех металлов характерно отсутствие полиморфизма. Вплоть до температуры плавления они обладают ОЦК-решеткой. В химическом отношении хром, молибден и вольфрам довольно инертны. При обычных условиях они устойчивы по отношению к воде и кислороду воздуха. Хром реагирует с разбавленными растворами НС1 и h3SO4, поскольку в этих условиях пассивирующая пленка поверхностного оксида (близка по составу к Сr2О3) постепенно разрушается. В ряду стандартных электродных потенциалов хром располагается между цинком и железом. У молибдена и вольфрама коррозионная устойчивость в кислых средах резко возрастает, поскольку состав их пассивирующих пленок близок к кислотообразующим оксидам соответствующих кислот (МоОз и W0з). Лучшими растворителями для Мо и W являются расплавы щелочей в присутствии окислителей и горячая смесь 
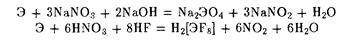
Хром при высоких температурах растворяет водород, а молибден и особенно вольфрам водород практически не поглощают.
Элементы подгруппы хрома при нагревании реагируют с галогенами, халькогенами, пниктогенами (кроме висмута), неметаллами IV A-группы, бором. Кроме того, они реагируют с большинством металлов с образованием твердых растворов или интерметаллических соединений.
Характеристические соединения. В соединениях с кислородом хром проявляет степени окисления +2, +3, +4, +6 и образует соответствующие оксиды СгО, Сг2Оз, СгО2 и СгОз- Для молибдена известны оксиды МоО2, Мо2O5 и МоОз- Для вольфрама известны всего лишь два оксида: W02 и WОз- Таким образом, в ряду Сг — Мо — W наблюдается, как и в предшествующих В- группах, повышение стабильности высших степеней окисления и уменьшение разнообразия соединений с кислородом.
Оксид хрома (+3) представляет собой порошок темно-зеленого цвета, нерастворимый в воде, кислотах и щелочах. Удобным лабораторным способом получения Сг2Оз является термическое разложение дихромата аммония:

Гидроксид хрома обладает амфотерными свойствами. Со структурной точки зрения, гидроксид хрома (+3), имеющий переменный состав Сг2Оз*xН2О, обладает пространственным строением многоядерного комплекса. Структурными единицами его являются октаэдры [Сг(ОН)6]3- и [Сг(Н2О)б]3+, связанные между собой oловыми ОН-мостиками. Относительное количество лигандов ОН- и Н2О может меняться в зависимости от условий получения гидроксида хрома. Равновесия между различными формами гидроксо- и аквакомплексов для Сг(+3) представлены схемой:
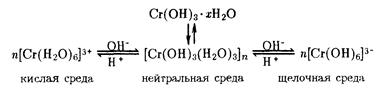
Как следует из этой схемы, для Сг(+3) характерным является координационное число 6. Оксид хрома (+3) и соответствующий гидроксид по свойствам сильно напоминают соединения алюминия AI2O3 и А1(ОН)з. В частности, при сплавлении Сг2Оз с оксидами или карбонатами щелочных металлов образуются мета-производные Me СгО2. Подобное же взаимодействие с производными щелочно-земельных металлов, магния, железа (+2) приводит к образованию хромовых шпинелей Me Сr2О4, относящихся к тому же классу соединений, что и собственно шпинель MgAl2O4. Свободная НСгО2 представляет собой синевато-серые кристаллы. Она теряет воду при 430°С с сильным саморазогреванием. В водных растворах щелочей метапроизводные (хромиты) не существуют вследствие образования гидроксокомплексов, например
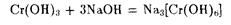
Из характеристических соединений хрома в низшей положительной степени окисления +2 известны черный оксид СгО и соответствующий гидроксид Сг(ОН)2 желтого цвета. Сг(ОН)2 обладает только основными свойствами. Осторожным обезвоживанием Сг(ОН)2 в восстановительной атмосфере можно получить оксид СгО, который при небольшом нагревании диспропорционирует на Cr2O3 + Cr.
В степени окисления +4 .Известны черный оксид СгО2, коричневато-фиолетовый Мо02 и коричневый WO2. Оксид СгО2 представляет собой фазу переменного состава с дефектами в подрешетке кислорода (твердый раствор вычитания СгО2-х). Кристаллизуется в решетке рутила ТiO2. Диоксиды хрома и его аналогов нерастворимы в воде, трудно растворимы в кислотах и щелочах. Отвечающие им гидроксиды неизвестны.
Наиболее типичной степенью окисления для молибдена и вольфрама и одной из важнейших для хрома является +6. МоОз и WO3 получаются непосредственным термическим окислением металлов газообразным кислородом. СгОз кристаллизуется в виде ярко-красных игл при действии на раствор дихромата калия концентрированной серной кислотой:

СгОз обладает цепочечной структурой из тетраэдров [СгО4], соединенных вершинами. МоОз и WO3 имеют координационные структуры, построенные из октаэдров [ЭО6], связанных между собой вершинами. Низкая температура плавления СгОз (187°С) свидетельствует о заметном ван-дер-ваальсовом вкладе между цепочками, а высокие температуры плавления МоОз и WO3 (735 и 1473°С) подтверждают их координационную структуру. С химической точки зрения, СгОз, МоОз и WO3 представляют собой типичные кислотообразующие оксиды соответствующих кислот: хромовой Н2СЮ4, молибденовой Н2МoО4 и вольфрамовой h3WO4- Этим кислотам отвечают многочисленные соли: хроматы, молибдаты и вольфраматы. Обычно соли хромовой кислоты окрашены в желтый цвет, свойственный иону CrO42- , соли молибденовой и вольфрамовой кислот бесцветны.
Одной из характерных особенностей элементов VIB-группы в высшей степени окисления является способность к образованию полисоединений. Для Сг свойственно образование лишь производных изополикислот, для Мо и W существуют и производные гетерополикислот. Если в разбавленных водных растворах для хрома характерно образование иона CrO42- , то по мере повышения концентрации раствора происходит образование полихромат-анионов СrnОзn+1 2- . Сами изополихромовые кислоты известны только в растворах. Однако их соли довольно многочисленны. Наибольшее значение имеют дихроматы; они в отличие от желтых хроматов имеют красно-оранжевую окраску и лучше растворимы в воде. Растворы дихроматов имеют кислую реакцию, что объясняется взаимодействием дихромат-иона с водой по схеме
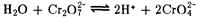
Отсюда следует, что в кислой среде равновесие смещено влево, а при разбавлении водой или в щелочной среде — вправо.
Все хроматы являются сильными окислителями. Так, на холоду они окисляют HI, h3S, h3SO3 и их соли, а при нагревании — НВг и даже НСl:

Образуются и пероксокислоты хрома h3Cr2O12 и HзСrО8. Все пероксохроматы неустойчивы, являются сильнейшими окислителями.
Для Мо(+6) и W(+6) еще более характерно образование изо- и гетерополи- соединений. Структурной единицей сложных анионов изо- и гетерополикислот молибдена и вольфрама является октаэдр [ЭОб]. Эти октаэдры могут соединяться между собой вершинами или ребрами, образуя сложные каркасы. По мере усложнения состава аниона связь с атомами водорода во внешней сфере комплекса становится более полярной вследствие перераспределения электронной плотности и сила поликислот возрастает. Однако в целом, как отмечено выше, в ряду Сг — Mo — W кислотный характер высших оксидов и гидроксидов быстро ослабевает.
В частности, Н2МoО4 и h3WO4 проявляют заметные признаки амфотерности, что выражается в их взаимодействии с сильными кислотами:
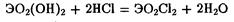
Эта реакция может быть проведена и с Н2СгO4, однако в этом случае равновесие сильно смещено влево. Соединения ЭО2Сl2 в водных растворах диссоциируют по схеме

Оксокатион ЭО2+ называют хромилом, молибденилом или вольфрамилом.
Действием пероксида водорода в щелочной среде на растворы молибдатов и вольфраматов можно получить пероксопроизводные общей формулы Ме2ЭОn (где n = 5 — 8). Со структурной точки зрения, они аналогичны соответствующим производным хрома и содержат от одной до четырех пероксогрупп —О—О—, замещающих атомы кислорода в анионах ЭО42- . Это твердые вещества, окрашенные в яркие тона от красного до желтого. При нагревании разлагаются со взрывом, а при комнатной температуре медленно отщепляют кислород, вследствие чего обладают сильными окислительными свойствами. В ряду Сг — Mo — W устойчивость пероксосоединений в высшей степени окисления заметно возрастает.
Соединения с другими неметаллами. Фтор, как наиболее энергичный окислитель, способен образовывать высшие галогениды ЭF6, из которых CrF6 — твердое вещество, MoF6— легкокипящая жидкость, a WF6 — газ, что свидетельствует об увеличении тенденции к образованию молекулярных структур. Наибольшее число фторидов образует хром, для которого реализуются все степени окисления от +2 до +6 (в том числе и нехарактерная +5, не наблюдаемая в ряду оксидов). Низшие фториды CrF2 и CrF3 солеобразны и тугоплавки. У молибдена и особенно у вольфрама число известных фторидов значительно меньше. Ни один из фторидов Мо и W не является солеобразным.
В ряду хлоридов хрома и его аналогов наиболее ярко видна стабилизация высших степеней окисления от хрома к вольфраму. Хлор способен окислить хром только до CrCl4, молибден — до MoCI5, а вольфрам — даже до высшего хлорида WCl6. Низшие хлориды хрома СгСl2 и СгСlз — типичные солеобразные соединения. СгСl2 — бесцветное кристаллическое вещество, гигроскопическое и хорошо растворимое в воде. Из раствора выделяется в виде кристаллогидрата СгСl2*4Н2О, который следует рассматривать как аквакомплекс [Сг(Н2О)4]Сl2. Хлорид хрома (+3) также образует кристаллогидрат СгСlз*6Н2О, представляющий собой аквакомплекс [Сг(Н2О)6]Сlз сине-фиолетового цвета.
В отличие от низших хлоридов хрома МоСl2 и WCl2 не являются солеобразными соединениями, а представляют собой так называемые кластеры, т.е. многоядерные комплексы с непосредственной связью между атомами комплексообразователя. Молекула МоСl2 представляет собой агрегат Mo6Cl12, причем восемь атомов хлора находятся во внутренней сфере комплексного многоядерного кластера [Мо6Сl8]4+ (рис. 153), а четыре атома Сl — во внешней сфере. Непосредственно связанные между собой атомы Мо образуют правильный октаэдр. На всех ребрах располагаются мостиковые атомы хлора, каждый из которых связан одновременно с тремя атомами Мо, причем образуются тетраэдры с атомом Сl в вершине и атомами металла в основании.
Таким образом, ковалентность хлора равна трем, а ковалентность молибдена — восьми (каждый атом Мо связан с четырьмя другими атомами металла и четырьмя атомами Сl). Аналогична структура и хлорида вольфрама (+2).
Большой интерес представляет сопоставление свойств и структуры таких комплексных ионов, как [Э2Сl9]3- . В противоположность парамагнитному [Сr2Сl9]3- аналогичные по составу ионы на основе молибдена и вольфрама диамагнитны и значительно более прочны. Причина этого различия заключается в разной структуре и разном характере связей рассматриваемых ионов. Строение парамагнитного комплекса [СггСЩ3" представлено ниже:

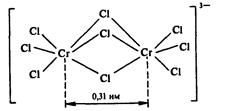
Неспаренные электроны у каждого иона Сг3+ (по три электрона) обеспечивают парамагнетизм комплексного иона в целом. Расстояние между атомами хрома в этом комплексе довольно велико и составляет 0,31 нм. Таким образом, комплекс [Cr2CI9]3- не является кластером. Аналогичные по составу комплексы [Mo2CI9]3- и [W2Cl9]3- отличаются от [Cr2CI9]3- значительно меньшим расстоянием между атомами металла, несмотря на то что размеры самих атомов больше. Так, расстояние W—W в таком комплексе равно всего лишь 0,24 нм. Это обусловлено тем, что более удаленные от ядра и более рыхлые валентные 4d- или 5d-орбитали соседних атомов металла, содержащие по одному электрону, перекрываются по обменному механизму, образуя тройную ковалентную связь. Именно поэтому эти комплексы диамагнитны. Таким образом, комплексы [Mo2CI9]3- и [W2Cl9]3- в отличие от [Cr2CI9]3- представляют собой кластеры с непосредственной тройной связью Ме=Ме:

Бром с металлами рассматриваемой группы образует соединения, в общем напоминающие аналогичные производные хлора. При этом, однако, в силу несколько меньшей окислительной активности брома высший бромид молибдена отвечает формуле МоВг4. Иод как наименее активный окислитель среди галогенов образует соединения с еще меньшими степенями окисления катионообразования СгIз и СгI2, обладающие солеобразным характером, и соединения ЭI2, ЭIз и ЭI4 для молибдена и вольфрама. Низшие бромиды и иодиды молибдена и вольфрама (ЭГ2), как и хлориды этих элементов, представляют собой кластеры и в этом отношении заметно отличаются от аналогичных производных хрома.
Все сульфиды металлов подгруппы хрома (CrS, Cr2S3, ЭS2 и ЭSз для Мо и W) достаточно термически устойчивы и обладают полупроводниковыми свойствами, что подчеркивает их неметаллическую природу. Все они представляют собой координационные кристаллы и обладают переменным составом, что особенно характерно для низших сульфидов. В этом отношении они заметно отличаются от галогенидов, которые нередко образуют или молекулярные структуры, или кластеры. Взаимодействие хрома, молибдена и вольфрама с селеном и теллуром протекает менее энергично, причем вольфрам с теллуром соединений не образует, а в остальных случаях в системах образуется небольшое число соединений, отвечающих лишь наиболее стабильным степеням окисления (СгХ, СГ2Х3, WSe2, WSe3, MoTe2, MoTe3).
Фосфиды, арсениды и стибидыхрома и его аналогов принадлежат к классу аномально построенных дальтонидов, содержащих "анион-анионные" и "катион-катионные" связи. Наиболее характерны для фосфидов соединения состава Э3Р, ЭР и ЭР2- Образование моно- и дифосфидов вообще весьма характерно для переходных металлов.
Для всех трех элементов существуют дисилициды ЭSi2, представляющие собой тугоплавкие соединения, обладающие полупроводниковыми свойствами. Дисилициды устойчивы к агрессивным средам при повышенных температурах. В системе Cr — Si установлено существование соединений CrSi, Cr2Si, Cr3Si, первое из которых является полупроводником, а два других — металлиды. Таким образом, в ряду силицидов хрома наблюдается та же закономерность, что была отмечена для фосфидов.
Соли кислородсодержащих кислот и комплексные соединения. Относительной стабильностью обладает CrSO4 в разбавленной серной кислоте в отсутствие кислорода. В твердом состоянии сульфат хрома (+2) изоморфен сульфату железа (+2) и они оба образуют кристаллогидраты ЭSO4*7h3O. Химия хрома (+2) в определенном смысле подобна химии железа (+2). Так, для Сг (+2) известно соединение К4[Сг(СN)6], аналогичное по составу желтой кровяной соли K4[Fe(CN)6], а также существует роданидный комплекс K4[Cr(CNS)6].
Оксид Сr2Оз при сплавлении с пиросульфатом калия дает сульфат Cr2(SO4)3, который образует с сульфатами щелочных металлов двойные соли типа квасцов. Тенденция к образованию квасцов у хрома выражена еще ярче, чем у алюминия, и эти двойные соли более устойчивы. Хром является лучшим комплексообразователем, чем алюминий. У хрома в отличие от алюминия существует внутренняя 3d- оболочка с частично свободными орбиталями, способными принять участие в донорно-акцепторном взаимодействии с лигандами. У алюминия Зd-оболочка также существует, но она является внешней и полностью вакантной. Таким образом, при координационном числе 6 для хрома характерна внутренняя d2sр3-гибридизация, а для алюминия — внешняя sp3d2-гибридизация с меньшей прочностью связей.
Все три металла подгруппы хрома образуют однотипные гексакарбонилы Ме(СО)б, в которых степень окисления металла формально равна нулю. Все эти карбонилы представляют собой бесцветные ромбические кристаллы, устойчивые на воздухе до 180—200°С. В карбонильных комплексах атомы металлов выступают в аномально низких степенях окисления и лиганды, подобные СО, способствуют стабилизации этого состояния. Такие лиганды помимо неподеленных эл. пар. металлов подгруппы марганца содержит всего два ns-электрона, а подстилающая электронная оболочка — стабильная, наполовину заполненная (n — 1)d. По этой причине элементы подгруппы марганца в первую очередь выступают как типичные переходные металлы. В то же время химия элементов подгруппы марганца в высшей степени окисления приобретает закономерную аналогию с химией второго типического элемента — хлора.
Хромирование — диффузионное насыщение поверхности стальных изделий хромом, либо процесс осаждения на поверхность детали слоя хрома из электролита под действием электрического тока.
Слой хрома может наноситься для декоративных целей, для обеспечения защиты от коррозии или для увеличения твердости поверхности.
Типичными являются следующие растворы для хромирования:
Шестивалентный хром, чей основной ингредиент — хромовый ангидрид.
Трехвалентный хром, чей основной ингредиент — Сульфат хрома или хлорид хрома. Ванны с трехвалентным хромом используются довольно редко из-за ограничений, накладываемых на цвет, яркость и толщину покрытия.
Вольфрамовые бронзы представляют собой особые солеобразные соединения с дефектной структурой. По мере уменьшения числа ионов Na увеличивается количество дефектов решетки. При малых концентрациях Na решетка бронзы из кубической переходит в тетрагональную
| Вольфрамовая синь | смесь W10O29(OH) и W3O8(OH) |
| Молибденовая синь | смесь Mo4O10(OH)2 и Mo2O4(OH)2 |
megaobuchalka.ru
Подгруппа хрома

Подгруппу хрома образуют металлы побочной подгруппы,
шестой группы – хром, молибден и вольфрам.
Наружный электронный слой атомов элементов подгруппы хрома содержит один или два электрона, что обусловливаетметаллический характер этих элементов и их отличие от элементов главной подгруппы.
Вместе с тем их максимальная степень окисленности равна+6, так как, помимо наружных электронов, в образовании связей может участвовать еще соответствующее число электронов из недостроенного предпоследнего слоя.
Для хрома и его аналогов наиболее типичны производныевысшей степени окисленности, во многом сходные с соответствующими соединениями серы.

Хром
Запишем электронно-графическуюформулу атома хрома :
24 Cr 1s22s22 p63s23 p64s13d 5 |
|
| 3d |
4s | В'=6 |
|
Степени окисления хрома в соединениях:
Cr+2, Cr+3, Cr+6.

Нахождение в природе
Содержание хрома в земной коре составляет 0,02 % по массеи он
встречается в виде минералахромистого железняка: FeO·Cr2O3.
Богатые месторождения имеются в
Казахстане и на Урале.
Хром обнаружен на звездах, солнце и в метеоритах.

Получение
При восстановлениихромистого железняка углем получают феррохром– сплав железа с хромом:
FeО Сr2O3 +Сt →Fe−Cr+СO2 ↑.
феррохром
Для получения чистого хрома сначала получаютСr2O3, а затем восстанавливают
алюминием:
FeО Сr2O3 t →FeО+Cr2O3.
Cr2O3 + Alt →Cr+ Al2O3.
Чистый металл также получаютэлектролизом водных растворов солей хрома.

Физические свойства
Хром – самый твердый и блестящий
металл, покрыт плотной оксидной пленкой,
защищающей его от дальнейшего окисления.
Для хрома:
температура плавления – | Тпл =18900 С; |
плотность – ρ = 7,19 г/ см3 | ; |
стандартный электродный потенциал-
ϕCr0 2+ = − 0.91B.

Химические свойства
1. Отношение к кислороду.
Если очистить оксидную пленку, то хром легко окисляется кислородом воздуха:
Cr +О2 →Cr2O3.
2. Отношение к воде.
Хром вытесняет водородиз воды:
Cr + Н2Оt →Cr2O3 + h3 ↑.

Химические свойства
3.С неметаллами хром образует хлориды, сульфиды и т.д.:
Cr +Cl2 →CrCl2 ,
Cr +St →Cr2 S3 и т.д.
4. Отношение к щелочам.
Сr + KOH+ h3Ot →KCrO2 + h3 ↑.

Химические свойства
5. Отношение к кислотам.
а)хром вытесняетводород из неокислительных кислот:
Cr + HСl→CrCl2 + h3 ↑,
Сr + h3 SO4 разб.→CrSO4 + h3 ↑.
б)концентрированные окислительные кислотыпри комнатной температуре
пассивируют хром, но при нагревании
хром растворяется, проявляя степень окисления+2:
+6 | + h3O | +CrSO4. |
Cr + h3 SO4 конц. t → S0 |

Таблица. Взаимодействие металлов с кислотами
металлов с кислотами
Ca Na Mg Al Mn Cr Zn Fe Co Ni Sn Pb H Sb Bi Cu Hg Ag Au
НNO3 конц
NO2
Н2SO4 конц
НNO3 разб

Химические свойства
|
|
| +4 |
|
+5 |
| |||
H NO3 конц.+Crt → N О2 | + h3O+Сr(NO3 )2 . | |||

Таблица. Взаимодействие металлов с кислотами
металлов с кислотами
Ca Na Mg Al Mn Cr Zn Fe Co Ni Sn Pb H Sb Bi Cu Hg Ag Au
|
| НNO3 | конц |
| |
|
| NO2 |
|
| |
|
| Н2SO4 конц |
| ||
Н2S |
| S |
| SO2 | |
|
| НNO3 | разб |
| |
Nh5+ | N2 |
|
| N O | NO |
|
|
|
| 2 |
|

Химические свойства
|
|
|
|
|
|
|
+5 |
| +Cr→ N0 | + H | O +Сr(NO) | . | |
| H NO | 3 разб | ||||
|
| 2 | 2 | 3 2 |
| |

Таблица. Взаимодействие металлов с кислотами
металлов с кислотами
Ca Na Mg Al Mn Cr Zn Fe Co Ni Sn Pb H Sb Bi Cu Hg Ag Au
|
| НNO3 | конц |
| |
|
| NO2 |
|
| |
|
| Н2SO4 конц |
| ||
Н2S |
| S |
| SO2 | |
|
| НNO3 | разб |
| |
Nh5+ | N2 |
|
| N O | NO |
|
|
|
| 2 |
|
|
|
|
|
|
|

Применение
Хром – важнейший компонент
легированных сталей и сплавов.
Для легирования стали применяют
феррохром Fe – Cr.
Такие стали обладают повышенной
твердостью, стойкостьюпротив коррозии, кислотоупорностью и жаропрочностью.
Хром применяют для нанесения защитных покрытий – хромирования.

Соединения хрома
+2+3
Cr Сr
CrO Cr2O3
Cr(OH)2 Cr(OH)3 HCrO2
CrSO4 | Cr2 (SO4 )3 КCrO2 |
| хромит |
+6
Cr
СrO3
h3CrO4
К2CrO4
хромат
HCrO2 → хромистая; | h3CrO4 → хромовая. |

Соединения хрома: Cr2+
Сr + HCl→CrCl2 + h3O.
СrCl2 + NaOH→Cr(OH)2 ↓ +NaCl.
желтый
Соединения Сr2+ неустойчивы и сразу окисляются в соединенияхрома (III):
Cr(OH)2 +О2 + Н2О→ Cr(OH)3 .
желтый синевато−серый
Cr2O3 – тугоплавкоевещество зеленого
цвета (зеленый крон), применяетсядля приготовления клеевой и масляной красок.

Cоединения хрома: Cr3+
Cr2O3 – амфотерныйоксид.
Cr2O3 + HCl→CrCl3 + h3O.
Cr2O3 + NaOHt →NaCrO2 + h3O.
хромит
Cr2O3 – тугоплавкоевещество зеленого
цвета (зеленый крон), входит в состав
полирующих паст, применяетсядля приготовления клеевой и масляной красоки
для окраски стекла и фарфорав зеленый
цвет.

Соединения хрома: Cr2+
Сr + HCl→CrCl2 + h3O.
СrCl2 + NaOH→Cr(OH)2 ↓ +NaCl.
желтый
Соединения Сr2+ неустойчивы и сразу окисляются в соединенияхрома (III):
Cr(OH)2 +О2 + Н2О→ Cr(OH)3 .
желтый синевато−серый
Cr2O3 – тугоплавкоевещество зеленого
цвета (зеленый крон), применяетсядля приготовления клеевой и масляной красок.

Cоединения хрома: Cr3+
Cr(OН)3 – амфотерный гидроксид.
CrCl3 + NaOH→Cr(OH)3 ↓ +NaCl.
Cr(OН)3 + h3 SO4 →Cr2 (SO4 )3 + h3O.
При растворении в щелочах образуются
изумруднозелёные растворы хромитов
Cr(OН)3 + NaOH→ Na3[Cr(OH)6 ] .
гексагидроксохромит натрия
Cr(OН)3 +3OH− =[Cr(OH)6 ]3−.

Cоединения хрома: Cr3+
Хромиты получают сплавлениемCr2O3 с
оксидами других металлов.
Это соли метахромистой кислотыHCrO2. К ним относится и природныйхромистый железняк Fe(CrO2)2 .
Из солей хрома (III) самой распространенной является двойная соль хрома и калия –
хромо-калиевыеквасцы:
КCr(SO4 )2 12h3O,
сине−фиолетовые кристаллы.

Свойства соединений Cr3+
Хромо-калиевыеквасцыприменяют при дублении кож и в качестве протравы при крашении тканей.
Соль в растворе сильно гидролизована.
|
|
| слабый | сильная |
Cr2 (SO4 )3 (Cr(OH)3 и h3 SO4 ). | ||||
Cr (SO) | 3 | = 2Cr3+ | +3SO2− | |
2 | 4 |
| 4 | |
H +OH−
Cr3+ + HOH=CrOh3+ + H+, pН< 7, Iступень
Cr2 (SO4 )3 +2h3O= 2CrOHSO4 + h3 SO4 .

Свойства соединений Cr3+
После увеличения температуры иразведения гидролиз идет по II-ой ступени:
CrOH 2+ + НОН=Cr(OH)+2 + H+, pН< 7,
CrOHSO4 + h3O= (Cr(OH)2 )2 SO4 + h3 SO4 .
После увеличения температуры иразведения гидролиз идет по III-ей ступени:
Cr(OH)+2 + НОН=Cr(OH)3 ↓ +H+, pН< 7,
(Cr(OH)2 )2 SO4 +2h3O= 2Cr(OH)3 ↓ +h3 SO4 .

Соединения хрома: Сr6+
Если к насыщенному раствору дихромата калияК2Сr2O7 прилить концентрированную серную кислоту, то выпадаеттемно-красный кристаллический осадок СrO3.
+h3 SO4 =CrО3 ↓ +K2 SO4 + h3O.
CrO3 + h3O→ h3Cr2O7 ,
избыток двухромовая
CrO3 + h3O→ h3CrO4 .
недостаток хромовая
h3Cr2O7 + h3O→ h3CrO4 .
Кислоты существуют только в растворе.

Соединения хрома: Сr6+
В ОВРСrO3 – сильный окислитель:
0
CrО3 250 С→Сr2O3 +O2 ↑.
Соли кислот – это хроматы идихроматы:
KCrO2 | + Br2 + KOH→ К2CrO4 | + KBr+ h3O, | ||||
изумрудно−зеленый | ярко−желтый |
|
| |||
Cr O + КОН+ KClOt →K | 2 | CrО + KCl+ H | O. | |||
2 | 3 | 3 | 4 | 2 |
| |
В зависимости от среды раствора хроматы переходят в дихроматы и наоборот:
2K2CrO4 + h3 SO4 = K2Cr2О7 + K2 SO4 + h3O,
2CrO42− +2H+ =Cr2О72− + h3O.

Соединения хрома: Сr6+
K2Cr2O7 +2КОН= 2K2CrО4 + h3O,
2Cr2O72− +2ОН− = 2CrО42− + h3O.
Хроматы устойчивы вщелочной среде, а
дихроматы – в кислой.
Окислительные свойства соединений
хрома (VI) наиболее сильно выражены в
кислой среде.
K2Cr2О7 + h3 S+ h3 SO4 → S↓ +Cr2 (SO4 )3 + K2 SO4 + h3O,
K2Cr2О7 + HСl→Cl2 ↑ +CrCl3 + KCl+ h3O.

Соединения хрома: Сr6+
Наиболее важными из дихроматов являются
хромпики: K2Cr2O7 и Na2Cr2О7 2h3O,
образующие оранжево-красныекристаллы.
Их используют в качестве окислителей припроизводстве органических соединений, в
кожевенной, спичечной итекстильной
промышленности.
PbCrO4 используют для приготовлениякрасок.
Для мытья химической посуды применяют
«хромовую смесь»: р− р K2Cr2О7 + h3 SO4 конц.
Все соли хромовых кислот ядовиты.

Молибден
Главным природным соединением молибдена является молибденит, илимолибденовый блеск,
MoS2 – минерал, очень похожий по внешнему виду на графит и долгое время считавшийся таковым.
В 1778 году Шееле показал, что при обработке молибденового блеска азотной кислотой получается белый остаток, обладающий свойствами кислоты.
Шееле назвал его молибденовой кислотойи
сделал заключение, что сам минерал представляет собой сульфид нового элемента.
Пять лет спустя этот элемент был получен в свободном состоянии путем прокаливания молибденовой кислоты сдревесным углем.

Молибден
Общее содержание молибдена в земной коре составляет 0,001 % (масс).
Для получения металлического молибдена из молибденового блеска последний переводят обжигом в МоО3, из которого металл восстанавливают водородом.
При этом молибден получается в виде порошка.
Компактный молибден получают главным образом методом порошковой металлургии.
Этот способ состоит из прессования порошка в заготовку и спекания заготовки.

Молибден
При прессовании порошка из него получают заготовки
– тела определенной формы, обычно бруски
(штабики).
Штабики молибдена получают в стальных прессформах при давлении до 300 МПа.
Спекание штабиков в атмосфере водорода проводят в две стадии.
Первая из них – предварительное спекание проводится при1100 –1200°Си имеет целью повысить прочность и электропроводность штабиков.
Вторая стадия – высокотемпературное спекание осуществляется пропусканием электрического тока, постепенно нагревающего штабики до2200 –2400°С.

Молибден
При этом получается компактный металл.
Спеченные штабики поступают на механическую обработку: ковку,протяжку.
Для получения крупных заготовок молибдена применяют дуговую плавку, позволяющую получать слитки массой до 2000 кг.
Плавку в дуговых печах ведут в вакууме.
Между катодом (пакет спеченных штабиков молибдена) ианодом (охлаждаемый медный тигель) зажигают дугу.
Металл катода плавится и собирается в тигле.
Вследствие высокой теплопроводности меди и быстрого отвода теплоты молибден затвердевает.

Молибден
Для получения особо чистого молибдена и других тугоплавких металлов применяется плавка вэлектронном пучке (электронно-лучеваяплавка).
Нагревание металла электронным пучком основано на превращении в теплоту большей, части
кинетической энергии электронов при их столкновении с поверхностью металла.
Плавку ведут в высоком вакууме, что обеспечиваетудаление примесей, испаряющихся при температуре плавки (О, N, Р, As, Fe, Си, Ni и
др.).
После электронно-лучевойплавки чистота молибдена повышается до99,9 %.

Молибден
Молибден –серебристо-белыйметалл плотностью10,2 г/см3, плавящийся при2620°С.
При комнатной температуре он не изменяется на воздухе, но при накаливании окисляется вбелый триоксидМоО3.
Соляная и разбавленная сернаякислоты при комнатной температурене действуют на молибден.
Он растворяется в азотной кислоте или горячей концентрированной серной кислоте.

Молибден
Около 80% всего добываемого молибдена расходуется на производство специальных сортовстали.
Он входит в состав многих нержавеющих сталей, его введение способствует увеличению их
жаропрочности.
Из сплава молибдена с танталом изготовляют лабораторную посуду, применяемую в химических лабораториях вместо платиновой.
Из чистого молибденаизготовляют детали электронных ламп и ламп накаливания: аноды, сетки,
катоды, вводы тока, держатели нитей накала.
Молибден проявляет положительные степени окисленности: шесть,пять,четыре,три идва.

Молибден
Наиболее стойкими являются соединения молибдена
(VI).
Важнейшие из них – соли молибденовой кислоты
Н2МоО4 (молибдаты), часто имеющие сложный состав.
Молибдат аммония (Nh5)6Mo7О24·4h3О
применяется в анализе для открытия и количественного определения фосфорной кислоты, с которой он образует характерныйжелтый осадок состава(NН4)3РO4·12МоO3·6Н2O.
Последний представляет собою аммонийную соль комплексной фосфорномолибденовой кислоты, относящейся к классугетерополикислот.

Вольфрам
По распространенности в земной коре 0,007 % (масс.) вольфрам уступает хрому, но превосходит молибден.
Природные соединения вольфрама представляют собой вольфраматы – соливольфрамовой кислоты
h3WO4.
Так, важнейшая вольфрамовая руда – вольфрамит – состоит из вольфраматов железа и марганца.
Часто встречается также минерал шеелит CaWO4.
Для выделения вольфрама из вольфрамита последний сплавляют в присутствии воздуха с содой.

Вольфрам
Вольфрам переходит ввольфрамат натрияNa2WO4, который извлекают из полученного сплава водой, а железо и марганец превращаются в нерастворимые в воде соединенияFe2O3 иМn3O4.
Из водного раствора выделяют свободную вольфрамовую кислоту в виде аморфного желтого осадка:
Na2 WO4 +2HCl= h3 WO4 ↓ +2NaCl.
При прокаливании вольфрамовая кислота переходит в триоксид вольфрама WO3.

Вольфрам
Восстанавливая его водородом или углеродом (для чего используют чистые сорта сажи), получают порошок металлического вольфрама, подвергаемый в дальнейшем для получениякомпактного металла.
Вольфрам –тяжелый белый металл плотностью19,3 г/см3.
Его температура плавления (около3400°С) выше, чем температура плавления всех других металлов.
Вольфрам можно сваривать ивытягивать в тонкие нити.
На воздухе вольфрам окисляется только при температуре красного каления.

Вольфрам
Он очень стоек по отношению ккислотам, даже к царской водке, но растворяется в смеси азотной кислоты и фтороводорода.
Большая часть добываемого вольфрама расходуется в металлургии для приготовления специальных сталей и
сплавов.
Быстрорежущая инструментальная сталь содержит до20 % вольфрама и обладает способностью
самозакаливаться.
Такая сталь не теряет своей твердости даже при нагревании докрасна.
Поэтому применение резцов, сделанных из вольфрамовой стали, позволяет значительно увеличить скорость резания металлов.

Вольфрам
Сталь, содержащая от3 до6 % вольфрама и до2 % хрома, применяется для изготовленияпил,фрез,штампов.
Как самый тугоплавкий металл, вольфрам входит в состав ряда жаропрочных сплавов.
В частности, его сплавы с кобальтом и хромом –
стеллиты обладают высокимитвердостью,износоустойчивостью,жаростойкостью.
Сплавы вольфрама с медью и с серебром сочетают в себе высокие электро- и теплопроводность и износоустойчивость.
Они применяются для изготовления рабочих частей рубильников, выключателей, электродов для точечной сварки.

Вольфрам
Чистый вольфрам в виде проволоки, ленты и различных деталей применяют в производстве
электрических ламп, в радиоэлектронике, в рентгенотехнике.
Вольфрам – лучший материал для нитейламп накаливания:
высокая рабочая температура (2200 –2500°С) обеспечиваетбольшую светоотдачу,
очень малое испарение – длительный срок службы нитей из вольфрама.
Вольфрамовую проволоку и прутки применяют также в качестве нагревательных элементов
высокотемпературных печей (до 3000°С).

Вольфрам
Карбид вольфрама WC обладает очень высокойтвердостью (близкой к твердости алмаза), износоустойчивостью и тугоплавкостью.
На основе этого вещества созданы самые производительные инструментальные твердые сплавы.
В их состав входит 85 –95 %WC и5 –15 % кобальта, придающего сплаву необходимую прочность.
Некоторые сорта таких сплавов содержат, кроме карбида вольфрама, карбиды титана, тантала и ниобия.
Все эти сплавы получают методами порошковой металлургии и применяют для изготовления рабочих частейрежущих и буровых инструментов.
Из них наибольшее значение имеют вольфрамовая кислота h3WO4 и ее соли.
studfiles.net
Подгруппа хрома - это... Что такое Подгруппа хрома?
| ||||||
| ||||||
| ||||||
Подгру́ппа хро́ма — химические элементы 6-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы побочной подгруппы VI группы)[1].
В группу входят хром Сr, молибден Mo и вольфрам W[2]. На внешнем энергетическом уровне у атомов хрома и молибдена находится один электрон, у вольфрама — два, поэтому характерным признаком данных элементов является металлический блеск, что и отличает эту побочную подгруппу от главной. Степень окисления в соединениях всех элементов подгруппы хрома равна +6, а также +5, +4, +3 и +2. По возрастанию порядкового номера элементов возрастает и температура плавления. Например, вольфрам — самый тугоплавкий метал, его температура плавления составляет 3390 °C. Элементы подгруппы достаточно устойчивы к внешним факторам (воздух, вода). По физическим и химическим свойствам молибден и вольфрам сходны, но отличаются от хрома[3].Применение
Вольфрам, как самый тугоплавкий из всех элементов, широко применяется в металлургии[4]. Молибден широко применяется в металлургии. Наиболее часто хром находит свое применение при производстве легированных сталей[5].
Свойства
Физические свойства
хром – серовато-белый металл с характерным металлическим блеском. Природный хром состоит из смеси 5 изотопов: 50, 52, 53, 54, 56. Это самый твердый из всех известных металлов, его плотность 7,2 г/см3. Температура плавления – 1855 °C, температура кипения – 2642 °C. При обычной температуре хром устойчив к воздействию воды и воздуха.
Химические свойства
Химические свойства: электронная конфигурация: 1s22s22p63s23p63d54s1. В образовании химических связей хрома участвуют не только электроны внешнего 4 уровня, но и электроны предпоследнего уровня – 3d-подуровня. При высокой температуре хром горит в кислороде: 4Cr + 3О2 = 2Cr2О3. Раскаленный хром реагирует с парами воды, вытесняя из нее кислород: 2Cr + 3Н2О = Cr2О3 + 3Н2?. При нагревании реагирует с галогеноводородами, S, N2, P4, C, Si, B:
С галогенами реагирует не одинаково: а) со фтором взаимодействует даже на холоде: Cr + 3F2 = CrF6; б) с хлором реагирует при нагревании: 2Cr + 3Cl2 = 2CrCl3. Разбавленная соляная и серная кислоты растворяют хром с выделением водорода, а в холодной азотной он пассивируется. Хром образует три оксида: CrО, Cr2О3 и CrО3. Оксид хрома II (CrО) – основный оксид – черный порошок. Сильный восстановитель. CrО растворяется в разбавленной соляной кислоте: CrО + 2НСl = CrСl2 + Н2О. При нагревании на воздухе выше 100 °C CrО превращается в Cr2О3: 4CrО + О2 = 2Cr2О3. Оксид хрома III (Cr2О3) – тугоплавкий порошок зеленого цвета (температура плавления – 2265 °C). Твердость кристаллов близка к корунду, поэтому его вводят в состав полирующих средств. Получают из хромистого железняка (FeCr2O4). При окислительно-щелочном сплавлении последнего с содой образуются хромат натрия NaCrO4: 2Fe(CrO2)2 + 4Na2CO3 + 1/2O2 = 4Na2CrO4 + Fe2O3 + 4CO2. Затем Na2CrO4 переводят в Na2Cr2O7 – дихромат: Na2CrO4 + Н2SO4 = Na2Cr2O7 + Н2О + Na2SO4. Далее дихромат восстанавливают углем и получают Cr2О3: Na2Cr2O7 + 2С = Na2CO3 + Cr2О3 + СО?. В лаборатории Cr2О3 получают термическим разложением дихромата аммония: (Nh5)2Cr2O7?Cr2О3 + N2 + 4Н2О. Cr2О3 – амфотерный оксид: реагирует с основаниями и кислотами при сплавлении его со щелочами образует хромиты: Cr2О3 + NaОН = 2NaCrO2 + Н2О. Оксид хрома VI (CrО3) – темно-красные кристаллы, хорошо растворимые в воде. CrО3 – кислотный оксид, с избытком воды образует хромовую кислоту: CrO3 + h3O?h3CrO4. CrO3 – ангидрид хромовой кислоты. При большой концентрации CrO3 образуются дихромовая кислота: 2CrO3 + h3O?h3CrO7. CrO3 при нагревании до 250 °C разлагается: 4CrO3?2Cr2О3 + 3О2?. Получение: взаимодействием дихромата калия с концентрированной h3S04: К2CrO7 + Н2SO4 = CrO3? + К2SO4 + h3O. CrO3 – сильный окислитель – окисляет йод, серу, уголь, фосфор, превращаясь при этом в Cr2О3. Гидроксид хрома II Сг(ОН)2 желтого цвета, в воде не растворим, обладает основными свойствами, является восстановителем, получается действием щелочи на хлорид хрома CrСl2, получаемого при взаимодействии Cr c НСl:
Соединения Cr II неустойчивы и легко окисляются кислородом воздуха:
Гидроксид хрома III (Cr(OH)3)n – это сложный полимер зеленого цвета, не растворимый в воде, обладает амфотерными свойствами – растворяется в кислотах и в щелочах; реагирует с кислотами с образованием солей хрома (III):
со щелочами – с образованием сине-фиолетовых растворов – гидроксохромитов:
При сплавлении Cr(ОН)3 со щелочами получают хромиты, а с избытком – метахромиты:
Примечания
dic.academic.ru
Подгруппа хрома Википедия
| ||||||
| ||||||
| ||||||
Подгру́ппа хро́ма — химические элементы 6-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы побочной подгруппы VI группы)[1]. В группу входят хром Сr, молибден Mo и вольфрам W[2]. На внешнем энергетическом уровне у атомов хрома и молибдена находится один электрон, у вольфрама — два, поэтому характерным признаком данных элементов является металлический блеск, что и отличает эту побочную подгруппу от главной. Степень окисления в соединениях всех элементов подгруппы хрома равна +6, а также +5, +4, +3 и +2. По возрастанию порядкового номера элементов возрастает и температура плавления. Например, вольфрам — самый тугоплавкий метал, его температура плавления составляет 3390 °C. Элементы подгруппы достаточно устойчивы к внешним факторам (воздух, вода). По физическим и химическим свойствам молибден и вольфрам сходны, но отличаются от хрома[3].
Применение[ | код]
Вольфрам, как самый тугоплавкий из всех элементов, широко применяется в металлургии[4]. Молибден широко применяется в металлургии. Наиболее часто хром находит своё применение при производстве легированных сталей[5].
Свойства[ | код]
Физические свойства[ | код]
ru-wiki.ru
Подгруппа хрома Википедия
| ||||||
| ||||||
| ||||||
Подгру́ппа хро́ма — химические элементы 6-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы побочной подгруппы VI группы)[1]. В группу входят хром Сr, молибден Mo и вольфрам W[2]. На внешнем энергетическом уровне у атомов хрома и молибдена находится один электрон, у вольфрама — два, поэтому характерным признаком данных элементов является металлический блеск, что и отличает эту побочную подгруппу от главной. Степень окисления в соединениях всех элементов подгруппы хрома равна +6, а также +5, +4, +3 и +2. По возрастанию порядкового номера элементов возрастает и температура плавления. Например, вольфрам — самый тугоплавкий метал, его температура плавления составляет 3390 °C. Элементы подгруппы достаточно устойчивы к внешним факторам (воздух, вода). По физическим и химическим свойствам молибден и вольфрам сходны, но отличаются от хрома[3].
Применение
Вольфрам, как самый тугоплавкий из всех элементов, широко применяется в металлургии[4]. Молибден широко применяется в металлургии. Наиболее часто хром находит своё применение при производстве легированных сталей[5].
Свойства
Физические свойства
Химические свойства
Примечания
wikiredia.ru