2. Основные классы электролитов. Диссоциация гидроксид хрома 3
Диссоциация - гидроксид - Большая Энциклопедия Нефти и Газа, статья, страница 1
Диссоциация - гидроксид
Cтраница 1
Диссоциация гидроксида В ( ОН) 3 в растворе идет по кислотному типу. Однако борная кислота очень слаба и поэтому из растворов своих солей легко выделяется большинством других кислот. Последняя является кислотой значительно более сильной, чем ортоборная. [1]
Диссоциация гидроксидов алюминия и хрома ( III) рассматривается позже - при изучении свойств этих металлов. [2]
Характер диссоциации гидроксидов ЗОН зависит от сравнительной степени полярности связей: Э - О и О - Н, которая определяется в основном радиусом и зарядом иона элемента, образующего гидроксид. [3]
Константа диссоциации гидроксида аммония при 18 и 25 С равна соответственно 17 2 - 10 - 6 и 18ЫО-6. [4]
Константа диссоциации гидроксида аммония при 25 С равна 1 8 - 10-в. Константа диссоциации гидроксида аммония, в котором все атомы водорода заменены дейтерием, ND OD составляет 1ЫО-5. [5]
Кислота подавляет диссоциацию гидроксида по кислотному варианту и связывает ионы ОН - в практически недиссоциированные молекулы воды. [6]
Кислоты подавляют диссоциацию гидроксидов по кислотному варианту и связывают ионы ОН в практически недиссоциированные молекулы воды. [7]
Как меняется характер диссоциации гидроксидов марганца в зависимости от степени окисления металла. [8]
Как влияет на характер диссоциации гидроксида величина заряда и радиус иона. [9]
Используя данные о константе диссоциации гидроксида аммония, приведенные в задаче 5.7, определите рН 1 5 М раствора гидроксида аммония. [10]
Рассмотрим, от чего зависит диссоциация гидроксида по основному ( с отщеплением гидроксид-иона) или по кислотному ( с отщеплением иона водорода) типу. [11]
На рис. 47 дана схема диссоциации гидроксидов. Пунктирной линией показаны места разрыва связей при электролитической диссоциации. С уменьшением радиуса и увеличением заряда центрального атома связь его с ионом кислорода увеличивается и в то же время ослабляется связь с ионами водорода. У гидроксида натрия заряд центрального иона Na наименьший, а радиус наибольший, поэтому связь его с кислородом менее прочна, чем кислорода с водородом. При диссоциации отщепляются только гидроксильные ионы. [13]
Как и почему изменяется степень диссоциации гидроксидов элементов главной подгруппы второй группы периодической системы. [14]
Составить вторую таблицу, относящуюся к диссоциации гидроксидов магния, никеля и цинка, когда ионы элементов имеют одинаковые заряды и близкие радиусы. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Cr(OH)3 + HCl = ? уравнение реакции
В результате взаимодействия гидроксида хрома (III) с соляной кислотой (Cr(OH)3 + HCl = ?) происходит образование средней соли хлорида хрома (III) и воды (обмен). Молекулярное уравнение реакции имеет вид:
![Rendered by QuickLaTeX.com \[ Cr(OH)_3 + 3HCl \rightarrow CrCl_3 + 3H_2O.\]](/800/600/http/ru.solverbook.com/wp-content/ql-cache/quicklatex.com-95dab6ac0470feedd4d2166b797a5a4a_l3.png)
Запишем ионные уравнения, учитывая, что гидроксид хрома (III) и вода на ионы не распадаются, т.е. не диссоциируют.
![Rendered by QuickLaTeX.com \[ Cr(OH)_3 + 3H^{+} + 3Cl^{-} \rightarrow Cr^{3+} + 3Cl^{-} + 3H_2O;\]](/800/600/http/ru.solverbook.com/wp-content/ql-cache/quicklatex.com-83815637193007a3bdaa6a512d26cb89_l3.png)
![Rendered by QuickLaTeX.com \[ Cr(OH)_3 + 3H^{+} \rightarrow Cr^{3+} + 3H_2O.\]](/800/600/http/ru.solverbook.com/wp-content/ql-cache/quicklatex.com-49fe3fdf4213f0a588abae0c6ed1da35_l3.png)
Первое уравнение называют полным ионным, а второе – сокращенным ионным.Хлорид хрома (III) представляет собой тугоплавкие кристаллы фиолетово-красного цвета, разлагающиеся при прокаливании и сублимирующиеся при нагревании в потоке хлора. Хорошо растворяется в холодной воде (но чрезвычайно медленно, растворение ускоряется в присутствии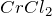 ), гидролизуется по катиону. Образует кристаллогидраты состава
), гидролизуется по катиону. Образует кристаллогидраты состава 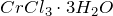 и
и 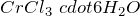 .Хлорид хрома (III) реагирует со щелочами, гидратом аммиака. Слабый окислитель, в растворе восстанавливается атомным водородом, при высокой температуре — водородом, кальцием, хромом. Слабый восстановитель, в растворе окисляется хлорноватой кислотой, перманганатом калия, галогенами, при высокой температуре — фтором. Вступает в реакции обмена и комплексообразования.Хлорид хрома (III) в промышленных масштабах получают путем хлорирования оксида хрома (III) в присутствии углерода при температуре
.Хлорид хрома (III) реагирует со щелочами, гидратом аммиака. Слабый окислитель, в растворе восстанавливается атомным водородом, при высокой температуре — водородом, кальцием, хромом. Слабый восстановитель, в растворе окисляется хлорноватой кислотой, перманганатом калия, галогенами, при высокой температуре — фтором. Вступает в реакции обмена и комплексообразования.Хлорид хрома (III) в промышленных масштабах получают путем хлорирования оксида хрома (III) в присутствии углерода при температуре 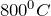 :
:
![Rendered by QuickLaTeX.com \[ Cr_2O_3 + 3C + 3Cl_2 \rightarrow 2CrCl_3 + 3CO_gas.\]](/800/600/http/ru.solverbook.com/wp-content/ql-cache/quicklatex.com-a65f1d2eb9658761762bd863ebf197fd_l3.png)
ru.solverbook.com
2. Основные классы электролитов.
По химическому составу ионов, образующихся при диссоциации, электролиты делятся на четыре основных класса: кислоты, основания, амфолиты и соли.
По Аррениусу, кислотами называются электролиты, при первичной диссоциации которых образуются ионы Н+. Например: HCl = H+ +Cl-; h3SO4 = 2H+ + SO42-. По сравнению с нейтральными растворами растворы кислот содержат избыточное количество ионов H+. Поэтому значения рН растворов кислот находятся в области рН7.
Имеется 2 группы кислот: бескислородные и кислородсодержащие (оксокислоты). Среди бескислородных кислот сильными являются три: HCl, HBr, HI; остальные бескислородные кислоты - слабые. Для определения силы оксокислот следует руководствоваться правилом: если степень окисления кислотообразующего элемента равна +6 и выше, такая кислота – сильная (исключение HNO3). Например, h3SO4 - сильная кислота, поскольку степень окисления серы в ней равна +6, а h3SO3 - слабая кислота т.к. степень окисления серы здесь равна +4.
Основаниями являются электролиты, при первичной диссоциации которых образуются гидроксид-ионы ОН-. Например: NaOH = Na+ + OH-; Cu(OH)2Cu2+ + 2OH-. Значения рН растворов оснований находятся в области рН7.
Сильными основаниями являются гидроксиды щелочных и щелочноземельных металлов. Гидроксиды этих металлов хорошо растворимы в воде и поэтому получили название щелочей.
Среди гидроксидов металлов имеются соединения, способные к диссоциации как по кислотному, так и по основному типу. Такие гидроксиды называются амфотерными (амфолитами). Например, Be(OH)2, Zn(OH)2, Al(OH)3, Cr(OH)3.
Соли – электролиты, при первичной диссоциации которых не образуются ни ионы Н+, ни ионы ОН-. Например: Cr2(SO4)3=2Cr3++3SO42- - диссоциация средней соли; Ca(HCO3)2=Ca2++2HCO3- - диссоциация кислой соли; AlOH(NO3)2=AlOh3++2NO3-- диссоциация основной соли.
Особую группу электролитов составляют комплексные кислоты, основания и соли. Эти электролиты, как правило, диссоциируют полностью на ионы внешней и внутренней координационной сферы, т.е. являются сильными электролитами. Например, процесс первичной диссоциации комплексной соли [Cr(h3O)6]Cl3 выражается уравнением: [Cr(h3O)6]Cl3 = [Cr(h3O)6]3+ + 3Cl-
3. Смещение ионных равновесий.
Равновесия в растворах слабых электролитов, как и любые химические равновесия подчиняется принципу Ле Шателье, а именно: при уменьшении концентрации ионов в растворе ( например, путем их связывания в слабый электролит ) ионное равновесие смещается вправо, т.е. степень диссоциации слабого электролита увеличивается; при увеличении концентрации ионов ( например, путем добавления к раствору слабого электролита сильного электролита, содержащего одноименные ионы ) ионное равновесие смещается влево, т.е. степень диссоциации слабого электролита уменьшается.
Пример 3.1. Смещение ионного равновесия в 0,1М растворе уксусной кислоты при добавлении кристаллического ацетата натрия.
Уксусная кислота – слабый электролит, диссоциирующий согласно уравнению: СН3СООН СН3СОО- + Н+. Ацетат натрия – хорошо растворимая соль, диссоциирующая в растворе полностью согласно уравнению: СН3СООNa = СН3СОО- + Na+. Поэтому при введении в раствор уксусной кислоты сильного электролита – ацетата натрия – происходит резкое увеличение концентрации ацетат-ионов, что согласно принципу Ле Шателье должно вызвать смещение ионного равновесия влево – в сторону образования дополнительного количества недиссоциированной уксусной кислоты. Подтвердим это рассчётом.
В 0,1М растворе СН3СООН концентрация ионов Н+ равна 1,310-3, а рН = 2,9 (см. примеры 1.2, 1.3). После добавления к раствору уксусной кислоты ацетата натрия вследствие смещения ионного равновесия влево концентрация недиссоциированной кислоты возрастёт, но это возрастание незначительно, т.к. согласно примеру 1.2. концентрация связываемых ионов Н+ не может превышать величину 1,310-3. Так как изменением объёма раствора в результате добавления кристаллической соли можно пренебречь принимаем, что [СН3СООН] = Ск Сик, где Сик = 0,1 моль/л – исходная концентрация взятой кислоты, а Ск – концентрация уксусной кислоты в смеси с ацетатом натрия.
Дальнейший рассчёт произведём для 0,1М раствора СН3СООН, в который добавлен кристаллический СН3СООNa в количестве, соответствующим его концентрации 1моль/л (82г соли, добавленной к 1л кислоты). Согласно выражению (1.1) концентрация ионов Н+ в смеси СН3СООН и СН3СООNa равна: Н+ = Ксн3соон [СН3СООН/СН3СОО-. Неизвестное значение концентрации ацетат-ионов в смеси кислоты и соли определяем, исходя из того, что количество ионов, образуемых сильным электролитом неизмеримо больше, по сравнению с количеством ионов, образуемых слабым электролитом. В связи с этим можно считать, что концентрация ацетат-ионов в смеси практически определяется принятой концентрацией добавленной соли Сс. В нашем случае СН3СОО- = Сс 1моль/л.
Подставляя численные значения концентраций и константы диссоциации в ваышезаписанное выражение для определения концентрации ионов Н+, получаем: Н+ = Ксн3соон [СН3СООН/СН3СОО- = 1.75 10-50,1/1 = 1.75 10-6, откуда рН = 5,76. Полученные результаты однозначно указывают на то, что при добавлении к раствору уксусной кислоты ацетата натрия происходит уменьшение концентрации ионов Н+, вызывающее увеличение рН, т.е. происходит сдвиг ионного равновесия влево – в сторону образования дополнительного количества недиссоциированных молекул уксусной кислоты.
Вывод о направлении сдвига ионного равновесия в растворе уксусной кислоты при добавлении к нему ацетата натрия можно распространить на все ионные равновесия: при добавлении к раствору слабого электролита одноимённых ионов, образующихся в результате диссоциации сильного электролита, происходит сдвиг ионного равновесия в сторону образования недиссоциированного слабого электролита.
Смещение ионного равновесия в противоположную сторону, т.е. в направлении усиления диссоциации слабого электролита, происходит при добавлении к раствору слабого электролита любого другого электролита, ионы которого способны связывать ионы слабого электролита.
Пример 3.2. Смещение ионного равновесия при добавлении к раствору уксусной кислоты раствора гидроксида натрия.
Добавляемый к раствору СН3СООН гидроксид натрия – сильный электролит, диссоциирующий полностью согласно уравнению: NaOH = Na+ + OH-.
В смеси СН3СООН и NaOH одновременно протекают 2 взаимосвязанных процесса:
1) СН3СООН СН3СОО- + Н+– обратимая диссоциация слабой кислоты;
2) Н+ + OH- = Н2О – связывание ионов Н+ слабой кислоты ионами OH- щёлочи, вызывающее согласно принципу Ле Шателье смещение ионного равновесия 1) вправо, т.е. дополнительную диссоциацию уксусной кислоты вплоть до её полного израсходования, если количество добавленного NaOH достаточно для связывания всех ионов Н+ уксусной кислоты.
Суммарно процессы 1) и 2), протекающие в смеси растворов СН3СООН и NaOH, выражаются уравнением: СН3СООН + OH- = СН3СОО- + Н2О. Записанное суммарное уравнение представляет собой ионно-молекулярное уравнение реакции между уксусной кислотой и гидроксидом натрия.
Связывание ионов слабого электролита, вызывающее смещение ионного равновесия – вправо – в сторону усиления диссоциации слабого электролита, может происходить в результате образования неэлектролита (например, газообразного соединения) или любого слабодиссоциирующего химического образования – труднорастворимого электролита, растворимого слабого электролита, комплекса и пр.
Одновременное влияние связывания ионов и введения одноимённых ионов на состояние ионных равновесий удобно проследить на примере гетерогенных равновесий, устанавливающихся в растворах амфотерных электролитов.
Пример 3.3. Смещение гетерогенных ионных равновесий в растворе трунорастворимого гидроксида хрома (III) при добавлении к нему кислоты и щёлочи.
Как уже указывалось (см. п. 2), амфотерные гидроксиды способны диссоциировать и по кислотному, и по основному типу. Диссоциацию амфотерного Cr(OH)3 можно выразить схемой:
Диссоциация по кислотному типу Диссоциация по основному типу
[Cr(OH)6]3- + 3H+ Cr(OH)3 + 3h3O Cr3+ + 3OH- + 3h3O
При добавлении к раствору Cr(OH)3 кислоты (ионов H+) равновесие диссоциации по кислотному типу из-за действия одноимённых ионов H+ смещается вправо; одновременно, в результате связывания ионов OH- ионами H+ добавленной кислоты равновесие диссоциации по основному типу смещается также вправо вплоть до полного растворения Cr(OH)3, если количество добавленной кислоты достаточно для полного связывания всех ионов OH- гидроксида хрома. Иначе говоря, при взаимодействии с кислотами Cr(OH)3 ведёт себя как основание.
При добавлении к раствору Cr(OH)3 щёлочи (ионов OH-) равновесие диссоциации по основному типу из-за действия одноимённых ионов OH- смещается влево; одновременно, в результате связывания ионов H+ ионами OH- добавленной щёлочи равновесие диссоциации по кислотному типу смещается также влево вплоть до полного растворения Cr(OH)3, если количество добавленной щёлочи достаточно для полного связывания всех ионов H+ гидроксида хрома. Т.е., при взаимодействии со щелочами Cr(OH)3 ведёт себя как кислота.
В общем случае, в результате смещения гетерогенного ионного равновесия растворимость труднорастворимого электролита увеличивается при связывании любого из его ионов и, наоборот, происходит осаждение труднорастворимого электролита из раствора, если произведение концентраций его ионов превышает значение ПР.
Пример 3.4. Определение возможности осаждения гидроксида железа (II) из раствора, содержащего ионы Fe2+ и OH-, концентрации которых, соответственно, равны 10-4М и 10-7М.
Записываем выражение произведения растворимости Fe(OH)2 и отмечаем его численное значение (см. пример 1.1): ПР = [Fe2+][ OH-]2 = 210-15. Вычисляем произведение концентраций (ПС) имеющихся в растворе ионов Fe2+ и OH-: ПС = 10-4(10-7)2 = 10-18. Видно, что ПС ПР. Следовательно, раствор является ненасыщенным, условие осаждения не выполняется и осадок Fe(OH)2 не образуется.
studfiles.net