Как определить количество протонов и нейтронов. Количество нейтронов в хроме
Как определить количество протонов и нейтронов
Атом всякого химического элемента состоит из ядерного ядра и, обращающихся вокруг него, электронов. А из чего состоит ядерное ядро? В 1932 году было установлено, что ядерное ядро состоит из протонов и нейтронов .

Вам понадобится
- — периодическая таблица химических элементов Д.И. Менделеева.
Инструкция
1. Протон представляет собой одобрительно заряженную частицу с массой превышающей в 1836 раз массу электрона. Электрический заряд протона совпадает по модулю с зарядом электрона, а значит, заряд протона равен 1,6*10 ^ (-19) Кулон. Ядра различных атомов содержат различное число протонов . К примеру, в ядре атома водорода только один протон, а в ядре атома золота – семьдесят девять. Число протонов в ядре совпадает с порядковым номером данного элемента в таблице Д.И. Менделеева. Следственно для того, дабы определить число протонов в ядре химического элемента, надобно взять таблицу Менделеева, обнаружить в ней необходимый элемент. Указанное вверху целое число является порядковым номером элемента — это и есть число протонов в ядре. Пример1. Пускай необходимо определить число протонов в ядре атома полония. Обнаружьте в таблице Менделеева химический элемент полоний, он размещен под номером 84, значит в его ядре находится 84 протона.
2. Увлекательно, что число протонов в ядре совпадает с числом электронов, движущихся вокруг ядра. То есть число электронов в атоме элемента определяется так же, как и число протонов – порядковым номером элемента. Пример 2. Если порядковый номер полония — 84, то в нем 84 протона (в ядре) и столько же — 84 электронов.
3. Нейтрон представляет собой незаряженную частицу с массой, которая огромнее массы электрона в 1839 раз. Помимо порядкового номера, в периодической таблице химических элементов для всего вещества указано еще одно число, которое, если его округлить, показывает всеобщее число частиц (протонов и нейтронов ) в ядерном ядре. Это число именуется массовым числом. Для определения числа нейтронов в ядре необходимо вычесть из массового числа число протонов . Пример 3. Число протонов в атоме полония – 84. Его массовое число равно 210, значит, для определения числа нейтронов обнаружьте разность массового числа и порядкового номера: 210 – 84 = 126.
Атом химического элемента состоит из ядерного ядра и электронов. В состав ядерного ядра входят два типа частиц — протоны и нейтроны. Примерно каждая масса атома сфокусирована в ядре, потому что протоны и нейтроны гораздо тяжелее электронов.

Вам понадобится
- атомный номер элемента, изотопы
Инструкция
1. В различие от протонов, нейтроны не имеют электрического заряда, то есть их электрический заряд равен нулю. Следственно, зная ядерный номер элемента, невозможно однозначно сказать, сколько нейтронов содержится в его ядре. К примеру в ядре атома углерода неизменно содержится 6 протонов, впрочем протонов в нем может быть 6 и 7. Разновидности ядер химического элемента с различным числом нейтронов в ядре именуются изотопами этого элемента. Изотопы могут быть как природными, так и полученными неестественно.
2. Ядерные ядра обозначаются буквенным символом химического элемента из таблицы Менделеева. Справа от символа вверху и внизу стоят два числа. Верхнее число A — это массовое число атома, A = Z+N, где Z — заряд ядра (число протонов),а N — число нейтронов . Нижнее число — это Z — заряд ядра. Такая запись дает информацию о числе нейтронов в ядре. Видимо, оно равно N = A-Z.
3. У различных изотопов одного химического элемента число A меняется, что отражено в записи этого изотопа. Определенные изотопы имеют свои подлинные наименования. Скажем, обыкновенное ядро водорода не имеет нейтронов и имеет один протон. Изотоп водорода дейтерий имеет один нейтрон (A = 2), а изотоп тритий — два нейтрона (A = 3).
4. Связанность числа нейтронов от числа протонов отражена на N-Z диаграмме ядерных ядер. Стабильность ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов особенно устойчивы при N/Z = 1, то есть при равенстве числа нейтронов и протонов. С ростом массового числа область стабильности сдвигается к величинам N/Z>1, достигая величины N/Z ~ 1,5 для особенно тяжелых ядер.
Видео по теме
Атом химического элемента состоит из ядерного ядра и электронной оболочки. В состав ядерного ядра входят два типа частиц — протоны и нейтроны. Примерно каждая масса атома сконцентрирована в ядре, так как протоны и нейтроны гораздо тяжелее электронов.

Вам понадобится
- атомный номер элемента, N-Z диаграмма.
Инструкция
1. Нейтроны не имеют электрического заряда, то есть их электрический заряд равен нулю. Это и представляет основную трудность при определении числа нейтронов — ядерный номер элемента либо его электронная оболочка не дают однозначного результата на данный вопрос. Скажем, в ядре атома углерода неизменно содержится 6 протонов, впрочем протонов в нем может быть 6 и 7. Разновидности ядер химического элемента с различным числом нейтронов в ядре именуются изотопами этого элемента. Изотопы могут быть природными, а могут быть и получены неестественно.
2. Ядра атомов обозначают буквенным символом химического элемента из таблицы Менделеева. Справа от символа вверху и внизу стоят два числа. Верхнее число A — это массовое число атома. A = Z+N, где Z — заряд ядра (число протонов), а N — число нейтронов. Нижнее число — это Z — заряд ядра. Такая запись дает информацию о числе нейтронов в ядре. Видимо, что оно равно N = A-Z.
3. У различных изотопов одного химического элемента число A меняется, что дозволено увидеть в записи этого изотопа. Определенные изотопы имеют свои подлинные наименования. Скажем, обыкновенное ядро водорода не имеет нейтронов и имеет один протон. Изотоп водорода дейтерий имеет один нейтрон (A = 2, цифра 2 сверху, 1 снизу), а изотоп тритий — два нейтрона (A = 3, цифра 3 сверху, 1 снизу).
4. Связанность числа нейтронов от числа протонов отражена на так называемой N-Z диаграмме ядерных ядер. Стабильность ядер зависит от отношения числа нейтронов и числа протонов. Ядра легких нуклидов особенно устойчивы при N/Z = 1, то есть при равенстве числа нейтронов и протонов. С ростом массового числа область стабильности сдвигается к величинам N/Z>1, достигая величины N/Z ~ 1,5 для особенно тяжелых ядер.
Видео по теме
Дабы обнаружить число протонов в атоме, определите его место в таблице Менделеева. Обнаружьте его порядковый номер в периодической таблице. Он будет равен числу протонов в ядерном ядре. Если изучается изотоп, посмотрите на пару чисел, описывающие его свойства, нижнее число будет равно числу протонов. В том случае, если знаменит заряд ядерного ядра, дозволено узнать число протонов, поделив его значение на заряд одного протона.
Вам понадобится
- Для того дабы обнаружить число протонов, узнайте значение заряда протона либо электрона, возьмите таблицу изотопов, периодическую таблицу Менделеева.
Инструкция
1. Определение числа протонов вестимого атома.В том случае, когда знаменито, какой атом изучается, обнаружьте его расположение в периодической таблице. Определите его номер в этой таблице, обнаружив ячейку соответствующего элемента. В данной ячейке обнаружьте порядковый номер элемента, тот, что соответствует постигаемому атому. Данный порядковый номер и будет соответствовать числу протонов в ядерном ядре.
2. Как обнаружить протоны в изотопе.Многие атомы имеют изотопы, отличающиеся массами ядер. Именно следственно только лишь массы ядра неудовлетворительно для однозначного определения ядерного ядра. При изложении изотопа перед записью его химического обозначения неизменно записывается пара чисел. Верхнее число показывает массу атома в ядерных единицах массы, а нижнее обозначает заряд ядра. Вся единица заряда ядра в такой записи соответствует одному протону. Таким образом, число протонов равно нижнему числу в записи данного изотопа.
3. Как обнаружить протоны, зная заряд ядра.Зачастую свойства атома характеризуется зарядом его ядра. Для того дабы определить число протонов в нем, нужно перевести его в кулоны (если он подан в кратных единицах). После этого поделите заряд ядра на модуль заряда электрона. Это связано с тем, что от того что атом электрически нейтрален, то число протонов в нем равно числу электронов. Причем заряды их равны по модулю и противоположны по знаку (протон имеет правильный заряд, электрон – негативный). Следственно заряд ядра атома поделите на число 1,6022•10^(-19) кулон. В итоге получится число протонов. От того что способы измерения заряда атома неудовлетворительно точны, в том случае, если при делении получилось дробное число, округлите его до целого.
Видео по теме
Атомы состоят из субатомных частиц — протонов, нейтронов и электронов. Протоны представляют собой позитивно заряженные частицы, которые находятся в центре атома, в его ядре. Вычислить число протонов изотопа дозволено по ядерному номеру соответствующего химического элемента.
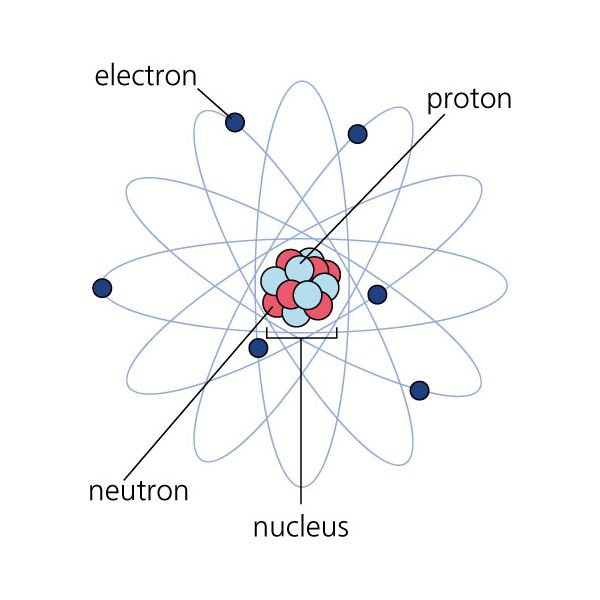
Модель атома
Для изложения свойств атома и его конструкции применяется модель, знаменитая под наименованием «Модель атома по Бору». В соответствии с ней конструкция атома напоминает ясную систему — весомый центр (ядро) находится в центре, а больше легкие частицы движутся по орбите вокруг него. Нейтроны и протоны образуют позитивно заряженное ядро, а негативно заряженные электроны движутся вокруг центра, притягиваясь к нему электростатическими силами.Элементом называют вещество, состоящее из атомов одного типа, он определяется числом протонов в всем из них. Элементу присваивают свое имя и символ, скажем, водород (H) либо кислород (О). Химические свойства элемента зависят от числа электронов и, соответственно, числа протонов, содержащихся в атомах. Химические колляции атома не зависят от числа нейтронов, потому что нейтроны не имеют электрического заряда. Впрочем их число влияет на устойчивость ядра, изменяя всеобщую массу атома.
Изотопы и число протонов
Изотопами называют атомы отдельных элементов с разным числом нейтронов. Данные атомы химически одинаковым, впрочем владеют различной массой, также они отличаются своей способностью испускать излучение.Ядерный номер (Z) — это порядковый номер химического элемента в периодической системе Менделеева, он определяется числом протонов в ядре. Всякий атом характеризуется ядерным номером и массовым числом (А), которое равно суммарному числу протонов и нейтронов в ядре. Элемент может иметь атомы с разным числом нейтронов, но число протонов остается постоянным и равно числу электронов нейтрального атома. Для того, дабы определить, сколько протонов содержится в ядре изотопа, довольно посмотреть на его ядерный номер. Число протонов равно номеру соответствующего химического элемента в периодической таблице Менделеева.
Примеры
В качестве примера дозволено разглядеть изотопы водорода. В природе особенно распространены атомы водорода с одним протоном и без нейтронов. В то же время существуют изотопы водорода с одним либо двумя нейтронами, они имеют соответствующие наименования. Впрочем у них у всех один протон, что соответствует порядковому номеру водорода в периодической таблице. Изотоп водорода с одним нейтроном и массовым числом 2 называют дейтерием либо тяжелым водородом, он стабилен. Тритий, изотоп водорода с массовым числом 3 и двумя нейтронами, радиоактивен. Его изредка называют сверхтяжелым водородом, а ядро трития — тритоном.
Полоний — радиоактивный химический элемент VI группы периодической системы Менделеева, он относится к халькогенам. Полоний представляет собой мягкий серебристо-белый металл. Стабильных изотопов у данного элемента нет, но вестимо 27 радиоактивных.
Инструкция
1. Полоний был одним из первых открытых радиоактивных элементов, его нашли Пьер Кюри и Мария Склодовская-Кюри в 1898 году. Свое наименование он получил в честь Польши — родины Марии Склодовской-Кюри. Впервой полоний был выделен из урановой смоляной руды.
2. Полоний — редкий элемент, знамениты две его кристаллические модификации: низкотемпературная форма с кубическая решеткой, при температуре выше 36°С устойчива форма с ромбоэдрической решеткой.
3. Полоний присутствует в маленьких числах в морской воде, его могут накапливать разные морские организмы. Данный элемент попадает в тело человека совместно с пищей, позже чего равномерно распределяется по отдельным органам.
4. В высоких концентрациях полоний исключительно токсичен, для работы с ним применяют особые боксы. Токсичность полония была исследована в навыках на звериных, он вызывал метаморфозы состава периферической крови и уменьшал длительность жизни. У звериных прогрессировали опухоли разных органов. Биологическое влияние полония в мелких концентрациях неудовлетворительно изучено.
5. По своим химическим свойствам полоний близок к теллуру, в соединениях данный элемент проявляет степени окисления -2, +2, +4 и +6. Полоний окисляется на воздухе, он реагирует с растворами кислот с образованием ионов. При взаимодействии с водородом данный элемент дает летучий гидрид.
6. Нагревая металлы с парами полония при температуре 400-1000°С, получают полониды. Диоксид полония может существовать в 2-х кристаллических модификациях: при температуре ниже 54°С стабильна желтая форма с гранецентрированной кубической решеткой, при нагревании диоксид переходит в красную форму с тетрагональной решеткой. Монооксид полония представляет собой твердое вещество черного цвета, он образуется при беспричинном разложении селенита либо сульфита полония.
7. В граммовых числах полоний получают при помощи облучения металлического висмута нейтронами, процесс проходит в ядерных реакторах. В микроскопичных числах он может быть выделен из отходов переработки урановых руд. Его получают экстракцией, электроосаждением, возгонкой и ионным обменом. Полоний также образуется при облучении висмута протонами в циклотроне.
8. Полоний применяют в качестве источника энергии в ядерных батареях космических агрегатов, а также в переносных устройствах. Его используют для изготовления ампульных источников нейтронов.
Видео по теме
jprosto.ru
Рений нейтронов - Справочник химика 21
При определении рения в различных технических продуктах чаще всего используются спектрофотометрические, спектральные и полярографические методы, а также нейтронно-активационный метод с применением ампульных источников нейтронов (Ро—Ве и Ас—Ве) с потоком 1-10 нейтрон/см -сек. [c.246]Сколько нейтронов в ядре атома наиболее распространенного изотопа рения Массовое число 187. [c.220]
К первой группе относятся наиболее распространенный нейтронно-активационный метод и фотонейтронный, основанный на реакции (у, п), практически не используемый вследствие относительно малого значения сечения активации. К этой же группе может быть отнесен также пока не используемый метод, основанный на реакции d, р). Б процессе протекания ядерных реакций происходит образование радиоизотопов рения, некоторые свойства которых приведены в табл. 23. В работах [1205, 1353] описаны у-спектры изотопов Ве и Ве. [c.168]Определение рения нейтронно-активационным методом [c.239]
Еще одно отличие от рентгеновских спектров наблюдается для атомов, магнитный момент которых обусловлен наличием неспа-ренных электронов. Такие атомы дают добавочное рассеивание нейтронного пучка, поскольку нейтрон обладает магнитным моментом. Это дает информацию об ориентации магнитных моментов в кристаллической решетке. [c.208]
Анализ лунного грунта. Нейтронно-активационный метод использовали для определения содержания рения и его изотопного состава в образцах лунного грунта [1352, 1356]. [c.241]
Анализ исходных материалов и продуктов их переработки на рений проводили с привлечением высокочувствительных физико-химических методов анализа радиофизических (нейтронно-активационного, гамма-активационного), масс-спектрометрии, кинетических. [c.80]
Шен и Реньо [292] предложили использовать солянокислые растворы для извлечения и- из тория, облученного в ядерном реакторе, и- образуется вследствие действия тепловых нейтронов на атомы Задача заключается в отделении урана от промежуточных элементов Т[1- - и Ра [c.317]
Нейтронно-активационный метод широко используется для определения рения в различных объектах. Чувствительность определения рения, рассчитанная для типичных условий активации тепловыми нейтронами в реакторе с потоком 1,8 -10 нейтрон см -сек и времени облучения 1 час., равна по р-счету Ве (7 i =91 час.) после радиохимического выделения рения—0,001 мкг и по Р-счету Ве (Ji/, = 17 час.) — 0,0005 мкг, а с использованием 7-спектрометрии — 0,05 и 0,001 мкг соответственно (0,01 мкг соответствует 10" % в образце весом 1 г и 10 % — в 10 г). Эта чувствительность может быть повышена путем увеличения потока нейтронов или продолжительности облучения [1334]. [c.168]
НОГО заряда, что соответствует процессу окисления. Так, например, при облучении хлорида четырехвалентного рения нейтронами было обнаружено образование иона перрената. При облу-чешии гидратов солей трехвалентного хрома было найдено, что до 10% радиоактивного хрома оказываются в шестивалентном состоянии. [c.257]
Вариант недеструктивного анализа является более экспрессным, однако он непригоден для определения небольших количеств рения в объектах, содержащих микро- и макрокомпоненты, которые образуют по (и, у)-реакциям радиоизотопы с близкими к радиоизотопам рения значениями энергий -квантов и периодов полураспада. Кроме того, этот метод не может быть использован при определении малых количество рения в присутствии повышенных количество осмия и родия из-за конкурирующих ядерных реакций (п,р) и (и, а). Проведение определения рения в такого рода объектах (с значительно меньшей чувствительностью) возможно лишь с использованием резонансных нейтронов Ри—Ве-нейтрон-ного источника 881 об использовании ампульных нейтронных источников на основе Ро—Ве и Ас—Ве см. также [137]. В работе [139] описана методика недеструктивного активационного определения рения в молибденитовых концентратах с чувствительностью (1-2)-10-2% Ве. [c.169]
Наибольшее распространение получили нейтронно-активационные методы, основанные на определении рения после радиохимического выделения и очистки его радиоизотопов. В образцах, содержащих повышенные концентрации вольфрама, необходим учет образования радиоизотопов рения в результате ядерных реакций [c.169]
Недостатками радиоактивационных методов являются значительные сложности определения рения в объектах с высокими значениями сечений захвата нейтронов (бор, кадмий, некоторые РЗЭ) и необходимость использования сложного и дорогого электронного оборудования. Кроме того, точность определения рения этим методом не превышает 20—30%. [c.171]
В настоящее время генераторы рения-188 производятся на коммерческой основе в трёх странах России, США и Финляндии. Выпускаемые генераторы рения-188 являются аналогами генераторов технеция-99т, т.е. в основе лежит сорбционный процесс на оксиде алюминия. Для изготовления таких генераторов необходим вольфрам-188 высокой удельной активности (> 5 Ки/г), который может быть получен на высокопоточных реакторах с потоком нейтронов > 10 см с , которые имеются только в США (Ок-Ридж) и России (Димитровград). Такая ситуация снижает надёжность поставок и доступность [c.551]
Наиболее чувствительным методом определения рения является нейтронно-активационный (подробно см. стр. 168). Метод широко используется для определения рения в породах, рудах и минералах [147, 377, 658, 786, 836, 871, 950, 983, 1025, 1042, 1044, 1053,1056—1058, 1135,1170, 1205, 1353], а также в объектах космического происхождения (в лунном грунте) [1352, 1356 и др.]. Чувствительность определения репия этим методом может регулироваться подбором величины потока нейтронов и времени облучения. [c.239]
Анализ молибденита. Нейтронно-активационным методом определяют содержание рения в молибденитах [147, 377, 661, 786, 1053, 1205]. Для определения рения измеряют активность радиоизотопов реиия при различных энергиях после предварительного радиохимического выделения рения или без него. Ниже приведена методика анализа молибденита с радиохимическим выделением рения [318]. [c.240]
Для определения рения в молибденовых и медных концентратах, медных рудах (сланцах) применяется нейтронно-активационный метод с радиохимической очисткой изотопов и без нее [137, 138, 147, 746, 786, 1104]. [c.249]
В металлическом технеции рений определяют нейтронно-активационным методом [497]. Метод позволяет определять до 10 г Re в 1 г образца при облучении потоком нейтронов 1,2- 10 нейтрон с.н сек. [c.261]
В селене высокой чистоты содержание примеси рения определяют нейтронно-активационным методом [1298]. [c.261]
Для установления содержания рения в кварце высокой чистоты его облучают в реакторе потоком 9-10 нейтрон см -сек в течение недели [10531. [c.263]
На первых порах надежды сбывались. Из облученного нейтронами урана Д Агостино выделил излучатель с периодом полураспада 13 минут. Во всех химических процедурах неизвестная активность следовала за рением. Напрашивался вывод химические свойства рения и полученного в нейтронной бомбардировке радиоактивного изотопа близки между собой. Из урана после нейтронного захвата мог получиться только очень тяжелый элемент. Среди тяжелых элементов химическим аналогом рения мог быть только элемент № 93. Во всяком случае, так считалось в 1934 г. [c.379]
Анализ метеоритов. Углцстые метеориты, хондриты, ахондриты анализируют на содержание рения нейтронно-активационным методом с применением субстехиометрического разделения [377]. Чувствительность метода позволяет определять до l-10-i г Re с точностью до 10 отн. %. Увеличивая период выдержки образцов после облучения, достигают повышения селективности метода. T (VII) мешает определению, поэтому его восстанавливают Sn(II) до T (IV). Методика определения заключается в следующем. [c.240]
Основную массу марганца выплавляют в виде ферромарганца (сплав 60—90% Мп и 40—10% Fe) при восстановлении смеси железных и марганцевых руд. Около 90% марганца применяется в металлургии для раскисления и легирования сталей. Он придает сплавам железа коррозионную стойкость, вязкость и твердость. Технеций коррозионностоек и устойчив против действия нейтронов, поэтому может применяться как конструкционный материал для атомных реакторов. Рений в основном используется в электротехнической промьшленности и как катализатор. [c.571]
РЕНИЙ (от лат. Rhenus-рака Рейн Rhenium) Re, хим. элемент VII гр. периодич. системы, ат.н. 75, ат.м. 186,207. Природный Р. состоит из двух изотопов стабильного Re (37,4%) и слаборадиоактивного Re (62,6%, Tj/2 5-10 ° лет). Поперечное сечение захвата тепловых нейтронов для природного Р. 8,6-10 м . [c.236]
Кроме радиоактивных продуктов деления урана или плутония в глобальных радиоактивных выпадениях могут присутствовать радиоактивные изотопы, возникающие в результате взаимодействия нейтронов, образующихся при ядерном взрыве, с атомами элементов заряда, конструкций и элементов, содержащихся в воздухе, почве, породах. Вследствие взаимодействия нейтронов с элементами заряда образуется нептуний-239, а при термоядерном взрыве — тритий и уран-237. При взаимодействии нейтронов с консфуктивными элементами устройства образуются кобальт-60, кобальт-57, вольфрам-185, вольфрам-181, вольфрам-187, рений-188 и родий-102. При взаимодействии с компонентами воздуха образуются аргон-41, углерод-14 и тритий. При взаимодействии с почвой активируются алюминий, кремний, натрий, марганец, железо, кобальт и другие элементы (табл. 8). [c.33]
Нейтронно-активационный метод анализа может выполняться в трех вариантах недеструктивный — прямое у-спектрометричес-кое определение рения в облученных образцах определение noeles [c.168]
Согласно [13651, уровень помех в определении рения при облучении потоком 5 -10 нейтрон/см -сек в течение 10 сек. составляет сиитветственно 20 и 2 мкг W на 1 г пробы. По другим данным, присутствие 100 ч. (распространенность 28,4%) приводит к образованию радиоизотопа Re, эквивалентного содержанию [c.170]
Для определения рения в природных материалах с различным содержанием рения (от 1-10- до 1-10" %) применяются спектро-фотомётрические, каталитические, полярографические, спектральные, нейтронно-активационные и другие методы. [c.239]
Отделение рения от примесей при нейтронно-активационном определении рения осуществляют обычно после облучения анализируемого материала. Как правило, комбинируют несколько приемов очистки для получения радиохимически чистых изотопов a Re и Re. На первой стадии после разложения проб с NajOj или СаО (с добавлением КМПО4) отделяют многие элементы в виде гидроокисей и дополнительно очищают рений экстракцией [1053], дистилляцией [871, 955], хроматографией [894] и другими методами, после чего выделяют радиохимически чистые изотопы ia Re и Re на носителе (несколько миллиграммов рения в виде перрената тетрафениларсония, RejS, и др.). Активность Re и Йе измеряют на "- или 7-спектрометре. Содержание рения устанавливают сравнением полученных величин с активностью стандартных проб с известным содержанием репия. [c.239]
Для определения рения в технологических растворах, в частности в электролитных растворах сульфата цинка, использован нейтронно-активационный метод [137а, 741]. [c.251]
Раствор упаривают в кварцевой ампуле почти досуха, облучают вместе со стандартом нейтронами (поток 6 10 2 нейтрон см сек) и выдерживают 3—4 дня после облучения. Облученную пробу растворяют в 0,5 N HNOg, вводят носитель 0,1 жг Re (а также носители для других примесей — Мо, Hg, Р, Си). Раствор пропускают через колонку с анионитом дауэкс-1 Х8 в NOg-форме, промывают колонку 0,5 N раствором HNO3 до полного удаления цинка (75 объемов колонки) и вымывают рений 0,2 N раствором H IO4 (38 объемов колонки), отбрасывая первые 19 объемов. Измеряют активность i Re по -шшу 63 и 137 кэв [741]. [c.251]
Содержание примеси рения в ниобии и тантале также определяется нейтронно-активационным методом. Металлы облучают потоком 10 нейтрон см сек в течение нескольких дней. Растворяют в смеси HF и HNOg. Отделяют примеси и основу хроматографическим методом на анионите дауэкс-1 и катионите дау-экс-50. Re(VII) десорбируют с анионита дауэкс-1 0,5 М раствором H IO4. Активность рения измеряют на у-снектрометре [618]. [c.261]
В металлическом осмии рений определяют найтронно-актива-ционным методом [1296]. Для этого 10—15 мг порошка осмия с соответствуюш им эталоном облучают 30 мин. в потоке нейтронов 1,8-10 нейтрон см -сек. Из облученной пробы отгоняют осмий в виде OSO4 при 100—120° С в течение 10—15 мин. В остатке измеряют активность Re час.) но у-пику 137 кэв [c.261]
Разработан пейтронно-активационный метод определения содержания до 2-10 % Re в трихлорсилане, пригодный и для анализа кремния, карбида кремния и германия. Около 300 мкг трихлорметилсилана подвергают гидролизу, остаток высушивают и облучают в течение 8 час. потоком медленных нейтронов 1,8-10 нейтрон см -сек. После облучения образцы протравливают соляной кислотой, обмывают водой и дальше выделяют группы элементов экстракцией по схеме (стр. 264, приведена часть схемы, относящаяся к выделению рения) [1288]. [c.263]
Этот гордиев узел единым ударом разрубили в 1938 г немецкие химики Отто Ган и Фриц Штрассман, открывшие деление урановых ядер под действием нейтронов, Стали понятны ошибки тридцать четвертого года. Нейтроны расщепляли урановые ядра на десятки радиоактивных изотопов. Излучение, приписываемое экарению , в дей-ствительности могло быть излучением самого рения. Или даже его более легких аналогов. Изотопы с периодом полураспада от 10 до 17 минут есть и у рения, и у технеция, открытого спустя несколько лет после нейтронных опытов Ферми его коллегой и другом Эмилио Сегре. [c.380]
chem21.info
Как определить количество протонов и нейтронов
Атом любого химического элемента состоит из атомного ядра и, обращающихся вокруг него, электронов. А из чего состоит атомное ядро? В 1932 году было установлено, что атомное ядро состоит из протонов и нейтронов.Вам понадобится
- - периодическая таблица химических элементов Д.И. Менделеева.
Инструкция
- Протон представляет собой положительно заряженную частицу с массой превышающей в 1836 раз массу электрона. Электрический заряд протона совпадает по модулю с зарядом электрона, а значит, заряд протона равен 1,6*10 ^ (-19) Кулон. Ядра разных атомов содержат разное число протонов. К примеру, в ядре атома водорода только один протон, а в ядре атома золота – семьдесят девять. Число протонов в ядре совпадает с порядковым номером данного элемента в таблице Д.И. Менделеева. Поэтому для того, чтобы определить число протонов в ядре химического элемента, нужно взять таблицу Менделеева, найти в ней нужный элемент. Указанное вверху целое число является порядковым номером элемента - это и есть число протонов в ядре. Пример1. Пусть нужно определить число протонов в ядре атома полония. Найдите в таблице Менделеева химический элемент полоний, он расположен под номером 84, значит в его ядре находится 84 протона.
- Интересно, что количество протонов в ядре совпадает с числом электронов, движущихся вокруг ядра. То есть число электронов в атоме элемента определяется так же, как и число протонов – порядковым номером элемента. Пример 2. Если порядковый номер полония - 84, то в нем 84 протона (в ядре) и столько же - 84 электронов.
- Нейтрон представляет собой незаряженную частицу с массой, которая больше массы электрона в 1839 раз. Помимо порядкового номера, в периодической таблице химических элементов для каждого вещества указано еще одно число, которое, если его округлить, показывает общее количество частиц (протонов и нейтронов) в атомном ядре. Это число называется массовым числом. Для определения количества нейтронов в ядре нужно вычесть из массового числа количество протонов. Пример 3. Количество протонов в атоме полония – 84. Его массовое число равно 210, значит, для определения числа нейтронов найдите разность массового числа и порядкового номера: 210 – 84 = 126.
completerepair.ru
Сечение - захват - медленный нейтрон
Сечение - захват - медленный нейтрон
Cтраница 1
Сечение захвата медленных нейтронов ядрами металла-восстановителя и содержание в нем примесей со значительными сечениями захвата должны быть незначительными. [1]
При атомном весе 12 он имеет очень низкое сечение захвата медленных нейтронов, равное 3 2 0 2 миллибар-на - условной единицы, характеризующей количество нейтронов не замедленных, а поглощенных средой материала на единицу его поверхности. К примеру, бор имеет аналогичное сечение захвата, равное 750 барн, или в 250 тыс. раз выше, чем у углерода. Иными словами, один атом бора, являясь примесью графита, увеличивает собственное поглощение нейтронов двухсот пятидесяти тысяч атомов углерода вдвое. Поглощение, захват нейтронов тушит цепную реакцию урана. [2]
Первое время завод часто попадал в тяжелое положение из-за брака продукции по допустимой величине сечения захвата медленных нейтронов, а проще - из-за загрязнения графита бором. [3]
В самом деле, если бы этот закон был справедлив для Ag и Rh, то сечение захвата медленных нейтронов ( умедл УНТ) должно бы быть меньше сечения захвата тепловых и эффект от медленных нейтронов не мог бы быть так велик. [4]
Принципы нейтронного активациониого анализа теперь уже хорошо установлены и больше по нуждаются в подробном разборе. Так как сечение захвата быстрых нейтронов обычно много меньше, чем сечение захвата медленных нейтронов [4], ошибки за счет самоэкрапирования при активационпом анализе на быстрых нейтронах будут меньше. Так, например, в то время как для мышьяка сечение захвата медленных, или тепловых, нейтронов ( эффективная энергия около 0 02 зв) равно 4 3 барк, его сечение поглощения для быстрых нейтронов, или нейтронов деления ( эффективная энергия около 1 Мае), составляет всего несколько миллибарн. Для хрома сечение захвата медленных нейтронов равно 3 1 барн, а для быстрых нейтронов сечение захвата не определено. Однако активация быстрыми нейтронами дает преимущества лишь в том случае, когда получается отвечающая предъявляемым требованиям чувствительность определения следов примесей. [5]
Максимальные ошибки, вызванные этим явлением, могут составлять несколько процентов. При использовании больших рабочих сосудов и в присутствии примесей элементов с высокими значениями сечений захвата медленных нейтронов пользуются данными нескольких измерений, выполненных в аналогичных условиях, но в рабочих сосудах разного объема, заполненных до одинакового уровня. [6]
Применению радиоактивационного метода благоприятствует то, что у алюминия мало по сравнению с примесными элементами сечение захвата медленных нейтронов, следовательно, незначителен распад его при облучении. К тому же алюминий не имеет долгоживущих радиоизотопов, его собственное излучение не накладывается на излучение примесей. Это позволяет определять в одной пробе до 40 элементов. [7]
Определим, какое количество мышьяка можно обнаружить в образце, используя источник нейтронов, дающий поток 1012 нейтр / см2 - сек, и имея в распоряжении счетчик, позволяющий определять активности порядка 100 имп / мин. Находим в таблицах, что мышьяк состоит из единственного изотопа с массой 75 ( 9100), для которого сечение захвата медленных нейтронов составляет 5 2 барна. [8]
Кроме того, необходимо было построить мощную установку газоочистки с пропусканием отходящих газов от хлорной графитации через скрубберы с известковым молоком, новый пролет, оснащенный станками полной механической обработки и специальную станцию физпроверки блоков на сечение захвата медленных нейтронов. [9]
Принципы нейтронного активациониого анализа теперь уже хорошо установлены и больше по нуждаются в подробном разборе. Так как сечение захвата быстрых нейтронов обычно много меньше, чем сечение захвата медленных нейтронов [4], ошибки за счет самоэкрапирования при активационпом анализе на быстрых нейтронах будут меньше. Так, например, в то время как для мышьяка сечение захвата медленных, или тепловых, нейтронов ( эффективная энергия около 0 02 зв) равно 4 3 барк, его сечение поглощения для быстрых нейтронов, или нейтронов деления ( эффективная энергия около 1 Мае), составляет всего несколько миллибарн. Для хрома сечение захвата медленных нейтронов равно 3 1 барн, а для быстрых нейтронов сечение захвата не определено. Однако активация быстрыми нейтронами дает преимущества лишь в том случае, когда получается отвечающая предъявляемым требованиям чувствительность определения следов примесей. [10]
Страницы: 1
www.ngpedia.ru