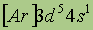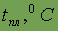Большая Энциклопедия Нефти и Газа. Соли хрома
Соль - хром - Большая Энциклопедия Нефти и Газа, статья, страница 3
Соль - хром
Cтраница 3
Соли хрома ( III) окрашены от зеленых до сине-фиолетовых оттенков; из водных растворов они кристаллизуются с различным количеством воды. Растворимые соли - галогениды, нитрат хрома Cr ( NO3) 3, сульфат хрома Cr2 ( SO4) 3 и др. Одна из наиболее распространенных растворимых двойных солей хрома - хромока-лиевые квасцы KCr ( SO4) 3 - 12h3O - представляет собой фиолетовые октаэдрические кристаллы. При нагревании до 50 - 70 С сине-фиолетовый водный раствор квасцов в результате изменения гидратации [ Сг3 ] становится светло-зеленым. [31]
Соли хрома ( III) имеют изумрудно-зеленый ( иногда фиолетовый) цвет. Они легко гидролизу ются. Эти соли легко окисляются свободными галогенами или перекисью водорода до хроматов. Из солей трехвалентного хрома наиболее известными являются двойные соли - хромовые квасцы KCr ( SO4) 2 12Н2О, соли типа ЗКС1 СгС13, аммиакаты - СгС13 6Nh4 и др. Хромовые квасцы служат исходными веществом при электролитическом получении свободного хрома. [32]
Соли хрома восстановители и ются. [34]
Соли хрома могут образовать с сульфат-ионами комплексные сое-динени я, что приводит к неполному осаждению сульфата бария. В этом случае следует ввести в раствор ацетат-ионы, которые с хромом образуют более устойчивый комплекс. [35]
Соли хрома могут образовать с сульфат-ионами комплексные соединения, что приводит к неполному осаждению сульфата бария. В этом случае следует ввести в раствор ацетат-ионы, которые с хромом образуют более устойчивый комплекс. [36]
Соли хрома ( III) сходны с солями алюминия. Они легко подвергаются гидролизу. [37]
Соли хрома ( III) весьма разнообразны по окраске: фиолетовые, синие, зеленые, коричневые, оранжевые, красные и черные. [38]
Соли хрома ( III) во многом похожи на соли алюминия. В водных растворах они сильно гидролизованы и легко превращаются в основные соли. Со слабыми кислотами хром ( III), подобно алюминию, солей не образует. [39]
Соли хрома ( III) сходны с солями алюминия. Они легко подвергаются гидролизу. [40]
Соли хрома ( III) весьма разнообразны по окраске: фиолетовые, синие, зеленые коричневые, оранжевые, красные и черные. [41]
Соли хрома ( III) сходны с солями алюминия. Они легко подвергаются гидролизу. [42]
Соли хрома ( II) не так широко применяют для количественного анализа восстанавливаемых органических соединений, как соли трехвалентного титана. [43]
Соли хрома часто существуют i лагается водой; нр. [44]
Страницы: 1 2 3 4
www.ngpedia.ru
Хром | Учеба-Легко.РФ - крупнейший портал по учебе
Свойства 24Cr.
| Атомная масса | 51,99 | кларк, ат.% (распространненость в природе) | 6×10-3 |
| Электронная конфигурация* | | Агрегатное состояние (н. у.). | твердое вещество |
| | 0,125 |
Цвет | серебристо-белый |
| | 0,035 | | 1903 |
| Энергия ионизации |
6,764 |  | 2642 |
| Относительная электроотрицательность |
1,6 | Плотность | 7,2 |
| Возможные степени окисления |
+1 ¸ +6 | Стандартный электродный потенциал |
+0,29 |
*Приведена конфигурация внешних электронных уровней атома элемента. Конфигурация остальных электронных уровней совпадает с таковой для благородного газа, завершающего предыдущий период и указанного в скобках.
Нахождение в природе. Хром встречается в виде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr2O4, богатые месторождения которого имеются на Урале и в Казахстане. Хром обнаружен на Солнце, звездах и в метеоритах.
Получение. Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
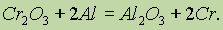
Металлический хром получают также электролизом водных растворов соединений хрома.
Физические свойства. Хром — серовато-белый блестящий металл. Из металлов он самый твердый, его плотность 7,2 г/см3, Tпл. 1855° С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Как и все d-элементы, хром обладает рядом характерных свойств: переменные состояния окисления; способность к образованию комплексных ионов; образование окрашенных соединений.
Химические свойства. При высоких температурах хром горит в кислороде с образованием Сr2O3, в раскаленном состоянии он реагирует с парами воды:

при нагревании с галогенами хром образует галогениды состава СrНаl3.
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние.
Хром пассивируется холодными концентрированными Н2SO4 и HNO3. Однако при сильном нагревании эти кислоты растворяют хром:

Пассивацию хрома можно устранить очисткой поверхности металла.
Хром растворяется при обычной температуре в разбавленных кислотах (НСl, HBr, HI, h3SO4) с выделением водорода. В этих случаях в отсутствие воздуха образуются соли Сr2+, а на воздухе — соли Сr3+.
При высокой температуре хром горит в кислороде, образуя оксид Сr2О3.
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:

Хром образует три оксида: СrО, Сr2O3 и СrO3.
Оксид хрома (II) СrО — пирофорный черный порошок (пирофорность — способность в тонкораздробленном состоянии воспламеняться на воздухе). Получается окислением амальгамы хрома кислородом воздуха. Растворяется в разбавленной соляной кислоте:

На воздухе при нагревании выше 100° С оксид хрома (II) превращается в оксид хрома (III).
Соли хрома (II). По своим химическим свойствам соли Cr2+ похожи на соли Fe2+. Обрабатывая их растворы щелочами в отсутствие кислорода, можно получить желтый осадок гидроксида хрома (II):

который обладает типичными основными свойствами. Является восстановителем. При прокаливании Cr(OH)2 в отсутствие кислорода образуется оксид хрома (II) СrО. При прокаливании на воздухе превращается в Сr2О3.
Все соединения хрома (II) довольно неустойчивы и легко окисляются кислородом воздуха в соединения хрома (III):
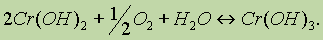
Соли хрома (III). Соли трехвалентного хрома сходны с солями алюминия по составу, строению кристаллической решетки и растворимости. В водных растворах катион Сr3+ встречается только в виде гидратированного иона [Сr(h3O)6]3+, который придает раствору фиолетовый цвет (для простоты пишут Сr3+).
При действии щелочей на соли хрома (Ш) выпадает студнеобразный осадок гидроксида хрома (III) — Сr(ОН)3 зеленого цвета:

Гидроксид хрома (III) обладает амфотерными свойствами, растворяясь как в кислотах с образованием солей хрома (III):

так и в щелочах с образованием тетрагидроксихромитов, т. е. солей, в которых Сг3+ входит в состав аниона:


Оксид хрома (III) Сr2O3 — тугоплавкий порошок зеленого цвета. По твердости близок к корунду, поэтому его вводят в состав полирующих средств. Получается соединением элементов при высокой температуре.
Сr2О3 представляет собой зеленые кристаллы, практически нерастворимые в воде. Сr2О3 может быть также получен при прокаливании дихроматов калия и аммония:

При сплавлении Cr2O3 со щелочами, содой и кислыми солями получаются соединения Сг3+, растворимые в воде:

Оксид хрома (VI) — кислотный оксид, ангидрид хромовой h3CrO4 и дихромовой h3Cr2O7 кислот.
Получается при взаимодействии концентрированной серной кислоты с насыщенным раствором дихромата натрия или калия:

СrО3 имеет кислотный характер: легко растворяется в воде, образуя хромовые кислоты. С избытком воды образует хромовую кислоту h3CrO4:

При большой концентрации СrО3 образуется дихромовая кислота h3Cr2O7:

которая при разбавлении переходит в хромовую кислоту:

Хромовые кислоты существуют только в водном растворе. Однако, их соли весьма устойчивы.
СrО3 представляет собой ярко-красные кристаллы, легко растворимые в воде. Сильный окислитель: окисляет иод, серу, фосфор, уголь, превращаясь при этом в Cr2O3. Например:

При нагревании до 250° С разлагается:

Он реагирует со щелочами, образуя желтые хроматы СrO42- :


В кислой среде ион СrO42- превращается в ион Сr2O72- .
В щелочной среде эта реакция протекает в обратном направлении:
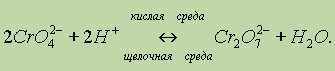
В кислой среде дихромат-ион восстанавливается до Сr3+:

Если сопоставить гидроксиды хрома с разной степенью окисления
Сr2+(ОН)2, Сr3+(ОН)3 и Н2Сr6+O4, то легко сделать вывод, что с возрастанием степени окисления основные свойства гидроксидов ослабевают, а кислотные усиливаются.
Сr(ОН)2 проявляет основные свойства, Сr(ОН)3 — амфотерные, а h3CrO4 — кислотные.
Хроматы и дихроматы (VI). Наиболее важными соединениями хрома в высшей степени окисления 6+ являются хромат (VI) калия К2СrО4 и дихромат (VI) калия K2Cr2O7.
Хромовые кислоты образуют два ряда солей: хроматы — так называются соли хромовой кислоты, и дихроматы — так называются соли дихромовой кислоты. Хроматы окрашены в желтый цвет (цвет хромат-иона СrO42- ), дихроматы — в оранжевый (цвет дихромат-иона Сr2O72-).
Дихроматы Na2Cr2O7× 2Н2O и K2Cr2O7 называются хромпиками. Они как окислители применяются в кожевенной (дубление кож), лакокрасочной, спичечной и текстильной промышленности. Хромовая смесь — так называется 3%-ный раствор дихромата калия в концентрированной серной кислоте — применяется в химических лабораториях для мытья стеклянной посуды.
Соли хромовых кислот в кислой среде — сильные окислители:

Соединения хрома (III) в щелочной среде играют роль восстановителей. Под действием различных окислителей — Cl2, Br2, h3O2, КмnO4 и др. — они переходят в соединения хрома (IV) — хроматы:


Здесь соединение Cr (III) изображено в форме Na[Cr(OH)4(h3O)2], так как в виде ионов Na+ и [Cr(OH)4(h3O)2]- оно существует в избытке раствора щелочи.
Сильные окислители, такие, как KMnO4, (Nh5)2S2O8 в кислой среде переводят соединения Cr (III) в дихроматы:
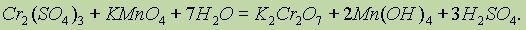
Таким образом, окислительные свойства последовательно усиливаются с изменением степеней окисления в ряду: Cr2+ ® Cr3+ ® Cr6+ .Соединения Cr (II) — сильные восстановители, легко окисляются, превращаясь в соединения крома. (III). Соединения хрома (VI) — сильные окислители, легко восстанавливаются в соединения хрома (III). Соединения с промежуточной степенью окисления, т. е. соединения хрома (III),могут при взаимодействии с сильными восстановителями проявлять окислительные свойства, переходя в соединения хрома (II), а при взаимодействии с сильными окислителями (например, бромом, KMnO4) проявлять восстановительные свойства, превращаясь в соединения хрома (VI).
Соли хрома (III) весьма разнообразны по окраске: фиолетовые, синие, зеленые, коричневые, оранжевые, красные и черные. Все хромовые кислоты и их соли, а также оксид хрома (VI) ядовиты: поражают кожу, дыхательные пути, вызывают воспаление глаз, поэтому, работая с ними, необходимо соблюдать все меры предосторожности.
uclg.ru
Хрома соли, растворимость - Справочник химика 21
При сплавлении СгаОз со щелочами, содой, кислыми солями получаются соединения хрома (3+), растворимые в воде [c.342]Фосфорнокислая соль трехвалентного хрома легко растворима в минеральных кислотах и в холодной уксусной кислоте. При кипячении уксуснокислого раствора фосфат хрома снова выпадает. Щавелевая кислота препятствует осаждению фосфата [c.220]
Большое практическое значение имеют и соли уксусной кислоты — натрия, алюминия, хрома, железа, меди, свинца и др. Большинство этих солей растворимо в воде при нагревании их водных растворов происходит ступенчатый гидролиз. Например, соли трехвалентных металлов (А1, Ре, Сг) гидролизуются по схеме [c.187]Растворимость хромата бария необходимо определить (при 30°) по окраске продукта, образующегося при действии дифенилкарбазида на насыщенный раствор соли. Избыток твердого хромата бария встряхивают с водой в термостате при постоянной температуре до тех пор, пока не будет достигнуто равновесие. 10 мл этого раствора переносят в мерную колбу емкостью 25 мл и обрабатывают 1 мл 5 н. раствора серной кислоты и 1 мл 0,25%-ного раствора реактива. Затем устанавливают оптическую плотность с зеленым светофильтром (л=540 m j.). Измеряют также стандартный раствор, содержащий 8-10 % хрома (в шестивалентном состоянии). Получены следующие результаты Аст= = 0,440, Л с=0,200. В литературе имеются указания, что окрашенный продукт реакции довольно точно следует закону Бера, по крайней мере при концентрации 1-10 % хрома. Рассчитайте растворимость хромата бария в граммах на 100 г воды. [c.241]
Отношения, подобные рассмотренным выше, наблюдаются не ТОЛЬКО у сульфидов, но и у других труднорастворимых электролитов. Например, в 32 указывалось, что гидроокиси магния (ПР=5-10" ), марганца (ПР=4-10" ), двухвалентного железа (ПР=4,8-10 ) и т. д. легко растворимы в солях аммония вследствие образования слабого основания NH OH. В то же время Ре(ОН)з (ПР=3,8-10 ), равно как и гидроокиси алюминия и хрома, произведения растворимости которых весьма малы, в солях аммония не растворяются. Этим пользуются в ходе анализа для разделения катионов HI группы на две подгруппы. [c.216]
При применении в качестве окислителя хромпика следует учитывать расход кислоты на перевод калия и хрома в растворимые соли [c.595]
При обработке азокрасителя, содержащего две оксигруппы в орто-положении к азогруппе, солями тяжелых металлов — кобальта, никеля, железа, хрома (последнего в особенности) — образуются комплексные соли, растворимые в спирте, например [c.721]
Чистая винная кислота образует бесцветные кристаллы. В воде растворима. Из ее нейтральных солей (называемых тартратами) легко растворимы соли щелочных металлов—алюминия, железа и хрома, соли же остальных металлов трудно растворимы. Так как винная кислота представляет собой слабую кислоту, то и трудно растворимые соли ее растворяются в сильных кислотах. Кислые виннокислые соли калия и аммония трудно растворимы в воде. [c.273]
Соли алюминия, ванадия, железа, кобальта, марганца, никеля, титана и хрома. Соли алюминия—это кристаллические или аморфные вещества, окрашенные только при окрашенных анионах. Соли двухвалентного железа имеют окраску зеленую или голубоватую, кобальта — темно-розовую и красную, хрома — темно-фиолетовую или темно-зеленую, никеля — зеленую. Многие соли хорошо растворимы в воде, углекислые и фосфорнокислые соли — нерастворимы, а фтористые — мало или вовсе нерастворимы. [c.31]
Большинство солей хрома(III) растворимо в воде. Растворы их в зависимости от условий имеют зеленую или сине-фиолетовую окраску. Для соединений хрома(III) характерно проявление восстановительных свойств. Под действием окислителей они переходят в соединения хрома (VI). [c.195]
Большинство солей трехвалентного хрома хорошо растворимо в воде. Цвет растворов этих солей меняется от фиолетового до зеленого, в зависимости от температуры раствора, концентрации и других условий. Изменение цвета растворов зависит от различной гидратации ионов В кристаллическом состоянии боль- [c.289]
С другой стороны, эффективное действие анионов может быть объяснено тем, что эти ионы в наибольшей степени, по сравнению с анионами N0 , С1 , Вг и Л , адсорбируются гидратами окиси и основными солями хрома и способны давать с трехвалентным хромом хорошо растворимые в воде хромо- [c.58]
Образующаяся соль растворима в щелочи. Ионы алюминия и хрома не мешают анализу. [c.57]
Растворимость солей. Растворимость солей хрома (П1) близка к растворимости солей алюминия. [c.336]
При окончательном обезвоживании сухих солей следует избегать сильного нагревания их (выше 130°), чтобы п е допустить образования труднорастворимых основных солей. Это также имеет особенное значение в случае определения кремния в высокохромистом материале, так как основные соли хрома весьма трудно растворяются в кислотах. При неправильно проведенном выпаривании, кремнекислота может оказаться сильно загрязненной. Чтобы избежать образования основных солей,, рекомендуется добавить перед выпариванием 5 г хлористого аммония, с которым хром дает растворимое комплексное соединение. [c.26]
При этом образуется вулканообразный конус объемистого аморфного оксида хрома (III) зеленого цвета. Изменение степени окисления хрома в растворе сопровождается изменением окраски, что позволяет аналитически определить концентрацию хрома путем добавления раствора восстановителя известной концентрации. Соединения хрома (III) похожи на аналогичные соединения железа (особенно растворимые соли). Сульфат хрома (III) образует квасцы (как алюминий и железо). Хромокалиевые квасцы окраше-.чы в темно-фиолетовый цвет. Соединения хрома (II) — сильные восстановители и неустойчивы в присутствии влаги и воздуха (ср. со свойствами железа (II), с. 157). [c.155]
Весьма важной характеристикой эмульгатора служит его отношение к обеим жидкостям, образующим эмульсию. Вещества, растворимые в воде и нерастворимые в масле, являются хорошими эмульгаторами и стабилизируют эмульсии типа масло в воде. Это олеат натрия и другие соли жирных кислот и щелочных металлов. Наоборот вещества, хорошо растворимые в неполярных жидкостях типа масла и мало растворимые в воде, образуют устойчивые эмульсии типа вода в масле. Это соли жирных кислот и щелочноземельных и тяжелых металлов кальция, цинка, алюминия, магния, железа, хрома и др. Присутствие в углеводородной части молекулы двойных связей усиливает гидрофильные свойства эмульгаторов. В последнее время ценные эмульгаторы получают на основе щелочных солей сульфоновых кислот. [c.81]
Амфотерные свойства гидроксида хрома (П1). К 1 мл раствора соли хрома (И ) по каплям прибавьте раствор аммиака или разбавленный раствор щелочи до образования осадка гидроксида хрома (П1). Осадок разделите на две части, исследуйте его растворимость в растворах кислоты и гидроксида натрия. Каков цвет гидроксида хрома (И ) и продуктов его взаимодействия с кислотой и щелочью Напишите уравнения реакций в молекулярной и ионной формах. [c.150]
Соединения Сг + во многом похожи на соединения алюминия Подобно гидроксиду алюминия Сг(ОН)з амфотерен соли алюминия и хрома имеют близкие растворимости для хрома характерно [c.210]
Опыт 5. Взаимодействие растворов солей хрома (III) и алюминия с растворимыми карбонатами. Налейте в одну пробирку 4— [c.207]
Однако для получения удовлетворительных по качеству осадков хрома необходимо чтобы в электролите содержалось незначительное количество посторонних анионов, например ионов ЗО -Эффективное действие анионов 804" объясняется тем, что эти ионы в наибольшей степени, по сравнению с другими анионами (М0Г,С1 ) адсорбируются гидратами окиси и основными солями хрома и способны давать с трехвалентным хромом хорошо растворимые в воде хромовосерные сложные кислоты, диссоциирующие на ионы [Сг2(Н20) (804)4 -, [Сг2(Н20) (804)5 -, [Сгз(804)в -. Образование таких соединений способствует разрыхлению и растворению пленки. Таким образом, при электролизе устанавливается динамическое равновесие между двумя процессами — образования и растворения пленки. [c.191]
Действительно, хромит калня — растворимое в воде вещество зеленого цвета. Водный раствор хромита калия имеет сильнощелочную реакцию. Калиевые соли окрашивают бесцветное пламя горелки в фиолетовый цвет. Соединения хрома окрашивают перл буры в зеленый цвет. В состав хромита калия никакие анионы, кроме СЮ, и СгО,, не входят. Соединения хрома (111) не выделяют 1а из раствора К1 и обесцвечивают раствор КМПО4 с образованием соединений хрома (VI). [c.452]
Металлы церий, торий, висмут, уран, алюминий, кадмий и железо образуют фосфаты, не растворимые в воде, но растворимые в фосфо рной кислоте. Окись или гидроокись тория или какую-либо соль (растворимую в концентрированной фосфорной киелсте) растворяют в избытке 89—100% фосфорной кислоты (применяемое количество около двухкратного или даже может быть десятикратным), смесь выливают в воду, осажденные фосфаты отфильтровывает под уменьшенным давлением и промывают. Фосфаты могут быть активированы добавкой сурьмы, хрома, кобальта, меди, магния, марганца, никеля, серебра, вольфрама, цинка или олова (фосфаты которых не растворимы в концентрированной фосфорной кислоте) в виде их окисей или фосфатов. Приготовленный таким образом катализатор пригоден для получения формальдегида путем окисления метана воздухом, ацетальдегида из ацетилена и паров воды, формальдегида и ацетальдегида из этилена и кислорода и спирта из этилена и воды. Приготовление уранового катализатора основано на том же принципе. Две части окиси урана, смешанные с одной частью хлористого висмута, растворяют в 102 частях 89% фосфорной кислоты при температуре 160°. После охлаждения смесь выливают в 75 частей воды, осадок декантируют, фильтруют под уменьшенным давлением, промывают и высушивают при 120°. Контактная масса представляет собой высокоактивный пористый катализатор, стабильный при высоких температурах [96]. [c.294]
Крон желтый (ГОСТ 478—63) —сульфохроматы и оксихроматы свинца—пигмент желтого или оранжевого цвета тРЬСг04лРЬ0 НаО и РЬСг04пРЬ04 — получают при взаимодействии водорастворимых солей свинца или глета с моно- или бихроматами щелочных металлов, выпускается следующих марок высокодисперсный желтый, цельный О, крон-1 и крон-2. Соответственно указанным сортам продукт содержит соединений свинца в пересчете на окись свинца не менее 69, 69—80, 68—79, 34—39 и 17—19,5% соединений хрома в пересчете на хромовый ангидрид — 30 13,9—27,8 13,8—27 6,9—13,5 и 3,45—6,75% свинца металлического не более 1,0% солей, растворимых в воде, не более 0,4—0,88% влаги гигроскопической не более [c.221]
Подобные соотношения наблюдаются не только у сульфидов, но и у других трудно растворимых электролитов. Так, например, в 26 уже указывалось, что гидроокиси магния (ПР = 5 10 2) и марганца (ПР — 4 10 ) легко растворимы в аммонийных солях вследствие образования слабого основания Nh5OH. В то же время Ре(ОН)з (ПР = 3,8 10 ), а также гидроокиси алюминия и хрома, произведения растворимости которых весьма малы, в солях аммония не растворяются. [c.134]
Подобные явления наблюдаются не только для сульфидов рассмотренных катионов, но и для других малорастворимых электролитов. Так, в 34 указывалось, что гидроокиси магния (ПР = = 6-10 °), марганца (ПР = 4,5-10 ) двухвалентного железа (ПР = 1 10 ) и т. д. легко растворимы в солях аммония вследствие связывания 0Н в слабое основание Nh5OH. В то же время Ре(ОН)з (ПР = 3,2-10" ), равно как и гидроокиси алюминия и хрома, произведения растворимости которых весьма малы, в солях аммония не растворяются. Этим пользуются в ходе анализа для разделения катионов III группы на две подгруппы. [c.216]
Переведение в растворимое состояние окиси хрома и хромистого железняка 1учше всего производить сплавлением не со смесью соды и поташа, а со смесью равных частей соды и селитры. Таким путем окись хрома благодаря окислительной смеси превращается в хромовокислую соль, растворимую в воде. Сплавление лучше всего производить в платиновом тигле или на платиновой крышке последнего, но можно также пользоваться кварцевым или фарфоровым тиглем,, а для сплавления со смесью соды и поташа можно, 1фоме того, применять также серебряные, никелевые или железные тигли. Следует, однако, принять во внимание, что при всех этих опытах немного вещества тигля переходит в раствор. [c.165]
Действительно, хромит калия — растворимое в воде вещество зеленого цвета. Водный раствор хромита калия имеет сильнощелочную реакцию. Калиевые соли окращивают бесцветное пламя горелки в фиолетовый цвет. Соединения хрома окрашивают перл буры в зеленый цвет. В состав хромита калия никакие анионы, [c.384]
Отношения, подобные рассмотренным выше, наблюдаются не только у сульфидов, но и в других классах соединений. Так, например, в 28 уже указывалось, что гидроокиси Mg (ПР = 5. 10-12), (ПР = 4. 10-14), Fe (ПР = 4,8 10- б) и т. д. легко растворимы в аммолийных солях вследствие образования слабого основания Nh5OH. В то же время Ре(ОН)з (ПР = 3,8 10- ), равно как и гидроокиси алюминия и хрома, произведения растворимости которых весьма малы, в аммонийных солях не растворяются. Этим мы воспользуемся в ходе ана-Л1иза для разделения катионов III группы на две подгруппы. [c.144]
С другой стороны, эффективное действие анионов может быть объяснено тем, что эти ионы в наибольшей степени, по сравнению с анионами С1 , Вг и Л , адсорбируются гидратами окиси и основными солями хрома и способны давать с трехвалентным хромом хорошо растворимые в воде хромовосерные сложные кислоты [22], диссоциирующие на ионы [ r, U,0) S0,),] -, [Сг2(Н,0)(30.2)5]= -, [Сг2(804)б] -. Образование таких соединений способствует растворению пленки и уносу коллоидных гидратов в направлении к аноду в область более низких pH. Учитывая благоприятное действие 80 , необходимо все же иметь в виду, что растворение вязкой пленки из труднорастворимых соединений хрома происходит неравномерно по поверхности катода. Равномерность распределения гидроокиси нарушается также бурным газовыделением, на основании чего можно высказать гипотезу о том, что коллоидные гидраты образуют кочующий передвижной слой, блокирующий отдельные участки поверхности, и таким образом играют роль регуляторов образования зародышей и роста кристаллов в сторону измельчения кристаллической структуры осадка. [c.58]
Соли алюминия и железа, а также хрома в водной среде реакцией обменного разлон ения с натровыми солями нафтеновых кислот образуют только основные соли. Эти соли не растворимы в воде, но набухают в минеральных маслах, сообщая им большую вязкость, имеющую, внрочем, только структурный характер. [c.138]
По Фишеру, прн действии на бензол прн повышенной температуре безводного треххлористого хрома образуется окрашенный в желт1> й цвет катион дибензолхрома [Сг(СбНб)д]+, из которого могут быть получены различные соли. При их восстановлении получается дибензолхром (СсНг,)2Сг, который перегоняется в высоком вакууме при 150° и образует растворимые в бензоле темно-коричневые кристаллы его дипольный момент равен 0. [c.194]
Того же результата можно достигнуть и с амальгамой натрия. Трехвалентная окись хрома СггОз имеет амфотерные свойства. С сильными кислотами образуются соли [СгС1з, Сгг(804)3], хорошо растворимые в воде. [c.516]
Гидроксиды алюминия, хрома (П1) и цинка обладают амфотерными свойствами. В некоторой степени можно говорить и об амфо-терности гидроксида железа (П1) с очень слабо выраженными кислотными свойствами, проявляю[цимися лишь по отношению к концентрированным и горячим растворам ителочей, в которых Р е(ОН)з заметно растворяется с образованием гидроксоферра-тов (П1) натрия или калия. Гидроксиды низшей степени окисления Ре(0Н)2, Мп(ОИ)2, Ni(OH)2 и Со(ОН)2 являются слабыми основаниями, растворимыми в кислотах и в растворах аммониевых солей. [c.259]
chem21.info
Хрома соли - Справочник химика 21
Применяется хром главным образом для выработки нержавеющей стали, для покрытия поверхности стальных изделий (хромирования) с целью придать им коррозионную стойкость. Находят применение также и соединения хрома. Соли хрома используются, например, при хромовом дублении кож. Широко применяются хроматы, или соли хромовой кислоты. Их используют как протраву в текстильной промышленности, для приготовления дубителей, для обработки поверхности металлов с целью повысить их коррозионную устойчивость. В лабораторной практике хроматы используются в качестве окислителей, широко применяетмытья посуды так называемая хромовая смесь . [c.273] Гидролиз солей окиси хрома. Соли окиси хрома в водных растворах в значительной степени гидролизованы. Гидролиз солей окиси хрома, образованных сильными кислотами, сопровождается увеличением концентрации ионов Н+ в растворе и образованием основных солей, например [c.251]Чистая винная кислота образует бесцветные кристаллы. В воде растворима. Из ее нейтральных солей (называемых тартратами) легко растворимы соли щелочных металлов—алюминия, железа и хрома, соли же остальных металлов трудно растворимы. Так как винная кислота представляет собой слабую кислоту, то и трудно растворимые соли ее растворяются в сильных кислотах. Кислые виннокислые соли калия и аммония трудно растворимы в воде. [c.273]
Соли алюминия, ванадия, железа, кобальта, марганца, никеля, титана и хрома. Соли алюминия—это кристаллические или аморфные вещества, окрашенные только при окрашенных анионах. Соли двухвалентного железа имеют окраску зеленую или голубоватую, кобальта — темно-розовую и красную, хрома — темно-фиолетовую или темно-зеленую, никеля — зеленую. Многие соли хорошо растворимы в воде, углекислые и фосфорнокислые соли — нерастворимы, а фтористые — мало или вовсе нерастворимы. [c.31]
Нормальный окислительно-восстановительный потенциал системы Sn +/Sn равен 0,15 в поэтому ион Sn + восстанавливает окислители с большим окислительно-восстановительным потенциалом. Так, хлорид олова (II) восстанавливает ионы Fe до Fe2+, арсенаты до арсенитов, хроматы до солей трехвалентного хрома, соли двухвалентной ртути до солей одновалентной ртути, а последние—до металла. Станниты в щелочном растворе восстанавливают ионы Bi3+ до металла. [c.509]
В больших количествах в капиталистические страны поставлялись традиционные продукты советской химии — хромовые соединения (бихроматы натрия и калия и оксид хрома), соли органических и неорганических кислот, реактивы и т. д. В то же время в списке экспортных товаров закрепился и ряд новых продуктов, среди них — метанол, пластмассы (полиэтилен, полистирол) и мономеры (винилхлорид), полупродукты для анилинокрасочной иромышленности и другие химикаты. В целом продукты с высокой степенью переработки заняли важное место в структуре советского экспорта. [c.131]
В противоположность меди и хрому, соли марганца и никеля, присутствуя в железном электролите, оказывают благоприятное действие на качество железного покрытия. [c.76]
По механизму действия все катализаторы Ота делит на три группы [132]. К первой группе относятся нафтенаты- натрия, магния, бария, двухвалентной ртути и алюминия. Они вызывают незначительное разложение гидроиероксидов и не препятствуют их накоплению. Окисление в присутствии этих катализаторов обычно прекращается на неглубоких стадиях прев раще-ния исходного углеводорода при максимальной скорости (мол.) в 1 ч. Ко второй группе отнесены нафтенаты свинца, серебра, цинка, марганца, никеля, трехвалентното железа, кобальта, хрома. Соли металлов второй группы интенсивно разлагают гидропероксиды с образованием свободных радикалов при этом максимальная скорость окисления достигает 3—4% (мол.) в 1 ч. Нафтенаты калия, ванадия и двухвалентной меди, отнесенные к третьей группе, вызывают интенсивное разложение гидропероксидов и ингибируют 0 кисление [c.37]
Можно ли титровать марганец в присутствии солей алюминия солей хрома солей железа солей кальция в присутствии больших количеств хлоридов [c.383]
Соединения двухвалентного хрома. Соли Сг(П) легко получают восстановлением цинком подкисленных растворов солей r(III) (лучше всего фиолетовых). Соли Сг(П) образуются также при растворении металлического хрома в кислотах. Эти реакции проводят в атмосфере неактивного газа (Нг), так как в присутствии воздуха легко проходит окисление до Сг(П1). [c.643]
Натрий хромовокислый + хрома соли. [c.120]
Хлорный хром. . Соли цинка Хлористый цинк. [c.242]
Дубильные операции проводят для придания коже термо- и водостойкости, а также стойкости к действию различных бактерий и ферментов. Для этого голье обрабатывают различными органическими (папр., таинидами, альдегидами) и неорганическими (нанр., основными солями трехвалентного хрома, солями четырехвалентного циркония) соединениями, т. паз. дубящими веществами, или дубителями. При дублении происходит сшивание макромолекул, располо/кепных на поверхности структурных образований коллагена. Критерием дубления обычпо служит темп-ра сваривания кожи, величина к-рой зависит от вида дубителя и стенени иродубленности. Методы дубления весьма разнообразны. Выбор дубителей и режим дубления определяются видом исходного сырья и пазиачением 1 ожи. [c.526]
Если проследить за изменением основных валентностей катионов Зй-элементов, то вновь вырисовывается любопытная закономерность. У скандия такая валентность равна 3+, у титана 4- - соединения двухвалентного и трехвалентного ванадия, куда элемент входит в виде катионов и V , примерно одинаково устойчивы аналогичную картину наблюдаем и у хрома. Соли двухвалентного марганца (Мп ) устохпивы. Далее основная валентность катионов изменяется следующим образом 3+ у железа, 2+ у кобальта и никеля, 2+ у меди, причем довольно устойчивы и соединения одновалентной меди. Наконец, цинк фактически только двухвалентен. Иными словами, в ряду Зй-элементов основная валентность катионов имеет тенденцию к повышению у элементов после кальция (предшествующего декаде), затем понижается перед марганцем, снова повышается после марганца и опять понижается перед цинком. У редкоземельных элементов изменение валентностей примерно такое же. Таким образом, можно было бы говорить о своеобразной систематике Зй-элементов, которая выражалась бы следующей схемой [c.108]
Хотя окись хрома при накаливании в водороде не изменяется, но в растворах своих солей СгХ она восстановляется сравнительно легко, притом такие восстановители, как 2п с Н 50, переводят в соли закиси СгХ , а такие, как щелочная амальгама натрия, восстановляют даже до металлического хрома. Соли закиси СгХ дают растворы голубого цвета и действуют сами как сильные восстановители, поглощая даже свободный кислород. [c.238]
Чаще всего гены усто Чивости уже меются в хромо-сол ах, но находятся в подавленном — рецессивном со-стояшш. В результате систематического де1 ствия инсектицида на популяцию насекомого происходит отбор — менее устойчивые особи гибнут, усто 1Ч вые выживают. При скрещ вании развивается новая популяция, в кото-ро 1 преобладают особ , носящие ген усто1 Чивост 1. Если [c.179]
Л а в р е н ч у к В. М. О химизме восстаиовления шестивалеитного хрома соля.ми двухвалентного железа. Ученые записки ЦНИИОлово . 1964, ЛЪ 2. [c.104]
Лавренчук В. И. О химизме восстановления шестивалентного хрома солями двухвалентного железа. Ученые записки ЦНИИОлово , 1964, № 2. [c.104]
С целью экономии платины применяют двухстадийное контактирование, при котором аммиак частично окисляется на платиноидных сетках, а затем доокисляется в слое неплатинового зернистого катализатора. В качестве неплатиновых катализаторов применяют различные композиции оксидов или солей, в том числе оксиды железа или хрома, соли кобальта. [c.247]
Трибромид циркония образуется в виде черного порошка, он растворяется в воде с выделением водорода, распадается на ZrBr4 и ZrBra при 350° и иа ZrBr4 и металлический Zr нри 827°, восстанавливает хроматы до соединений трехвалентного хрома, соли трехвалептного железа до двухвалентного, соединения двухвалентной меди до одновалентной, соли четырехвалентного титана до трехвалентного. [c.115]
Технологический процесс крашения шерсти кислотно-протравными красителями с последующим хромированием складывается из двух этапов выбирания красителя из ванны и закрепления окраски на волокне солями комплексообразующего металла, чаще всего хрома. Соли хрома обычно вводятся в красильную ванну после того, как закончено выбирание красителя шерстью, это предотвращает лакообразо-вание в красильной ванне и исключает опасность загрязнения цвета и снижения прочности окраски. [c.8]
chem21.info
Раствор - соль - хром
Раствор - соль - хром
Cтраница 1
Раствор соли хрома ( II) имеет характерную светло-голубую окраску без зеленоватого оттенка. [1]
Растворы солей хрома ( II) и ванадия ( II) неустойчивы и их следует готовить непосредственно перед употреблением. [2]
Растворы солей хрома ( III) - сульфата, хлорида и нитрата равной молярности ( по атомам металла) в первом приближении имеют одинаковое значение рН, однако точные измерения показывают небольшие различия значений рН растворов этих солей. [3]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [4]
Растворы солей хрома ( П) окрашены в небесно-голубой цвет. [5]
Растворы солей хрома ( III) имеют зеленую или фиолетовую окраску, растворы хроматов - желтую, растворы бихроматов - оранжевую окраску. [6]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся, зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [7]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [8]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окра: ки объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [9]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [10]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [11]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова прибретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [12]
Растворы солей хрома окрашены в характерный фиолетовый или зеленый цвет. [13]
Растворы солей хрома ( Ш) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [14]
Растворы солей хрома ( III) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Соли хрома растворы - Справочник химика 21
Амфотерные свойства гидроксида хрома (П1). К 1 мл раствора соли хрома (И ) по каплям прибавьте раствор аммиака или разбавленный раствор щелочи до образования осадка гидроксида хрома (П1). Осадок разделите на две части, исследуйте его растворимость в растворах кислоты и гидроксида натрия. Каков цвет гидроксида хрома (И ) и продуктов его взаимодействия с кислотой и щелочью Напишите уравнения реакций в молекулярной и ионной формах. [c.150] В результате взаимодействия избытка раствора гидроксида натрия иа раствор соли хрома (П1) образуется раствор хромита натрия. Разделите его поровну в две пробирки. В одну пробирку добавьте раствор пероксида водорода и нагрейте его до изменения зеленого цвета хромита в желтый цвет хромата натрия. В другую пробирку прилейте бромной воды и раствор нагрейте до образования желтого цвета раствора. При неполном окислении хромита натрия к раствору добавьте еще бромной воды и опять нагрейте. Напишите уравнения реакций в молекулярной и ионной формах. [c.151]Метод замещения. Этот метод применяют тогда, когда по тем или иным причинам трудно определить точку эквивалентности, например при работе с неустойчивыми веществами и т. п. Так, при определении Сг +, который легко окисляется кислородом воздуха и кото )ый прп непосредственном титровании окислителем определить трудно, поступают следующим образом к определенному объему соли хрома(II) прибавляют избыток титрованного раствора соли железа (III), происходит реакция [c.199]
Растворы солей хрома (III) обычно имеют сине-фиолетовым цвет, но при нагревания становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. В некоторых случаях такие гидраты удалось выделить в твердом виде. Так, кристаллогидрат хлорида хрома (JII) r ls- HjO известен в трех изомерных формах в виде сине-фиолетовых, темно-зеленых н светло-зеленых кристаллов одинакового состава. Строение тих изомеров можно установить на основании различного отношения их свежеприготовленных растворов к нитрату серебра. При действии последнего на раствор сине-фиолетового [c.655]
Гидролиз солей хрома (П1). I. В пробирку внесите несколько кристаллов соли хрома (П1) и растворите их в воде. Чему равняется pH полученного раствора Напишите уравнения реакций гидролиза в молекулярной и ионной формах. Могут ли при гидролизе солей хрома (П1) образовываться многоядерные гидроксо-аквакомплексы и каково их строение [c.150]
Опустить проволоку с перлом в пробирку с раствором соли кобальта Со(ЫОз)г или соли хрома Сг(ЫО)з. Наблюдать окрашивание перла в синий или зеленый цвет в зависимости от природы взятой соли. Составить уравнения реакций [c.74]
При- растворении Сг(ОН)з в кислотах образуются соли хрома, растворы которых окрашены в зеленовато-фиолетовый цвет [c.276]
Реактивы. Соли хрома (//), раствор В капельницу наливают приблизительно 0,5 AI раствор хлорида хрома (III) в 1 и. соляной кислоте, прибавляют [c.1071]
Особенности хромового покрытия. Хромовое покрытие стойко против действия большинства газов, щелочей, растворов кислот и солей хром растворяется в горячей серной и азотной кислотах. Блеск и цвет хромового покрытия не изменяются от воздействия атмосферы. При нагревании твердость хро.мового покрытия уменьшается. При температуре нагрева от 200 до 600° С уменьшение твердости происходит медленно, а при температуре свыше 600° С — очень быстро. Для появления цветов побежалости критической температурой является 450° С. При нагреве до температуры, близкой к 450° С, хромовое покрытие начинает менять цвет. С точки зрения противокоррозийной защиты хром как электроотрицательный металл в принципе защищает железо от ржавления. Но поскольку на воздухе хром пассивируется (на покрытии образуется тонкая пленка окиси хрома), то его электроотрицательные и защитные свойства снижаются. Это относится только к тонким пористым хромовым покрытиям. [c.164]
Хроматы и дихроматы— сильные окислители. Поэтому ими широко пользуются для окисления различных веществ. Окисление производится в кислом растворе и обычно сопровонсдается резким изменением окраски (дихроматы окрашены в оранжевый цвет, а соли хрома(И1)—в зеленый или зеленовато-фиолетовый). [c.657]
Соли хрома (HI) во многом похожи на соли алюминия. В водных растворах они сильно гидролизованы и легко превращаются в основные соли. Со слабыми кислотами хром (ИI), подобно алюминию, солей не образует. [c.655]
К 5—7 каплям раствора сульфата хрома (III), подкисленного разбавленной серной кислотой, добавьте 1—2 капли раствора нитрата серебра (катализатор), нагрейте пробирку и внесите несколько кристаллов пероксодисуль-фата аммония или калия и опять нагрейте. Наблюдаемый переход зеленой окраски соли хрома (III) в оранжевую обусловлен окислением последнего [c.138]
По этой схеме взаимного усиления гидролиза, приводящего к образованию основания и кислоты, взаимодействуют соли железа (П1) и хрома (1П) с карбонатами щелочных металлов, соли алюминия и хрома с сульфидом аммония, алюминаты с солями аммония, растворы которых имеют кислую реакцию, и некоторые другие. [c.139]
НИ присутствие в растворе небольших количеств солей хрома(111). [c.200]
Выполнение определения. Для приготовления эталонных растворов в пять мерных колб вместимостью 50 мл вводят по 20 мл воды, стандартный раствор соли хрома(VI) с содержанием хрома (мг) 0,01 [c.62]
Применение двухвалентного хрома в качестве восстановителя имеет тот недостаток, что растворы солей хрома (двух- и трехвалентного) довольно сильно окрашены поэтому трудно определить полноту восстановления железа, а также точку эквивалентности при титровании железа. [c.367]
На существование пленки основных солей хрома указывают два обстоятельства структура осадка электролитического хрома имеет слоистый характер, который наблюдается при осаждении металлов из растворов, содержащих добавки адсорбирующихся коллоидов вращение катода заметно снижает выход по току (см. рис. 248). Это вызвано тем, что тонкий слой католита, образующегося на поверхно сти катода, смывается трением катода б раствор и отбрасывается центробежной силой. [c.532]
Теоретическая сторона разряда ионов Сг + и Сг + в растворах простых солей рассмотрена в 3. В данном случае примет няют растворы с высоким содержанием аммонийных солей. Соли хрома должны быть предельно чисты в отношении содержания в них примесей более электроположительных металлов. Содержание в растворе ионов железа благоприятствует повышению [c.536]
Титрование растворами соединений Сг(И). Стандартный окислительно-восстановительный потенциал системы Сг(П)/ y r(III) Ео —0,41 В. Растворы солей хрома(II) имеют более сильные восстановительные свойства, чем растворы солей титана (III), и дают возможность проводить ряд важных определе-лий обычно с использованием потенциометрической индикации конечной точки титрования. [c.178]
Техническое осуществление электролиза растворов аммонийно-сульфатных солей хрома возможно в ваннах, используемых для электролитического получения марганца (см. рис. 235). [c.537]
Кроме того, в электролитическом хроме содержится до 0,020% азота. Повышенное содержание железа объясняется специальными добавками его солей в раствор. Обращает на себя внимание значительное содержание, водорода и кислорода (в форме основных солей и гидрата окиси хрома). Как будет показано ниже, водород и кислород легко удаляются при плавке или прокаливании в водороде и вакууме. Что же касается азота, являющегося наиболее нежелательной примесью, ради которой необходима высшая очистка хрома, то его удаление весьма затруднительно. [c.538]
После охлаждения реакционной смеси в нее вливают 120 мл воды и вновь охлаждают. Выделившуюся нитробензойную кислоту отфильтровывают на воронке Бюхнера, промьшают водой. Для удаления солей хрома сырую нитробензойную кислоту растворяют в 5%-ном растворе едкого натра осадок гидроокиси хрома отфильтровывают и к фильтрату, содержащему натриевую соль п-нитробензой-ной кислоты, добавляют при перемешивании концентрированную серную кислоту до кислой реакции по конго. При этом выпадает желтый кристаллический осадок п-нитробензойной кислоты, который отфильтровывают и тщательно промывают водой. [c.143]
Соли хрома (П), окрашенные в водных растворах, как правило, в голубой цвет, весьма чувствительны к кислороду и обладают сильным восстановительным действием [c.618]
Для следующих опытов используют раствор соли хрома(III). [c.622]
III) и его свойства. В пробирку с 5—6 каплями раствора соли хрома (III) прилить по каплям разбавленный [c.97]
В две пробирки налейте по 1 мл раствора соли хрома (П1). В первую пробирку прилейте такой же объем раствора сульфида щелочного металла или аммония, а во вто- [c.150]
В небольшой фарфоровый тигель возьмите три микрошпателя ( 0,3 г) соды, приблизительно столько же по объему пероксида натрия и несколько растертых в порошок кристаллов соли хрома (П1) (на кончике микрошпателя). Смесь тщательно перемешайте стеклянной палочкой, поставьте в фарфоровый треугольник и нагрейте на пламени горелки до сплавления смеси (плав вспенивается из-за выделения СО2). Плав охладите, прибавьте 1 —1,5 мл воды, перемешайте и слейте раствор в пробирку. Обратите внимание на окраску раствора, обусловленную наличием в растворе ионов СгО . [c.265]
В начале титрования раствор имеет желтую окраску, а к концу титрования - вблизи точки эквивалентности - титруемый раствор становится грязно-зеленым вследствие наличия в нем смеси хинона и солей хрома(1П). Массовую долю (%) гидрохинона в анализируемом веществе находят по формуле [c.123]
В трехгорлую колбу вместимостью 250 мл, снабженную мешалкой, обратным холодильником и капельной воронкой, помещают 90 мл воды, дихромат натрия и tt-нитрото-луол. При перемешивании из капельной воронки прибавляют в течение 20 мин концентрированную серную кислоту. Происходит разогревание, при котором п-нитротолуол плавится и начинается энергичная реакция. Ход реакции окисления регулируют скоростью прибавления серной кислоты (избегают бурного кипения). После прибавления всей серной кислоты и прекращения саморазогревания реакционной смеси содержимое колбы нагревают при слабом кипении в течение 30 мин. Охладив реакционную смесь, в колбу вливают 120 мл воды и снова охлаждают. Выделившуюся 4-нитробензойную кислоту отфильтровывают и промывают водой (50 мл). Для удаления солей хрома кислоту растворяют в 100 мл 5%-ного раствора гидроксида натрия. Осадок гидроксида хрома удаляют фильтрованием, а к фильтрату при перемешивании добавляют концентрированную серную кислоту до кислой реакции (по конго красному). Выпавшие желтые кристаллы 4-нитробензойной кислоты отфильтровывают, тщательно промывают водой и сушат на воздухе. Продукт очищают перекристаллизацией из водного спирта. Т, пл. 242 С. Выход около 10 г (66 %). [c.101]
Ход анализа. Навеску ОЛ г борида хрома растворяют в 50 мл серной кислоты (1 4) в стакане емкостью 250 мл, накрытом часовым стеклом. После прекращения растворения осторожно добавляют 2—3 мл азотной кислоты, нагревают до выделения паров серной кислоты, давая им выделяться в течение 2—3 мин (длительное выделение паров серной кислоты п . иводит к выпадению нерастворимых солей хрома). Раствор охлаждают, разбавляют водой до 200 мл, нагревают и переносят в колбу емкостью 500 мл. Прибавляют 5 мл раствора нитрата серебра, 20—25 мл раствора персульфата аммония, нагревают до кипячения и кипятят до полного разложения персульфата аммония. Затем раствор охлаждают н титруют раствором соли Мора в присутствии фенилантраниловой кислоты. [c.183]
При крашении с последующим хромированием шерсть сначала окрашивают кислотным красителем, способным образовать хромовые комплексы, как описано выше, и затем подвергают хромироваг нию в той же ванне, после полного ее истощения. Ванна должна быть сначала охлаждена не менее чем до 70 °С, так как в противном случае может произойти неравномерное хромирование и окисление шерсти. Для хромирования применяют бихромат натрия, хроматы или трехфтористый хром. Комплексы с красителем способен образовывать только трехвалентный хром, и поэтому бихромат и хроматы должны быть сначала восстановлены. В процессе последующего хромирования восстановление происходит за счет самой шерсти, в то время как в других случаях приходится применять органические кислоты, обладающие восстановительным действием. Количество соли хрома зависит от требующейся глубины тона и обычно равно половине количества взятого красителя. Во всяком случае, берут не меньше 0,1% и не больше 3% хромата (от массы материала). После добавления соли хрома раствор в ванне снова доводят до кипения и проводят хромирование при кипении в течение 45—60 мин. Затем материал тщательно прополаскивают и сушат обычным способом. [c.61]
Pt I Сг Сг " — электрод. Этот электрод состоит из инертного электрода, онущенного в смесь 25 мл 0,1 М раствора хромата калия К.2СГО4 и 5 мл 0,001 М раствора хромовых квасцов. В случае помутнения (выпадение основных солей хрома) подкисляют полученную смесь одной-двумя каплями концентрированной серной кислоты. [c.305]
Для исследования были выбраны соли хрома, марганца, меди, цинка (первый переходный период), циркония и молибдена (второй переходный период). Приготовленные бензольные растворы пиридина А хинолина с известной концентрацией ( 0,2% азота) или дизельное топливо (0,024 % основного азота 0,04% общего азота) пропускались через слой исследуемой соли, помещенной в колонку диаметром 10 мм при комнатной температуре. Время обработки составляло 4 ч. Соотношение количества соли и раствора составляло 1 (по весу) с той целью, чтобы различие в свойствах солей были более отчетливы. Концентрация растворов определялась потенциометрически, как описано в [19], после промывки растворов горячей дистиллированной водой и осушки поташом в течение суток. Достоверность результатов была проверена сравнением данных, полученных по методу Кьельдаля и потенциометрического титрования. Было установлено, что присутствие следов металлов в титруемом растворе не влияет на положение точки эквивалентности. Таким образом была определена степень удаления азота из бензольных растворов пиридина и хинолина солями железа — хлорным, хлористым, азотнокислым окисным, ферри-цианидсм калия и хлористым цинком. Результаты приведены в табл. 1. [c.110]
Прокопчик [42] изучал действие многих добавок на активность катализаторов. Гидроокись железа теряет свои каталитические свойства в присутствии избытка твердой (нера-створенной) гидроокиси кальция в растворе. Интенсивное ингибирующее действие оказывает двуокись кремния. Действие катализаторов подавляется также присутствием солей хрома, мышьяка, свинца. [c.13]
Крашение шерсти напоминает процессы, протекающие в ионообменных смолах. Кератин шерсти, образующий за счет остатков цистина сетчатую структуру, является цвиттерионом. В качестве основания он обладает эквивалентным весом 1200 и окрашивается в уксуснокислом растворе красителями, имеющими кислотные группы. В результате двойного обмена соли шерсти с натриевой солью сульфо-кислотного красителя последний связывается в виде соли и в процессе крашения примерно при 90° медленно диффундирует в шерстяное волокно. Небольшие молекулы красителя, например моноазосоединения или производные аминоантрахинона с одной сульфогруппой в молекуле, дают очень ровные выкраски по шерсти соединения с двумя сульфо-группами закрепляются сильнее и поэтому более прочны к стирке (суп-раноловые или полярные красители), но зато дают менее ровные выкраски. Большое значение для крашения шерсти имеет, кроме того, способность некоторых красителей (см. стр. 608) образовывать с солями хрома комплексные соединения, очень прочные к стирке и свету. [c.600]
Из раствора с концентрацией соли хрома (III) 0,01 моль/л осаждение начинается при pH 5,0. При дальнейшем добавлении гидроксида щелочного металла при pH 13—14 начинается растворение осадка r20з aq с образованием Сг(0Н)4] и [Сг(ОН)б] ". В избытке аммиака r20з aq также растворяется, причем хром частично переходит в комплексный ион 1Сг(ЫНз)б +. [c.618]
Немного фиолетовой соли хрома (III) растворяют на холоду в небольшом количестве воды. В фиолетовом растворе присутствует кислотноосновной комплекс Сг[(Н20)аР+. При нагревании раствор становится темнозеленым вследствие образования ацидоаквакомплекса (гидратная изомерия). [c.622]
К раствору соли хрома(III) добавляют раствор (Nh5)2S происходит протолитическое осаждение> Сг(ОН)а ( raOj-aq) [c.622]
К раствору соли хрома(III) добавляют смесь растворов NaOH и Н2О2. Наблюдается желтое окрашивание [c.622]
К раствору соли хрома(1П), подкисленному разб. h3SO4, добавляют немного твердого пероксодисульфата калия и раствор короткое время кипятят. Вследствие образования иона дихромата раствор окрашивается в оранжевый цвет [c.623]
К 0,5 мл раствора ацетата натрия прибавьте 0,5 мл раствора хлорида хрома (II). Выпадает красный осадок дигидрата ацетата хрома (II) Сг(СНзС00)2-2Н20. Полученное соединение является одним из самых устойчивых солей хрома (II). [c.149]
К 0,5 мл раствора соли хрома (П1) добавьте несколько капель разбавленной серной кислоты и небольшими порциями прибавьте раствор пероксоднсульфата аммония до перехода зеленой окраски в оранжевую (содержимое пробирки можно подогреть). Напишите уравнение реакции окисления хрома (И1) в хром (VI). [c.151]
chem21.info
Мора соль хрома - Справочник химика 21
Так, комплексы с железом (в ф-ле Я = Я = = Н, М = Ре, 2 = Ка, 2з-пл = 2 или 3) имеют зеленый цвет (соотв. пигмент зеленый или кислотный зеленый), с хромом (М = Сг, и = = 3)-оливковый, с кобальтом (М = Со, и = 3)-красио-коричневый, с никелем (М = N1, 2 = Ка, и = 2) и вдгнком (М = 2п, 2 = Ка, и = 2)-желтый разных оттенков. Наиб, практич. значение имеют комплексы с Ре (2 = Ка) пигмент зеленый, к-рый применяют в лакокрасочной и полиграфич. пром-сти, в произ-ве цветных карандашей, для крашения резин, пластмасс, обоев кислотный зеленый 4Ж (К = ЗОзКа, К = Н), используемый для крашения шерсти и шелка нитрозол А (Я = Н, К = СбНдКНСО), пригодный для крашения белого портландцемента в яркий зеленый цвет, устойчивый к действию света и воды. Водные р-ры кислотного зеленого 4Ж даже при разведении 1 300 ООО настолько интенсивно поглощают световые лучи красной видимой и ближней ИК частей спектра, преобразуя их в теплоту, что заметно ускоряется испарение воды под действием солнечных лучей. Благодаря этому ев-ву краситель используют для извлечения солей из воды морей и соленых озер. [c.273] Объем стандартного раствора соли Мора (СГ ), затраченный в этом титровании, соответствует суммарному содержанию марганца, хрома и ванадия в аликвотной части испытуемого раствора. [c.185]Обратное титрование. Например, при титриметрическом определении содержания хрома в хромовых рудах и концентратах, содержащих >0,05 %V (см. Хром ), содержание оксида хрома (Xi %) вычисляют по формуле X =(VK—V )T lOO/ G, в которой V—объем раствора соли Мора, взятый для анализа, мл К — поправочный коэффициент или соотношение объемов растворов перманганата калия и соли Мора Vi — объем раствора перманганата калия, израсходованный яа титрование избытка раствора соли Мора, мл Ti — титр 0,1 н. раствора перманганата калия, выраженный в граммах оксида хрома в 1 мл раствора G — навеска руды или концентрата, г. [c.32]
Одновременно в другой стакан такой же емкости, одинаковый с первым по диаметру и цвету стекла, приливаю, из бюретки 25 мл раствора соли Мора и, если в анализируемой стали присутствует хром, вводят бихромат калия до получения одинаковой окраски с анализируемым раствором. Затем в оба стакана добавляют по 15 мл серной кислоты (1 4), 5 мл раствора роданида калия и 15 мл раствора хлорида олова, после чего хорошо перемешивают растворы в обоих стаканах. При этом окраска анализируемого раствора из интенсивной кроваво-красной должна перейти в оранжево-красную, контрольная же проба должна остаться бесцветной или слегка окрашенной в зеленый цвет солями хрома. Ставят оба стакана рядом на лист белой бумаги и по каплям прибавляют в контрольную пробу титрованный раствор молибдена, все время перемешивая раствор до тех пор, пока интенсивности окраски жидкости в обоих стаканах станут одинаковыми. Если потребуется, объем жидкости в обоих стаканах уравнивают путем прибавления воды. [c.79]
Помимо соли Мора титровать хром (VI) можно другими восстановителями ферроцианидом калия (см. Ванадий ) и иодидом калия (см. Ванадий и Марганец ). [c.291]
Потенциометрическое титрование марганца, хрома и ванадия широко применяют при анализе сплавов, минералов, руд и прочих технически важных материалов, после разложения которых определяемые компоненты, как правило, переходят в раствор в степенях окисления марганец(П), хром(III), ванадий(V) и частично(1У). Определение основано на титровании стандартным раствором соли Мора после переведения их в высшую степень окисления. [c.132]
Для точного титрования смеси компонентов берут новую порцию испытуемого раствора и выполняют все операции, указанные в п. 1. Титрование проводят, прибавляя титрант в области к. т. т. порциями по две капли. Объем титрованного раствора соли Мора (Vi), затраченного на титрование, соответствует суммарному содержанию хрома и ванадия или марганца и ванадия. [c.133]
В присутствии ванадия результаты титрования дают сумму хрома и ванадия. В этом случае определяют отдельно ванадий и вычитают из общего объема раствора соли Мора, израсходованного на титрование обоих элементов, тот объем, который соответствует определенному количеству ванадия. [c.190]
Расчет аликвоты и приготовление раствора для анализа. Рассчитывают концентрацию хрома в растворе, взятом для титрования, исходя из того, что на титрование 5 мл его должно пойти от 1 до 4 мл раствора титранта (0,01М раствор соли Мора). Учитывая полученный результат, рассчитывают, во сколько раз следует разбавить исходный раствор электролита (см. рецептуру), чтобы получить раствор для титрования. При этом разбавление может быть однократным или многократным. В соответствии с расчетом готовят один или несколько разбавленных растворов исходного электролита. Разбавление ведут водой, добавляя в последний разбавленный раствор 10 мл 0,5М раствора h3SO4. Для приготовления разбавленных растворов используют пипетки и мерные колбы, а раствор исходного электролита отбирают с помощью резиновой груши. [c.278]
Для отдельных сортов сталей методику несколько видоизменяют. Если в растворе присутствуют шестивалентный хром и пятивалентный ванадий, то прибавляют около 2 г соли Мора перед осаждением молибдена а-бензоиноксимом. Хром и ванадий восстанавливаются соответственно до трех- и четырехвалентного состояния и не осаждаются а-бензоиноксимом. [c.235]
Полученный раствор охлаждают, приливают 300— 350 мл воды и перемешивают. Затем приливают 1 мл раствора сульфата марганца, 10 мл раствора нитрата серебра или 10 мл раствора кобальто-никелевого катализатора, 25 мл раствора персульфата аммония и нагревают до появления малиновой окраски, что указывает на полное окисление хрома. Раствор кг,пятят 12—15 мин (до пре-краш,ения выделения пузырьков кислорода), прибавляют к нему 10 мл раствора хлорида натрия и снова кипятят до исчезновения малиновой окраски. После этого раствор охлаждают, приливают к нему 25 мл разбавленной Г. 1 серной кислоты. Раствор вновь охлаждают, вводят 5—6 капель фенилантраниловой кислоты и титруЮт раствором соли Мора до перехода вишневой окраски раствора в зеленую. [c.65]
Для руд и концентратов, содержащих >0,05%У, анализ проводят так же, как и в рассмотренном выше случае до момента исчезновения малиновой окраски раствора. Затем раствор охлаждают и приливают к нему раствор соли Мора до изменения желтой окраски на зеленую, после чего вводят 5—6 мл избытка соли Мора, который оттитровывают раствором перманганата калия до появления розовой окраски, устойчивой в течение 1—2 мин. 1 мл 0,1 н. соли Мора соответствует 1,7332 мг хрома 1 мл 0,1 н. перманганата калия соответствует 1,7332 мг хрома. [c.65]
Смесь Эшке Соль Мора. ... Соль Рейиеке Сурьмы (V) хлорид Сурьмы (III) хлорид Титана (III) сульфат Титана (III) хлорид Фосфора (V) оксид Хрома (II) хлорид. [c.3]
После остывания смеси в колбе пипеткой Мора по каплям добавляют 3—10 мл дистиллята (в зависимости от содержания в нем алкоголя) при взбалтывании После этого колбу оставляют на 15 мин при комнатной температуре, затем накрывают часовым стеклом и 10 мин нагревают на горелке или спиртовке, избегая бурного кипения. Смесь количественно с 250 мл переносят в колбу Эрленмейера емкостью 500 мл, прибавляют 2—2,5 г KI, предварительно растворенного в небольшом количестве воды. Колбу закрывают часовым стеклом и оставляют на 2—3 мин. Выделившийся иод титруют 0,1 н. раствором NajSjOs при добавлении 1 мл 1%-ного раствора крахмала. Оттитрованный раствор часто бывает окрашен в голубовато-зеленый цвет вследствие присутствия солей хрома. Если на титрование затрачивается менее 6— [c.199]
Для анализа стали на содержание хрома навеску 1,017 г растворили и окислили. На восстановление получившейся хромовой кислоты взяли 40,00 см раствора соли Мора. На титрование избытка восстановителя израсходовали 5,02 см раствора перманганата калия 0(1/5 КМПО4) = 0,02394 моль/дм . 10,00 см раствора соли Мора эквивалентны 9,63 см раствора КМПО4. Определить массовую долю хрома в образце. [c.83]
Ход анализа. Навеску ОЛ г борида хрома растворяют в 50 мл серной кислоты (1 4) в стакане емкостью 250 мл, накрытом часовым стеклом. После прекращения растворения осторожно добавляют 2—3 мл азотной кислоты, нагревают до выделения паров серной кислоты, давая им выделяться в течение 2—3 мин (длительное выделение паров серной кислоты п . иводит к выпадению нерастворимых солей хрома). Раствор охлаждают, разбавляют водой до 200 мл, нагревают и переносят в колбу емкостью 500 мл. Прибавляют 5 мл раствора нитрата серебра, 20—25 мл раствора персульфата аммония, нагревают до кипячения и кипятят до полного разложения персульфата аммония. Затем раствор охлаждают н титруют раствором соли Мора в присутствии фенилантраниловой кислоты. [c.183]
В результате реакции в растворе появляется количество ионов Ре +, эквивалентное количеству СиС1 в исходной пробе. Окислители титруют по остатку. Например, хром в сталях окисляют до СггО , добавляют избыток титрованного раствора соли Мора Ре(КН4)2(504)2-6Н20 и не вошедшее в реакцию количество оттитровывают дихроматом. [c.286]
Сущность работы. Хроматный электролит представляет собой щелочной раствор СгОз, в котором хром находится в виде хромата. Определение последнего основано на тифовании раствора солью Мора с амперомефической индикацией точки эквивалентности. [c.277]
Титрование исследуемого раствора. Пипеткой отбирают 5 мл наиболее разбавленного кислого раствора электролита, приготовленного по п. 2, помещают его в стакан для титрования, добавляют 5 мл раствора К2804, включают мешалку и титруют так, как это делали при стандартизации раствора соли Мора (см. п. 3). Строят кривую титрования, находят объем титранта в точке эквивалентности и рассчитывают концентрацию хрома в электролите (г/л), учитывая все произведенные разбавления. [c.279]
После растворения 1,2430 г стали хром окислили до СгО . К раствору прибавили 35,00 мл раствора соли Мора и избыток Fe + оттитровали 16,12 мл раствора КМп04 (Т кмпо. = 0,001510 25,00 мл раствора соли Мора эквивалентны 24,10 мл раствора КМПО4). Рассчитать процентное содержание Сг в стали. [c.121]
Приборы и реактивы. Водяная баня. Капельная пипетка. Хлорид кобальта (шестиводный). Хлорид хрома (шестиводный). Соль Мора. Лакмусовая бумага красная. Амиловый спирт. Олово гранулированное. Цинк гранулированный. Растворы хлороводородной кислоты (2 и.) серной кислоты (2 и.) щавелевон [c.120]
Рассчитать процентное содержание хрома встали по следующим данным. После растворения 1,050 г анализируемой стали хром был окислен до СгО . Затем к раствору прибавили 25,00 мл раствора соли Мора — (Nh5)2pe(S04)2-6h30 и избыток Ре2+ оттитровали [c.121]
Разработан метод определения марганца, хрома и ванадия при их совместном присутствии [98]. Суш ность метода состоит в последовательном титровании раствором соли Мора суммы марганца, хрома и ванадия, окисленных до Mn(VII), r(VI) и V(V) персульфатом аммония в присутствии ионов Ag(I), затем суммы r(VI) и V(V) после разрушения МпО добавлением в раствор Na l и титровании одного V(V) после окисления его КМПО4. Все три этапа титрования проводят при постоянном потенциале + 1,0 S (нас. к.э.) с платиновым анодом, враш аюш имся со скоростью 800—1000 об1мин. Метод применяют при анализе сталей [158, 236, 658-660]. [c.51]
Определению молибдена в сталях три помощи а-бензоиноксима ие мешает 0,4% мышьяка [760]. 1 г (МЫшьяксодержащей стали растворяют в серной кислоте, затем прибавляют азотную кислоту для окисления, нагревают с добавлением серной кислоты до Появления густых белых паров. После растворения солей в воде восстанавливают пятивалентный ванадий и шестивалентный хром добавлением раствора соли Мора, смесь охлаждают до температуры ниже -1-10° С, прибавляют раствор а-бензоиноксима, бромную воду и фкльтро-бумажную массу. Осадок отфильтровывают, прокаливают я взвешивают МоОз. Последний растворяют в водно1М аммиаке, раствор фильтруют, осадок озоляют, вычитают вес остатка из веса осадка. При определении 0,73% Мо в сталях, содержащих 0,4% Ав, получены удовлетворительные результаты. [c.124]
Персульфатно-серебрян ый метод с применением фенилантраниловой кислоты. Определение основано на окислении хрома до дихромат-иона в сернокислой среде (1,8 н.) персульфатом аммония в присутствии натрата серебра (катализатор). Дихромат-ион оттитровывают 0,1 н. раствором соли Мора в присутствии индикатора фенилантраниловой кислоты. [c.339]
Определение хрома в сталях и хромовых сп.павах проводят методом обратного титрования избытка раствора соли Мора раствором КМПО4 до появления устойчивой бледно-розовой окраски [823]. Показана возможность определения V (V), r(VI) и e(IV) в их двух- и трехкомпонентиых смесях [1062]. Избыток ионов Fe(II) титруют раствором e(S04)2 в 7,0—8,5 М СН3СООН в присутствии индикатора ферроина. [c.32]
Определение r(VI) и V(V) при совместном присутствии проводят в 6,5 М НдР04- Титруют 0,05 или 0,1 7V раствором соли Мора [75]. Первый скачок потенциала соответствует концу восстановления r(VI) до Сг(1П) и V(V) до V(IV), второй — концу восстановления V(1V) до V(III). Мешает определениюMo(VI). u(Il) в количестве 0,2 г затрудняет быстрое установление равновесного потенциала. Максимальное количество определяедгого хрома равно 0,01 г. Метод применяют при анализе сплавов. Погрешность определения не превышает 10% [75]. [c.35]
Мп(П) и У(1У) [20, 160] их окисляют в сернокислой среде с по-мощ ью (N114)28208 в присутствии Ag(I) и оттитровывают раствором соли Мора. Затем снова добавляют персульфат аммония избыток его разрушают кипячением. Мп(УП) восстанавливают до Мп (II) хлоридом натрия или NaN02 в присутствии мочевины и титруют Сг(У1) и У(У) раствором соли Мора. Ионы У(1 ) окисляют с помощью КМпО при температуре не выше 20° С избыток последнего восстанавливают как описано выше, и титруют ионы У( ) раствором соли Мора. Содержание Сг и Мп определяют по разности. Электродом сравнения служит вращающийся Р1-электрод в сернокислом растворе КМПО4 в качестве индикаторного электрода используют вращающийся Р1-электрод [160]. Определение Мп, Сг и V в силикатных породах проводят методом амперометрического титрования с двумя индикаторными электродами [20], а для определения Сг и V в шлаках используют установку с вращающимся Р1-электродом [72]. Предел обнаружения хрома при анализе горных пород — 0,01 мг в 20 мл. Погрешность определения сотых долей процента хрома +15%. [c.37]
Разработан атомно-абсорбционный метод определения хрома и других элементов с предварительным их обогаш ением путем соосаждения с 8-оксихинолинатом кадмия в присутствии органических комплексообразующих веществ [789]. Микроколичества хрома в природных водах определяются после концентрирования Сг04 на анионите AG-1X4 и элюирования раствором, содержащим 30 мл i М Na l ж iO мл 0,5 М раствора соли Мора в 1 М НС1 [945]. Анализ фосфатных горных пород на содержание хрома проводится с предварительным отделением мешающих примесей на катионите Дауэкс-50 WX8 в Na -форме [803]. Сг(1П) окисляют до r(VI) раствор подщелачивают до pH 12 и пропускают через колонку. [c.94]
Хром (VI) титруют раствором соли Мора (N1 4)2 [Fe (304)2] в присутствии в качестве индикатора фенилантраниловой кислоты. При содержании 0,05 %V хром восстанавливают раствором соли Мора и его избыток титруют раствором перманганата калия. Метод применим при содержании 10—65 7оСг в пробе. Относительное стандартное отклонение результатов определений 0,015 при содержании 10—65% хрома. [c.63]
Титр раствора соли Мора (Г), выраженный в граммах оксида хрома, вычисляют по формуле 7 = 0,1226-0,5166/1 , в которой 0,1226 — масса дихромата калия, содержащаяся в 25 мл раствора, взятого для установления титра, г 0,5166 — ко.эффициеит пересчета дихромата калия на оксид хрома У — объем 0,1 н. раствора соли Мора, израсходованный на титрование, мл. [c.64]
Весовой метод основан на отделении осадка молибдена с а-бен-зоиноксимом Комплекс осаждают из холодного раствора серной кислоты (1 20), но допускаются и большие концентрации кислоты (1 4). Для предотвращения восстановления пятивалентного молибдена в раствор добавляют небольшой избыток брома. Для полного перевода хрома и ванадия соответственно в трех- и четырехвалентное состояние в раствор добавляют также соль Мора, так как эти элементы в более высоких валентных состояниях мешают анализу. [c.64]
В первом методе определение ванадия или хрома завершается титрованием раствора стандартным раствором соли Мора с дифенил-аминосульфонатом " . [c.106]
Второй метод аналогичен первому до стадии разложения нитрита. К раствору приливают измеренное количество стандартного раствора срли Мора для перевода хрома и ванадия соответственно в трех-и четырехвалентное состояние. Затем избыток соли Мора оттитро-вывается стандартным раствором перманганата калия, окисляюш,им также ванадий до пятивашентного состояния, и определяют содержание хрома в пробе. [c.106]
chem21.info