Братья железа (кобальт, никель, хром и др.). Хром кобальт
Штифтовая культевая вкладка хром-кобальт
В стоматологии установка зубной коронки может производиться на штифт и на специальную вкладку под коронку, которую так и называют — штифтовая культевая вкладка. Предназначение таких элементов заключается в возможности восстановить слишком тонкие или даже полностью разрушенные стенки зуба. После того как зуб будет восстановлен с помощью вкладки, на него устанавливается коронка, крепление которой обеспечивается специальным цементным составом.
Штифтовая культевая вкладка – это специально изготовленное по индивидуальному слепку зубопротезное изделие, которое имеет 2 части (корневую и коронковую). Корневая фиксируется в канале разрушенного зуба, а верхняя часть устанавливается под коронку вместо культи зуба.
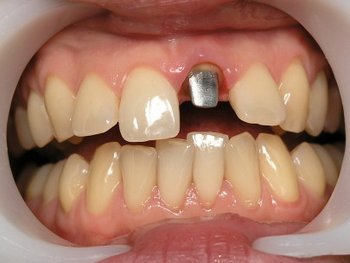
Штифтовые культевые вкладки изготовливаются индивидуально под каждый зуб, с учетом строения и толщины корней зуба.
Материалом для штифтовой культевой вкладки может быть металл (кобальто-хромовый сплав), золото, керамика и д.р.
Для достижения желаемого результата крайне важно, чтобы материал, из которого будет изготавливаться вкладка, отвечал следующим требованиям:
- должен быть твердым, но при этом упругим;
- иметь низкий коэффициент теплопроводности;
- обладать свойством биоинертности;
- обеспечивать качественное сцепление с литьем.
Говоря о преимуществах таких конструкций, нужно отметить их надежность, долговечность и практичность. За счет того, что такая вкладка располагается в каждом корневом канале — многоканальные культевые вкладки, она обеспечивает равномерную нагрузку, а использование цементного состава гарантирует прочность крепления и герметичность, тем самым предотвращая возможность образования просветов, в которых могла бы застревать пища. Такой зуб не имеет гарантийного срока.
Хром-кобальтовая культевая вкладка - это цельная или разборная конструкция из кобальтохромового сплава, которая ставится на зубной корень и служит основой для коронки. Перед установкой культевой вкладки проводится эндодонтическое лечение, в ходе которого врач тщательно пломбирует каналы зуба и подготавливает протезное ложе. Затем вкладка фиксируется стоматологическим цементом, после чего устанавливается постоянная коронка.
Хром-кобальт – это сплав широко используется в стоматологии для изготовления протезов и имплантатов. Он не окисляется под воздействием пищи и слюны, не теряет цвет, биосовместим. Из кобальтохромового сплава возможно изготовление максимально точных слепков зубов.
stomatology.me
Сплавы неблагородных металлов
Кобальт-хромовые сплавыСо — Сг сплавы впервые в стоматологической практике начали использоваться в 30-х годах, и с этого времени они успешно заменяют золотосодержащие сплавы IV типа при изготовлении каркасов частичных зубных протезов, прежде всего благодаря их относительно низкой стоимости, что является существенным фактором при изготовлении таких больших отливок.
Состав
Сплав содержит кобальт (55 — 65%) и хром (до 30%). Другие основные легирующие элементы — молибден (4 — 5%) и реже титан (5%) (Таблица 3.3.6). Кобальт и хром формируют твердый раствор с содержанием хрома до 30%, что является пределом растворимости хрома в кобальте; избыток хрома образует вторую хрупкую фазу.
В целом, чем выше содержание хрома, тем устойчивее сплав к коррозии. Поэтому производители стараются максимально увеличить количество хрома, не допуская образования второй хрупкой фазы. Молибден вводят для образования мелкозернистой структуры материала путем создания большего количества центров кристаллизации во время процесса затвердевания. Это имеет дополнительное преимущество, так как молибден вместе с железом дают существенное упрочнение твердого раствора. Тем не менее, зерна имеют довольно большие размеры, хотя их границы очень трудно определить из-за грубой дендритной структуры сплава.
Углерод, присутствующий только в небольших количествах, является чрезвычайно важным компонентом сплава, поскольку незначительные изменения в его количественном содержании могут существенно изменить прочность, твердость и пластичность сплава. Углерод может сочетаться с любым другим легирующим элементом с образованием карбидов. Тонкий слой карбидов в структуре может значительно повысить прочность и твердость сплава. Однако, слишком большое количество карбидов может привести к чрезмерной хрупкости сплава. Это представляет проблему для зубного техника, которому необходимо гарантировать, что во время плавки и литья сплав не абсорбировал излишнее количество углерода. Распределение карбидов также зависит от температуры литья и степени охлаждения, т.к. единичные кристаллы карбидов по границам зерен лучше, чем их сплошной слой вокруг зерна.
Свойства
Для зубного техника работа с этими сплавами труднее, чем с золотосодержащими сплавами, поскольку перед литьем, их нужно нагреть до очень высоких температур. Температура литья этих сплавов в пределах 1500-1550°С, а связанная с ней литейная усадка равна примерно 2%.
Эту проблему в основном решили с появлением оборудования для индукционного литья и огнеупорных формовочных материалов на фосфатной основе.
Точность отливки страдает при таких высоких температурах, что значительно ограничивает использование этих сплавов, в основном для изготовления частичных зубных протезов.
Эти сплавы трудно полировать обычным механическим способом из-за их высокой твердости. Для внутренних поверхностей протезов, непосредственно прилегающих к тканям полости рта, применяется метод электролитической полировки, чтобы не снизить качество прилегания протеза, но внешние поверхности приходится полировать механическим способом. Преимущество такого способа в том, что чисто отполированная поверхность сохраняется более длительное время, что является существенным достоинством для съемных зубных протезов.
Недостаток пластичности, усугубляемый включениями углерода, представляет собой особую проблему, и в частности потому, что эти сплавы склонны к образованию пор при литье. При сочетании эти недостатки могут приводить к поломкам кламмеров съемных протезов.
Тем не менее, существует несколько свойств этих сплавов, которые делают их почти идеальными для изготовления каркасов частичных зубных протезов. Модуль упругости Со — Сг сплава обычно равен 250 ГПа, в то время как для сплавов, рассмотренных ра нее, этот показатель находится в диапазоне 70 — 100 ГПа. Такой высокий модуль упругости имеет преимущество в том, что протез, и особенно плечи кламмера, могут быть изготовлены с более тонким поперечным сечением, сохраняя при этом необходимую жесткость.
Сочетание такого высокого показателя модуля упругости с плотностью, которая приблизительно вполовину ниже, чем у золотосодержащих сплавов, значительно облегчают вес отливок. Это, несомненно, большое преимущество для комфортности пациента. Добавление хрома обеспечивает получение коррозионностойких сплавов, которые применяют для изготовления многих имплантатов, включая бедренные и коленные суставы. Поэтому можно с уверенностью утверждать, что эти сплавы обладают высокой степенью биосовместимости.
Некоторые сплавы также содержат никель, который добавляют производители при получении сплава ш усиления вязкости и снижения твердости. Однако никель известный аллерген, и его применение может вызывать аллергические реакции слизистой полости рта.
Титановые сплавы
Интерес к титану с точки зрения использования его при изготовлении съемных и несъемных зубных протезов появился одновременно с внедрением титано
вых стоматологических имплантатов. Титан обладает целым рядом уникальных свойств, в том числе высокой прочностью при низкой плотности и биосовместимостью. Кроме того, предполагали, что, если для изготовления коронок и мостовидных протезов, опирающихся на титановые имплантаты, использовать другой металл, а не титан, это может привести к гальваническому эффекту.
Открытие элемента титана связывают с именем Reverend William Gregor в 1790, но первый образец чистого титана был получен лишь в 1910 году. Чистый титан получают из титановой руды (например, рутила) в присутствии углерода или хлора. Полученный в результате нагревания TiCl4 восстанавливается расплавленным натрием с образованием титановой губки, которая затем плавится в условиях вакуума или в среде аргона для получения заготовки (слитка) металла.
Состав
В клиническом аспекте наибольший интерес представляют две формы титана. Это технически чистая форма титана и сплав титана — 6% алюминий — 4% ванадий.
Технически чистый титан
Титан — металл, склонный к аллотропическим или полиморфным превращениям, с гексагональной плотноупакованной структурой (а) при низких температурах и структурой ОЦК (Р) при температуре выше 882С. Чистый титан фактически является сплавом титана с кислородом (до 0,5%). Кислород находится в растворе, так что металл является единственной кристаллической фазой. Такие элементы, как кислород, азот и углерод обладают большей растворимостью в гексагональной плотноупакованной структуре а-фазы, чем в кубической структуре 3-фазы. Эти элементы формируют промежуточные твердые растворы с титаном и способствуют стабилизации а-фазы. Такие элементы, как молибден, ниобий и ванадий, выступают в качестве Р-стабилизаторов.
Сплав титан - 6% алюминий - 4% ванадий
При добавлении к титану алюминия и ванадия в небольших количествах, прочность сплава становится выше, чем у чистого титана Ti. Считается, что алюминий является а-стабилизатором, а ванадий выступает в качестве В-стабилизатора. Когда их добавляют к титану, температура, при которой происходит переход гх—Р, понижается настолько, что обе и формы могут существовать при комнатной температуре. Таким образом, Ti — 6% Al — 4% V имеет двухфазную структуру а— и 3-зерен.
Свойства
Чистый титан это белый блестящий металл, который обладает низкой плотностью, высокой прочностью и коррозионной стойкостью. Он пластичный и является легирующим элементом для многих других металлов. Сплавы титана широко применяются в авиационной промышленности и в военной области благодаря высокой прочности на разрыв (-500 МПа) и способности выдерживать воздействие высоких температур. Модуль упругости чистого титана тех.ч.Т равен ПО ГПа, т.е. вдвое ниже модуля упругости нержавеющей стали и кобальт-хромового сплава.
Свойства при растяжении чистого титана Tex.4.Ti в значительной степени зависят от содержания кислорода, и хотя предел прочности при растяжении, показатель постоянной деформации и твердость увеличиваются с повышением концентрации кислорода, все это происходит за счет снижения пластичности металла.
Путем легирования титана алюминием и ванадием возможно получение широкого спектра механических свойств сплава, превосходящих свойства технически чистого титана тех.ч.Тг Такие сплавы титана являются смесью а— и Р-фаз, где ос-фаза относительно мягкая и пластичная, а Р-фаза жестче и тверже, хотя и обладает некоторой пластичностью. Таким образом, меняя относительные пропорции фаз можно получить большое разнообразие механических свойств.
Для сплава Ti — 6% Al —4% V можно добиться более высокой прочности при растяжении (-1030 МПа), чем для чистого титана, что расширяет область применения сплава, в том числе при воздействии больших нагрузок, например, при изготовлении частичных зубных протезов.
Важным свойством титановых сплавов является их усталостная прочность. Как чистый титан тех.ч.Т1, так и сплав Ti — 6% Al — 4%V имеют четко определенный предел усталости с кривой S — N (напряжение — число циклов), выравнивающейся после 10 — 10 циклов знакопеременного напряжения, величина которого устанавливается на 40-50% ниже предела прочности на растяжение. Таким образом, тех. ч. Ti не следует применять в случаях, где требуется усталостная прочность выше 175 МПа. Наоборот, для сплава Ti — 6% Al — 4% V этот показатель составляет примерно 450 МПа.
Как известно, коррозия металла является основной причиной разрушения протеза, а также возникновения аллергических реакций у пациентов под воздействием выделяющихся токсичных компонентов. Титан стал широко использоваться именно потому, что это один из самых устойчивых к коррозии металлов. В полной мере эти качества можно отнести и к его сплавам. Титан обладает высокой реакционной способностью, что является в данном случае его сильной стороной, поскольку оксид, образующийся на поверхности (ТЮ2), чрезвычайно стабилен, и он оказывает пассивирующий эффект на весь остальной металл. Высокая устойчивость титана к коррозии в биологической области применения хорошо изучена и подтверждена многими исследованиями.
Литье титановых сплавов представляет серьезную технологическую проблему. Титан имеет высокую температуру плавления (~1670°С), что затрудняет компенсацию усадки отливки при охлаждении. В связи с высокой реакционной способностью металла, литье необходимо выполнять в условиях вакуума или в инертной среде, что требует использования специального оборудования. Другая проблема заключается в том в том, что расплав имеет тенденцию вступать в реакцию с литейной формой из огнеупорного формовочного материала, образуя слой окалины на поверхности отливки, что снижает качество прилегания протеза. При конструировании протезов, опирающихся на имплантаты (супраструктуры) следует выдерживать очень жесткий допуск для получения хорошего прилегания к имплантату. В противном случае можно нарушить ретенцию имплантата в кости. В титановых отливках также часто можно наблюдать внутреннюю пористость. Поэтому используются и другие технологии для изготовления зубных протезов из титана, например, такие как CAD/САМ-технологии в сочетании с прокаткой и методом искровой эрозии.
Некоторые свойства сплавов неблагородных металлов, рассмотренных выше, представлены в Таблице 3.3.7.

Выводы
В настоящее время в стоматологии используется множество различных сплавов. Для того чтобы сделать рациональный выбор из существующего многообразия сплавов с высоким содержанием золота или друга типов сплавов, врачу-стоматологу, как никогда раньше, необходимо обладать знаниями о природе сплавов, их физических и механических свойствах.
Стоимость сплава является существенной частьюв сумме затрат на протезирование. Однако, недорогие сплавы, как правило, требуют дополнительных расходов на изготовление протезов и в конечном итоге меньшая стоимость сплава часто нивелируется повышенной стоимостью производства протеза. Важно также отметить, что высокое содержание золота в сплаве открывает большую возможность изготовления высококачественного зубного протеза.
Клиническое значение
Полную ответственность за выбор материалов для изготовления зубных протезов несет врач-стоматолог, а не зубной техник.
Основы стоматологического материаловедения Ричард ван Нурт
medbe.ru
chrome-cobalt — с английского на русский
CHROME — Le chrome (symbole Cr, numéro atomique 24) est un métal placé en tête de la colonne VIa de la classification périodique; il appartient donc à la première famille des éléments de transition. Il a de nombreuses analogies avec le molybdène, le… … Encyclopédie Universelle
Cobalt-chrome — disc with dental bridges and crowns manufactured using WorkNC Dental Cobalt chrome (Co Cr) is a metal alloy of cobalt and chromium. Cobalt chrome has a very high specific strength and is commonly used in gas t … Wikipedia
Cobalt (Maladie Professionnelle) — Cet article décrit les critères administratifs pour qu une intoxication au cobalt soit reconnue comme maladie professionnelle. Ce sujet relève du domaine de la législation sur la protection sociale et a un caractère davantage juridique que… … Wikipédia en Français
Chrome Affections Respiratoires (Maladie Professionnelle) — Cet article décrit les critères administratifs pour qu une affection respiratoire due au chrome soit reconnue comme maladie professionnelle. Cet article relève du domaine de la législation sur la protection sociale et a un caractère davantage… … Wikipédia en Français
Chrome (Maladie Professionnelle) — Cet article décrit les critères administratifs pour qu une intoxication au chrome soit reconnue comme maladie professionnelle. Cet article relève du domaine de la législation sur la protection sociale et a un caractère davantage juridique que… … Wikipédia en Français
Chrome Cancers (Maladie Professionnelle) — Cet article décrit les critères administratifs pour qu une intoxication au chrome soit reconnue comme maladie professionnelle. Cet article relève du domaine de la législation sur la protection sociale et a un caractère davantage juridique que… … Wikipédia en Français
Cobalt (maladie professionnelle) — Cet article décrit les critères administratifs pour qu une intoxication au cobalt soit reconnue comme maladie professionnelle. Ce sujet relève du domaine de la législation sur la protection sociale et a un caractère davantage juridique que… … Wikipédia en Français
Chrome affections respiratoires (maladie professionnelle) — Cet article décrit les critères administratifs pour qu une affection respiratoire due au chrome soit reconnue comme maladie professionnelle. Cet article relève du domaine de la législation sur la protection sociale et a un caractère davantage… … Wikipédia en Français
Chrome (maladie professionnelle) — Pour les articles homonymes, voir Chrome (homonymie). Cet article décrit les critères administratifs pour qu une intoxication au chrome soit reconnue comme maladie professionnelle. Cet article relève du domaine de la législation sur la protection … Wikipédia en Français
Chrome cancers (maladie professionnelle) — Cet article décrit les critères administratifs pour qu une intoxication au chrome soit reconnue comme maladie professionnelle. Cet article relève du domaine de la législation sur la protection sociale et a un caractère davantage juridique que… … Wikipédia en Français
Chevrolet Cobalt SS — Manufacturer General Motors Model years 2005–2010 Assembly … Wikipedia
translate.academic.ru
Братья железа (кобальт, никель, хром и др.)
Из нашей повседневной жизни мы знаем, что наряду с семью основными металлами существует ряд других металлов. У этих металлов, таких как кобальт, никель, хром, марганец и т.д. бросается в глаза, прежде всего, их родство с железом. Прежде всего, месторождения всех их находятся рядом с железом. Многие железные руды, прежде всего, так называемые блеклые руды, почти всегда содержат те или иные или несколько из этих побочных металлов. Для химиков нелегко бывает идентифицировать эти металлы в смесях, ввиду их близкого химического родства.
Продолжение ниже ⇓Металлы
... совершенно новом свете и проявляет вещи в их важных отношениях между собой. Так, сначала с этой стороны можно приблизиться к особому характеру металлов и их отношению к другим субстанциям Земли. Когда мы находим где-нибудь кусок горного хрусталя, или кальцита, или мрамора, или другой ...Читать дальше...
всё на эту тему
При рассмотрении больших различий между металлами вообще и так называемыми неметаллами или землями, уже указывалось на периодическую систему, в которой для металлов вообще нет правильного места. Особенно для металлов VIII группы, к которым, по большей части, принадлежат и эти побочные, родственные железу металлы; они стоят изолированно и без связи со всей системой рядом друг с другом. Также последовательность никеля и кобальта, например, определена неоднозначно, поскольку оба имеют один и тот же атомный вес. Периодическая система, без сомнения, приобрела бы большую наглядность и реальность, если исключить ряды металлических элементов, как показано ниже. Таким образом, одиннадцать рядов периодической системы превратились бы в семь, а восемь групп — в семь.
В этом рассмотрении из металлов остаются только мышьяк, сурьма и висмут в группе V периодической системы, вещества, занимающие промежуточное положение между металлами и неметаллами, и все-таки по своим свойствам близкие V группе.
Взаимопринадлежность металлов железной группы документируется одинаковыми или подобными отношениями части этих металлов к магнетизму. Так же, как железо, ведут себя в магнитном поле кобальт и никель.
Подобным же образом характеризуется отношение всех черных металлов к земному веществу. Все они, как и железо, образуют с земным веществом твердые и хрупкие карбиды, которые растворяются в расплавленном металле. При легировании стали достаточно совсем небольших добавок побочных металлов, чтобы получить сорта стали со специальными качествами твердости, вязкости, упругости. Хромистая сталь, никелевая сталь, вольфрамовая сталь и так далее сегодня и неспециалисту известны как материалы, которые обладают самыми высокими свойствами стали.
Металлы железной группы поддаются обработке как железо. Они ковки и обладают литейными качествами. По блеску и звуку они мало отличаются от железа. В особенности они обладают одинаковой проводимостью для тепла и электричества.
Почему у железа столько братьев? Было показано, что железные силы с мировой периферии направлены к центру и что они являются носителями уплотнения в земном бытии. Всегда и повсюду мы имеем процесс Марса как носитель инкарнационной силы на Земле. В правремена, когда Земля еще не была твердым телом, существовала более тесная связь между Землей и Марсом. В таком случае можно было бы предположить, что субстанция Марса осталась на Земле в своей праформе – например, при пересечении орбит. Эта марсианская субстанция, которую, конечно, можно представлять не в материальной форме, но в сверхматериальном состоянии, и которую мы назвали процессом железа, подверглась бы всем влияниям земных сил, так что могли бы произойти преобразования по различным направлениям.
Какого рода были эти преобразования, можно изучить по обликам братьев железа, которые сегодня представляют собой продукты этих варьирующих сил.
Кобальт
При изучении кобальта складывается впечатление, что это железо с оттенком еще более сильной земной природы. Кроме того, что он реагирует магнетически как железо, образует карбиды с земным веществом (углеродом) и в прочих химических реакциях показывает характер железа, многие его другие феномены обнаруживают более сильную связь с Землей.
Руды, а также его соли тингированы темным, меланхолическим элементом – сине-фиолетовым. Кобальт показывает еще меньшую связь с водой, чем железо. Красные водосодержащие соли кобальта уже на сухом воздухе благодаря отдаче воды становятся темно-голубыми. На этом основано использование раствора кобальтовой соли в качестве симпатических чернил. Вначале невидимые строки письма становятся при нагревании темно-синими. Кобальтовая соль используется также как датчик влажности, она принимает тем более темный оттенок синего цвета, чем суше атмосфера.
Если в своих солях кобальт кажется подвижнее, как металл он более устойчив, чем железо, Поэтому его применяют для покрытия железных изделий в виде тонкого слоя, например, гальваническим методом.
Откуда взялся кобальт? В первобытные времена Земля была еще мало материальным телом, но полная подвижной брезжащей жизни. Эта в известной степени бестелесная жизнь переживалась в прежние времена как многообразный и пестрый мир природных духов. Греческая и, прежде всего, германо-кельтская мифология заполнена образами природных сил, которые властвуют за видимыми природными фактами. Немецкие сказки, например, это не просто примитивный материал для забавы маленьких детей, но образно представленные процессы; они ведут нас в мир гномов (Kobolde), русалок (Nickelmanner), сильфов (духов воздуха) и саламандр (духов огня), мир, представленный в образах подвижной природной духовности.
Сегодня мы склонны эти сказочные образы относить к царству фантазии или, в лучшем случае, рассматривать как персонификацию природных сил. Но разве, по крайней мере, не настолько же логично предположить обратное: природные силы являются проявлением этих природных духовных существ. Люди, живущие в тесном контакте с природой, как пастухи, крестьяне и лесники, особенно в северных странах, где в одиночестве интимная связь с природой и сердечная наивность еще могут существовать, не нарушаемые такими достижениями цивилизации, как радио и кино, убеждались неоднократно в реальности этих сказочных обликов. Шахтеры и металлурги средневековья, имевшие дело с обработкой железных руд, знали природу этих побочных металлов, которые при выплавке железа часто вызывали их злость и разочарование. В простоте своей – или мудрости! – они связывали это, как с причиной, с деятельностью кобольдов и русалок и дали им соответствующие наименования.
То есть кобальт означает, собственно говоря, кобольд. Кобольды, именем которых назван металл, известны также как гномы или земные духи, описываются всегда в связи с землей и недрами земли. Они работают в рудных жилах, собирают драгоценные камни и металлы, рубят скалы и подготавливают землю для растений, в корнях которых они действуют. Они описываются как очень разумные, способные все рассчитать и исчислить. Они нередко доставляют страдания и мучения людям, но часто им помогают. Их характер меланхоличен, и трогательно их стремление к светлому дню. Как велика бывает их радость, например, по поводу красного кафтанчика.
Так мы находим кобальт как родственный железу металл, тингированный темным меланхолическим оттенком и связанный с землей сильнее, чем само железо. Его можно рассматривать как преувеличенно железную субстанцию.
Никель
Металл никель представляется как железо, которое отклонилось более на русалочную сторону, то есть особенно тингировано водными существами. Уже блеск никеля содержит в себе элемент, напоминающий зеркальную поверхность водоема.
Соли никеля пронизаны великолепным водно-зеленым глубоким цветом. Как соли меди, они содержат большое количество кристаллической воды и легко растворяются в красивую зеленую жидкость, напоминающую глубокие альпийские озера.
Влияние медной природы сказывается также в образовании комплексных солей: если на раствор соли никеля подействовать аммиаком, то получится зеленый осадок гидроокиси никеля, который при избытке аммиака снова растворяется с голубой, цвета сапфира, окраской. Конечно, и некоторые другие братья железа дают подобные комплексные соли, но именно у никеля феномен так впечатляющ великолепием красок, что непосредственно напоминает характер Венеры. Кроме того, никель так же хорошо поддается растяжению, как медь.
Никель заимствует свое наименование от водных духов, русалок (Nickelmannern), которые называются также ундинами. Они описаны как духи – хранительницы рек, озер, прудов и источников. Они движутся и живут в зелени растений и регулируют растительные процессы в природе.
С другой стороны, никель – это все-таки истинный железный металл; он, как и железо, обладает магнитной чувствительностью. Как и железо, он растворяет в себе земное вещество (углерод) и образует карбиды. Последние, легируя железо, служат основой для никелевой стали, которая, благодаря своей вязкости, используется для производства орудийных стволов и других устройств, испытываемых на вязкость. Никелевая сталь, таким образом, не столько твердая, сколько вязкая. Она растягивается в длину почти вдвое без разрыва.
Как у кобальта, так и у никеля, по сравнению с железом, наблюдается более сильное сопротивление воздействию химических агентов. Посредством никелирования железных изделий получаем относительно стойкую против воздействия среды поверхность. Это свойство становится тем более выраженным, чем более мы продвигаемся в группе железных металлов.
В том же направлении идет процесс гидрогенизации жира посредством никеля. При этом совершается превращение жидких масел в твердые жиры, проходящее при воздействии измельченного никеля, причем сам никель в реакцию не вступает, но просто передает реагентам химическую энергию, оставаясь вещественно неповрежденным. Такой процесс называется каталитическим, а вызывающее его вещество катализатором. Также и это свойство усиливается по мере продвижения от никеля через хром и марганец до платины.
Общим образом никеля является образ марсианской субстанции, которая хотя и посредством водных духов – слуг Венеры – сохраняет свойства меди и свободную химическую живость, то есть способность к катализу, но как железный металл стоит одной ступенью ниже в своем уплотнении.
Хром
Также нельзя отрицать железную природу хрома. В руде он всегда связан с железом. Важнейшей рудой является хромистый железняк.
Хром, как и железо, растворяет углерод и образует с ним карбиды. При легировании им железа получается знаменитая хромистая сталь, известная своей особой твердостью, следовательно, он стоит еще на ступень ниже в части склеротизации.
Но сильнее, чем у железа, у хрома, с другой стороны, выражены юпитериальные свойства, то есть он проявляет определенные свойства олова. Было описано, как олово организует свет и воздух и как в процессе этой деятельности начаровывает цвета, где бы они ни содержались. Поэтому олово применяется для травления при окраске шелковых и шерстяных тканей. Такой же способностью обладает хром. То, что у железа лишь намечено в этом направлении, у хрома развертывается полностью. Травление хромом играет важную роль в мареновом или ализариновом крашении. Если получаемые при этом цвета имеют более темный оттенок, чем при использовании олова, то это вполне понятно, поскольку хром как железный металл пронизан земными свойствами железа. По этой же причине у хрома мы находим фиксированный цвет его солей (желтый крон, красный крон и т.д.)
Как кобальт может рассматриваться как результат действия земных духов на железо, и никель – как земная субстанция, тинтированная духами воды, так в хроме мы можем увидеть железо, преобразованное деятельностью духов, действующих в воздушном элементе. В сагах и мифах эти духи названы сильфами или эльфами. Там описано, как они живут в ветре и в воздушных потоках, которые образуются при полете птиц. В духе античности царственный орел, пробиваясь через пронизанные светом облака, как птица Юпитера, приближается к трону своего господина. Как водные существа сродни действующим в воде силам Венеры, так воздушные духи или эльфы являются слугами Юпитера.
Характерным свойством хрома является его дубильная способность. Дубление было представлено как процесс мумификации, и ускоренные методы дубления с применением хрома показывают повышенную склонность к атрофическим состояниям.
Эта сторона хрома представляется вначале противоречащей легкости воздушных сил, живущих в птичьем полете. Но этот контраст мы можем заметить также у самой птицы: ведь у птицы эти склеротические процессы приближаются к высшей точке, когда она одновременно овладевает свободными воздушными силами. Например, нога птицы вряд ли является чем-то большим, чем кожа и кости, и весь организм птицы склеротичен. Всю птицу мы можем сравнить с тем, что у человека является головным процессом. Птица – это головное животное, у которого процесс обмена веществ и конечностей – всего лишь некий вид придатка. Как голова человека за счет вегетативных процессов имеет способность сознания, так и птица – свою способность к пению и полету.
Хром, в химическом смысле, еще более атрофирован, чем никель и кобальт, то есть он еще меньше поддается воздействиям химических и атмосферных агентов, чем они. Поэтому для защиты от вредных воздействий поверхности металлических изделий хромируются.
Марганец
Марганец – это древний magnesium nigrum Плиния. Этим названием он, вероятно, указывал на огненную природу марганца. Помимо железных свойств, марганец постоянно сопровождает железо в его рудах, имеет те же отношения к земному веществу и образует очень твердые марганцевые стали – он целым рядом замечательных свойств демонстрирует свою огненную природу.
Соли его имеют окраску от розово-красной до огненно-фиолетовой. Пиролюзит, часто встречающаяся в природе двуокись марганца, в тонкой дисперсии, приводит к воспламенению паров спирта и эфира. Эта двуокись марганца, являющаяся в виде пиролюзита самой важной и наиболее распространенной марганцевой рудой, играет важную роль в производстве стекла. Окрашенное и нечистое стекло посредством сплавления с тонко распыленным пиролюзитом становится светлым и прозрачным, как будто бы через него действует очищающая сила огня. Название «пиролюзит» означает «очищающий огонь».
Пиролюзит по внешнему виду полностью склеротичный — он выглядит как отожженный шлак, – с другой стороны, проявляющий огненную силу, демонстрирует тем самым сатурническую природу.
Склеротическую тенденцию марганца можно проиллюстрировать следующим интересным феноменом. Для получения масляных красок применяется льняное масло, поскольку оно постепенно осмоляется и образует твердую пленку. Оно названо поэтому высыхающим маслом. Сюда же относится маковое масло, служащее для производства более тонких масляных красок для живописи. Высыхание поверхности, покрытой масляной краской, если она получена с применением простого льняного масла, длится недели и даже месяцы. Но если сюда добавить марганец в виде солей жирных кислот, то процесс высыхания ускоряется до дней и даже часов. Эти соединения марганца названы поэтому сиккативами. Обработанные таким образом поверхности приобретают особенно теплый оттенок.
Такую склонность к высыханию при одновременном развертывании тепловых качеств в животном мире находим мы в царстве насекомых. Они склеротизированы в высшей мере. Пчелы, осы, шершни или какие-нибудь жуки, полностью высохшие в своих формах, одновременно имеют особые отношения к тепловым свойствам атмосферы, природы и растений. Пчелы сродни цветам, осы – более плодам. И все эти части растения представляют собой результат кульминации космических тепловых процессов. Кроме того, скрытый огонь содержится, в более резкой форме, в яде их жала.
За всеми этими огненными процессами в природе древние видели действие огненных духов. В сказках и сагах они связывались с процессами цветения, созревания и плодоношения, или с гостеприимным огнем домашнего очага, они как бы касаются своими огненными пальцами такой отвердевшей субстанции, как марганец.
Вольфрам
По мере того как мы продвигаемся по семейству железа, мы встречаем металлы, которые проявляют все более отверждающие свойства. Вольфрам, например, в этом смысле, с недавнего времени стал играть значительную роль в стальной индустрии. Когда он легирует железо, он делает его твердым до такой степени, что получаемая сталь приобретает почти твердость алмаза. Эту твердость она не теряет – в отличие от обычной стали – при нагревании до степени красного каления. Поэтому она оказывается незаменимой в производстве инструмента для обработки стальных изделий. Благодаря этим свойствам вольфрамовая сталь получила название «благородной стали».
В том же направлении вольфрам обладает кислотоупорными свойствами. Вольфрам не поддается действию даже «царской водки». Это производит впечатление, как если бы вольфрам был своего рода благородным металлом.
Вольфрам при накаливании испускает красивый белый свет и, поскольку он стоек к химическим превращениям, он уже много лет применяется для производства нитей накала в лампах.
Ванадий
Железная природа ванадия видна из многих свойств этого металла. Он постоянно сопровождает железные руды, в особенности в бобовых железных рудах он всегда присутствует в небольших количествах. Примечательно, что его находят также в составе многих сельскохозяйственных почв и в пепле виноградных кустов и дуба.
Ванадий, как и железо, имеет связи с земным веществом (углеродом) и образует с ним серебристо-белые карбиды.
Подобно вольфраму, легируя железо, он дает ванадиевую сталь, по своей твердости приближающуюся к алмазу. Она также применяется для изготовления инструмента и причисляется к высококачественным сталям.
Платина
Платина заимствует свое название от испанского слова «плата», то есть серебро. Действительно, платина может рассматриваться как омертвевшее железо с оттенком серебряных свойств. Когда платина застывает, она образует изъеденную поверхность, как серебро; в расплавленном состоянии она абсорбирует воздух, который в момент застывания снова выделяет. Самым выдающимся свойством платины являются ее неподверженность воздействию химических агентов и ее действие в качестве катализатора.
Тот, кто работал с платиновыми сосудами, например, нагревал субстанции в платиновом тигле, помнит, как тщательно нужно оберегать его от светящегося, т.е. углеродсодержащего газового пламени. В светящемся пламени тигель может стать ломким и хрупким. Причиной этого является соединение расплавленного металла с земным веществом (углеродом). И это, за исключением разъедания «царской водкой», единственно возможное химическое соединение платины. Это карбидное образование следует расценивать всего лишь слабую реминисценцию железа.
Платина – это самый выдающийся катализатор, катализатор по своей сущности. Один из известнейших в технике примеров ее применения – это контактный способ в производстве серной кислоты. Сера, сгорая, превращается в двуокись серы, и для того, чтобы далее окислить ее до трехокиси серы, ангидрида серной кислоты, требовались громоздкие и исключительно сложные процессы и установки, как, например, камерный способ получения серной кислоты. С того времени, как узнали каталитическое действие платины, ее стали использовать в тонко распыленном состоянии в качестве контактной субстанции, с помощью которой окисление в триоксид серы проходит легко и быстро, причем сама платина не вступает в реакцию.
Следующая реакция, на которую платина воздействует как катализатор, это реакция между огненным веществом (водородом) и жизненным веществом (кислородом). Реакция ускоряется так, что происходит самовозгорание. Те, кто помнит еще эпоху горелок Ауэра, помнят запальники, которые надевались на стеклянные цилиндры. На них была в минимальных количествах нанесены распыленная платина, и вытекающая газовая смесь, при соприкосновении с ней, возгоралась сама собой.
Также многие другие реакции, особенно в органической химии, вызываются и ускоряются платиной как катализатором.
Поскольку в платине мы имеем каталитическое действие в наивысшей степени, попытаемся понять существо катализа.
Уже говорилось, что никель, когда он действует как катализатор при гидрогенизации жиров, не участвует в химическом процессе как активное вещество, но просто передает химическую энергию, излучаемую, так сказать, самой субстанцией никеля. Это излучение сопровождается склеротическими явлениями в самом веществе.
Весь процесс станет более прозрачным и понятным, если рассматривать подобную же ситуацию в высших природных царствах. Там это полярное развитие можно сравнить с нервным процессом. Нерв имеет постоянную склонность к склеротизации; он находится в состоянии непрерывного отмирания, и, как следствие этого, происходит высвобождение связанной с ним, хотя и слабо, жизни. Это излучение бестелесных сил является базой чувственной и мыслительной жизни. В этом отношении нерв полярно противоположен крови, в которой жизнь действует со всей полнотой и участвует во всех органических, субстанциально-физиологических процессах и превращениях нашего физического тела. Этот процесс отмирания отражается также в животном царстве, как уже было это описано у птиц и насекомых. Чем более физическое тело животного в определенном смысле кажется атрофичным или склеротичным, тем больше высвобождается соответствующей данному виду интеллектуальной силы. Эти способности исходят не от отдельной особи животного, но от всего вида, к которому оно принадлежит. Этот удивительный интеллект господствует, например, в полете перелетных птиц, этот интеллект проявляется в организации жизни муравейника и пчелиной семьи! Никто серьезно не думает, что этот интеллект присущ отдельной ласточке, отдельному муравью или отдельной пчеле. Нет сомнения, что эти животные образуют группы, управляемые более высоким интеллектом, который заключен не в отдельной особи, но извне осуществляет поддержку, руководство и организацию перелета ласточек, жизни муравейника или пчелиной семьи.
В минеральном царстве то же самое можно наблюдать у металлов, принадлежащих к семье железа, когда химическое существо металла выходит из него и действие его проявляется в непосредственной близости от самого вещества. Это наблюдается у никеля в процессе гидрогенизации жиров, у марганца, когда он как сиккатив ускоряет процесс осмоления масляных красок или окисление спирта и эфира, вплоть до самовозгорания. Также у вольфрама и ванадия в возрастающей степени заметна склонность к атрофии, благодаря чему оба также являются сильными катализаторами. Высшей точки это свойство достигает у платины и платиновых металлов (осмий, иридий, палладий и так далее). Платина, как химическая субстанция, почти полностью атрофична и склеротична. Она действительно до такой степени мертва, что более не в состоянии участвовать в какой-либо химической реакции. Но зато она окружена как бы аурой химической энергии, которая может вызвать и ускорить многие химические реакции, – которые без этого не могли бы состояться, – сама же она, как вещество, при этом не испытывает никаких изменений. Иными словами: благородное свойство придавать силы было оплачено смертью.
Теперь мы понимаем, почему платина не восприимчива к химическим воздействиям и ведет себя как благородный металл. Но эта благородная природа платины совсем другого свойства, чем у золота. Золото благородно в силу активного удержания дистанции в отношении других веществ, а платина не может реагировать с другими веществами, поскольку она мертва. Она стала благородной, пожертвовав свою химическую сущность.
Так, в братьях железа мы видим только металлы, которые продолжают главное направление металла Марса, а именно, все более подвержены отверждающим силам Земли. При этом они развивают свойства, которые являются отражением других космических сфер, Венеры в водной, Юпитера в воздушной, Сатурна в его в огненной природе.
© Авторы и рецензенты: редакционный коллектив оздоровительного портала "На здоровье!". Все права защищены.
www.nazdor.ru
Кобальт, литий, марганец, мышьяк, хром

Микроэлементы – это пища для ферментов, так как они являются регуляторами жизненных процессов. В воздействии на организм все микроэлементы взаимосвязаны и взаимозависимы. Потребности в них для каждого индивидуальны. Однако если баланс между микроэлементами нарушается, появляются разные недомогания и болезни.
КОБАЛЬТ
Биологическая ценность кобальта обнаружена сравнительно недавно. Кобальт, как и марганец, фтор, литий, хром, медь, тиамин, кремнезем, относят к элементам «и добрым, и злым» — в зависимости от их количества: чуть меньше — плохо, чуть больше — опасно!
Какова роль кобальта в организме человека?
Содержание кобальта в организме достаточно велико: в селезенке он составляет 35 мкг% сухой массы, в печени — 25, в мышцах — 2,5, в крови — около 60 мкг %.
Без кобальта невозможно создать здоровые кровяные тельца, а значит, одна из причин болезней, связанных с любым видом малокровия — инфекционным, токсическим, злокачественным, — недостаток кобальта.
Известно, что обычно малокровие поражает людей и домашних животных именно в тех районах, где наблюдается недостаток кобальта в почве.
Кобальт необходим для нормальной деятельности поджелудочной железы. Поэтому для питания тех, кто болен диабетом, кобальт имеет важное значение.
Кобальт также регулирует обменные процессы, особенно содержание адреналина в крови (адреналин — гормон надпочечников, а надпочечники — железы выживания!).
Сегодня уже точно известно, что кобальт связан с витамином В12 и его производными. Он является со ставной частью витамина В12, холина, инозитола, ПБКА.
Кроме того, кобальт и марганец (а также медь) предупреждают раннюю седину в волосах и улучшает их состояние.
Кобальт увеличивает синтез нуклеиновых кислот, с исключительной активностью стимулирует процессы кроветворения, активно участвует в общем восстановлении (регенерации) организма, особенно после тяжелых заболеваний. Он необходим для обмена аминокислот, то есть для образования белка.
Основные пищевые источники кобальта — печень, почки, кислое молоко, яйца, но больше всего кобальта содержится в пшенице и гречке (0,35 мг на 1,кг), много кобальта в какао, кукурузе, но в остальных продуктах — всего до тысячных долей миллиграмма.
Для полноценности диеты следует помнить, что продукты, богатые кобальтом, необходимо сочетать с продуктами, содержащими марганец и витамин В12.
ЛИТИЙ
Литий является одним из ценнейших микроэлементов, или, как о нем еще говорят, миниметаллов. Когда-то литием лечили подагру и экзему. А в 1971 г. в журнале «Медицинские новости» появилось интересное сообщение: в тех местностях, где в питьевой воде содержится большое количество лития, люди добрее и спокойнее, среди них меньше грубиянов и скандалистов, значительно меньше психических заболеваний. Были выявлены психотропные свойства этого металла. Его начали применять при лечении депрессии, ипохондрии, агрессивности и даже наркомании.
Однако литий может быть как «добрым», так и «злым». Поэтому необходимые элементы всегда надо получать не в инъекциях или таблетках, а в естественном их виде — с водой или растениями. Тогда можно надеяться, что организм сам распорядится, сколько ему необходимо тех или иных элементов, компонентов, и как избавиться от их излишков.
Литий содержится в некоторых минеральных водах, а также в морской и каменной соли. Содержится он и в растениях, но концентрация его, как и любых микроэлементов, зависит не только от вида и части растения, но и от времени года и даже суток, от условий сбора и погоды, а также от местности, где растет это растение.
В нашей стране литий исследовали сотрудники Института геохимии имени академика В. И. Вернадского в Москве. Было установлено, что наземные части растений богаче литием, чем корни. Больше всего лития в растениях семейства розоцветных, гвоздичных, пасленовых, к которым относятся помидоры и картофель. Хотя в рамках одного семейства разница в его содержании может быть огромной — в несколько десятков раз. Зависит это, как упоминалось, от географического положения и содержания лития в почве.
Сейчас известно, что, кроме психотропного действия, литий обладает свойствами предупреждать склероз, болезни сердца, в какой-то степени диабет и гипертонию. Он «помогает» магнию в его антисклеротической защите.
В конце 1977 г. были опубликованы результаты исследований, проведенных в Краковской гематологической клинике. Исследования были посвящены вопросам влияния лития на кровеносную систему. Оказалось, что этот микроэлемент активизирует действие еще не погибших клеток костного мозга. Сделанное открытие может сыграть важную роль в борьбе с раком крови. Исследования продолжаются. Хочется верить, что их результаты принесут людям неоценимую помощь.
МАРГАНЕЦ
Марганец необходим для правильного развития клеток, оптимального усвоения тиамина (витамина В1), железа и меди, также необходимых для кроветворения.
Без витамина В1 невозможно создание клеток, особенно нервных, при недостатке этого витамина возникают полиневриты (например бери-бери), запоры. А при недостатке марганца витамин В1 может стать токсичным.
Мало того, марганец помогает смягчить токсические свойства многих других соединений. Вот почему при любых желудочно-кишечных отравлениях после очищения кишечника принято пить слабый раствор марганцовокислого калия.
Потребность в марганце незначительна — всего 0,2-0,3 мг на 1 кг массы тела в день.
В каких продуктах содержится марганец? Больше всего марганца в клюкве, немного меньше в съедобных каштанах, перце.
МЫШЬЯК
С древних времен мышьяк был известен и как лекарство, и как яд. И, тем не менее, мышьяк необходим нашему организму: он препятствует потере фосфора. Как витамин D регулирует фосфорно-кальциевый обмен, так мышьяк регулирует обмен фосфорный.
Известно, что некоторые формы аллергии могут быть вызваны дефицитом мышьяка в организме. Мышьяк применяют при анемии, для повышения аппетита. Когда происходит отравление большими дозами селена, мышьяк может стать хорошим противоядием. В экспериментах, проведенных на мышах, удалось уменьшить заболеваемость раком именно с помощью специально выбранных доз мышьяка.
Но если концентрация мышьяка в продуктах питания или в почве переступит границу и приблизится к ядовитым дозам, то число смертельных случаев, вызванных раком гортани, глаз или белокровием, увеличится.
В организме человека, особенно в волосах и ногтях, находится от 15 до 20 мг мышьяка. Заботиться об этом микроэлементе специально не надо, потому что он находится во всех продуктах растительного и животного происхождения. Кроме того, количества мышьяка, которое обычно присутствует в растениях, вполне достаточно для человека. Однако, с обилием некоторых продуктов можно получить и нежелательное количество яда. В первую очередь это касается таких даров моря как омары, креветки, мяса криля, лангусты и т. п.
Самым богатым источником мышьяка в пище можно считать съедобные моллюски, некоторые виды морских рыб.
ХРОМ
Хром необходим нашему организму в определенных дозах, но если его слишком много, он опасен.
Считается, что нормой для взрослого человека является 150 мг в сутки. Биологическая роль хрома активация процессов обмена углеводистых соединений.
Так, определенное соединение хрома облегчает проникновение глюкозы через мембрану внутрь клеток. Это так называемый глюкозотолерантный фактор (ГТФ). Наш организм способен вырабатывать ГТФ, но в очень малых количествах.
Если хрома в организме недостаточно, уровень холестерина и сахара повышается. Аналогичными свойствами обладает витамин В6.
Когда содержание хрома в организме в норме, происходит оптимальное усвоение глюкозы, если же содержание этого элемента снижено, усвоение сахаров нарушается.
Как влияет хром на организм человека?
В 1973 г. канадский доктор Эдвард Конецко сообщил о том, что хром, принимаемый по 1 мг через день, цинк (50 мг ежедневно) и цистеин (5 мг ежедневно) способны предупредить и даже лечить катаракту. Однако хром и цинк должны сочетаться с аминокислотами, так как только таким образом они могут переходить в усваиваемую форму. Это означает, что микроэлементы могут усваиваться только в органических соединениях. Поэтому все эти источники надо искать в «живых» натуральных продуктах.
Недостаток хрома можно восполнить здоровой, не очищенной промышленными методами пищей.
Отличные источники хрома — пивные дрожжи, печень, картофель, сваренный в кожуре, свежие овощи, хлеб из муки грубого помола, говядина, куриные ножки.
Беременным женщинам и кормящим матерям, больным диабетом, людям старше 45 лет, а также после переломов рекомендуется дополнять диету хромом, то есть ежедневно принимать 12-16 таблеток или 3 столовые ложки порошка пивных дрожжей. Пивные дрожжи перед употреблением нужно предварительно запарить кипятком и настоять 15-30 минут.
На эту тему Вы также можете почитатьrybelm.ru
| Сплавы на основе кобальта, хрома и никеля. В нашей стране и за рубежом уже много лет широко применяют кобальто-хромоникелевые сплавы. Этому способствовало предпочтение, отдаваемое при ортопедическом лечении. конструкциям, позволяющим создавать избирательную нагрузку на зубы, группы зубов, слизистую оболочку протезного ложа. Такне сложные конструкции являются, как правило, бюгельными и могут быть фиксированы на зубных рядах при условии нч высокой объемной и линейной точности. Изготовимте конструкций высокой точности возможно только методом литья из металлических сплавов, обладающих хорошими механическими свойствами, имеющих небольшую усадку. Для этих целей можно применять сплав золота с платиной, однако их малая прочность, большая плотность, дефицит и высокая стоимость ограничивают возможности его применения. Кобальто-хромоникелевые сплавы более прочны, дают точные отливки. Впервые такие сплавы для зуботехнических целей были предложены в начале IO x годов. В 1953 г. в нашей стране нами (А. И. Дойников) разработан и выпускается промышленностью кобальто-хромоникелевый сплав КХС. Он состоит из (%): кобальта — 67, хрома — 26, никеля — 6, молибдена и марганца —по 0,5.Основу сплава составляет кобальт, имеющий высокие механические свойства. Хром вводится для придания сплаву твердости и антикоррозийных свойств. Молибден сообщает сплаву мелкокристаллическую структуру, что усиливает прочностные свойства сплава. Никель усиливает вязкость сплава. Марганец в небольших количествах повышает качество литья, улучшает жидкотекучесть. Марганец понижает температуру плавления, способствует удалению газов и сернистых соединений.В качестве нежелательной примеси он может содержать железо, которое увеличивает усадку сплава при литье и ухудшает физико-химические свойства сплава. Примесь его не должна быть более 0,5%.За рубежом подобные сплавы известны под названием виталлиум, визил, тикониум и др.Сплав KXC применяют для получения только литых изделий. Штамповке он не поддается, так как обладает большой упругостью и твердостью.Из сплава изготавливают цельнолитые съемные зубные протезы различных конструкций, шинирующие аппараты, кламмеры и другие части, требующие повышенной прочности и упругости.В связи с высокими качествами никеля в настоящее время все шире начинают применять сплавы на основе никеля и хрома. Известны сплавы, содержащие до 50% (ультротек и др.). Они находят применение для изготовления металлокерамических протезов. Никель-хромовые сплавы дают точные отливки, устойчивы к коррозии, при литье на их поверхности образуется окисная пленка, к которой хорошо припекается фарфоровая масса.
Следующие статьи: Предыдущие статьи: 111 |
article-factory.ru
Кобальт хромом - Справочник химика 21
Разложение перекисных соединений происходит в присутствии некоторых металлов (железа, меди, марганца, кобальта, хрома) и их солей, являющихся катализаторами. Поэтому концентрированная перекись водорода, надуксусная кислота, а также ряд других перекисей способны взрываться в отсутствие органических веществ. [c.107]Составить уравнения реакций получения перлов буры с солями ионов кобальта, хрома и марганца ( o +, Сг +, Мп +). [c.233]
Применение в технике и в других областях. Кобальт находит применение преимущественно в виде сплавов. Сталь, содержащая кобальт, обладает очень большой твердостью и употребляется для изготовления быстрорежущих инструментов. Она получает необыкновенную способность к намагничиванию. Сплав кобальта с хромом и вольфрамом дает стеллит — металл, отличающийся большой твердостью и также применяющийся для изготовления быстрорежущих инструментов. Еще тверже сплавы кобальта, хрома и молибдена. В ювелирном деле употребляют сплавы кобальта с медью и алюминием. В последнее время кобальтом стали пользоваться для кобальтирования, т. е. для покрытия других металлов с целью предохранения их от окисления — коррозии. [c.370]Окисление может проводиться также в присутствии катализаторов — ацетатов марганца, кобальта, хрома, никеля и др. В указанном процессе температура в реакционной зоне составляет 150—250°. Процесс проводится под давлением 60 ama. С увеличением давления скорость процесса возрастает вследствие увеличения растворимости углеводорода. Период индукции при окислении может быть значительно уменьшен добавлением перекиси в качестве инициатора. [c.97]
Мышьяк, кобальт, хром. 0,2-0,04 [c.441]
В диффузионной области горения наибольшее влияние на выжиг коксовых отложений оказывает добавление железа. На образце катализатора, содержащем 0,8 вес. % железа, отложенный кокс сгорает в два раза быстрее, чем на исходном катализаторе. Остальные металлы в какой-то степени ускоряют выжиг кокса при их содержании в катализаторе в больших концентрациях. Так, на образцах, содержащих до 0,5—0,8 вес. % никеля, меди, кобальта, хрома, молибдена и до 1,5—1,3 вес. % лития, натрия, калия, бериллия, магния, кальция, стронция, кокс выжигается в 1,2 раза быстрее. На образцах, содержащих микродобавки этих металлов, скорость горения кокса такая же, как исходного образца катализатора. Добавка свинца не влияет на скорость регенерации катализатора. [c.167]
Изучением металлов вначале в основном занимались геохимики [342], затем, после того как стало известно о вредном действии металлов на технологию переработки и эксплуатационные свойства топлив, ими начали заниматься химики и технологи (табл. 110). Изучение распределения микроэлементов по нефтяным фракциям также выявило определенные зависимости, важные для технологических процессов [344] (табл. 111). Например, железо, кобальт, хром, марганец, рубидий в повышенных концентрациях обнаружены во фракциях тяжелых нафтеновых нефтей. Ртуть, сурьма, скандий, наоборот, обнаружены в более высоких концентрациях в сравнительно легких метановых нефтях. Независимо от типа нефти выделены микроэлементы, для которых отмечена четкая приуроченность, с одной стороны, к легким фракциям, а с другой— к тяжелым (кобальт, хром, железо). [c.300]
Многие металлы в твердом состоянии растворяют водород. К ним в первую очередь принадлежат палладий, платина, железо, никель, кобальт, хром л марганец. [c.45]
Предварительные испытания. Как и при анализе смеси катионов II и III аналитических групп, следует обратить внимание на окраску раствора. Вместе с окрашенными катионами III группы возможно присутствие в растворе гидратированных ионов меди [Си(НгО)4], голубой цвет которых может быть маскирован ионами кобальта, хрома и некоторыми другими. [c.298]
Возможно ли вытеснение кобальтом хрома из раствора его соли и, наоборот, вытеснение хромом кобальта из раствора его соли [c.262]
Ионы металлов находятся в водных растворах в виде аквокомплексов. Особенно прочны аквокомплексы типичных комплексообразователей (кобальта, хрома, меди и др.). Окислительно-восстановительные потенциалы простых ионов по существу неизвестны, и имеющиеся данные относятся к аквокомплексам, в которых лигандом является вода. На величину окислительновосстановительного потенциала образующего иона большое влияние оказывает химическая природа лигандов. Например, по- [c.391]
Среди других металлоорганических соединений высокими антидетонационными свойствами обладают некоторые соединения, содержащие железо, медь, кобальт, хром, калий, теллур, таллий и др. Наиболее исследованы в качестве антидетонаторов соединения железа и меди пентакарбонил железа (ПКЖ), дициклонентадиенил железа (ферроцен) и внутрикомплексные солн меди. Физические свойства железоорганических антидетонаторов приведены в табл. 5. 36. [c.306]
При гидратации ацетилена в присутствии нертутных катализаторов ацетилен разбавляют азотом, смешивают с водяным паром и полученную парогазовую смесь пропускают при высокой температуре над нертутным катализатором, например окислами цинка, кобальта, хрома или других металлов. Продолжительность контакта парогазовой смеси с катализатором составляет доли секунды, вследствие этого отсутствуют побочные реакции, что приводит к увеличению выхода ацетальдегида и получению более чистого продукта. [c.137]
Возможно ли вытеснение кобальтом хрома из раствора его соли, [c.377]
Сплавы железо — никель — кобальт —хром с разным процентным содержанием этих элементов применяют в основном в крупном промышленном производстве электровакуумных приборов. В практике стеклодувных работ довольно редко приходится встречаться с вводами из таких сплавов, так как их с успехом можно заменить коваром. Спаивают такие сплавы с легкоплавкими стеклами С87-1, 23 и др. Спаи получаются вакуумноплотные, в холодном состоянии они могут иметь цвет от металлического до серого и серо-зеленого. [c.142]
Медь-кобальт- хром-железо- пикель- марганец (1/1/1/1/1/1) Углерод Газ 16.82 83,18 23.63 76.37 31,82 68.18 47,72 52,28 37,72 62,28 18,18 81,82 22,73 77,27 [c.46]
Сталями сплавам на основе карбидов (металлокерамическим, литым и типа стеллитов) вольфрам придает твердость, прочность, износостойкость с сохранением этих свойств до высоких температур. Быстрорежущие стали содержат вольфрама до 20%, инструментальные — до 2%, конструкционные — десятые доли процента. В стеллитах (литые сплавы вольфрама, кобальта, хрома) до 50—55% вольфрама (в основном в виде карбидов), в металлокерамических твердых сплавах 30—92% (в виде карбида W ), в литых карбидах 98% вольфрама, остальное углерод, что соответствует почти чистому карбиду Wa . [c.245]
Многие металлы, такие, как медь, цинк, марганец, никель, кобальт, хром, железо, серебро, золото, часть промышленного выпуска олова, свинца, кадмия, висмута, сурьмы и других металлов, получают электролизом водных растворов. [c.295]
В качестве катализаторов обычно используют металлы или оксиды металлов. Наилучшие катализаторы разрабатываются на основе благородных металлов, а среди других наиболее активны катализаторы из окислов кобальта, хрома, железа, марганца, никеля и др. Однако они имеют меньшую активность, чем катализаторы из благородных мегаллов, а также низкую химическую и термическую стойкость. [c.419]
Уильям Джексон Поуп (1870—1939) продемонстрировал, что трехмерную модель можно распространить также на атомы серы, селена и олова, а несколько позднее швейцарский химик Альфред Вернер (1866—1919) добавил к этому списку кобальт, хром, родий и ряд других металлов. (Начиная с 1891 г. Вернер занимался разработкой координационной теории, которая позволила бы объяснить свойства некоторых необычных неорганических соединений . Согласно этой теории, кроме главных валентных сил имеются еще и силы побочной валентности. Первоначально считалось, что они резко отличаются от основных валентных сил, но впоследствии выяснилось, что существенного различия между ними не существует. [c.89]
Впервые реакция гидроформилирования была осуществлена в присутствии кобальтового катализатора процесса Фишера—Тропша. Впоследствии были исследованы и запатентованы в качестве катализатора многие другие металлы. В литературе сообщается о каталитической активности родия, кобальта, хрома, иридия, железа, марганца, натрия, магния, кальция, платины, рения, осмия и рутения. Однако в промышленности до настоящего времени преимущественно используются кобальтовые катализаторы. [c.255]
По механизму карбидного цикла процесс закоксовыва-ния протекает наиболее иитенсивно на металлах, способных образовывать неустойчивые карбиды (железо, никель, кобальт, хром). Отлагающийся кокс представляет собой углерод, в большей или меньшей степени сформированный в структуру графита. Морфологические характеристики углерода зависят от условий образования ядер, зародышей [c.63]
Для улучшения сгорания могут быть использованы также катализаторы горения, представляюпцие собой главным образом органические соединения металлов — меди, железа, кобальта, хрома, никеля или марганца [74]. [c.314]
В заключение отметим, что для нестационарного способа обезвреживания газовых выбросов промышленных предприятий целесообразно использовать окисные катализаторы. Классификация катализаторов глубокого окисления органических соединений и оксида углерода, их важнейшие характеристики приведены в ряде обзорных работ [12—14], Катализаторы на основе металлов платиновой группы являются наиболее активными и универсальными. Однако благородные металлы имеют высокую стоимость. В этом плане перспективны катализаторы на основе оксидов или солей переходных металлов (меди, кобальта, хрома, никеля, марганца), которые, несколько уступая по своей активности катализаторам, содержащим благородные металлы, значительно дешевле и доступнее. В научной и патентной литературе описаны разнообразные каталитические системы, применяемые для обезвреживания токсичных выбросов. Перечислим здесь лишь несколько марок окисных катализаторов, вы-1гускаемых в СССР. [c.174]
Наиболее полно и достаточно селективно (свыше 95%) реакции гидродеалкилирования протекают в нс нсутствии окисных катализаторов, содержащих молибден, кобальт, хром иа окиси алюминия. Для предотвращения коксообразования, протекающего преимущественно на кислотных активных центрах, в катализатор вводят соединения щелочных металлов или воду. Вода обладает иовы-шепной способностью к хемосорбцни на окислах типа АЬОз и, [c.311]
Одним из компонентов комбинированной антистатической присадки, очевидно, должна быть соль двухвалентного или поливалентного металла (магния, щелочноземельных, меди, железа, марганца, никеля, кобальта, хрома, тория и др.) и различных кислот. Металлы, по-видимому, следует предпочитать двухвалентные, а кислоту — салициловую [21, 22]. Второй компонент должен быть хорошим электролитом. При добавлении менее 0,1% такого компонента электропроводность бензола должна возрастать до десятков тысяч пикосименсов. В качестве второго компонента оказались хороши тетраизоамилпикрат аммония, соли сульфоновых кислот и др. [c.235]
Каталитический процесс требует дополнительных затрат, которые должны компенсироваться увеличением скорости реакцииТ снижением температуры или повышением глубины превращения за один проход, а также избирательности, т. е. меньшим образованием легких газов, смолистых веществ или кокса, что, в свою очередь, снижает расход водорода. Многое также зависит от типа применяемого катализатора (алюмосиликатные, алюмоникелевые, алюмомолибденовые, алюмохромовые, никель на кремнеземе и алюмосиликате, никельалюмохромовые, кобальт, хром и молибден на окиси алюминия и промотированная окись железа). [c.292]
В смолисто-асфальтеновых веществах найдены железо-, кобальт-, хром-, и марганецпорфирины.[261], а также соединения золота и серебра в виде комплексов с тетрадентатными лигандами [266]. [c.275]
Кобальт можно анодно запассивировать в 0,5 т растворе h3SO4. Для этого необходима минимальная плотность тока 5000 А/м , что в 14 раз больше соответствующей плотности тока для никеля [1 ]. Легирование кобальта хромом приводит к уменьшению плотности тока для пассивации сплава с 10 % Сг требуется плотность тока лишь в Ю А/м (1 мА/см ). Сплав, содержащий 10—12 % Сг, почти не подвергается коррозии в горячем и холодном 10 % растворе HNO3, однако в 10 % растворе h3SO4 ИЛИ НС пассивации не происходит, и скорость коррозии достигает очень высоких значений. Легирование сплавов Со—Сг молибденом или вольфрамом ослабляет воздействие на них серной или соляной кислоты, но не азотной. i [c.369]
Бенар обобщил результаты многочисленных исследований взаимодействия металлов с окислителем (кислородом, серой) в, условиях, когда возможно образование сорбционного монослоя, а не обычного оксида или сульфида. Атомы кислорода или серы образуют в условиях равновесия металл — окислитель химические связи с атомами металла (железа, никеля, кобальта, хрома, вольфрама, серебра, меди, палладия, платины), которые прочнее, чем связи М — О или М — S в соответствующих оксидах и сульфидах. Разница между теплотой образования оксида и начальной теплотой химической сорбции кислорода для серебра достигает 47 ккал/моль, для хрома—15 ккал/моль. Теплота химической сорбции серы на меди почти на 70% превышает теплоту образования U2S. [c.55]
Для кадмия, олова, свинца, осаждающихся почти без перенапряжения (поляризации), приходится изыскивать специальные условия. В противном случае получаются грубокристаллические некомпактные осадки, совершенно не обладающие защитными свойствами. Металлы, разряд и выделение которых сопровождается высоким перенапряжением, — железо, никель, кобальт, хром — осаждаются в виде мелкокристаллических компактных осадков. Такие металлы, как молибден, вольфрам, титан, тантал и ниобий, вообще не удалось выделить из водных растворов в чистом виде. Они выделяются только в виде оксидов, гидроксидов или очень тонких (до 0,3 мкм) металлических пленок. [c.364]
Для окисления Fe (И) в Ре (П1) используют азотную кислоту, а также другие окислители в зависимости от природы анализируемого объекта пероксидисульфат аммония, перманганат калия. Проведению реакции мешает ряд веш,еств. Прежде всего должны отсутствовать анионы кислот, которые дают более прочные ко1 шлексиые соединения, чем роданиды железа фосфаты, ацетаты, арсенаты, фториды, бораты, а также значительные количества хлоридов и сульфатов. Также должны отсутствовать элементы, ионы которых дают комплексные соединения с роданидом кобальт, хром, висмут, медь молибден, вольфрам, титан (III, IV), ниобий, палладий, кадмий, цинк, ртуть. [c.151]
Порошки ЖС-6КП получали из отходов электроконтактной обработки прутков сплава, легированного кобальтом, хромом, титаном, алюминием, мо 1ибденом. [c.111]
Возможность образования двух модификаций при катодном выделении металла — явление нередкое (например, никель, кобальт, хром) и для электролитического получения этих металлов обычно значения не имеет. При катодном осаждении марганца процесс полностью нарушается, если условия электролиза не подобраны таким образом, чтобы образовалась только одна модификация. Основным условием является концентрация микродобавок. Помимо того, что они способствуют образованию многоатомной решетки а-модификации (возможно, это связано с образованием пленки из соединений серы, селена и теллура, сдвигающих потенциал), микродобавки значительно снижают чувствительность процесса электролиза к наличию яримесей, высокой температуре и уменьшению концентрации. [c.397]
В качестве катализаторов применяли иикепь металлический, оксид никеля, никель азотнокислый, никель сернокислый, никель муравьинокислый, никель шавелевокислый, оксид кобальта, оксид марганца, оксид хрома, оксид железа, предварительно восстановленные водородом при температуре 500°С, промьниленные катализаторы никель-марганцевый, железо-хромовый, алюмо-никель-молибденовый, интерметаллическое соединение цирконий-никелевый гидрид ультрадисперсные оксиды металлов кобальт-никель-марганец-хром, медь-хром-марганец-кобальт, медь-хром-кобальт-1шкель-марганец, медь-кобальт-хром-железо-ннкель-марганец, а также двухкомпонентные катализаторы на основе металлов подгруппы железа. Физико-химические свойства их приведены в табл.7. [c.42]
chem21.info