Задача С2 на ЕГЭ по химии. Особенности и подводные камни. Оксид хрома сплавили с сульфитом натрия полученный продукт внесли в воду
Задание С2 на ЕГЭ по химии
Автор статьи — профессиональный репетитор О. В. Овчинникова.
 Условие задачи С2 на ЕГЭ по химии — это текст, описывающий последовательность экспериментальных действий. Данный текст нужно превратить в уравнения реакций.
Условие задачи С2 на ЕГЭ по химии — это текст, описывающий последовательность экспериментальных действий. Данный текст нужно превратить в уравнения реакций.
Трудность такого задания в том, что школьники слабо представляют себе экспериментальную, не "бумажную" химию. Не все понимают используемые термины и протекающие процессы. Попробуем разобраться.
Очень часто понятия, которые химику кажутся совершенно ясными, абитуриентами воспринимаются неправильно. Вот кратких словарь таких понятий.
Словарь непонятных терминов.
- Навеска — это просто некоторая порция вещества определенной массы (её взвесили на весах). Она не имеет отношения к навесу над крыльцом :-)
- Прокалить — нагреть вещество до высокой температуры и греть до окончания химических реакций. Это не «смешивание с калием» и не «прокалывание гвоздём».
- «Взорвали смесь газов» — это значит, что вещества прореагировали со взрывом. Обычно для этого используют электрическую искру. Колба или сосуд при этом не взрываются!
- Отфильтровать — отделить осадок от раствора.
- Профильтровать — пропустить раствор через фильтр, чтобы отделить осадок.
- Фильтрат — это профильтрованный раствор.
- Растворение вещества — это переход вещества в раствор. Оно может происходить без химических реакций (например, при растворении в воде поваренной соли NaCl получается раствор поваренной же соли NaCl, а не щелочь и кислота отдельно), либо в процессе растворения вещество реагирует с водой и образует раствор другого вещества (при растворении оксида бария получится раствор гидроксида бария). Растворять можно вещества не только в воде, но и в кислотах, в щелочах и т.д.
- Выпаривание — это удаление из раствора воды и летучих веществ без разложения содержащихся в растворе твёрдых веществ.
- Упаривание — это просто уменьшение массы воды в растворе с помощью кипячения.
- Сплавление — это совместное нагревание двух или более твёрдых веществ до температуры, когда начинается их плавление и взаимодействие. С плаванием по реке ничего общего не имеет :-)
- Осадок и остаток.Очень часто путают эти термины. Хотя это совершенно разные понятия.«Реакция протекает с выделением осадка» — это означает, что одно из веществ, получающихся в реакции, малорастворимо. Такие вещества выпадают на дно реакционного сосуда (пробирки или колбы).«Остаток» — это вещество, которое осталось, не истратилось полностью или вообще не прореагировало. Например, если смесь нескольких металлов обработали кислотой, а один из металлов не прореагировал — его могут назвать остатком.
- Насыщенный раствор — это раствор, в котором при данной температуре концентрация вещества максимально возможная и больше уже не растворяется.
Ненасыщенный раствор — это раствор, концентрация вещества в котором не является максимально возможной, в таком растворе можно дополнительно растворить ещё какое-то количество данного вещества, до тех пор, пока он не станет насыщенным.
Разбавленный и «очень» разбавленный раствор — это весьма условные понятия, скорее качественные, чем количественные. Подразумевается, что концентрация вещества невелика.
Для кислот и щелочей также используют термин «концентрированный» раствор. Это тоже характеристика условная. Например, концентрированная соляная кислота имеет концентрацию всего около 40%. А концентрированная серная — это безводная, 100%-ная кислота.
Для того, чтобы решать такие задачи, надо чётко знать свойства большинства металлов, неметаллов и их соединений: оксидов, гидроксидов, солей. Необходимо повторить свойства азотной и серной кислот, перманганата и дихромата калия, окислительно-восстановительные свойства различных соединений, электролиз растворов и расплавов различных веществ, реакции разложения соединений разных классов, амфотерность, гидролиз солей и других соединений, взаимный гидролиз двух солей.
Кроме того, необходимо иметь представление о цвете и агрегатном состоянии большинства изучаемых веществ — металлов, неметаллов, оксидов, солей.
Именно поэтому мы разбираем этот вид заданий в самом конце изучения общей и неорганической химии.Рассмотрим несколько примеров подобных заданий.
-
Пример 1: Продукт взаимодействия лития с азотом обработали водой. Полученный газ пропустили через раствор серной кислоты до прекращения химических реакций. Полученный раствор обработали хлоридом бария. Раствор профильтровали, а фильтрат смешали с раствором нитрита натрия и нагрели.
Решение:
- Литий реагирует с азотом при комнатной температуре, образуя твёрдый нитрид лития:
- При взаимодействии нитридов с водой образуется аммиак:
- Аммиак реагирует с кислотами, образуя средние и кислые соли. Слова в тексте «до прекращения химических реакций» означают, что образуется средняя соль, ведь первоначально получившаяся кислая соль далее будет взаимодействовать с аммиаком и в итоге в растворе будет сульфат аммония:
- Обменная реакция между сульфатом аммония и хлоридом бария протекает с образованием осадка сульфата бария:
- После удаления осадка фильтрат содержит хлорид аммония, при взаимодействии которого с раствором нитрита натрия выделяется азот, причём эта реакция идёт уже при 85 градусах:
-
Пример 2: Навеску алюминия растворили в разбавленной азотной кислоте, при этом выделялось газообразное простое вещество. К полученному раствору добавили карбонат натрия до полного прекращения выделения газа. Выпавший осадок отфильтровали и прокалили, фильтрат упарили, полученный твёрдый остаток сплавили с хлоридом аммония. Выделившийся газ смешали с аммиаком и нагрели полученную смесь.
Решение:
- Алюминий окисляется азотной кислотой, образуя нитрат алюминия. А вот продукт восстановления азота может быть разным, в зависимости от концентрации кислоты. Но надо помнить, что при взаимодействии азотной кислоты с металлами не выделяется водород! Поэтому простым веществом может быть только азот:
- Если к раствору нитрата алюминия добавить карбонат натрия, то идёт процесс взаимного гидролиза (карбонат алюминия не существует в водном растворе, поэтому катион алюминия и карбонат-анион взаимодействуют с водой). Образуется осадок гидроксида алюминия и выделяется углекислый газ:
- Осадок — гидроксид алюминия, при нагревании разлагается на оксид и воду:
- В растворе остался нитрат натрия. При его сплавлении с солями аммония идёт окислительно-восстановительная реакция и выделяется оксид азота (I) (такой же процесс происходит при прокаливании нитрата аммония):
- Оксид азота (I) — является активным окислителем, реагирует с восстановителями, образуя азот:
-
Пример 3: Оксид алюминия сплавили с карбонатом натрия, полученное твёрдое вещество растворили в воде. Через полученный раствор пропускали сернистый газ до полного прекращения взаимодействия. Выпавший осадок отфильтровали, а к профильтрованному раствору прибавили бромную воду. Полученный раствор нейтрализовали гидроксидом натрия.
Решение:
- Оксид алюминия — амфотерный оксид, при сплавлении со щелочами или карбонатами щелочных металлов образует алюминаты:
- Алюминат натрия при растворении в воде образует гидроксокомплекс:
- Растворы гидроксокомплексов реагируют с кислотами и кислотными оксидами в растворе, образуя соли. Однако, сульфит алюминия в водном растворе не существует, поэтому будет выпадать осадок гидроксида алюминия. Обратите внимание, что в реакции получится кислая соль — гидросульфит калия:
- Гидросульфит калия является восстановителем и окисляется бромной водой до гидросульфата:
- Полученный раствор содержит гидросульфат калия и бромоводородную кислоту. При добавлении щелочи нужно учесть взаимодействие с ней обоих веществ:
-
Пример 4: Сульфид цинка обработали раствором соляной кислоты, полученный газ пропустили через избыток раствора гидроксида натрия, затем добавили раствор хлорида железа (II). Полученный осадок подвергли обжигу. Полученный газ смешали с кислородом и пропустили над катализатором.
Решение:
- Сульфид цинка реагирует с соляной кислотой, при этом выделяется газ — сероводород:
- Сероводород — в водном растворе реагирует со щелочами, образуя кислые и средние соли. Поскольку в задании говорится про избыток гидроксида натрия, следовательно, образуется средняя соль — сульфид натрия:
- Сульфид натрия реагирует с хлоридом двухвалентного железа, образуется осадок сульфида железа (II):
- Обжиг — это взаимодействие твёрдых веществ с кислородом при высокой температуре. При обжиге сульфидов выделяется сернистый газ и образуется оксид железа (III):
- Сернистый газ реагирует с кислородом в присутствии катализатора, образуя серный ангидрид:
-
Пример 5: Оксид кремния прокалили с большим избытком магния. Полученную смесь веществ обработали водой. При этом выделился газ, который сожгли в кислороде. Твёрдый продукт сжигания растворили в концентрированном растворе гидроксида цезия. К полученному раствору добавили соляную кислоту.
Решение:
- При восстановлении оксида кремния магнием образуется кремний, который реагирует с избытком магния. При этом получается силицид магния:
Можно записать при большом избытке магния суммарное уравнение реакции:
- При растворении в воде полученной смеси растворяется силицид магния, образуется гидроксид магния и силан (окисд магния реагирует с водой только при кипячении):
- Силан при сгорании образует оксид кремния:
- Оксид кремния — кислотный оксид, он реагирует со щелочами, образуя силикаты:
- При действии на растворы силикатов кислот, более сильных, чем кремниевая, она выделяется в виде осадка:
Ты нашел то, что искал? Поделись с друзьями!
Задания С2 из вариантов ЕГЭ по химии для самостоятельной работы.
- Нитрат меди прокалили, полученный твёрдый осадок растворили в серной кислоте. Через раствор пропустили сероводород, полученный чёрный осадок подвергли обжигу, а твёрдый остаток растворили при нагревании в концентрированной азотной кислоте.
- Фосфат кальция сплавили с углём и песком, затем полученное простое вещество сожгли в избытке кислорода, продукт сжигания растворили в избытке едкого натра. К полученному раствору прилили раствор хлорида бария. Полученный осадок обработали избытком фосфорной кислоты.
- Медь растворили в концентрированной азотной кислоте, полученный газ смешали с кислородом и растворили в воде. В полученном растворе растворили оксид цинка, затем к раствору прибавили большой избыток раствора гидроксида натрия.
- На сухой хлорид натрия подействовали концентрированной серной кислотой при слабом нагревании, образующийся газ пропустили в раствор гидроксида бария. К полученному раствору прилили раствор сульфата калия. Полученный осадок сплавили с углем. Полученное вещество обработали соляной кислотой.
- Навеску сульфида алюминия обработали соляной кислотой. При этом выделился газ и образовался бесцветный раствор. К полученному раствору добавили раствор аммиака, а газ пропустили через раствор нитрата свинца. Полученный при этом осадок обработали раствором пероксида водорода.
- Порошок алюминия смешали с порошком серы, смесь нагрели, полученное вещество обработали водой, при этом выделился газ и образовался осадок, к которому добавили избыток раствора гидроксида калия до полного растворения. Этот раствор выпарили и прокалили. К полученному твёрдому веществу добавили избыток раствора соляной кислоты.
- Раствор иодида калия обработали раствором хлора. Полученный осадок обработали раствором сульфита натрия. К полученному раствору прибавили сначала раствор хлорида бария, а после отделения осадка — добавили раствор нитрата серебра.
- Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился тёмно-зелёный раствор. К полученному щелочному раствору прибавили пероксид водорода. Получился раствор желтого цвета, который при добавлении серной кислоты приобретает оранжевый цвет. При пропускании сероводорода через полученный подкисленный оранжевый раствор он мутнеет и вновь становится зелёным.
- (МИОО 2011, тренинговая работа) Алюминий растворили в концентрированном растворе гидроксида калия. Через полученный раствор пропускали углекислый газ до прекращения выделения осадка. Осадок отфильтровали и прокалили. Полученный твердый остаток сплавили с карбонатом натрия.
- (МИОО 2011, тренинговая работа) Кремний растворили в концентрированном растворе гидроксида калия. К полученному раствору добавили избыток соляной кислоты. Помутневший раствор нагрели. Выделившийся осадок отфильтровали и прокалили с карбонатом кальция. Напишите уравнения описанных реакций.
Ответы к заданиям для самостоятельного решения:
- или
-
или -
или
Читаем дальше: Задачи на сплавы и смеси на ЕГЭ по химии.Задача С5 на ЕГЭ по химии. Определение формул органических веществ.
Звоните нам: 8 (800) 775-06-82 (бесплатный звонок по России) +7 (495) 984-09-27 (бесплатный звонок по Москве)
Или нажмите на кнопку «Узнать больше», чтобы заполнить контактную форму. Мы обязательно Вам перезвоним.
ege-study.ru
| 1 | tsu.ru | 5 600 | да | 6 | да | 37 027 | 6 300 | IV. Химия элементов-металлов | 10.8. Соединения хрома (III) | При сплавлении с кислотным реагентом – дисульфатом калия – образует сульфат хрома (III), проявляя основные свойства ... Оксид хрома (III) получается при термическом разложении дихромата аммония |
| 2 | mail.ru | 190 000 | да | 8 | да | 7 228 974 | 15 700 000 | Ответы@Mail.Ru: ...Оксид хрома (III) с гидрооксидом калия? | Во насмешил MariO: хром и калий теперь двухвалентный?? ? Ответ: по идеи если прокипятить вместе, то должны: кислотный оксид и сильное основание: Cr2O3 + 6KOH >>> 2K3CrO3 + 3h30. |
| 3 | mail.ru | 190 000 | да | 8 | да | 7 228 974 | 15 700 000 | Ответы@Mail.Ru: ...порошок оксида хрома (III) сплавили... | Метахромит в комплекс перейдёт,не разберётесь-пишите... |
| 4 | tutoronline.ru | 350 | да | 3 | да | 30 904 | 18 600 | Хром и его соединения | В природе встречаются также оксид хрома (3) и некоторые другие его соединения. ... В результате этой реакции образуется сплав хрома с железом, отличающийся ... Если смешать растворы сульфата меди и дихромата калия и добавить немного раствора... |
| 5 | wikipedia.org | 97 000 | да | 9 | да | 3 695 401 | 18 800 000 | Сульфат хрома(III)-калия — Википедия | Сульфат хрома(III)-калия — неорганическое соединение, соль металлов калия и хрома и серной кислоты с формулой KСr(SO4)2, красные кристаллы, растворимые в воде, образует кристаллогидраты — хромокалиевые квасцы. |
| 6 | chem100.ru | 70 | — | 2 | — | 6 596 | 6 800 | Хром - Свойства химических элементов | Хром загорается в кислороде при 2000 °С с образованием темно-зеленого оксида Хрома (III) Сr2О3. ... Сырьем обычно служат хромшпинелиды, которые подвергают обогащению, а затем сплавляют с поташом (или содой) в присутствии кислорода... |
| 7 | znanija.com | 325 | да | 4 | — | 677 855 | 179 000 | Решите задания !!! Сделайте на... - Школьные Знания.com | В 120 г 18%-ной ортофосфорной кислоты растворили 5,68г оксида фосфора (V) и полученный раствор прокипятили. ... Оксид хрома 3 сплавили с сульфитом калия и продукт реакции внесли в воду. |
| 8 | himege.ru | 20 | — | 1 | — | 12 163 | 4 300 | ЕГЭ химия задания С2 » HimEge.ru | 12.Сульфат бария сплавили с коксом. Твердый остаток растворили в соляной кислоте, выделившийся газ вступил в реакцию с оксидом серы (IV), а ... При взаимодействии этого соединения с гидроксидом калия выпадает осадок гидроксида хрома(Ш) |
| 9 | distant.ru | 100 | — | 1 | да | 9 255 | 1 400 | Важнейшие соединения хрома | Оксид хрома (II) CrO. Пирофорный черный порошок. На воздухе при температуре выше 100°С превращается в Cr2O3. ... Выпадают при выпаривании водного раствора, полученного смешением сульфата калия и сульфата хрома (III) в... |
| 10 | ege-study.ru | 120 | да | 3 | — | 13 699 | 26 000 | Задача С2 на ЕГЭ по химии | К полученному раствору прилили раствор сульфата калия. ... Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился тёмно-зелёный раствор. |
| 11 | piroforum.info | 40 | — | 1 | — | 2 076 | 350 | Оксид хрома VI (CrO3) | Автор. Тема: Оксид хрома VI (CrO3) (Прочитано 14847 раз). ... обменку провести? есть нитраты стронция, нитрат бария, хлорид калия,нитрат аммония, сульфат марганца. ну в теории можно прокалить дихромат аммония, полученный Cr2O3 сплавить с... |
| 12 | docload.ru | 650 | — | 4 | — | 28 070 | 11 800 | ГОСТ 2642.9-97 | Методы определения оксида хрома (III) | 7. Фотометрический метод определения оксида хрома (iii) в высокомагнезиальных ... Остывший сплав вместе с тиглем опускают в стакан, в который предварительно ... Калия бихромат по ГОСТ 4220. Стандартный раствор оксида хрома (III): 0,1934 г... |
| 13 | allbest.ru | 3 000 | да | 6 | — | 833 039 | 146 000 | Хром и его соединения | А при сплавлении с дисульфатом калия образует сульфат хрома (III). Сначала при нагревании K2S2O7 разлагается на сульфат калия и оксид серы (VI) ... Стеллит - сплав хрома и кобальта. Применяется в металлообрабатывающей промышленности. |
| 14 | bankreferatov.ru | 500 | да | 5 | да | 101 894 | 16 100 | Хром (Chromium), Банк Рефератов | При восстановления хромистого железняка углём появляется сплав хрома с ... Хром образует три оксида: оксид хрома (II), или закись хрома, CrO, имеющий основной ... Из солей хрома (III) самой распространённой является двойная соль хрома и калия... |
| 15 | krugosvet.ru | 4 000 | да | 6 | да | 73 339 | 74 800 | ХРОМ | Энциклопедия Кругосвет | Оксид хрома(III) довольно токсичен. ... Могут быть получены при выпаривании водного раствора, содержащего стехиометрическую смесь сульфатов калия и хрома, или восстановлением дихромата калия этанолом |
| 16 | bestreferat.ru | 1 100 | да | 5 | да | 513 547 | 119 000 | Реферат: Исследование свойств хрома и его соединений... | Феррохром - сплав хрома с железом, вводимый в жидкую сталь для ее легирования. ... Важнейшие окислители - галогены, перманганат калия, манганат калия, оксид марганца (IV), азотная кислота, кислород, озон, пероксид водорода... |
| 17 | himege.ru | 20 | — | 1 | — | 12 163 | 4 300 | Задания С2 ЕГЭ по химии с решениями » HimEge.ru | 7) Раствор иодида калия обработали раствором хлора. Полученный осадок обработали раствором сульфита натрия. ... 8) Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился... |
| 18 | wikipedia.org | 97 000 | да | 9 | да | 3 695 401 | 18 800 000 | Оксид хрома(III) — Википедия | Окси́д хро́ма (III) Cr2O3 (сесквиоксид хрома, хромовая зелень, эсколаит) — очень твёрдый тугоплавкий порошок зелёного цвета. Температура плавления 2435 °C, кипения ок. 4000 °C. Плотность 5,21 г/см³. Нерастворим в воде. |
| 19 | ege-study.ru | 120 | да | 3 | — | 13 699 | 26 000 | Новая версия задачи С2 в ЕГЭ по химии 2012. Особенности... | Раствор иодида калия обработали раствором хлора. Полученный осадок обработали раствором сульфита натрия. ... Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился... |
| 20 | xreferat.com | 0 | — | 0 | — | 264 405 | 113 000 | Реферат: Исследование свойств хрома и его соединений... | При прокаливании гидроксида хрома (III) образуется оксид хрома (III) Cr2O3. ... Приборы и реактивы: раствор бихромата калия K2Cr2O7; раствор сульфита натрия ... Феррохром - сплав хрома с железом, вводимый в жидкую сталь для ее легирования. |
advodka.com
Задания №31
Задания для самостоятельного решения (ответы ниже)
1. Даны: хлорид хрома (III), поташ, бромоводородная кислота, гидроксид лития. Напишите уравнения четырех возможных реакций между этими веществами.
2. Даны: бромид магния, карбонат натрия, хлороводородная кислота, гидроксид лития. Напишите уравнения четырех возможных реакций между этими веществами.
3. Даны: перманганат калия, сульфит калия, гидроксид калия. Напишите уравнения четырех возможных реакций между этими веществами.
4. Даны: бромид алюминия, сульфид натрия, соляная кислота, гидроксид лития. Напишите уравнения четырех возможных реакций между этими веществами.
5. Даны: сера, хлор, бромид калия, гидроксид натрия. Напишите уравнения четырех возможных реакций между этими веществами.
6. Даны: хлорид кальция, карбонат натрия, бромоводородная кислота, гидроксид бария. Напишите уравнения четырех возможных реакций между этими веществами.
7. Даны: сера, гидроксид калия, азотная кислота, бром. Напишите уравнения четырех возможных реакций между этими веществами.
8. Даны: фосфор, хлор, азотная кислота, гидроксид лития. Напишите уравнения четырех возможных реакций между этими веществами.
9. Даны: хлор, сера, железо, водород. Напишите уравнения четырех возможных реакций между этими веществами.
10. Даны:бром, железо, соляная кислота, гидроксид калия. Напишите уравнения четырех возможных реакций между этими веществами.
11. Даны: перманганат калия, сульфит калия, бромоводородная кислота, гидроксид калия. Напишите уравнения четырех возможных реакций между этими веществами.
12. Даны: Перманганат калия, сероводород, азотная кислота, карбонат калия. Напишите уравнения четырех возможных реакций между этими веществами.
13. Даны: бром, йодид натрия, карбонат натрия, серная кислота. Напишите уравнения четырех возможных реакций между этими веществами.
14. Даны: сульфид натрия, нитрат серебра, соляная кислота, перекись водорода. Напишите уравнения четырех возможных реакций между этими веществами.
15. Даны: калий, бром, сероводородная кислота, азотная кислота. Напишите уравнения четырех возможных реакций между этими веществами.
16. Даны: сероводород, оксид серы (IV), карбонат калия, перманганат калия. Напишите уравнения четырех возможных реакций между этими веществами.
17. Даны: фосфор, сера, гидроксид натрия, азотная кислота. Напишите уравнения четырех возможных реакций между этими веществами.
18. Даны: фосфор, хлор, гидроксид калия, азотная кислота. Напишите уравнения четырех возможных реакций между этими веществами.
19. Даны: железо, хлор, соляная кислота, сера. Напишите уравнения четырех возможных реакций между этими веществами.
20. Даны: кислород, бромоводород, оксид меди (II), алюминий. Напишите уравнения четырех возможных реакций между этими веществами.
21. Даны: гидроксид хрома (III), бромоводородная кислота, хлор, гидроксид калия. Напишите уравнения четырех возможных реакций между этими веществами.
22. Даны: гидроксид цинка, азотная кислота, бром, гидроксид натрия. Напишите уравнения четырех возможных реакций между этими веществами.
23. Даны: хлорноватая кислота, соляная кислота, йод, гидроксид натрия. Напишите уравнения четырех возможных реакций между этими веществами.
24. Даны: бром, йодид натрия, сера, азотная кислота. Напишите уравнения четырех возможных реакций между этими веществами.
25. Осадок, полученный при взаимодействии растворов сульфата железа (III) и нитрата бария, отфильтровали. Фильтрат обработали избытком едкого натра. Выпавший осадок отделили и прокалили. Полученное вещество обработали избытком раствора соляной кислоты. Напишите уравнения описанных реакций.
26. Литий сплавили с серой. Полученную соль обработали разбавленной соляной кислотой, при этом выделился газ с запахом тухлых яиц. Этот газ сожгли в избытке кислорода, при этом выделился газ с характерным резким запахом. При пропускании этого газа в избыток гидроксида натрия образовалась средняя соль. Напишите уравнения описанных реакций.
27. Нитрат калия подвергли термическому разложению. Выделившийся газ на свету пропустили через насыщенный раствор сероводорода в воде. Выпавшее вещество желтого цвета сплавили с железом, а полученную соль обработали разбавленной соляной кислотой. Напишите уравнения описанных реакций.
28. Расплав хлорида натрия подвергли электролизу. Газ, выделившийся на аноде, прореагировал с водородом с образованием нового газообразного вещества с характерным резким запахом. Его растворили в воде и обработали расчетным количеством перманганата калия, при этом образовался газ желто-зеленого цвета. Это вещество вступает при охлаждении в реакцию в гидроксидом натрия. Напишите уравнения описанных реакция.
29. Нитрат натрия сплавили с оксидом хрома в присутствии карбоната натрия. Выделившийся при этом газ прореагировал с избытком раствора гидроксида бария с выпадением осадка белого цвета. Осадок растворили в избытке раствора соляной кислоты и в полученный раствор добавили нитрат серебра до прекращения выделения осадка. Напишите уравнения описанных реакций.
30. Литий прореагировал с водородом. Продукт реакции растворили в воде, при этом образовался газ, реагирующий с бромом, а полученный раствор при нагревании прореагировал с хлором с образованием смеси двух солей. Напишите уравнения описанных реакций.
31. Натрий сожгли на воздухе. Образовавшееся при этом твердое вещество поглощает углекислый газ с выделением кислорода и выделением соли. Последнюю соль растворили в соляной кислоте, а к полученному при этом раствору добавили раствор нитрата серебра. При этом выпал белый творожистый осадок. Напишите уравнения описанных реакций.
32. Калия сплавили с серой. Полученную соль обработали соляной кислотой. Выделившийся при этом газ пропустили через раствор бихромата калия в серной кислоте. Выпавшее вещество желтого цвета отфильтровали и сплавили с алюминием. Напишите уравнения описанных реакций.
33. Магний растворили в разбавленной азотной кислоте. К полученному раствору последовательно добавили гидроксид натрия, бромоводородную кислоту, фосфат натрия. Напишите уравнения описанных реакций.
34. Кальций сожгли в атмосфере азота. Полученную соль разложили кипящей водой. Выделившийся газ сожгли в кислороде в присутствии катализатора, а к суспензии прибавили раствор соляной кислоты. Напишите уравнения описанных реакций.
35. Барий растворили в разбавленной азотной кислоте, при этом выделился бесцветный газ - несолеобразующий оксид . Полученный раствор разделили на три части. Первую - выпарили досуха, полученный осадок прокалили. Ко второй части прилили раствор сульфата натрия до прекращения выделения осадка; к третьей добавили раствор карбоната натрия. Напишите уравнения описанных реакций.
36. Алюминий вступил в реакцию с Fe3O4. Полученную смесь веществ растворили в концентрированном растворе гидроксида натрия и отфильтровали. Твердое вещество сожгли в атмосфере хлора, а фильтрат обработали концентрированным раствором хлорида алюминия. Напишите уравнения описанных реакций.
37. Сульфат бария сплавили с коксом. Твердый остаток растворили в соляной кислоте, выделившийся газ вступил в реакцию с оксидом серы (IV), а раствор - с сульфатом натрия. Напишите уравнения описанных реакций.
38. Кремний растворили в концентрированном растворе гидроксида натрия. Через полученный раствор пропустили углекислый газ. Выпавший осадок отфильтровали, высушили и разделили на две части. Первую растворили в плавиковой кислоте, вторую сплавили с магнием. Напишите уравнения описанных реакций.
39. Азот при нагревании на катализаторе прореагировал с водородом. Полученный газ поглотили раствором азотной кислоты, выпарили досуха и полученное кристаллическое вещество разделили на две части. Первую разложили при температуре 190-240С, при этом образовался только один газ и водяные пары. Вторую часть нагрели с концентрированным раствором едкого натра. Напишите уравнения описанных реакций.
40. Красный фосфор окислили кипящей азотной кислотой. Выделившийся при этом газ поглотили раствором гидроксида калия. Продукт окисления в первой реакции нейтрализовали гидроксидом натрия, а к образовавшейся реакционной массе по каплям добавили раствор хлорида кальция до прекращения выделения осадка. Напишите уравнения описанных реакций.
41. Кислород подвергли воздействию электроразряда в озонаторе. Полученный газ пропустили через водный раствор йодида калия, при этом выделился новый газ без цвета и запаха, поддерживающий горение и дыхание. В атмосфере последнего газа сожгли натрий, а полученное при этом твердое вещество прорегировало с углекислым газом. Напишите уравнения описанных реакций.
42. Концентрированная серная кислота прорегировала с медью. Выделившийся при этом газ полностью поглотили избытком раствора гидроксида калия. Продукт окисления меди смешали с расчетным количеством гидроксида натрия до прекращения выделения осадка. Последний растворили в избытке соляной кислоты. Напишите уравнения описанных реакций.
43. Хром сожгли в атмосфере хлора. К образовавшейся соли добавили по каплям гидроксид калия до прекращения выделения осадка. Полученный осадок окислили перекисью водорода в среде едкого кали и упарили. К полученному твердому остатку добавили избыток горячего раствора концентрированной соляной кислоты. Напишите уравнения описанных реакций.
44. Перманганат калия обработали концентрированной горячей соляной кислотой. Выделившийся при этом газ собрали, а к реакционной массе по каплям прибавили раствор гидроксида калия до прекращения выделения осадка. Собранный газ пропустили через горячий раствор гидроксида калия, при этом образовалась смесь двух солей. Раствор выпарили, твердый остаток прокалили в присутствии катализатора, после чего в твердом остатке осталась одна соль. Напишите уравнения описанных реакций.
1. Железо растворили в разбавленном растворе серной кислоты, образовавшуюся соль выделили. При взаимодействии полученной соли со щелочным раствором перманганата калия наблюдается выпадение осадка и изменение цвета раствора на зеленый. Осадок отделили и растворили в соляной кислоте. Полученный раствор нагрели и поместили в него порошок меди, при этом наблюдали изменение цвета раствора. Напишите уравнения четырех описанных реакций.
2. Нитрат серебра прокалили. К образовавшемуся твердому остатку добавили концентрированную азотную кислоту и наблюдали интенсивное выделение бурого газа. Газ собрали и полностью поглотили раствором гидроксида калия при охлаждении. К образовавшемуся раствору прилили раствор дихромата калия, подкисленный серной кислотой. Напишите уравнения четырех описанных реакций.
3. Железо растворили в соляной кислоте. Через образовавшийся раствор пропустили аммиак. Образовавшийся при этом осадок отделили и обработали пероксидом водорода без нагревания, при этом наблюдали изменение цвета осадка. Полученное бурое вещество сплавили с твердым гидроксидом натрия. Напишите уравнения четырех описанных реакций.
4. На перманганат калия подействовали концентрированной серной кислотой. Образовавшийся желто-зеленый газ пропустили над нагретым порошком меди. Полученное вещество растворили в воде и смешали с раствором нитрата серебра (I), выпавший при этом осадок отделили. К оставшемуся раствору добавили раствор йодида калия. Напишите уравнения четырех описанных реакций.
5. Фосфат кальция прокалили с углем в присутствии речного песка. Образовавшееся простое вещество прореагировало с избытком хлора. Полученный продукт внесли в избыток раствора гидроксида калия. На образовавшийся раствор подействовали известковой водой. Запишите уравнения описанных реакций.
6. Металлический алюминий растворили в растворе гидроксида натрия. Через полученный раствор пропустили избыток углекислого газа. Выпавший осадок прокалили и полученный продукт сплавили с карбонатом натрия. Запишите уравнения описанных реакций.
7. Металлическую медь обработали при нагревании йодом. Полученный продукт растворили в концентрированной серной кислоте при нагревании. Образовавшийся раствор обработали гидроксидом калия. Выпавший осадок прокалили. Запишите уравнения описанных реакций.
8. К раствору хлорида меди (II) добавили избыток раствора соды. Выпавший осадок прокалили, а полученный продукт нагрели в атмосфере водорода. Полученный порошок растворили в разбавленной азотной кислоте. Запишите уравнения описанных реакций.
9. Оксид алюминия сплавили с содой. Полученный продукт растворили в соляной кислоте и обработали избытком аммиачной воды. Выпавший осадок растворили в избытке раствора гидроксида натрия. Запишите уравнения описанных реакций.
10. Провели электролиз раствора хлорида натрия. К полученному раствору добавили хлорид железа (III). Выпавший осадок отфильтровали и прокалили. Твердый остаток растворили в йодоводородной кислоте. Напишите уравнения четырех описанных реакций.
11. Алюминий прореагировал с раствором гидроксида натрия. Выделившийся газ пропустили над нагретым порошком оксида меди (II). Образовавшееся простое вещество растворили при нагревании в концентрированной серной кислоте. Полученную соль выделили и добавили к раствору йодида калия. Напишите уравнения четырех описанных реакций.
12. Хлорат калия нагрели в присутствии катализатора, при этом выделился бесцветный газ. Сжиганием железа в атмосфере этого газа была получена железная окалина. Ее растворили в избытке соляной кислоты. К полученному при этом раствору добавили раствор, содержащий дихромат натрия и соляную кислоту. Напишите уравнения четырех описанных реакций.
13. Порошок магния нагрели в атмосфере азота. При взаимодействии полученного вещества с водой выделился газ. Газ пропустили через водный раствор сульфата хрома (III), в результате чего образовался серый осадок. Осадок отделили и обработали при нагревании раствором, содержащим пероксид водорода и гидроксид калия. Напишите уравнения описанных реакций.
14. Оксид хрома (VI) прореагировал с гидроксидом калия. Полученное вещество обработали серной кислотой, из образовавшегося раствора выделили соль оранжевого цвета. Эту соль обработали бромоводородной кислотой. Полученное простое вещество вступило в реакцию с сероводородом. Напишите уравнения четырех описанных реакций.
15. Твердый хлорид лития нагрели с концентрированной серной кислотой, выделившийся при этом газ растворили в воде. При взаимодействии полученного раствора с перманганатом калия образовалось простое газообразное вещество желто-зеленого цвета. При горении железной проволоки в этом веществе получили соль. Соль растворили в воде и смешали с раствором карбоната натрия. Напишите уравнения четырех описанных реакций.
Ответы: (в ответах представлены возможные варианты, в ЕГЭ вы можете написать свой вариант ответа. если он не противоречит химическим свойствам и методам получения веществ)
1. 2CrCl3 + 3K2CO3 + 3h3O → 2Cr(OH)3 + 3CO2↑ + 6KCl
CrCl3 +3LiOH → Cr(OH)3 + 3LiCl
K2CO3 + 2HBr → 2KBr + CO2 ↑ + h3O
HBr + LiOH → LiBr + h3O
2. MgBr2 + Na2CO3 → MgCO3 + 2NaBr
MgBr2 + 2LiOH → Mg(OH)2 + 2LiBr
Na2CO3 + 2HCl → 2NaCl + h3O + CO2↑
HCl + LiOH → LiCl + h3O
3. 2KMnO4 + K2SO3 + 2KOH → 2K2MnO4 + K2SO4 + h3O
2KMnO4 + 2K2SO3 + h3O → 2MnO2 + 3K2SO4 + 2KOH
2KMnO4 + 16HCl → 2MnCl2 + 5Cl2 + 2KcL + 8h3O
KOH + HCl → KCl + h3O
4. 2AlBr3 + 3Na2S + 6h3O → 2Al(OH)3 + 3h3S + 6AlBr
AlBr3 + 3LiOH → 3LiBr + Al(OH)3
Na2S + 2HCl → 2NaCl + h3S↑
HCl + LiOH → LiCl + h3O
5. S + Cl2 → SCl2
3S + 6NaOH → Na2SO3 + 2Na2S + 3h3O
Cl2 + 2KBr → 2KCl + Br2
Cl2 + 6NaOH → 5NaCl + NaClO3 + 3h3O
6. CaCl2 + Na2CO3 → CaCO3 + 2NaCl
CaCl2 + Ba(OH)2 → Ca(OH)2 + BaCl2
Na2CO3 + 2HBr → BaBr2 + 2h3O
2HBr + Ba(OH)2 → BaBr2 + 2h3O
7. 3S + 6KOH → K2SO3 + 2K2S + 3h3O
S + 6HNO3 → h3SO4 + 6NO2 + 2h3O
2S + Br2 → S2Br2
Br2 + 2NaOH → NaBr + NaBrO + h3O
8. 2P + 5Cl2 → 2PCl5
P + 5HNO3 → h4PO4 + 5NO2 + h3O
HNO3 + LiOH → LiNO3 + h3O
Cl2 + 6LiOH → 5LiClO3 + LiCl + 3h3O
9. Cl2 + S → SCl2
3Cl2 + 2Fe → 2FeCl3
Cl2 + h3 → 2HCl
Fe + S → FeS
10. 3Br2 + 2Fe → 2FeBr3
HCl + KOH → KCl + h3O
Fe + 2HCl → FeCl2 + h3↑
Br2 + 2KOH → KBr + KBrO + h3O
11. 2KMnO4 + 2KOH + K2SO3 → 2K2MnO4 + K2SO4 + h3O
2KMnO4 + 16HBr → 2MnBr2 + 5Br2 + 2KBr + 8h3O
K2SO3 + 2HBr → 2KBr + SO2↑ + h3O
KOH + HBr → KBr + h3O
12. 3h3S + 2KMnO4 → 2MnO2 + 3S + 2KOH + 2h3O
h3S + K2CO3 → KHCO3 + KHS
h3S + 8HNO3 → h3SO4 + 8NO2↑ + 4h3O
2HNO3 + K2CO3 → 2KNO3 + h3O + CO2
13. Br2 + 2NaI → 2NaI + Br2
2Br2 + 3Na2CO3 → 5NaBr + NaBrO3 + 3CO2↑
8NaI + 9h3SO4 → 4I2 + h3S + 8NaHSO4 + 4h3O
Na2CO3 + h3SO4 → Na2SO4 + CO2 + h3O
14. Na2S + 2AgNO3 → Ag2S + 2NaNO3
Na2S + 2HCl → 2NaCl + h3S↑
Na2S + 4h3O2 → Na2SO4 + 4h3O
AgNO3 + HCl → AgCl + HNO3
15. 2K + Br2 → 2KBr
2K + 2h3S → 2KHS + h3↑
Br2 + h3S → S + 2HBr
h3S + 8HNO3 → h3SO4 + 8NO2 + 4h3O
16. 2h3S + SO2 → 3S + 2h3O
h3S + Na2CO3 → NaHS + NaHCO3
3h3S + 2KMnO4 → 2MnO2 + 3S + 2KOH + 2h3O
2KMnO4 + 5SO2 + 2h3O → 2MnSO4 + 2h3SO4 + K2SO4
17. 2P + 5S → P2S5
P + 5HNO3 → h4PO4 + 5NO2 + h3O
S + 6HNO3 → h3SO4 + 6NO2 + 2h3O
HNO3 + NaOH → NaNO3 + h3O
18. 2P + 5Cl2 → 2PCl5
3Cl2 + 6KOH → 5KCl + KClO3 + 3h3O
P + 5HNO3 → h4PO4 + 5NO2 + h3O
HNO3 + KOH → KNO3 + h3O
19. 2Fe + 3Cl2 → 2FeCl3
Fe + 2HCl → FeCl2 + h3↑
Fe + S → FeS
S + Cl2 → SCl2
20. O2 + 4HBr → 2Br2 + 2h3O
2HBr + CuO → CuBr2 + h3O
6HBr + 2Al → 2AlBr3 + 3h3↑
3CuO + 2Al → Al2O3 + 3Cu
21. Cr(OH)3 + 3HBr → CrBr3 + 3h3O
Cr(OH)3 + 3KOH → K3[Cr(OH)6]
Cl2 + 2HBr → Br2 + 2HCl
3Cl2 + 6KOH → 5KCl + KClO3 + 3h3O
22. Zn(OH)2 + 2HNO3 → Zn(NO3)2 + 2h3O
Zn(OH)2 + 2NaOH → Na2[Zn(OH)4]
Br2 + 2NaOH → NaBr + NaBrO + h3O
Br2 + 6NaOH → 5NaBr + NaBrO3 + 3h3O
23. HClO3 + 5HCl → 3Cl2↑ + 3h3O
2HClO3 + I2 → Cl2 + 2HIO3
HCl + NaOH → NaCl + h3O
I2 + 2NaOH → NaI + NaIO + h3O
24. Br2 + 2NaI → 2NaBr + I2
Br2 + 2S → S2Br2
S + 6HNO3 → h3SO4 + 6NO2 + 2h3O
2NaI + 4HNO3 → I2 + 2NO2 + 2NaNO3 + h3O
25. Fe2(SO4)3 + 3Ba(NO3)2 → 3BaSO4↓ + 2Fe(NO3)3
Fe(NO3)3 + 3NaOH → Fe(OH)3↓ + 3NaNO3
2Fe(OH)3 → Fe2O3 + 3h3O
Fe2O3 + 6HCl → 2FeCl3 + 3h3O
26. 2Li + S → Li2S
Li2S + 2HCl → 2LiCl + h3S↓
2h3S + 3O2 → 2SO2 + 2h3O
SO2 + 2NaOH → Na2SO3 + h3O
27. 2KNO3 → 2KNO2 + O2↑
2h3S + O2 → 2S + 2h3O
S + Fe → FeS
FeS + 2HCl → FeCl2 + h3S↑
28. 2NaCl → 2Na + Cl2
Cl2 + h3 → 2HCl
16HCl + 2KMnO4 → 2MnCl2 + 5Cl2↑ + 2KCl + 8h3O
Cl2 + 2NaOH → NaCl + NaClO + h3O
29. 3NaNO3 + Cr2O3 + 2NaCO3 → 2Na2CrO4 + 3NaNO2 + 2CO2
CO2 + Ba(OH)2 → BaCO3↓ + h3O
BaCO3 + 2HCl → BaCl2 + CO2↑ + h3O
BaCl2 + 2AgNO3 → 2AgCl↑ + Ba(NO3)2
30. 2Li + h3 → 2LiH
LiH + h3O → LiOH + h3↑
h3 + Br2 → 2HBr
6LiOH + 3Cl2 → 5LiCl + LiClO3 + 3h3O
31. 2Na + O2 → Na2O2
2Na2O2 + 2CO2 → 2Na2CO3 + O2↑
Na2CO3 + 2HCl → 2NaCl + CO2↑ + h3O
NaCl + AgNO3 → AgCl↓ + NaNO3
32. 2K + S → K2S
K2S + 2HCl → h3S↑ + 2KCl
3h3S + K2Cr2O7 + 4h3SO4 → 3S↓ + Cr2(SO4)3 + K2SO4 + 7h3O
3S + 2Al → Al2S3
33. 4Mg + 10HNO3(разб.) → 4Mg(NO3)2 + N2O↑ + 5h3O
Mg(NO3)2 + 2NaOH → Mg(OH)2↓ + 2NaNO3
Mg(OH)2 + 2HBr → MgBr2 + 2h3O
3MgBr2 + 2Na3PO4 → Mg3(PO4)2↓ + 6NaBr
34. 3Ca + N2 → Ca3N2
Ca3N2 + 6h3O → 3Ca(OH)2 + 2Nh4↑
4Nh4 + SO2 → 4NO + 6h3O
Ca(OH)2 + 2HCl → CaCl2 + 2h3O
35. 4Ba + 10HNO3 → 4Ba(NO3)2 + N2O↑ + 5h3O
Ba(NO3)2 → Ba(NO2)2 + O2↑
Ba(NO3)2 + Na2SO4 → BaSO4↓ + 2NaNO3
Ba(NO3)2 + NaCO3 → BaCO3↓ + 2NaNO3
36. 8Al + 3Fe3O4 → 4Al2O3 + 9Fe
Al2O3 + 2NaOH + 3h3O → 2Na[Al(OH)4]
2Fe + 3Cl2 → 2FeCl3
3Na[Al(OH)4] + AlCl3 → 4Al(OH)3 + 3NaCl
37. BaSO4 + 4C → BaS + 4CO↑
BaS + 2HCl → BaCl2 + h3S↑
2h3S + SO2 → 2h3O + 3S
BaCl2 + Na2SO3 → BaSO3↓ + 2NaCl
38. Si + 2NfOH + h3O → NaSiO3 + 2h3↑
Na2SiO3 + CO2 → Na2CO3 + SiO2↓
SiO2 + 4HF → SiF4 + 2h3O
SiO2 + 2Mg → Si + 2MgO
39. N2 + 3h3 → 2Nh4
Nh4 + HNO3 → Nh5NO3
Nh5NO3 → N2O + 2h3O
Nh5NO3 + NaOH → NaNO3 + Nh4↑ + h3O
40. P + 5HNO3 → h4PO4 + 5NO2 + h3O
2NO2 + 2KOH → KNO2 + KNO3 + h3O
h4PO4 + 3NaOH → Na3PO4 + 3h3O
2Na3PO4 + 3CaCl2 → Ca3(PO4)2↓ + 6NaCl
41. 3O2 ↔ 2O3
O3 + 2KI + h3O → I2↓ + O2↑ + 2KOH
O2 + 2Na → Na2O2
2Na2O2 + CO2 → 2Na2CO3 + O2
42. Cu + 2h3SO4 → CuSO4 + SO2↑ + 2h3O
SO2 + 2KOH → K2SO3 + h3O
CuSO4 + 2NaOH → NaSO4 + Cu(OH)2↓
Cu(OH)2 + 2HCl → CuCl2 + 2h3O
43. 2Cr + 3Cl2 → 2CrCl2
CrCl3 + 2KOH → Cr(OH)3↓ + 3KCl
2Cr(OH)3 + 3h3O2 + 4KOH → 2K2CrO4 + 8h3O
2K2CrO4 + 16HCl → 2CrCl3 + 4KCl + 3Cl2↑ + 8h3O
44. 2KMnO4 + 16HCl → 2MnCl2 + 5Cl2 + 2KCl + 8h3O
MnCl2 + 2KOH → Mn(OH)2↓ + 2KCl
6KOH + 3Cl2 → 5KCl + KClO3 + 3h3O
2KClO3 → 2KCl + 3O2
1. Fe + h3SO4 → FeSO4 + h3↑
FeSO4 + KMnO4 + 3KOH → Fe(OH)3 + K2MnO4 + K2SO4
Fe(OH)3 + 3HCl → FeCl3 + 3h3O
2FeCl2 + Cu → CuCl2 + 2FeCl2
2. 2AgNO3 →(t) 2Ag + 2NO2 + O2
Ag + 2HNO3(конц) → AgNO3 + NO2↑ + h3O
2NO2 + 2KOH → KNO3 + KNO2 + h3O
3KNO2 + K2Cr2O7 + 4h3SO4 → 3KNO3 + Cr2(SO4)3 +K2SO4 + 4h3O
3. Fe + 2HCl → FeCl2 + h3↑
FeCl2 + 2Nh4 + 2h3O →Fe(OH)2↓ + 2Nh5Cl
2Fe(OH)2↓ + h3O2 → 2Fe(OH)3↓
Fe(OH)3 + NaOH →(t) NaFeO2 + 2h3O↑
4. 2KMnO4 + 16HCl → 2MnCl2 + 5Cl2↑ + 2KCl + 8h3O
Cu + Cl2 →(t) CuCl2
CuCl2 + 2AgNO3 → 2AgCl↓ + Cu(NO3)2
2Cu(NO3)2 + 4KI → 2CuI↓ + I2 + 4KNO3
5. Ca3(PO4)2 + 5C + 3SiO2 →(t) 2P + 5CO↑ + 3CaSiO3
2P + 5Cl2 → 2PCl5
PCl5 + 8KOH → K3PO4 + 5KCl + 4h3O
2K3PO4 + 3Ca(OH)2 → Ca3(PO4)2 + 6KOH
6. 2Al + 2NaOH + 6h3O → 2Na[Al(OH)4] + 3h3↑
Na[Al(OH)4] + CO2 → NaHCO3 + Al(OH)3↓
2Al(OH)3 →(t) Al2O3 + 3h3O
Al2O3 + Na2CO3 →(t) 2NaAlO2 + CO2
7. 2Cu + I2 → 2CuI
2CuI + 4h3SO4 →(t) 2CuSO4 + 2SO2 + I2 + 4h3O
CuSO4 + 2KOH → Cu(OH)2↓ + K2SO4
Cu(OH)2 →(t) CuO + h3O
8. 2CuCl2 + 2 Na2CO3 + h3O → (CuOH)2CO3↓ + CO2 + 4NaCl
(CuOH)2CO3 →(t) 2CuO + h3O + CO2↑
CuO + h3 →(t) Cu + h3O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO↑ + 4h3O
9. Al2O3 + Na2CO3 →(t) 2NaAlO2 + CO2
NaAlO2 + 4HCl → NaCl + AlCl3 + 2h3O
AlCl3 + 3Nh4xh3O → Al(OH)3↓ + 3Nh5Cl
Al(OH)3 + 3NaOH → Na3[Al(OH)6]
10. 2NaCl + 2h3O → 2NaOH + h3 + Cl2 (электролиз)
3NaOH + FeCl3 → Fe(OH)3↓ + 3NaCl
2Fe(OH)3 →(t) Fe2O3 + 3h3O
Fe2O3 + 6HI → 2FeI2 + I2 + 3h3O
11. 2Al + 2NaOH + 6h3O → 2Na[Al(OH)4] + 3h3↑
CuO + h3 →(t) Cu + h3O
Cu + 2h3SO4 → CuSO4 + SO2 + 2h3O
2CuSO4 + 4KI → 2CuI + I2 + 2K2SO4
12. 2KClO3 →(t) 2KCl + 3O2↑
3Fe + 2O2 →(t) Fe3O4
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4h3O
6FeCl2 + Na2Cr2O7 + 14HCl → 6FeCl3 + 2CrCl3 + 2NaCl + 7h3O
13. 3Mg + N2 → Mg3N2
Mg2N2 + 6h3O → 3Mg(OH)2 + 2Nh4↑
6Nh4 + Cr2(SO4)3 + 6h3O → 2Cr(OH)3↓ + 3(Nh5)2SO4
2Cr(OH)3 +3h3O2 + 4KOH → 2K2CrO4 + 8h3O
14. CrO3 + 2KOH → K2CrO4 + h3O
2K2CrO4 + h3SO4 → K2Cr2O7 + K2SO4 + h3O
K2Cr2O7 + 14 HBr → 3Br2 + 2CrBr3 + 2KBr + 7h3O
h3S + Br2 → S + 2HBr
15. LiCl + h3SO4 → HCl↑ + LiHSO4
2KMnO4 + 16HCl → 2MnCl2 + 5Cl2↑ + 2KCl + 8h3O
2Fe + 3Cl2 → 2FeCl3
2FeCl3 + 3Na2CO3 + 3h3O → 2Fe(OH)3↓ + 6NaCl + 3CO2↑
cleverpenguin.ru
Тренировочные задания. Реакции, подтверждающие взаимосвязь различных классов неорганических веществ

1. Натрий сплавили с серой. Образовавшееся соединение обработали соляной кислотой, выделившийся газ нацело прореагировал с оксидом серы (IV). Образовавшееся вещество обработали концентрированной азотной кислотой. Напишите уравнения описанных реакций.
2. Натрий сожгли в избытке кислорода. Образовавшееся вещество обработали водой. Полученную смесь прокипятили, после чего в горячий раствор пропустили хлор. Напишите уравнения описанных реакций.
3. Калий нагрели в атмосфере азота. Полученное соединение обработали избытком соляной кислоты, после чего к образовавшейся смеси солей добавили суспензию гидроксида кальция и нагрели. Полученный газ пропустили над раскаленным оксидом меди (II). Напишите уравнения описанных реакций.
4. Калий сожгли в атмосфере хлора, образовавшуюся соль обработали избытком водного раствора нитрата серебра. Выпавший осадок отфильтровали, фильтрат выпарили и осторожно нагрели. Образовавшуюся соль обработали водным раствором брома. Напишите уравнения описанных реакций.
5. Барий растворили в избытке соляной кислоты, к полученному раствору добавили избыток раствора сульфата натрия. Выпавший осадок отфильтровали и прокалили с углем. Образовавшийся газ пропустили над оксидом железа (III). Напишите уравнения описанных реакций.
6. Барий растворили в воде. К полученному раствору добавили сульфат калия, выпавший осадок отфильтровали, после чего через горячий фильтрат пропустили газообразный хлор. Реакционную массу выпарили, а затем прокалили до образования одной соли. Напишите уравнения описанных реакций.
7. Алюминий растворили в соляной кислоте. К полученному раствору добавили избыток раствора карбоната калия. Выпавший осадок растворили в избытке раствора едкого калия, а выделившийся газ пропустили над раскаленным углем. Напишите уравнения описанных реакций.
8. Алюминий растворили в водном растворе горячего гидроксида натрия. К полученному раствору добавили по каплям разбавленную соляную кислоту до прекращения выделения осадка. Выделившийся в первой реакции газ пропустили над раскаленным оксидом меди (II). Полученное простое вещество растворили в разбавленной азотной кислоте. Напишите уравнения описанных реакций.
9. Углерод сожгли в недостатке кислорода, образовавшийся газ пропустили над оксидом меди (II). Полученное простое вещество сплавили с серой, а продукт этой реакции сожгли в кислороде. Напишите уравнения описанных реакций.
10. Кремний сожгли в кислороде. Продукт реакции сплавили с карбонатом натрия, образовавшееся вещество обработали избытком соляной кислоты при нагревании. Осадок отфильтровали, а к фильтрату добавили раствор нитрата серебра. Напишите уравнения описанных реакций.
11. Газ, образовавшийся при взаимодействии азота и водорода, разделили на две части. Первую пропустили над раскаленным оксидом меди (II), вторую сожгли в кислороде в присутствии катализатора. Образовавшийся газ в избытке кислорода превратился в газ бурого цвета. Напишите уравнения описанных реакций.
12. Разбавленная азотная кислота прореагировала с магнием с выделением бесцветного газа. В его атмосфере сожгли графит с образованием простого и сложного веществ. Простое вещество при нагревании вступило в реакцию с кальцием, а сложное прореагировало с избытком раствора гидроксида натрия. Напишите уравнения описанных реакций.
13. Аммиак поглотили азотной кислотой, полученную соль нагрели до образования только двух оксидов. Один из них прореагировал с натрием, а второй при высокой температуре прореагировал с медью. Напишите уравнения описанных реакций.
14. Оксид азота (II) доокислили кислородом. Продукт реакции поглотили раствором гидроксида калия, через полученный раствор пропускали кислород до тех пор, пока в нем не образовалась только одна соль. Напишите уравнения описанных реакций.
15. Фосфат кальция прокалили с песком и углем. Полученное простое вещество сожгли в кислороде, продукт реакции растворили в воде и нейтрализовали гидроксидом натрия. Напишите уравнения описанных реакций.
16. Фосфор сожгли в избытке кислорода, а образовавшееся вещество сплавили с оксидом натрия. Полученную соль разделили на две части: первую ввели в реакцию с хлоридом кальция, а вторую — с нитратом серебра. Напишите уравнения описанных реакций.
17. Железо сплавили с серой, полученную соль обработали разбавленной серной кислотой. Выделившийся газ сожгли в избытке кислорода, а образовавшееся соединение поглотили раствором гидроксида калия. Напишите уравнения описанных реакций.
18. Серу сплавили с алюминием, полученную соль растворили в воде. Выпавший осадок растворили в избытке гидроксида калия, а газ сожгли в избытке кислорода. Напишите уравнения описанных реакций.
19. Серу растворили в кипящем растворе гидроксида натрия. К полученному раствору добавили хлорид цинка, выпавший осадок отфильтровали и сожгли в кислор оде. Образовавшийся при этом газ прореагировал с сероводородом. Напишите уравнения описанных реакций.
20. Оксид серы (IV) окислили кислородом в присутствии катализатора. Образовавшееся вещество поглотили избытком гидроксида натрия, а к полученному раствору добавили раствор хлорида бария. Выпавший осадок отфильтровали и прокалили с коксом. Напишите уравнения описанных реакций.
21. Железо сожгли в атмосфере хлора. Полученную соль растворили в воде и добавили к ней раствор йодида калия. Выпавший осадок простого вещества отделили и разделили на две части. Первую обработали разбавленной азотной кислотой, а вторую нагрели в атмосфере водорода. Напишите уравнения описанных реакций.
22. Железо растворили в соляной кислоте, к полученному раствору добавили гидроксид натрия до прекращения выделения осадка. В полученную реакционную массу вначале пропустили кислород, а затем добавили избыток йодоводородной кислоты до прекращения выделения осадка. Напишите уравнения описанных реакций.
23. Цинк растворили в растворе гидроксида калия. Выделившийся газ прореагировал с литием, а к полученному раствору по каплям добавляли соляную кислоту до прекращения выделения осадка. Его отфильтровали и прокалили. Напишите уравнения описанных реакций.
24. Перманганат калия обработали избытком раствора соляной кислоты, образовался раствор, и выделился газ. Раствор разделили на две части: к первой добавили гидроксид калия, а ко второй — нитрат серебра. Выделившийся газ прореагировал с раствором гидроксида калия при охлаждении. Напишите уравнения описанных реакций.
25. Осадок, полученный при взаимодействии растворов сульфата железа (III) и нитрата бария, отфильтровали. Фильтрат обработали избытком едкого натра. Выпавший осадок отделили и прокалили. Полученное вещество обработали избытком раствора соляной кислоты. Напишите уравнения описанных реакций.
26. Литий сплавили с серой. Полученную соль обработали разбавленной соляной кислотой, при этом выделился газ с запахом тухлых яиц. Этот газ сожгли в избытке кислорода, при этом выделился газ с характерным резким запахом. При пропускании этого газа в избыток гидроксида натрия образовалась средняя соль. Напишите уравнения описанных реакций.
27. Нитрат калия подвергли термическому разложению. Выделившийся газ на свету пропустили через насыщенный раствор сероводорода в воде. Выпавшее вещество желтого цвета сплавили с железом, а полученную соль обработали разбавленной соляной кислотой. Напишите уравнения описанных реакций.
28. Расплав хлорида натрия подвергли электролизу. Газ, выделившийся на аноде, прореагировал с водородом с образованием нового газообразного вещества с характерным резким запахом. Его растворили в воде и обработали расчетным количеством перманганата калия, при этом образовался газ желто-зеленого цвета. Это вещество вступает при охлаждении в реакцию с гидроксидом натрия. Напишите уравнения описанных реакций.
29. Нитрат натрия сплавили с оксидом хрома в присутствии карбоната натрия. Выделившийся при этом газ прореагировал с избытком раствора гидроксида бария с выпадением осадка белого цвета. Осадок растворили в избытке раствора соляной кислоты и в полученный раствор добавили нитрат серебра до прекращения выделения осадка. Напишите уравнения описанных реакций.
30. Литий прореагировал с водородом. Продукт реакции растворили в воде, при этом образовался газ, реагирующий с бромом, а полученный раствор при нагревании прореагировал с хлором с образованием смеси двух солей. Напишите уравнения описанных реакций.
31. Натрий сожгли на воздухе. Образовавшееся при этом твердое вещество поглощает углекислый газ с выделением кислорода и выделением соли. Последнюю соль растворили в соляной кислоте, а к полученному при этом раствору добавили раствор нитрата серебра. При этом выпал белый творожистый осадок. Напишите уравнения описанных реакций.
32. Калий сплавили с серой. Полученную соль обработали соляной кислотой. Выделившийся при этом газ пропустили через раствор бихромата калия в серной кислоте. Выпавшее вещество желтого цвета отфильтровали и сплавили с алюминием. Напишите уравнения описанных реакций.
33. Магний растворили в разбавленной азотной кислоте. К полученному раствору последовательно добавили гидроксид натрия, бромоводородную кислоту, фосфат натрия. Напишите уравнения описанных реакций.
34. Кальций сожгли в атмосфере азота. Полученную соль разложили кипящей водой. Выделившийся газ сожгли в кислороде в присутствии катализатора, а к суспензии прибавили раствор соляной кислоты. Напишите уравнения описанных реакций.
35. Барий растворили в разбавленной азотной кислоте, при этом выделился бесцветный газ — несолеобразующий оксид. Полученный раствор разделили на три части. Первую — выпарили досуха, полученный осадок прокалили. Ко второй части прилили раствор сульфата натрия до прекращения выделения осадка; к третьей добавили раствор карбоната натрия. Напишите уравнения описанных реакций.
36. Алюминий вступил в реакцию с Fe3O4. Полученную смесь веществ растворили в концентрированном растворе гидроксида натрия и отфильтровали. Твердое вещество сожгли в атмосфере хлора, а фильтрат обработали концентрированным раствором хлорида алюминия. Напишите уравнения описанных реакций.
37. Сульфат бария сплавили с коксом. Твердый остаток растворили в соляной кислоте, выделившийся газ вступил в реакцию с оксидом серы (IV), а раствор — с сульфитом натрия. Напишите уравнения описанных реакций.
38. Кремний растворили в концентрированном растворе гидроксида натрия. Через полученный раствор пропустили углекислый газ. Выпавший осадок отфильтровали, высушили и разделили на две части. Первую растворили в плавиковой кислоте, вторую сплавили с магнием. Напишите уравнения описанных реакций.
39. Азот при нагревании на катализаторе прореагировал с водородом. Полученный газ поглотили раствором азотной кислоты, выпарили досуха и полученное кристаллическое вещество разделили на две части. Первую разложили при температуре 190–240 °C, при этом образовался только один газ и водяные пары. Вторую часть нагрели с концентрированным раствором едкого натра. Напишите уравнения описанных реакций.
40. Красный фосфор окислили кипящей азотной кислотой. Выделившийся при этом газ поглотили раствором гидроксида калия. Продукт окисления в первой реакции нейтрализовали гидроксидом натрия, а к образовавшейся реакционной массе по каплям добавили раствор хлорида кальция до прекращения выделения осадка. Напишите уравнения описанных реакций.
41. Кислород подвергли воздействию электроразряда в озонаторе. Полученный газ пропустили через водный раствор йодида калия, при этом выделился новый газ без цвета и запаха, поддерживающий горение и дыхание. В атмосфере последнего газа сожгли натрий, а полученное при этом твердое вещество прореагировало с углекислым газом. Напишите уравнения описанных реакций.
42. Концентрированная серная кислота прореагировала с медью. Выделившийся при этом газ полностью поглотили избытком раствора гидроксида калия. Продукт окисления меди смешали с расчетным количеством гидроксида натрия до прекращения выделения осадка. Последний растворили в избытке соляной кислоты. Напишите уравнения описанных реакций.
43. Хром сожгли в атмосфере хлора. К образовавшейся соли добавили по каплям гидроксид калия до прекращения выделения осадка. Полученный осадок окислили перекисью водорода в среде едкого калия и упарили. К полученному твердому остатку добавили избыток горячего раствора концентрированной соляной кислоты. Напишите уравнения описанных реакций.
44. Перманганат калия обработали концентрированной горячей соляной кислотой. Выделившийся при этом газ собрали, а к реакционной массе по каплям прибавили раствор гидроксида калия до прекращения выделения осадка. Собранный газ пропустили через горячий раствор гидроксида калия, при этом образовалась смесь двух солей. Раствор выпарили, твердый остаток прокалили в присутствии катализатора, после чего в твердом остатке осталась одна соль. Напишите уравнения описанных реакций.
Ответы




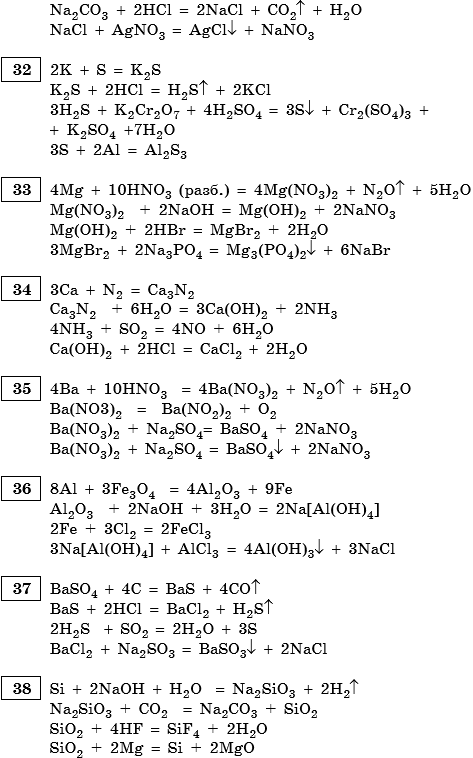

himi4ka.ru
С-2 2013 год - Содержательные блоки курса химии - ЕГЭ - Каталог статей
1) Нитрат меди прокалили, полученный твёрдый осадок растворили в серной кислоте. Через раствор пропустили сероводород, полученный чёрный осадок подвергли обжигу, а твёрдый остаток растворили при нагревании в концентрированной азотной кислоте.
2) Фосфат кальция сплавили с углём и песком, затем полученное простое вещество сожгли в избытке кислорода, продукт сжигания растворили в избытке едкого натра. К полученному раствору прилили раствор хлорида бария. Полученный осадок обработали избытком фосфорной кислоты.
3) Медь растворили в концентрированной азотной кислоте, полученный газ смешали с кислородом и растворили в воде. В полученном растворе растворили оксид цинка, затем к раствору прибавили большой избыток раствора гидроксида натрия.
4) На сухой хлорид натрия подействовали концентрированной серной кислотой при слабом нагревании, образующийся газ пропустили в раствор гидроксида бария. К полученному раствору прилили раствор сульфата калия. Полученный осадок сплавили с углем. Полученное вещество обработали соляной кислотой.
5) Навеску сульфида алюминия обработали соляной кислотой. При этом выделился газ и образовался бесцветный раствор. К полученному раствору добавили раствор аммиака, а газ пропустили через раствор нитрата свинца. Полученный при этом осадок обработали раствором пероксида водорода.
6) Порошок алюминия смешали с порошком серы, смесь нагрели, полученное вещество обработали водой, при этом выделился газ и образовался осадок, к которому добавили избыток раствора гидроксида калия до полного растворения. Этот раствор выпарили и прокалили. К полученному твёрдому веществу добавили избыток раствора соляной кислоты.
7) Раствор иодида калия обработали раствором хлора. Полученный осадок обработали раствором сульфита натрия. К полученному раствору прибавили сначала раствор хлорида бария, а после отделения осадка — добавили раствор нитрата серебра.
8) Серо-зелёный порошок оксида хрома (III) сплавили с избытком щёлочи, полученное вещество растворили в воде, при этом получился тёмно-зелёный раствор. К полученному щелочному раствору прибавили пероксид водорода. Получился раствор желтого цвета, который при добавлении серной кислоты приобретает оранжевый цвет. При пропускании сероводорода через полученный подкисленный оранжевый раствор он мутнеет и вновь становится зелёным.
9) Алюминий растворили в концентрированном растворе гидроксида калия. Через полученный раствор пропускали углекислый газ до прекращения выделения осадка. Осадок отфильтровали и прокалили. Полученный твердый остаток сплавили с карбонатом натрия.
10) Кремний растворили в концентрированном растворе гидроксида калия. К полученному раствору добавили избыток соляной кислоты. Помутневший раствор нагрели. Выделившийся осадок отфильтровали и прокалили с карбонатом кальция. Напишите уравнения описанных реакций.
11) Оксид меди(II) нагрели в токе угарного газа. Полученное вещество сожгли в атмосфере хлора. Продукт реакции растворили в воде. Полученный раствор разделили на две части. К одной части добавили раствор иодида калия, ко второй – раствор нитрата серебра. И в том и в другом случае наблюдали образование осадка. Напишите уравнения четырех описанных реакций.
12) Нитрат меди прокалили, образовавшееся твердое вещество растворили в разбавленной серной кислоте. Раствор полученной соли подвергли электролизу. Выделившееся на катоде вещество растворили в концентрированной азотной кислоте. Растворение протекало с выделением бурого газа. Напишите уравнения четырех описанных реакций.
13) Железо сожгли в атмосфере хлора. Полученное вещество обработали избытком раствора гидроксида натрия. Образовался бурый осадок, который отфильтровали и прокалили. Остаток после прокаливания растворили в иодоводородной кислоте. Напишите уравнения четырех описанных реакций.
14) Порошок металлического алюминия смешали с твердым иодом и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка. Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдали выпадение осадка. Напишите уравнения четырех описанных реакций.
15) В результате неполного сгорания угля получили газ, в токе которого нагрели оксид железа(III). Полученное вещество растворили в горячей концентрированной серной кислоте. Образовавшийся раствор соли подвергли электролизу. Напишите уравнения четырех описанных реакций.
16) Некоторое количество сульфида цинка разделили на две части. Одну из них обработали азотной кислотой, а другую подвергли обжигу на воздухе. При взаимодействии выделившихся газов образовалось простое вещество. Это вещество нагрели с концентрированной азотной кислотой, причем выделился бурый газ. Напишите уравнения четырех описанных реакций.
17) Серу сплавили с железом. Продукт реакции растворили в воде. Выделившийся при этом газ сожгли в избытке кислорода. Продукты горения поглотили водным раствором сульфата железа(III). Напишите уравнения четырех описанных реакций.
18) Железо сожгли в хлоре. Полученную соль добавили к раствору карбоната натрия, при этом выпал бурый осадок. Этот осадок отфильтровали и прокалили. Полученное вещество растворили в иодоводородной кислоте. Напишите уравнения четырех описанных реакций.
19) Раствор иодида калия обработали избытком хлорной воды, при этом наблюдали сначала образование осадка, а затем – его полное растворение. Образовавшуюся при этом иодосодержащую кислоту выделили из раствора, высушили и осторожно нагрели. Полученный оксид прореагировал с угарным газом. Запишите уравнения описанных реакций.
20) Порошок сульфида хрома(III) растворили в серной кислоте. При этом выделился газ и образовался окрашенный раствор. К полученному раствору добавили избыток раствора аммиака, а газ пропустили через нитрата свинца. Полученный при этом черный осадок побелел после обработки его пероксидом водорода. Запишите уравнения описанных реакций.
21) Порошок алюминия нагрели с порошком серы, полученное вещество обработали водой. Выделившийся при этом осадок обработали избытком концентрированного раствора гидроксида калия до его полного растворения. К полученному раствору добавили раствор хлорида алюминия и вновь наблюдали образование белого осадка. Запишите уравнения описанных реакций.
22) Нитрат калия нагрели с порошкообразным свинцом до прекращения реакции. Смесь продуктов обработали водой, а затем полученный раствор профильтровали. Фильтрат подкислили серной кислотой и обработали иодидом калия. Выделившееся простое вещество нагрели с концентрированной азотной кислотой. В атмосфере образовавшегося при этом бурого газа сожгли красный фосфор. Запишите уравнения описанных реакций.
23) Медь растворили в разбавленной азотной кислоте. К полученному раствору добавили избыток раствора аммиака, наблюдая сначала образование осадка, а затем – его полное растворение с образованием темно-синего раствора. Полученный раствор обработали серной кислотой до появления характерной голубой окраски солей меди. Запишите уравнения описанных реакций.
24) Магний растворили в разбавленной азотной кислоте, причем выделение газа не наблюдалось. Полученный раствор обработали избытком раствора гидроксида калия при нагревании. Выделившийся при этом газ сожгли в кислороде. Запишите уравнения описанных реакций.
25) Смесь порошков нитрита калия и хлорида аммония растворили в воде и раствор осторожно нагрели. Выделившийся газ прореагировал с магнием. Продукт реакции внесли в избыток раствора соляной кислоты, при этом выделение газа не наблюдалось. Полученную магниевую соль в растворе обработали карбонатом натрия. Запишите уравнения описанных реакций.
26) Оксид алюминия сплавили с гидроксидом натрия. Продукт реакции внесли в раствор хлорида аммония. Выделившийся газ с резким запахом поглощен серной кислотой. Образовавшуюся при этом среднюю соль прокалили. Запишите уравнения описанных реакций.
27) Хлор прореагировал с горячим раствором гидроксида калия. При охлаждении раствора выпали кристаллы бертолетовой соли. Полученные кристаллы внесли в раствор соляной кислоты. Образовавшееся простое вещество прореагировало с металлическим железом. Продукт реакции нагрели с новой навеской железа. Запишите уравнения описанных реакций.
28) Медь растворили в концентрированной азотной кислоте. К полученному раствору добавили избыток раствора аммиака, наблюдая сначала образование осадка, а затем – его полное растворение. Полученный раствор обработали избытком соляной кислоты. Запишите уравнения описанных реакций.
29) Железо растворили в горячей концентрированной серной кислоте. Полученную соль обработали избытком раствора гидроксида натрия. Выпавший бурый осадок отфильтровали и прокалили. Полученное вещество сплавили с железом. Напишите уравнения четырёх описанных реакций.
svetlanka-good.ucoz.ru