3.4 Электронное строение комплексов хрома (III). Комплексы хрома
Комплекс - хром - Большая Энциклопедия Нефти и Газа, статья, страница 1
Комплекс - хром
Cтраница 1
Комплексы хрома хемосорбируются на отрицательно заряженной стеклянной поверхности, приводя к уменьшению адсорбционной способности. В качестве полифункциональных гидрофобно-адгезионных соединений, способных взаимодействовать не с одним, а с многими типами полимеров, применяются так называемые универсальные аппретуры. [1]
Комплексы хрома и марганца характеризуются значительным вкладом дативной компоненты в образование связи металл - лиганд. [2]
Комплексы хрома ( Ш) и кобальта ( Ш) мало реакционноспо-собны; для объяснения этого факта выдвинут ряд теорий. Так, например, можно в течение нескольких часов нагревать с обратным холодильником смесь соли Co ( Nh4) 6Cl3 с 6 М соляной кислотой без ее изменения, хотя при этом образуются СоС12, хлористый аммоний и хлор. [3]
Комплекс хрома ( III) парамагнитен, поэтому метод ЯМР нельзя непосредственно использовать для определения цис - траке-изомерии. Однако Фай и Пайпер смогли разделить изомеры методом жидкостной хроматографии и идентифицировать их рентгенографически. В растворах комплексов хрома ( III), родия ( III) и кобальта ( III) содержится при равновесии приблизительно 80 % транс - и 20 % мс-изомера. [4]
Комплексы хрома, меди и никеля легко разрушаются азотной кислотой при нагревании исследуемого раствора. [5]
Комплекс хрома имеет дипольный мо - мент 1 18 0 1D и вступает ъ реакцию каталитического гидрирования ненасыщенных колец. На основании этих данных и ИК-н ЯМР-спектров предложена структура 6.4, согласно которой вещество представляет собой производное комплекса л - С7Н7Сг - - л - CsHs. Комплекс железа не окисляется и не полярен, но он вступает в реакцию восстановления колец. [6]
Арентрикарбонильные комплексы хрома и их молибденовые аналоги были широко изучены с целью выяснения степени реакционной способности ароматической части таких молекул. [7]
Все комплексы хрома ( III), которые имеют структуру, показанную в предыдущем примере, обладают шестью лигандами, каждый из которых связан с центральным атомом ковалентной связью. Поэтому мы можем утверждать, что координационное число хрома ( III) равно шести. В общем случае координационное число зависит от электронной структуры атома металла, а также от структуры, заряда и электроотрицательности лигандов. [8]
Алл ильные комплексы хрома, ниобия и титана являются катализаторами 1 2-полимеризации бутадиена, а бис-я - ал л ил никель и / прис-я-аллилкобальт - катализаторами олигомеризации, в первом случае с образованием циклододекатриена, во втором случае - линейных димеров. Продукты взаимодействия всех этих соединений с растворами безводных кислот являются катализаторами 1 4 - г ( ыс-полимеризации бутадиена. [9]
Например, комплексы хрома ( III) кинетически инертны и, следовательно, комплексы с ЭДТА образуются слишком медленно. [11]
Среди - комплексов хрома ( II) необходимо отметить хромоцен - [ Cr ( C5Hs) 2 ] - кристаллическое вещество красного цвета, с температурой плавления, близкой к ферроцену, и по молекулярной структуре аналогичное последнему. [13]
Каждый из комплексов хрома ( III) в приведенной реакции обладает совершенной октаэдрической геометрией. Другими словами, лиган-ды симметрично расположены вокруг центрального атома и длина шести связей хром ( III) - лиганд идентична. Лиганд может быть нейтральной молекулой, как вода, или может быть ионом, как цианид-ион. В других случаях комплекс может быть нейтральной молекулой. В данном примере центральный атом - хром - - имеет степень окисления 3 в обоих комплексах. [14]
При рН 2 комплекс хрома неустойчив. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
3.4 Электронное строение комплексов хрома (III).
Магнитные свойства октаэдрических комплексов хрома (III) можно объяснить довольно просто. Во всех таких комплексах должно быть три неспаренных электрона независимо от силы поля лигандов, что подтверждается на опыте для всех известных одноядерных соединений. Далее, теория предсказывает, что значения магнитных моментов должны приближаться или быть несколько ниже чисто спинового значения. Это также подтверждается данными эксперимента.
Спектры комплексных соединений CrIII также легко поддаются теоретической интерпретации. Здесь возможны три перехода, разрешенные по спину, которые и наблюдаются у большинства комплексов.
Интересными должны быть магнитные свойства комплексных ацетатов хрома с 2,2-dipy и 1,10-phen. Поскольку карбоксилатам хрома (III) свойственно образование кластеров типа [Cr3O(Ac)6h3O]+, здесь наблюдается понижение магнитных моментов по сравнению с только спиновыми.
От всех рассмотренных выше комплексов отличается производное нитрата фенантролинового комплекса Cr(phen)2(NO3)I2. Этой формуле отвечает пятерная координация центрального иона, и именно этим, очевидно, можно объяснить спектральные особенности, проявляющиеся в отсутсвии каких-либо признаков расщепления, характерного для искаженных октаэдрических полей. По-видимому, каждый атом хрома в катионе окружен двумя молекулами бидентатного лиганда, на внешней сфере – ионы йода, и взаимодействие спинов происходит через NO3-.
Конечно, аномалии магнитных свойств некоторых комплексов хрома обусловлены не только антиферромагнетизмом, но и другими факторами: спин-орбитальное взаимодействие, тетрагональное искажение и др.
3.5 Фосфоресцирующие комплексы. 16
Первоначальное возбуждение комплекса обычно приводит к заселению состояния посредством перехода, разрешенного по спину, поэтому механизм фосфоресценции включает безызлучательное превращение начального возбужденного состояния в другое возбужденное состояние, отличающееся по мультиплетности17. Это второе состояние действует как накопитель энергии, потому что переход в основное состояние запрещен по спину. Излучательный переход в основное состояние происходит медленно, так что фосфоресценция комплексов хрома, как и всех d-металлов может длиться в течение нескольких микросекунд или даже дольше.
Известный пример фосфоресценции представляет собой рубин, в котором ионы Cr3+ замещают небольшую часть ионов Al3+ в оксиде алюминия.
Каждый ион Cr3+ окружен октаэдрически шестью ионами O2-, и исходным возбуждением является разрешенный по спину процесс:
t2g2eg1 ← t2g3: 4T2g ← 4A2g и 4T1g ← 4A2g.
Поглощение наблюдается в зеленой и фиолетовой областях спектра и отвечает за красный цвет драгоценного кампя (см. рис. 5).
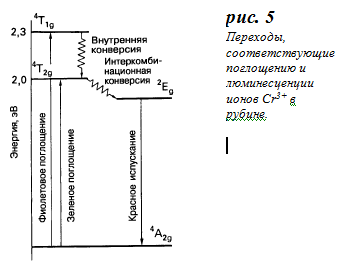
Подобная 2Е → 4А фосфоресценция может наблюдаться для многих комплексов хрома (III) в растворе. Испускание происходит всегда в красной области, и значения длин волн близки к длине волны излучения рубина. Терм 2Е принадлежит t2g3 – конфигурации, которая является основным состоянием, и сила поля лигандов не имеет значение.
studfiles.net
3.3 Многоядерные комплексы хрома (III). Комплексные соединения хрома. Соль Рейнеке
Похожие главы из других работ:
Вискозиметрическое исследование комплексообразования ЭЭАКК/АК с ионом стронция
1.1 Комплексы водорастворимых полимеров с различными классами соединений
Исследование взаимодействий комплементарных макромолекул и продуктов этих реакций - полимерных комплексов представляет одну из важнейших проблем химии и физики полимеров и молекулярной биологии...
Вискозиметрическое исследование комплексообразования ЭЭАКК/АК с ионом стронция
1.2 Интерполимерные комплексы водорастворимых полимеров
Интерполимерные (полимер-полимерные) комплексы образуются при взаимодействии химически и структурно комплементарных макромолекул. Интерполимерные комплексы (ИПК) могут быть стабилизированы системой ионных связей...
Вискозиметрическое исследование комплексообразования ЭЭАКК/АК с ионом стронция
1.3 Комплексы полимеров с низкомолекулярными соединениями
...
Вискозиметрическое исследование комплексообразования ЭЭАКК/АК с ионом стронция
1.3.1 Комплексы полимер - ион металла
Полимер-металлические комплексы образуются в результате взаимодействия между функциональными группами макромолекул и ионами переходным металлов (Cu2+, Cd2+, Zn2+, Ni2+, Co2+, Mg2+, Fe2+ и др.)...
Вискозиметрическое исследование комплексообразования ЭЭАКК/АК с ионом стронция
1.3.3 Молекулярные комплексы полимеров
Молекулярные комплексы полимеров являются продуктами нековалентных взаимодействий, в основном, между неиоными полимерами и различными низкомолекулярными соединениями. Это комплексы полиэтиленгликоля (ПЭГ) с резорцином...
Инфра-красная-люминесценция комплексов эрбия (III), иттербия (III), неодима (III)
4. Комплексы неодима, иттербия и эрбия с 8-гидроксихинолином
В настоящее время используют бидентатные и полидентатные комплексы на основе хинолина (рис. 5). Рис. 5. Некоторые производные хинолина, используемые для подготовки люминесцентных комплексов с ионами лантанидов. Ранее предполагалось...
Инфра-красная-люминесценция комплексов эрбия (III), иттербия (III), неодима (III)
5. Комплексы с полидентатными лигандами на основе 8-гидроксихинолина
Рассмотренные выше примеры показывают, что реакция с 8-гидроксихинолином и его производными с металлами лантаноидов дает различные комплексы с различной ядерностью и стехиометрией...
Исследование каталитических свойств полимерных комплексов
1.1 Полимерметаллические комплексы
Полимерметаллические комплексы образуются в результате взаимодействия между функциональными группами макромолекул и ионами переходным металлов (Cu2+, Cd2+, Zn2+, Ni2+, Co2+, Mg2+, Fe2+ и др.)...
Исследование каталитических свойств полимерных комплексов
1.4 Комплексы полимеров с простыми веществами и другими низкомолекулярными соединениями
Молекулярные комплексы полимеров являются продуктами нековалентных взаимодействий, в основном, между неионными полимерами и различными низкомолекулярными соединениями. Это комплексы полиэтиленгликоля (ПЭГ) с резорцином...
Исследование каталитических свойств полимерных комплексов
1.6 Интерполиэлектролитные комплексы
Широкое применение разнообразных химических фармакологических препаратов в сочетании с ухудшением экологической обстановки окружающей среды привело к резкому увеличению чувствительности человека к лекарствам (аллергические заболевания...
Исследование комплексообразования ПКЭАК с ионами двухвалентных металлов
1.1 Комплексы водорастворимых полимеров с различными классами соединений
Исследование взаимодействий комплементарных макромолекул и продуктов этих реакций - полимерных комплексов представляет одну из важнейших проблем химии и физики полимеров и молекулярной биологии [1-3]...
Исследование комплексообразования ПКЭАК с ионами двухвалентных металлов
1.2 Комплексы полимеров с низкомолекулярными соединениями
...
Исследование комплексообразования ПКЭАК с ионами двухвалентных металлов
1.2.1 Комплексы полимер - ион металла
Полимер-металлические комплексы образуются в результате взаимодействия полимеров содержащих функциональные группы (поликатионов, полианионов, неионогенных полимеров), с ионами переходных металлов (Cu2+, Cd2+, Zn2+, Ni2+, Co2+, Mg2+, Fe2+ и др.)[14]...
Комплексные соединения хрома. Соль Рейнеке
4.3 Соединения хрома (VI) (d0)
Галогенидные комплексы типа [МX6+x] x - неизвестны, поэтому координационная химия хрома в этой степени окисления относится в основном к оксо - и пероксокомплексам. Соединения хрома (VI) очень широко известны...
Методы получения дистиллированной и деионизированной воды
2.1 СОВРЕМЕННЫЕ КОМПЛЕКСЫ ОБОРУДОВАНИЯ ДЛЯ ПОЛУЧЕНИЯ ДЕИОНИЗОВАННОЙ ВОДЫ
Мембранный процесс разделения жидкостей осуществляется следующим образом (рис. 1): исходный раствор под давлением подается на полупроницаемую мембрану. Мембрана разделяет поток на две части: очищенный раствор (фильтрат или пермеат)...
him.bobrodobro.ru
Хром, комплексы соединения - Справочник химика 21
Разделение хрома и ванадия принадлежит к числу трудных задач. Для аналитических целей применяется осаждение органических комплексов соединений металлов [499] или экстракция метал- [c.453]Число мешающих ионов велико, это ионы, образующие труднорастворимые соли серебра (например, цианид и роданид) или осаждающиеся в кипящей НЫОз [например, висмут(И1), сурьма (П1)], металлы, образующие галогенидные комплексы [например, ртуть(П), кадмий(П), олово(1У), хром(П1)], соединения, восстанавливающие серебро (I) и, наконец, железо (Н1). Бромид и иодид хорошо отделяются при окислении и могут быть определены в виде свободных галогенов. [c.291]
Соединения Сг (II), Мо (II), У (II). Для хрома в степени окисления +2 характерно координационное число 6. Это соответствует образованию, как правило, высокоспиновых комплексов (и структурных единиц) с электронной конфигурацией [c.553]Соединения Сг (VI), Мо (VI), У (VI). Степень окисления +6 хрома, молибдена и вольфрама проявляется в галидах, оксогалидах, оксидах и отвечающих им анионных комплексах [c.563]
Некоторые соединения проявляют амфотерность в среде жидкого НР. К их числу относятся фториды алюминия и хрОма, Например, фторид хрома может образовать фторидный комплекс, проявляя кислотные свойства [c.275]
Хром (Е° = —0,74 В) более отрицателен в ряду напряжений, чем железо (Е° = —0,44 В). Однако благодаря склонности к пассивации (Ер = 0,2 В) потенциал хрома в водных средах обычно положителен по отношению к потенциалу стали. При контакте со сталью, особенно в кислых средах, хром активируется. Следо вательно, коррозионный потенциал стали с хромовым покрьггием которое в некоторой степени всегда пористо, более отрицателен, чем потенциал пассивации хрома [191. В указанных условиях хром, подобно олову, выполняет функцию протекторного покрытия однако это связано с его активацией, а не с образованием комплекс ных соединений металлов. Благодаря стойкости слоя металличе ского хрома предупреждается подтравливание наружного полимер ного покрытия. [c.241]
В рассматриваемом аспекте для химизма, механизма, кинетики и термодинамики процесса карбонизации большое значение имеет присутствие в нефтяном сырье различных функциональных групп, содержащих кислород, серу и азот, и их термическая стабильность (химическая активность), металлов, их соединений и комплексов, обладающих каталитическим действием на реакции распада, дегидрирования, полимеризации, конденсации и другие. С этой точки зрения,особо следует отметить такие металлы, как ванадий, никель, хром, молибден, кобальт, алюминий, железо и другие. [c.11]
Кобальт(П1) относится к тем немногим ионам металлов, для которых характерно образование инертных комплексов такими свойствами обладают еще хром(П1), пла-тина(1У) и платина(П). Комплексы этих ионов сохраняются в растворе достаточно долго, чтобы можно было изучить их структуру и свойства. Поэтому они принадлежат к числу тех комплексов, которые были изучены ранее всего и на примере которых химики изучали структуру и изомерию координационных соединений. [c.385]
Многие ранние исследования комплексных соединений, послужившие основой современных представлений о природе этих веществ, проводились на комплексах хрома(1П), кобальта(П1), платины(П) и платины(1У). Комплексы этих ионов являются инертными, т.е. характеризуются малой скоростью замещения лигандов. Комплексы, характеризуемые быстрым замещением лигандов, называются лабильными. [c.400]
При растворении следует стремиться к тому, чтобы вещество растворилось полностью, независимо от того, полный или неполный анализ требуется провести. Многие неорганические соли и некоторые органические соединения хорошо растворяются в воде, подкисленной минеральными кислотами, чтобы предотвратить гидролиз (соли железа, висмута и др.). Органические соединения хорошо растворяются в органических растворителях - спирте, ацетоне, хлороформе и др. Большинство металлов и сплавов, а также оксидов, карбонатов, сульфидов и др. растворяется в разбавленных или концентрированных кислотах. Выбор кислот осуществляется на основании химических свойств растворяемых веществ. Так, сплавы и оксиды железа лучше растворять в хлороводородной (соляной) кислоте вследствие склонности Ре " к образованию хлоридных комплексов хром и алюминий не растворяются в азотной кислоте из-за образования на поверхности пассивирующей оксидной пленки и т.д. [c.49]
Таким образом, необходимым условием для существования геометрических изомеров является наличие во внутренней сфере комплекса заместителей разного типа. Такие соединения известны для элементов восьмой группы, хрома, меди и некоторых других элементов. [c.45]
Образование труднорастворимых комплексных соединений фтора. Из этой группы реакций наибольшее значение имеет образование соединений типа криолита Na.,[AlFJ аналогичные труднорастворимые комплексы образуют ионы трехвалентного железа и трехвалентного хрома. Эти соединения используются для отделения названных элементов, а также для весового и объемноаналитического их определения. В последнем случае необходимо иметь в виду, что состав осадка в обычных условиях не точно отвечает приведенной формуле, а именно содержание фтора в нем меньше (2А1Рз 5КаР) криолит Na,[AlP,. 1 устойчив только в присутствии определенного избытка фтористого натрия в растворе. [c.427]
Ни один из этих элементов в своих соединениях не достигает степени окисления, соответствующей номеру группы. Наиболее устойчивы степени окисления +2 и Ч-З, причем для никеля, за некоторыми исключениями (например, в K [NiFe], см. также опыт 1), наиболее типична степень окисления +2 (конфигурация d ) (опыт 1). Во многих соединениях кобальта он также имеет степень окисления 4-2 (d ) степень окисления 4-3 (d ) характерна главным образом для комплексных соединений кобальта, которые имеют сходство с комплексами хрома (1П). Соединения железа в степени окисления -j-2 (d ) сходны с соединениями цинка реакции иона железа(III) (d ) во многом похожи с реакциями ионов алюминия и хрома(III). Обладающие сильным окислительным действием ферраты (VI) (d ) РеОч напоминают хроматы (VI) и мaнгaнaты(VI) ферраты имеют тот же состав, что и сульфаты, и часто им изоморфны. Реакции соединений железа, кобальта и никеля в своем больщинстве определяются склонностью этих металлов к изменению степени окисления и их способностью к комплексообразованию. [c.635]
Для хрома характерны соединения со степенью окисления +3. Их получают непосредственным взаимодействием хрома с галогенами или в других химических процессах. Так, соль СгС1з — кристаллы красно-фиолетового цвета — чаще всего находится в полимерном состоянии. Ион Сг + склонен к образованию многочисленных комплексных солей, в которых лигандами являются НзО С1 ЫНз. Склонность к образованию комплексов с координационным числом 6 объясняется структурой иона [c.345]
Существуют и другие примеры применения собственной люминесценции в анализе, основанные, например, на излучении комплексов Си (I) и Аи (I) с пиридином и его производными, тиоцианатов хрома (III), соединений платиновых металлов в низших степенях окисления с 1,10-фенантролином, 2,2 -дшшридилом. [c.309]
Работы Хейна и его сотрудников по полифенилхромовым комплексам были продолжены, и в них была внесена некоторая ясность теперь ряд веществ, описанных Хейном, рассматривают как соединения, в которых между хромом и ароматическими щестичленными кольцами существуют тт-связи [122]. Совершенно независимо от этого класса аренных комплексов, аналогичных циклопентадиенильным соединениям переходных металлов, известно несколько примеров о-связанных хром-углеродных соединений, не считая карбонилов хрома и их изоцианидных аналогов. [c.495]
На основании наших последних исследований цветности молекулярных комплексов, соединений с отделенными неконъюгированными хромо форными системами, сравнительного влияния структурных факторов на поглощение света в кристаллах и растворе, мы пришли к расширению представлений о мезостроении—к гипотезе о мезоэффекте в молекулярном комплексе посредством тг-связей особого вида, без наличия одновременной а-связи ( Комплексная мезомерия , 1939 и, подробнее, в 1947 г.). [c.164]
Второй из наиболее часто применяемых способов превращения метилзамещенных бензолов в соответствующие бенз-альдегиды состоит в обработке их хлористым хромилом в инертном растворителе (в четыреххлористом углероде или сероуглероде). Реакцию обычно проводят при комнатной температуре. Вначале окисляемое ароматическое соединение образует с двумя молекулами хлористого хромила комплекс, который выпадает в осадок. При обработке комплекса водой образуется альдегид. Механизм этого превращения, называемого реакцией Этара, окончательно не выяснен [c.191]
Из тридцати пяти кристаллических структур, описанных ниже в разделе Хром , одиннадцать относятся к соединениям хрома в его высших состояниях окисления (от IV до VI), шесть — к соединениям трехвалентного хрома, в двух присутствуют одновременно атомы Сг 1 и Сг , шестнадцать структур относятся к карбонильным соединениям (включая полусандви-чевые комплексы с органическими лигандами) и две — к некарбонильным я-комплексам хрома. Все соединения хрома высших валентностей являются кислородными, из восьми соединений, содержащих Сг , три кислородных, остальные содержат в качестве лигандов хлор, циано-, нитрозо- и гидроксогруппы, аммиак, триметиламин, воду и некоторые огранические моно- [c.9]
Электронная конфигурация молибдена 4 s2, 4 рв, 4d5, 5s П вгоряет конфигурацию хрома, и магнитные свойства атомов м> либдена в соединениях сходны со свойствами атомов хрома, с те] однако, характерным исключением, что атом молибдена больи и имеет координационное число восемь, а не шесть. Для преобл. дающих ковалентных комплексов это обстоятельство часто пр] водит к диамагнетизму, между тем как соответствующие хром вые соединения могут быть парамагнитными. [c.162]
Разработанными методами проанализированы производные аренхромтрикарбонилов, циклопентадиенильные комплексы хрома, производные гексакарбонила хрома, полимерные соединения, содержащие хром, хромфосфаты, хромсилоксаны и другие ЭОС, содержавшие В, Ое, Ре, 81, Мп, Мо, Hg, Р, Ридр. Стандартное отклонение составляет 0,12% (абс.). [c.201]
Соединения Сг([П), Мо(П1), W (III). У хрома степень окисления -ЬЗ является наиболее устойчивой. Координационное число хрома (HI) равно шести, поэтому его комплексы (структурные единицы) имеют форму октаэдра. Валентные электроны в октаэдрических комплексах Сг (HI) располагаются только на связывающих и несвязывающих орбиталях [c.558]
Увеличение электронного дефицита на атоме металла благоприятствует, как правило, повышению доли 1,4-структур. Из табл. 6 следует, что в присутствии аллилгалогенидных комплексов получаются полимеры с большим содержанием 1,4-звеньев, чем в присутствии чистых комплексов того же переходного металла. В полиизопренах, образующихся в присутствии продуктов реакции соединений кобальта, молибдена, никеля, хрома и циркония с галогенидами или алкилгалогенидами алюминия или титан.а, содержание 1,4-структур увеличивается с повышением электроноакцепторной способности сокатализатора и мольного отношения соката-лизатора к металлу. [c.104]
Как видно из приведенных выше экспериментальных данных, путем подбора соответствующих катализаторов можно синтезировать полидиены с любой микроструктурой. В первую очередь, микроструктура полимеров определяется природой переходного металла катализатора. Как правило, соединения металлов VIII группы (кобальта, никеля, родия, железа), а также титана и ванадия являются более подходящими для синтеза 1,4-полибутадиенов комплексы металлов V и VI групп (хрома, молибдена, вольфрама, ниобия) и палладия дают полимеры с боковыми винильными звеньями. В то же время стереоселективность катализаторов может быть существенно изменена путем введения в состав каталитических комплексов различных лигандов. [c.105]
Растворы солей хрома (III) обычно имеют сине-фиолетовым цвет, но при нагревания становятся зелеными, а спустя некоторое время после охлаждения снова приобретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или часть молекул воды координационно связаны во внутренней сфере комплекса. В некоторых случаях такие гидраты удалось выделить в твердом виде. Так, кристаллогидрат хлорида хрома (JII) r ls- HjO известен в трех изомерных формах в виде сине-фиолетовых, темно-зеленых н светло-зеленых кристаллов одинакового состава. Строение тих изомеров можно установить на основании различного отношения их свежеприготовленных растворов к нитрату серебра. При действии последнего на раствор сине-фиолетового [c.655]
В сущности железо обладает не большей реакционной способностью, чем другие обсуждавшиеся выше переходные металлы. Однако, к сожалению, оксиды железа непрочно пристают к поверхности металлического железа, Ржавчина (оксид железа) отслаивается по мере образования и предоставляет возможность новой поверхности металла реагировать с окружающей средой. Содержащая хром нержавеющая сталь больше сопротивляется коррозии, но для защиты железа чаще используются покрытия из хрома, олова, никеля или красок. Соединения железа(П) обычно имеют зеленую окраску, а гидратированный ион железа(Ш), Ре(Н20) , окрашен в бледно-фиолетовый цвет. В состояниях окисления - - 2 и -Ь 3 железо образует октаэдрические комплексы с цнанидными ионами, Ре(СК) и Pe( N)g . Традиционные названия этих иоиов - ферроцианид и феррициа- ид. Согласно ссБрсмснной систематической номенклатуре, их называют гексацианоферрат 11) и гексацианоферрат(Ш). Номенклатура комплексных ионов излагается в гл. 20. [c.445]
В самом деле, если гидрирование протекает через образование л-комплексов, то катализаторами этой реакции должны быть все переходные металлы. Было показано что в присутствии коицлексов никеля, кобальта, железа, марганца, хрома и ванадия, активированных алюмоорганическими соединениями, олефины гидрируются с высокими скоростями, т. е. эти комплексы достаточно хорошо активируют водород. Основываясь на этом, удалось показать что бензол гидрируется в присутствии комплексных металлоорганических катализаторов на основе всех переходных металлов четвертого периода. [c.137]
Образование комплексов. Азотсодержащие соединения нефтей за счет неподеленных пар электронов азота способны образовывать донорно-акцепторные связи и комплексные соединения с галогенами, солями металлов ртути, цинка, олова, хрома(П1), меди (II) и других, карбонилами железа [207]. Однако из-за наложения электрических моментов диполя серу-, азот- и кислородсодержащих соединений, например для иодидов, амино-, тио- и ал-коксицодидов (6,67—33,33) 10 Кл-м с помощью комплексообразования невозможно селективное выделение или разделение этих классов соединений. [c.91]
В смолисто-асфальтеновых веществах найдены железо-, кобальт-, хром-, и марганецпорфирины.[261], а также соединения золота и серебра в виде комплексов с тетрадентатными лигандами [266]. [c.275]
Обычно при титровании ионов металлов ЭДТА при pH 10 в конечной точке титрования фиолетовый цвет раствора (наложение синего цвета индикатора на красный цвет комплексного соединения) изменяется на чисто синий (цвет индикатора комплексы металлов кальция, магния, цинка и др. с ЭДТА бесцветны). Эрио-хромов 1Й черный Т обладает очень интенсивной окраской, поэтому его готовят, смешивая с сухим хлорицом натрия в отношениях от 1 100 до 1 400. Для каждого титрования берут шпателем 20-30 мг смеси. [c.117]
СЫ. В ЭТИХ соединениях донором электронов являются я-элект-ронные системы ароматических или непредельных соединений, а в результате реакции с веществом-кислотой также образуется я-связь. Типичные представители таких соединений — бис (бензол ) хром (СбНб)гСг, а также бис(я-циклопентадие нил)железо ((я-С5Н5)2ре — ферроцен), которые имеют структуру сандвича или двойной кегли к комплексам непредельных соединений относится и соль Цейзе К[С2Н4Р1С1з]1 Структура этих соединений изображена на рис. В.12. [c.399]
Химическая связь в ферроцене между двумя пентадентатными лигандами и атомом железа осуществляется за счет того, что тг-электроны лигандов (по 5 от каждого лиганда) и 8 валентных электронов атома железа заполняют связывающие и несвязывающие МО комплекса, обеспечивая его устойчивость. Хром имеет на два ва тентных электрона меньше, поэтому необходимые 18 суммарных электронов для заполнения МО в соответствующем комплексе хрома достигаются, если в качестве лигандов взять бензольные кольца. Дибензолхром (СбНб)2Сг так же, как и ферроцен, относится к тт-комплексам, называемым ио причине участия в образовании комплекса лигандов с тг-электронными системами, О важности таких соединений говорит то, что большую часть современной органической химии переходных элементов составляет химия тг-комплексов. [c.369]
Для хрома и его аналогов наиболее типичны производные высщей степени окисления, во многом сходные с соответствующими соединениями серы. Соединения хрома (VI) отличаются неустойчивостью в растворах и являются сильными окислителями. При этом они чаще всего восстанавливаются до анионных или катионных комплексов хрома (Ш). Хотя хром располагается в четной группе, наиболее устойчивой его степенью окисления является Ч-З. Это связано с тем, что соединения хрома (III) являются, как правило, комплексными с координационным числом 6 и октаэдрической пространственной конфигурацией расположения лигандов. В этом случае три Зй-электрона иона Сг + равномерно заселяют трижды вырожденные несвязывающие МО комплекса (см. рис. 13,5 д). Возникающая стабилизация системы за счет суммарного спина 3 V2 = V2 (по правилу Хунда) в этом случае больше, чем если бы степень окисления хрома была + 2, -f-4 и т. д. [c.511]
chem21.info
Комплекс - хром - Большая Энциклопедия Нефти и Газа, статья, страница 1
Комплекс - хром
Cтраница 1
Комплексы хрома хемосорбируются на отрицательно заряженной стеклянной поверхности, приводя к уменьшению адсорбционной способности. В качестве полифункциональных гидрофобно-адгезионных соединений, способных взаимодействовать не с одним, а с многими типами полимеров, применяются так называемые универсальные аппретуры. [1]
Комплексы хрома и марганца характеризуются значительным вкладом дативной компоненты в образование связи металл - лиганд. [2]
Комплексы хрома ( Ш) и кобальта ( Ш) мало реакционноспо-собны; для объяснения этого факта выдвинут ряд теорий. Так, например, можно в течение нескольких часов нагревать с обратным холодильником смесь соли Co ( Nh4) 6Cl3 с 6 М соляной кислотой без ее изменения, хотя при этом образуются СоС12, хлористый аммоний и хлор. [3]
Комплекс хрома ( III) парамагнитен, поэтому метод ЯМР нельзя непосредственно использовать для определения цис - траке-изомерии. Однако Фай и Пайпер смогли разделить изомеры методом жидкостной хроматографии и идентифицировать их рентгенографически. В растворах комплексов хрома ( III), родия ( III) и кобальта ( III) содержится при равновесии приблизительно 80 % транс - и 20 % мс-изомера. [4]
Комплексы хрома, меди и никеля легко разрушаются азотной кислотой при нагревании исследуемого раствора. [5]
Комплекс хрома имеет дипольный мо - мент 1 18 0 1D и вступает ъ реакцию каталитического гидрирования ненасыщенных колец. На основании этих данных и ИК-н ЯМР-спектров предложена структура 6.4, согласно которой вещество представляет собой производное комплекса л - С7Н7Сг - - л - CsHs. Комплекс железа не окисляется и не полярен, но он вступает в реакцию восстановления колец. [6]
Арентрикарбонильные комплексы хрома и их молибденовые аналоги были широко изучены с целью выяснения степени реакционной способности ароматической части таких молекул. [7]
Все комплексы хрома ( III), которые имеют структуру, показанную в предыдущем примере, обладают шестью лигандами, каждый из которых связан с центральным атомом ковалентной связью. Поэтому мы можем утверждать, что координационное число хрома ( III) равно шести. В общем случае координационное число зависит от электронной структуры атома металла, а также от структуры, заряда и электроотрицательности лигандов. [8]
Алл ильные комплексы хрома, ниобия и титана являются катализаторами 1 2-полимеризации бутадиена, а бис-я - ал л ил никель и / прис-я-аллилкобальт - катализаторами олигомеризации, в первом случае с образованием циклододекатриена, во втором случае - линейных димеров. Продукты взаимодействия всех этих соединений с растворами безводных кислот являются катализаторами 1 4 - г ( ыс-полимеризации бутадиена. [9]
Например, комплексы хрома ( III) кинетически инертны и, следовательно, комплексы с ЭДТА образуются слишком медленно. [11]
Среди - комплексов хрома ( II) необходимо отметить хромоцен - [ Cr ( C5Hs) 2 ] - кристаллическое вещество красного цвета, с температурой плавления, близкой к ферроцену, и по молекулярной структуре аналогичное последнему. [13]
Каждый из комплексов хрома ( III) в приведенной реакции обладает совершенной октаэдрической геометрией. Другими словами, лиган-ды симметрично расположены вокруг центрального атома и длина шести связей хром ( III) - лиганд идентична. Лиганд может быть нейтральной молекулой, как вода, или может быть ионом, как цианид-ион. В других случаях комплекс может быть нейтральной молекулой. В данном примере центральный атом - хром - - имеет степень окисления 3 в обоих комплексах. [14]
При рН 2 комплекс хрома неустойчив. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
§1. Степени окисления, электронные конфигурации, координационные числа и геометрия соединений хрома.
Следуя общим тенденциям заполнения d-подуровня при движении по периоду для элементов VI группы нужно было бы предположить конфигурацию валентных электронов в основном состоянии (n-1)d4ns2. В атоме хрома выигрыш энергии, вызванный стабилизацией наполовину заполненного подуровня и полным отсутствием дестабилизирующего вклада энергии спаривания, оказывается больше энергии, которую необходимо затратить на переход одного из s-электронов на d-подуровень. Это приводит к «перескоку» («провалу») электрона, т.к. известно, что электроны с параллельными спинами испытывают меньшее взаимное отталкивание, чем электроны с противоположными спинами, разность энергий у хрома достигает своего максимума – 3d54s1 (3d44s2). 1
В различных соединениях хром проявляет степени окисления от -4 до +6.
| Степень окисления | Электронная конфигурация | Координационное число | Геометрия | Примеры соединений |
| -4 | d10 | 4 | Тетраэдр | Na4[Cr(CO)4] |
| -2 | d8 | 5 | Тригональная бипирамида | Na2[Cr(CO)5] |
| -1 | d7 | 6 | Октаэдр | Na2[Cr2(CO)10] |
| 0 | d6 | 6 | Октаэдр | Cr(CO)6, [Cr(CO)5I]- |
| +1 | d5 | 6 | Октаэдр | K3[Cr(CN)5NO], [Cr({C5h5N}2)3]+ или [Cr(dipy)3]+ |
| +2 | d4 | 4 | Плоский квадрат Октаэдр | Cr(Ch4COCHCOCh4)2 или Cr(acac)22 K4[Cr(CN)6], CrF2 |
| +3 | d3 | 4 6 | Тетраэдр Октаэдр | [CrCl4]- [Cr(Nh4)6]3+ |
| +4 | d2 | 6 | Октаэдр | K2[CrF6] |
| +5 | d1 | 6 | Октаэдр | K2[CrOCl5] |
| +6 | d0 | 4 | Тетраэдр Октаэдр | CrO42- CrF6 |
§2. Хром (II).
Известно много соединений хрома (II), все они сильные и быстродействующие восстановители. Водные растворы, содержащие ион Cr2+, имеют небесно-голубой цвет. Этот ион очень легко окисляется
Cr3+ + ē → Cr2+ ( Е°= -0,41 В).
Легко окисляются кислородом воздуха:
4[Cr(h3O)6]2++O2+4H+=4[Cr(h3O)6]3++2h3O.
Будет восстанавливать воду с выделением водорода, причем скорость разложения зависит от кислотности раствора.
Высокоспиновые3 октаэдрические комплексы характеризуются большим магнитным моментом (4,7 – 4,9 μВ4). Это свидетельствует о тетрагональном искажении, которое является следствием эффекта Яна-Теллера5 и вызвано наличием одного электрона на eg –орбитали, что приводит к геометрическому искажению и понижению симметрии d4 –комплексов: два аксиальных лиганда находятся на большем расстоянии от атома Cr(II), чем четыре экваториальных. Такая структура обусловливает склонность высокоспиновых комплексов к гидролизу. Помимо аквакомплексов ([Cr(h3O)4(OH)2; [Cr(h3O)6]2+) к высокоспиновым относятся ацетилацетонат (Cr(acac)2) , а также аммиакаты ([Cr(Nh4)5Cl]Cl, [Cr(Nh4)6]Cl2).
Низкоспиновые6 комплексы хром (II) образует с лигандами сильного поля, например с цианидом K4[Cr(CN)6]. Эти комплексы интенсивно окрашены, их магнитный момент составляет 2,74-3,40 μВ, а связь Cr-L характеризуется существенной долей π-связывания.
Так же для хрома(II) известны и кластерные соединения, простейшее из них – ацетат хрома (II) Cr2(Ch4COO)4(h3O)2, выпадающий красный осадок при действии на CrII ацетатов, либо уксусной кислоты:
2CrCl2+4NaCh4COO+2h3O=[Cr2(h3O)2(Ch4COO)4]↓+4NaCl
На наличие связи Cr-Cr указывает диамагнетизм этого соединения: в нем нет неспаренных электронов. Поскольку каждый ион Cr2+ содержит четыре неспаренных электрона, связь имеет кратность 4. Именно поэтому расстояние Cr-Cr в ацетате (0,230 нм) оказывается короче, чем в металлическом хроме (0,256 нм). Атомы хрома соединены друг с другом также четырьмя бидентатными мостиковыми ацетатными группами. Координационную сферу каждого атома хрома дополняет молекула воды.
П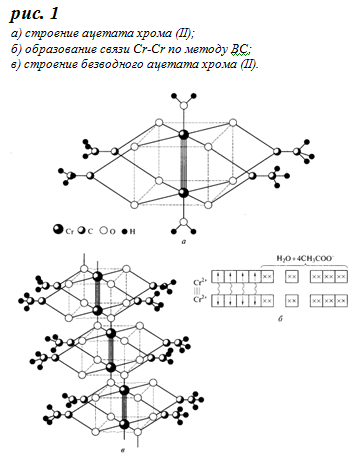
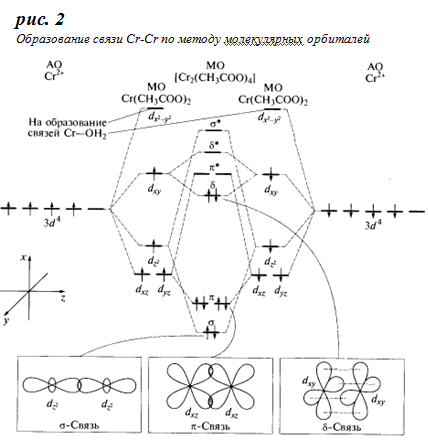 о методу валентных связей (ВС) четырехкратная связьCr-Cr образуется в результате объединения неспаренных 3d – электронов двух ионов хрома в четыре электронные пары, принадлежащие совместно обоим атомам. Вакантые орбитали ионов Cr2+ выступают в качестве акцепторов для образования пяти ковалентных связей с ацетатными группами и молекулами воды. В образующейся частице все электроны спарены, т.е. она является диамагнитной (см. рис 1 (б)). При нагревании в вакууме до 120°С ацетат хрома теряет воду, превращаясь в коричневый порошок, в котором кластеры Cr2(Ch4COO)4 связаны между собой дополнительным взаимодействием атомов хрома с атомами кислорода соседних ацетатных групп (см. рис 1 (в)). Образование связи Cr-Cr по методу молекулярных орбиталей (МО) представлено на рис. 2. Для простоты рассмотрено взаимодействие двух фрагментов молекулы состава Cr(Ch4COO)2, каждый из которых имеет форму плоского квадрата, что видно из расщепления исходных d-орбиталей хрома. Из пяти d-орбиталей каждого фрагмента четыре идут на образование связи Cr-Cr, а одна - на образование σ-связи с молекулой воды. Из восьми d-орбиталей, предоставленных в общее пользование двумя атомами хрома, образуются восемь молекулярных орбиталей (МО) – две из них σ-типа, четыре – π-типа и две δ-типа. Электронами заполнены четыре связывающие МО, что обусловливает образование четырехкратной связи Cr-Cr.
о методу валентных связей (ВС) четырехкратная связьCr-Cr образуется в результате объединения неспаренных 3d – электронов двух ионов хрома в четыре электронные пары, принадлежащие совместно обоим атомам. Вакантые орбитали ионов Cr2+ выступают в качестве акцепторов для образования пяти ковалентных связей с ацетатными группами и молекулами воды. В образующейся частице все электроны спарены, т.е. она является диамагнитной (см. рис 1 (б)). При нагревании в вакууме до 120°С ацетат хрома теряет воду, превращаясь в коричневый порошок, в котором кластеры Cr2(Ch4COO)4 связаны между собой дополнительным взаимодействием атомов хрома с атомами кислорода соседних ацетатных групп (см. рис 1 (в)). Образование связи Cr-Cr по методу молекулярных орбиталей (МО) представлено на рис. 2. Для простоты рассмотрено взаимодействие двух фрагментов молекулы состава Cr(Ch4COO)2, каждый из которых имеет форму плоского квадрата, что видно из расщепления исходных d-орбиталей хрома. Из пяти d-орбиталей каждого фрагмента четыре идут на образование связи Cr-Cr, а одна - на образование σ-связи с молекулой воды. Из восьми d-орбиталей, предоставленных в общее пользование двумя атомами хрома, образуются восемь молекулярных орбиталей (МО) – две из них σ-типа, четыре – π-типа и две δ-типа. Электронами заполнены четыре связывающие МО, что обусловливает образование четырехкратной связи Cr-Cr.
Благодаря кластерному строению ацетат хрома (II) гораздо более устойчив к окислению, чем простые соли хрома (II). В качестве исходного вещества его используют для синтеза других соединений CrII.
studfiles.net
Оглавление
Санкт-Петербургский государственный университет.
Химический факультет.

Курсовая работа
Тема: «Комплексные соединения хрома.
Синтез соли Рейнеке Nh5[Cr(Nh4)2(NCS)4]».
Студент I курса
Воронаев Иван Геннадьевич
2 группа.
Преподаватель
профессор, д.х.н. Хрипун Мария Кирилловна
Санкт-Петербург
2010
Введение 3
§1. Степени окисления, электронные конфигурации, координационные числа и геометрия соединений хрома 4
§2. Хром (II) 4-7
§3. Хром (III) 7-14
3.1 Общая характеристика комплексных соединений хрома (III) 7-10
3.2 Соль Рейнеке 10-12
3.2.1 Общие сведения 10
3.2.2 Применение 11-12
3.3 Многоядерные комплексы хрома (III) 12
3.4 Электронное строение комплексов хрома (III) 12-13
3.5 Фосфоресцирующие комплексы 13-14
3.6 Получение комплексных соединений хрома (III) 14
§4. Высшие состояния окисления хрома 14-15
4.1 Соединения хрома (IV) 14
4.2 Соединения хрома (V) 14-15
4.3 Соединения хрома (VI) 15
§5. Практическая часть. Синтез соли Рейнеке 15-16
5.1 Реактивы, используемые в работе 15
5.2 Синтез соли Рейнеке 15-16
5.3 Данные рентгеноструктурного анализа 16
5.4 Изучение свойств соли Рейнеке 16-17
Выводы 17
Список литературы 18
Введение.
Все возрастающее значение комплексных соединений в различных областях теоретического и практического применения диктует настоятельную необходимость их глубокого и всестороннего изучения.
Подразделение всех химических соединений на так называемые простые (атомные) и комплексные (молекулярные), наметилось после создания учения о валентности и внедрения в химию структурных представлений А.М. Бутлерова. Основоположником учения о комплексных соединениях является А. Вернер, он разделил все вещества на два типа: соединения первого порядка (простые соединения) и соединения высшего порядка (продукты взаимного сочетания соединений первого порядка), к ним он относил комплексные соединения. Другие крупные специалисты в данной области (Л.А. Чугаев, П. Прейффер и др.) определяют комплексные соединения как продукты сочетания молекул соединений первого порядка. Все же это определение отнюдь не является безупречным.
Понятие комплекса в растворе до сих пор не получило точного определения. Сегодня мы знаем, что комплексная частица может диссоциировать, и по константе диссоциации можно судить об ее устойчивости. Правда, комплексы в растворе не характеризуются высокой степенью диссоциации, как сильные электролиты, и далеко не всегда комплексная частица бывает соединением высшего порядка. И, наконец, известно, что не существует никаких принципиальных различий между «обычными» и «координационными» связями.
После всего сказанного очевидно, что безупречного определения понятия комплексное соединение существовать не может. Но так как все же желательно дать хотя бы приближенное определение понятия, то можно остановиться на следующем.
Комплексные соединения – это частицы, которые образуются в результате присоединения к данному иону (или атому), называемому комплексообразователем (центральным атомом или металлоцентром), нейтральных молекул или других ионов, называемых лигандами.
Явление комплексообразования лежит в основе целого ряда биологических процессов, каталитических реакций, электролитического осаждения. Особенно велико значение комплексных соединений в растворах, поскольку в широком смысле можно считать, что химия растворов – это химия комплексных соединений. Д.И. Менделеев указывал на роль химического взаимодействия между компонентами в растворе: «Все формы взаимодействия в растворе, а следовательно, и равновесие в нем, связаны прежде всего с химической природой как растворителя, так и растворенных в нем веществ».
В связи с изложенным, представляется интересным изучение комплексных соединений.
studfiles.net