Способ получения борида хрома. Хрома борид
Хрома, Циркония бориды - Справочник химика 21
Свойства боридов титана, циркония, хрома и вольфрама [c.65]БОРИДЫ — соединения бора с металлами образуются при высоких температурах. Имеют повышенную твердость. Стойкость против истирания и коррозионную стойкость. 5. никеля используют как катализатор. Б. хрома, циркония, Титана, ниобия и тантала, благодаря их тугоплавкости, применяют для изготовления деталей реактивных двигателей, лопаток газовых турбин и др. Б. лантана, церия и бария используют в электронных приборах. Поверхностным борированием резко повышается твердость, стойкость к срабатыванию и коррозионная стойкость изделий из стали, молибдена, вольфрама и др. [c.46]
ДОВОДОЧНАЯ ПАСТА - паста, состоящая из смеси мелкозернистых абразивных порошков и поверхност-но-активных веществ. Применяется для отделочной (доводочной) обработки с целью получения у изделий чистой (10—14-го классов) поверхности и точных размеров (1—2-го классов). В качестве абразивных используются порошки карбидов кремния и бора, окислов алюминия и хрома, натуральных и синтетических алмазов, боразона и металлоподобных тугоплавких соединений (карбидов и боридов титана, циркония, вольфрама, молибдена, хрома). Поверхностноактивными веществами служат стеариновые и олеиновые кислоты, парафин, минер, масла, полиизобутилен, [c.400]Разработанный метод получения диборидов титана, циркония, ванадия, хрома, марганца и других переходных металлов при совместном восстановлении углем смесей окислов соответствующего металла и бора позволяет получать бориды в больших количествах из недефицитного сырья. [c.111]
Универсальный метод для анализа боридов разработан Блюменталем [39—41]. Метод основан на сплавлении в платиновом тигле боридов с 10-кратным избытком карбонатов калия-натрия с добавкой 6,1—0,2 г нитрата натрия. Блюменталь разработал метод анализа большей части боридов в трех вариантах 1) сплавление с бисульфатом калия в кварцевом тигле для анализа боридов железа, циркония и титана 2) сплавление со смесью карбоната и нитрата натрия для анализа боридов алюминия, кальция, магния, хрома, марганца, ванадия, молибдена, тория, вольфрама 3) сплавление со смесью карбоната и нитрата калия для анализа боридов ниобия и тантала. [c.178]
На основании литературных данных о растворении бора [35, 46, 48, 49] и некоторых боридов [50] в различных окислителях была исследована возможность определения свободного бора в некоторых тугоплавких соединениях [51] и разработан метод определения обш,его и свободного бора в карбиде бора, нитриде бора, боридах циркония, гафния, тантала и хрома [1]. [c.179]
Ход анализа. Навеску 0,5—1,0 г борида хрома растворяют при нагревании в колбе с обратным холодильником в 50 мл соляной кислоты (1 1) в течение часа. Нерастворимый остаток, состоящий из карбида бора и свободного бора, отфильтровывают и промывают соляной кислотой (1 20). Осадок с фильтром помещают в колбу и приливают смесь, состоящую из 30 мл перекиси водорода (1 3) и пяти капель азотной кислоты. Растворение ведут при нагревании с обратным холодильником в течение 30—40 мин. Остаток карбида бора отфильтровывают и в фильтрате определяют содержание свободного бора. Фильтрат нейтрализуют раствором едкого натра по метиловому красному и определяют бор, как описано при определении бора в бориде циркония [1]. [c.184]
Особый интерес представляют покрытия, содержа-и ие высокотемпературные бориды. Но бориды титана, циркония и хрома в кислых электролитах меднения [c.97]
Описанная выше отчужденность хрома к включениям относится в первую очередь к частицам-изоляторам. Несколько иное отношение покрытия хромом к веществам, обладающим заметной проводимостью,— сульфидам и боридам циркония, вольфрама, нитриду циркония и карбиду молибдена Получение [c.100]
Описан промышленный метод получения покрытий хром — борид циркония. В обычную ванну хромирования (состав и условия не приведены) добавляют от 10 до 60% порошка борида циркония с. й = - 4 мкм (при этом происходит бурное разогревание раствора). Электролиз проводят при 1 к=32- 54 а дм в течение 2,5 ч. В результате получают покрытие, стойкое к действию температур 2000—2500° С. [c.102]
В качестве металлов, кроме никеля, можно применять кобальт, алюминий, железо или их сплавы с хромом, титаном, вольфрамом, цирконием в качестве окислов—окислы алюминия, бериллия, кремния, циркония. Вместо окислов применяют также карбиды, бориды, силициды, нитриды соответствующих металлов. [c.108]
Бориды таких металлов, как титан, хром, цирконий, ниобий, тантал (например, ТаоВ, ТаВ, Та>,В4, ТаВг), в настоящее в])омя применяют для изготовлени деталей реактивных двигателей, ло- [c.349]
Бориды обладают высокими температурами плавления, значительной твердостью, химической устойчивостью, жаропрочностью и жаростойкостью. Бориды металлов хрома, циркония, титана, ниобия, тантала (например, ТагВ, ТаВ, 13384, ТаВа) и др. стали применять для изготовления деталей реактивных двигателей, лопаток газовых турбин и т. п. [c.174]
Высокотемпературное покрытие хромом е боридом циркония лолу чают т стандартной ваиггы хромирования, содержащей от 10 до 60 % порошка борида циркония с частицами величиной 1—4 мкм При обра зопанин суспензии происходит ее бурный пагрев Электролиз ведут прн 7,1=32- 54 А/дм в течение 2.5 ч. Покрытие стойко нри 2000—2500 [35] [c.190]
Покрытия из металлов п сплавов используют в качестве антикоррозионных (хром, никель, нихром), жаростойких (ниобий, мо либден), жароэрозионностойких (вольфрам). Хромоникелевые само-флюсующиеся сплавы обладают износостойкостью, эрозионной и коррозионной стойкостью, стойкостью к окислению при высокой температуре. Оксиды (оксид алминия, оксид хрома, диоксиды циркония или титана) применяют как теплозащитные покрытия, обладающие высокой жаро- и коррозионной стойкостью, твердостью. Бориды различных металлов имеют высокую твердость и хорошую жаростойкость, силициды — высокую термо- и жаростойкость. Карбиды металлов в большинстве случаев характеризуются высокой твердостью, износо- и жаростойкостью нитриды титана, циркония, гафния — высокой твердостью, износо- и термостойкостью, устойчивостью к коррозии. [c.139]
При изготовлении деталей методами порошковой металлургии широко применяются порошки железа, никеля, хрома, кобальта, меди, а из числа неметаллических материалов, графита, окислов ряда элементов (например, А1зОз) карбидов (карбид вольфрама, титана и др.), боридов (бориды титана, циркония) и некоторых других соединений. Путем подбора составляющих материалов в смеси и их соотношения удается получить новый материал, в котором до известной степени сочетаются ценные свойства входящих в него компонентов. [c.303]
По литературным данным, раствори.мость окислов титана, циркония и хрома в В2О3 при температурах ниже 1200 мала, боратов эти металлы не образуют (в настоящей работе эти положения были проверены и подтверждены). Таким образом, в первый момент окисления при "-1000° на поверхности боридов образуется механическая смесь В2О3 и окисла соответствующего металла. [c.65]
Гидроокись натрия применяется для отделения Fe +, Ni +, Сг +, Ti +, Мп2+ в сталях и ферросплавах. Соосаж-дение бора устраняется осаждением этих катионов в сильнощелочной среде. При pH 7—10 еще наблюдается соосаждение бора [21]. Метод осаждения едким натром применяется при определении бора в боридах титана, циркония и хрома [60]. Определяя микроколичества бора, осаждение металлов щелочами необходимо проводить в кварцевой посуде, поскольку стеклянная посуда всегда содержит бор. Так как борная кислота соосаж-дается вследствие образования аморфных или гелеподобных осадков, внимания заслуживает способ осаждения металлов с оксихинолинатом натрия [12]. При использовании 8-оксихинолина для осаждения металлов получаются кристаллические хорошо фильтрующиеся осадки. Метод применяется для осаждения цинка, свинца, алюминия, железа, никеля. Известен способ отделения никеля, ванадия и молибдена экстрагированием их диэтилди-тиокарблматных комплексов хлороформом [94]. [c.27]
Образованию спеченных композиций с волокнами на основе усов из боридов, карбидов, нитридов и оксидов мешает плохая смачиваемость последних многими металлами матрицы. Так, для создания композиции Ай—А1гОз требовалось предварительно покрывать усы слоем никеля или платины толщиной 0,1 мкм. Иногда смачиваемость усов улучшалась от добавки к матрице (никель) других металлов, а именно титана, циркония или хрома, понижающих поверхностное натяжение на границе волокно — жидкий металл. [c.143]
Композиционные материалы состоят из основы (матрицы) и добавок (порошков, волокон, стружки и т.д.). в качестве основы применяют металлы, полимеры, керамику и другие материалы. Если основой служат металлы, то добавками являются металлические нитевидные кристаллы, неорганические волокна и порошки (оксиды алюминия, кварц, алюмосиликаты и др.). Композиты, матрицей которых служит керамика, а добавками — металлы, называются керамикометаллическими материалами или керметами. В качестве матрицы керметов обычно применяют оксиды алюминия, хрома, магния, циркония, карбиды вольфрама, кобальта, бориды циркония и хрома. Добавками могут служить металлы, сродство которых соответственно к кислороду, углероду, бору меньше, чем сродство к этим элементам металлов основы. Наиболее распространены сочетания оксидов алюминия с молибденом, вольфрамом, танталом, никелем, кобальтом, оксида хрома с вольфрамом, оксида магния с никелем, диоксида циркония с молибденом, карбидов титана и хрома с никелем и кобальтом. [c.356]
Температуры плавления рассматриваемых соединений изменяются сходным образом (рис. 88). Максимумы температур плавления обнаруживаются у карбидов и нитридов титана, циркония, гафния. При переходе к соединениям высоковалентных металлов VI—VII групп (хрома, молибдена, марганца) наблюдается интенсивное падение температур плавления, затем новый подъем температур плавления при переходе к соединениям железа и дальнейшее понижение температур плавления соединений никеля. Максимальные температуры плавления среди моноборидов имеют бориды металлов V группы ванадия и ниобия. Среди моноокислов и моносульфидов наиболее тугоплавкими являются соединения щелочноземельных металлов. [c.186]
chem21.info
Борид хрома - WikiVisually
1. Химическая формула – These are limited to a single typographic line of symbols, which may include subscripts and superscripts. A chemical formula is not a name, and it contains no words. Although a chemical formula may imply certain simple chemical structures, it is not the same as a full chemical structural formula. Chemical formulas can fully specify the structure of only the simplest of molecules and chemical substances, the simplest types of chemical formulas are called empirical formulas, which use letters and numbers indicating the numerical proportions of atoms of each type. Molecular formulas indicate the numbers of each type of atom in a molecule. For example, the formula for glucose is Ch3O, while its molecular formula is C6h22O6. This is possible if the relevant bonding is easy to show in one dimension, an example is the condensed molecular/chemical formula for ethanol, which is Ch4-Ch3-OH or Ch4Ch3OH. For reasons of structural complexity, there is no condensed chemical formula that specifies glucose, chemical formulas may be used in chemical equations to describe chemical reactions and other chemical transformations, such as the dissolving of ionic compounds into solution. A chemical formula identifies each constituent element by its chemical symbol, in empirical formulas, these proportions begin with a key element and then assign numbers of atoms of the other elements in the compound, as ratios to the key element. For molecular compounds, these numbers can all be expressed as whole numbers. For example, the formula of ethanol may be written C2H6O because the molecules of ethanol all contain two carbon atoms, six hydrogen atoms, and one oxygen atom. Some types of compounds, however, cannot be written with entirely whole-number empirical formulas. An example is boron carbide, whose formula of CBn is a variable non-whole number ratio with n ranging from over 4 to more than 6.5. When the chemical compound of the consists of simple molecules. These types of formulas are known as molecular formulas and condensed formulas. A molecular formula enumerates the number of atoms to reflect those in the molecule, so that the formula for glucose is C6h22O6 rather than the glucose empirical formula. However, except for very simple substances, molecular chemical formulas lack needed structural information, for simple molecules, a condensed formula is a type of chemical formula that may fully imply a correct structural formula. For example, ethanol may be represented by the chemical formula Ch4Ch3OH
2. Агрегатное состояние – In physics, a state of matter is one of the distinct forms that matter takes on. Four states of matter are observable in everyday life, solid, liquid, gas, some other states are believed to be possible but remain theoretical for now. For a complete list of all states of matter, see the list of states of matter. Historically, the distinction is based on qualitative differences in properties. Matter in the state maintains a fixed volume and shape, with component particles close together. Matter in the state maintains a fixed volume, but has a variable shape that adapts to fit its container. Its particles are close together but move freely. Matter in the state has both variable volume and shape, adapting both to fit its container. Its particles are close together nor fixed in place. Matter in the state has variable volume and shape, but as well as neutral atoms, it contains a significant number of ions and electrons. Plasma is the most common form of matter in the universe. The term phase is used as a synonym for state of matter. In a solid the particles are packed together. The forces between particles are strong so that the particles move freely but can only vibrate. As a result, a solid has a stable, definite shape, solids can only change their shape by force, as when broken or cut. In crystalline solids, the particles are packed in a regularly ordered, there are various different crystal structures, and the same substance can have more than one structure. For example, iron has a cubic structure at temperatures below 912 °C. Ice has fifteen known crystal structures, or fifteen solid phases, glasses and other non-crystalline, amorphous solids without long-range order are not thermal equilibrium ground states, therefore they are described below as nonclassical states of matter
3. Плотность – The density, or more precisely, the volumetric mass density, of a substance is its mass per unit volume. The symbol most often used for density is ρ, although the Latin letter D can also be used. Mathematically, density is defined as mass divided by volume, ρ = m V, where ρ is the density, m is the mass, and V is the volume. In some cases, density is defined as its weight per unit volume. For a pure substance the density has the numerical value as its mass concentration. Different materials usually have different densities, and density may be relevant to buoyancy, purity, osmium and iridium are the densest known elements at standard conditions for temperature and pressure but certain chemical compounds may be denser. Thus a relative density less than one means that the floats in water. The density of a material varies with temperature and pressure and this variation is typically small for solids and liquids but much greater for gases. Increasing the pressure on an object decreases the volume of the object, increasing the temperature of a substance decreases its density by increasing its volume. In most materials, heating the bottom of a results in convection of the heat from the bottom to the top. This causes it to rise relative to more dense unheated material, the reciprocal of the density of a substance is occasionally called its specific volume, a term sometimes used in thermodynamics. Density is a property in that increasing the amount of a substance does not increase its density. Archimedes knew that the irregularly shaped wreath could be crushed into a cube whose volume could be calculated easily and compared with the mass, upon this discovery, he leapt from his bath and ran naked through the streets shouting, Eureka. As a result, the term eureka entered common parlance and is used today to indicate a moment of enlightenment, the story first appeared in written form in Vitruvius books of architecture, two centuries after it supposedly took place. Some scholars have doubted the accuracy of this tale, saying among other things that the method would have required precise measurements that would have been difficult to make at the time, from the equation for density, mass density has units of mass divided by volume. As there are units of mass and volume covering many different magnitudes there are a large number of units for mass density in use. The SI unit of kilogram per metre and the cgs unit of gram per cubic centimetre are probably the most commonly used units for density.1,000 kg/m3 equals 1 g/cm3. In industry, other larger or smaller units of mass and or volume are often more practical, see below for a list of some of the most common units of density
4. Кельвин – The kelvin is a unit of measure for temperature based upon an absolute scale. It is one of the seven units in the International System of Units and is assigned the unit symbol K. The kelvin is defined as the fraction 1⁄273.16 of the temperature of the triple point of water. In other words, it is defined such that the point of water is exactly 273.16 K. The Kelvin scale is named after the Belfast-born, Glasgow University engineer and physicist William Lord Kelvin, unlike the degree Fahrenheit and degree Celsius, the kelvin is not referred to or typeset as a degree. The kelvin is the unit of temperature measurement in the physical sciences, but is often used in conjunction with the Celsius degree. The definition implies that absolute zero is equivalent to −273.15 °C, Kelvin calculated that absolute zero was equivalent to −273 °C on the air thermometers of the time. This absolute scale is known today as the Kelvin thermodynamic temperature scale, when spelled out or spoken, the unit is pluralised using the same grammatical rules as for other SI units such as the volt or ohm. When reference is made to the Kelvin scale, the word kelvin—which is normally a noun—functions adjectivally to modify the noun scale and is capitalized, as with most other SI unit symbols there is a space between the numeric value and the kelvin symbol. Before the 13th CGPM in 1967–1968, the unit kelvin was called a degree and it was distinguished from the other scales with either the adjective suffix Kelvin or with absolute and its symbol was °K. The latter term, which was the official name from 1948 until 1954, was ambiguous since it could also be interpreted as referring to the Rankine scale. Before the 13th CGPM, the form was degrees absolute. The 13th CGPM changed the name to simply kelvin. Its measured value was 7002273160280000000♠0.01028 °C with an uncertainty of 60 µK, the use of SI prefixed forms of the degree Celsius to express a temperature interval has not been widely adopted. In 2005 the CIPM embarked on a program to redefine the kelvin using a more experimentally rigorous methodology, the current definition as of 2016 is unsatisfactory for temperatures below 20 K and above 7003130000000000000♠1300 K. In particular, the committee proposed redefining the kelvin such that Boltzmanns constant takes the exact value 6977138065049999999♠1. 3806505×10−23 J/K, from a scientific point of view, this will link temperature to the rest of SI and result in a stable definition that is independent of any particular substance. From a practical point of view, the redefinition will pass unnoticed, the kelvin is often used in the measure of the colour temperature of light sources. Colour temperature is based upon the principle that a black body radiator emits light whose colour depends on the temperature of the radiator, black bodies with temperatures below about 7003400000000000000♠4000 K appear reddish, whereas those above about 7003750000000000000♠7500 K appear bluish
5. Температура плавления – The melting point of a solid is the temperature at which it changes state from solid to liquid at atmospheric pressure. At the melting point the solid and liquid phase exist in equilibrium, the melting point of a substance depends on pressure and is usually specified at standard pressure. When considered as the temperature of the change from liquid to solid. Because of the ability of some substances to supercool, the point is not considered as a characteristic property of a substance. For most substances, melting and freezing points are approximately equal, for example, the melting point and freezing point of mercury is 234.32 kelvins. However, certain substances possess differing solid-liquid transition temperatures, for example, agar melts at 85 °C and solidifies from 31 °C to 40 °C, such direction dependence is known as hysteresis. The melting point of ice at 1 atmosphere of pressure is close to 0 °C. In the presence of nucleating substances the freezing point of water is the same as the melting point, the chemical element with the highest melting point is tungsten, at 3687 K, this property makes tungsten excellent for use as filaments in light bulbs. Many laboratory techniques exist for the determination of melting points, a Kofler bench is a metal strip with a temperature gradient. Any substance can be placed on a section of the strip revealing its thermal behaviour at the temperature at that point, differential scanning calorimetry gives information on melting point together with its enthalpy of fusion. A basic melting point apparatus for the analysis of crystalline solids consists of an oil bath with a transparent window, the several grains of a solid are placed in a thin glass tube and partially immersed in the oil bath. The oil bath is heated and with the aid of the melting of the individual crystals at a certain temperature can be observed. In large/small devices, the sample is placed in a heating block, the measurement can also be made continuously with an operating process. For instance, oil refineries measure the point of diesel fuel online, meaning that the sample is taken from the process. This allows for more frequent measurements as the sample does not have to be manually collected, for refractory materials the extremely high melting point may be determined by heating the material in a black body furnace and measuring the black-body temperature with an optical pyrometer. For the highest melting materials, this may require extrapolation by several hundred degrees, the spectral radiance from an incandescent body is known to be a function of its temperature. An optical pyrometer matches the radiance of a body under study to the radiance of a source that has been previously calibrated as a function of temperature, in this way, the measurement of the absolute magnitude of the intensity of radiation is unnecessary. However, known temperatures must be used to determine the calibration of the pyrometer, for temperatures above the calibration range of the source, an extrapolation technique must be employed
6. Теплопроводность – In physics, thermal conductivity is the property of a material to conduct heat. It is evaluated primarily in terms of Fouriers Law for heat conduction, heat transfer occurs at a lower rate across materials of low thermal conductivity than across materials of high thermal conductivity. Correspondingly, materials of high thermal conductivity are used in heat sink applications. The thermal conductivity of a material may depend on temperature, the reciprocal of thermal conductivity is called thermal resistivity. Thermal conductivity is actually a tensor, which means it is possible to have different values in different directions, in SI units, thermal conductivity is measured in watts per meter-kelvin. The dimension of thermal conductivity is M1L1T−3Θ−1 and these variables are mass, length, time, and temperature. In Imperial units, thermal conductivity is measured in BTU/, other units which are closely related to the thermal conductivity are in common use in the construction and textile industries. The construction industry makes use of such as the R-value. Although related to the conductivity of a material used in an insulation product, R-. Likewise the textile industry has several units including the tog and the clo which express thermal resistance of a material in a way analogous to the R-values used in the construction industry, there are a number of ways to measure thermal conductivity. Each of these is suitable for a range of materials, depending on the thermal properties. There is a distinction between steady-state and transient techniques, in general, steady-state techniques are useful when the temperature of the material does not change with time. This makes the signal analysis straightforward, the disadvantage is that a well-engineered experimental setup is usually needed. The Divided Bar is the most common used for consolidated rock solids. Thermal conductivity is important in science, research, electronics, building insulation and related fields. Several materials are shown in the list of thermal conductivities and these should be considered approximate due to the uncertainties related to material definitions. High energy generation rates within electronics or turbines require the use of materials with high thermal conductivity such as copper, aluminium, the reciprocal of thermal conductivity is thermal resistivity, usually expressed in kelvin-meters per watt. For a given thickness of a material, that particular constructions thermal resistance, unfortunately, there are differing definitions for these terms
7. SMILES – The simplified molecular-input line-entry system is a specification in form of a line notation for describing the structure of chemical species using short ASCII strings. SMILES strings can be imported by most molecule editors for conversion back into two-dimensional drawings or three-dimensional models of the molecules, the original SMILES specification was initiated in the 1980s. It has since modified and extended. In 2007, a standard called OpenSMILES was developed in the open-source chemistry community. Other linear notations include the Wiswesser Line Notation, ROSDAL and SLN, the original SMILES specification was initiated by David Weininger at the USEPA Mid-Continent Ecology Division Laboratory in Duluth in the 1980s. The Environmental Protection Agency funded the project to develop SMILES. It has since modified and extended by others, most notably by Daylight Chemical Information Systems. In 2007, a standard called OpenSMILES was developed by the Blue Obelisk open-source chemistry community. Other linear notations include the Wiswesser Line Notation, ROSDAL and SLN, in July 2006, the IUPAC introduced the InChI as a standard for formula representation. SMILES is generally considered to have the advantage of being slightly more human-readable than InChI, the term SMILES refers to a line notation for encoding molecular structures and specific instances should strictly be called SMILES strings. However, the term SMILES is also used to refer to both a single SMILES string and a number of SMILES strings, the exact meaning is usually apparent from the context. The terms canonical and isomeric can lead to confusion when applied to SMILES. The terms describe different attributes of SMILES strings and are not mutually exclusive, typically, a number of equally valid SMILES strings can be written for a molecule. For example, CCO, OCC and CC all specify the structure of ethanol, algorithms have been developed to generate the same SMILES string for a given molecule, of the many possible strings, these algorithms choose only one of them. This SMILES is unique for each structure, although dependent on the algorithm used to generate it. These algorithms first convert the SMILES to a representation of the molecular structure. A common application of canonical SMILES is indexing and ensuring uniqueness of molecules in a database, there is currently no systematic comparison across commercial software to test if such flaws exist in those packages. SMILES notation allows the specification of configuration at tetrahedral centers, and these are structural features that cannot be specified by connectivity alone and SMILES which encode this information are termed isomeric SMILES
8. International Chemical Identifier – Initially developed by IUPAC and NIST from 2000 to 2005, the format and algorithms are non-proprietary. The continuing development of the standard has supported since 2010 by the not-for-profit InChI Trust. The current version is 1.04 and was released in September 2011, prior to 1.04, the software was freely available under the open source LGPL license, but it now uses a custom license called IUPAC-InChI Trust License. Not all layers have to be provided, for instance, the layer can be omitted if that type of information is not relevant to the particular application. InChIs can thus be seen as akin to a general and extremely formalized version of IUPAC names and they can express more information than the simpler SMILES notation and differ in that every structure has a unique InChI string, which is important in database applications. Information about the 3-dimensional coordinates of atoms is not represented in InChI, the InChI algorithm converts input structural information into a unique InChI identifier in a three-step process, normalization, canonicalization, and serialization. The InChIKey, sometimes referred to as a hashed InChI, is a fixed length condensed digital representation of the InChI that is not human-understandable. The InChIKey specification was released in September 2007 in order to facilitate web searches for chemical compounds and it should be noted that, unlike the InChI, the InChIKey is not unique, though collisions can be calculated to be very rare, they happen. In January 2009 the final 1.02 version of the InChI software was released and this provided a means to generate so called standard InChI, which does not allow for user selectable options in dealing with the stereochemistry and tautomeric layers of the InChI string. The standard InChIKey is then the hashed version of the standard InChI string, the standard InChI will simplify comparison of InChI strings and keys generated by different groups, and subsequently accessed via diverse sources such as databases and web resources. Every InChI starts with the string InChI= followed by the version number and this is followed by the letter S for standard InChIs. The remaining information is structured as a sequence of layers and sub-layers, the layers and sub-layers are separated by the delimiter / and start with a characteristic prefix letter. The six layers with important sublayers are, Main layer Chemical formula and this is the only sublayer that must occur in every InChI. The atoms in the formula are numbered in sequence, this sublayer describes which atoms are connected by bonds to which other ones. Describes how many hydrogen atoms are connected to each of the other atoms, the condensed,27 character standard InChIKey is a hashed version of the full standard InChI, designed to allow for easy web searches of chemical compounds. Most chemical structures on the Web up to 2007 have been represented as GIF files, the full InChI turned out to be too lengthy for easy searching, and therefore the InChIKey was developed. With all databases currently having below 50 million structures, such duplication appears unlikely at present, a recent study more extensively studies the collision rate finding that the experimental collision rate is in agreement with the theoretical expectations. Example, Morphine has the structure shown on the right, as the InChI cannot be reconstructed from the InChIKey, an InChIKey always needs to be linked to the original InChI to get back to the original structure
9. ChemSpider – ChemSpider is a database of chemicals. ChemSpider is owned by the Royal Society of Chemistry, the database contains information on more than 50 million molecules from over 500 data sources including, Each chemical is given a unique identifier, which forms part of a corresponding URL. This is an approach to develop an online chemistry database. The search can be used to widen or restrict already found results, structure searching on mobile devices can be done using free apps for iOS and for the Android. The ChemSpider database has been used in combination with text mining as the basis of document markup. The result is a system between chemistry documents and information look-up via ChemSpider into over 150 data sources. ChemSpider was acquired by the Royal Society of Chemistry in May,2009, prior to the acquisition by RSC, ChemSpider was controlled by a private corporation, ChemZoo Inc. The system was first launched in March 2007 in a release form. ChemSpider has expanded the generic support of a database to include support of the Wikipedia chemical structure collection via their WiChempedia implementation. A number of services are available online. SyntheticPages is an interactive database of synthetic chemistry procedures operated by the Royal Society of Chemistry. Users submit synthetic procedures which they have conducted themselves for publication on the site and these procedures may be original works, but they are more often based on literature reactions. Citations to the published procedure are made where appropriate. They are checked by an editor before posting. The pages do not undergo formal peer-review like a journal article. The comments are moderated by scientific editors. The intention is to collect practical experience of how to conduct useful chemical synthesis in the lab, while experimental methods published in an ordinary academic journal are listed formally and concisely, the procedures in ChemSpider SyntheticPages are given with more practical detail. Comments by submitters are included as well, other publications with comparable amounts of detail include Organic Syntheses and Inorganic Syntheses
10. Хром – Chromium is a chemical element with symbol Cr and atomic number 24. It is the first element in Group 6 and it is a steely-grey, lustrous, hard and brittle metal which takes a high polish, resists tarnishing, and has a high melting point. The name of the element is derived from the Greek word χρῶμα, chrōma, meaning color, Chromium metal is of high value for its high corrosion resistance and hardness. A major development was the discovery that steel could be highly resistant to corrosion and discoloration by adding metallic chromium to form stainless steel. Stainless steel and chrome plating together comprise 85% of the commercial use, trivalent chromium ion is an essential nutrient in trace amounts in humans for insulin, sugar and lipid metabolism, although the issue is debated. While chromium metal and Cr ions are not considered toxic, hexavalent chromium is toxic and carcinogenic, abandoned chromium production sites often require environmental cleanup. Chromium is remarkable for its properties, it is the only elemental solid which shows antiferromagnetic ordering at room temperature. Above 38 °C, it changes to paramagnetic, Chromium metal left standing in air is passivated by oxidation, forming a thin, protective, surface layer. This layer is a structure only a few molecules thick. It is very dense, and prevents the diffusion of oxygen into the underlying metal and this is different from the oxide that forms on iron and carbon steel, through which elemental oxygen continues to migrate, reaching the underlying material to cause incessant rusting. Passivation can be enhanced by short contact with oxidizing acids like nitric acid, passivated chromium is stable against acids. Passivation can be removed with a reducing agent that destroys the protective oxide layer on the metal. Chromium metal treated in this way readily dissolves in weak acids, Chromium, unlike such metals as iron and nickel, does not suffer from hydrogen embrittlement. However, it suffer from nitrogen embrittlement, reacting with nitrogen from air. Chromium is the 22nd most abundant element in Earths crust with a concentration of 100 ppm. Chromium compounds are found in the environment from the erosion of chromium-containing rocks, Chromium is mined as chromite ore. About two-fifths of the ores and concentrates in the world are produced in South Africa, while Kazakhstan, India, Russia. Untapped chromite deposits are plentiful, but geographically concentrated in Kazakhstan, although rare, deposits of native chromium exist
wikivisually.com
Способ получения борида хрома
Сущность изобретения: процесс выплавки продукта в руднотермической электропечи на блок ведут с использованием шихты, в которой отношение триоксида бора к хрому сесквиоксиду и углерода в шихте к сумме оксидов хрома и бора соответственно равно 0,3 - 0,45 и 0,25 - 0,4. Затем полученный в руднотермической печи блок подвергают тонкому измельчению с последующим рассевом, отделяя класс минус 0,4, а годную фракцию подвергают гравитационно-воздушной очистке до концентрации углерода 1,0 - 2,0. Полученный полупродукт доизмельчают до крупности минус 0,4 мм, смешивают с отсевами, отсевают фракцию минус 0,2 и оставшуюся часть подвергают гравитационно-воздушной или гидравлической очистке от свободного углерода до концентрации 0,5 - 1%. Затем полупродукт доизмельчают до крупности минус 0,2, смешивают с отсевами, подвергают их гидравлической очистке от свободного углерода с последующей обработкой минеральными кислотами. 3 з.п. ф-лы, 6 табл.
Изобретение относится к металлургии, в частности к способам получения карбидов металлов в рудно-термической электропечи.
Известен способ получения карбидов металлов в электропечи [1]. Наиболее близким техническим решением является способ получения карбоборида хрома [2], состава, мас.%: Сr 68-72; бор 10-12; связанный углерод 13,6-15,8. Этот способ осуществляют в дуговой электропечи плавкой на блок, чередуя шихту двух видов, на первой стадии используют шихту, в которой отношение триоксида дибора к сесквиоксиду хрома равно 0,4-0,6, а отношение углерода к сумме оксидов и бора равно 0,5-0,55, вторую стадию - корректировку шихты осуществляют, используя шихту, в которой при прежнем отношении триоксида дибора к сесквиоксиду дихрома, отношение углерода к сумме оксидов хрома и бора берут равным 0,45-0,49. Этот прием обеспечивает заданное содержание связанного углерода в карбориде хрома, однако сплав получают неравновесным по углероду и, кроме того, он содержит до 15 мас.% Сч3С2. Использование шихты двух составов усложняет процесс и приводит к получению блока сплава неравномерного состава. Этот продукт обладает положительными свойствами при использовании его в качестве наплавочного материала. Однако он имеет и целый ряд недостатков. Поскольку кристаллизация сплава идет на блок, то он содержит 13-16% связанного. При наплавке, например, порошковой лентой поверхности детали в результате выделения углерода по границам зерен образуются поры. Наличие пор недопустимо, поскольку они являются местами значительного разрушения, например, засыпных аппаратов доменных печей при одновременном воздействии на контактную поверхность колошниковой пыли и агрессивного газа. Наличие в продукте в равновесном состоянии трех фаз борида хрома (CrB) 80-85%, Cr3C2(10-15% ) и графита до 6%, приводит к тому, что не достигается необходимая степень легирования поверхности бором, а поверхность детали имеет более низкую твердость (на 10-20%). Кроме этого, наличие Cr3C2, фазы, имеющей низкую пластичность, приводит к тому, что она слабо сопротивляется ударным нагрузкам. Указанные недостатки могут быть устранены при использовании для этих целей твердых растворов хром-бор-углерод с отношением бора к хрому, равным 0,2-0,3, и отношением углерода связанного к сумме бора и хрома в сплаве, равным 0,05-0,1. При таком соотношении будет получаться однофазный продукт - борид хрома, содержащий от 5 до 8 мас.% углерода в твердом растворе. Состав продукта, следующий мас.%: хром 75-82, бор 14-17 и связанный углерод 5-8. Микротвердость этого материала составляет 2000-2400 кг/мм2, модуль упругости повышается до 4500 кгс/мм2, наличие пор при наплавке, образующихся за счет выделения графита, исключается. Отсутствие хрупкой фазы Cr3C2 повышает износостойкость на 20-25%. Целью изобретения является получение однофазного борида хрома с отношением бора к хрому и углерода связанного к сумме элементов, равным, соответственно, 0,2-0,3 и 0,05-0,1, повышение износостойкости покрытий на деталях, упрощение процесса и повышение выхода годного. Сущность изобретения заключается в том, что процесс выплавки продукта в рудно-термической электропечи на блок ведут с использованием шихты, в которой отношение триоксида дибора к хрому сесквиоксиду составляет 0,3-0,45, а отношение углерода к сумме оксидов бора и хрома равно 0,25-0,4. С целью снижения потерь мелких фракций борида хрома при удалении свободного углерода и примесей продукт сначала измельчают до крупности минус 5 мм, затем отсевают фракцию минус 0,4 мм, а фракцию 5-0,4 мм подвергают гравитационно-воздушной очистке с удалением свободного углерода до концентраций 1,0-2,0% , затем диспергируют его до фракции минус 0,4 мм, смешивают с отсевами предыдущей операции, отсевают фракцию минус 0,2 мм, а класс 0,4-0,2 мм подвергают гравитационно-воздушной или гидравлической очистке от порошка от свободного углерода до концентраций 0,5-1,0% , затем диспергируют класс минус 0,4-0,2 до крупности минус 0,2, смешивают его с отсевами предыдущей операции и подвергают гидравлической очистке от свободного углерода с последующей обработкой минеральными кислотами для удаления примесей серы. Если использовать шихту, в которой отношение триоксида дибора к хрому сесквиоксиду будет меньше 0,3, то не будет обеспечено условие получения твердого раствора углерода в бориде хрома из-за низкого содержания бора. Отношение оксида бора к оксиду хрома более 0,45 не обеспечит получения однофазного твердого раствора углерода в бориде хрома из-за низкого содержания хрома. Если отношение углерода к сумме оксидов хрома и бору будет меньше 0,25, то не будет обеспечено получение однофазного твердого раствора углерода в бориде хрома из-за низкого содержания углерода, наличия недовосстановленных оксидов. Отношение углерода к сумме оксидов хрома и бора более 0,04 недопустимо из-за высокого избытка углерода, получения неравновесных твердых растворов и значительного выделения графита при наплавке. При стадии очистки обеспечивают оптимальные условия удаления свободного углерода и других примесей при незначительных потерях годного продукта мелких фракций. Если для гравитационно-воздушной очистки использовать продукт крупностью более 5 мм, то не обеспечится глубина очистки от свободного углерода менее 1%. Измельчение материала до крупности менее 0,4 мм недопустимо из-за высоких потерь продукта при очистке. Предварительный отсев фракции минус 0,4 мм исключает потери продукта при гравитационно-воздушной очистке. Продукт класса 5-0,4 мм используется самостоятельно для легирования специальных материалов, используемых для напыления и служит полупродуктом для получения сплава более мелких классов. Последующее измельчение продукта крупностью 5-0,4 мм до крупности минус 0,4 с возвратом отсева предыдущей операции с отсевом фракции минус 0,2 мм обеспечивает не только стабильное удаление свободного углерода до концентрации 0,5-1,0% , но и исключает потери фракций минус 0,2 мм и обеспечивает высокую производительность процесса и выход годного. Порошок класса 0,4-0,2 мм - самостоятельный продукт, который используется как материал для электродов, наплавочных лент, создания композиционных порошков, так и служит полупродуктом для получения порошка фракции минус 0,2 мм. Последующее измельчение класса 0,4-0,2 мм до фракции минус 0,2 мм с возвратом отсевов фракции предыдущей операции (класс - 0,2 мм) без измельчения исключает переизмельчение отсевов фракции минус 0,02 мм, а, следовательно, повышен выход годного при очистке продукта. Отработка класса минус 0,2 мм минеральными кислотами обеспечивает удаление примесей серы до концентрации менее 0,04 %. Борид хрома класса минус 0,2 мм использовали для производства наплавочных материалов повышенного качества и особого назначения, а также как композиционный порошок для напыления. В табл.1 представлен химический состав элементов (борид хрома). Гранулометрический состав представлен в табл. 2. В табл. 3 представлен химический состав полупродукта и показатели плавки. Состав полупродукта плавок 2 и 3 соответствует требованиям по всем элементам и свободного углерода, кроме серы для марки БХ-1. В табл. 4 представлен состав продукта БХ-1 и БХ-2 после дробления до фракции 5,0-0,4 и без отсева фракции минус 0,4, отсева фракции минус 0,4 и гравитационной очистки от свободного углерода плавок 2 и 3. Таким образом, для класса 0,4-5,0 мм обеспечиваются оптимальные условия удаления свободного углерода при минимальных потерях. Продукт соответствует марке БХ-2 по всем элементам. Для марки БХ-1 сера выше требований. Переизмельчение или измельчение до минус 6,0 приводит к очень большим потерям. В табл. 5 представлен состав продукта после диспергирования до минус 0,4; минус 0,5 и выделения класса 0,4-0,2 смешиванием с отсевами с последующей гидравлической отмывкой. Помол крупнее 0,4 и менее 0,2 недопустим из-за очень высоких потерь. Продукт полностью соответствует марке БХ-2 и БХ-1 по всем элементам, кроме серы. В табл. 6 представлен состав продукта после измельчения до фракции минус 0,2 смешением с отсевами класса минус 0,2 и последующей обработкой 5%-ной соляной кислотой при Т:Ж=1:5. По всем элементам продукт соответствует маркам БХ-1 и БХ-2, кроме вариантов помола до крупности минус 0,4 по сере. Таким образом выбранный интервал обеспечивает получение продукта в соответствии с требованиями с минимальными потерями. Изучение микроструктуры, локальный и рентгено-структурный анализы показали, что предложенный способ обеспечивает получение однофазных твердых растворов углерода в бориде хрома. Микротвердость составляет 2000-2400 кг/мм2, модуль упругости 4000-4500 кгс/мм2, износостойкость наплавленного слоя увеличивается до 900-1100 ч, т. е. на 20-30%.Формула изобретения
1. СПОСОБ ПОЛУЧЕНИЯ БОРИДА ХРОМА, включающий приготовление шихты путем смешивания порошков оксидов хрома и бора и углеродистого восстановителя с окомкованием ее, порционную загрузку шихты в руднотермическую печь, термообработку и последующее измельчение полупродукта с отделением свободного углерода и примесей, отличающийся тем, что, с целью повышения однофазного борида хрома с отношением бора к хрому и связанного углерода к сумме элементов, соответственно 0,2 - 0,3 и 0,05 - 0,1, повышения износостойкости покрытий на делатях, упрощения процесса и повышения выхода годного, термообработку шихты проводят при отношении триоксида бора к хрому сесквиоксиду и углерода в шихте к сумме оксидов хрома и бора соответственно 0,3 - 0,45 и 0,25 - 0,4. 2. Способ по п. 1, отличающийся тем, что, с целью снижения потерь и получения продукта класса 0,4 - 5,0 мм, после термообработки полупродукт подвергают тонкому измельчению и рассеву с отделением фракции -0,4 и последующей гравитационно-воздушной очистке годной фракции до концентрации углерода 1,0 - 2,0. 3. Способ по пп. 1 и 2, отличающийся тем, что, с целью повышения степени очистки, выхода годного и получения фракции 0,2 - 0,4, полупродукт по п.2, доизмельчают до крупности -0,4 мм, смешивают с отсевами, отделяют фракцию -0,2 и оставшуюся часть подвергают гравитационно-воздушной или гидравлической очистке от свободного углерода до концентрации 0,5 - 1%. 4. Способ по пп. 1 - 3, отличающийся тем, что, с целью повышения степени очистки от серы и получения продукта фракции -0,2, полупродукт по п.3 доизмельчают до крупности -0,2, смешивают с отсевами по п.3, подвергают их гидравлической очистке от свободного углерода с последующей обработкой минеральными кислотами.РИСУНКИ
Рисунок 1, Рисунок 2www.findpatent.ru
Способ получения борида хрома
Изобретение предназначено для химической промышленности и атомной энергетики и может быть использовано при получении нейтронопоглощающих материалов и высокотемпературных огнеупоров. Бор аморфный, полученный магнийтермическим способом, с содержанием бора общего не менее 93,0 мас.% и магния не менее 1,4 мас.% смешивают с порошком хрома, размер частиц которого не превышает 250 мкм. Соотношение бора и хрома близкое к стехиометрическому. Полученную шихту брикетируют при увлажнении до влажности 16-22 мас.% и давлении прессования 280-400 кг/см2. Синтез борида хрома проводят в вакууме при остаточном давлении не более 6,5 Па при повышении температуры до 1600-1700 С в течение не менее 2,5 часов. Выход CrB2 – не менее 98,0 мас.%, содержание углерода – менее 0,5 мас.%. Способ прост, экономичен, себестоимость конечного продукта снижена в 1,3-1,5 раза при его высоком качестве. 3 з.п. ф-лы, 1 табл.
С в течение не менее 2,5 часов. Выход CrB2 – не менее 98,0 мас.%, содержание углерода – менее 0,5 мас.%. Способ прост, экономичен, себестоимость конечного продукта снижена в 1,3-1,5 раза при его высоком качестве. 3 з.п. ф-лы, 1 табл.
Изобретение предназначено для химической промышленности, а именно для получения тугоплавкого соединения преимущественного состава СrВ2, которое может найти применение в атомной энергетике (нейтронопоглощающие материалы - боропласты), в промышленности в качестве износостойкого наплавочного компонента и при получении высокотемпературных огнеупоров.
Известен способ получения борида хрома состава СrВ2 высокотемпературным восстановлением оксидов хрома и бора углеродом в токе инертного газа. При этом получается диборид хрома, содержащий 65,0% Сr, 26,7% В (H.Blumenthal. Pow. Metal. Bull., 7, 79, 1956).
Недостатком данного способа является низкий выход основного продукта (не более 93,0 мас.%) и, как следствие, большое содержание примеси (1,8 маc.%) в виде остаточного углерода.
Известен способ получения диборида хрома методом синтеза из элементов, заключающийся в спекании брикетов, спрессованных из порошков хрома и бора при температуре 1150-1350 С в продолжение 36 часов в атмосфере аргона (В.А.Эпельбаум и др. ЖНХ, 1957, т.2, с.1847. и Г.В.Самсонов и др. Бор, его соединения и сплавы. Киев: Издат. АН УССР, 1960, с.394).
С в продолжение 36 часов в атмосфере аргона (В.А.Эпельбаум и др. ЖНХ, 1957, т.2, с.1847. и Г.В.Самсонов и др. Бор, его соединения и сплавы. Киев: Издат. АН УССР, 1960, с.394).
К недостаткам способа относится высокая себестоимость продукта из-за использования чистого и очень дорогого бора, а также длительности и энергоемкости синтеза в атмосфере аргона.
Таким образом, технической задачей является получение диборида хрома с содержанием углерода менее 0,5 мас.% из относительно дешевого сырья с обеспечением выхода конечного продукта не менее 98,0 мас.%.
Поставленная задача решается в способе получения борида хрома (преимущественно состава СrВ2) синтезом из элементов, включающем стадии смешения бора и хрома, брикетирования шихты и высокотемпературного синтеза и размола. Для синтеза используют бор аморфный, полученный магнийтермическим способом, с содержанием бора общего не менее 93,0 мас.% и магния не менее 1,4 мас.%. При этом размер частиц порошка хрома не превышает 250 мкм. Смешение бора и хрома проводят при соотношении, близком к эквимолярному (стехиометрическому по СrВ2). Брикетирование смеси проводят при ее увлажнении до влажности 16-22 мас.% и давлении прессования 280-400 кг/см2. Синтез проводят в вакууме при повышении температуры до 1600-1700 С в течение не менее 2,5 часов.
С в течение не менее 2,5 часов.
Отличие предлагаемого способа от прототипа и аналогов заключается, главным образом, в использовании сырья - аморфного бора - с относительно низким содержанием основного вещества (за счет чего более дешевого - в 2 раза), но с регламентированным содержанием примеси магния (1,4-4,5 мас.%), что возможно при использовании только магнийтермического бора. Магний, содержащийся в аморфном боре в виде боридов магния, при температуре выше 1500 С начинает испаряться, что способствует ускорению гетерофазных процессов за счет повышения пористости.
С начинает испаряться, что способствует ускорению гетерофазных процессов за счет повышения пористости.
Использование в качестве исходного борсодержащего материала аморфного бора чистотой не менее 93 мас.% и содержащего не менее 1,4 мас.% магния обеспечивает высокий выход получаемого борида хрома. Снижение чистоты основного вещества менее 93,0 мас.% приводит к повышенному содержанию магния, высокой пористости в продукте синтеза и пониженному выходу из-за большей потере бора. Меньшее содержание магния в боре (менее 1,4 мас.%) способствует образованию более плотной массы синтезируемого продукта, что приводит к повышению длительности процесса, и следовательно, большим потерям бора за счет его испарения. Использование хрома в виде порошка с размером частиц менее 250 мкм (наиболее оптимально менее 160 мкм) обеспечивает высокую скорость реакции, полноту синтеза и гомогенизацию продуктов синтеза. При размере частиц хрома более 250 мкм повышается длительность синтеза. Проведение высокотемпературного синтеза в вакууме облегчает удаление паров магния из реакционной массы при меньших температурах и, следовательно, обеспечивает проведение синтеза также при более низких температурах. Брикетирование увлажненной смеси компонентов при давлении прессования 280-400 кг/см2 обеспечивает оптимальную площадь контакта между твердофазными реагентами и облегчает прохождение диффузионного механизма образования борида хрома. При давлении прессования менее 280 кг/см2 выход диборида хрома снижается из-за недостаточной площади контакта между твердофазными реагентами. При давлении прессования выше 400 кг/см2 синтезируемый продукт имеет слишком высокую механическую прочность, что усложняет в дальнейшем его измельчение. Предложенный режим нагрева исходных твердофазных реагентов (при нагреве до 1600-1700 С в течение не менее 2,5 часов) обеспечивает заданный выход и характеристики продукта. При температуре синтеза менее 1600
С в течение не менее 2,5 часов) обеспечивает заданный выход и характеристики продукта. При температуре синтеза менее 1600 С или нагреве в течение менее 2,5 часов снижается выход диборида хрома из-за низкой степени участия в реакции компонентов (наличие несвязанных исходных элементов). При температуре синтеза более 1700
С или нагреве в течение менее 2,5 часов снижается выход диборида хрома из-за низкой степени участия в реакции компонентов (наличие несвязанных исходных элементов). При температуре синтеза более 1700 С образуется очень прочный материал, измельчение которого затруднительно. При этом увеличиваются потери бора за счет его испарения и снижается выход диборида хрома.
С образуется очень прочный материал, измельчение которого затруднительно. При этом увеличиваются потери бора за счет его испарения и снижается выход диборида хрома.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1. Порошковый аморфный бор (чистотой 93,0 мас.%) с содержанием 2,9% Mg) смешивают с порошком хрома, имеющего размер частиц менее 250 мкм, в соотношении 1:2,25 соответственно. Полученную смесь увлажняют до влажности 16 маc.% и запрессовывают при давлении 400 кг/см2 в брикеты диаметром 120 мм и высотой не более 70 мм. Брикеты помещают в графитовый тигель с внешней теплоизоляцией и последний устанавливают в индукционную печь. Синтез ведут при нагреве до 1600 С в течение 3,0 часов в вакууме при остаточном давлении не более 6,5 Па. Затем нагрев отключают и после охлаждения печи брикеты извлекают и подвергают измельчению до заданного дисперсного состава.
С в течение 3,0 часов в вакууме при остаточном давлении не более 6,5 Па. Затем нагрев отключают и после охлаждения печи брикеты извлекают и подвергают измельчению до заданного дисперсного состава.
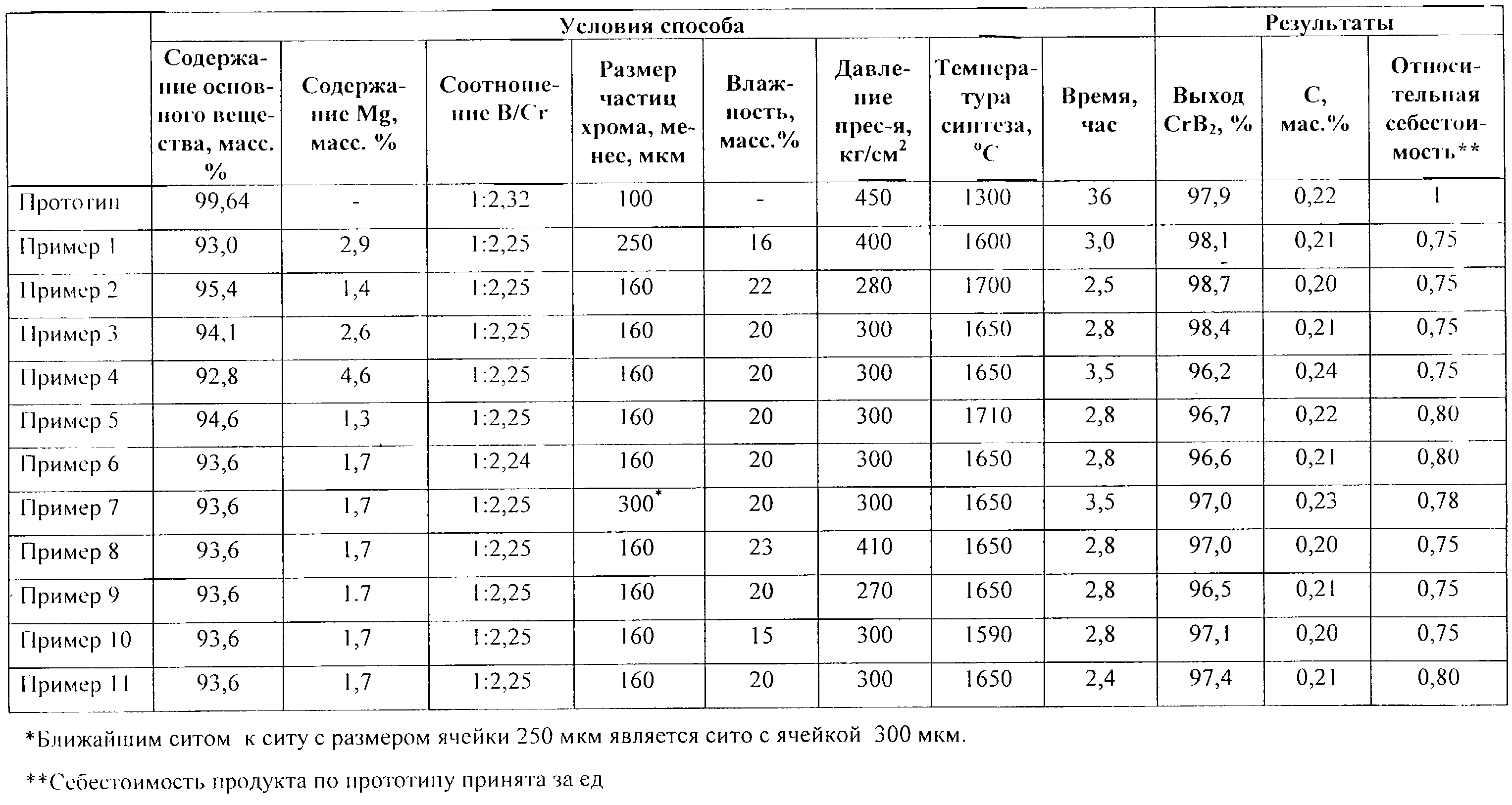
Примеры 2-15 проведены аналогично примеру 1 с изменением ряда характеристик способа. Остальные характеристики способа и полученные результаты приведены в таблице.
Из данных таблицы следует, что предлагаемый способ позволяет получить диборид хрома с выходом не меньшим, чем у прототипа, и с содержанием углерода менее 0,22 мас.%. При этом себестоимость диборида хрома в 1,3-1,5 раза ниже, чем при использовании способа-прототипа.
Формула изобретения
1. Способ получения борида хрома (преимущественно диборида) методом синтеза из элементов, включающий стадии смешения бора и хрома при соотношении, близком к стехиометрическому, брикетирования шихты, высокотемпературного синтеза и размола, отличающийся тем, что для синтеза используют бор аморфный, полученный магнийтермическим способом, с содержанием бора общего не менее 93,0 мас.% и магния не менее 1,4 мас.%.
2. Способ по п.1, отличающийся тем, что размер частиц порошка хрома не превышает 250 мкм.
3. Способ по п.1, отличающийся тем, что брикетирование смеси проводят при ее увлажнении до влажности 16-22 мас.% и давлении прессования 280-400 кг/см2.
4. Способ по п.1, отличающийся тем, что синтез проводят в вакууме при повышении температуры до 1600-1700°С в течение не менее 2,5 ч.
Похожие патенты:
Изобретение относится к способу получения слоистых высокотемпературных сверхпроводников состава MgB2, которые могут найти применение в атомной энергетике (легкие поглощающие материалы), в промышленности (абразивные порошки), а также в различных приборах электронной, измерительной и вычислительной техники в качестве высокотемпературного сверхпроводящего материала с температурой перехода в сверхпроводящее состояние Тc40 К

Изобретение относится к неорганической химии, а именно к способу получения боридов редкоземельных металлов, которые могут быть использованы при производстве термокатодных материалов

Изобретение относится к неорганической химии и порошковой металлургии, в частности к сложным (композиционным) поликристаллическим материалам системы Ti-B, которые могут быть использованы в качестве износостойких и абразивных материалов

Изобретение относится к порошковой металлургии, в частности к способам получения порошков тугоплавких неорганических соединений, а именно боридов переходных металлов, синтезом в режиме горения, которые могут быть использованы в авиационной, станкостроительной и обрабатывающей промышленности, а также в цветной металлургии

Изобретение относится к порошковой металлургии, в частности к соединениям титана с высоким содержанием бора, которые могут быть использованы в качестве износостойких, абразивных материалов и покрытий

Изобретение относится к получению борсодержащего материала на основе боридов магния который может быть использован как исходный продуккт для извлечения элементарного бора


Изобретение относится к производству жаро- и радиационностойких материалов на основе циркония, в частности к производству его диборида
Изобретение относится к технологии производства высокотвердых жаростойких материалов на основе циркония, а именно к способам получения диборида циркония

Изобретение относится к области изготовления керамических изделий, а именно к способам приготовления шихты для изготовления изделий из полученного борокарбидным методом чернового диборида циркония
Изобретение относится к металлургии тугоплавких соединений и может быть использовано в качестве керамики и защитного покрытия в высокотемпературных агрегатах

Изобретение относится к электролитическим способам получения неорганических соединений, в частности соединений неодима
Изобретение относится к электролитическим способам получения неорганических соединений, в частности соединений празеодима

Изобретение относится к получению электропроводящих соединений металлов

Изобретение относится к области химической технологии, а именно к получению новых сверхпроводящих борсодержащих соединений
Изобретение относится к электрохимическому синтезу соединений иттрия и может быть использовано для получения нанодисперсного чистого порошка гексаборида иттрия, обладающего развитой поверхностью, полупроводниковыми свойствами
Способ получения борида хрома
www.findpatent.ru
Способ получения порошка борида хрома
Сущность изобретения: процесс выплавки борида хрома в рудно-термической электропечи на блок ведут с использованием шихты, в которой отношение триоксида дибора к хрому сесквиоксиду составляет 0,46-0,8, а отношение углерода к сумме оксидов бора и хрома берут равным 0,41-0,55. Способ обеспечивает получение однофазного твердого раствора борхром. 3 табл.
Изобретение относится к металлургии, в частности к способам получения каpбидов металлов в руднотермической электропечи.
Известны способы получения карбидов металлов, например, в электропечи [1] Наиболее близким к предлагаемому является способ получения борида хрома [2] Известный способ осуществляют в другой руднотермической электропечи для получения борида хрома с отношением бора к хрому и углерода, связанного к сумме элементов равными соответственно 0,2-0,3 и 0,05-0,1 путем порционной загрузки окомкованной шихты, в которой отношение триоксида дибора к хрома сесквиоксиду и углерода в шихте к сумме оксидов хрома и бора соответственно равно 0,3-0,45 и 0,25-0,4. Этот прием обеспечивает получение сплава заданного состава, однако высокое содержание углерода приводит к получению в сплаве серы более 0,05% что недопустимо из-за резкого ухудшения условий труда при наплавке (выделение серосодержащих газов), к разбрызгиванию жидкого сплава при наплавке и образованию вторичных выделений графита, при частичном растворении хрома и бора в матрице. Газы и графит приводят к образованию пор, что снижает срок службы направленной поверхности или требует трудоемкой операции по выявлению и заварке пор. Указанные недостатки могут быть устранены при использовании для этих целей твердых растворов хром-бор с отношением бора к хрому, равным 0,15-0,35, и отношением углерода к сумме бора их рома в сплаве, равном 0,005-0,049. При таком соотношении будет получаться однофазный продукт-борид хрома, содержащий от 0,1 до 4,4 мас. углерода в виде карбоборида хрома. Состав продукта пир этом будет следующим, мас. углерод 0,1-4,4, бор 13-25, сера 0,01-0,05, хром остальное. Микроструктура будет представлена практически боридами хрома (ВС и ВхС). Количество серы в металле зависит от содержания углерода в нем. Микротвердость этого материала будет не ниже 2000 кг/мм2, при модуле упругости не менее 4500 кг/мм2. Низкое содержание углерода в сплаве обеспечит получение в структуре наплавленного слоя борида хрома, даже при частичном растворении хрома и бора в материале матрицы. При этом будут отсутствовать рыхлоты за счет выделения графита и не будет разбрызгиваться металл при наплавке ввиду отсутствия выделений газов (СО и серосодержащих). Известными методами получение борида хрома в промышленном масштабе невозможно. При использовании прототипа не обеспечивается получение равновесного, однофазного твердого раствора хром-бор. Целью изобретения является повышение качества порошка за счет получения твердого раствора бор-хром с отношением бора к хрому и углерода в сплаве к сумме основных элементов соответственно 0,15-0,35 и 0,005-0,0049, повышение износостойкости покрытий, улучшение условий труда и при наплавке и выходе годного. Эта цель достигается тем, что процесс выплавки продукта в руднотермической электропечи на блок ведут с использованием шихты, в которой отношение триоксида дибора к хрому сесквиоксиду составляет 0,46-0,8, а отношение углерода к сумме оксидов бора и хрома берут равным 0,41-0,55. Если использовать шихту, в которой отношение триоксида дибора к хрому сесквиоксиду будет меньше 0,46, то не будет обеспечено условие получения твердого раствора бор-хром с отношением бора к хрому более 0,15 из-за низкого содержания бора, что приведет к получению второй фазы. Отношение оксида бора к оксиду хрома более 0,8 не обеспечит получение твердого раствора бор-хром с отношением бора к хрому до 0,36, а следовательно, приведет к получению второй фазы в виде металлического бора или сложных соединений бора и хрома, что понизит микротвердость. Если отношение углерода к сумме оксидов хрома и бора будет меньше 0,41, то сплав будет содержать недовосстановленные оксиды, т.е. кислород, что приведет при наплавке к значительному окислению легирующих компонентов и разбрызгиванию сплава. Отношение углерода к сумме оксидов хрома и бора более 0,55 недопустимо из-за высокого избытка углерода в сплаве и приводит к значительному выделению графита при наплавке. По техническим условиям борид хрома должен содержать элементы, химический состав которых представлен в табл.1. В табл. 2 представлен химический состав полупродукта после дробления до фракции минус 0,2 и показатели плавки. Состав полупродукта плавок 2 и 3 соответствует требованиям ТУ по всем элементам, кроме серы для марки БХ-М2 по общему углероду (сумма Ссвяз+Ссвоб>4,4) и серы (более 0,05). В табл.3 представлены продукт плавок 2 и 3 после гравитационно-воздушной очистки фракции минус 0,2. По всем элементам продукт соответствует маркам БХ-М1 и БХ-М2. Таким образом выбранный интервал обеспечивает получение продукта в соответствии с минимальными потерями. Изучение микроструктуры, локальной и рентгеновские анализы показали, что предложенный способ обеспечивает получение однофазного твердого раствора бор-хром. Микротвердость составляет 2400 кг/мм2, модуль упругости не менее 4500 кг/мм2, износостойкость не менее 1500 ч.Формула изобретения
СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА БОРИДА ХРОМА, включающий приготовление шихты путем смешивания порошков оксидов металлов и углеродистого восстановителя с последующим окомкованием ее, порционную загрузку в рудно-термическую печь, выплавку, измельчение полупродукта и отделение свободного углерода и примесей, отличающийся тем, что, с целью повышения качества порошка за счет получения твердого раствора бор-хром с отношением бора к хрому и углерода в сплаве к сумме основных элементов соответственно 0,15-0,35 и 0,005-0,049, повышения износостойкости покрытий, улучшения условий труда при наплавке и выходе годного, выплавку ведут при отношении в шихте триоксида дибора к хрому сесквиоксиду и углерода к сумме оксидов хрома и бора соответственно 0,46-0,8 и 0,41-0,55.РИСУНКИ
Рисунок 1www.findpatent.ru










