Строение атома бария. Хром порядковый номер
Побочная подгруппа VI группы периодической системы (подгруппа хрома)
Общая характеристика неметаллов шестой группы периодической системы. Элементы VI группы периодической системы подразделяют на две подгруппы. Главную подгруппу составляют кислород, сера, селен, теллур и полоний. К побочной подгруппе относят хром, молибден, вольфрам и уран. [c.140]Элементы подгруппы хрома. Хром Сг и его электронные аналоги — молибден Мо и вольфрам — являются элементами побочной подгруппы шестой группы периодической системы элементов Д. И. Менделеева. Электронная -структура их атомов выражается формулой. ..(п — или. .. п — 1)й п8 . у атомов хрома и молибдена про- [c.288]
Элементы побочной подгруппы VI группы периодической системы хром, молибден и вольфрам являются -переходными металлами последний представитель этой подгруппы — уран принадлежит к /-переходным элементам и включается в семейство актинидов. Различие в строении электронных уровней проявляется в заметном отличии свойств урана от свойств остальных элементов подгруппы. Вместе с тем в химическом поведении элементов имеется достаточно много общего для того, чтобы рассматривать химические (и каталитические) свойства урана совместно е остальными элементами подгруппы. [c.569]Молибден и вольфрам относятся к редким элементам VI группы периодической системы. Вместе с хромом они составляют побочную подгруппу, элементы которой характеризуются недостроенными -подуровнями электронных оболочек. Электронные структуры элементов подгруппы хрома представлены в табл. 60. [c.271]
Характеристика подгруппы. Молибден — элемент VI группы периодической системы. Вместе с хромом и вольфрамом он составляет побочную подгруппу —с недостроенным -подуровнем. Их электронные формулы [c.159]
Положение хрома в периодической системе химических элементов и строение атома. Хром возглавляет побочную подгруппу VI группы. Его электронная формула следующая [c.111]
Марганец. Распределение электронов по слоям 2 8 13 2. Марганец находится в побочной подгруппе УП группы периодической системы в середине четвертого (большого) периода между хромом и железом. На внешнем электронном слое его атом имеет [c.253]
В побочную подгруппу шестой группы периодической системы входят хром Сг, молибден Мо и вольфрам У. У атомов хрома и молибдена вследствие особой устойчивости наполовину заполненного -подуровня (й ) валентные электроны (л—1)с1 п5 [c.376]
В побочной подгруппе VI группы периодической системы находятся переходные металлы — хром, молибден и вольфрам. Электронные конфигурации атомов этих элементов представлены в табл. 1. [c.337]
Марганец. Распределение электронов по слоям 2 8 13 2. Марганец находится в побочной подгруппе УП группы периодической системы в середине четвертого (большого) периода между хромом и железом. На внешнем электронном слое его атом имеет два электрона, а предпоследний электронный слой, как и у атомов хрома и железа, неустойчив. Марганец легко отдает два внешних электрона, проявляя металлические свойства. Кроме внешних электронов, марганец способен отдавать до пяти электронов с предпоследнего слоя, проявляя переменную валентность. [c.281]
Железо находится в третьем периоде побочной подгруппы Vni группы периодической системы и, как хром, относится к -элементам. [c.277]
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром он возглавляет побочную подгруппу VI группы. Его название происходит от греческого слова хрома — краска все соединения хрома имеют яркие окраски. При химических реакциях атом хрома может отдавать, кроме электрона внешнего слоя, до [c.148]
Металлы VI группы. В VI группе периодической системы металлы образуют побочную подгруппу, в которую входят хром, молибден, вольфрам и уран (подгруппа хрома). Эти металлы в таблице элементов Менделеева занимают четные ряды больших периодов. [c.366]
Хром, являясь -элементом, находится в побочной подгруппе VI группы периодической системы. Наиболее типичные валентные состояния хрома три (СгЗ+ в кислой среде и хромит-ион СгОГ в щелочной) и шесть (бихромат-ион СгаО в кислой среде и хромат-ион СгС в щелочной среде). [c.205]
Главной и побочной подгрупп шестой группы периодической системы на примере атомов серы и хрома. [c.259]
I. Подгруппа хрома. Хром, молибден и вольфрам составляют побочную подгруппу VI группы периодической системы. Они расположены в серединах больших периодов. [c.207]
Побочную подгруппу VI группы Периодической системы Д. И. Менделеева составляют хром Сг, молибден Мо и вольфрам VJ. [c.268]
Элементы подгруппы хрома по химическим свойствам значительно больще отличаются от элементов подгруппы серы, чем это имеет место в главной и побочной подгруппах V группы периодической системы, и проявляют заметное сходство с соседями по V группе — ванадием, ниобием и танталом. [c.569]
В периодической системе хром находится в побочной подгруппе VI группы. Внешний слой атомов элементов подгруппы хрома заполняют один или два электрона, что определяет их как металлы. Вместе с тем максимальная положительная валентность хрома и его аналогов равна шести, так как кроме наружных электронов, валентными являются еще электроны предпоследнего слоя. [c.168]
Хром. Хром возглавляет побочную подгруппу VI группы периодической системы, в которую входят хром, молибден, вольфрам и уран. Эти элементы близки по свойствам, но наибольшее практическое значение среди них имеет хром. [c.278]
Хром, молибден и вольфрам составляют побочную подгруппу шестой группы периодической системы. По многим своим свойствам эти элементы сильно отличаются от элементов главной подгруппы — серы, селена и теллура, однако в некоторых свойствах между ними проявляется сходство. [c.223]
Хром является представителем побочной подгруппы VI группы периодической системы, т. е. (-элементом. Главная подгруппа VI группы состоит из элементов, являющихся типичными неметаллами. В побочной подгруппе находятся элементы четных рядов, т. е. первых половин больщих периодов, для атомов которых характерны недостроенные предпоследние электронные энергетические уровни у хрома 2,8, 13,1, т. е. (га—1) 5 , а у молибдена и вольфрама Поэтому у всех -элементов IV периода на внещнем [c.453]
ПОБОЧНАЯ ПОДГРУППА VI ГРУППЫ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ (ПОДГРУППА ХРОМА) [c.215]
В побочной подгруппе VI группы периодической системы химических элементов (подгруппе хрома) находятся переходные металлы хром (Сг), молибден (Мо) и вольфрам (W). [c.215]
Хром. Хром возглавляет побочную подгруппу VI группы периодической системы, в которую входят хром, молибден, вольфрам и уран. Эти элементы близки по свойствам, но наибольшее практическое значение среди них имеет хром. В атоме хрома распределение электронов по слоям следующее 2 8 13 1 (см. 38). [c.251]
Большинство элементов главных подгрупп IV — УП групп периодической системы представляют собой неметаллы, в то время как элементы побочных подгрупп — металлы. Поэтому в правой части периодической системы различия в свойствах элементов главных и побочных подгрупп проявляются особенно резко. Однако в тех случаях, когда элементы главной и побочной подгруппы находятся в высшей степени окисления, их аналогичные соединения проявляют существенное сходство. Так, хром, расположенный в побочной подгруппе VI группы, образует кислотный оксид СгОз, близкий по свойствам к триоксиду серы ЗОз-Оба эти вещества в обычных условиях находятся в твердом состоянии и образуют при взаимодействии с водой кислоты состава Н2ЭО4. Точно так же оксиды марганца и хлора, соответствующие высшей степени окисления этих элементов, [c.496]
Форма Периодической системы, которую предложил Д. И. Менделеев, называется короткопериодной, или классической. В настоящее время все П1ире используется другая форма Периодической системы - длиннопериодная, в которой все периоды-малые и большие-вытянуты в длинные ряды, начинающиеся щелочным металлом и заканчивающиеся благородным газом. Каждая вертикальная последовательность элементов называется группой, которая нумеруется римской цифрой от I до VIII и русскими буквами А или Б. Например, I А-группа - это щелочные металлы (т.е. главная подгруппа I группы в короткопериодной форме), а 1Б-группа - это )лементЫ медь, серебро и золото (т.е. побочная подгруппа I группы) аналогично VI А-группа - это халькогены, а VIB-группа-Э1 0 элементы хром, молибден и вольфрам. Таким образом, главные подгруппы - это А-группы в длиннопериодной форме, а побочные подгруппы -это Б-группы номера групп в обеих формах Периодической системы совпадают. [c.35]
Шестая группа периодической системы Д. П. Мепделоева сосюит из подгруппы кислорода (главная подгруппа) и подгруппы хрома (побочная подгруппа). [c.201]
К существенным противоречиям короткой формы периодической системы относили, пребывание элементов побочных подгрупп — марганца, технеция, рения в одной группе с галогенами хрома, молибдена, вольфрама в группе с халькогенами ванадия, ниобия, тантала в группе с пниктогенами меди, серебра, золота — со щелочными металлами цинка, кадмия, ртути — со щелочноземельными металлами и т. д., — а также и осложнения, вносимые элементами побочных подгрупп в порядок изменения свойств элементов в вертикальных группах. Однако на самом деле эта особенность короткопериодной формы может рассматриваться для элементов, начиная со второй и и кончая седьмой группой, скорее как преимущество по сравнению с другими формами — в одной группе находятся вместе как полные, [c.26]
Хром относится к переходным d-элементам и находится в побочной подгруппе VI группы периодической системы элемеп-тов Д. И. Менделеева. В соответствии с электронной конфигурацией валентных подуровней (3dHs ) хром может проявлять степень окисления от I до VI. Наиболее устойчивы соединения дрома(1П) и хрома (VI). При обычных температурах могут ыть получены и соединения хрома (И). [c.257]
Элементы подгруппы хрома. Хром Сг и его электронные аналоги-молибден Мо и вольфрам Ш — являются элементами побочной подгруппы шестой группы периодической системы элементов Д. И. Менделеева. Электронная структура их атомов выражается формулой. ..(п—1)с1 п8 или. .. п — 1)с1 пз. У атомов хрома и молибдена происходит провал одного л -электрона с внешнего слоя на предвнешний. Однако соединения, в которых Сг и Мо были бы одновалентны, неизвестны. Минимальная валентность хрома, молибдена и вольфрама отвечает возбуждению внешних б -электронов и равна двум. [c.320]
Отмечается, что в подтеме Хром учащиеся впервые встретятся с изучением элементов побочной подгруппы одной из групп периодической системы Д. И. ЛАенделеева, а такое положение в системе позволяет ожидать у этих элементов особые свойства, отличающие их от элементов-металлов главных подгрупп. Какие это свойства, будет выяснено на следующих уроках. [c.145]
Соли окислов шестивалентных металлов побочной подгруппы VI группы периодической системы существуют в виде нормальных солей общей формулы МеЭ0.4 и в виде полисоединений типа Мег Э04 ЭОз. Образование полисоединений особенно характерно для окислов молибдена и вольфрама, окислы хрома и урана образуют полисоединения в гораздо [c.574]
Хром — химический элемент побочной подгруппы VI группы периодической системы элементов Д. И. Менделеева. Химический знакСг, порядковый номер 24, металл, электронная формула 8 28 2р 38 3р 3(145 . [c.285]
Различие в энергии связи электронов одноименных подгрупп двух оболочек больше различия в энергии связи электронов двух соседних подгрупп одной оболочки. Однако энергия связи электронов первых подгрупп данной оболочки может быть больше, чем знергия связи электронов последней подгруппы предыдушей оболочки. Например, первая электронная пара четвертой оболочки (4з-электроны) обладает несколько большей энергией связи, чем электроны последней подг11Уппы третьей оболочки (Зс1-электроны). Поэтому 19-й электрон атома калия и 20-й электрон атома кальция не начинают постройки 3(1-подгруппы, а занимают 4з-положение, что соответствует большей энергии связи их в атоме. Этим нарушается последовательность в образовании электронами оболочек атома. Когда наиболее выгодная в энергетическом отношении з-подгруппа четвертой оболочки достроена, следующие электроны в атомах скандия, титана, ванадия, хрома,. марганца, железа, кобальта, никеля и меди окончательно достраивают третью оболочку. То же самое повторяется и при заполнении следующих оболочек. Этим объясняется образование побочных групп в периодической системе элементов. [c.492]
Подгруппа титана — Знаешь как
| Элемент | Символ | Атомный вес | Порядковый номер | Распределение электронов по словм | |||||
| Титан | Ti | 47,90 | 22 | 2 | 8 | 10 | 2 | ||
| Цирконий | Zr | 91,22 | 40 | 2 | 8 | 18 | 10 | 2 | |
| Гафний | Hf | 178,50 | 72 | 2 | 8 | 18 | 32 | 10 | 2 |
Общая характеристика подгруппы титана. В состав подгруппы титана входят элементы четвертой группы периодической системы — титан, цирконий и гафний, стоящие в четных рядах больших периодов. К этой же подгруппе раньше относили элемент торий, который в настоящее время причисляется к актинидам . Так как по химическим свойствам торий сходен с элементами подгруппы титана, то мы описываем его вместе с этими элементами.
В отличие от элементов нечетной подгруппы, атомы элементов подгруппы титана имеют в наружном слое только два электрона и не способны присоединять электроны. Поэтому соединения, в которых они были бы отрицательно валентны, не известны. В то же время максимальная положительная валентность этих элементов равна четырем, так как, кроме двух внешних электронов, они могут отдавать еще два электрона из недостроенного предыдущего слоя, содержащего десять электронов.
В связи с наличием только двух электронов в наружном слое атома металлические свойства элементов подгруппы титана выражены гораздо сильнее, чем те же свойства элементов подгруппы германия, и увеличиваются с возрастанием порядкового номера. Так, например, гидроокись титана Ti(OH)4 амфотерна, у гидроокисей циркония и гафния преобладают основные свойства, а гидроокись тория имеет только основной характер.
В свободном состоянии все четыре элемента представляют собой типичные металлы, похожие на сталь. Все они обладают довольно высокими температурами плавления. Элементы подгруппы титана устойчивы по отношению к воде и воздуху и трудно поддаются действию кислот.
Кроме титана, который довольно легко восстанавливается до низших степеней валентности, остальные элементы описываемой подгруппы в своих соединениях почти всегда четырехвалентны.
236 237 238
Вы читаете, статья на тему Подгруппа титана
znaesh-kak.com
Подгруппа меди — Знаешь как
| Элемент | Символ | Атомный вес | Порядковый номер | Распределение электронов по слоям | |||||
| Медь | Сu | 63,54 | 29 | 2 | 8 | 18 | 1 | ||
| Серебро | Ag | 107,880 | 47 | 2 | 8 | 18 | 18 | 1 | |
| Золото | Au | 197,0 | 79 | 2 | 8 | 18 | 32 | 18 | 1 |
Общая характеристика подгруппы меди. К подгруппе меди относятся три элемента — медь, серебро и золото, с которых начинаются нечетные ряды больших периодов в таблице Менделеева. Подобно щелочным металлам, все три элемента имеют в наружном слое атома по одному электрону, предпоследний же их электронный слой построен по-иному: в атомах щелочных металлов (кроме лития) он состоит из восьми электронов, а в атомах элементов подгруппы меди из 18.
Различие в строении предпоследнего слоя вызывает и довольно резкое различие в свойствах элементов обеих подгрупп зависящее, повидимому, от относительных размеров их атомов В табл. 29 сопоставлены радиусы атомов и ионизационные потенциалы элементов подгруппы меди и щелочных металлов, находящихся в тех же периодах.
Таблица 29
Радиусы атомов и ионизационные потенциалы элементов подгруппы меди и щелочных металлов
| Элемент | Радиус атома в Å | Ионизационный потенциал в в | Элемент | Радиус атома о в А | Ионизационный потенциал в в |
| Медь | 1,27 | 7,72 | Калий | 2,36 | 4,32 |
| Серебро | 1,44 | 7,51 | Рубидий | 2,53 | 4,10 |
| Золото | 1,44 | 9,22 | Цезий | 2,74 | 3,87 |
Данные, приведенные в этой таблице, показывают, что в атомах меди, серебра и золота наружный электрон находится гораздо ближе к ядру, а следовательно, должен сильнее притягиваться к нему, чем в атомах соответствующих щелочных металлов. В связи с этим и ионизационные потенциалы, т. е. энергия, которую надо затратить, чтобы оторвать электрон от атома, у элементов подгруппы меди гораздо больше, чем у щелочных металлов. Действительно, щелочные металлы очень легко отдают внешний электрон, элементы же подгруппы меди удерживают его довольно прочно. Поэтому они гораздо труднее окисляются и, наоборот, их ионы легко восстанавливаются; они не разлагают воду, гидроокиси их являются сравнительно слабыми основаниями и т. д. В то же время 18-электронный слой, устойчивый у других элементов, здесь еще не вполне стабилизировался и способен к частичной потере электронов. Так, медь наряду с одновалентными катионами образует и двухвалентные, которые даже более характерны для нее. Точно так же для золота более характерны соединения, в которых оно трехвалентно. Серебро в своих обычных соединениях одновалентно, но иногда бывает двух- и трехвалентным.
209 210 211
Вы читаете, статья на тему
znaesh-kak.com
Строение атома бария (Ba), схема и примеры
Общие сведения о строении атома бария
Относится к семейству s-элементов. Металл. Обозначение – Ba. Порядковый номер – 56. Относительная атомная масса – 137,34 а.е.м.
Электронное строение атома бария
Атом бария состоит из положительно заряженного ядра (+56), внутри которого есть 56 протонов и 81 нейтрон, а вокруг, по шести орбитам движутся 56 электронов.
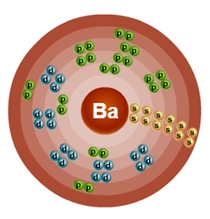
Рис.1. Схематическое строение атома бария.
Распределение электронов по орбиталям выглядит следующим образом:
+56Ba)2)8)18)18)8)2;
1s22s22p63s23p63d104s24p64d105s25p66s2.
Внешний энергетический уровень атома бария содержит 2 электрона, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:

Для атома бария характерно наличие возбужденного состояния. Электроны 6s-подуровня распариваются и один из них занимает вакантную орбиталь 6p-подуровня:
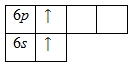
Наличие двух неспаренных электронов свидетельствует о том, что для бария характерна степень окисления +2.
Валентные электроны атома бария можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
6 |
0 |
0 |
+1/2 |
|
s |
6 |
0 |
0 |
-1/2 |
Примеры решения задач

| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
100 советов о том, как пользоваться Chromebook
Хотите узнать как пользоваться Chromebook? Очень легко! Но чтобы стать продвинутым пользователем, вам необходимо знать много хитростей, приемов и секретов. Ниже мы собрали для вас сто подсказок, прочитав которые, пользоваться Chrome OS будет комфортнее.
1. Наш первый совет по Chrome OS – прочтите 100 советов по работе в Google Chrome. Удивлены? Так как основой Chrome OS является браузер Google Chrome и работа в нем, большинство советов, что мы написали для него, являются актуальными и для работы непосредственно в Chrome OS.
2. Обязательно добавьте Dropbox в ваши закладки. Второй сервис облачного хранения данных не только увеличит вашу память, но и позволит дополнительно обезопасить файлы от потери.

3. Пособие по оффлайн-работе с вашим Chromebook.
4. Ищете капс-лок? Нажмите Alt + Search
5. Вы можете настроить клавишу поиска и для других функций. Перейдите в общие настройки и найдите настройки клавиатуры. Там вы можете назначить клавишу как дублирующую Alt, Ctrl, Caps Lock или вовсе отключить ее.
6. Чтобы воспроизвести функцию кнопки Home, используйте комбинацию клавиш Ctrl + Alt + Стрелка Вверх.Клавиша End: Ctrl + Alt + Стрелка Вниз.Delete: Alt + Backspace.Вы можете использовать эти сочетания клавиш также при удалении файлов из файлового менеджера или Google Drive.
7. Чтобы быстро заблокировать экран вашего Chromebook, нажмите Ctrl+Shift+L.
8. Приложения, закрепленные на панели быстрого запуска (строка в нижней части экрана), могут быть открыты с помощью сочетания клавиш Alt + Порядковый номер приложения. Первое приложение слева — после Chrome — означает 1, следующее — 2, и так далее до 8.
9. Чтобы узнать версию BIOS, установленную на вашем Chromebook, введите в терминале crosh/shell в режиме разработчика следующую команду: /usr/sbin/chromeos-firmwareupdate -V | grep “BIOS version”
Или в браузере Chrome введите chrome://chrome/help.
10. Как печатать с помощью Chromebook.
11. Как импортировать свою музыку из iTunes в Google Music.
12. Чтобы сбросить все настройки вашего Chromebook до заводских, откройте окно логина, нажмите комбинацию клавиш Ctrl + Alt + R и подтвердите действие. Очень полезная функция, если вы собираетесь продать или подарить ваш ноутбук, или просто хотите его хорошенько почистить.
13. Чтобы провести диагностику работы Wi-Fi или 3G, введите в строке поиска chrome://diagnostics. После того, как вы выберите, что именно необходимо проверить, Chrome начнет диагностику.
14. Ваш Chromebook полноценно работает с торрентами! Используйте программы JSTorrent или uTorrent для наибольшего удобства.
15. Google Music, как и большинство других плееров, использует Adobe Flash, который печально известен своей прожорливостью в плане заряда аккумулятора и требованиями к производительности железа. Вы можете переключить Google Music на HTML5, чтобы избавиться от недостатков Flash и получить максимальное удовольствие от сервиса:
- Откройте Google Music
- Нажмите на иконку настроек в верхней правой части
- Выберите Music Labs (Музыкальная лаборатория)
- Найдите в списке пункт HTML5 Audio
- Нажмите «Включено»
- Сохраните изменения
16. Нажмите комбинацию клавиш Ctrl+Alt+Shift+Reload, чтобы ваш Chromebook сделал бочку 🙂
17. Чтобы найти сотни приложений, работающих без подключения к сети, зайдите в соответствующий раздел в Интернет-магазине Chrome.
18.Чтобы сделать скриншот всего экрана, одновременно нажмите Ctrl и Клавишу показа всех окон:

Нужно сделать скриншот лишь части экрана? Следующая комбинация клавиш позволит вам выбрать раздел экрана для снимка:

19. Если ваш Chromebook обладает тачскрином, Зайдите в «Настройки – Дополнительные инструменты – Сделать скриншот», чтобы сделать снимок экрана.
20. Обновите кэш Google Drive, нажав Ctrl + Refresh.
21. Изменение версии программного обеспечения – отличный способ получить новые функции для вашего Chromebook. Пройдите по адресу chrome://help и нажмите «Дополнительная информация».
22. Чтобы вставить в текст необычные символы из коллекции Unicode, используйте комбинацию клавиш Ctrl + Shift + U + номер символа юникода.
23. Чтобы очистить кэш и перезагрузить Google Drive, зажмите Ctrl и нажмите на значок настройки в программе. Вы увидите дополнительные опции, появившиеся в меню настроек. Если это не сработает (зависит от версии Chrome OS), пройдите по ссылке chrome://drive-internals/ и выберите «Очистить локальные данные».
24. Чтобы открыть окно командной строки, нажмите Ctrl + Alt + T. Чтобы открыть оболочку, введите команду shell.

25. Зажмите Ctrl и нажмите на значок «Домой», чтобы открыть домашнюю страницу в новой вкладке.
26. Если ваш Chromebook построен на архитектуре ARM, зажмите Esc + Refresh, а затем нажмите на кнопку включения, чтобы войти в режим разработчика.
27. Для просмотра сведений об оборудовании вашего Chromebook, во время включения нажмите Ctrl + i или Tab + i.

28. Чтобы узнать версию ОС с помощью командной строки, в режиме разработчика введите /opt/google/chrome/chrome –version
29. Для просмотра свободного места на локальном диске вашего Chromebook (HDD или SSD), введите в браузере chrome://quota-internals/. Также вы можете просто нажать на значок настроек в файловом менеджере.
30. Добавьте специальные возможности браузеру Chrome.
31. В настройках специальных возможностей включите функцию перетаскивания после нажатия.
32. Нажмите Shift + Alt + M, чтобы открыть файловый менеджер.

33. При просмотре фотографий через файловый менеджер Chrome OS нажмите E, чтобы быстро отредактировать изображение, используя встроенный редактор.
34. Установите Pixlr Editor на ваш Chromebook, если ищете альтернативу фотошопу на Chrome OS.
35. Вы можете создать флешку для восстановления системы Chrome OS. Вам понадобится USB-накопитель или SD-карта размером не менее 4Gb. Очистите накопитель, пройдите по адресу chrome://imageburner и следуйте инструкциям на экране.
36. Для просмотра общего количества оперативной памяти, откройте chrome://system, найдите meminfo и нажмите «Развернуть»
37. Чтобы узнать MAC-адрес вашего устройства, зайдите в «Настройки – Интернет-соединение – Подключение к интернету». Теперь нажмите на соединение, к которому вы в данный момент подключены. Во всплывающем окне будут указаны различные данные, среди которых и ваш MAC-адрес.
38. Чтобы узнать пропускную способность сети, к которой вы подключены, введите в адресной строке chrome://net-internals/#bandwidth.
39. Зажмите Shift и нажмите на любое приложение, чтобы открыть его в новом окне. Так оно будет больше похоже на отдельное приложение, а не сайт. Нажмите правой кнопкой мыши по любому приложению, чтобы выбрать, в каком виде оно будет открываться по умолчанию: полный экран, новая вкладка, новое окно и т.д.
40. Чтобы изменить MAC-адрес вашего Chromebook, откройте командную строку Shell в режиме разработчика и последовательно введите:
sudo ifconfig eth0 down, чтобы отключить интернет-соединение
sudo ifconfig eth0 hw ether 00:11:22:33:44:55, чтобы изменить ваш MAC-адрес
sudo ifconfig eth0 up, чтобы восстановить ваше интернет-соединение.
Если вы подключены к интернету через Wi-Fi, замените eth0 на wlan0.Будьте осторожны, при перезагрузке Chromebook стандартный MAC-адрес будет восстановлен.
41. Чтобы изменить положение панели запуска, щелкните по ней правой кнопкой мыши и выберите другой вид.
42. Используйте комбинацию Ctrl + S, чтобы сохранить страницу для оффлайн-чтения.

43. Закачайте вашу любимую музыку в Google Drive, а затем – в Google Play Music, используя Music Manager.
44. Для того, чтобы создать локального пользователя без необходимости регистрации Google аккаунта, при предложении входа в Chrome нажмите «Нет, спасибо». Вы войдете под именем «Пользователь 1» и сможете полноценно настроить свой локальный аккаунт.
45. Чтобы быстро получить доступ к изменению картинки профиля Google, нажмите на нее в нижнем правом углу рабочего стола Chrome OS.
46. Нажмите правой кнопкой мыши на «Сохраненные файлы» в файловом менеджере, чтобы узнать количество свободного места на вашем диске.
47. Найдите в настройках функцию «Использовать режим высокой контрастности» и включите ее, чтобы пользоваться Chrome OS в этом режиме.
48. Если вы попробуете открыть файл в формате .swf (Flash) в файловом менеджере, у вас ничего не получится. Перетащите файл в браузер Chrome, и все заработает.
49. Комбинация клавиш Alt + Shift + N открывает центр уведомлений.
50. Как сбросить настройки вашего Chromebook.
51. Используем файловый менеджер в Chrome OS.
52. Для повышения уровня безопасности выполняйте резервное копирование, запретите отслеживание исходящего трафика в настройках Chrome, установите ввод пароля после выхода из спящего режима, а также проверьте разрешения, которые доступны установленным расширениям. Кроме того, ни в коем случае не устанавливайте расширения, скачанные не из Интернет-магазина Chrome.
53. Скачайте официальное приложение для удобной работы с файлами Microsoft Office.
54.Комбинация клавиш Alt + Tab отображает все открытые окна.
55. Чтобы создать новую папку в менеджере файлов, нажмите Ctrl + E.

56. Установите Google Hangouts, чтобы не отвлекаться на телефон для переписки с друзьями и родственниками.
57. Во время перетаскивания файлов, задержите указатель мыши над папкой, чтобы открыть ее. Чтобы открыть папку немедленно, нажмите кл
cloudspace.news
Элементы подгруппы хрома VI группы периодической системы
Элементы подгруппы хрома. Хром Сг и его электронные аналоги — молибден Мо и вольфрам — являются элементами побочной подгруппы шестой группы периодической системы элементов Д. И. Менделеева. Электронная -структура их атомов выражается формулой. ..(п — или. .. п — 1)й п8 . у атомов хрома и молибдена про- [c.288]Элементы побочной подгруппы VI группы периодической системы хром, молибден и вольфрам являются -переходными металлами последний представитель этой подгруппы — уран принадлежит к /-переходным элементам и включается в семейство актинидов. Различие в строении электронных уровней проявляется в заметном отличии свойств урана от свойств остальных элементов подгруппы. Вместе с тем в химическом поведении элементов имеется достаточно много общего для того, чтобы рассматривать химические (и каталитические) свойства урана совместно е остальными элементами подгруппы. [c.569]
Хром — химический элемент побочной подгруппы VI группы периодической системы Д. И. Менделеева. Химический знак — Сг (хром), порядковый (aтo ный) номер — 24, электронная конфигурация атома ls 2з 2p 3s 3p 3d 4s электронно-графическая формула [c.316]Таким образом, можно ввести представление о полной и неполной электронной аналогии. Полными электронными аналогами называются элементы, которые имеют сходное электронное строение во всех степенях окисления, чем и объясняется близкое подобие их химических свойств. Например, в рассматриваемой VI группе Периодической системы полными электронными аналогами являются кислород и сера [О] — [ У28 2р [8] — [Ке] 03823р , селен, теллур и полоний [8е]34 [Аг]183 104524р4 [Те]52 - [Щ Чё Ъз Ър -, [Ро] - [Хе] Ч Ъ %8Чр, а также хром, молибден и вольфрам [Сг] — [Аг]> 3 [ У] — [Хе]5 4/ 5(/ бв2 У полония и вольфрама в отличие от остальных элементов присутствует внутренняя завершенная 4/оболочка, наличие которой проявляется в лантаноидном сжатии. Поскольку 4/юболочка располагается глубоко, она мало влияет на свойства и не нарушает з арактер электронной аналогии. Атомы типических элементов — кислорода и серы — по электронному строению отличаются как от атомов элементов подгруппы селена (в высшей степени окисления), так и от атомов элементов подгруппы хрома (во всех степенях окисления, кроме высшей). Это значит, что кислород и сера по отношению к остальным элементам [c.229]
Положение хрома в периодической системе химических элементов и строение атома. Хром возглавляет побочную подгруппу VI группы. Его электронная формула следующая [c.111]
Характеристика подгруппы. Молибден — элемент VI группы периодической системы. Вместе с хромом и вольфрамом он составляет побочную подгруппу —с недостроенным -подуровнем. Их электронные формулы [c.159]
В побочной подгруппе VI группы периодической системы находятся переходные металлы — хром, молибден и вольфрам. Электронные конфигурации атомов этих элементов представлены в табл. 1. [c.337]
Железо находится в третьем периоде побочной подгруппы Vni группы периодической системы и, как хром, относится к -элементам. [c.277]
В побочную подгруппу шестой группы периодической системы Д. И. Менделеева входят металлы хром, молибден, вольфрам и уран. Атомы всех этих ( -элементов имеют по шесть валентных электронов один располагается на орбитали наружного энергетического уровня s (за исключением атома вольфрама s ), остальные 5 электронов — на предпоследнем энергетическом уровне d . [c.240]
Хром, являясь -элементом, находится в побочной подгруппе VI группы периодической системы. Наиболее типичные валентные состояния хрома три (СгЗ+ в кислой среде и хромит-ион СгОГ в щелочной) и шесть (бихромат-ион СгаО в кислой среде и хромат-ион СгС в щелочной среде). [c.205]
Обосновать размещение хрома, молибдена и вольфрама в VI группе периодической системы. В чем проявляется сходство этих элементов с элементами главной подгруппы [c.248]
Цирконий находится в подгруппе титана IV группы периодической системы элементов Д. И. Менделеева, Содержание циркония в земной коре выше, чем таких металлов, как хром, ванадий, цинк, никель и медь. [c.22]
Элементы подгруппы хрома по химическим свойствам значительно больще отличаются от элементов подгруппы серы, чем это имеет место в главной и побочной подгруппах V группы периодической системы, и проявляют заметное сходство с соседями по V группе — ванадием, ниобием и танталом. [c.569]
Хром. Хром возглавляет побочную подгруппу VI группы периодической системы, в которую входят хром, молибден, вольфрам и уран. Эти элементы близки по свойствам, но наибольшее практическое значение среди них имеет хром. [c.278]
Хром, молибден и вольфрам составляют побочную подгруппу шестой группы периодической системы. По многим своим свойствам эти элементы сильно отличаются от элементов главной подгруппы — серы, селена и теллура, однако в некоторых свойствах между ними проявляется сходство. [c.223]
Хром является представителем побочной подгруппы VI группы периодической системы, т. е. (-элементом. Главная подгруппа VI группы состоит из элементов, являющихся типичными неметаллами. В побочной подгруппе находятся элементы четных рядов, т. е. первых половин больщих периодов, для атомов которых характерны недостроенные предпоследние электронные энергетические уровни у хрома 2,8, 13,1, т. е. (га—1) 5 , а у молибдена и вольфрама Поэтому у всех -элементов IV периода на внещнем [c.453]
В побочной подгруппе VI группы периодической системы химических элементов (подгруппе хрома) находятся переходные металлы хром (Сг), молибден (Мо) и вольфрам (W). [c.215]
Хром. Хром возглавляет побочную подгруппу VI группы периодической системы, в которую входят хром, молибден, вольфрам и уран. Эти элементы близки по свойствам, но наибольшее практическое значение среди них имеет хром. В атоме хрома распределение электронов по слоям следующее 2 8 13 1 (см. 38). [c.251]
К элементам VIB-группы периодической системы относятся хром, молибден и вольфрам. Они располагаются вблизи середины ii-рядов. В силу стабильности конфигурации у атомов первых двух элементов подгруппы — хрома и молибдена — наблюдается проскок одного электрона с оболочки ns на оболочку (п— )d. У вольфрама валентной электронной конфигурации предшествует завершенная 4/ -оболочка. Поэтому на его свойствах сказывается влияние лантаноидной контракции, хотя в меньшей мере, чем у элементов подгруппы титана и ванадия. Ниже сопоставлены некоторые характеристики элементов и простых веществ VIB-группы. [c.334]
В периодической системе хром находится в побочной подгруппе VI группы. Внешний слой атомов элементов подгруппы хрома заполняют один или два электрона, что определяет их как металлы. Вместе с тем максимальная положительная валентность хрома и его аналогов равна шести, так как кроме наружных электронов, валентными являются еще электроны предпоследнего слоя. [c.168]
Металлы VI группы. В VI группе периодической системы металлы образуют побочную подгруппу, в которую входят хром, молибден, вольфрам и уран (подгруппа хрома). Эти металлы в таблице элементов Менделеева занимают четные ряды больших периодов. [c.366]
Молибден находится в подгруппе хрома VI группы периодической системы элементов Д. И. Менделеева. Запасы этого элемента в земной коре составляют 0,001%. Молибден имеет большое сходство по некоторым свойствам с вольфрамом, с которым совместно встречается в рудах. Оба эти элемента относятся к широко применяемым в технике тугоплавким металлам и являются основой современных наиболее тугоплавких сплавов. [c.91]
Хром находится в VI группе периодической системы. В отличие от элементов подгруппы кислорода он является металлом, что обусловлено строением его атома. Последний во внешнем слое содержит один электрон и поэтому не присоединяет электронов, отдавать же он может их максимально шесть (один внешний и пять с соседнего недостроенного слоя с 13 электронами). Таким образом, в своих соединениях хром проявляет только положительную валентность, изменяющуюся от 2 до 6. Наибольшее значение имеют производные трехвалентного и шестивалентного хрома, [c.276]
Хром относится к переходным d-элементам и находится в побочной подгруппе VI группы периодической системы элемеп-тов Д. И. Менделеева. В соответствии с электронной конфигурацией валентных подуровней (3dHs ) хром может проявлять степень окисления от I до VI. Наиболее устойчивы соединения дрома(1П) и хрома (VI). При обычных температурах могут ыть получены и соединения хрома (И). [c.257]
Элементы подгруппы хрома. Хром Сг и его электронные аналоги-молибден Мо и вольфрам Ш — являются элементами побочной подгруппы шестой группы периодической системы элементов Д. И. Менделеева. Электронная структура их атомов выражается формулой. ..(п—1)с1 п8 или. .. п — 1)с1 пз. У атомов хрома и молибдена происходит провал одного л -электрона с внешнего слоя на предвнешний. Однако соединения, в которых Сг и Мо были бы одновалентны, неизвестны. Минимальная валентность хрома, молибдена и вольфрама отвечает возбуждению внешних б -электронов и равна двум. [c.320]
Хром — химический элемент побочной подгруппы VI группы периодической системы элементов Д. И. Менделеева. Химический знакСг, порядковый номер 24, металл, электронная формула 8 28 2р 38 3р 3(145 . [c.285]
Хром является представителем побочной подгруппы шестой группы периодической системы. Главная подгруппа шестой группы, как мы уже знаем, состоит из элементов, являющихся типичными металлоидами. В побочной подгруппе находятся элементы четных рядов, т. е. первых половин больших периодов, атомы которых характеризуются недостроенными предпоследними энергетическими уровнями. Поэтому у всех элементов побочной подгруппы, на внешнем электронном слое аюмов находится не более двух электронов-что и обусловливает их металлические свойства. Эти элементы не дают отрицательных ионов, поскольку они но могут присоединять электронов, подобно элементам главной подгруппы. В этом их коренное отличие. Отдавать электроны атомы элементов побочной группы могут не только с внешнего слоя, но и с предпоследнего недостроенного слоя, который содержит 12 электронов (у хрома 13). Таким образом, при химическом взаимодействии у атомов этих элементов принимают участие 2 электронных слоя внешний и предпоследний. Общее количество электронов, которые они могут отдать, равно шести. В этом проявляется их сходство с элементами главной подгруппы. К побочной подгруппе элементов шестой группы относятся металлы хром, молибден, вольфрам и уран. Все они имеют очень важпое значение уран как радиоактивный элемент, остальные как металлы, применяющиеся в технике для получения различных сплавов. Среди них наиболее важным является хром. [c.263]
Большинство элементов главных подгрупп IV — УП групп периодической системы представляют собой неметаллы, в то время как элементы побочных подгрупп — металлы. Поэтому в правой части периодической системы различия в свойствах элементов главных и побочных подгрупп проявляются особенно резко. Однако в тех случаях, когда элементы главной и побочной подгруппы находятся в высшей степени окисления, их аналогичные соединения проявляют существенное сходство. Так, хром, расположенный в побочной подгруппе VI группы, образует кислотный оксид СгОз, близкий по свойствам к триоксиду серы ЗОз-Оба эти вещества в обычных условиях находятся в твердом состоянии и образуют при взаимодействии с водой кислоты состава Н2ЭО4. Точно так же оксиды марганца и хлора, соответствующие высшей степени окисления этих элементов, [c.496]
Из таблицы видно, что аналитические группы ионов занимают определенные участки в периодической системе элементов. Наибольшее совпадение между группами периодической системы и аналитическими группами отмечается у I и II аналитических групп первая аналитическая группа (без Mg +) соответствует группе IA щелочных металлов, а вторая — подгруппе щелочно-земельных металлов, входящих в группу ИА. Наиболее многочисленная III аналитическая группа включает в себя катионы элементов групп IIIА и IIIB, а также лантаноидов, актиноидов и ряда других переходных металлов, например хрома, марганца, железа, кобальта, никеля, цинка. При этом часть ионов III аналитической группы — Zn +, [c.230]
Отмечается, что в подтеме Хром учащиеся впервые встретятся с изучением элементов побочной подгруппы одной из групп периодической системы Д. И. ЛАенделеева, а такое положение в системе позволяет ожидать у этих элементов особые свойства, отличающие их от элементов-металлов главных подгрупп. Какие это свойства, будет выяснено на следующих уроках. [c.145]
Молибден и вольфрам относятся к шестой группе периодической системы и входят в подгруппу хрома. Атомньш вес молибдена 95,95, заряд ядра 42. Атомный вес вольфрама 183,82, заряд ядра 74 находясь в пятом периоде, т. е. во втором большом периоде, молибден и вольфрам имеют следующее расположение электронов 2, 8, 18 13, 1 и 2, 8, 18, 32,12, 2 соответственно. Вследствие такого расположения электронов молибден и вольфрам обладают переменной валентностью, причем наиболее устойчивой оказывается валентность 4 и 6 при валентности 6 атомы обоих элементов освобождаются от одного электрона с наружной оболочки и пяти электронов со второй, приобретая вследствие этого структуру атома инертного газа криптона. Благодаря высокой валентности молибден и вольфрам входят в большинство соединений в виде кислородсодержащего аниона ШоОГ и [c.48]
chem21.info









