Константы диссоциации Кb и константы основности pКb=-lg(Кb) неорганических оснований в водных растворах. Диссоциация гидроксида хрома
Готовимся к углубленному изучению химии : 6.3 Амфотерные гидроксиды
6.3. Амфотерные гидроксиды, их свойства Амфотерные гидроксиды – электролиты, образующие при диссоциации одновременно катионы Н+и анионы ОН–: X+ + OH– ⇌ ХOH = HXO ⇌ H++ XO–. Амфотерные гидроксиды в кислой среде ведут себя как основания, а в щелочной – как кислоты. K амфотерным гидроксидам относятся Be(OH)2, Zn(OH)2, Pb(OH)2, Sn(OH)2, Al(OH)3, Fe(OH)3,Cr(OH)3 и некоторые другие, им соответствуют амфотерные оксиды. Практически все они нерастворимы в воде, являются слабыми электролитами и диссоциируют ступенчато. Химические свойства амфотерных гидроксидов
Химические свойства амфотерных гидроксидов 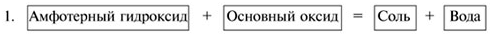
 Некоторые амфотерные гидроксиды (Be(OH)2, Zn(OH)2, Pb(OH)2) реагируют с кислотным оксидом СО2 с образованием осадков основных солей и воды. Например: 2Be(OH)2 + CO2 = (BeOH)2CO3 + h3O.
Некоторые амфотерные гидроксиды (Be(OH)2, Zn(OH)2, Pb(OH)2) реагируют с кислотным оксидом СО2 с образованием осадков основных солей и воды. Например: 2Be(OH)2 + CO2 = (BeOH)2CO3 + h3O. 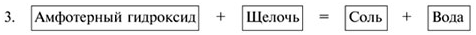 Zn(OH)2 + 2KOH (тв.) K2ZnO2 + 2h3O↑, Zn(OH)2 + 2KOH = K2[Zn(OH)4].
Zn(OH)2 + 2KOH (тв.) K2ZnO2 + 2h3O↑, Zn(OH)2 + 2KOH = K2[Zn(OH)4]. 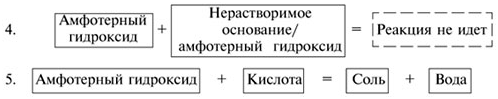
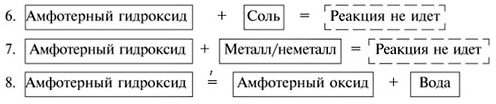 Все амфотерные гидроксиды (как и большинство оснований) разлагаются при нагревании на оксид и воду. Например: 2Al(OH)3 Al2O3 + 3h3O. В связи с этим нужно учитывать, что фактически в процессе сплавления их со щелочами и оксидами участвует не сам амфотерный гидроксид, а соответствующий ему оксид.
Все амфотерные гидроксиды (как и большинство оснований) разлагаются при нагревании на оксид и воду. Например: 2Al(OH)3 Al2O3 + 3h3O. В связи с этим нужно учитывать, что фактически в процессе сплавления их со щелочами и оксидами участвует не сам амфотерный гидроксид, а соответствующий ему оксид. 
 1) СО2 и HCl 2) Н2 и NaOH 3) NО и NaNO3 4) h3SO4 и NaOH Решение: Гидроксид хрома – амфотерный гидроксид. Амфотерные гидроксиды реагируют с кислотами и щелочами, с кислотыми и основными оксидами. Поэтому нам подходит вариант 4 –серная кислота и гидроксид натрия (щелочь): 2Cr(OH)3 + 3h3SO4 = Cr2(SO4)3 + 6h3O Cr(OH)3 + NaOH = Na[Cr(OH)4] ________________________________________________________________ 2. Гидроксид калия взаимодействует с каждым из двух веществ 1) нитратом натрия и нитратом серебра 2) гидроксидом алюминия и нитратом серебра 3) гидроксидом цинка и оксидом меди(I) 4) хлоридом бария и оксидом фосфора(V) Гидроксид калия это щелочь. она взаимодействует с кислотами,кислотными оксидами, амфотерными оксидами и гидроксидами,растворами солей при условии, если есть признак необратимости реакции (осадок, газ, слабый электролит). Данному условию соответствует набор веществ в варианте 2 — амфотерный гидроксид и соль. ________________________________________________________________ 3. Осуществить превращения:
1) СО2 и HCl 2) Н2 и NaOH 3) NО и NaNO3 4) h3SO4 и NaOH Решение: Гидроксид хрома – амфотерный гидроксид. Амфотерные гидроксиды реагируют с кислотами и щелочами, с кислотыми и основными оксидами. Поэтому нам подходит вариант 4 –серная кислота и гидроксид натрия (щелочь): 2Cr(OH)3 + 3h3SO4 = Cr2(SO4)3 + 6h3O Cr(OH)3 + NaOH = Na[Cr(OH)4] ________________________________________________________________ 2. Гидроксид калия взаимодействует с каждым из двух веществ 1) нитратом натрия и нитратом серебра 2) гидроксидом алюминия и нитратом серебра 3) гидроксидом цинка и оксидом меди(I) 4) хлоридом бария и оксидом фосфора(V) Гидроксид калия это щелочь. она взаимодействует с кислотами,кислотными оксидами, амфотерными оксидами и гидроксидами,растворами солей при условии, если есть признак необратимости реакции (осадок, газ, слабый электролит). Данному условию соответствует набор веществ в варианте 2 — амфотерный гидроксид и соль. ________________________________________________________________ 3. Осуществить превращения: | Al-1- Al2O3 -2-- NaAlO2 -3-- Al (OH)3 -4-- Al2O3 |

 Al2O3 +3h3O ________________________________________________________________ 4. Осуществить превращения:
Al2O3 +3h3O ________________________________________________________________ 4. Осуществить превращения: | AlCl3 --1-- Al(OH)3 -2--- Na[Al (OH)4] --3-- AlCl3 |
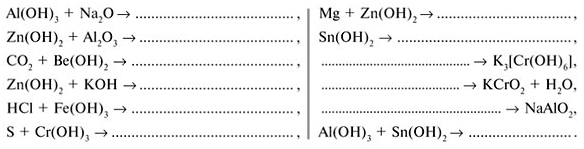
1) Zn Na2→ZnO2 → ZnSO4 → Zn(OH)2 → ZnO;
2) Al2O3 → X → Al(OH)3 → Y → AlCl3; 6. Предложи cпособ разделения смеси KOH, Mg(OH)2, Fe(OH)3. Напиши уравнения реакций. ……………………………………………………………………………………… …………………………………………………………………………………….. ……………………………………………………………………………………… 7. Осуществите следующие превращения: Al2O3 → Al → Al2O3 → NaAlO2 → AlCl3 8. Из порошкообразной смеси, содержащей Na2CO3, Fe, Al и BaSO4, выделите химическим путем все соединения в чистом виде. Напишите уравнения реакций и последовательность их проведения (опишите технологию всей работы). 9. Напишите схему диссоциации гидроксида хрома (III), а также молекулярное и ионное уравнения реакций растворения его в: а) азотной кислоте; б) растворе гидроксида натрия. 10. Заполни таблицу по химическим свойствам амфотерных гидроксидов (укажи продукты реакций). Напиши уравнения реакций на примере Zn(OH)2.| Вещества-реагенты | Продукты реакции с амфотерными гидроксидами | |
| Основный оксид | щелочных/ щелочно-земельных металлов | ………………………………………………………….. |
| остальных металлов | ………………………………………………………….. | |
| Амфотерный оксид | ………………………………………………………….. | |
| Kислотный оксид | ………………………………………………………….. | |
| растворимое (щелочь) | ………………………………………………………….. | |
| нерастворимое | ………………………………………………………….. | |
| Амфотерный гидроксид | ………………………………………………………….. | |
| ………………………………………………………….. | ||
| ………………………………………………………….. | ||
| ………………………………………………………….. | ||
| ………………………………………………………….. | ||
| Термическое разложение | ………………………………………………………….. | |

ВИДЕО ОПЫТ
| 1. В отличие от гидроксида калия гидроксид алюминия реагирует с: | |
| а) хлоридом натрия | б) соляной кислотой |
| в) гидроксидом натрия (р-р) | г) серной кислотой |
| 2. Гидроксид меди (II) можно получить при взаимодействии: | |
| а) оксида меди (II) с водой | б) меди с водой |
| в) водных растворов хлорида меди (II) и гидроксида натрия | г) меди и водного раствора гидроксида натрия |
| 3. В каких группах указаны формулы веществ, все из которых реагируют с разбавленным раствором гидроксида калия: | |
| в) Mn2O7, ZnO, Na2CO3 | г) CO2, FeCl2, Zn(OH)2 |
| 4. Действием каких веществ из гидроксида калия нельзя получить нитрат калия: | |
| а) нитрат натрия | б) азотная кислота |
| в) нитрат меди (II) | г) оксид азота (V) |
| 5. Укажите схемы реакций, в результате протекания которых образуется гидроксид алюминия: | |
| б)Al2O3 + KOH (р-р)→ | |
| г) Al2(SO4)3 + 3Ba(OH)2 → | |
| 6. В каких парах между веществами при определенных условиях возможно химическое взаимодействие: | |
| а) гидроксид калия и оксид кремния (IV) | б) хлорид калия и гидроксид бария |
| г) гидроксид кальция и оксид углерода (IV) | |
| 7. Щелочи могут реагировать: | |
| а) только с сильными кислотами | б) все ответы верны |
| в) только с кислотными оксидами | г) как с кислотными, так и с амфотерными оксидами |
| 8. Укажите формулы веществ, с водными растворами которых реагирует Cu(OH)2: | |
| в) все ответы верны | |
| 9. Основание не образуется при взаимодействии избытка разбавленного раствора щелочи с: | |
| а) сульфатом алюминия | б) хлоридом железа (II) |
| в) нитратом аммония | г) все ответы верны |
| 10. Гидроксид алюминия проявляет кислотные свойства, реагируя с: | |
| а) соляной кислотой | б) гироксидом калия |
| в) серной кислотой | г) нет верного ответа |
himiy88.blogspot.com
1. Напишите уравнения диссоциации следующих веществ:...
Для начала разберу самый нестандартный вариант - с фосфорной кислотой.Все реакции диссоциации обратимы и равновесны (т.е. в любом растворе любого вещества, сколь-нибудь способного к распадению на ионы, будет какое-то кол-во распавшегося на ионы вещества и какое-то кол-во нераспавшегося (обычно это осадок), хотя иногда чего-то будет очень мало, а чего-то очень много). Одним из главных моментов при распадании на ионы является энергетическая "выгода". Наиболее чувствителен в этом плане гидрид-ион (он в 1000 с лишним раз меньше любого другого иона). Именно поэтому в кислотах отделение водорода от кислот идёт поэтапно, и это очень ярко выраженный процесс. Почему: (на пальцах и интуитивно ясно) потому что электропритяжение. Отделиться от нейтральной молекулы и отдалиться от получившегося дигидрофосфат-аниона (заряженного отрицательно, но на всего лишь на один -) проще, чем отделиться от дигидрофосфат-аниона и "убегать" уже от гидрофосфат-аниона (с зарядом 2-). Та же история и дальше. Итого:
Что же касается "обычных" солей, то эффект "поэтапного" разделения на ионы их не касается (кроме кислых солей, разумеется).
Итак, получается:Фосфорная кислота.Получаются гидрид-катион (заряжен положительно на одну единицу) и дигидрофосфат-ион (заряжен отрицательно на одну единицу). Гидрид-ион состоит из водорода(уточнение: , лишенного электронной оболочки, а посему просто протона), а дигидрофосфат-ион состоит из 1 атома фосфора, 4 атомов кислорода, 2 атомов водорода. Фосфор связан исключительно с кислородами, 2 атома кислорода связаны с атомами водородов, оставшиеся два - прикреплены "обеими связями" к фосфору (не буду вдаваться в другую трактовку строения).
Нитрат хрома(III)Нитрат хрома(III) диссоциирует на катион металла (хрома, с зарядом 3+) и 3 нитрат-аниона (состоящих из атома азота, связанного с 3 атомами кислорода)
Гидроксид рубидия диссоциирует на катион металла (рубидия, с зарядом 1+) и 1 гидроксид-анион (состоящих из атома кислорода, связанного атомом водорода).
Если есть какие-то вопросы, прошу писать. Всегда будут рад ответить :)Удачи и успехов
Оцени ответ
napyaterku.com
Диссоциация оснований, кислот, амфотерных гидроксидов, солей в водных растворах
Количество просмотров публикации Диссоциация оснований, кислот, амфотерных гидроксидов, солей в водных растворах - 1831
Диссоциация оснований.Согласно теории электролитической диссоциации, основания - это электролиты, которые при диссоциации образуют только один вид анионов - гидроксид-ионы ОН-˸
NaOH →Na+ + ОН- ; Са(ОН)2 → СаОН+ + ОН-; СаОН+ → Са2+ + ОН-.
Диссоциация кислот.Кислоты - это электролиты, которые при диссоциации образуют только один вид катионов - катионы водорода Н+.
Одноосновные кислоты диссоциируют на ионы в одну стадию˸
НС1 → Н+ + С1-; HNO3 → Н+ + NO3 .
Многоосновные кислоты (h3SO3, h3SO4, h3S, h4PO4 и др.) диссоциируют ступенчато.
Первая ступень˸ h3SO4 → Н+ + HSO4 .
Вторая ступень˸ HSO4 → Н+ + SO-4 .
По второй ступени диссоциация HSO-4 затруднена.
Диссоциация фосфорной кислоты протекает по трем ступеням, причем по первой ступени диссоциация протекает в большей степени, чем по второй, а по второй — больше, чем по третьей.
Первая ступень˸ Н3РО4 ↔ Н+ + Н2РО-4 .
Вторая ступень˸ Н2РО4 ↔ Н+ + НРО2-4.
Третья ступень˸ НРО2-4↔ H+ + РО3-4.
Водный раствор фосфорной кислоты содержит ионы водорода Н+, дигидрофосфат-ионы Н2РО-4 , гидрофосфат-ионы НРО2-4 и фосфат-ионы РО3-4 , причем ионов Н2РО-4 больше, чем НРО2-4 и РО3-4 -ионов.
Диссоциация амфотерных гидроксидов. Амфотерные гидроксиды диссоциируют в водном растворе как по типу кислоты, так и по типу основания. При их диссоциации; одновременно образуются катионы Н+ и гидроксид-анионы ОН-. Амфотерные гидроксиды способны реагировать и с кислотами, и с основаниями. К ним относятся гидроксиды цинка, алюминия, хрома, свинца и др. Размещено на реф.рфАмфотерным электролитом является также вода.
Диссоциация амфотерных гидроксидов по типу кислот и оснований происходит потому, что прочность химических связей между атомами металла и кислорода (Ме-О-) и между атомами кислорода и водорода (-О-Н) почти одинакова. В результате эти связи в водных растворах разрываются одновременно и появляются катионы Н+ и анионы ОН-˸
Н+ + МеО- ↔ МеОН ↔Ме+ + ОН-.
Тогда диссоциацию амфотерного гидроксида цинка в водном растворе можно представить схемой˸
2Н+ + ZnO2-2 ↔ h3ZnО2 ↔ Zn(OH)2 ↔ Zn2+ + 2OH-.
Диссоциация солей. 1. Диссоциация средней соли. При растворении в воде средняя соль образует катионы металла и анионы кислотного остатка˸

Na2CO3 → 2Na+ + CO2-3 ; A12(SO4)3 → 2Al3+ + 3 SO2-4.
Таким образом, с точки зрения теории электролитической диссоциации, средние соли можно определить как электролиты, при диссоциации которых в водных растворах образуются катионы металла и анионы кислотного остатка.
2. Диссоциация кислой соли. При растворении в воде кислая соль образует катион металла и сложный анион, в состав которого входят атомы водорода и кислотный остаток˸
NaHCO3 → Na+ + НСО-3 (α= 1).
Сложный анион НСО3 (гидрокарбонат-ион) частично диссоциирует и дает анион СО2-3˸
НСО3 ^ Н+ + СО§" (α ʼʼ 1).
3. Диссоциация основной соли. При диссоциации основной соли образуются анионы кислотного остатка и сложные катионы, состоящие из атомов металла и гидроксогрупп ОН-˸
referatwork.ru
Константы диссоциации кислот и оснований неорганических (Таблица)
Справочная таблица константы диссоциации кислот и оснований по общей и неорганической химии содержит следующую информацию: название и формула гидрооксида и кислоты и соответствующие им константы диссоциации . Таблица содержит справочный материал, необходимый для решения задач по общей и неорганической химии. Предназначено для школьников и студентов.
К - константа диссоциации кислот и оснований
pK - величина, которая определяется как отрицательный десятичный логарифм константы диссоциации (часто используется вместо константы).
Смотрите также таблицу "константы кислотности сопряженных пар".
Константы диссоциации неорганических оснований (таблица)
| Гидроксид | Формула вещества | Константы диссоциации, Кв | рКв |
| Алюминия | Al(OH)3 | 1,38 · 10-9 | 8,86 |
| Аммония | Nh5OH | 1,79 · 10-5 | 4,75 |
| Бария | Ba(OH)2 | 2,30 · 10-1 | 0,64 |
| Галлия | Ga(OH)3 | 1,60 · 10-11 (2) | 10,8 |
| Железа (2) | Fe(OH)2 | 1,30 · 10-4 | 3,89 |
| Железа (3)
| Fe(OH)3
| 1,82 · 10-11 (2) | 10,74 |
| 1,35 · 10-12 (3) | 11,87 | ||
| Кадмия | Cd(OH)2 | 5,00 · 10-3 (2) | 2,30 |
| Кальция | Ca(OH)2 | 4,30 · 10-2 (2) | 1,37 |
| Кобальта (2) | Co(OH)2 | 4,00 · 10-5 (2) | 4,40 |
| Лантана | La(OH)2 | 5,20 · 10-4 (3) | 3,30 |
| Лития | LiOH | 6,75 · 10-1 | 0,17 |
| Магния | Mg(OH)2 | 2,50 · 10-3 (2) | 2,60 |
| Марганца (2) | Mn(OH)2 | 5,00 · 10-4 (2) | 3,30 |
| Меди (2) | Cu(OH)2 | 3,40 · 10-7 (2) | 6,47 |
| Натрия | NaOH | 5,90 | -0,77 |
| Никеля | Ni(OH)2 | 2,50 · 10-5 (2) | 4,60 |
| Свинца | Pb(OH)2 | 9,60 · 10-4 (1) | 3,02 |
| Стронция | Sr(OH)2 | 1,50 · 10-1 (2) | 0,82 |
| Хрома (3) | Cr(OH)3 | 1,02 · 10-10 (3) | 9,90 |
| Цинка | Zn(OH)2 | 4,00 · 10-5 (2) | 4,40 |
Константы диссоциации неорганических кислот (таблица)
| Кислота | Формула вещества | Константа диссоциации, Ка | рКа |
| Азотистая | HNO2 | 4,00 · 10-4 | 3,4 |
| Азотистоводородная | HN3 | 2,60 · 10-5 |
|
| Азотная | HNO3 | 4,36 · 10 | -1,64 |
| Алюминиевая (мета) | HAlO2 | 4,00 · 10-13 | 12,4 |
| Борная (мета) | HBO2 | 7,50 · 10-10 | 9,12 |
| Борная (орто)
| h4BO3
| 5,80 · 10-10(1) | 9,24 |
| 1,80 · 10-13(2) | 12,74 | ||
| 1,60 · 10-14(3) | 13,80 | ||
| Борная (тетра)
| h3B4O7
| ~10-4(1) | ~4 |
| ~10-9(2) | ~9 | ||
| Бромоводородная | HBr | 1,00 · 109 | -9 |
| Бромноватая | HBrO3 | 2,00 · 10-1 | 0,7 |
| Бромноватистая | HBrO | 2,06 · 10-9 | 8,7 |
| Вода | Н2О | 1,8 · 10-16 |
|
| Водорода пероксид | h3O2 | 2,63 · 10-12(1) | 11,58 |
| Галлиевая
| h4GaO3
| 5,00 · 10-11(2) | 10,3 |
| 2,00 · 10-12(3) | 11,7 | ||
| Германиевая | h3GeO3 | 1,70 · 10-9(1) | 8,77 |
| Иодоводородная | HI | 1,00 · Ю11 | -11 |
| Иодная (мета) | HIO4 | 2,30 · 10-2 | 1,64 |
| Иодная (орто)
| H5IO6
| 3,09 · 10-2(1) | 1,51 |
| 7,08 · 10-9(2) | 8.15 | ||
| 2,50 · 10-13(3) | 12,60 | ||
| Иодноватая | HIO3 | 1,70 · 10-1 | 0,77 |
| Кремневая (мета) | h3SiO3 | 2,20 · 10-10(1) | 9,66 |
| Кремневая (орто)
| h5SiO4
| 2,00 · 10-10(1) | 9,7 |
| 2,00 · 10-12(2) | 11,7 | ||
| 1,00 · 10-12(3) | 12,0 | ||
| 1,00 · 10-12(4) | 12,0 | ||
| Марганцовая | HMnO4 | 2,00 · 102 | -2,3 |
| Молибденовая | h3MoO4 | 1,00 · 10-6(2) | 6,0 |
| Мышьяковая (орто)
| h4ASO4
| 5,89 · 10-3(1) | 2,22 |
| 1,05 · 10-7(2) | 6,98 | ||
| 3,89 · 10-12(3) | 11,41 | ||
| Мышьяковистая (мета) | HASO2 | 6,00 · 10-10 | 9,2 |
| Мышьяковистая (орто)
| h4ASO3
| 6,00 · 10-10(1) | 9,2 |
| 1,70 · 10-14(2) | 13,77 | ||
| Оловянистая | h3SnO2 | 6,00 · 10-18 | 17,2 |
| Оловянная | h3SnO3 | 4,00 · 10-10 | 9,4 |
| Роданистоводородная | HCNS | 1,40 · 10-1 |
|
| Свинцовистая | h3PbO2 | 2,00 · 10-16 | 15,7 |
| Селенистая
| h3SeO3
| 3,50 · 10-3(1) | 2,46 |
| 5,00 · 10-8(2) | 7,3 | ||
| Селеновая
| h3SeO4
| 1,00 · 103(1) | -3 |
| 1,20 · 10-2(2) | 1,9 | ||
| Селеноводородная
| h3Se
| 1,70 · 10-4(1) | 3,77 |
| 1,00 · 10-11(2) | 11,0 | ||
| Серная
| h3SO4
| 1,00 · 103(1) | -3 |
| 1,20 · 10-2(2) | 1,9 | ||
| Сернистая
| h3SO3
| 1,58 · 10-2(1) | 1,8 |
| 6,31 · 10-8(2) | 7,2 | ||
| Сероводородная
| h3S | 6,00 · 10-8(1) | 7,2 |
| 1,00 · 10-14(2) | 14 | ||
| Сурьмяная(орто) | h4SbO4 | 4,00 · 10-5 | 4,4 |
| Сурьмянистая (мета) | HSbO2 | 1,00 · 10-11 | 11 |
| Теллуристая
| h3TeO3
| 3,00 · 10-3(1) | 2,5 |
| 2,00 · 10-8(2) | 7,7 | ||
| Теллуровая
| h3TeO4
| 2,29 · 10-8(1) | 7,64 |
| 6,46 · 10-12(2) | 11,19 | ||
| Теллуроводородная | h3Te | 1,00 · 10-3 | 3,0 |
| Тиосерная
| h3S2O3
| 2,20 · 10-1(1) | 0,66 |
| 2,80 · 10-2(2) | 1,56 | ||
| Угольная
| h3CO3
| 4,45 · 10-7(1) | 6,35 |
| 4,69 · 10-11(2) | 10,33 | ||
| Фосфористая (орто)
| h4PO3
| 1,60 · 10-3(1) | 1,8 |
| 6,30 · 10-7(2) | 6,2 | ||
| Фосфорная (орто)
| h4PO4
| 7,52 · 10-3(1) | 2,12 |
| 6,31 · 10-8(2) | 7,20 | ||
| 1,26 · 10-12(3) | 11,9 | ||
| Фосфорная (пиро)
| h5P2O7
| 1,40 · 10-1(1) | 0,85 |
| 1,10 · 10-2(2) | 1,95 | ||
| 2,10 · 10-7(3) | 6,68 | ||
| Фтороводородная | HF | 6,61 · 10-4 | 3,18 |
| Хлороводородная | HCl | 1 · 107 | -7 |
| Хлорноватистая | HClO | 5,01 · 10-8 | 7,3 |
| Хромовая
| h3CrO4
| 1 · 10 (1) | -1 |
| 3,16 · 10-7 | 6,5 | ||
| Циановодородная | HCN | 7,90 · 10-10 | 9,1 |
_______________
Источник информации: Справочные таблицы по общей и неорганической химии / Учебное пособие. Новосибирск, 2008
infotables.ru
| Константы диссоциации Кb и константы основности pКb=-lg(Кb) неорганических оснований в водных растворах
Источник: Новый справочник химика и технолога. Химическое равновесие. Свойства растворов. — СПб.: АНО НПО «Профессионал», 2004. — 998 с. |
tehtab.ru
| Масляная Молибденовая Муравьиная Мышьяковая Пропионовая Селенистая Селенистоводородная Селеновая Серная Сернистая Сероводородная Синильная Теллуристая Теллуристоводородная Тиосерная Угольная Уксусная Фосфористая Фосфорная (орто) Фтористоводородная Хлористая Хлорноватистая Хромовая Щавелевая | Ch4(Ch3)2COOH h3MoO4 HCOOH h4AsO4 Ch4Ch3COOH h3SeO3 h3Se h3SeO4 h3SO4 h3SO3 h3S HCN h3TeO3 h3Te h3S2O3 h3CO3 Ch4COOH h4PO3 h4PO4 HF HClO2 HClO h3CrO4 h3C2O4 | 1,5·10-5 2,9·10-3 1,8·10-4 5,6·10-3 1,3·10-5 1,8·10-3 1,3·10-4 1,4·10-2 1,0·10-7 5,0·10-10 2,7·10-3 2,3·10-3 2,5·10-1 4,5·10-7 1,7·10-5 3,1·10-2 7,1·10-3 6,2·10-4 1,1·10-2 3,0·10-8 1,6·10-1 5,6·10-2 | 1,4·10-4 1,7·10-7 3,2·10-9 1,0·10-11 1,2·10-2 1,15·10-2 6,2·10-8 2,5·10-13 1,8·10-8 6,9·10-13 1,9·10-2 4,8·10-11 1,6·10-7 6,2·10-8 3,2·10-7 5,4·10-5 | 3,0·10-12 5,0·10-13 | Алюминия гидроксид Аммония гидроксид Бериллия гидроксид Висмута гидроксид Железа (II)гидроксид Железа (III)гидроксид Кадмия гидроксид Кобальта гидроксид Магния гидроксид Марганца гидроксид Меди гидроксид Никеля гидроксид Олова гидроксид Ртути (II)гидроксид Свинца гидроксид Серебра гидроксид Хрома (III)гидроксид Цинка гидроксид | Al(OH)3 Nh5OH Be(OH)2 Bi(OH)3 Fe(OH)2 Fe(OH)3 Cd(OH)2 Co(OH)2 Mg(OH)2 Mn(OH)2 Cu(OH)2 Ni(OH)2 Sn(OH)2 Hg(OH)2 Pb(OH)2 AgOH Cr(OH)3 Zn(OH)2 | 1,8·10-5 3,0·10-7 6,2·10-5 3,2·10-10 2,4·10-3 1,6·10-5 6,6·10-8 2,6·10-4 9,8·10-10 3,9·10-12 9,6·10-4 5,0·10-3 1,3·10-5 | 3,3·10-8 4,0·10-4 2,8·10-6 5,0·10-10 1,5·10-7 4,0·10-5 2,5·10-3 1,2·10-4 1,0·10-6 1,1·10-5 1,2·10-12 5·10-11 3,0·10-8 2·10-8 4,9·10-7 | 1·10-9 4,0·10-13 1,3·10-12 7,9·10-11 |
studfiles.net
2. Основные классы электролитов.
По химическому составу ионов, образующихся при диссоциации, электролиты делятся на четыре основных класса: кислоты, основания, амфолиты и соли.
По Аррениусу, кислотами называются электролиты, при первичной диссоциации которых образуются ионы Н+. Например: HCl = H+ +Cl-; h3SO4 = 2H+ + SO42-. По сравнению с нейтральными растворами растворы кислот содержат избыточное количество ионов H+. Поэтому значения рН растворов кислот находятся в области рН7.
Имеется 2 группы кислот: бескислородные и кислородсодержащие (оксокислоты). Среди бескислородных кислот сильными являются три: HCl, HBr, HI; остальные бескислородные кислоты - слабые. Для определения силы оксокислот следует руководствоваться правилом: если степень окисления кислотообразующего элемента равна +6 и выше, такая кислота – сильная (исключение HNO3). Например, h3SO4 - сильная кислота, поскольку степень окисления серы в ней равна +6, а h3SO3 - слабая кислота т.к. степень окисления серы здесь равна +4.
Основаниями являются электролиты, при первичной диссоциации которых образуются гидроксид-ионы ОН-. Например: NaOH = Na+ + OH-; Cu(OH)2Cu2+ + 2OH-. Значения рН растворов оснований находятся в области рН7.
Сильными основаниями являются гидроксиды щелочных и щелочноземельных металлов. Гидроксиды этих металлов хорошо растворимы в воде и поэтому получили название щелочей.
Среди гидроксидов металлов имеются соединения, способные к диссоциации как по кислотному, так и по основному типу. Такие гидроксиды называются амфотерными (амфолитами). Например, Be(OH)2, Zn(OH)2, Al(OH)3, Cr(OH)3.
Соли – электролиты, при первичной диссоциации которых не образуются ни ионы Н+, ни ионы ОН-. Например: Cr2(SO4)3=2Cr3++3SO42- - диссоциация средней соли; Ca(HCO3)2=Ca2++2HCO3- - диссоциация кислой соли; AlOH(NO3)2=AlOh3++2NO3-- диссоциация основной соли.
Особую группу электролитов составляют комплексные кислоты, основания и соли. Эти электролиты, как правило, диссоциируют полностью на ионы внешней и внутренней координационной сферы, т.е. являются сильными электролитами. Например, процесс первичной диссоциации комплексной соли [Cr(h3O)6]Cl3 выражается уравнением: [Cr(h3O)6]Cl3 = [Cr(h3O)6]3+ + 3Cl-
3. Смещение ионных равновесий.
Равновесия в растворах слабых электролитов, как и любые химические равновесия подчиняется принципу Ле Шателье, а именно: при уменьшении концентрации ионов в растворе ( например, путем их связывания в слабый электролит ) ионное равновесие смещается вправо, т.е. степень диссоциации слабого электролита увеличивается; при увеличении концентрации ионов ( например, путем добавления к раствору слабого электролита сильного электролита, содержащего одноименные ионы ) ионное равновесие смещается влево, т.е. степень диссоциации слабого электролита уменьшается.
Пример 3.1. Смещение ионного равновесия в 0,1М растворе уксусной кислоты при добавлении кристаллического ацетата натрия.
Уксусная кислота – слабый электролит, диссоциирующий согласно уравнению: СН3СООН СН3СОО- + Н+. Ацетат натрия – хорошо растворимая соль, диссоциирующая в растворе полностью согласно уравнению: СН3СООNa = СН3СОО- + Na+. Поэтому при введении в раствор уксусной кислоты сильного электролита – ацетата натрия – происходит резкое увеличение концентрации ацетат-ионов, что согласно принципу Ле Шателье должно вызвать смещение ионного равновесия влево – в сторону образования дополнительного количества недиссоциированной уксусной кислоты. Подтвердим это рассчётом.
В 0,1М растворе СН3СООН концентрация ионов Н+ равна 1,310-3, а рН = 2,9 (см. примеры 1.2, 1.3). После добавления к раствору уксусной кислоты ацетата натрия вследствие смещения ионного равновесия влево концентрация недиссоциированной кислоты возрастёт, но это возрастание незначительно, т.к. согласно примеру 1.2. концентрация связываемых ионов Н+ не может превышать величину 1,310-3. Так как изменением объёма раствора в результате добавления кристаллической соли можно пренебречь принимаем, что [СН3СООН] = Ск Сик, где Сик = 0,1 моль/л – исходная концентрация взятой кислоты, а Ск – концентрация уксусной кислоты в смеси с ацетатом натрия.
Дальнейший рассчёт произведём для 0,1М раствора СН3СООН, в который добавлен кристаллический СН3СООNa в количестве, соответствующим его концентрации 1моль/л (82г соли, добавленной к 1л кислоты). Согласно выражению (1.1) концентрация ионов Н+ в смеси СН3СООН и СН3СООNa равна: Н+ = Ксн3соон [СН3СООН/СН3СОО-. Неизвестное значение концентрации ацетат-ионов в смеси кислоты и соли определяем, исходя из того, что количество ионов, образуемых сильным электролитом неизмеримо больше, по сравнению с количеством ионов, образуемых слабым электролитом. В связи с этим можно считать, что концентрация ацетат-ионов в смеси практически определяется принятой концентрацией добавленной соли Сс. В нашем случае СН3СОО- = Сс 1моль/л.
Подставляя численные значения концентраций и константы диссоциации в ваышезаписанное выражение для определения концентрации ионов Н+, получаем: Н+ = Ксн3соон [СН3СООН/СН3СОО- = 1.75 10-50,1/1 = 1.75 10-6, откуда рН = 5,76. Полученные результаты однозначно указывают на то, что при добавлении к раствору уксусной кислоты ацетата натрия происходит уменьшение концентрации ионов Н+, вызывающее увеличение рН, т.е. происходит сдвиг ионного равновесия влево – в сторону образования дополнительного количества недиссоциированных молекул уксусной кислоты.
Вывод о направлении сдвига ионного равновесия в растворе уксусной кислоты при добавлении к нему ацетата натрия можно распространить на все ионные равновесия: при добавлении к раствору слабого электролита одноимённых ионов, образующихся в результате диссоциации сильного электролита, происходит сдвиг ионного равновесия в сторону образования недиссоциированного слабого электролита.
Смещение ионного равновесия в противоположную сторону, т.е. в направлении усиления диссоциации слабого электролита, происходит при добавлении к раствору слабого электролита любого другого электролита, ионы которого способны связывать ионы слабого электролита.
Пример 3.2. Смещение ионного равновесия при добавлении к раствору уксусной кислоты раствора гидроксида натрия.
Добавляемый к раствору СН3СООН гидроксид натрия – сильный электролит, диссоциирующий полностью согласно уравнению: NaOH = Na+ + OH-.
В смеси СН3СООН и NaOH одновременно протекают 2 взаимосвязанных процесса:
1) СН3СООН СН3СОО- + Н+– обратимая диссоциация слабой кислоты;
2) Н+ + OH- = Н2О – связывание ионов Н+ слабой кислоты ионами OH- щёлочи, вызывающее согласно принципу Ле Шателье смещение ионного равновесия 1) вправо, т.е. дополнительную диссоциацию уксусной кислоты вплоть до её полного израсходования, если количество добавленного NaOH достаточно для связывания всех ионов Н+ уксусной кислоты.
Суммарно процессы 1) и 2), протекающие в смеси растворов СН3СООН и NaOH, выражаются уравнением: СН3СООН + OH- = СН3СОО- + Н2О. Записанное суммарное уравнение представляет собой ионно-молекулярное уравнение реакции между уксусной кислотой и гидроксидом натрия.
Связывание ионов слабого электролита, вызывающее смещение ионного равновесия – вправо – в сторону усиления диссоциации слабого электролита, может происходить в результате образования неэлектролита (например, газообразного соединения) или любого слабодиссоциирующего химического образования – труднорастворимого электролита, растворимого слабого электролита, комплекса и пр.
Одновременное влияние связывания ионов и введения одноимённых ионов на состояние ионных равновесий удобно проследить на примере гетерогенных равновесий, устанавливающихся в растворах амфотерных электролитов.
Пример 3.3. Смещение гетерогенных ионных равновесий в растворе трунорастворимого гидроксида хрома (III) при добавлении к нему кислоты и щёлочи.
Как уже указывалось (см. п. 2), амфотерные гидроксиды способны диссоциировать и по кислотному, и по основному типу. Диссоциацию амфотерного Cr(OH)3 можно выразить схемой:
Диссоциация по кислотному типу Диссоциация по основному типу
[Cr(OH)6]3- + 3H+ Cr(OH)3 + 3h3O Cr3+ + 3OH- + 3h3O
При добавлении к раствору Cr(OH)3 кислоты (ионов H+) равновесие диссоциации по кислотному типу из-за действия одноимённых ионов H+ смещается вправо; одновременно, в результате связывания ионов OH- ионами H+ добавленной кислоты равновесие диссоциации по основному типу смещается также вправо вплоть до полного растворения Cr(OH)3, если количество добавленной кислоты достаточно для полного связывания всех ионов OH- гидроксида хрома. Иначе говоря, при взаимодействии с кислотами Cr(OH)3 ведёт себя как основание.
При добавлении к раствору Cr(OH)3 щёлочи (ионов OH-) равновесие диссоциации по основному типу из-за действия одноимённых ионов OH- смещается влево; одновременно, в результате связывания ионов H+ ионами OH- добавленной щёлочи равновесие диссоциации по кислотному типу смещается также влево вплоть до полного растворения Cr(OH)3, если количество добавленной щёлочи достаточно для полного связывания всех ионов H+ гидроксида хрома. Т.е., при взаимодействии со щелочами Cr(OH)3 ведёт себя как кислота.
В общем случае, в результате смещения гетерогенного ионного равновесия растворимость труднорастворимого электролита увеличивается при связывании любого из его ионов и, наоборот, происходит осаждение труднорастворимого электролита из раствора, если произведение концентраций его ионов превышает значение ПР.
Пример 3.4. Определение возможности осаждения гидроксида железа (II) из раствора, содержащего ионы Fe2+ и OH-, концентрации которых, соответственно, равны 10-4М и 10-7М.
Записываем выражение произведения растворимости Fe(OH)2 и отмечаем его численное значение (см. пример 1.1): ПР = [Fe2+][ OH-]2 = 210-15. Вычисляем произведение концентраций (ПС) имеющихся в растворе ионов Fe2+ и OH-: ПС = 10-4(10-7)2 = 10-18. Видно, что ПС ПР. Следовательно, раствор является ненасыщенным, условие осаждения не выполняется и осадок Fe(OH)2 не образуется.
studfiles.net