Диаграмма Пурбе. Диаграмма пурбе для хрома
Диаграмма Пурбе — WiKi
Диаграмма Пурбе строится в координатах E (ордината) — pH (абсцисса). Она отражает формы, которые термодинамически устойчивы при данном значении рН и окислительно-восстановительного потенциала среды. При меньшем потенциале соответствующая форма может быть восстановлена до нижележащей (если таковая существует), при более высоком — окислена до вышележащей (если таковая существует). Границы между формами существования раствор-твёрдое или раствор-газ обычно зависят от концентрации растворенных форм; границы между формами существования растворённых форм от их концентрации, как правило, не зависят.
Часто на диаграмму Пурбе наносят границы области существования воды. Верхняя из них (E=1.23-0.059pH) соответствует выделению кислорода (то есть при более высоких потенциалах возможно окисление воды до кислорода):
4h3O — 4e- = 4H+ + O2 (pH<7) 4OH- — 4e- = 2h3O + O2 (pH>7)Нижняя граница (E=-0.059pH) соответствует выделению водорода (то есть при меньших потенциалах возможно восстановление воды до водорода):
На иллюстрациях к данной статье область существования воды ограничена голубыми линиями.
Диаграмма Пурбе — мощнейшее средство предсказания направления химических реакций соединений данного элемента. Из неё можно определить условия большинства кислотно-основных и окислительно-восстановительных реакций соединений данного элемента без учета взаимодействия с посторонними ионами. По ней можно предсказать процессы диспропорционирования и конпропорционирования разных форм, возможность выделения ими водорода и кислорода. Сопоставляя диаграммы Пурбе для двух элементов можно предсказать окислительно-восстановительные реакции между их соединениями. Таким образом, диаграмма Пурбе для некоего элемента в сжатой форме отображает его неорганическую химию.
Весьма важное значения диаграммы Пурбе имеют в предсказании коррозии в разных условиях[1].
Ограничения применимости диаграммы Пурбе
Диаграмма Пурбе отображает только термодинамически устойчивые формы. Кинетически устойчивые (они же метастабильные) формы на ней не отображаются. Поэтому она неприменима для предсказания образования метастабильных форм. Например такая форма, как гипохлорит-ион OCl- метастабильна (неустойчива термодинамически, но диспропорционирует крайне медленно). Поэтому на диаграмме Пурбе для хлора её нет и предсказать её образование (в частности, при диспропорционировании хлора) по диаграмме Пурбе невозможно: Cl2 + 2OH- = Cl- + ClO- + h3O Кроме того, далеко не все процессы, предсказаные по диаграмме Пурбе имеют достаточно большую скорость, чтобы быть заметными.
Предсказание гидролиза
Если при каком-то значении рН существует гидроксид, значит, свободный ион при этом значении рН гидролизуется. Пример 1. На диаграмме Пурбе для железа при рН>4 устойчив Fe(OH)3, а Fe3+ неустойчив. Значит, при pH>4 ион Fe3+ будет полностью гидролизоваться: Fe3+ + 3h3O = Fe(OH)3 + 3H+Гидролиз иона Fe3+ идёт при рН<4. Точное значение рН зависит от концентрации иона Fe3+ (размазанная граница).
Предсказание конпропорционирования
Если при данном значении рН две формы разделены третьей, то эти две формы будут конпропорционировать с образованием третьей.Пример 1. На диаграмме Пурбе для марганца при рН 0-3 Mn2+ и MnO4- разделены MnO2. Значит, Mn2+ и MnO4- будут конпрпорционировать:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+Пример 2. На диаграмме Пурбе для марганца при рН 4-7 Mn2+ и MnO4- разделены двумя формами (MnO2, Mn2O3). Это значит, что Mn2+ и MnO4 будут конпропорционировать. При этом возможно два продукта, причем преобладающий продукт зависит от соотношения реагентов или взаимной скорости двух конкурирующих реакций:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+8Mn2+ + 2MnO4- + 7h3O = 5Mn2O3 + 14H+Пример 3. На диаграмме Пурбе для марганца в диапазоне рН 0-14 между MnO2 и MnO4- промежуточных форм нет. Значит, в этом диапазоне рН MnO2 и MnO4- конпропорционировать не будут.
Предсказание диспропорционирования
Если форма в данной степени окисления при данном рН на диаграмме Пурбе отсутствует, значит, она будет диспропорционировать на соседние формы, имеющиеся на диаграмме Пурбе. Пример 1. На диаграмме Пурбе для марганца при рH<14 отсутствует манганат MnO42- (степень окисления марганца +6). Это значит, что при этих рН манганат будет диспропорционировать[2]. Ближайшая устойчивая степень окисления снизу +4 (MnO2), сверху — +7 (MnO4-). Они и будут образовываться при диспропорционировании: 3MnO42- + 2h3O = MnO2 + 2MnO4- + 4OH-Этот процесс, в частности, будет происходить при растворении твёрдого манганата в воде или при подкислении сильнощелочного раствора, в котором манганат устойчив.Пример 2. На диаграмме Пурбе для марганца соединения марганца (+3) отсутствуют вовсе. Это значит, что при растворении в воде соединений марганца (+3) они будут диспропорционировать на ближайшие устойчивые степени окисления +2 снизу (в виде Mn2+) и +4 сверху (в виде MnO2): 2Mn3+ + 2h3O = Mn2+ + MnO2 + 4H+
Предсказание вытеснения водорода
Если область существования данной формы лежит ниже области устойчивости воды (нижняя голубая линия на цветных диаграммах), то данная форма при соответствующих рН способна реагировать с водой, вытесняя водород. Реально вследствие кинетических проблем (то есть малой скорости подобных реакций) возникает т. н. эффект перенапряжения выделения водорода, и для реального выделения водорода соответствующая форма должна лежать ниже области устойчивости воды как минимум на 0.4-0.8В. Кроме того, гидроксиды металлов, как правило, пассивируют металл, поэтому в нейтральных и щелочных средах водород, как правило, не выделяется, даже если область существования металла лежит сильно ниже области устойчивости воды. Пример 1. На диаграмме Пурбе для марганца его область существования лежит заметно ниже нижней границы устойчивости воды. Значит, он способен вытеснять водород: Mn + 2H+ = Mn2+ + h3Это соответствует тому факту, что металл в ряду активности стоит левее водорода.
Предсказание окисления кислородом воздуха
Если область существования некой формы лежит заметно ниже верхней границы устойчивости воды, то эта форма может окисляться кислородом воздуха. При этом образуется форма, которую пересекает верхняя граница устойчивости воды. Пример 1. На диаграмме Пурбе для марганца область существования Mn(OH)2 лежит сильно ниже верхней границы устойчивости воды (верхняя голубая линия). Это значит, что он может быть окислен до Mn3O4, Mn2O3 и, в конце концов, до MnO2 (но не MnO4-, так как эта форма лежит выше области существования воды): 2Mn(OH)2 + O2 = 2MnO2 + 2h3O И действительно, Mn(OH)2 на воздухе очень быстро коричневеет[3]. Пример 2. На диаграмме Пурбе для железа область существования металлического железа лежит намного ниже верхней границы существования воды. Это значит, что оно может быть окислено кислородом до Fe(OH)3, что мы и наблюдаем в процессе ржавления. При этом, поскольку процесс протекает долго, получаются дегидратированные формы (Fe3O4, Fe2O3 и др.), которые более устойчивы термодинамически, но образуются медленно.
Окисление металлов кислородом происходит далеко не всегда за счёт эффекта пассивирования.
Предсказание выделения кислорода
Если некая форма целиком лежит выше области существования воды, она может разлагаться с выделением кислорода. Пример. На диаграмме Пурбе для железа область существования ферратов FeO42- лежит гораздо выше области существования воды (особенно в кислой области). Поэтому при подкислении ферраты разлагаются с выделением кислорода[4]: 4FeO42- + 20H+ = 4Fe3+ + 3O2 + 10h3O
Предсказание окислительно-восстановительных реакций между соединениями двух элементов
Если при некотором рН форма существования одного элемента лежит заметно (хотя бы на 0.2 В) выше формы существования другого элемента, то вышележащая форма окислит нижележащую. При этом образуются формы, область устойчивости которых лежит между ними. Пример. Область существования MnO4- (диаграмма для марганца) лежит выше, чем область существования Fe2+ (диаграмма для железа). Значит,MnO4- может окислять Fe2+. В кислой среде при этом образуется Fe3+ и (в зависимости от соотношения реагентов) MnO2 или Mn2+: MnO4- + 3Fe2+ + 4H+ = MnO2 + 3Fe3+ + 2h3O MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4h3O В нейтральной среде образуются MnO2 и Fe(OH)3:MnO4- + 3Fe2+ + 7h3O = MnO2 + 3Fe(OH)3 + 5H+
ru-wiki.org
Диаграмма Пурбе Википедия
Диаграмма Пурбе для системы Fe-h3O Диаграмма Пурбе для системы Mn-h3OДиаграмма Пурбе (диаграмма преобладающих форм, E-pH диаграмма) — диаграмма, наглядно отображающая термодинамически устойчивые формы существования элементов (ионов, молекул, атомных кристаллов и металлов) в растворах при различных значениях водородного показателя pH и окислительно-восстановительного потенциала E. Предложена Марселем Пурбе.
Для каждого элемента можно построить свою диаграмму Пурбе. Диаграммы Пурбе для одного элемента могут отличаться в зависимости от температуры, растворителя и присутствия лигандов в растворе. Однако как правило приводятся диаграммы Пурбе для водных растворов при 25 °С. Диаграммы Пурбе строятся на основании уравнения Нернста и стандартных окислительно-восстановительных потенциалов.
Построение
Диаграмма Пурбе строится в координатах E (ордината) — pH (абсцисса). Она отражает формы, которые термодинамически устойчивы при данном значении рН и окислительно-восстановительного потенциала среды. При меньшем потенциале соответствующая форма может быть восстановлена до нижележащей (если таковая существует), при более высоком — окислена до вышележащей (если таковая существует). Границы между формами существования раствор-твёрдое или раствор-газ обычно зависят от концентрации растворенных форм; границы между формами существования растворённых форм от их концентрации, как правило, не зависят.
Часто на диаграмму Пурбе наносят границы области существования воды. Верхняя из них (E=1.23-0.059pH) соответствует выделению кислорода (то есть при более высоких потенциалах возможно окисление воды до кислорода):
4h3O — 4e- = 4H+ + O2 (pH<7) 4OH- — 4e- = 2h3O + O2 (pH>7)Нижняя граница (E=-0.059pH) соответствует выделению водорода (то есть при меньших потенциалах возможно восстановление воды до водорода):
2H+ + 2e- = h3 (pH<7) 2h3O + 2e- = h3 + 2OH- (pH>7)Применение
Диаграмма Пурбе — мощнейшее средство предсказания направления химических реакций соединений данного элемента. Из неё можно определить условия большинства кислотно-основных и окислительно-восстановительных реакций соединений данного элемента без учета взаимодействия с посторонними ионами. По ней можно предсказать процессы диспропорционирования и конпропорционирования разных форм, возможность выделения ими водорода и кислорода. Сопоставляя диаграммы Пурбе для двух элементов можно предсказать окислительно-восстановительные реакции между их соединениями. Таким образом, диаграмма Пурбе для некоего элемента в сжатой форме отображает его неорганическую химию.
Весьма важное значения диаграммы Пурбе имеют в предсказании коррозии в разных условиях[1].
Ограничения применимости диаграммы Пурбе
Диаграмма Пурбе отображает только термодинамически устойчивые формы. Кинетически устойчивые (они же метастабильные) формы на ней не отображаются. Поэтому она неприменима для предсказания образования метастабильных форм. Например такая форма, как гипохлорит-ион OCl- метастабильна (неустойчива термодинамически, но диспропорционирует крайне медленно). Поэтому на диаграмме Пурбе для хлора её нет и предсказать её образование (в частности, при диспропорционировании хлора) по диаграмме Пурбе невозможно: Cl2 + 2OH- = Cl- + ClO- + h3O Кроме того, далеко не все процессы, предсказаные по диаграмме Пурбе имеют достаточно большую скорость, чтобы быть заметными.
Предсказание гидролиза
Если при каком-то значении рН существует гидроксид, значит, свободный ион при этом значении рН гидролизуется. Пример 1. На диаграмме Пурбе для железа при рН>4 устойчив Fe(OH)3, а Fe3+ неустойчив. Значит, при pH>4 ион Fe3+ будет полностью гидролизоваться: Fe3+ + 3h3O = Fe(OH)3 + 3H+Гидролиз иона Fe3+ идёт при рН<4. Точное значение рН зависит от концентрации иона Fe3+ (размазанная граница).
Предсказание конпропорционирования
Если при данном значении рН две формы разделены третьей, то эти две формы будут конпропорционировать с образованием третьей.Пример 1. На диаграмме Пурбе для марганца при рН 0-3 Mn2+ и MnO4- разделены MnO2. Значит, Mn2+ и MnO4- будут конпрпорционировать:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+Пример 2. На диаграмме Пурбе для марганца при рН 4-7 Mn2+ и MnO4- разделены двумя формами (MnO2, Mn2O3). Это значит, что Mn2+ и MnO4 будут конпропорционировать. При этом возможно два продукта, причем преобладающий продукт зависит от соотношения реагентов или взаимной скорости двух конкурирующих реакций:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+8Mn2+ + 2MnO4- + 7h3O = 5Mn2O3 + 14H+Пример 3. На диаграмме Пурбе для марганца в диапазоне рН 0-14 между MnO2 и MnO4- промежуточных форм нет. Значит, в этом диапазоне рН MnO2 и MnO4- конпропорционировать не будут.
Предсказание диспропорционирования
Если форма в данной степени окисления при данном рН на диаграмме Пурбе отсутствует, значит, она будет диспропорционировать на соседние формы, имеющиеся на диаграмме Пурбе. Пример 1. На диаграмме Пурбе для марганца при рH<14 отсутствует манганат MnO42- (степень окисления марганца +6). Это значит, что при этих рН манганат будет диспропорционировать[2]. Ближайшая устойчивая степень окисления снизу +4 (MnO2), сверху — +7 (MnO4-). Они и будут образовываться при диспропорционировании: 3MnO42- + 2h3O = MnO2 + 2MnO4- + 4OH-Этот процесс, в частности, будет происходить при растворении твёрдого манганата в воде или при подкислении сильнощелочного раствора, в котором манганат устойчив.Пример 2. На диаграмме Пурбе для марганца соединения марганца (+3) отсутствуют вовсе. Это значит, что при растворении в воде соединений марганца (+3) они будут диспропорционировать на ближайшие устойчивые степени окисления +2 снизу (в виде Mn2+) и +4 сверху (в виде MnO2): 2Mn3+ + 2h3O = Mn2+ + MnO2 + 4H+
Предсказание вытеснения водорода
Если область существования данной формы лежит ниже области устойчивости воды (нижняя голубая линия на цветных диаграммах), то данная форма при соответствующих рН способна реагировать с водой, вытесняя водород. Реально вследствие кинетических проблем (то есть малой скорости подобных реакций) возникает т. н. эффект перенапряжения выделения водорода, и для реального выделения водорода соответствующая форма должна лежать ниже области устойчивости воды как минимум на 0.4-0.8В. Кроме того, гидроксиды металлов, как правило, пассивируют металл, поэтому в нейтральных и щелочных средах водород, как правило, не выделяется, даже если область существования металла лежит сильно ниже области устойчивости воды. Пример 1. На диаграмме Пурбе для марганца его область существования лежит заметно ниже нижней границы устойчивости воды. Значит, он способен вытеснять водород: Mn + 2H+ = Mn2+ + h3Это соответствует тому факту, что металл в ряду активности стоит левее водорода.
Предсказание окисления кислородом воздуха
Если область существования некой формы лежит заметно ниже верхней границы устойчивости воды, то эта форма может окисляться кислородом воздуха. При этом образуется форма, которую пересекает верхняя граница устойчивости воды. Пример 1. На диаграмме Пурбе для марганца область существования Mn(OH)2 лежит сильно ниже верхней границы устойчивости воды (верхняя голубая линия). Это значит, что он может быть окислен до Mn3O4, Mn2O3 и, в конце концов, до MnO2 (но не MnO4-, так как эта форма лежит выше области существования воды): 2Mn(OH)2 + O2 = 2MnO2 + 2h3O И действительно, Mn(OH)2 на воздухе очень быстро коричневеет[3]. Пример 2. На диаграмме Пурбе для железа область существования металлического железа лежит намного ниже верхней границы существования воды. Это значит, что оно может быть окислено кислородом до Fe(OH)3, что мы и наблюдаем в процессе ржавления. При этом, поскольку процесс протекает долго, получаются дегидратированные формы (Fe3O4, Fe2O3 и др.), которые более устойчивы термодинамически, но образуются медленно.
Окисление металлов кислородом происходит далеко не всегда за счёт эффекта пассивирования.
Предсказание выделения кислорода
Если некая форма целиком лежит выше области существования воды, она может разлагаться с выделением кислорода. Пример. На диаграмме Пурбе для железа область существования ферратов FeO42- лежит гораздо выше области существования воды (особенно в кислой области). Поэтому при подкислении ферраты разлагаются с выделением кислорода[4]: 4FeO42- + 20H+ = 4Fe3+ + 3O2 + 10h3O
Предсказание окислительно-восстановительных реакций между соединениями двух элементов
Если при некотором рН форма существования одного элемента лежит заметно (хотя бы на 0.2 В) выше формы существования другого элемента, то вышележащая форма окислит нижележащую. При этом образуются формы, область устойчивости которых лежит между ними. Пример. Область существования MnO4- (диаграмма для марганца) лежит выше, чем область существования Fe2+ (диаграмма для железа). Значит,MnO4- может окислять Fe2+. В кислой среде при этом образуется Fe3+ и (в зависимости от соотношения реагентов) MnO2 или Mn2+: MnO4- + 3Fe2+ + 4H+ = MnO2 + 3Fe3+ + 2h3O MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4h3O В нейтральной среде образуются MnO2 и Fe(OH)3:MnO4- + 3Fe2+ + 7h3O = MnO2 + 3Fe(OH)3 + 5H+
Литература
- ↑ Pourbaix M. Thermodynamics and corrosion. Corrosion Science, Vol. 3(1), No. 10, pp. 963—988, 1990
- ↑ Реми Г. Курс неорганической химии. т. 2. М., Мир, 1966. С. 246.
- ↑ Реми Г. Курс неорганической химии. т. 2. М., Мир, 1966. С. 232.
- ↑ Реми Г. Курс неорганической химии. т. 2. М., Мир, 1966. С. 309.
Ссылки
wikiredia.ru
Диаграмма Пурбе — Википедия
Материал из Википедии — свободной энциклопедии
Диаграмма Пурбе для системы Fe-h3O Диаграмма Пурбе для системы Mn-h3OДиаграмма Пурбе (диаграмма преобладающих форм, E-pH диаграмма) — диаграмма, наглядно отображающая термодинамически устойчивые формы существования элементов (ионов, молекул, атомных кристаллов и металлов) в растворах при различных значениях водородного показателя pH и окислительно-восстановительного потенциала E. Предложена Марселем Пурбе.
Для каждого элемента можно построить свою диаграмму Пурбе. Диаграммы Пурбе для одного элемента могут отличаться в зависимости от температуры, растворителя и присутствия лигандов в растворе. Однако как правило приводятся диаграммы Пурбе для водных растворов при 25 °С. Диаграммы Пурбе строятся на основании уравнения Нернста и стандартных окислительно-восстановительных потенциалов.
Диаграмма Пурбе строится в координатах E (ордината) — pH (абсцисса). Она отражает формы, которые термодинамически устойчивы при данном значении рН и окислительно-восстановительного потенциала среды. При меньшем потенциале соответствующая форма может быть восстановлена до нижележащей (если таковая существует), при более высоком — окислена до вышележащей (если таковая существует). Границы между формами существования раствор-твёрдое или раствор-газ обычно зависят от концентрации растворенных форм; г
ru.bywiki.com
Диаграмма Пурбе — Википедия РУ
Диаграмма Пурбе строится в координатах E (ордината) — pH (абсцисса). Она отражает формы, которые термодинамически устойчивы при данном значении рН и окислительно-восстановительного потенциала среды. При меньшем потенциале соответствующая форма может быть восстановлена до нижележащей (если таковая существует), при более высоком — окислена до вышележащей (если таковая существует). Границы между формами существования раствор-твёрдое или раствор-газ обычно зависят от концентрации растворенных форм; границы между формами существования растворённых форм от их концентрации, как правило, не зависят.
Часто на диаграмму Пурбе наносят границы области существования воды. Верхняя из них (E=1.23-0.059pH) соответствует выделению кислорода (то есть при более высоких потенциалах возможно окисление воды до кислорода):
4h3O — 4e- = 4H+ + O2 (pH<7) 4OH- — 4e- = 2h3O + O2 (pH>7)Нижняя граница (E=-0.059pH) соответствует выделению водорода (то есть при меньших потенциалах возможно восстановление воды до водорода):
2H+ + 2e- = h3 (pH<7) 2h3O + 2e- = h3 + 2OH- (pH>7)На иллюстрациях к данной статье область существования воды ограничена голубыми линиями.
Диаграмма Пурбе — мощнейшее средство предсказания направления химических реакций соединений данного элемента. Из неё можно определить условия большинства кислотно-основных и окислительно-восстановительных реакций соединений данного элемента без учета взаимодействия с посторонними ионами. По ней можно предсказать процессы диспропорционирования и конпропорционирования разных форм, возможность выделения ими водорода и кислорода. Сопоставляя диаграммы Пурбе для двух элементов можно предсказать окислительно-восстановительные реакции между их соединениями. Таким образом, диаграмма Пурбе для некоего элемента в сжатой форме отображает его неорганическую химию.
Весьма важное значения диаграммы Пурбе имеют в предсказании коррозии в разных условиях[1].
Ограничения применимости диаграммы Пурбе
Диаграмма Пурбе отображает только термодинамически устойчивые формы. Кинетически устойчивые (они же метастабильные) формы на ней не отображаются. Поэтому она неприменима для предсказания образования метастабильных форм. Например такая форма, как гипохлорит-ион OCl- метастабильна (неустойчива термодинамически, но диспропорционирует крайне медленно). Поэтому на диаграмме Пурбе для хлора её нет и предсказать её образование (в частности, при диспропорционировании хлора) по диаграмме Пурбе невозможно: Cl2 + 2OH- = Cl- + ClO- + h3O Кроме того, далеко не все процессы, предсказаные по диаграмме Пурбе имеют достаточно большую скорость, чтобы быть заметными.
Предсказание гидролиза
Если при каком-то значении рН существует гидроксид, значит, свободный ион при этом значении рН гидролизуется. Пример 1. На диаграмме Пурбе для железа при рН>4 устойчив Fe(OH)3, а Fe3+ неустойчив. Значит, при pH>4 ион Fe3+ будет полностью гидролизоваться: Fe3+ + 3h3O = Fe(OH)3 + 3H+Гидролиз иона Fe3+ идёт при рН<4. Точное значение рН зависит от концентрации иона Fe3+ (размазанная граница).
Предсказание конпропорционирования
Если при данном значении рН две формы разделены третьей, то эти две формы будут конпропорционировать с образованием третьей.Пример 1. На диаграмме Пурбе для марганца при рН 0-3 Mn2+ и MnO4- разделены MnO2. Значит, Mn2+ и MnO4- будут конпрпорционировать:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+Пример 2. На диаграмме Пурбе для марганца при рН 4-7 Mn2+ и MnO4- разделены двумя формами (MnO2, Mn2O3). Это значит, что Mn2+ и MnO4 будут конпропорционировать. При этом возможно два продукта, причем преобладающий продукт зависит от соотношения реагентов или взаимной скорости двух конкурирующих реакций:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+8Mn2+ + 2MnO4- + 7h3O = 5Mn2O3 + 14H+Пример 3. На диаграмме Пурбе для марганца в диапазоне рН 0-14 между MnO2 и MnO4- промежуточных форм нет. Значит, в этом диапазоне рН MnO2 и MnO4- конпропорционировать не будут.
Предсказание диспропорционирования
Если форма в данной степени окисления при данном рН на диаграмме Пурбе отсутствует, значит, она будет диспропорционировать на соседние формы, имеющиеся на диаграмме Пурбе. Пример 1. На диаграмме Пурбе для марганца при рH<14 отсутствует манганат MnO42- (степень окисления марганца +6). Это значит, что при этих рН манганат будет диспропорционировать[2]. Ближайшая устойчивая степень окисления снизу +4 (MnO2), сверху — +7 (MnO4-). Они и будут образовываться при диспропорционировании: 3MnO42- + 2h3O = MnO2 + 2MnO4- + 4OH-Этот процесс, в частности, будет происходить при растворении твёрдого манганата в воде или при подкислении сильнощелочного раствора, в котором манганат устойчив.Пример 2. На диаграмме Пурбе для марганца соединения марганца (+3) отсутствуют вовсе. Это значит, что при растворении в воде соединений марганца (+3) они будут диспропорционировать на ближайшие устойчивые степени окисления +2 снизу (в виде Mn2+) и +4 сверху (в виде MnO2): 2Mn3+ + 2h3O = Mn2+ + MnO2 + 4H+
Предсказание вытеснения водорода
Если область существования данной формы лежит ниже области устойчивости воды (нижняя голубая линия на цветных диаграммах), то данная форма при соответствующих рН способна реагировать с водой, вытесняя водород. Реально вследствие кинетических проблем (то есть малой скорости подобных реакций) возникает т. н. эффект перенапряжения выделения водорода, и для реального выделения водорода соответствующая форма должна лежать ниже области устойчивости воды как минимум на 0.4-0.8В. Кроме того, гидроксиды металлов, как правило, пассивируют металл, поэтому в нейтральных и щелочных средах водород, как правило, не выделяется, даже если область существования металла лежит сильно ниже области устойчивости воды. Пример 1. На диаграмме Пурбе для марганца его область существования лежит заметно ниже нижней границы устойчивости воды. Значит, он способен вытеснять водород: Mn + 2H+ = Mn2+ + h3Это соответствует тому факту, что металл в ряду активности стоит левее водорода.
Предсказание окисления кислородом воздуха
Если область существования некой формы лежит заметно ниже верхней границы устойчивости воды, то эта форма может окисляться кислородом воздуха. При этом образуется форма, которую пересекает верхняя граница устойчивости воды. Пример 1. На диаграмме Пурбе для марганца область существования Mn(OH)2 лежит сильно ниже верхней границы устойчивости воды (верхняя голубая линия). Это значит, что он может быть окислен до Mn3O4, Mn2O3 и, в конце концов, до MnO2 (но не MnO4-, так как эта форма лежит выше области существования воды): 2Mn(OH)2 + O2 = 2MnO2 + 2h3O И действительно, Mn(OH)2 на воздухе очень быстро коричневеет[3]. Пример 2. На диаграмме Пурбе для железа область существования металлического железа лежит намного ниже верхней границы существования воды. Это значит, что оно может быть окислено кислородом до Fe(OH)3, что мы и наблюдаем в процессе ржавления. При этом, поскольку процесс протекает долго, получаются дегидратированные формы (Fe3O4, Fe2O3 и др.), которые более устойчивы термодинамически, но образуются медленно.
Окисление металлов кислородом происходит далеко не всегда за счёт эффекта пассивирования.
Предсказание выделения кислорода
Если некая форма целиком лежит выше области существования воды, она может разлагаться с выделением кислорода. Пример. На диаграмме Пурбе для железа область существования ферратов FeO42- лежит гораздо выше области существования воды (особенно в кислой области). Поэтому при подкислении ферраты разлагаются с выделением кислорода[4]: 4FeO42- + 20H+ = 4Fe3+ + 3O2 + 10h3O
Предсказание окислительно-восстановительных реакций между соединениями двух элементов
Если при некотором рН форма существования одного элемента лежит заметно (хотя бы на 0.2 В) выше формы существования другого элемента, то вышележащая форма окислит нижележащую. При этом образуются формы, область устойчивости которых лежит между ними. Пример. Область существования MnO4- (диаграмма для марганца) лежит выше, чем область существования Fe2+ (диаграмма для железа). Значит,MnO4- может окислять Fe2+. В кислой среде при этом образуется Fe3+ и (в зависимости от соотношения реагентов) MnO2 или Mn2+: MnO4- + 3Fe2+ + 4H+ = MnO2 + 3Fe3+ + 2h3O MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4h3O В нейтральной среде образуются MnO2 и Fe(OH)3:MnO4- + 3Fe2+ + 7h3O = MnO2 + 3Fe(OH)3 + 5H+
http-wikipediya.ru
Измерение рН.
Активность водородных ионов для удобства обычно выражают единицах рН:
рН = —Ig ан+
Следовательно, для реакции 2Н+ + 2е = Н2 полуэлемента давлением водорода 1 ат: Еh3 = —0,0592рН.
Чистая вода содержит ионы H+ и ОН− в разных концентрациях, находящихся в равновесии с недиссоциированной водой, поэтому можно рассчитать активность как водородного иона, так и гидроксид - иона, исходя из константы диссоциации, значение которой при 25 °С составляет 1,01.10 −14. Отсюда совершенно очевидно, что для чистой воды при 25 °С .
рH < 7 – кислая среда; pH > 7 – щелочная среда.
Диаграммы Пурбе.
М. Пурбе предложил представлять термодинамические данные, касающиеся электрохимического и коррозионного поведения металлов в водных средах, в форме компактных сводных диаграмм потенциал — рН. Такие диаграммы составлены для большинства распространенных металлов. Они наглядно показывают условия (области потенциалов и рН), при которых металл термодинамически устойчив (иммунность), либо может реагировать, образуя ионы, оксиды или комплексные соединения, и в этом их преимущество. Но диаграммы содержат только термодинамические данные, поэтому в них отсутствует информация о скоростях реакций.
Диаграммы указывают условия образования на поверхности
электрода диффузионно-барьерных пленок, но не содержат данных об их защитных свойствах в присутствии специфических анионов, таких как или. Они не содержат также сведений о возможности образования пленок нестехиометрического состава. Некоторые из этих пленок существенно влияют на скорость коррозии, однако отчетливо показывают природу стехиометрических соединений, в которые при достижении равновесия могут превратиться любые менее устойчивые соединения. Учитывая вышеупомянутые ограничения, диаграммы весьма полезны
для описания равновесных состояний системы металл-вода
в кислых и щелочных средах как при наложении внешней
поляризации, так и без нее.
Диаграмма Пурбе для железа.
На рисунке каждая линия отвечает условиям термодинамического равновесия для некоторой реакции. Горизонтальные линия соответствуют реакциям, протекающим без участия ионов Н+ или ОН−. Вертикальная линия отвечает равновесию с участием ионов Н+ или ОН−, но без участия электронов. Наклонные линии соответствуют реакциям, в которых участвуют и ионы Н+ или ОН−, и электроны. Например, наклонная линия, разделяющая области существования Fe2+ и Fe2О3, отвечает реакции:
Вертикальный участок линии, разделяющий области существования Fe3+ И Fe2O3 соответствует реакции:
Следует подчеркнуть, что значения рН на диаграмме представляют собой рН растворов, непосредственно контактирующих с поверхностью металла. Эти значения в некоторых случаях, например, для Fe в аэрированной НаО, отличаются от рН в толще раствора.
Область выделения кислорода располагается выше линии b, которая отвечает реакции:
Водород образуется в области ниже линии а, соответствующей реакции:
Растворимые гипоферриты могут образовываться в очень щелочных растворах в узком интервале отрицательных значений потенциала, а растворимые ферраты- в щелочных растворах при очень положительных значениях потенциала, однако область их стабильности недостаточно точно определена.
Когда в реакции помимо Н+ и ОН− принимают участие другие ионы, их активность в общем случае принята равной 10 −6. Таким образом, в согласии c Fe= Fe2+ + 2 e,
ниже горизонтальной линии, проходящей через Е = - 0,62 В, железо практически не корродирует (содержание ионов Fe 2+ в растворе не превышает 10−6 моль/кг).
Области диаграммы, в которых устойчиво существуют Fe3O3 и Fe3O4, иногда называют областями пассивности, исходя из предположения, что на железе при этих значениях Е и рН образуются защитные оксидные пленки. Это справедливо только в той степени, в какой пассивность может быть обусловлена диффузионным барьером, создаваемым оксидным слоем. В реальных условиях в средах типа растворов h3SO4 или HNO3 линия, отвечающая Фладе-потенциалам, выше которых наблюдается пассивность железа, параллельна линиям а и b пересекает Е = 0,6 В при
рН = 0. Это указывает, что пассивирующая пленка видимо не представляет собой равновесный стехиометрический оксид железа.
studfiles.net
Диаграмма Пурбе — википедия орг
Диаграмма Пурбе строится в координатах E (ордината) — pH (абсцисса). Она отражает формы, которые термодинамически устойчивы при данном значении рН и окислительно-восстановительного потенциала среды. При меньшем потенциале соответствующая форма может быть восстановлена до нижележащей (если таковая существует), при более высоком — окислена до вышележащей (если таковая существует). Границы между формами существования раствор-твёрдое или раствор-газ обычно зависят от концентрации растворенных форм; границы между формами существования растворённых форм от их концентрации, как правило, не зависят.
Часто на диаграмму Пурбе наносят границы области существования воды. Верхняя из них (E=1.23-0.059pH) соответствует выделению кислорода (то есть при более высоких потенциалах возможно окисление воды до кислорода):
4h3O — 4e- = 4H+ + O2 (pH<7) 4OH- — 4e- = 2h3O + O2 (pH>7)Нижняя граница (E=-0.059pH) соответствует выделению водорода (то есть при меньших потенциалах возможно восстановление воды до водорода):
2H+ + 2e- = h3 (pH<7) 2h3O + 2e- = h3 + 2OH- (pH>7)На иллюстрациях к данной статье область существования воды ограничена голубыми линиями.
Диаграмма Пурбе — мощнейшее средство предсказания направления химических реакций соединений данного элемента. Из неё можно определить условия большинства кислотно-основных и окислительно-восстановительных реакций соединений данного элемента без учета взаимодействия с посторонними ионами. По ней можно предсказать процессы диспропорционирования и конпропорционирования разных форм, возможность выделения ими водорода и кислорода. Сопоставляя диаграммы Пурбе для двух элементов можно предсказать окислительно-восстановительные реакции между их соединениями. Таким образом, диаграмма Пурбе для некоего элемента в сжатой форме отображает его неорганическую химию.
Весьма важное значения диаграммы Пурбе имеют в предсказании коррозии в разных условиях[1].
Ограничения применимости диаграммы Пурбе
Диаграмма Пурбе отображает только термодинамически устойчивые формы. Кинетически устойчивые (они же метастабильные) формы на ней не отображаются. Поэтому она неприменима для предсказания образования метастабильных форм. Например такая форма, как гипохлорит-ион OCl- метастабильна (неустойчива термодинамически, но диспропорционирует крайне медленно). Поэтому на диаграмме Пурбе для хлора её нет и предсказать её образование (в частности, при диспропорционировании хлора) по диаграмме Пурбе невозможно: Cl2 + 2OH- = Cl- + ClO- + h3O Кроме того, далеко не все процессы, предсказаные по диаграмме Пурбе имеют достаточно большую скорость, чтобы быть заметными.
Предсказание гидролиза
Если при каком-то значении рН существует гидроксид, значит, свободный ион при этом значении рН гидролизуется. Пример 1. На диаграмме Пурбе для железа при рН>4 устойчив Fe(OH)3, а Fe3+ неустойчив. Значит, при pH>4 ион Fe3+ будет полностью гидролизоваться: Fe3+ + 3h3O = Fe(OH)3 + 3H+Гидролиз иона Fe3+ идёт при рН<4. Точное значение рН зависит от концентрации иона Fe3+ (размазанная граница).
Предсказание конпропорционирования
Если при данном значении рН две формы разделены третьей, то эти две формы будут конпропорционировать с образованием третьей.Пример 1. На диаграмме Пурбе для марганца при рН 0-3 Mn2+ и MnO4- разделены MnO2. Значит, Mn2+ и MnO4- будут конпрпорционировать:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+Пример 2. На диаграмме Пурбе для марганца при рН 4-7 Mn2+ и MnO4- разделены двумя формами (MnO2, Mn2O3). Это значит, что Mn2+ и MnO4 будут конпропорционировать. При этом возможно два продукта, причем преобладающий продукт зависит от соотношения реагентов или взаимной скорости двух конкурирующих реакций:3Mn2+ + 2MnO4- + 2h3O = 5MnO2 + 4H+8Mn2+ + 2MnO4- + 7h3O = 5Mn2O3 + 14H+Пример 3. На диаграмме Пурбе для марганца в диапазоне рН 0-14 между MnO2 и MnO4- промежуточных форм нет. Значит, в этом диапазоне рН MnO2 и MnO4- конпропорционировать не будут.
Предсказание диспропорционирования
Если форма в данной степени окисления при данном рН на диаграмме Пурбе отсутствует, значит, она будет диспропорционировать на соседние формы, имеющиеся на диаграмме Пурбе. Пример 1. На диаграмме Пурбе для марганца при рH<14 отсутствует манганат MnO42- (степень окисления марганца +6). Это значит, что при этих рН манганат будет диспропорционировать[2]. Ближайшая устойчивая степень окисления снизу +4 (MnO2), сверху — +7 (MnO4-). Они и будут образовываться при диспропорционировании: 3MnO42- + 2h3O = MnO2 + 2MnO4- + 4OH-Этот процесс, в частности, будет происходить при растворении твёрдого манганата в воде или при подкислении сильнощелочного раствора, в котором манганат устойчив.Пример 2. На диаграмме Пурбе для марганца соединения марганца (+3) отсутствуют вовсе. Это значит, что при растворении в воде соединений марганца (+3) они будут диспропорционировать на ближайшие устойчивые степени окисления +2 снизу (в виде Mn2+) и +4 сверху (в виде MnO2): 2Mn3+ + 2h3O = Mn2+ + MnO2 + 4H+
Предсказание вытеснения водорода
Если область существования данной формы лежит ниже области устойчивости воды (нижняя голубая линия на цветных диаграммах), то данная форма при соответствующих рН способна реагировать с водой, вытесняя водород. Реально вследствие кинетических проблем (то есть малой скорости подобных реакций) возникает т. н. эффект перенапряжения выделения водорода, и для реального выделения водорода соответствующая форма должна лежать ниже области устойчивости воды как минимум на 0.4-0.8В. Кроме того, гидроксиды металлов, как правило, пассивируют металл, поэтому в нейтральных и щелочных средах водород, как правило, не выделяется, даже если область существования металла лежит сильно ниже области устойчивости воды. Пример 1. На диаграмме Пурбе для марганца его область существования лежит заметно ниже нижней границы устойчивости воды. Значит, он способен вытеснять водород: Mn + 2H+ = Mn2+ + h3Это соответствует тому факту, что металл в ряду активности стоит левее водорода.
Предсказание окисления кислородом воздуха
Если область существования некой формы лежит заметно ниже верхней границы устойчивости воды, то эта форма может окисляться кислородом воздуха. При этом образуется форма, которую пересекает верхняя граница устойчивости воды. Пример 1. На диаграмме Пурбе для марганца область существования Mn(OH)2 лежит сильно ниже верхней границы устойчивости воды (верхняя голубая линия). Это значит, что он может быть окислен до Mn3O4, Mn2O3 и, в конце концов, до MnO2 (но не MnO4-, так как эта форма лежит выше области существования воды): 2Mn(OH)2 + O2 = 2MnO2 + 2h3O И действительно, Mn(OH)2 на воздухе очень быстро коричневеет[3]. Пример 2. На диаграмме Пурбе для железа область существования металлического железа лежит намного ниже верхней границы существования воды. Это значит, что оно может быть окислено кислородом до Fe(OH)3, что мы и наблюдаем в процессе ржавления. При этом, поскольку процесс протекает долго, получаются дегидратированные формы (Fe3O4, Fe2O3 и др.), которые более устойчивы термодинамически, но образуются медленно.
Окисление металлов кислородом происходит далеко не всегда за счёт эффекта пассивирования.
Предсказание выделения кислорода
Если некая форма целиком лежит выше области существования воды, она может разлагаться с выделением кислорода. Пример. На диаграмме Пурбе для железа область существования ферратов FeO42- лежит гораздо выше области существования воды (особенно в кислой области). Поэтому при подкислении ферраты разлагаются с выделением кислорода[4]: 4FeO42- + 20H+ = 4Fe3+ + 3O2 + 10h3O
Предсказание окислительно-восстановительных реакций между соединениями двух элементов
Если при некотором рН форма существования одного элемента лежит заметно (хотя бы на 0.2 В) выше формы существования другого элемента, то вышележащая форма окислит нижележащую. При этом образуются формы, область устойчивости которых лежит между ними. Пример. Область существования MnO4- (диаграмма для марганца) лежит выше, чем область существования Fe2+ (диаграмма для железа). Значит,MnO4- может окислять Fe2+. В кислой среде при этом образуется Fe3+ и (в зависимости от соотношения реагентов) MnO2 или Mn2+: MnO4- + 3Fe2+ + 4H+ = MnO2 + 3Fe3+ + 2h3O MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4h3O В нейтральной среде образуются MnO2 и Fe(OH)3:MnO4- + 3Fe2+ + 7h3O = MnO2 + 3Fe(OH)3 + 5H+
www-wikipediya.ru
Диаграмма Пурбэ - Справочник химика 21
Об устойчивости тех или иных состояний системы кадмий — вода п возможности протекания соответствующих реакций можно судить по диаграмме Пурбэ [693, стр. 414], приведенной на рис. 5 (представлены графики зависимости электродных потенциалов Е (в) от pH раствора для реально устанавливающихся равновесий между различными формами кадмия вертикальными прямыми показаны значения pH образования гидратов). [c.21]Зависимость потенциала от pH, изображенная графически, наглядно иллюстрирует область существования доминирующих форм окислительно-восстановительной системы в зависимости от протолитических и окислительно-восстановительных свойств ее и называется диаграммой Пурбэ. Использование таких диаграмм позволяет предсказывать, [c.266]
Из новых материалов для изготовления конденсаторных трубок перспективны титан и сплавы на его основе. О термодинамической устойчивости титана в водных средах можно судить по диаграмме Пурбэ (рис. 2.9). Уравнения электрохимических реакций, по которым построена эта диаграмма, приведены в табл. 2.9. [c.52]
Рис. 1.1. Упрощенная диаграмма Пурбэ (потенциал — pH) для системы железо — НзО при температуре [c.5]
Диаграмма Пурбэ позволяет определить условия термодинамического равновесия между металлом, его иона- [c.5]
| Рис. 1.2. Диаграмма Пурбэ (потенциал — pH) для системы Ре8-НзО |  |
Для определения условий образования отложений необходимо знать, какие соединения меди в условиях эксплуатации систем водяного охлаждения находятся в растворе, а какие выпадают в осадок. Это можно показать с помощью диаграммы Пурбэ (рис. 11.11), рассчитанной из термодинамических данных для системы Си—НзО при 25 и 100 °С [3]. Заштрихованная область соответствует потенциалам и реальным концентрациям медных ионов в дистилляте систем охлаждения действующих ГЭС. Из диаграммы Е—pH видно, что в реальных условиях термодинамически возможно образование только твердого оксида меди, что подтверждается практикой отложения в каналах статоров преимущественно (на 95—97 %) состоят из СиО. [c.213]
Второй случай — водород, присутствующий в растворе в виде (гидратированных) ионов Н+, например, в кислотных средах. Даже в растворах с высоким pH довольно кислая среда может возникать в трещинах и питтингах, где типичное значение pH составляет 1—3,5 [2, 175—178, 298, 306] точное значение pH зависит от произведения растворимости в реакции гидролиза и от вида конкретной диаграммы Пурбэ для данной системы [176, 307]. В этом случае, как показано на рис, 49, б, в результате захвата электронов происходит образование атомов водорода, которые могут либо объединяться, формируя молекулы Нг, удаляющиеся в виде пузырьков газа, либо проникать в металл в виде [Н]. На микроскопическом уровне такой процесс можно, конечно, предотвратить или ослабить путем приложения анодного потенциала, однако процессы у вершины трещины могут изменять локальные потенциалы и приводить к значительному поглощению водорода [178, 297]. [c.128]
Диаграмма Пурбэ для рассмотренной системы изображена на рис. 14.2. [c.267]
Коррозионное поведение железа в крепких щелочах до сих пор не вполне выяснено. Пурбэ [27] на основе термодинамических расчетов для равновесной системы Ре—НгО, содержащей Ог, дал диаграмму потенциал — pH при 25°С. Согласно этой диаграмме, область интересующих нас концентраций электролита (рН>10) от обратимого кислородного потенциала почти до обратимого водородного потенциала должна быть областью пассивности железа. В этой области, где серебряные ДСК-электроды работают как кислородные диффузионные электроды, железо покрыто защитной окисной пленкой. Для рН>11,5 возле обратимого водородного потенциала существует небольшая агрессивная область, в которой железо разрушается с образованием ферритов. Для электролита с pH = 14 эта область охватывает потенциалы от +0,1 до —0,2 в по отношению к обратимому водородному потенциалу в данном растворе. Однако применение диаграммы Пурбэ для практических коррозионных процессов невозможно без оговорок, так как на равновесие влияют растворенные в воде соли, а это влияние еще не вполне ясно. [c.370]
Питтинговая или точечная коррозия (рис. 1.4.1, е), наблюдаемая у металлов и сплавов в пассивном состоянии, связана с разрушением защитной пленки и часто возникает на совершенно гладкой новерхности. Она появляется там, где защитная оксидная пленка на металле подвержена только местному разрушению, а в остальной своей части устойчива к раствору, который воздействует на металл. Область вероятных значений pH при этом, согласно диаграммам Пурбэ, соответствует нейтральной — слабощелочной области. [c.61]
В электрохимическом ряду никель занимает промежуточное положение Ni +/Ni == —0>25 В, поэтому он более благороден, чем цинк и железо, но менее благороден, чем олово, свинец или медь. На рис. 3.5 показана упрощенная равновесная диаграмма потенциал — pH (диаграмма Пурбэ) системы Ni—HjO при 25 С, из анализа которой следует [c.173]
На рис. 18 приведена схема одной из наиболее простых диаграмм Пурбэ для цинка. Линии диаграммы отвечают следующим равновесиям [c.39]
| Рис. 18. Диаграмма Пурбэ для цинка (схематическое изображение) | 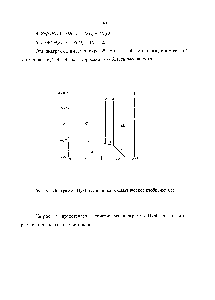 |
| Рис.20. Диаграмма Пурбэ для системы Ре - Я2О при 25 С (гидратированная форма оксидов) | 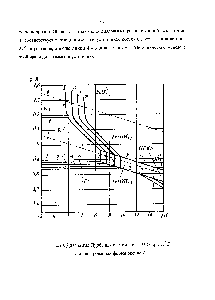 |
Фнг. 33. Диаграмма Пурбэ для железа [47]. [c.73]
Классический пример прогноза термодинамической вероятности коррозии — диаграммы Пурбэ, показывающие характер зависимости электродного потенциала от pH среды. Применение диаграмм э.д.с. — pH для прогнозирования коррозии описано в работе [101]. В этой работе представлена программа для ЭВМ, позволяющая получать диаграммы Пурбэ для любой системы, если известны термодинамические свойства составляющих ее веществ. [c.177]
| Рис. 1. Упрощенная диаграмма Пурбэ (потенциал — pH) для железа температура 25°С [2]. | ![Рис. 1. Упрощенная диаграмма Пурбэ (потенциал — pH) для железа температура 25°С [2].](/800/600/http/chem21.info/pic2/076175195139045213083099088093219084043222134147.png) |
Пурбэ [47, 49] измерил, собрал и рассчитал термодинамические характеристики для реакций между многими металлами и водой. На основании этих характеристик в комбинации с данными о растворимостях окисей и гидроокисей, а также с константами равновесия протекающих при этом реакций были построены диаграммы Пурбэ, которые указывают термодинамически стойкие фазы в зависимости от электродного потенциала и pH среды. [c.74]
Упрощенные диаграммы Пурбэ для цинка и хрома представлены на фиг. 35а и 356. Цинк подвергается коррозии в широком диапазоне значений pH, так как образует катионы при pH 9 и оксианионы в щелочных средах, как об этом уже упоминалось. Твердая пленка стабильна на хроме в более широком диапазоне значений pH, но не при благородных потенциалах, так как в последнем случае образуются растворимые шестивалентные ионы хрома и коррозия возникает во всем диапазоне значений pH. [c.76]
Диаграммы Пурбэ обеспечивают прочную термодинамическую основу для понимания процессов коррозии. Однако эти диаграммы нельзя безоговорочно считать единственным руководством, которому Можно слепо следовать при объяснении и предсказании поведения металлов. При использовании этих диаграмм имеются два прин- [c.76]
| Фиг. 35а. Упрощенная диаграмма Пурбэ для цинка [47]. | ![Фиг. 35а. Упрощенная диаграмма Пурбэ для цинка [47].](/800/600/http/chem21.info/pic2/021145241164209227096010143198237117251034189157.png) |
Диаграммы позволяют предсказать пути повышения коррозионной стойкости металлов. Пусть необходимо найти условия, при которых коррозия металла в воде практически не происходит, т. е. к моменту наступления равновесия количество продуктов коррозии очень мало (например, не более 10 моль л-1). Тогда по энтальпиям образования можно для различных pH рассчитать равновесные потенциалы всех возможных реакций в системе металл — вода (учитывая, что активности продуктов реакции равны 10 моль д-1). Если по полученным данным построить диаграмму, то по ней можно найти граничные условия стабильности различных продуктов реакции для области иммунности (устойчивое состояние металла), коррозии (металл переходит в ионное состояние), пассивности (стабильны некоторые труднорастворимые продукты реакции, главным образом окислы). В частности, диаграммы Пурбэ позволяют определить потенциалы и кислотности раствора, при которых возможны катодная или анодная защита, самопас-сивация, ингибирование с помощью добавки. Прим. перев.) [c.788]
На рис. 2.10 дана упрощенная диаграмма Пурбэ для системы А1—Н2О. Сплошными линиями (/—5) на диаграмме ограничены области, в которых вероятен процесс образования на алюминии оксидных пленок в зависимости от pH. Пунктирные линии указывают пределы стабильности воды. Анализ диаграммы Е — pH позволяет определить условия, при которых термодинамически возможна коррозия алюминия с образованием AF+ при низких значениях pH и АЮг при высоких значениях pH, а также условия возникновения пассивного состояния при образовании пленок гидраргилита АЬОз-ЗНгО (при почти нейтральных значениях pH) либо условия отсутствия коррозии при больших отрицательных потенциалах металла. Следует иметь в виду, что в представленной диаграмме не учитывается влияние ионов-активаторов на коррозию алюминия в нейтральных водных средах. [c.54]
Из анализа полученных данных и диаграммы Пурбэ систеш п- 1 0 сделан вывод, что обсувдаемая коррозия, олова обусловлена протеканием двух сопряженных реакций - катодного восстановления 5/702 негферывно образующейся на поверхности металла за счет химического взаимодействия его с перекисью водорода по следующим уравнениям [c.21]
Таким образом, эта линия отражает условия возникновения твердых нерастворимых продуктов коррозии. Нерастворимым продуктом коррозии в данном случае считается такой продукт реакции, который находится в равновесии с концентрацией Ре " в растворе, равной 10 N. Выше указанной линии располагается область существования нерастворимых продуктов коррозии, дающих в растворе концентрацию Ре ниже 10" . Такая область на диаграммах Пурбэ называется областью пассивности. В этой области металл термодинамически неустойчив, но вследствие образования нерастворимых продуктов реакции коррозионный процесс в некоторых условиях может блокироваться. Небольшая вторая область коррозии находится у правого края диаграммы и относится к случаю образования ферратов железа (НРеОа) в сильнощелочных растворах. Две наклонные пунктирные прямые, относятся нижняя (в) к равновесию Н + е На, верхняя (г) — к равновесию О2 + 2е + Н.р 20Н", т. е., другими словами, они характеризуют зависимость потенциала водородного и соответственно кислородного электродов от pH. [c.8]
Фиг1 34. Упрощенная форма диаграммы Пурбэ для железа [47]. [c.75]
Полное описание фиг. 33 выходит за рамки данной. книги. Поэтому на более простой диаграмме (фиг. 34) представлены три различные области диаграммы Пурбэ, охватывающие коррозию, имму-нитет и пассивность. [c.76]
chem21.info