Урок 2. Относительная атомная масса химических элементов. Атомная относительная масса хрома
Относительная атомная масса элемента - Ида Тен
Абсолютные массы атомов
Одним из фундаментальных свойств атомов, является их масса. Абсолютная (истинная) масса атома – величина чрезвычайно малая. Взвесить атомы на весах невозможно, поскольку таких точных весов не существует. Их массы были определены с помощью расчетов.
Например, масса одного атома водорода равна 0,000 000 000 000 000 000 000 001 663 грамма! Масса атома урана – одного из самых тяжелых атомов, составляет приблизительно 0,000 000 000 000 000 000 000 4 грамма.
Записывать и читать эти числа непросто; можно ошибиться, пропустив ноль или добавить лишний. Существует другой способ записи – в виде произведения: 4 ∙ 10−22 (22 – количество нулей в предыдущем числе).
Точное значение массы атома урана – 3,952 ∙ 10−22 г, а атома водорода, самого легкого среди всех атомов, – 1,673 ∙ 10−24 г.
Производить расчеты с малыми числами неудобно. Поэтому вместо абсолютных масс атомов используют их относительные массы.
Относительная атомная масса
О массе любого атома можно судить, сравнивая ее с массой другого атома (находить отношение их масс). С момента определения относительных атомных масс элементов использовались различные атомы в качестве сравнения. Своеобразными эталонами для сравнения в свое время были атомы водорода и кислорода.
Единая шкала относительных атомных масс и новая единица атомной массы, принята Международным съездом физиков (1960) и унифицирована Международным съездом химиков (1961).
По сегодняшний день эталоном для сравнения является 1/12 часть массы атома углерода. Данное значение называют атомной единицей массы, сокращенно а.е.м
Атомная единица массы (а.е.м.) – масса 1/12 части атома углерода

Сравним, во сколько раз отличается абсолютная масса атома водорода и урана от 1 а.е.м., для этого разделим эти числа одно на другое:

Полученные при расчетах значения и являются относительными атомными массами элементов – относительно 1/12 массы атома углерода.
Так, относительная атомная масса водорода приблизительно равна 1, а урана – 238. Обратите внимание, что относительная атомная масса не имеет единиц измерения, так как при делении единицы измерения абсолютных масс (граммы) сокращаются.
Относительные атомные массы всех элементов указаны в Периодической Системе химических элементов Д.И. Менделеева. Символ, при помощи которого обозначают относительную атомную массу – Аr (буква r – сокращение от слова relative, что означает относительный).
Значения относительных атомных масс элементов используются во многих расчетах. Как правило, значения, приведенные в Периодической Системе, округляются до целых чисел. Обратите внимание, что элементы в Периодической Системе размещены в порядке увеличения относительных атомных масс.
Например, при помощи Периодической Системы определим относительные атомные массы ряда элементов:
Ar(O) = 16; Ar(Na) = 23; Ar(P) = 31.Относительную атомную массу хлора принято записывать равной 35,5!Ar(Сl) = 35,5
- Относительные атомные массы пропорциональны абсолютным массам атомов
- Эталоном для определения относительной атомной массы является 1/12 часть массы атома углерода
- 1 а.е.м. = 1,662 ∙ 10−24 г
- Относительную атомную массу обозначают Ar
- Для расчетов значения относительных атомных масс округляют до целых, исключение – хлор, для которого Ar = 35,5
- Относительная атомная масса не имеет единиц измерения
idaten.ru
Масса атома. Относительная атомная масса
ОПРЕДЕЛЕНИЕ
Железо - двадцать шестой элемент Периодической таблицы. Обозначение - Fe от латинского «ferrum». Расположен в четвертом периоде, VIIIB группе. Относится к металлам. Заряд ядра равен 26.
Железо - самый распространенный после алюминия металл на земном шаре: оно составляет 4% (масс.) земной коры. Встречается железо в виде различных соединений: оксидов, сульфидов, силикатов. В свободном состоянии железо находят только в метеоритах.
К важнейшим рудам железа относятся магнитный железняк Fe 3 O 4 , красный железняк Fe 2 O 3 , бурый железняк 2Fe 2 O 3 ×3H 2 O и шпатовый железняк FeCO 3 .
Железо - серебристый (рис. 1) пластичный металл. Оно хорошо поддается ковке, прокатке и другим видам механической обработки. Механические свойства железа сильно зависят от его чистоты - от содержания в нем даже весьма малых количеств других элементов.
Рис. 1. Железо. Внешний вид.
Атомная и молекулярная масса железа
Относительной молекулярная масса вещества (M r) - это число, показывающее, во сколько раз масса данной молекулы больше 1/12 массы атома углерода, а относительная атомная масса элемента (A r) — во сколько раз средняя масса атомов химического элемента больше 1/12 массы атома углерода.
Поскольку в свободном состоянии железо существует в виде одноатомных молекул Fe значения его атомной и молекулярной масс совпадают. Они равны 55,847.
Аллотропия и аллотропные модификации железа
Железо образует две кристаллические модификации: α-железо и γ-железо. Первая из них имеет кубическую объемноцентрированную решетку, вторая - кубическую гранецентрированную. α-Железо термодинамически устойчиво в двух интервалах температур: ниже 912 o С и от 1394 o С до температуры плавления. Температура плавления железа равна 1539 ± 5 o С. Между 912 o С и от 1394 o С устойчиво γ-железо.
Температурные интервалы устойчивости α- и γ-железа обусловлены характером изменения энергии Гиббса обеих модификаций при изменении температуры. При температурах ниже 912 o С и выше 1394 o С энергия Гиббса α-железа меньше энергии Гиббса γ-железа, а в интервале 912 — 1394 o С - больше.
Изотопы железа
Известно, что в природе железо может находиться в виде четырех стабильных изотопов 54 Fe, 56 Fe, 57 Fe и 57 Fe. Их массовые числа равны 54, 56, 57 и 58 соответственно. Ядро атома изотопа железа 54 Fe содержит двадцать шесть протонов и двадцать восемь нейтронов, а остальные изотопы отличаются от него только числом нейтронов.
Существуют искусственные изотопы железа с массовыми числами от 45-ти до 72-х, а также 6 изомерных состояний ядер. Наиболее долгоживущим среди вышеперечисленных изотопов является 60 Fe с периодом полураспада равным 2,6 млн. лет.
Ионы железа
Электронная формула, демонстрирующая распределение по орбиталям электронов железа выглядит следующим образом:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 4s 2 .
В результате химического взаимодействия железо отдает свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион:
Fe 0 -2e → Fe 2+ ;
Fe 0 -3e → Fe 3+ .
Молекула и атом железа
В свободном с
overmedic.ru
Список элементов по атомной массе | Virtual Laboratory Wiki
Это список химических элементов отсортированных по относительной атомной массе, с наиболее стабильными изотопами для искусственно полученных элементов. Цветом закодирован тип элемента. В таблице приведены атомный номер, название, символ химического элемента, а также группа и период элементов. Число в круглых скобках даёт неопределённость в последних цифрах (см. «краткое примечание» на IUPAC). Например, 1.00794 (7) означает 1.00794 ± 0.00007. Для искусственных элементов атомная масса приводится для наиболее устойчивого изотопа в квадратных скобках.
- ↑ 1,001,011,021,031,041,051,061,071,081,091,101,111,121,131,141,151,161,171,181,191,201,211,221,231,241,251,261,271,281,291,301,311,321,331,341,351,361,371,38Изотопический состав этого элемента изменяется по некоторым геологическим экземплярам, и изменение может превысить ошибку, заявленную в таблице.
- ↑ 2,02,12,22,32,42,52,62,7Изотопический состав элемента может измениться в коммерческих материалах, что приводит к значительному отклонению атомного веса от данного значения.
- ↑ 3,003,013,023,033,043,053,063,073,083,093,103,113,123,133,14Изотопический состав изменяется в земных материалах так, что более точный атомный вес нельзя указать.
- ↑ Атомный вес коммерческого лития может измениться между 6.939 и 6.996 — необходим анализ определенного материала, ятобы найти более точное значение.
- ↑ 5,005,015,025,035,045,055,065,075,085,095,105,115,125,135,145,155,165,175,185,195,205,215,225,235,245,255,265,275,285,295,305,315,325,335,345,35Элемент не имеет никаких устойчивых изотопов, и значение в скобках, например [209], указывает массовое число самого долго живущего нуклида. Однако, три элемента: торий, протактиний и уран, имеют характерный земной изотопический состав и, поэтому, для них приведены стандартные атомные веса.
Эта страница использует содержимое раздела Википедии на русском языке. Оригинальная статья находится по адресу: Список элементов по атомной массе. Список первоначальных авторов статьи можно посмотреть в истории правок. Эта статья так же, как и статья, размещённая в Википедии, доступна на условиях CC-BY-SA .
ru.vlab.wikia.com
Относительная атомная масса элемента в химии и история её определения :: SYL.ru
В процессе развития науки химия столкнулась с проблемой подсчёта количества вещества для проведения реакций и полученных в их ходе веществ.
На сегодня для подобных расчётов химической реакции между веществами и смесями используют значение относительной атомной массы, внесённой в периодическую таблицу химических элементов Д. И. Менделеева.
Химические процессы и влияние доли элемента в веществах на ход реакции
Современная наука под определением «относительная атомная масса химического элемента» подразумевает, во сколько раз масса атома данного химического элемента больше одной двенадцатой части атома углерода.
С зарождением эры химии потребность в точных определениях хода химической реакции и её результатов росла. Поэтому химики постоянно пытались решить вопрос о точных массах взаимодействующих элементов в веществе. Одним из лучших решений на то время была привязка к самому лёгкому элементу. И вес его атома был взят за единицу.
Исторический ход подсчёта вещества
Изначально использовался водород, затем кислород. Но этот способ расчёта оказался неточным. Причиной тому послужило наличие в кислороде изотопов с массой 17 и 18.
Поэтому, имея смесь изотопов, технически получали число, отличное от шестнадцати. На сегодня относительная атомная масса элемента рассчитывается исходя из принятого за основу веса атома углерода, в соотношении 1/12.
Дальтон заложил основы относительной атомной массы элемента
Лишь спустя некоторое время, в 19-м веке, Дальтон предложил вести расчёт по самому лёгкому химическому элементу – водороду. На лекциях своим студентам он демонстрировал на вырезанных из дерева фигурках, как соединяются атомы. По другим элементам он использовал данные, ранее полученные другими учёными.
По экспериментам Лавуазье в воде содержится пятнадцать процентов водорода и восемьдесят пять процентов кислорода. Имея эти данные, Дальтон рассчитал, что относительная атомная масса элемента, входящего в состав воды, в данном случае кислорода, составляет 5,67. Ошибочность его расчётов связана с тем, что он считал неверно относительно количества атомов водорода в молекуле воды.
По его мнению, на один атом кислорода приходился один атом водорода. Воспользовавшись данными химика Остина о том, что в составе аммиака 20 процентов водорода и 80 процентов азота, он рассчитал, чему равна относительная атомная масса азота. Имея этот результат, он пришёл к интересному выводу. Получалось, что относительная атомная масса (формула аммиака ошибочно была принята с одной молекулой водорода и азота) составляет четыре. В своих расчетах ученый опирался на периодическую систему Менделеева. По анализу он рассчитал, что относительная атомная масса углерода - 4,4, вместо принятых до этого двенадцати.
Несмотря на свои серьёзные промашки, именно Дальтон первым создал таблицу некоторых элементов. Она претерпела неоднократные изменения ещё при жизни учёного.
Изотопная составляющая вещества влияет на значение точности относительного атомного веса
При рассмотрении атомных масс элементов можно заметить, что точность по каждому элементу разная. К примеру, по литию она четырёхзначная, а по фтору - восьмизначная. Проблема в том, что изотопная составляющая каждого элемента своя и непостоянна. Например, в обычной воде содержится три типа изотопа водорода. В их число, кроме обычного водорода, входит дейтерий и тритий.
Относительная атомная масса изотопов водорода составляет соответственно два и три. «Тяжёлая» вода (образованная дейтерием и тритием) испаряется хуже. Поэтому в парообразном состоянии изотопов воды меньше, чем в жидком состоянии.
Избирательность живых организмов к различным изотопам
Живые организмы обладают селективным свойством по отношению к углероду. На построение органических молекул используют углерод с относительной атомной массой, равной двенадцати. Поэтому вещества органического происхождения, а также ряд полезных ископаемых, таких как уголь и нефть, содержат меньше изотопной составляющей, чем неорганические материалы.Микроорганизмы, перерабатывающие и накапливающие серу, оставляют после себя изотоп серы 32. В зонах, где бактерии не перерабатывают, доля изотопа серы - 34, то есть гораздо выше. Именно на основании соотношения серы в породах почвы геологи приходят к выводу о природе происхождения слоя - магматическую природу он имеет или же осадочную.
Из всех химических элементов только один не имеет изотопов - фтор. Поэтому его относительная атомная масса более точная, чем других элементов.
Существование в природе нестабильных веществ
У некоторых элементов относительная масса указана в квадратных скобках. Как видно, это элементы, расположенные после урана. Дело в том, что они не имеют устойчивых изотопов и распадаются с выделением радиоактивного излучения. Поэтому в скобках указан наиболее устойчивый изотоп. Со временем выяснилось, что у некоторых из них возможно получить в искусственных условиях устойчивый изотоп. Пришлось менять в периодической таблице Менделеева атомные массы некоторых трансурановых элементов.
В процессе синтеза новых изотопов и измерения их продолжительности жизни порой удавалось обнаружить нуклиды с продолжительностью полураспада в миллионы раз дольше.
Наука не стоит на месте, постоянно открываются новые элементы, законы, взаимосвязи различных процессов в химии и природе. Поэтому, в каком виде окажется химия и периодическая система химических элементов Менделеева в будущем, лет через сто, - является туманным и неопределённым. Но хочется верить, что накопленные за прошедшие века труды химиков послужат новому, более совершенному знанию наших потомков.
www.syl.ru
Урок 2. Относительная атомная масса химических элементов – HIMI4KA
В уроке 2 «Относительная атомная масса химических элементов» из курса «Химия для чайников» рассмотрим разные способы выражения массы химических элементов. Напоминаю, что в прошлом уроке «Атомы и химические элементы» мы рассмотрели, кто и когда высказал идею о том, что все вокруг состоит из атомов; также выяснили, что из себя представляет химический элемент и каким образом обозначается.

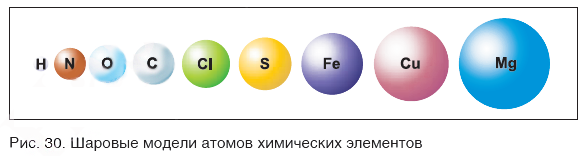
Чем различаются атомы разных элементов между собой? Вы уже знаете: массой, размерами и строением. На рисунке 30 показаны шаровые модели атомов некоторых химических элементов, конечно, не в реальных размерах, а многократно увеличенные. В действительности атомы настолько малы, что их невозможно рассмотреть даже в самые лучшие оптические микроскопы.
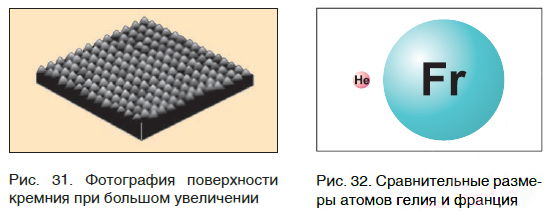
На заметку: В конце XX в. у ученых появились более совершенные микроскопы, позволяющие достигать увеличения в несколько десятков миллионов раз. Они называются туннельными микроскопами. На рисунке 31 показана фотография поверхности кремния. На ней отчетливо видны отдельные атомы, расположенные на поверхности этого вещества.
Размеры и масса атомов
Современная наука обладает методами, позволяющими определять размеры и массы атомов. Так, например, самый легкий атом — атом водорода. Его масса равна 0,0000000000000000000000000016735 кг. Самым маленьким является атом гелия He. Диаметр этого атома равен приблизительно 0,00000000098 м. Записывать и читать такие числа затруднительно, поэтому обычно их представляют в более удобном виде: 1,6735·10−27 кг и 9,8·10−10 м. Атомы большинства химических элементов по своим размерам значительно больше атома гелия. Самый большой из них — атом элемента франция Fr. Его диаметр в 7 раз больше диаметра атома гелия (рис. 32).
Еще больше различаются атомы разных элементов по массе. Масса атома обозначается символом ma и выражается в единицах массы СИ (кг). Так, например, масса атома углерода равна: ma(С) = 19,94·10−27 кг, а атома кислорода — ma(О) = 26,56·10−27 кг. Масса атома самого тяжелого из существующих на Земле элементов — урана U — почти в 237 раз больше массы атома водорода.
Атомная единица массы
Пользоваться такими маленькими величинами масс атомов при расчетах неудобно. К тому же, когда в XIX в. начало формироваться атомно- молекулярное учение, ученые еще не представляли реальных размеров и масс атомов. Поэтому на практике вместо истинных масс атомов стали применять их относительные значения. Они рассчитывались по массовым отношениям простых веществ в реакциях друг с другом. Химики предположили, что эти отношения пропорциональны массам соответствующих атомов. Именно так в начале XIX в. Дж. Дальтон ввел понятие относительной атомной массы, приняв за единицу сравнения массу самого легкого атома — водорода.

В настоящее время в качестве такой единицы сравнения используется 1/12 часть массы атома углерода (рис. 33). Она получила название атомной единицы массы (а. е. м.). Ее международное обозначение — u (от английского слова «unit» — единица):
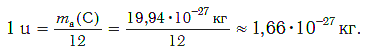
Атомная единица массы — это 1/12 часть массы атома углерода, которая равна 1,66·10−27 кг.
Относительная атомная масса
Сравнивая средние массы атомов различных элементов с атомной единицей массы, получают значения относительных атомных масс химических элементов.
Относительная атомная масса элемента — это физическая величина, которая показывает, во сколько раз масса атома данного химического элемента больше 1/12 части массы атома углерода.
Относительная атомная масса обозначается символами Ar (А — первая буква английского слова «atomic» —атомный, r — первая буква английского слова «relative», что значит относительный), следовательно:

где Х — символ данного элемента.
Например, относительная атомная масса водорода:

а кислорода:
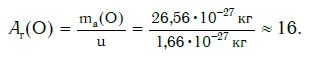
Как видите, относительная атомная масса показывает, во сколько раз масса атома данного элемента больше атомной единицы массы u.
В таблице Менделеева приведены относительные атомные массы всех элементов. В расчетах при решении задач мы будем пользоваться округленными до целых значениями этих величин (см. урок 1).
Внимание! Очень часто относительную атомную массу называют просто атомной массой. Однако следует отличать атомную массу — величину относительную (например, Ar(О) = 16) — от массы атома — величины, выражаемой в единицах массы — килограммах (ma(O) = 26,56·10−27 кг) или атомных единицах массы (ma(O) = 16·u).
Пример. Во сколько раз атом ртути тяжелее атома кальция?
Решение. Относительные атомные массы элементов равны: Ar(Hg) = 201 и Ar(Ca) = 40.
Масса атома ртути равна: ma(Hg) = Ar(Hg)·u (кг).Масса атома кальция равна: ma(Са) = Ar(Са)·u (кг).

Другими словами, отношение масс атомов этих элементов равно отношению их относительных атомных масс. Следовательно, отношение масс атомов ртути и кальция равно:
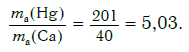
Ответ: в 5,03 раза.
Краткие выводы урока:
- Атомная единица массы представляет собой 1/12 часть массы атома углерода.
- Относительная атомная масса химического элемента равна отношению массы его атома к 1/12 части массы атома углерода.
- Относительная атомная масса химического элемента является величиной безразмерной и показывает, во сколько раз масса атома данного элемента больше атомной единицы массы.
Надеюсь урок 2 «Относительная атомная масса химических элементов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
himi4ka.ru
Атомные массы химических элементов
|
|
raal100.narod.ru
Химический элемент. Относительная атомная масса. Простые и сложные вещества - Предмет химии. Первоначальные химические понятия - ХИМИЯ 8 КЛАСС КОНТРОЛЬНЫЕ ИЗМЕРИТЕЛЬНЫЕ МАТЕРИАЛЫ
Раздел 1. Предмет химии. Первоначальные химические понятия
Химический элемент. Относительная атомная масса. Простые и сложные вещества
Вариант 1
1. О кислороде как о простом веществе говорится в суждении:
1) в состав молекул угарного газа входят углерод и кислород;
2) кислород входит в состав воды;
3) в сернистом газе 50% кислорода;
4) кислород мало растворим в воде.
2. О сере как о химическом элементе говорится в суждении:
1) сера не растворяется в воде;
2) сера входит в состав мазей, применяемых при кожных заболеваниях;
3) молекулы серы состоят из восьми атомов;
4) относительная атомная масса серы больше, чем относительная атомная масса кислорода.
3. Относительная атомная масса калия равна:
1) 20;
2) 19;
3) 39;
4) 40.
4. Относительная атомная масса калия больше, чем относительная атомная масса:
1) натрия;
2) кальция;
3) железа;
4) мышьяка.
5. К простым веществам относится вещество, формула которого:
1) SO2;
2) NaOH;
3) CuO;
4) N2.
6. К сложным веществам относится каждое из двух веществ, формулы которых:
1) NO2и S8;
2) NaOH и СаСO3;
3) СuО и Аl;
4) N2 и h3SO4.
Вариант 2
1. О кислороде как о химическом элементе говорится в суждении:
1) кислород — газ без цвета и запаха;
2) молекулы кислорода состоят из двух атомов;
3) молекулы сахарозы образованы углеродом, кислородом и водородом;
4) в результате фотосинтеза образуется кислород.
2. О железе как о простом веществе говорится в суждении:
1) железо входит в состав гемоглобина;
2) железо входит в состав различных сплавов;
3) относительная атомная масса железа больше, чем относительная атомная масса хрома;
4) порядковый номер железа в таблице Д.И. Менделеева равен 26.
3. Относительная атомная масса углерода равна:
1) 16;
2) 6;
3) 12;
4) 32.
4. Относительная атомная масса у кислорода больше, чем:
1) у фосфора;
2) у углерода;
3) у хлора;
4) у алюминия.
5. К простым веществам относится каждое из двух веществ, формулы которых:
1) Mg и h3S;
2) O3и Аl;
3) S8и K2SiO3;
4) Nh4 и Аl2O3.
6. К сложным веществам относится вещество, формула которого:
1) F2;
2) Сu;
3) СаО;
4) Mg.
Вариант 3
1. Разделите на две равные группы суждения:
1) из алюминия изготавливают посуду;
2) алюминий занимает 3-е место по распространённости в земной коре;
3) алюминий хорошо проводит электрический ток;
4) алюминий входит в состав глины;
5) алюминий лёгкий и пластичный;
6) валентность алюминия постоянна.
Укажите признак, по которому проведено деление.
2. Используя офисное приложение Excel, составьте диаграмму, отражающую изменение относительных атомных масс химических элементов:
1) 2-го периода;
2) VIIА группы.
3. Укажите формулу лишнего вещества в каждой группе:
1) HNO2, Аl2O3, Са, К2O;
2) N2, К, N2O5, Fe.
Ответ объясните.
www.compendium.su