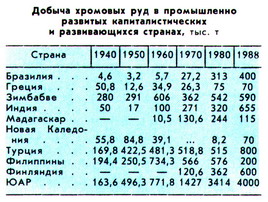
3.2 Соль Рейнеке. 3 хрома
§3. Хром (III) (d3).
3.1. Общая характеристика комплексных соединений хрома (III).
Степень окисления +3 наиболее характерна для хрома. Для этого состояния характерно большое число кинетически устойчивых комплексов. Именно из-за такой кинетической инертности удалось выделить в твердом состоянии большое число комплексных соединений хрома, которые в растворе остаются неизменными в течение длительного времени.
Наличие трех неспаренных электронов обусловливает парамагнетизм соединений Cr(III), большинство из которых интенсивно окрашены.7
В литературе описано множество комплексов трехвалентного хрома. Во всех без исключения комплексах CrIII имеет координационное число (КЧ) шесть.
Ярко выраженная способность трехвалентного хрома к образованию комплексных соединений особенно отчетливо проявляется в его различных комплексных продуктов присоединения аммиака.
В соответствии со своим КЧ 6 ион хрома (III) может координационно связать шесть молекул аммиака. При этом образуется комплексный ион [Cr(Nh4)6]3+, заряд которого совпадает с зарядом хрома, фигурирующего в качестве центрального атома, поскольку молекулы аммиака не заряжены.
Вследствие прочного связывания молекул аммиака при растворении в воде соединений, содержащих комплекс [Cr(Nh4)6]3+, не происходит моментального распада комплекса – он существует в растворе как ион и лишь постепенно происходит замещение аммиака молекулами воды.
[Cr(Nh4)6]3+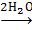 [Cr(h3O)2(Nh4)4]3+
[Cr(h3O)2(Nh4)4]3+ [Cr(h3O)4(Nh4)2]3+
[Cr(h3O)4(Nh4)2]3+ [Cr(h3O)6]3+
[Cr(h3O)6]3+
Исследования поведения гексаакваиона хрома (III) в растворах соляной кислоты во времени, позволили установить, что равновесие в системе Cr3+-h3O-Cl-8 устанавливается примерно 3,5 месяца. Комплексообразование в этих растворах протекает последовательно по ступеням во времени:
[Cr(h3O)6]3+
Спектры поглощения растворов показывают, что даже в самом концентрированном относительно соляной кислоты растворе (12 н) комплексообразование заканчивается на третьей ступени.
Таким образом, реакция внедрения ионов хлора в координационную сферу комплекса протекает крайне медленно, инертными являются не только гексааквокомплекс, но и смешанные аквахлориды хрома (III) по отношению к реакции обмена молекул воды на хлорид-ионы, происходящего в процессе образования комплексов; инертность смешанных комплексов уменьшается с увеличением числа ионов хлора в координационной сфере комплекса.
Процессы акватации транс- и цис- дихлородиэтилендиамминхроми-хлорида:
[Cr(en)2Cl2]+ [Cr(en)2Cl(h3O)]2+
[Cr(en)2Cl(h3O)]2+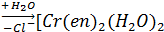
Гидроксил может образоваться из молекулы воды, содержащейся во внутренней координационной сфере, в результате отщепления протона. Вероятность образования гидроксила во внутренней координационной сфере растет при повышении рН и уменьшается при понижении рН. Поэтому прибавление кислоты понижает вероятность образования гидроксила во внутренней координационной сфере и, следовательно замедляет процессы акватации именно тех ацидокомплексов, во внутренней координационной сфере которых содержится молекула воды. Если же во внутренней координационной сфере нет молекулы воды, то такого рода влияние величины рН исключается.
Достаточно широко исследовано влияние ионов Cr2+ на процессы акватации ацидохроми-комплексов. Оказалось, что ионы Cr2+ катализируют процессы акватации изученных ацидохроми-комплексов.
Например, каталитический процесс акватации транс-дихлородиаминхроми-хлорида протекает следующим образом. Вероятно, катализатор образует промежуточный комплекс, в котором связь между атомами Cr2+ и Cr3+ осуществляется через ион хлора:
транс-[CrIII(en)2Cl2]+ + [CrII(h3O)6]2+ [Cl(en)2CrIII,II – Cl – CrII,III(h3O)5]3+.
[Cl(en)2CrIII,II – Cl – CrII,III(h3O)5]3+.
После передачи электрона может произойти распад комплекса. Наиболее вероятен распад по связи CrII – Cl:
[Cl(en)2CrII-Cl-CrIII(h3O)5]3+ → [Cl(en)2CrII(h3O)]+ + [ClCrIII(h3O)5]2+,
освободившееся координационное место у CrII заняла молекула воды.
Замена во внутренней сфере одних лигандов другими часто сопровождается отчетливым изменением окраски комплекса.
Ион [Cr(h3O)6]3+ поглощает свет в красной, голубой частях видимого спектра, а также в ближайшей ультрафиолетовой области, поэтому имеет фиолетовую окраску, вызванную наложением двух дополнительных цветов.
Известно много комплексных анионов состава [CrX6]3-, где Х – монодентатный лиганд типа F-, Cl-, NCS-, CN-, или часть полидентатного аниона типа оксалата (C2O42-). Существует, разумеется, множество смешанных ацидоамино- и и ацидоакво- комплексов.
Проведем некоторую их классификацию9:
1) [Cr(Nh4)6]3+, [Cr(Nh4)5(h3O)]3+, [Cr(Nh4)4(h3O)2]3+, [Cr(Nh4)3(h3O)3]3+, [Cr(Nh4)2(h3O)4]3+, [Cr(h3O)6]3+
2) [Cr(Nh4)5Cl]2+, [Cr(Nh4)4(h3O)Cl]2+, [Cr(Nh4)3(h3O)2Cl]2+, [Cr(Nh4)2(h3O)3Cl]2+, [Cr (h3O)5Cl]2+
3) [Cr(Nh4)4(SCN)2]+, [Cr(Nh4)3(h3O)(SCN)2]+, [Cr(Nh4)2(h3O)2(SCN)2]+, [Cr(h3O)4(SCN)2]+
4) [Cr(Nh4)3(OH)3], [Cr(Nh4)2(h3O)(OH)3], [Cr(h3O)3(OH)3]
5) [Cr(Nh4)2(SCN)4]-, [Cr(h3O)2(SCN)4]-
6) [Cr(h3O)(SCN)5]2-
7) [CrCl6]3-
Важно заметить, что во всех рядах отсутствуют моноамминные соединения, и отсутствуют только они, указывает на существование какой-то закономерности, проявляющейся в неспособности к существованию моноамминных соединений.
 Большой интерес представляют соединения типа: [CrAm4R2]+ [CrAm2R4]-. Из соединений первого типа известны главным образом соединения этилендиамина. Они интересны ввиду наблюдающегося у них явления изомерии (стереоизомерии)10.
Большой интерес представляют соединения типа: [CrAm4R2]+ [CrAm2R4]-. Из соединений первого типа известны главным образом соединения этилендиамина. Они интересны ввиду наблюдающегося у них явления изомерии (стереоизомерии)10.
В случае этилендиаминных соединений различие заключается еще и в том, что в противоположность транс-соединению цис-соединение представляет собой смесь двух оптически активных форм, поскольку, как видно из рис. 4, в этом случае могут существовать две цис-формы, относящиеся друг к другу, как предмет к его зеркальному отражению.
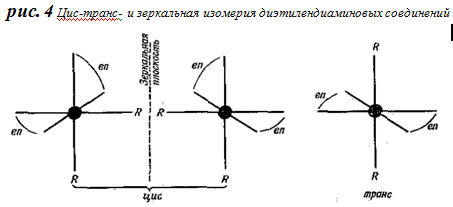
Переходя к рассмотрению второго типа соединений, нужно подчеркнуть, что поскольку в состав комплекса входят четыре отрицательных эквивалента, он представляет собой анион и образует соли с металлами. Хорошо известно соединение, принадлежащее к данному классу, так называемая соль Рейнеке Nh5[Cr(NCS)4(Nh4)2]×h3O, анион которой часто применяют для осаждения больших катионов, как органических, так и неорганических, соль Рейнеке удобно использовать для количественного определения меди, так как можно легко провести осаждение последней в форме Cu[Cr(NCS)4(Nh4)2], не удаляя из раствора другие металлы (кроме Ag, Hg, Tl). Реакция с солью Рейнеке может служить также и как очень чувствительная качественная проба на медь.
studfiles.net
3.6 Получение комплексных соединений хрома (III).
Соединения хрома (III) инертны, т.е. реакции замещения в их растворах протекают с низкой скоростью. Инертные комплексы не удается синтезировать по реакциям обмена в водных растворах. Для получения инертных комплексов либо используют очень большой избыток лиганда, что, например, достигается проведением реакции аминирования непосредственно в жидком аммиаке:
CrCl3+6Nh4(ж.) [Cr(Nh4)6]Cl3
[Cr(Nh4)6]Cl3
либо проводят окислительно-восстановительную реакцию:
4[Cr(Nh4)6]Cl2+2Nh5Cl+O2=2[(Nh4)5Cr(OH)Cr(Nh4)5]Cl5↓+6Nh4
§4. Высшие состояния окисления хрома.
4.1. Соединения хрома (IV) (d2).
Соединения хрома (IV) часто выступают в роли интермедиатов при восстановлении хроматов (VI) или окисления солей хрома (III). Как правило, они обладают низкой устойчивостью и не имеют практического значения.
Известны комплексные фториды состава МCrF5 и М2CrF6. Они имеют магнитный момент порядка 3,1 μВ и построены из октаэдров [CrF6]2-.
4.2 Соединения хрома (V) (d1).
Степень окисления +5 для хрома неустойчива – в настоящее время известно около трех десятков соединений, лишь половина из которых способна существовать в водном растворе. Являясь интермедиатами, соединения хрома (V) могут быть зафиксированы методом электронного парамагнитного резонанса. Введение в раствор α-г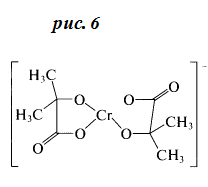 идроксикарбоновых кислот позволяет
идроксикарбоновых кислот позволяет
стабилизировать ситуацию благодаря возникновению устойчивых хелатов (см. рис. 6).
Это используют для изучения механизмов реакций восстановления хроматов в водных растворах. Например, с помощью хелатных соединений было доказано, что реакция хромата (VI) с иодид-ионами протекает как последовательность трех одноэлектронных переносов:
Cr(VI) → Cr(V) → Cr(IV) → Cr(III).
Единственным доказательством в пользу существования соединений CrV в растворе было получено при попытке растворить хроматы (VI) в 65%-ном олеуме. Данные о количестве выделившегося О2 и о магнитных свойствах образующегося голубого раствора согласуются с представлением об образовании CrV.
4.3 Соединения хрома (VI) (d0).
Галогенидные комплексы типа [МX6+x]x- неизвестны, поэтому координационная химия хрома в этой степени окисления относится в основном к оксо- и пероксокомплексам.
Соединения хрома (VI) очень широко известны, в качестве сильных окислителей они активно используются в технике и лабораторной практике.
§5. Практическая часть.
Синтез соли Рейнеке Nh5[Cr(NCS)4(Nh4)2]×h3O.
В настоящей работе была синтезирована соль тетрароданодиамминхромат (III) аммония, соль Рейнеке.
5.1 Реактивы, используемые в работе.
Для проведения синтеза соли использовали бихромат аммония, роданид аммония квалификации «х.ч.».
5.2 Синтез соли Рейнеке.
Растереть в ступке 8,5 г Бихромата аммония и 10 г Роданида аммония в тонкую смесь. Оставшиеся 40 г роданида аммония нагреть в фарфоровой чашке до 160ºС (при этом наблюдается его плавление) и, не допуская нагрева выше 160ºС (иначе происходит разложение соли), добавить смесь бихромата и роданида аммония маленькими порциями (по 0,6-0,9 г), постоянно помешивая расплав термометром. Температуру поддерживать постоянно160ºС. После добавления очередной порции смеси наблюдается выделение газа (аммиак Nh4-ТЯГА!) и разогрев расплава. Идет реакция:
(Nh5)2Cr2O7+8 Nh5CNS=2Nh5[Cr(CNS)4(Nh4)2]×h3O +2Nh4↑+ N2↑+5 h3O.
Дальнейшее нагревание смеси необязательно, т.к. выделяющейся энергии достаточно для поддержания температуры 160°С. После добавления всей смеси остудить расплав, постоянно помешивая термометром. После застывания смесь ещё теплой растереть в порошок и залить 37мл ледяной воды. Через 15 мин отфильтровать раствор и остаток без промывания растворить в 125 мл воды, нагретой до 60ºС.18 Не допускать нагревания раствора выше 65°С, т.к. при этом соль Рейнеке разлагается, что сопровождается посинением раствора и выделением газа (синильная кислота НСN – ТЯГА!!!).
Nh5[Cr(Nh4)2(NCS)4]×h3O  HCN↑+S↓+3Nh4↑+Cr(NCS)3+h3O
HCN↑+S↓+3Nh4↑+Cr(NCS)3+h3O
Отфильтровать горячий раствор и фильтрат оставить на ночь в холодильнике. Выпавшие кристаллы отфильтровать и высушить.
Соль Рейнеке легко разлагается под действием ультрафиолетового и видимого света, поэтому на протяжении всех стадий отчистки соли Рейнеке желательно препятствовать попаданию прямого солнечного света на растворы и твёрдые вещества, содержащие её, посредством оборачивания ёмкостей, содержащих их, алюминиевой фольгой. Хранить соль в бюксе, обёрнутом фольгой.
studfiles.net
3.2 Соль Рейнеке.
3.2.1 Общие сведения.
Из тетрацидодиаминовых комплексов хрома (III) наиболее давно известным является соль эмпирического состава Cr(NCS)3×Nh5SCN×2Nh4×2h3O. Координационная формула этого соединения представляется в виде Nh5[Cr(NCS)4(Nh4)2]×h3O. Соль эта, следовательно, может быть рационально названа тетрароданодиамминхромиат аммония.
Однако как эту соль, так и другие, образующиеся из нее путем замены аммония на другие катионы, часто называют просто солями Рейнеке. Свободную кислоту Н[Cr(NCS)4(Nh4)2], которая может быть получена при взаимодействии Ba[Cr(NCS)4(Nh4)2]2 с разбавленной серной кислотой, также часто называют кислотой Рейнеке. В литературе даже встречается иногда и термин «рейнекат» («рейнекеат»), применяемый для обозначения солей Рейнеке.
Пространственное строение данной соли было выяснено с помощью рентгеноструктурного анализа.
Оказалось, что молекулы аммиака расположены в транс-положении друг к другу11. В этой же работе было также показано, что в анионе соли Рейнеке роданогруппа связана с хромом через атом азота.12
Получены также производные иона тетрароданодиамминхрома (III), содержащие вместо одной роданогруппы остаток ОН-, т.е. соли типа М[Cr(Nh4)2(NCS)3OH]. Также получены диоксалатодиамминхромиаты типа Me[CrPy2(NCS)4] и другие аналогичные соли.
3.2.2 Применение.
Как уже отмечалось, соль Рейнеке довольно широко применяется в аналитической химии, для определения ионов меди, серебра, ртути, кадмия и висмута образуя пучки тонких игл. На серебро, как правило, используют соль Рейнеке в сочетании с тиомочевинной, образуется осадок состава: [Ag(SCN2h5)2]×[Cr(Nh4)2(SCN)4], предел обнаружения 0,4 мкг, предел разбавления 1:2500 (г/г).
Также она применяется и в органическом анализе, например для определения никотина13, атропина14, морфина15:

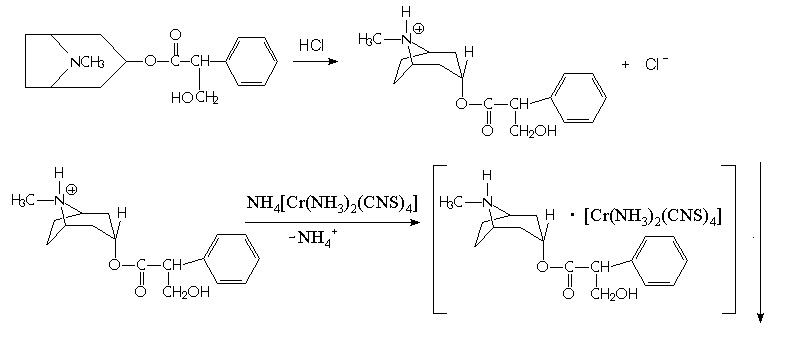
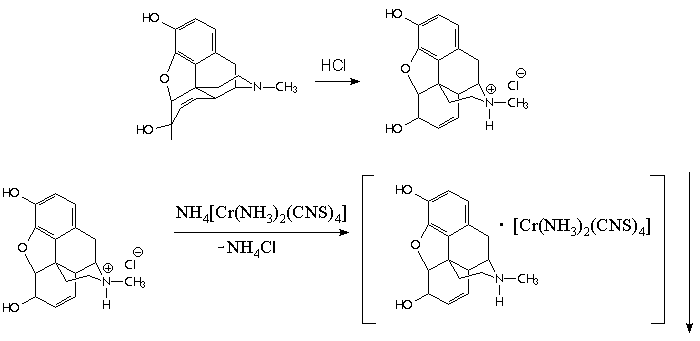
Сведения о соединениях содержащих анион [Cr(Nh4)2(NCS)4]- достаточно ограничены, не смотря на то, что тетраизотиоцианатодиамминхроматные комплексы могут обладать рядом специфических свойств.
3.3 Многоядерные комплексы хрома (III)
Многоядерные амминные комплексы хрома (III) содержат несколько центральных атомов хрома. В большинстве случаев они связаны между собой ОН-группами.
Важнейшими представителями двухъядерных комплексов являются так называемые родо- и эритрохромовые соли и соли ди-μ-гидроксодихрома (III).
Магнитные моменты биядерных комплексов зависят от температуры, а их значения несколько ниже, чем обычные для октаэдрического CrIII, что указывает на слабое антиферромагнитное взаимодействие через изогнутые мостики Cr-O(H)-Cr. Более сильное антиферромагнитное взаимодействие обнаружено у [(Nh4)5Cr(μ-OH)Cr(Nh4)5]X5:
[(Nh4)5Cr(μ-OH)Cr(Nh4)5]5+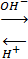 [(Nh4)5Cr-O-Cr(Nh4)5]4+
[(Nh4)5Cr-O-Cr(Nh4)5]4+
красный синий
Линейный мостик Cr-O-Cr, очевидно, допускает спаривание d-электронов двух атомов металла посредством dπ-pπ – связей намного легче, чем изогнутый мостик Cr-O(H)-Cr.
Гидролизованные полиядерные комплексы CrIII имеют большое значение в промышленном получении красителей и дубильных веществ. В первом случае они служат протравкой для красителя. В производстве кожи необходимо обрабатывать шкуры животных для предотвращения гниения, чтобы они были мягкими после высушивания. После вымачивания в серной кислоте шкуры насыщают раствором, содержащим CrIII. Раствор постепенно делают щелочным, при этом образуются полиядерные комплексы и связывают мостиками соседние цепочки белков, в основном координируясь к их карбоксильным группам.
studfiles.net