Графическое заполнение валентных энергетических слоев | Электронные конфигурации атомов. Указать особенности электронных конфигураций меди и хрома
При выборе задания исходить из того, что задала преподаватель на уст.Лекции!!! введение
Химия является одной из важнейших естественных наук. Без знания химии немыслимо понимание процессов превращения веществ, совершенствование и создание новых, в том числе, экологически чистых процессов, машин, приборов, установок, создание веществ и материалов, которых нет в природе.
Химизация народного хозяйства приносит большой экономический эффект. Знание законов химии и их использование, выбор оптимального пути процесса исключительно важны для повышения эффективности производства и качества продукции. Знание химии позволяет решать энергетические, сырьевые и экологические проблемы, являющиеся актуальными в любом производстве, бизнесе и жизни.
В методических указаниях кратко изложены основные разделы курса общей химии, представлены решения типовых задач и контрольные задания для студентов заочного отделения.
За основу в методических указаниях взято учебное пособие Глинка Н.Л. «Задачи и упражнения по общей химии»/под ред. В.А.Рабиновича и Х.М. Рубинной – 22-е изд. стереотипное. Также использован материал из методического пособия Бережной А.И. «Программа, методические указания, решение типовых задач и контрольные задания для студентов-заочников инженерно-технических специальностей вузов».
1.СТРОЕНИЕ АТОМА
1.1. Электронная структура атомов. Зависимость свойств элементов строения их атомов
При решении вопросов, связанных с электронной структурой атомов, следует исходить из того, что любое устойчивое состояние электрона в атоме характеризуется определенными значениями квантовых чисел n, l, m и s. Состояние электрона в атоме, отвечающее определенным значениям квантовых чисел n, l и m, называется атомной электронной орбиталью.
Каждая атомная орбиталь (АО) характеризуется определенным распределением в пространстве волновой функции j, квадрат которой определяет вероятность обнаружения электрона в соответствующей области пространства. Атомные орбитали, которым отвечают значения l, равные 0, 1, 2 и 3, называются соответственно s-, p-, d- и f- орбиталями. В графических схемах электронного строения атомов каждая орбиталь обозначается символом ÿ.
Согласно принципу Паули, в атоме не может быть двух электронов, характеризующихся одинаковым набором квантовых чисел. Из этого следует, что каждая атомная орбиталь может быть занята не более чем двумя электронами, причем их спиновые квантовые числа должны быть различными, что символически обозначают так: ↓↑
Устойчивому (невозбужденному) состоянию многоэлектронного атома отвечает такое распределение электронов по АО, при котором энергия атома минимальна. Поэтому АО заполняются в порядке последовательного возрастания их энергий (при этом не должен нарушаться принцип Паули!). Порядок заполнения электронами АО определяется правилами Клечковского, которые учитывают зависимость энергии орбитали от значений как главного (n), так и орбитального (l) квантовых чисел. Согласно этим правилам, АО заполняются электронами в порядке последовательного увеличения суммы n+l (1-е правило Клечковского), а при одинаковых значениях этой суммы – в порядке последовательного возрастания главного квантового числа n (2-е правило Клечковского).
Размещение электронов по АО в пределах одного энергетического подуровня определяется правилом Хунда, согласно которому минимальной энергии атома соответствует такое распределение электронов по АО данного подуровня, при котором абсолютное значение суммарного спина атома максимально; при любом другом размещении электронов атом будет находиться в возбужденном состоянии, т. е. будет характеризоваться более высокой энергией.
Электронными аналогами называются элементы, у которых валентные электроны расположены на орбиталях, описываемых общей для всех элементов формулой. В периодической системе элементов электронные аналоги входят в состав одной подгруппы.
Энергией ионизации называют энергию, которую нужно затратить для отрыва электрона от атома с превращением последнего в положительно заряженный ион. Энергию ионизации обычно выражают в электрон-вольтах (эВ).
Энергию ионизации можно определять, бомбардируя атомы электронами, ускоренными в электрическом поле. Наименьшую разность потенциалов, при которой скорость электрона становится достаточной для ионизации атомов, называют потенциалом ионизации атомов данного элемента. Потенциал ионизации (I), выраженный в вольтах (В), численно равен энергии ионизации (Е), выраженной в электрон-вольтах.
При затрате достаточной энергии можно удалить из атома два, три и более электрона. Первый потенциал ионизации соответствует энергии отрыва первого электрона, второй – энергии отрыва второго электрона и т. д.
По мере последовательного отрыва электронов от атома положительный заряд образующегося иона возрастает. Поэтому для удаления каждого последующего электрона требуется большая затрата энергии, так что последовательные потенциалы ионизации атома (I1, I2, I3, …) возрастают. Это видно на примере атомов бериллия, бора и углерода:
Ве В С
I1 9,3 8,3 11,3
I2 18,2 25,2 24,4
I3 253,9 37,9 47,9
Особенно резко возрастает потенциал ионизации при отрыве электрона с главным квантовым числом меньше, чем у предыдущего электрона. Так, в случае Ве (1s2 2s2) разность между I1 и I2 намного меньше, чем между I1и I3. это связано с большей затратой энергии на удаление третьего электрона, находящегося, в отличие от двух предыдущих, на более близком от ядра расстоянии.
При прочих равных условиях потенциал ионизации тем больше, чем больше заряд ядра и меньше радиус атома или иона. С этой точки зрения в периоде с ростом заряда ядра должна наблюдаться тенденция к возрастанию потенциала ионизации (при удалении электрона с одним и тем же главным квантовым числом). Действительно, значения I1 и I2 для Ве меньше, чем соответствующие значения для С.
Но, кроме того, потенциал ионизации зависит и от электронной конфигурации атома или иона. В частности, полностью или наполовину заполненные подуровни обладают повышенной устойчивостью. Из сравнения электронных конфигураций рассматриваемых атомов
Be 1S2 2S2; В 1S2 2S22р1 ; С 1S2 2S22Р2
следует, что наиболее устойчива электронная конфигурация атома Ве (полностью заполненный 2s-подуровень), поэтому на его ионизацию затрачивается повышенная энергия. У бора, несмотря на возрастание заряда ядра, отрыв 2р-электрона требует меньшей затраты энергии, чем отрыв 2s-электрона от атома бериллия.
Задачи
Сколько значений магнитного квантового числа возможно для электронов энергетического подуровня, орбитальное квантовое число которого ??
Какое максимальное число электронов может содержать атом в электронном слое с главным квантовым числом ?
Определить по правилу Клечковского последовательность заполнения электронных орбиталей, характеризующихся суммой n+l: а) 5; б) 6; в) 7.
Указать порядковый номер элемента, у которого: а) заканчивается заполнение электронами орбиталей 4d; б) начинается заполнение подуровня 4p.
Какой подуровень заполняется в атомах после подуровня 5s?
У какого элемента начинает заполняться подуровень 4f? У какого элемента завершается заполнение этого подуровня?
Какой подуровень заполняется в атомах после заполнения подуровня 5p?После заполнения подуровня 5d?
Записать электронные формулы атомов электронов с зарядами ядра: а) 8; б) 13; в) 18; г) 23; д) 53; е) 63; ж) 83. Составить графические схемы заполнения электронами валентных орбиталей этих атомов.
Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации: а) ; б); в); г); д); е); ж); З.); и).
Сколько вакантных 3d-орбиталей имеют возбужденные атомы: а) Cl; б) V; в) Mn?
Сколько неспаренных электронов содержат невозбужденные атомы: а) В; б) S; в) As; г) Cr; д) Hg; е) Eu?
Составить электронно–графические схемы ионов и. Чем можно объяснить особую устойчивость электронной конфигурации иона? Указать особенности электронных конфигураций атомов меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?
Структура валентного электронного слоя атома элемента выражается формулой: а) ; б). Определить порядковый номер и название элемента.
Электронная структура атома описывается формулой . Какой это элемент?
Написать электронные формулы ионов: а) ; б); в); г); д);е).
У элементов каких периодов электроны внешнего слоя характеризуются значением n+l=5?
Перечислить электронные аналоги среди элементов VI группы периодической системы элементов. Написать в общем виде электронные формулы валентных электронных подуровней атомов этих элементов.
На каком основании хром и сера, фосфор и ванадий расположены в одной группе периодической системы? Почему их помещают в разных подгруппах?
Почему медь имеет меньший атомный объем, чем калий, расположенный в той же группе и в том же периоде?
Для атома углерода значение последовательных потенциалов ионизации составляют (в В): I1=11,3, I2=24,4, I3=47,9, I4=64, I5=392. Объяснить: а) ход изменения потенциалов ионизации; б) чем вызван резкий скачок при переходе от I4 к I5.
Энергии ионизации атомов благородных газов составляют (в эВ): He – 24,6; Ne – 21,6; Ar – 15,8; Kr – 14,0; Xe – 12,1; Rn – 10,8. объяснить ход измерения энергии ионизации в этой подгруппе.
Значения первых потенциалов ионизации элементов I группы периодической системы элементов соответственно равны (в В): Li – 5,4; Cs – 3,9; Cu – 7,7; Ag – 9,2. Указать: а) у элементов какой подгруппы I группы металлические свойства выражены более резко; б) чем объяснить различный ход изменения значений потенциалов ионизации в подгруппах.
Одинакова ли энергия ионизации атома цезия и атома лития, у какого валентный электрон предварительно возбужден на 6s-подуровень? Ответ обосновать.
Как изменяется с ростом порядкового номера значение первого потенциала ионизации у элементов второго периода? Чем объяснить, что первый потенциал ионизации атома Ве больше, чем атомов Li и B?
Объяснить ход изменения энергии ионизации (в эВ) в ряду Mg – Al – Si:
Mg Al Si
7,6 6,0 8,2
15,0 18,8 16,3
80,1 28,4 33,5
studfiles.net
5. Электронная структура атомов и периодическая система химических элементов д.И.Менделеева
Как было установлено в первой половине XX века, состояние электрона в атоме (его энергия, форма, размер и ориентация орбиты при движении вокруг ядра, а также вращение электрона вокруг собственной оси) характеризуется определенными значениями четырех квантовых чисел - n, l, т и s.
Главное квантовое число п, принимающее целочисленные значения 1, 2, 3, и т. д., «задает» (квантует) энергию электрона в атоме (Е ~ п2) и размер электронного облака: с ростом п обе названные характеристики увеличиваются.
Состояние электрона с определенным значением главного квантового числа называют энергетическим уровнем. При этом различают первый энергетический уровень (n = 1), второй (п = 2) и т. д. Электроны, отвечающие одинаковым значениям п, образуют электронные облака примерно одинаковых размеров, которые принято называть электронными слоями или электронными оболочками. В зависимости от величины п (1, 2, 3, 4, 5, 6, 7) различают слои (или оболочки), обозначаемые буквами K, L, M, N, O, P, Q.
Как и энергия электрона в атоме, форма его облака тоже не может быть любой (она определяется величиной орбитального квантового числа l). Число l может принимать значения от 0 до п-1. Это значит, что при заданном значении главного квантового числа орбитальное квантовое число может принимать п разных значений, иначе говоря, возможно п различных вариантов формы электронного облака. Как оказалось, энергия электрона зависит не только от п, но и от l. По этой причине состояния электрона, отвечающие определенным значениям орбитального квантового числа, называют энергетическими подуровнями. Для электронов разных энергетических подуровней введены особые обозначения: s, p, d, f, которым отвечают значения l, равные, соответственно, 0, 1,2,3. Самой низкой энергией при заданном главном квантовом числе обладают s-электроны, затем следуют p-электроны, затем - d- и f-электроны. Состояния электрона с заданными значениями главного и орбитального квантовых чисел записывают следующим образом: 2р, 3d, 4f. Считается, что электронное облако s-электронов имеет сферическую форму, у р-электронов - ган-телевидную, у d- и f-электронов - еще более сложную. Форма электронного облака важна с точки зрения образования химических связей.
Ориентация электронного облака в пространстве квантуется магнитным квантовым числом т. Это квантовое число принимает все целочисленные значения в пределах от - l до + l, т. е. при заданном l возможно (2l+1) значение т. С этим квантовым числом связывают магнитный момент, возникающий при орбитальном движении электрона в атоме. Состояния электрона с заданными значениями n, l и т называют электронной орбиталью. Для s-электронов т=0, следовательно, нет никакого квантования ориентации сферически симметричного электронного облака в пространстве. Для p-электронов существует 3 различных ориентации облака, для d-электронов - 5, для f-электронов - 7. В многоэлектронных атомах энергия электрона зависит и от значения магнитного квантового числа.
Cпиновое квантовое число s принимает два значения (и) и квантует вращение электрона вокруг собственной оси в двух взаимно противоположных направлениях.
В соответствии с принципом Паули, у многоэлектронного атома не может быть двух электронов, у которых одинаковыми были бы все четыре квантовых числа. Это значит, что любая электронная орбиталь может быть занята только двумя электронами, спиновые квантовые числа которых имеют противоположные знаки. Два таких электрона называются спаренными, но на некоторых орбиталях могут располагаться неспаренные электроны. Орбиталь с двумя спаренными электронами, обладающими противоположно направленными спинами, обозначается клеточкой с двумя взаимно противоположными стрелками внутри нее.
Порядок заполнения атомных орбиталей электронами подчиняется правилам Клечковского: заполнение происходит в порядке увеличения суммы п+l (1-е правило), а при одинаковых значениях этой суммы - в порядке увеличения главного квантового числа п (2-е правило).
При постоянном значении l (т. е. в пределах подуровня) электроны заполняют максимально возможное число орбиталей (правило Хунда). Это означает, что стабильным будет такое состояние атома, при котором суммарное значение спина максимально (т. е. когда спины всех электронов, находящихся на данном подуровне, параллельны). В соответствии с этими правилами, заполнение электронами электронных орбиталей многоэлектронных атомов происходит в следующем порядке: . Одной и двумя чертами подчеркнуты случаи, когда в точном соответствии со 2-м правилом Клечковского заполняются сначала орбитали предыдущего уровня:3d, а не 4p; 4d, а не 5p; 4f, a не 5d; 5f, а не 6d, хотя в двух последних случаях из-за близости энергий орбиталей 4f и 5d, с одной стороны, и орбиталей 5f и 6d, с другой стороны, заполнение f-орбиталей может приостанавливаться, и электронами могут заполняться d-орбитали. Это наблюдается, например, у гадолиния в ряду лантаноидов и для кюрия в ряду актинидов. Отчасти это объясняется тем, что наибольшей стабильностью, а значит, меньшей энергией, отличаются состояния с полностью или наполовину (гадолиний и кюрий) заполненными атомными орбиталями. Именно этим объясняется инертность благородных газов, у которых полностью заполненными являются не только внутренние, но и внешние (валентные) орбитали. Максимальное число электронов на энергетическом уровне равно 2n2.
Электронная структура атома указывает последовательность заполнения атомных орбиталей по мере увеличения их энергии, а также число электронов на той или иной орбитали. Так, электронные структуры атомов азота, кислорода и фтора записываются, соответственно, следующим образом: 1s22s22p3 1s22s22p4 и 1s22s12p5. У всех этих трех атомов имеется по два электрона (указывается верхним индексом после обозначения орбитали) на орбиталях 1s и 2s, тогда как на орбитали 2р у азота 3 электрона, у кислорода - 4, а у фтора - 5. При ионизации (отрыв электрона от атома при сообщении последнему определенной энергии, называемой энергией ионизации) атом приобретает электронную конфигурацию своего предшественника, т. е. атома, расположенного в периодической системе на одну клеточку раньше. Энергия ионизации может быть определена при облучении атомов ускоренными в электрическом поле внешними электронами. При этом наименьшая разность потенциалов, при которой осуществляется ионизация атома, называется потенциалом ионизации. Поскольку образовавшийся в результате ионизации атома ион будет сильнее удерживать своим электростатическим полем оставшиеся электроны, потенциал каждой последующей ионизации всегда больше. В ряду элементов одной группы потенциал ионизации падает с ростом порядкового номера элемента, что обусловлено увеличением радиусов атомов и ионов, а, следовательно, уменьшением силы электростатического притягивания внешних электронов к ядрам атомов. Элементы с полностью или наполовину заполненными электронными подуровнями обладают повышенными потенциалами ионизации.
Пример 5.1. Записать электронную формулу атома хлора.
Решение:
Порядковый номер атома хлора – 17. Он имеет 17 электронов. Они распределяются следующим образом по орбиталям: 1s22s22p63s23p5.
Ответ: Электронная формула атома хлора 1s22s22p63s23p5.
Пример 5.2. Написать электронную формулу иона О2-. Какому элементу она соответствует?
Решение.
Порядковый номер атома кислорода - 8. Ему отвечает электронная конфигурация 1s22s22р4. У иона О2- на 2 электрона больше, чем у атома кислорода. Значит, электронная конфигурация иона О2- будет следующей: 1s22s22p6, эта конфигурация соответствует заполненной конфигурации атома Ne.
Ответ: Электронная конфигурация иона О2- - 1s22s22p6, она соответствует заполненной конфигурации атома Ne.
Пример 5.3. Определить максимально возможное число электронов на М-уровне.
Решение:
Обозначению М-уровень отвечает значение главного квантового числа n=3. При данном значении n возможно 3 значения орбитального квантового числа l: 0, 1 и 2. Им отвечают 1, 3 и 5 орбиталей, соответственно, т. е. в совокупности 9 орбиталей. На каждой из них, в соответствии с принципом Паули, могут размещаться по 2 электрона, следовательно, всего на М-уровне может разместиться 2*9 = 18 электронов. В свою очередь 18 = 2*9 = 2*32 = 2*n2.
Ответ: Максимальное число электронов, которое может разместиться на М-уровне, равно 18 (или 2*n2).
Задачи
5.1. Сколько значений магнитного квантового числа возможно для электронов энергетического подуровня, орбитальное квантовое число которого:
1) l = 2;
2) l = 3.
5.2. Записать электронные формулы атомов элементов с зарядом ядра:
1) 8;
2) 13;
3) 18;
4) 23;
5) 53;
6) 63;
7) 83.
Составить графические схемы заполнения электронами валентных орбиталей этих атомов.
5.3. Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации:
1) 1р3;
2) Зр6;
3) 3s2;
4) 2s2;
5) 2d5;
6) 5d2;
7) 3f12;
8) 2р4;
9) Зр7.
5.4. Сколько вакантных 3d-орбиталей имеют возбужденные атомы:
1) С1;
2) V;
3) Мn?
5.5. Сколько неспаренных электронов содержат невозбужденные атомы:
1) В;
2) S;
3) As;
4) Сr;
5) Hg;
6) Еu.
5.6. Составить электронно-графические схемы ионов Fe2+ и Fe3+. Чем объяснить особую устойчивость электронной конфигурации Fe3+?
5.7. Структура внешнего электронного слоя атома элемента выражается формулой:
1) 5s25p4;
2) 3d54s2.
Определить порядковый номер и название элемента.
5.8. Электронная структура атома описывается формулой 1s22s22p63s23p63d64s2. Какой это элемент?
5.9. Написать электронные формулы ионов:
1) Sn2+;
2) Sn4+;
3) Мп2+;
4) Сu2+;
5) Сг3+;
6) S2-.
5.10. У элементов каких периодов электроны внешнего слоя характеризуются значением n + l= 5?
5.11. Для атома углерода значения последовательных потенциалов ионизации составляют: I1, = 11,3 B; I2 = 24,4 В; I3 = 47,9; B I4 = 64 B; I5 = 392 B. Объяснить:
1) ход изменения потенциалов ионизации;
2) чем вызван резкий скачок при переходе от I4 к I5?
5.12. Указать особенности электронных конфигураций атомов меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?
5.13. Энергии ионизации (в вольтах, В) атомов благородных газов составляют: Не – 24,6; Ne – 21,6; Аг – 15,8; Кг – 14,0; Хе – 12,1; Rn – 10,8. Объяснить ход изменения энергии ионизации в этой группе.
5.14. Каково максимальное число электронов на 3- и 4-м энергетических уровнях? На каких подуровнях размещаются электроны в 3- и 4-м энергетических уровнях?
5.15. Дать мотивированный ответ, какой из подуровней заполняется электронами раньше: 5s или 4d, 3d или 4s?
5.16. Написать электронные формулы атомов элементов с порядковыми номерами 21, 35, 43.
5.17.Написать электронные формулы атомов элементов с порядковыми номерами 17, 29, 41.
5.18. Назвать элементы 4-, 5- и 6-го периодов, у атомов которых d-орбитали полностью заполнены электронами, и написать электронные формулы их атомов.
5.19. Каковы электронные структуры:
1) атома железа и иона железа Fe3+;
2) Ni0, Ni2+, Ni3+;
3) Sn2+, Sn4+, Sn0.
5.20. Определить, пользуясь правилом Клечковского, последовательность заполнения электронных орбиталей, характеризующихся суммой (n+l), равной:
1) 4;
2) 5;
3) 6;
4) 7.
5.21. Сколько электронов на внешней орбитале следующих ионов:
1) Pb+4;
2) I-1;
3) I+3;
4) Br+5.
5.22. Какое максимальное число электронов могут занимать s-, р-, 4d- и f- орбитали данного энергетического уровня. Почему? Напишите электронную форму атома элемента с порядковым номером 31.
5.23. Какие орбитали атома заполняются электронами раньше 4d или 5s; 6s или 5р? Почему? Напишите электронную форму атома элемента с порядковым номером 43.
5.24. Составьте электронные формулы атомов элементов с порядковыми номерами 14 и 40. Сколько свободных 3d-орбиталей у атома последнего элемента?
5.25. Составьте электронные формулы атомов элементов с порядковыми номерами 21 и 23. Сколько свободных 3d-орбиталей в атомах этих элементов?
studfiles.net
Электронные конфигурации атомов | Задачи 183
Задача 183. Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации: а) 1р3 б) 3p6 в) 3s2; г) 2s2; д) 2d5; е) 5d2; ж) 3f12; з) 2р4 и) 3p7.Решение:а) Электронная конфигурация 1p3 не реализуется, потому что первый энергетический уровень (n = 1 ) содержит только s-подуровень. Максимальное число электронов на каждом энергетическом уровне равно 2n2, где n - главное квантовое число. Так на первом энергетическом уровне (n = 1) может находиться максимальное число электронов 2(2 .12 = 2). Следовательно, не только неправильно указан подуровень, но общее число электронов.
б) 3p6 – электронная конфигурация возможна, потому что на третьем энергетическом уровне содержатся s-, p- и d-подуровни. На p-подуровне содержится три атомные орбитали, а в каждой орбитали, согласно правилу Хунда, может находиться максимальное число электронов равное двум. Поэтому на 3p-подуровне может максимально находиться шесть электронов (3 . 2 = 6).
в) Электронная конфигурация 3s2 верна, потому что на третьем энергетическом уровне (n = 3) находятся s-, p- и d-подуровни. Согласно правилу Хунда, на s-подуровне, состоящем из одной атомной орбитали, может находиться максимальное число электронов равное двум.
г) Электронная конфигурация 2s2 реализуется, потому что на втором энергетическом уровне (n = 2) содержатся s- и p-подуровни, и на s-подуровне, в его единственной атомной орбитали, может содержаться максимальное число электронов равное двум.
д) Электронная конфигурация 2d5 не реализуется, потому что во втором энергетическом уровне (n = 2) d-подуровень не содержится, в этом слое расположены только s- и p-подуровни.
е) Электронная конфигурация 5d2 реализуется, потому что на пятом энергетическом уровне (n = 5) содержатся s-, p- d- и f-подуровни. Подуровень d содержит пять атомных орбиталей, в которых может находиться максимальное число электронов равное десяти (5 . 2 = 10). Запись 5d2 означает, что на 5d-подуровне содержится два неспаренных электрона.
ж) Электронная конфигурация 3f12 не реализуется, потому что на третьем энергетическом уровне (n = 3) могут находиться только s-, p- и d-подуровни.
з) Электронная конфигурация 2p4 реализуется, потому что на втором энергетическом уровне (n = 2) могут находиться только s- и p-подуровни. Подуровень p состоит из трёх атомных орбиталей, на которых, согласно правилу Хунда, может находиться до шести электронов.
и) Электронная конфигурация 3p7 не реализуется, потому что на p-подуровне, состоящем из трёх атомных орбиталей, согласно правилу Хунда, максимальное число электронов равно 6.
Задача 184. Сколько вакантных Зd-орбиталей имеют возбужденные атомы: а) С1; б) V; в) Мn?Решение:а) электронная конфигурация атома хлора имеет вид: …3s23p53d0. Графическое заполнение валентного энергетического слоя атома хлора можно представить следующей схемой:
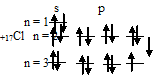
Таким образом, внешний энергетический уровень атома хлора имеет свободные орбитали на 3d-подуровне, что позволяет электронам переходить в возбуждённое состояние (перемещаться на более высокие свободные орбитали). У атома хлора возможно три состояния перемещения электронов на более высокие свободные орбитали, электроны с s- и p-подуровней переходят на 3d-подуровень:
1) При затрате некоторой энергии один из 3p-электронов атома хлора может быть переведён на вакантную 3d-орбиталь, при этом энергия атома возрастает, так что возникающая электронная конфигурация (1s22s22p63s23p43d1) соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
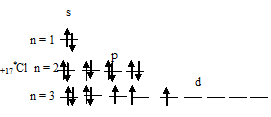
В данном случае 3d-подуровень содержит четыре вакантные орбитали возбуждённого атома хлора.
2) При затрате некоторой энергии два из 3p-электронов атома хлора могут быть переведены на вакантные 3d-орбитали, при этом энергия атома возрастает, так что возникает электронная конфигурация (1s22s22p63s23p33d2), которая соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
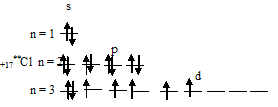
В таком возбуждённом состоянии атом хлора содержит три вакантные 3d-орбитали.
3) При затрате некоторой энергии один из 3s- и два 3p-электронов могут быть переведены на свободные 3d-орбитали, при этом энергия атома возрастает, так что возникающая конфигурация (1s22s22p63s13p33d3) также соответствует одному из возможных состояний хлора:
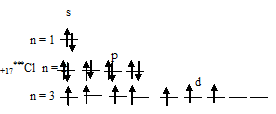
б) Электронная конфигурация валентного энергетического уровня атома ванадия имеет вид: …3d34s2. Графическая схема заполнения электронами имеет вид:
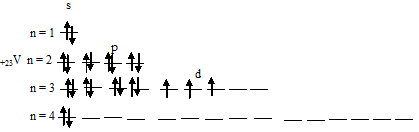
В возбуждённом состоянии атома ванадия один 4s-электрон может быть переведён на свободную 3d-орбиталь, так что возникающая электронная конфигурация валентного уровня (3d44s1) соответствует возбуждённому состоянию атома ванадия, что можно представить в виде схемы:
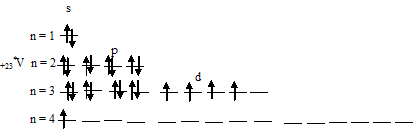
При возбуждении атома ванадия остаётся вакантной одна 3d-орбиталь.
в) Электронная конфигурация валентного энергетического уровня атома марганца имеет вид: …3d54s2. Графическая схема заполнения электронами имеет вид:
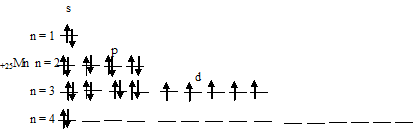
При возбуждении атома марганца один s-электрон переходит на 3d-орбиталь, при этом получается электронная конфигурация валентного уровня (3d64s1) соответствует возбуждённому состоянию атома марганца, что можно представить в виде схемы:
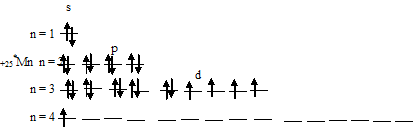
Из схемы вытекает, что при возбуждении атома марганца свободных d-орбиталей нет, так как на 3d-подуровне распределяются два спаренных электрона и четыре неспаренных. Таким образом, атом марганца ни в основном, ни в возбуждённом состоянии не имеет свободных d-орбиталей.
Задача 185. Сколько неспаренных электронов содержат невозбужденные атомы: а) В; б) S; в) Аs; г) Сг; д) Нg; е) Еu?Решение:а) Электронная формула атома бора 1s22s22p1. Валентность орбитали в этом атоме являются орбитали внешнего (второго) электронного, т.е. 2s-, 2p-орбитали. Графическая схема заполнения электронами этих орбиталей имеет следующий вид:
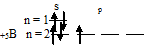
Следовательно, атом бора содержит один неспаренный 2p-электрон.
б) Электронная конфигурация валентного электронного слоя атома серы имеет вид: …2s22p4. Графическая схема заполнения электронами этого слоя имеет следующий вид:

Следовательно, атом серы в стационарном состоянии содержит два неспаренных электрона -, 2p-подуровне.
в) Электронная конфигурация валентного электронного слоя атома мышьяка имеет вид: …4s24p3. Графическая схема распределения валентных электронов имеет следующий вид:

Таким образом, атом мышьяка имеет три неспаренных электрона на 4p-подуровне.
г) Электронная конфигурация валентного электронного слоя атома хрома имеет вид: …3d5 4s1. Графическая схема заполнения электронами этого слоя имеет следующий вид:
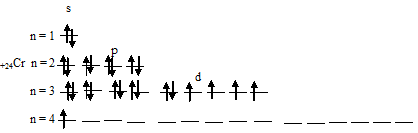
Следовательно, атом хрома в стационарном состоянии содержит шесть неспаренных электронов, из которых пять на 3d-подуровне и один на 4s-подуровне.
д) Электронная конфигурация валентного электронного слоя атома ртути имеет вид: … 6s26p0. Графическая схема заполнения электронами этого слоя имеет следующий вид:
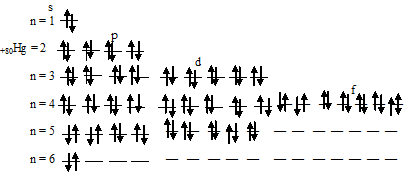
Атом ртути не содержит ни одного неспаренного электрона.
е) Электронная конфигурация валентного электронного слоя атома европия имеет вид: …4f7 6s2. Графическая схема заполнения электронами этого слоя имеет следующий вид:
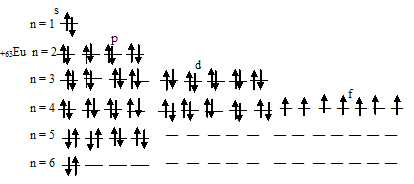
Таким образом, атом европия содержит семь неспаренных 4f-электронов.
Ответ: а) 1; б) 2; в) 3; г) 6; д) 0; е) 7.
Задача 186. Составить электронно-графические схемы ионов Ее2+ и Ее3+. Чем можно объяснить особую устойчивость электронной конфигурации иона Ее3+?Решение:Электронная формула атома железа имеет вид: 1s22s22p63s23p63d64s2. Графическая схема размещения электронов в квантовых ячейках атома железа будет иметь следующий вид:
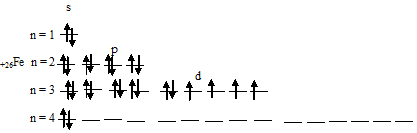
При отдаче двух 4s-электронов атомом железа образуется ион Ее2+, графическая схема размещения электронов в котором будет иметь вид:
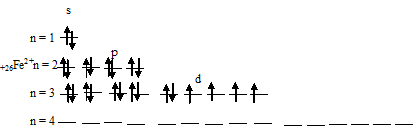
При отдаче трёх электронов (двух 4s- и одного 3d) атомом железа образуется ион Ее3+, графическая схема размещения электронов в котором будет иметь вид:
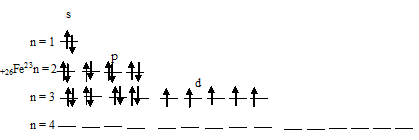
Таким образом, на внешнем энергетическом уровне иона Ее2+ содержится два 3s-, шесть 3p- и шесть 3d-электронов. Причём на 3d-подуровне содержатся четыре неспаренных и два спаренных электрона. Ион Ее3+ отличается от Ее2+ тем, что содержит на 3d-подуровне на один электрон меньше, и все они неспаренные, такая система 3d-подуровня является энергетически более устойчивой. Электростатическое взаимодействие между ядром и электронной плотностью у иона Ее3+ больше, чем у иона Ее2+.
Задача 187. Указать особенности электронных конфигураций меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?Решение:Так как число электронов в атоме элемента равно его порядковому номеру, то общее число электронов в атоме меди и хрома соответственно равно 29 и 24.
Последовательность заполнения энергетических уровней и подуровней в атоме элемента определяется правилами Клечковского, согласно которым электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией (меньшая сумма n + l). Порядок заполнения подуровней определяется правилом Хунда. Согласно правилу Хунда, минимальной энергии атома соответствует такое распределение электронов по атомным орбиталям данного подуровня, при котором абсолютное значение суммарного спина атома максимально.
Электронные формулы атомов хрома и меди можно выразить следующим образом:
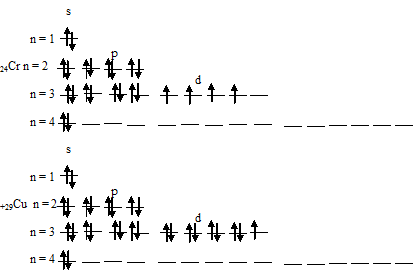
Экспериментально установлено, что на внешнем энергетическом уровне у хрома и меди находится по одному электрону. Объясняется это тем, что произошёл «провал» одного 4s-электрона у атомов хрома и меди на 3d-подуровень. Происходит это потому, что энергетически выгодным состоянием является состояние атома, когда при четырёх неспаренных электронах на 3d-подуровне происходит заполнение пятой свободной атомной орбитали. Поэтому электронная формула атома хрома имеет следующий вид: 1s22s22p63s23p63d54s1.
У атома меди все атомные орбитали 3d-подуровня заполнены, причём четыре полностью, а на пятой находится один неспаренный электрон. Такая система 3d-подуровня, состоящая из девяти электронов является энергетически неустойчивой, и поэтому происходит «провал электрона с 4s-орбитали на 3d-орбиталь. Электронную формулу атома меди можно теперь представить следующим образом: 1s22s22p63s23p63d104s1.
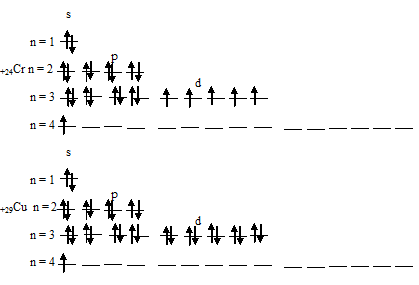
Таким образом, атомы хрома и меди на внешних энергетических уровнях содержат по одному 4-электрону. Графические схемы распределения электронов по квантовым ячейкам у атомов хрома и меди в стационарном состоянии будут иметь следующий вид:
buzani.ru
Электронные конфигурации атомов | Задачи 183
Задача 183. Среди приведенных ниже электронных конфигураций указать невозможные и объяснить причину невозможности их реализации: а) 1р3 б) 3p6 в) 3s2; г) 2s2; д) 2d5; е) 5d2; ж) 3f12; з) 2р4 и) 3p7.Решение:а) Электронная конфигурация 1p3 не реализуется, потому что первый энергетический уровень (n = 1 ) содержит только s-подуровень. Максимальное число электронов на каждом энергетическом уровне равно 2n2, где n - главное квантовое число. Так на первом энергетическом уровне (n = 1) может находиться максимальное число электронов 2(2 .12 = 2). Следовательно, не только неправильно указан подуровень, но общее число электронов.
б) 3p6 – электронная конфигурация возможна, потому что на третьем энергетическом уровне содержатся s-, p- и d-подуровни. На p-подуровне содержится три атомные орбитали, а в каждой орбитали, согласно правилу Хунда, может находиться максимальное число электронов равное двум. Поэтому на 3p-подуровне может максимально находиться шесть электронов (3 . 2 = 6).
в) Электронная конфигурация 3s2 верна, потому что на третьем энергетическом уровне (n = 3) находятся s-, p- и d-подуровни. Согласно правилу Хунда, на s-подуровне, состоящем из одной атомной орбитали, может находиться максимальное число электронов равное двум.
г) Электронная конфигурация 2s2 реализуется, потому что на втором энергетическом уровне (n = 2) содержатся s- и p-подуровни, и на s-подуровне, в его единственной атомной орбитали, может содержаться максимальное число электронов равное двум.
д) Электронная конфигурация 2d5 не реализуется, потому что во втором энергетическом уровне (n = 2) d-подуровень не содержится, в этом слое расположены только s- и p-подуровни.
е) Электронная конфигурация 5d2 реализуется, потому что на пятом энергетическом уровне (n = 5) содержатся s-, p- d- и f-подуровни. Подуровень d содержит пять атомных орбиталей, в которых может находиться максимальное число электронов равное десяти (5 . 2 = 10). Запись 5d2 означает, что на 5d-подуровне содержится два неспаренных электрона.
ж) Электронная конфигурация 3f12 не реализуется, потому что на третьем энергетическом уровне (n = 3) могут находиться только s-, p- и d-подуровни.
з) Электронная конфигурация 2p4 реализуется, потому что на втором энергетическом уровне (n = 2) могут находиться только s- и p-подуровни. Подуровень p состоит из трёх атомных орбиталей, на которых, согласно правилу Хунда, может находиться до шести электронов.
и) Электронная конфигурация 3p7 не реализуется, потому что на p-подуровне, состоящем из трёх атомных орбиталей, согласно правилу Хунда, максимальное число электронов равно 6.
Задача 184. Сколько вакантных Зd-орбиталей имеют возбужденные атомы: а) С1; б) V; в) Мn?Решение:а) электронная конфигурация атома хлора имеет вид: …3s23p53d0. Графическое заполнение валентного энергетического слоя атома хлора можно представить следующей схемой:
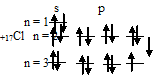
Таким образом, внешний энергетический уровень атома хлора имеет свободные орбитали на 3d-подуровне, что позволяет электронам переходить в возбуждённое состояние (перемещаться на более высокие свободные орбитали). У атома хлора возможно три состояния перемещения электронов на более высокие свободные орбитали, электроны с s- и p-подуровней переходят на 3d-подуровень:
1) При затрате некоторой энергии один из 3p-электронов атома хлора может быть переведён на вакантную 3d-орбиталь, при этом энергия атома возрастает, так что возникающая электронная конфигурация (1s22s22p63s23p43d1) соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:
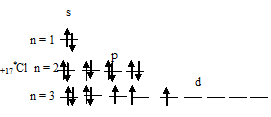
В данном случае 3d-подуровень содержит четыре вакантные орбитали возбуждённого атома хлора.
2) При затрате некоторой энергии два из 3p-электронов атома хлора могут быть переведены на вакантные 3d-орбитали, при этом энергия атома возрастает, так что возникает электронная конфигурация (1s22s22p63s23p33d2), которая соответствует одному из возбуждённых состояний атома хлора. Графически это можно представить схемой:

В таком возбуждённом состоянии атом хлора содержит три вакантные 3d-орбитали.
3) При затрате некоторой энергии один из 3s- и два 3p-электронов могут быть переведены на свободные 3d-орбитали, при этом энергия атома возрастает, так что возникающая конфигурация (1s22s22p63s13p33d3) также соответствует одному из возможных состояний хлора:

б) Электронная конфигурация валентного энергетического уровня атома ванадия имеет вид: …3d34s2. Графическая схема заполнения электронами имеет вид:

В возбуждённом состоянии атома ванадия один 4s-электрон может быть переведён на свободную 3d-орбиталь, так что возникающая электронная конфигурация валентного уровня (3d44s1) соответствует возбуждённому состоянию атома ванадия, что можно представить в виде схемы:

При возбуждении атома ванадия остаётся вакантной одна 3d-орбиталь.
в) Электронная конфигурация валентного энергетического уровня атома марганца имеет вид: …3d54s2. Графическая схема заполнения электронами имеет вид:

При возбуждении атома марганца один s-электрон переходит на 3d-орбиталь, при этом получается электронная конфигурация валентного уровня (3d64s1) соответствует возбуждённому состоянию атома марганца, что можно представить в виде схемы:

Из схемы вытекает, что при возбуждении атома марганца свободных d-орбиталей нет, так как на 3d-подуровне распределяются два спаренных электрона и четыре неспаренных. Таким образом, атом марганца ни в основном, ни в возбуждённом состоянии не имеет свободных d-орбиталей.
Задача 185. Сколько неспаренных электронов содержат невозбужденные атомы: а) В; б) S; в) Аs; г) Сг; д) Нg; е) Еu?Решение:а) Электронная формула атома бора 1s22s22p1. Валентность орбитали в этом атоме являются орбитали внешнего (второго) электронного, т.е. 2s-, 2p-орбитали. Графическая схема заполнения электронами этих орбиталей имеет следующий вид:
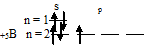
Следовательно, атом бора содержит один неспаренный 2p-электрон.
б) Электронная конфигурация валентного электронного слоя атома серы имеет вид: …2s22p4. Графическая схема заполнения электронами этого слоя имеет следующий вид:

Следовательно, атом серы в стационарном состоянии содержит два неспаренных электрона -, 2p-подуровне.
в) Электронная конфигурация валентного электронного слоя атома мышьяка имеет вид: …4s24p3. Графическая схема распределения валентных электронов имеет следующий вид:

Таким образом, атом мышьяка имеет три неспаренных электрона на 4p-подуровне.
г) Электронная конфигурация валентного электронного слоя атома хрома имеет вид: …3d5 4s1. Графическая схема заполнения электронами этого слоя имеет следующий вид:

Следовательно, атом хрома в стационарном состоянии содержит шесть неспаренных электронов, из которых пять на 3d-подуровне и один на 4s-подуровне.
д) Электронная конфигурация валентного электронного слоя атома ртути имеет вид: … 6s26p0. Графическая схема заполнения электронами этого слоя имеет следующий вид:

Атом ртути не содержит ни одного неспаренного электрона.
е) Электронная конфигурация валентного электронного слоя атома европия имеет вид: …4f7 6s2. Графическая схема заполнения электронами этого слоя имеет следующий вид:

Таким образом, атом европия содержит семь неспаренных 4f-электронов.
Ответ: а) 1; б) 2; в) 3; г) 6; д) 0; е) 7.
Задача 186. Составить электронно-графические схемы ионов Ее2+ и Ее3+. Чем можно объяснить особую устойчивость электронной конфигурации иона Ее3+?Решение:Электронная формула атома железа имеет вид: 1s22s22p63s23p63d64s2. Графическая схема размещения электронов в квантовых ячейках атома железа будет иметь следующий вид:

При отдаче двух 4s-электронов атомом железа образуется ион Ее2+, графическая схема размещения электронов в котором будет иметь вид:

При отдаче трёх электронов (двух 4s- и одного 3d) атомом железа образуется ион Ее3+, графическая схема размещения электронов в котором будет иметь вид:

Таким образом, на внешнем энергетическом уровне иона Ее2+ содержится два 3s-, шесть 3p- и шесть 3d-электронов. Причём на 3d-подуровне содержатся четыре неспаренных и два спаренных электрона. Ион Ее3+ отличается от Ее2+ тем, что содержит на 3d-подуровне на один электрон меньше, и все они неспаренные, такая система 3d-подуровня является энергетически более устойчивой. Электростатическое взаимодействие между ядром и электронной плотностью у иона Ее3+ больше, чем у иона Ее2+.
Задача 187. Указать особенности электронных конфигураций меди и хрома. Сколько 4s-электронов содержат невозбужденные атомы этих элементов?Решение:Так как число электронов в атоме элемента равно его порядковому номеру, то общее число электронов в атоме меди и хрома соответственно равно 29 и 24.
Последовательность заполнения энергетических уровней и подуровней в атоме элемента определяется правилами Клечковского, согласно которым электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией (меньшая сумма n + l). Порядок заполнения подуровней определяется правилом Хунда. Согласно правилу Хунда, минимальной энергии атома соответствует такое распределение электронов по атомным орбиталям данного подуровня, при котором абсолютное значение суммарного спина атома максимально.
Электронные формулы атомов хрома и меди можно выразить следующим образом:

Экспериментально установлено, что на внешнем энергетическом уровне у хрома и меди находится по одному электрону. Объясняется это тем, что произошёл «провал» одного 4s-электрона у атомов хрома и меди на 3d-подуровень. Происходит это потому, что энергетически выгодным состоянием является состояние атома, когда при четырёх неспаренных электронах на 3d-подуровне происходит заполнение пятой свободной атомной орбитали. Поэтому электронная формула атома хрома имеет следующий вид: 1s22s22p63s23p63d54s1.
У атома меди все атомные орбитали 3d-подуровня заполнены, причём четыре полностью, а на пятой находится один неспаренный электрон. Такая система 3d-подуровня, состоящая из девяти электронов является энергетически неустойчивой, и поэтому происходит «провал электрона с 4s-орбитали на 3d-орбиталь. Электронную формулу атома меди можно теперь представить следующим образом: 1s22s22p63s23p63d104s1.
Таким образом, атомы хрома и меди на внешних энергетических уровнях содержат по одному 4-электрону. Графические схемы распределения электронов по квантовым ячейкам у атомов хрома и меди в стационарном состоянии будут иметь следующий вид:

buzani.ru