Большая Энциклопедия Нефти и Газа. Степень окисления хрома
Cr2(SO4)3, степень окисления хрома и др элементов
Общие сведения о сульфате хрома (III) и степени окисления в Cr2(SO4)3
Брутто-формула — Cr2(SO4)3. Молярная масса равна – 392,16 г/моль.

Рис. 1. Сульфат хрома (III). Внешний вид.
Растворяется в воде (гидролизуется по катиону). Образует кристаллогидраты составов Cr2(SO4)3×18h3O иCr2(SO4)3×6h3O. Проявляет слабые окислительно-восстановительные свойства.
Cr2(SO4)3, степени окисления элементов в нем
Степень окисления кислотного остатка определяется числом атомов водорода, входящих в состав образующей его кислоты, указанных со знаком минус. Сульфат-ион – это кислотный остаток серной кислоты, формула которой h3SO4. В её составе имеется два атома водорода, следовательно, степень окисления сульфат-ионе равна (-2). Степень окисления кислорода в составе кислот, а, следовательно, и их остатков равна (-2). Для нахождения степени окисления серы в составе сульфат-иона примем её значение за «х» и определим его при помощи уравнения электронейтральности:
x + 4× (-2) = -2;
x — 8 = -2;
x = +6.
Степень окисления хрома найдем аналогичным образом:
2×у + 3× (+6) + 12× (-2) = 0;
2у + 18 – 24 = 0;
2у — 6 = 0;
2у = + 6;
y= +3.
Степень окисления хрома в сульфате хрома (III) равна (+3): Cr+32(SO4)3.
Примеры решения задач

| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
K2Cr2O7, степень окисления хрома и др элементов
Общие сведения о дихромате калия и степени окисления в K2Cr2O7
Плавится (397,5oC) без разложения и разлагается при дальнейшем нагревании. Брутто-формула – K2Cr2O7. Молярная масса дихромата калия равна 294,18 г/моль.

Рис. 1. Дихромат калия. Внешний вид.
Хорошо растворяется в воде: анион частично переходит в ион HCrO4—, который подвергается кислотному протолизу. Устойчив в кислотной среде. Кристаллогидратов не образует. Сильный окислитель в растворе и при спекании.
K2Cr2O7, степени окисления элементов в нем
Чтобы определить степени окисления элементов, входящих в состав дихромата калия, сначала необходимо разобраться с тем, для каких элементов эта величина точно известна.
Степень окисления калия постоянна и равна номеру группы в Периодической таблице Д.И. Менделеева, в которой он находится, со знаком плюс, т.е. (+1). Степень окисления кислорода в составе неорганических кислот, а, следовательно, и в составе их кислотных остатков, всегда равна (-2). Для нахождения степени окисления хрома примем её значение за «х» и определим его при помощи уравнения электронейтральности:
2 + 2х — 14 = 0;
2х — 12 = 0;
2х =12;
x = +6.
Значит степень окисления хрома в дихромате калия равна (+6):
K+12Cr+62O-27.
Примеры решения задач

| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Какая степень окисления у хрома?
Хром может существовать в виде простого вещества – металла, а степень окисления металлов в элементарном состоянии равна нулю, так как распределение электронной плотности в них равномерно.Степени окисления (+2) и (+3) хром проявляет в оксидах (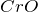 ,
, 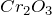
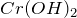 ,
, 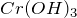 ), галогенидах (
), галогенидах (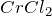 ,
, 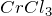 ), сульфатах (
), сульфатах (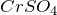 ,
, 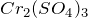
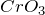 ,
, 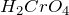 ,
, 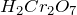 (ответ на вопрос «какая степень окисления у хрома»).Для того, чтобы найти определить степень окисления серы в составе предложенных соединений воспользуемся алгоритмом, предполагающим составление уравнение электронейтральности.Итак, в состав хромата калия
(ответ на вопрос «какая степень окисления у хрома»).Для того, чтобы найти определить степень окисления серы в составе предложенных соединений воспользуемся алгоритмом, предполагающим составление уравнение электронейтральности.Итак, в состав хромата калия 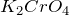 входят атомы калия, хрома и кислорода. Кислород, во всех веществах, кроме пероксидов и фторида кислорода проявляет степень окисления равную (-2). Калий имет постоянную степень окисления (+1). Для того, чтобы определить степень окисления хрома, примем её значение за «x». Тогда, уравнение электронейтральности примет следующим образом:
входят атомы калия, хрома и кислорода. Кислород, во всех веществах, кроме пероксидов и фторида кислорода проявляет степень окисления равную (-2). Калий имет постоянную степень окисления (+1). Для того, чтобы определить степень окисления хрома, примем её значение за «x». Тогда, уравнение электронейтральности примет следующим образом: ![Rendered by QuickLaTeX.com \[ 2 \times (+1) + x + 4 \times (-2) = 0;\]](/800/600/http/ru.solverbook.com//wp-content/ql-cache/quicklatex.com-76603e91f33a0264aa934c9b554dfacb_l3.png)
![Rendered by QuickLaTeX.com \[2 + x - 8= 0;\]](/800/600/http/ru.solverbook.com//wp-content/ql-cache/quicklatex.com-efc3921c90b2b3a75ada8c328fcb5c86_l3.png)
![Rendered by QuickLaTeX.com \[x - 6= 0;\]](/800/600/http/ru.solverbook.com//wp-content/ql-cache/quicklatex.com-40b7316e841dd8e5ff729008e7fa400f_l3.png)
![Rendered by QuickLaTeX.com \[x = +6.\]](/800/600/http/ru.solverbook.com//wp-content/ql-cache/quicklatex.com-6bc79a96ca26bfc2897a19129436767f_l3.png)
Аналогичным образом выясним степень окисления хрома в оставшихся соединениях: 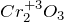 ,
, 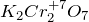 ,
, 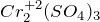 ,
, ![Rendered by QuickLaTeX.com Na_3[Cr^{+3}(OH)_6]](/800/600/http/ru.solverbook.com//wp-content/ql-cache/quicklatex.com-bc8c47e8c7480cc5326781e7b709ab28_l3.png) .
.
ru.solverbook.com
Степени окисления хрома - Справочник химика 21
| Рис. 3.28. Изменение профиля эмиссии бария в зависимости от степени окисления хрома и состава горючей смеси 1, —Г — Ва в отсутствие Сг 2, - 2 в присутствии СгШ 3, 3 — в присутствии СгУ1 1, 2, 3 — пламя стехиометрическое Г, 2, 3 — пламя восстановительное |  |
При этом образуется вулканообразный конус объемистого аморфного оксида хрома (III) зеленого цвета. Изменение степени окисления хрома в растворе сопровождается изменением окраски, что позволяет аналитически определить концентрацию хрома путем добавления раствора восстановителя известной концентрации. Соединения хрома (III) похожи на аналогичные соединения железа (особенно растворимые соли). Сульфат хрома (III) образует квасцы (как алюминий и железо). Хромокалиевые квасцы окраше-.чы в темно-фиолетовый цвет. Соединения хрома (II) — сильные восстановители и неустойчивы в присутствии влаги и воздуха (ср. со свойствами железа (II), с. 157). [c.155]
Аналогично находим степени окислений хрома в (NHj), r,0,, хлора +1+5-2 +1+5-2 [c.109]
Соединения хрома. В соединениях с кислородом хром проявляет ( степени окисления +6, -f 3 и +2. Из них наиболее устойчивы в обыч-1 ных условиях соединения со степенью окисления, равной трем. В этой же степени окисления хром входит большей частью и в природные соединения (хромистый железняк). Соединения хрома низшей сте- пени окисления (+2) легко окисляются, а соединения высшей степе- ни окисления (+6) все являются окислителями. [c.142]
Другой пример, подтверждающий сказанное выще, это химические свойства хрома. Из шкалы характерных степеней окисления хрома (рис. 20) очевидно, что Сг" обладает основными свойствами, Сг" -типично амфотерными (подобен алюминию), а Сг " -кислотными. [c.184]
При окислении хлорида олова (П) в солянокислой среде образуется хлорид олова (IV). Степень окисления хрома изменяется от +6 до +3. Образуются хлориды калия и хрома [c.108]
Определить степень окисления хрома, молибдена и вольфрама в следующих соединениях [c.228]
Изобразите структурные формулы хромата и дихромата калия и укажите степень окисления хрома в этих соединениях. [c.126]
Таким образом, храм, молибден и вольфрам имеют по 6 валентных электронов, т. е. их максимальное окислительное число +6. Большое число валентных электронов позволяет им проявлять переменную степень окисления хром (I), II, III, (IV), (V) и VI, молибден и вольфрам (И), (III), (IV) и VI (в скобках приведены окислительные числа, проявляемые элементами в неустойчивых соединениях). [c.101]
Пример 2. Определите степень окисления хрома в сложном ионе СгоО . Сумма всех степеней окисления атомов в сложном ионе должна быть равна заряду иона. Тогда искомую степень окисления определим из уравнения [c.57]
Сульфат железа (И) в сернокислой среде окисляется бихроматом калия до сульфата железа (III), а степень окисления хрома изменяется от +6 до +3. Калий и хром образуют сульфаты [c.109]
Пример 2. Определим степень окисления хрома в сложном ионе СгаО - [c.64]
Характерные степени окисления хрома +3 (отвечает устойчивой несвязывающей электронной конфигурации и в меньшей мере +6. У молибдена и вольфрама, как и у других 4й- и 5с -элементов, наиболее характерна высшая степень окисления, т. е. +6. Возможны также соединения, где хром и его аналоги проявляют степени окисления О, + 1, +2, - -4 и +5. [c.371]
Допустим, требуется найти степень окисления хрома в ионе СгаО ". Сумма всех степеней окисления атомов в ноне должна быть равна заряду иона. Тогда 2x-f (—2)-7=—2, отсюда 2х = + 12, а x=-f6. [c.83]
Соединения хрома(III) могут окисляться до степени окисления хрома -f6 как при действии окисляющих расплавов, так и в водных растворах. При этом всегда образуются оксосоеди-нения. В щелочном растворе также можно легко осуществить окисление до хроматов. [c.619]
Таким образом, характер оксидов и гидроксидов хрома закономерно изменяется с увеличением степени окисления хрома [c.319]
Соединения шестивалентного хрома. Известны многочисленные соединения шестивалентного хрома, например трехокись СгОз, хроматы (Сг04) -, бихроматы СггО ) , трихроматы (СгзОю) , тетрахроматы (Сг401з) . В высшей степени окисления хром проявляет неметаллические свойства и благодаря этому входит в состав анионов. [c.342]
Наиболее устойчивыми являются соединения со степенью окисления хрома -З. Соединения же хрома (И) являются сильными восстановителями и легко окис/яют-ся, при этом Сг+ превращается в Сг+ Сг+ —1ё=Сг . Например, гидроксид хрома (И) легко окисляется кислородом воздуха до гидроксида хрома И1) [c.320]
Какими реакциями можно получить оксиды хрома Как меняется их характер с увеличением степени окисления хрома Какова их растворимость в воде и какому из них соответствует гидроксид, который нельзя выделить в свободном состоянии [c.321]
Как видно из структур ионов, степень окисления хрома в обоих случаях равна +6 [c.517]
Исходя из степени окисления хрома, иода и серы в соединениях КаСгаО,, К1 и На80з, определите, какое из них является только окислителем, только восстановителем и какое может проявлять как окислительные, так и восстановительные свойства. Почему Расставьте коэффициенты в уравнении реакции, протекающей по схеме [c.394]
Отсюда получаем х = 6, т. е. степень окисления хрома в соединении равна +6. [c.59]
В случае более сложных соединений, например К2СГ2О7, ставят вначале степень окисления кислорода, затем калия, а далее, исходя из этих данных, определяют степень окисления хрома. Учитывая, что алгебраическая сумма степеней окисления всех атомов, входящих в молекулу, должна быть равна нулю, находят, что Сг в [c.23]
Характерные степени окисления хрома -1-3 (отвечает устойчиюй несвязывающей электронной конфигурации и в меньшей мере - 6. [c.548]
В разд. И было отмечено, что активация катализатора сухим воздухом прн повышенной температуре приводит к образованию на поверхности главным образом силилхромата Сг(У1). Это происходит независимо от исходной степени окисления хрома. Кроме того, большая часть хрома может содержаться в катализаторе в виде СггОз (зеленого), особенно если концентрация хрома выше 1 % или если катализатор нагревали до высокой температуры при значительной влажности. СГ2О3 неактивен в полимеризации. [c.180]
Выполнение работы. К раствору дихромата калия (2—3 каплн) прибавить 10—12 капель концентрированной хлороводородной кислоты (плотность 1,19 г/см ). Смесь нагреть до перехода оранжевой окраски в зеленую. Отметить выделение газа. Как изменилась степень окисления хрома Какой газ выделяется Написать уравнение реакции окисления хлороводородной кислоты дихроматом калия. [c.233]
Для хрома и его аналогов наиболее типичны производные высщей степени окисления, во многом сходные с соответствующими соединениями серы. Соединения хрома (VI) отличаются неустойчивостью в растворах и являются сильными окислителями. При этом они чаще всего восстанавливаются до анионных или катионных комплексов хрома (Ш). Хотя хром располагается в четной группе, наиболее устойчивой его степенью окисления является Ч-З. Это связано с тем, что соединения хрома (III) являются, как правило, комплексными с координационным числом 6 и октаэдрической пространственной конфигурацией расположения лигандов. В этом случае три Зй-электрона иона Сг + равномерно заселяют трижды вырожденные несвязывающие МО комплекса (см. рис. 13,5 д). Возникающая стабилизация системы за счет суммарного спина 3 V2 = V2 (по правилу Хунда) в этом случае больше, чем если бы степень окисления хрома была + 2, -f-4 и т. д. [c.511]
Валентными электронами у них, помимо электронов внешнего электронного уровня, являются еще 4—5 электронов соседнего с внешним (незаполненного ) уровня ( -электроны). Поэтому для всех этих элементов высшая степень окисления равна +6, причем для молибдена и вольфрама это состояние является наиболее устойчивым. Вместе с тем каждый из этих элементов образует и соединения, отвечающие другим степеням окисления. Хром проявляет в них степень окисления, равную трем и двум (эти соединения рассматриваются дальше), а молибден и вольфрам — степень окисления, равную четырем (М0О2, WOг). [c.141]
Депрессирующий эффект зависит от степени окисления и ионного состояния мешающего элемента. На рнс. 3.28 показано влияние степенн окисления хрома на испускагше бария. [c.65]
Оксид хрома (II) СгО проявляет основные свойства оксид хрома (ПОСгзОз — амфотерный оксид оксид хрома (VI) СгОз обладает кислотными свойствами. Соединения, в которых степень окисления хрома +2, легко окисляются и применения почти не имеют. [c.418]
Аквакатионы хрома (II) существуют в среде H IO4 в отсутс г-вие кислорода (иначе возможно повышение степени окисления хрома). В среде хлороводородной кислоты образуется хлоро-аквакомплекс [c.238]
МетолАЫ VIB-фуппы. Хром Сг, молибден Мо и вольфрам W — ( 4-э л е м е н т ы, которые в своих природных соединениях проявляют различные степени окисления хром -t-3 в [c.424]
Пероксид водорода может окислять хлорид хрома(1П) до хромат-иона Сг05" (в котором степень окисления хрома равна VI) по реакции [c.147]
Во втором случае SO2 выступает в роли восстановителя, пр этом степень окисления серы повышается до +6, а К2СГ2О7 — в рол окислителя, при этом степень окисления хрома понижается до +1 Реакция протекает по уравнению [c.522]
Хлорид низшей степени окисления хрома СгС1г — типичная соль ионного типа, сильный восстановитель [c.360]
Солп хромовой кислоты называются хроматами(VI) (часто степень окисления хрома не указывают), например К2СГО4 — хромат калия. Соли днхромовой кислоты [c.270]
chem21.info
Соединения хрома в степени окисления
Атомы металлических элементов в отличие от неметаллических обладают значительно большими размерами атомных радиусов. Поэтому атомы металлических элементов сравнительно легко отдают валентные электроны. Вследствие этого они обладают способностью образовывать положительно заряженные ионы, а в соединениях проявляют только положительную степень окисления. Многие металлические элементы, например медь Си, железо Ре, хром Сг, титан Т1, проявляют в соединениях разную степень окисления. [c.94] Если амфотерный элемент имеет в соединениях несколько степеней окисления, то амфотерные свойства наиболее ярко проявляются для промежуточной степени окисления. Например, у хрома известны три степени окисления-( +II), ( + 111) и ( + У1). Для Сг " кислотные и основные свойства выражены в равной степени, тогда как у Сг" наблюдается преобладание основных свойств, а у Сг преобладание кислотных свойств [c.99]Соединения хрома. В соединениях с кислородом хром проявляет ( степени окисления +6, -f 3 и +2. Из них наиболее устойчивы в обыч-1 ных условиях соединения со степенью окисления, равной трем. В этой же степени окисления хром входит большей частью и в природные соединения (хромистый железняк). Соединения хрома низшей сте- пени окисления (+2) легко окисляются, а соединения высшей степе- ни окисления (+6) все являются окислителями. [c.142]
Соединения Сг (Ш). У хрома степень окисления +3 является наиболее устойчивой. Координационное число хрома (П1) равно шести, [c.607]
Окисление железа (И) в железо (III) может быть осуществлено в щелочной среде большинством окислителей и кислородом воздуха, а в кислой среде — азотной и хлорной кислотами и кислородом воздуха. Ионы марганца окисляются различными окислителями, образуя окрашенные анионы различных степеней окисления марганца. Восстановители в кислой среде восстанавливают соединения марганца, хрома, железа и висмута из их высших степеней окисления до соединений низших степеней окисления, Bi -ионы могут восстанавливаться до металлического состояния. [c.39]
Характерная степень окисления +6. Наряду с этим хром дает устойчивые соединения со степенью окисления +3, молибден — иногда +4. В других степенях окисления (+1, +2, +4, +5) хром и его аналоги образуют неустойчивые соединения. Некоторые свойства элементов приведены в табл. 22.1. [c.376]
В противоположность хрому, шестивалентные Мо и даже в кислой среде могут быть восстановлены только сильными восстановителями. В частности, при действии водоро/ а в момент выделения последовательно образуются различно окрашенные соединення низших степеней окисления. [c.373]
Соединения железа, хрома, висмута низших степеней окисления способны окисляться, а соединения высших степеней окисления—восстанавливаться. [c.36]
Степени окисления тех элементов побочных подгрупп, соединения которых наиболее часто применяются в химической практике, слестепени окисления +6 и +3), марганец (+7, +6, +-4, +2) железо (+3, +2), кобальт, никель (+2, гораздо реже +3), медь (+2, +1), цинк (+2), [c.7]
Элементы подгруппы хрома в своих соединениях проявляют степени окисления от - -2 до +6. Сверху вниз в подгруппе устойчивость соединений с более высокими степенями окисления металлов увеличивается. [c.316]
Элементы подгруппы хрома проявляют также степени окисления +5, +4, -+-3, 4-2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют. [c.195]
Элементы подгруппы хрома проявляют также степени окисления 4-5, +4, - -3, -1-2, Но наиболее типичны соединения высшей степени окисления, которые во многом [c.253]
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6 из них наиболее устойчивы соединения хрома со степенями окислениями +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов -подуровня второго снаружи уровня. [c.254]
Наиболее устойчивыми являются соединения со степенью окисления хрома -З. Соединения же хрома (И) являются сильными восстановителями и легко окис/яют-ся, при этом Сг+ превращается в Сг+ Сг+ —1ё=Сг . Например, гидроксид хрома (И) легко окисляется кислородом воздуха до гидроксида хрома И1) [c.320]
Исследования, проведенные в нашей стране, позволили впервые в мировой практике предложить способ биохимической очистки соединений шестивалентного хрома (хроматов и бихроматов), а также хлоратов и перхлоратов. Метод основан на способности специально выведенных микроорганизмов использовать соединения хрома при окислении органических веществ, содержащихся в сточных водах. При этом в нейтральной или слабощелочной среде происходит восстановление ионов шестивалентного хрома до трехвалентного, который осаждается в виде гидроокиси, а хлораты и перхлораты восстанавливаются до практически безвредных хлоридов. Степень очистки достигает 99,4%, остаточное содержание хрома в стоках не превышает 0,4 мг/л. Технологическая схема включает усреднение производст- [c.57]
Действие окислителей и восстановителей. Сильные окислители окисляют трехвалентный хром и двухвалентные Ре++, N1++, Со и Мп++ до соединений высшей степени окисления. Так, окисление трехвалентного хрома в хромат осуществляется в щелочной среде хлором, бромом, перекисями, гипохлоритами, двуокисью свинца и марганца. [c.184]
Интересно отметить, что хром в металлическом состоянии имеет металлическую валентность 6, соответствующую степени окисления + 6, характерной для хроматов и бихроматов, а не более низкой степени окисления -ЬЗ, характерной для солей хрома металлы марганец,, железо, кобальт и никель тоже имеют металлическую валентность 6, хотя почти все эти элементы образуют соединения со степенями окисления + 2 и -ЬЗ. Ценные физические свойства переходных металлов обусловлены высокой металлической валентностью этих элементов. [c.494]
Соединения молибдена и хрома в степени окисления +6 в отличие от соединений хрома в той же степени окисления являются очень слабыми окислителями и могут быть восстановлены сильными восстановителями в соединения низших степеней окисления. [c.101]
Соединения Сг([П), Мо(П1), W (III). У хрома степень окисления -ЬЗ является наиболее устойчивой. Координационное число хрома (HI) равно шести, поэтому его комплексы (структурные единицы) имеют форму октаэдра. Валентные электроны в октаэдрических комплексах Сг (HI) располагаются только на связывающих и несвязывающих орбиталях [c.558]
Кроме того, они образуют соединения, отвечающие степени окисления +2 и -ЬЗ. Соединения хрома (III) по свойствам во многом сходны с соединениями алюминия (III). Это объясняется тем, что радиусы ионов Сг + (0,63А) и AF+ (0.54А) близки. Гидроксид хрома Сг(ОН)з, как и А1(0Н)з, амфотерное соединение. В отличие от соединений алюминия соединения хрома (III) обладают восстановительными свойствами. Высшие оксиды рассматриваемых элементов ЭО3 и соответствующие им гидроксиды Н2ЭО4 обладают кислотными свойствами. Соединения хрома (VI) СгОз, Н2СГО4, Н2СГ2О7 и их соли — сильные окислители. [c.97]
Действие окислителей и восстановителей. Сильные окислители окисляют Сг++ +, Fe++, Ni++, Со++ и Мп++ до соединений высшей степени окисления. Так, в щелочной среде хлор, бром, перекиси, гипохлориты, двуокись свинца, перманганат окисляют трехвалентный хром в хромат. [c.290]
ХРОМА СОЕДИНЕНИЯ. ОксмЭ хрома (111) rjOj — темно-зеленые тугоплавкке кристаллы, т. пл. 2275° С, применяется под названием зеленый крон для изготовления очень устойчивых клеевой н масляной красок. Из СГ2О3 изготовляют катализаторы, получают хром, им окрашивают стекло и керамику. Соединения со степенью окисления X. +3 имеют зеленую или фиолетовую окраску. Они устойчивы на воздухе. Производные ак- [c.279]
Наиболее устойчивая степень окисления молибдена и вольфрама +У1, для хрома характерны степени окисления 4-П1 и -НУ . Известны также и другие степени окисления данных элементов, однако соединения низших степеней окисления легко окисляются кислородом воздуха, поэтому с ними реже встречаются в лабораторной практике. [c.223]
Для элементов подгруппы хрома известны соединения, отвечающие различным валентностям, вплоть до VI. Из всех них сколько-нибудь значительное применение находят только производные шестивалентных элементов и трехвалентного хрома, причем важнее других хромовые препараты. Соединения низших степеней окисления Мо и еще сранительно плохо изучены. 2 [c.365]
Наиболее стабильная степень окисления молибдена и вольфрама + 6 для хрома характерны степени окисления +3 и - 6. Как и в других побочных подгруппах, в УШ подгруппе при переходе к элементам сверху вниз стабилизируются высокие степени окисления. Известны также другие степсни. окисления рассматриваемых элементов, однако соединения низших степеней окисления легко окисляются кислородом воздуха. Восста ювленнем соедиисний Сг " сравнительно легко получаются соединения Сг растворы этих соединений иногда применяют в качестве активных поглотителей кислорода. [c.210]
Для хрома характерны соединения со степенью окисления +3. Их получают непосредственным взаимодействием хрома с галогенами или в других химических процессах. Так, соль СгС1з — кристаллы красно-фиолетового цвета — чаще всего находится в полимерном состоянии. Ион Сг + склонен к образованию многочисленных комплексных солей, в которых лигандами являются НзО С1 ЫНз. Склонность к образованию комплексов с координационным числом 6 объясняется структурой иона [c.345]
Решете. Хром в соединениях имеет степени окисления +6, +3. Его оксиды — СгОз и СГ2О3. СГ2О3 — амфотерный оксид. Следовательно, СгОз — кислотный оксид. [c.11]
В химическом отношении все металлы характеризуются сравнительной легкостью отдачи валентных электронов и, как следствие этого, способностью образовывать положительно заряженные ионы и проявлять в своих соединениях только положительную окисленность. Многие металлы, например железо, хром, марганец, имеют в различных соединениях разную степень окисленности, но она всегда положительна. В связи с этим металлы в свободном состоянии являются восстановителями. Восстановительная способность разных металлов неодинакова. Для реакцщ в водных растворах она определяется положением металла в ряду напряжений и концентрацией (актив1юстью) его нонов в растворе. [c.514]
Хром находится в 6-й группе, в его электронной оболочке на два электрона больше, чем у титана. В основном состоянии атом хрома содержит две полузаполненные оболочки [Аг]3( 4з с шестью неспаренными электронами. Благодаря наличию шести валентных электронов и не очень высокой электроотрицательности хрома (1,6) химия его очень богата и разнообразна он проявляет все степени окисления от -2 до -Ьб. Как и в случае титана, самые низкие степени окисления (-2, -1,0 и -Ы) проявляются только в комплексных соединениях с л-акцепторными лигандами, например в карбониле Сг(СО)в. Наиболее характерна для хрома степень окисления -ЬЗ и, соответственно, электронная конфигурация иона В природе хром встречается в основном в виде соединений Сг(Ш), например хромистого железняка ГеО СГ2О3, правда на Урале встречается красная свинцовая руда РЬСгО , в которой хром находится в степени окисления -Ьб, характеризуюш ейся выраженными окислительными свойствами. [c.347]
В своих соединениях проявляет степень окисления от +2 до +б и обнаруживает двойную аналогию с актинием и с. чгеталладт У1В-группы. Уран, как и хром, реагирует с растворами Н2804 и НС1 с выделением водорода. Наиболее устойчивы для урана степени окисления -4 и +6. [c.122]
VI группы периодической систе.чы элементов ат. н. 24, ат. м. 51,996. Металл серебристого цвета. В соединениях проявляет степени окисления -f 2, -Ь 3 и + 6. Состоит из стабильных изотопов Сг (4,49%), Сг (83,78%), ИСг (9,43%) и Сг (2,30%). Из шести радиоактивных изотопов важнейшим является i r с периодом полураспада 27,8 дня. X. открыл (1797) франц. химик Д. Вокелен в мп-нера.ле крокоите, выделив его в металлическом состоянии. Чистый X. впервые получил (1854) нем. химик Р. Бунзен электролизом хлористого хрома. В пром. масштабе X. начали получать (1866 — 70) в виде феррохрома, восстанавливая хромовую руду углеродом. Содержание X. в земной коре 3,5-10 %. Из минералов наибольшее значение имеет хромит (хромистый железняк) FeO- raOg. Плотность X. (т-ра 20° С) 7,19 г/ст решетка кубическая объемноцентрированная с периодом а = 2,885 А [c.692]
Сильные восстановители (HJ, HaS, HNOg и др.) восстанавливают соединения хрома, марганца, железа, никеля и кобальта в высшей степени окисления до соединений низших степеней окисления. [c.185]
Тяжелые переходные элементы проявляют явную тенденцию к образованию соединений с более высокими степенями окисления. В то время как степень окисления (+П) известна для всех элементов первого переходного ряда, кроме скандия, для тяжелых переходных элементов она не характерна, и имеется лишь у С(3, Нд, Рс1 и Р1. Аналоги кобальта — родий и иридий — проявляют степени окисления только (+И1) и выше. Соединения хрома (П1) являются наиболее устойчивыми, а соединения молибдена и вольфрама в этой степени окисления — сильные восстановители в химии Мо и Ш преобладают соединения с их степенью окисления (-[-У ). В целом устойчивость соединений тяжелых переходных металлов, обладающих высшей степенью окисления (равной номеру группы) очень большая, Так, ион ДеОГ не является сильным окислителем, подобно иону МпОГ-Примерами соединений со степенью окисления (+УП1) являются тетраоксиды рутения и осмия Весьма устойчивыми по сравнению с элементами первого переходного ряда являются соединения Рс ", Pt и Аи" получены даже соединения Аи . [c.394]
Характерным свойством многих катионов -элементов (марганца, хрома, железа, никеля, кобальта, ртути) являются их способность к реакциям окисления — восстановления. Сильные окислители хлор, бром, перманганагТ, персульфаты и другие окисляют их до соединений высшей степени окисления. Восстановители HI, h3S, h3SO3 в кислой среде восстанавливают соединения хрома, марганца, железа, никеля и кобальта до соединений низших степеней окисления. Особенно [c.73]
Недавно были критически рассмотрены [192] и обобщены [193] новейшие направления в кинетических методах анализа. Иногда аналитика наиболее удовлетворяет простейшая форма использования катализа. Например, в смеси мышьяка(П1) и железа(И) сначала титруют церием(1У) железо(П), так как реакция между церием(1У) и мышь-яком(И1) идет очень медленно и не мешает определению железа, а затем, после того как все железо(Н) прореагировало, добавляют подходящий катализатор (OSO4) и тут же титруют мышьяк(И1). Поскольку церий не дает неустойчивых соединений промежуточных степеней окисления, индуцированные реакции в этом случае не мешают. Для ускорения реакции между хромом(У1) и ураном(1У) [c.358]
chem21.info
Как определить высшую степень окисления?
Степень окисления –формальный заряд, приписываемый атому химического элемента в соединении, для отображения на бумаге процессов его окисления и восстановления. Для того, чтобы указать знак степени окисления нужно знать значение электроотрицательности химического элемента. Также не следует забывать о том, что степень окисления не равняется заряду атома в молекуле.Теперь ответим на вопрос «как определить высшую степень окисления хрома». Максимальную положительную или высшую степень окисления хрома определяют по положению этого элемента в Периодической таблице Д.И. Менделеева, а точнее по номеру группы, в которой он находится. Хром расположен в VI группе, значит его высшая степень окисления равна +6.Минимальную или низшую степень окисления хрома равна +2 (без учета степени окисления равной 0, которая характерна для каждого химического элемента).Кроме этого, для хрома характерно наличие промежуточной степени окисления равной +3.Примеры соединений хрома, в которых он проявляет характерные степени окисления: 0 (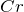 — простое вещество хром), +2 (
— простое вещество хром), +2 (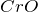 ,
, 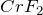 ), +3 (
), +3 (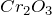 ,
, 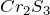 ,
, 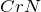 ), +6 (
), +6 (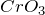 ,
, 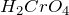 ,
, 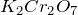 ).
).
ru.solverbook.com
Степень - окисление - хром
Степень - окисление - хром
Cтраница 4
В прокаленной массе определяли степень окисления хрома, которую рассчитывали как процентное отношение суммы водо - и кислоторастворимого хрома к общему его содержанию. [47]
Особенно велика роль температуры металла при производстве литых изделий. Снижение температуры металла увеличивает степень окисления хрома, титана и алюминия, а также продолжительность разливки, что отрицательно влияет на качество поверхности слитков. [48]
Оксид хрома ( II) СЮ проявляет основные свойства; оксид хрома ( Ш) Сг2О3 - амфотерный оксид; оксид хрома ( VI) СЮ3 обладает кислотными свойствами. Соединения, в которых степень окисления хрома 2, легко окисляются и применения почти не имеют. [49]
Рассматривается [285] вскрытие хромита с высоким содержанием А12О3 ( обжиг в смеси с Na2CO3 и А. Предложено [119, 1096] для повышения степени окисления хрома добавлять некоторое количество Na2CO3 в реакционную массу температурной зоны печи 1000 - 1200 С. [50]
Депрессирующий эффект зависит от степени окисления и ионного состояния мешающего элемента. На рис. 3.28 показано влияние степени окисления хрома на испускание бария. [52]
Предложен [119] принципиально новый способ переработки хромовой руды при обычной температуре путем перемешивания водной суспензии феррата ( 1У) и хромита; раствор Na2CrO4 отделяют от шлама, содержащего Fe ( III), а феррат ( 1У) регенерируют путем окислительного прокаливания при 400 С смеси шлама и щелочи. Исследовано [315] влияние различных факторов на степень окисления хрома при анодном окислении солей Cr ( III) в хроматы. [53]
Как меняется их характер с увеличением степени окисления хрома. Какова их растворимость в воде и какому из них соответствует гидроксид, который нельзя выделить в свободном состоянии. [54]
Увеличение содержания соды в шихте на 10 % дает увеличение степени окисления всего лишь на 2 - 3 % для шихт, содержащих менее 90 % соды от рассчитанного количества. Для этой шихты в пределах содержания окиси хрома от 15 до 18 % степень окисления хрома примерно равна содержанию соды. [55]
Вместо непосредственной величины константы С удобнее пользоваться выведенным выше магнитным моментом 2 84 С, так как эта величина более очевидным образом связана со степенью окисления хрома. На рис. 11 даны как), так и д как функции концентрации хрома. Сразу же отметим, что и остается почти постоянным, а Л заметно зависит от концентрации хрома. [56]
Из графика также следует, что с увеличением коэффициента избытка воздуха и температуры уходящих газов расход топлива повышается. Это происходит вследствие роста потерь тепла с уходящими газами. Так как с повышением температуры уходящих газов и содержания кислорода увеличивается производительность печи и степень окисления хрома, то прокалочные печи должны работать с максимально возможным коэффициентом избытка воздуха и с повышенными тепловыми нагрузками. [57]
В связи с тем, что скорость процесса в значительной степени лимитируется скоростью химического взаимодействия, принципиально возможно ускорение его катализаторами. Исламова, 1961 г.) нашли, что небольшие ( 0 2 %) добавки ряда окислов ( особенно PbO, CuO, ТЮ2) повышают степень окисления хрома; влияние добавок ослабевает по мере повышения температуры и продолжительности прокаливания. [58]
Страницы: 1 2 3 4
www.ngpedia.ru





