65. Хроматы и дихроматы. Степень окисления хрома в дихромате аммония
Степени окисления хрома дихромата аммония nh5 2cr2o7
Определите валентность каждого элемента в следующих соединениях: в нитрате цинка, в сульфате алюминия, в дихромате аммон
Какие есть эффектные окислительно восстановительные реакции или опыты?
ГдЕ купить или взять ДИХРОМАТ АММОНИЯ (Nh5)2Cr2O7
Наверняка он вам нужен для изготовления окиси хрома. Так уж сразу покупайте Пасту Гои http://www.polirovanie.ru/goi.php
Разложение дихромата аммония. ... Степень окисления хрома понижается с 6 до 3. Наблюдается изменение окраски реакционной массы с желто-оранжевого цвета до зеленого или фиолетового.
На кафедре
Установите формулу исходного бихромата аммония
Разложение дихромата аммония: (Nh5)2Cr2O7 = N2 + 4h3O + Cr2O3
Может быть получен при прокаливании гидроксида хрома III или дихроматов калия и аммония ... При сплавлении Cr2O3 со щелочами, содой и кислыми солями получаются соединения хрома со степенью окисления 3
1/ масса хрома в оксиде Cr2O3 = 15.2*0.6842 = 10.4г масса кислорода в Cr2O3 = 15.2*0.3158 = 4.8гмасса кислорода в Н2О = 16*7,2/18 = 6,4г водорода 2*7,2/18 = 0,8г, общая масса кислорода = 4,8+6,4= 11,2гмасса азота = 25,2-10,4-11,2-0,8 = 2,8г Сr : О :Н : N = 10.4/52 : 11,2/16 : 0,8/1 :2,8/14 = 2:7:8:2 (Nh5)2Cr2O7
Термическое разложение какой соли похоже на извержение вулкана?
Дихромат аммония
В лаборатории Cr2О3 получают термическим разложением дихромата аммония Nh5 2Cr2O7?Cr2О3 N2 4Н2О. ... Для них характерна степень окисления 2, 3, 4. Реже проявляются более высокие степени окисления.
Бихромата аммония (Nh5)2Cr2O7.Реакция разложения идет с выделением большого количества теплоты.(Nh5)2Cr2O7=Cr2O3+N2+4h3O
В каких веществах содержится бихромат аммония, которые мы используем в повседеневной жизни?
Дихромат аммония является токсичной и канцерогенной солью. Вдыхание пыли приводит к онкологическим заболеваниям. Смертельная доза 2 грамма.Лучше бы они наблюдали за чем-нибудь другим.Получается он исключительно синтетически.Используется в металлообрабатывающей, кожевенной, текстильной, химической, лакокрасочной, фармацевтической, керамической, спичечной промышленности.
Оксид хрома III получается при термическом разложении дихромата аммония ... Соли хрома III . Хром в степени окисления 3 образует два типа солей, в которые входит в состав катиона и аниона.
Я не думаю, что с такой страшной хар-кой, которую тут наплёл "оракул", бихромат аммония не клали в детский химический набор (в советское время) .А то, где он применяется, детям будет совершенно не интересно, т. к. не понятно. Успокойся.
Какие химические эксперименты сопровождаются самыми красивыми визуальными эффектами?
Самый интересный эксперимент проведен с распадом атомарного водорода, в результате эсперимента взрывная волна три раза прокатилась по нашей планете а прибор для эксперимента назвали водородной бомбой.К сожалению те кто видел эксперимент вблизи ничего не могут рассказать, потому что их не найти.
Дихромат аммония - неорганический состав с формулой Nh5 2Cr2O7. В этом составе, как во всех хроматах и дихроматах, хром находится в 6 степенях окисления, обычно известных как hexavalent хром.
Термическое разложение дихромата аммония.
Кусочек натрия в стаканчик с водичкой... главное с водичкой не переборщить и отойти подальше)))
Разложение бихромата аммония!!!
Нуправляемая термоядерная реакция . Красивые эффекты во время взрыва. Далее красивые живые организмы после взрыва. И различные мутации всего вокруг еще лет 100. Зависит от периода полураспада.
Кусочек марганца красиво горит!
Степень окисления у элементов подгруппы хрома сильно варьирует. В надлежащих условиях все элементы проявляют положительную ... В лаборатории Cr2О3 получают термическим разложением дихромата аммония Nh5 2Cr2O7?Cr2О3 N2 4Н2О.
Взрывы .особенно ядерные и термоядерные
Неорганическая химия,помогите,пожалуйста!
Подскажите кто-нибудь пожалуйста!
Отвечаю на вторую часть: 1) сульфит бария; 2) гидроксосульфат хрома; 3) ортофосфорная кислота; 4) хромит калия; 5) висмутат стронция (за 5 не уверен)
Соблюдайте осторожность! Дихромат аммония начинает разлагаться с выделением азота и паров воды, вспучивающих смесь, а также серо-зеленого оксида хрома III Nh5 2Cr2O7 Cr2O3 N2 4h3O .
Первая часть: 1) (Nh5)2Cr2O7 2) Sn(OH)4
Закончить и уравнять реакцию: 1) HCOOK + h3SO4 =>не знаю такой реакции 2) CuSO4 + 2Nh5OH =(Nh5)2SO4+Cu(OH)2 3) Hg(NO3)2 + h3S =>HgS+2HNO3 4) NaHCO3 + NaOH =>Na2CO3+h30 по моему 5) Zn(OH)2 + 2NaOH(избыток) =>Na2ZnO2+h3O Бромноватистая кислота, HBrO, неорганическая кислота. Существует только в водных растворах (желтоватая окраска, своеобразный запах), под действием света разлагается на HBr и кислород; обладает слабыми кислотными свойствами и является сильным окислителем. Некоторые соли Б. к. — гипобромиты (KBrO, NaBrO) — получены в свободном состоянии в виде кристаллогидратов. Все они очень неустойчивы, при нагревании (или подкислении растворов) тотчас распадаются на бромид и бромат: 3КВrO = 2KBr + KBrO3
Как сделать озот дома без всяких спец средств
Азот или озоН?)))
Разрушение кристаллов дихромата аммония сопровождается характерным потрескиванием. ... Окислителем является элемент хром, степень окисления которого изменяется от 6 до 3, а восстановителем азот, степень окисления которого...
"Озот" никак не получится "без спец. средств" - нужно, как минимум, курс русского языка.. . А, вот, АЗОТ- может его и делать не надо? Его в воздухе почти 70%
Только в сказке без ничего можно сделать что-то.
Приведите пример реакции разложения и условия которые нужно создать для того , чтобы реакция началась? помогите плиз))
Реакция разложения дихромата аммония, достаточно прикоснуться к соли нагретым предметом, например, стеклянной палочкой: (Nh5)2Cr2O7=Cr2O3 + N2 + 4h3O.Или нагреть пробирку, с находящимся в ней перманганатом калия:2KMnO4=K2MnO4 + MnO2 + O2.
Дихромат аммония Nh5 2Cr2O7 получают в промышленности из природного железохромового оксида хромита . ... Также хромовый ангидрид может быть получен при окислении оксида хрома Ш озоном или кислородом при повышенном давлении...
Подробно решить задачу по химии
Решение(Nh5)2Cr2O7 ---> Cr2O3 + N2 + 4h3O504 ----100%х ----------90%х = 453,6252 -----22,4453,6 -----хх = 40,32
Степень окисления. 24. Хром Cr. ... Оксид хрома III Cr2O3 зел ный, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома III или дихроматов калия и аммония
Помогите пожалуйста:Вычислите относительную плотность по гелию смеси газов, образовавшихся при прокаливании равномолярно
Напишем уравнении данных реакции:2NaHCO3=Na2CO3+CO2+h3O(Nh5)2Cr2O7=N2+Cr2O3+4h3OДопустим, был взять из каждого вещества по 2 моль. Тогда получиться 1моль СО2 и 2 моль азота. Находим среднюю молярную массу газовой смеси по формуле:Mср=(n1M1+n2M2)/(n1+n2)где n1,n2 количество газов и М1,М2 молярные массы газовMср=(1*44+2*28)/(1+2)=100/3 Плотность пр гелию: 100/12=8,33
Хром представляет собой ковкий тягучий металл серо-стального цвета. В степени окисления 2 соедин ения хрома проявляют основные свойства и являются ... Оксид хрома III должна быть получен разложением дихромата аммония при нагревании .
Как сделать свой домашний вулкан?
Какие вы знаете относительно безопасные химические приколы, что бы к НОВОМУ ГОДУ было чем удивить знакомых?
Химический вулкан. Для его проведения возьмите дихромат аммония и насыпьте его горкой на термостойкую поверхность (например, кафельную плитку) . Сверху сделайте «кратер» , в который поместите небольшой кусочек ваты, смоченный спиртом. Спирт подожгите. Соблюдайте осторожность! Дихромат аммония начинает разлагаться с выделением азота и паров воды, вспучивающих смесь, а также серо-зеленого оксида хрома (III):(Nh5)2Cr2O7 Cr2O3 + N2 + 4h3O.Реакция напоминает действующий вулкан. После ее завершения оксид хрома (III) занимает объем примерно в 2–3 раза больший, чем исходное вещество. Следует учесть, что частицы образующегося оксида хрома (III) – «вулканическая пыль» , будут оседать вокруг «вулкана» , поэтому опыт необходимо проводить на большом подносе.К дихромату аммония можно добавить немного порошка магния, тогда «вулкан» будет «извергаться» еще ярче.
4 4 Школьники имели дело с дихроматом аммония Nh5 2Cr2O7, который содержит азот в степени окисления -III и хром в степени окис ления VI Горящая спичка вызвала начало самопроизвольной внутри молекулярной окислительно...
Химия вопрос. Составьте уравнение химической реакции характеризующих химическое строение азота
Есть вопрос..
Трёх чеченцев и почти угнал их ПриоруИнцидент произошел около магазина для взрослых. Сообщается, что потасовка завязалась сразу после того, как вышедший из магазина молодой человек услышал в свой адрес оскорбительные высказывания касательно его сексуальной ориентации. Как стало известно позже, 27–летний дагестанец Амир Талбоев действительно является гомосексуалистом и, что немаловажно, чемпионом Европы по греко–римской борьбе. Все три выходца из Чеченской республики, сделавшие замечание борцу–гомосексуалисту, в данный момент госпитализированы. У каждого из них диагностированы многочисленные ушибы, переломы костей и сотрясения мозга. Все они воздерживаются от каких–либо комментариев. Амир Талбоев был задержан сотрудниками полиции в момент, когда пытался завести тонированную «Приору» потерпевших. Очевидцы сообщают, что молодой человек не собирался уезжать, а планировал переехать обидчиков на их же автомобиле, после чего — разбить его о ближайшую
Не все степени окисления у элементов стабильны, у хрома самая стабильная 3. ... В лаборатории Cr2О3 получают термическим разложением дихромата аммония Nh5 2Cr2O7?Cr2О3 N2 4Н2О.
Ночью плохо думается тезка)
Прокаливание аммония и получение азота. Помогите составить пропорцию, найти количество газа
Ты пытаешься решить такие задачи и при этом не умеешь находить молярную массу по известной формуле вещества? Ты где был-то, когда это проходили? Или ты это мимо проходил? Подскажу: с помощью таблицы Менделеева.
Не все степени окисления у элементов стабильны, у хрома самая стабильная 3. ... В лаборатории Cr2О3 получают термическим разложением дихромата аммония Nh5 2Cr2O7?Cr2О3 N2 4Н2О.
Как выделить дихромат калия из спички? хочу сделать вулчканчик
А он там вообще есть? если и есть то в мизерной дозировке
Вывод оксид хрома III Cr2O3 получается путем нагревания дихромата аммония. ... Окислителем является элемент хром, степень окисления которого изменяется от 6 до 3, а восстановителем азот, степень окисления которого изменяется от -3 до 0.
В спичках нет дихромата калия, в качестве окислителя используется бертолетова соль KClO3. Чтобы сделать "вулканчик" нужен бихромат аммония (Nh5)2Cr2O7.
Ребята,нужно подробно решить задачу
Решение(Nh5)2Cr2O7 ---> Cr2O3 + N2 + 4h3O504 ----100%х ----------90%х = 453,6252 -----22,4453,6 -----хх = 40,32
Дихромат аммония разлагается при нагревании 18 Nh5 2Cr2O7 В ряду гидроксидов хрома различных степеней окисления Cr ОН 2 Cr ОН 3 Н2CrО4 закономерно происходит ослабление основных свойств и усиление кислотных.
Помогите придумать прикольных реакций по химии
В списке отсутствует уксусная кислота. Спирт продали, а уксус нет?
Цинк Валентные электроны 3d104s2. Проявляет степень окисления 2. Голубовато-белый металл, хрупкий при комнатной температуре. ... Оксид хрома III получается при термиче Nh5 2Cr2O7 t рCr2O3 N2 4h3O ском разложении дихромата аммония...
Не "придумать", знать надо. Здесь таких реакций - куча мала. Надоест по клавишам щёлкать.
А что из себя представляет бихроматическая смола??
Это технологический метод в фото-промыщленности.бихроматическая смола наносится в несколько слоев на отпечаток.правда сложный у вас вопрос. )
Не все степени окисления у элементов стабильны, у хрома самая стабильная 3. ... В лаборатории Cr2О3 получают термическим разложением дихромата аммония Nh5 2Cr2O7?Cr2О3 N2 4Н2О.
1.2. За оказанные Агентом услуги Принципал выплачивает ему вознаграждение в размере 10% от реализованных санаторно-курортных услуг, оформленных санаторно-курортной путевкой.
1.3. Агенту выплачивается вознаграждение за реализацию санаторно-курортных услуг при наличии: - фактического поступления денежных средств на расчетный счет Принципала, - финансовых документов подтверждающих факт сделки через Агента, - отчета о реализации санаторно-курортных услуг, оформленных должным образом.
1.4. Агент реализует санаторно-курортные путевки по ценам указанным в прейскуранте (Приложение № 1).
2. Права и обязанности сторон
2.1. Агент обязан выполнять действия, предусмотренные в п. 1.1. настоящего договора, надлежащим образом и своевременно.
2.2. Агент производит бронирование мест в ЛПУП Санаторий «Ленинские скалы» не менее, чем за 30 дней до предполагаемой даты заезда.
2.3. Агент предоставляет Принципалу заявки на бронирование по электронному адресу, факсу или ISQ, указанным в договоре. Заявка должна содержать всю информацию, необходимую для оформления санаторно-курортной путевки и правильной идентификации отдыхающего.
2.4. Агент предоставляет Принципалу отчет о выполненных поручениях. Отчет направляется Принципалу в срок до 7-го числа месяца, следующего за отчетным. Одновременно с отчетом Агент обязан направить Принципалу счет-фактуру на сумму вознаграждения.
2.5. Агент вправе в целях исполнения настоящего договора заключать субагентский договор с другим лицом.
2.6. Агент сообщает Принципалу по его требованию все сведения о ходе исполнения поручения и без промедления передает ему все полученное в связи с исполнением поручения.
2.7. Агент не имеет права изменять сроки заездов по путевкам без согласования с Принципалом.
2.8. Агент обязан своевременно производить оплату за реализованные санаторно-курортные услуги в сроки и на условиях, указанных в настоящем договоре.
2.9. Агент обязан своевременно, не менее, чем за 20 дней, направлять Принципалу уведомление об отказе от ранее забронированных мест.
2.10. Принципал принимает клиентов Агента на основании подтвержденной заявки и выдает клиенту Агента санаторно-курортную путевку.
2.11. Принципал обязан выплатить Агенту вознаграждение, указанное в п.1.2 настоящего договора.
2.12. Принципал принимает больных по реализованным Агентом санаторно-курортным путевкам только после оплаты их стоимости и поступления денежных средств на расчетный счет Принципала.
3. Порядок расчетов
3.1. Средства, полученные Агентом за реализованные санаторно-курортные путевки, перечисляются им на расчетный счет Принципала в течение трех дней с момента реализации.
3.2. Сумма вознаграждения выплачивается Агенту Принципалом в течение десяти дней с момента предъявления Агентом отчета.
3.3. Вознаграждение включает в себя расходы Агента на выполнение поручения по настоящему договору, в том числе налоги.
3.4. Цены на санаторно-курортные путевки Принципала устанавливаются в рублях.
4. Ответственность по настоящему договору
4.1. За неисполнение или ненадлежащее исполнение условий настоящего договора Стороны несут ответственности в соответствии с действующим законодательством РФ.
4.2. В случае неисполнения либо ненадлежащего исполнения одной из сторон обязательств по настоящему договору, виновная сторона обязана возместить причиненные таким неисполнением убытки.
5.1. Стороны освобождаются от ответственности за частичное или полное неисполнение обязательств по настоящему договору, если это неисполнение явилось следствием обстоятельств непреодолимой силы, возникших после заключения настоящего договора в результате обстоятельств чрезвычайного характера, которые стороны не могли предвидеть или предотвратить.
5.2. При наступлении обстоятельств, указанных в п. 5.1., каждая из сторон обязана без промедления известить о них в письменном виде другую сторону. Извещение должно содержать данные о характере обстоятельств, а также официальные документы, удостоверяющие наличие этих обстоятельств и, по возможности, дающие оценку их влияния на возможность исполнения стороной своих обязательств по данному договору.
5.3. В случаях наступления обстоятельств, предусмотренных в п. 5.1. настоящего договора, срок выполнения стороной обязательств по настоящему договору отодвигается соразмерно времени, в течение которого действуют эти обстоятельства и их последствия.
6. Конфиденциальность
6.1. Условия настоящего договора конфиденциальны и не подлежат разглашению.
6.2. Стороны принимают все необходимые меры для того, чтобы, их сотрудники, агенты, правопреемники без предварительного согласия другой стороны не информировали третьих лиц о деталях данного договора и приложений к нему.
7. Разрешение споров
7.1. Все споры и разногласия, которые могут возникнуть между сторонами, регулируются в соответствии с действующим законодательством РФ.
8. Заключительные положения
8.1. Договор вступает в силу с момента подписания и действует до 31.12.2009 г.
8.2. Все изменения, дополнения настоящего Договора действительны лишь в том случае, если они оформлены в письменной форме и подписаны обеими Сторонами.
8.3. Настоящий договор составлен в двух экземплярах, имеющих одинаковую юридическую силу, один экземпляр для Принципала, один экземпляр для Агента.
9. Почтовые адреса и реквизиты сторон
Принципал: ЛПУП Санаторий «Ленинские скалы»357530, г. Пятигорск, гора Казачка ИНН 2632053843, Р/с 40703810060090000460 к/с 30101810600000000660БИК 040702660 в Пятигорском отделении № 30 Северо-Кавказскогоотделения АК СБ РФ (ОАО) КПП 263201001Директор - главный врач А.В. Михаэлис
Агент:
Приложение к договору №_________
от “____”____________200___г.
ПРЕЙСКУРАНТ НА МЕДИЦИНСКИЕ УСЛУГИ
ЛПУП Санаторий «Ленинские скалы»
на 2009 год
Категория палаты | Стоимость указана в рублях | |||
Январь - июнь
| Июль - декабрь
| |||
Стоимость 1 койко-дня
| Стоимос-ть на 21 день | Стоимость 1 койко-дня | Стоимость на 21 день | |
«Люкс» |
|
|
|
|
2-х местный 2-х комнатный | 2300 | 48300 | 2500 | 52500 |
1 местный1 комнатный | 2100 | 44100 | 2200 | 46200 |
«Полулюкс» |
|
|
|
|
2-х местный 2-х комнатный | 1800 | 37800 | 2000 | 42000 |
1 местный 1 комнатный | 1700 | 35700 | 1900 | 39900 |
«Базовый уровень» |
|
|
|
|
2-х местный 1 комнатный | 1400 | 29400 | 1500 | 31500 |
1 местный 1 комнатный | 1500 | 31500 | 1700 | 35700 |
Отделение «Мать и дитя» 2-х местный 1 комнатный в т. ч.для матери для ребенка | 2500
1400 1100 | 52500
29400 23100 | 2700
1500 1200 | 56700
31500 25200 |
Гинекологическое отделение 2-х местный 1 комнатный |
1700 |
35700 |
1900 |
39900 |
Неврологическое отделение 2-х местный 1 комнатный |
1700 |
35700 |
1900 |
39900 |
Эндокринологическое отделение 2-х местный 1 комнатный |
1700 |
35700 |
1900 |
39900 |
Заместитель директора-главного
врача по экономическим вопросам ____________________________ В.П. Мальцева
www.len-skaly.ru
Методические указания по выполнению лабораторных работ, страница 11
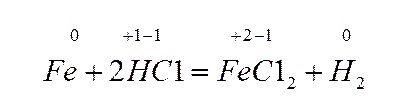
А эта реакция окислительно-восстановительная, т.к. железо и водород изменили степени окисления.
Процессы, происходящие в этой реакции, можно выразить уравнениями:
восстановитель 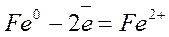 окисление
окисление
окислитель 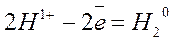 восстановление
восстановление
Атомы железа отдают электроны, при этом степень окисления увеличивается от 0 до +2.
Процесс отдачи электронов называется окислением. Окисление сопровождается увеличением степени окисления.
Ионы водорода присоединяют электроны, их степень окисления уменьшается от +1 до 0.
Процесс присоединения электронов называется восстановлением. Восстановление сопровождается уменьшением степени окисления.
Вещества, молекулы (атомы, ионы) которых отдают электроны в процессе реакции, называются восстановителями, а вещества, молекулы (атомы, ионы) которых присоединяют электроны ‑- окислителями.
Число электронов, отданных в реакции восстановителем, равно числу электронов, присоединяемых окислителем.
Классификация реакций окисления-восстановления
Все окислительно-восстановительные реакции можно разделить на три группы: реакции межмолекулярного окисления-восстановления, реакции диспропорционирования (самоокисления-самовосстановления), реакции внутримолекулярного окисления-восстановления.
Реакция межмолекулярного окисления-восстановления. В таких реакциях обмен электронами происходит между различными атомами, молекулами и ионами. Таковы, например простейшие реакции соединения и замещения:
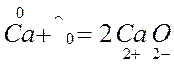
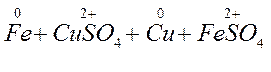
Степень окисления изменяется у меди и железа. Железо повышает степень окисления от 0 до +2, следовательно, является окислителем. Медь понижает степень от +2 до 0 и выступает в качестве восстановителя. Таким образом, обмен электронами происходит между атомами железа и ионами меди.
Реакции внутримолекулярного окисления-восстановления. Если нагревать кристаллический бихромат аммония, то произойдет бурная реакция по схеме:
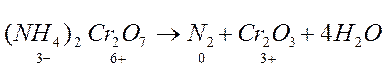
Степень окисления изменилась у хрома и азота. Хром понижает ее от +6 до +3, следовательно, является окислителем. Азот – восстановитель, т.к. повышает степень окисления от -3 до 0. Таким образом, в одной и той же молекуле содержится и окислитель, и восстановитель.
Реакции, в которых одна часть вещества выполняет функцию окислителя, другая – восстановителя, называются реакциями внутримолекулярного окисления-восстановления.
Реакции диспропорционирования (самоокисления-самовосстановления).
Азотистая кислота – вещество нестойкое и быстро разлагается по схеме:
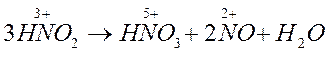
В реакциях диспропорционирования молекулы или ионы одного и того же вещества, содержащие атом с промежуточной степенью окисления, и повышают, и понижают ее, одновременно выступая и в качестве окислителя, и в качестве восстановителя.
В данном случае азот в степени окисления +3 и повысил ее до +5, и понизил до +2.
Ход работы:
Выполняя опыты, разобрать каждую ОВР, т.е.:
– составить схему ОВР;
– определить степени окисления атомов элементов, входящих в состав исходных и конечных веществ, выявить окислитель и восстановитель;
– составить электронные уравнения процессов окисления и восстановления, обеспечивающие электронный баланс;
– расставить стехиометрические коэффициенты в молекулярном уравнении ОВР;
– определить тип ОВР;
– охарактеризовать видимые признаки реакции.
Экспериментальная часть
Опыт 1. Вытеснение водорода из кислоты металлами.
В четыре пробирки налить по 2–3 мл раствора соляной кислоты. В одну пробирку внести кусочек магния, в другую – кусочек железа, в третью – кусочек меди, в четвертую – кусочек цинка.
Опыт 2. Вытеснение свинца цинком из раствора соли свинца.
В пробирку налить 2–3 мл раствора свинца (II) и внести кусочек цинка.
Опыт 3. Окислительные свойства перманганата калия.
В три пробирки налить по 1–2 мл раствора перманганата калия KMnO4. Затем в одну пробирку добавить 0,5–1 мл разбавленной серной кислоты, в другую – 0,5–1 мл воды, в третью – 0,5–1 мл раствора гидроксида калия. После этого во все пробирки добавлять по каплям раствор натрия до изменения окраски раствора.
Опыт 4. Окислительные свойства бихромата калия.
В пробирку налить 1–2 мл бихромата калия K2Cr2O7, 0,5–1 мл серной кислоты и добавлять по каплям раствор сульфита Na до изменения окраски раствора.
Опыт 5. Взаимодействие сульфата марганца (II) c перманганатом калия.
В пробирку налить 1–2 мл раствора сульфата Mn и добавлять по каплям раствор перманганата калия до изменения окраски раствора до желто-коричневого. Написать уравнение реакции учитывая, что Mn2+ и Mn7+ переходят в Mn4+.
Опыт 6. Разложение нитрата меди (вытяжной шкаф).
В пробирку поместить несколько кристаллов нитрата меди (II). Закрепить пробирку в штативе и осторожно нагревать малым пламенем. Написать уравнение реакции разложения нитрата меди учитывая что, продуктами являются оксид меди (II), оксид азота (IV) и кислород.
Лабораторная работа №8
Электролиз в растворах
Цель работы:
Ознакомиться с процессом электролиза в растворах и получить навыки составления уравнения электролиза.
Введение
vunivere.ru
65. Хроматы и дихроматы
Хроматы – соли хромовой кислоты Н2Сг04, существующей лишь водных растворах с концентрацией не выше 75 %. Валентность хрома в хроматах – 6. Хроматы щелочных металлов и магния имеют хорошую растворимость в воде, а растворимость щелочноземельных металлов очень резко снижается в ряду CaCrO4 – SrCrO4 – BaCrO4 – RaCrO4. Хроматы – желтые кристаллические вещества – желтую окраску обеспечивает хромат-ион Сг042- . Дихроматы – соли дихромовой кислоты Н2Сг07 . В отличие от хроматов, почти все соли-дихроматы хорошо растворимы в воде. Дихроматы имеют ярко-оранжевую окраску, обеспеченную дихромат-ионом: Сг072-. Хромат и дихромат-ионы способны к взаимопревращению в зависимости от кислотности среды: если раствор подкислить, то хромат-ионы будут переходить в дихромат-ионы по схеме:
Если добавить щелочи, то пойдет обратная реакция:
Хроматы получают взаимодействием оксида хрома (VI) или раствора хромовой кислоты h3CrO4 с оксидами, гидроксидами, карбонатами металлов или при обменной реакции с участием растворимых солей-хроматов, или путем окисления комплексных солей – гидроксохроматов в избыточном растворе щелочи:
Хромат калия K2CrO 4 – кристаллы желтого цвета, при нагревании краснеют. Кристаллогидратов не образует. Дихроматы – сильные окислители:
Получают дихроматы из соединений Cr (III) в кислой среде:
Дихромат аммония (Nh5)2Cr2O7 – оранжевые кристаллы, не образует кристаллогидратов. При слабом нагревании он самовоспламеняется с выбросом искр – раскаленных частиц Cr2O3 , N2 и паров воды – «химический вулкан».
Дихромат калия K2Cr2O7?2h3O и Na2Cr2O7 – хромпики, оранжево-красные кристаллы, кристаллогидратов не образует. Используется в пиротехнике, в хроматометрии, в производстве спичек. Смесь равных объемов раствора K2Cr2O7 и концентрированной серной кислоты – хромовая смесь – является очень сильным окислителем, в лабораториях применяется для мытья стеклянной посуды. Хроматы применяются для протравы семян, при крашении, в лакокрасочной, кожевенной (в качестве дубящих реагентов кожи), текстильной промышленности; используются в лабораторном способе разделения хрома-тов кальция, стронция и бария.
Наиболее распространенным в природе, минералом является минерал PbCrO 4 – крокоит . Хромат – тарапакаит и дихромат калия – лопецит – также являются природными минералами.
66. Общая характеристика семейства железа
Семейство железа входит в состав побочной подгруппы восьмой группы и является в ней первой триадой, включающей в себя железо, кобальт и никель . Эти элементы имеют два электрона на наружном слое атома, все они являются металлами. По свойствам все три элемента похожи между собой. Для них характерна степень окисления 2, 3, 4. Реже проявляются более высокие степени окисления. Ни один элемент из семейства железа не проявляет максимальной степени окисления +8. Все металлы триады образуют разнообразные соединения, проявляя степени окисления +2 и +3. Проявление высокой степени окисления и амфотерных свойств характерно для железа.
Температуры плавления элементов триады железа высокие, тем не менее, ниже, чем у элементов, находящихся в серединах серий переходных металлов.
Железо – первый элемент в переходных рядах, имеющий спаренный электрон на внутренней d-орбитали. Спаренные электроны с такой орбитали труднее участвуют в образовании химической связи, чем неспаренные. У триады железа существуют особенности орбитального строения, проявляющиеся в виде магнитных и ферромагнитных свойств. В результате ориентированности атомов металлы образуют постоянные магниты. Все металлы семейства железа проявляют электроположительное поведение. Инертны в среде окислителя, даже кислорода, так как образуют оксидные пленки.
Химические свойства железа:
1) взаимодействует с кислородом при высоких температурах;
2) оксиды в низшей степени окисления MO ;
3) при взаимодействии с галогенами образует галогениды, дигалогениды;
4) образует комплексные соединения;
5) образует карбонилы – соединения, в которых переходный металл образует связь с ионом металла или водорода и координированными карбониловыми группами (пентакарбонил кобальта [Co(CO)5]) ;
6) взаимодействуют с серой и сероводородом при нагревании, образуя сульфиды.
Железо – второй (после алюминия) по распространенности металл, встречается в виде различных руд, пригодных для переработки. Из них получают почти чистый Fe3O4 , который вместе с известняком и коксом используется для выплавки чугуна в доменной печи.
Кобальт выделяют из руд, содержащих много мышьяка и некоторой доли серебра, достаточной для промышленной переработки.
Никель – в руде много примесей: сульфиды никеля, меди и железа. Половина получаемого никеля расходуется в производстве стали для повышения ее коррозионной стойкости и твердости. Он используется также для создания прочных покрытий на стальных изделиях.
studfiles.net
Химия хрома и его соединений
Количество просмотров публикации Химия хрома и его соединений - 206
Химия d-элементов
В атомах d-элементов (переходных элементов) заполняется электронами d-подуровень предвнешнего уровня. На внешнем уровне атомы d-элеметов имеют, как правило, два s-электрона. Близость строения валентных уровней атомов переходных элементов определяет их общие свойства. Все они являются металлами, имеют высокую прочность, твердость, высокую электро- и теплопроводность. Многие из них электроположительны и растворяются в минеральных кислотах, однако среди них есть металлы, не взаимодействующие обычным способом с кислотами. Большинство переходных металлов имеют переменную валентность. Максимальная валентность, как и максимальная степень окисления, как правило, равно номеру группы, в которой находится данный элемент.
В природе хром находится в виде хромового железняка FeO×Cr2O3
или Fe(CrO2)2. Хром получают восстановлением хромового железняка углем в электрических печах в виде феррохрома, содержащего 60-65% хрома:
FeO×Cr2O3 + 4CO ® Fe + 2Cr + 4CO2
Чистый хром должна быть получен электролизом растворов или расплавов солей, методом алюминотермии из оксида хрома(III):
Cr2O3 + 2Al 2Cr + Al2O3
Хром представляет собой ковкий тягучий металл серо-стального цвета.
В степени окисления +2 соединения хрома проявляют основные свойства и являются восстановителями - легко окисляются до более высоких степеней окисления.
Оксид хрома(III) должна быть получен разложением дихромата аммония при нагревании:
(Nh5)2Cr2O7N2 + Cr2O3 + 4h3O
Соответствующий ему нерастворимый гидроксид хрома (III) получают при действии недостатка щелочей на соли хрома(III):
СrCl3 + 3NaOH ® Cr(OH)3¯ + 3NaCl
Серо-зеленый гидроксид хрома (III) имеет амфотерные свойства:
Cr(OH)3¯ + 3HCl ® CrCl3 + 3h3O
Cr(OH)3¯ +3NaOH ® Na3[Cr(OH)6]
Соединения хрома (III) в щелочной среде имеют восстановительные свойства и окисляются бромом, пероксидом водорода или другими окислителями. Зеленый раствор гексагидроксохромата(III) натрия желтеет вследствие образования хромата натрия:
2Na3[Cr(OH)6] + 4NaOH + 3Br2 ® 2Na2CrO4 + 6NaBr + 8h3O
Оксид хрома(VI) имеет кислотные свойства. Ему соответствуют две кислоты: хромовая h3CrO4 и дихромовая h3Cr2O7:
CrO3 + h3O ® h3CrO4
2CrO3 + h3O ® h3Cr2O7
В водных растворах между желтыми хромат ионами и оранжевыми дихромат ионами наблюдается равновесие:
2CrO42- + 2H+ ® Cr2O72- + h3O
Это равновесие в кислой среде сдвигается в сторону образования дихромат-ионов, а в щелочной среде - в сторону хромат-ионов:
2K2CrO4 + h3SO4 ® K2Cr2O7 + K2SO4 + h3O
K2Cr2O7 + 2KOH ® 2K2CrO4 + h3O
Существующие в кислой среде дихроматы являются сильными окислителями, восстанавливаясь до соединений хрома(III):
K2Cr2O7 + 4h3SO4 + 3K2SO3 ® Cr2(SO4)3 + 4K2SO4 + 4h3O
K2Cr2O7 + 7h3SO4 + 6KI ® Cr2(SO4)3 + 3I2 + 4K2SO4 + 7h3O
referatwork.ru
Дихромат аммония • ru.knowledgr.com
Дихромат аммония - неорганический состав с формулой (NH) CrO. В этом составе, как во всех хроматах и дихроматах, хром находится в +6 степенях окисления, обычно известных как hexavalent хром. Это - соль, состоящая из ионов аммония и ионов дихромата.
Дихромат аммония иногда известен как Огонь Vesuvian из-за его использования в демонстрациях стола «вулканы». Однако эта демонстрация стала непопулярной в школах из-за канцерогенного характера состава. Это также использовалось в пиротехнике и в первые годы фотографии.
Свойства
При комнатной температуре и давлении, состав существует как апельсиновые, кислые кристаллы, разрешимые в воде и алкоголе. Это сформировано действием хромовой кислоты на гидроокиси аммония с последующей кристаллизацией.
Кристалл CrO (NH) (C2/c, z=4) содержит единственный тип иона аммония на местах симметрии C (2,3). Каждый центр NH окружен нерегулярно восемью атомами кислорода в N — O расстояния в пределах от приблизительно 2.83 приблизительно к 3.17 Å, типичным для водородных связей.
Использование
Это использовалось в пиротехнике и в первые годы фотографии, а также в литографии как источник чистого азота в лаборатории, и как катализатор. Это также используется в качестве протравы для того, чтобы окрасить пигменты, в производстве ализарина, хромовых квасцов, дубления кожи и нефтяной очистки.
Светочувствительные фильмы, содержащие ПВА, дихромат аммония и фосфор, покрыты вращением как водные жидкие растворы в производстве люминесцентного растра телевизионных экранов и других устройств. Дихромат аммония действует как светочувствительное место.
Реакции
Настольные вулканы и тепловое разложение
Демонстрация вулкана включает разжигание груды соли, которая начинает следующее экзотермическое преобразование:
: → + + 4 (ΔH =−429.1 ± 3 ккал/молекулярных масс)
Как известный взрывчатый нитрат аммония, это термодинамически нестабильно. Его реакция разложения продолжается к завершению однажды начатый, производящий пространный темно-зеленый порошкообразный хром (III) окись. Не весь дихромат аммония разлагается в этой реакции. Когда зеленый порошок принесен в воду, желтое/оранжевое решение получено из перенесенного дихромата аммония.
Полученное использование наблюдений относительно высокой микроскопии усиления во время кинетического исследования теплового разложения дихромата аммония представило свидетельства, которые солят аварийные доходы с вмешательством промежуточной жидкой фазы, а не твердой фазы. Характерное затемнение кристаллов в результате начала разложения может быть приписано разобщающей потере аммиака, сопровождаемого прогрессивным уплотнением аниона к, и т.д., в конечном счете уступив. Идентифицированный как возможное литое промежуточное звено, участвующее в разложении.
Реакции окисления
Дихромат аммония - сильный агент окисления и реагирует, часто яростно, с любым уменьшающим агентом. Чем более сильный уменьшающий агент, тем более сильный реакция. Это также использовалось, чтобы продвинуть окисление alcohols и thiols. Дихромат аммония, в присутствии Mg (HSO) и влажного SiO может действовать как очень эффективный реактив для окислительного сцепления thiols под растворяющими свободными условиями. Реакции производят довольно хорошие урожаи при относительно умеренных условиях. Состав также используется в окислении алифатического alcohols к их соответствующим альдегидам и кетонам в ZrCl/wet SiO в растворяющих свободных условиях, снова с относительно высокими выработками.
Безопасность
Дихромат аммония, как весь хром (VI) составы, очень токсичен и доказанное канцерогенное вещество. Это - также сильный раздражитель.
Инциденты
В запечатанных контейнерах дихромат аммония, вероятно, взорвется, если нагрето. 19 января 1986 Нью-Йорк Таймс сообщила, что два рабочих были убиты, и 14 других ранены в Алмазных Химикатах Трилистника, Эштабуле, Огайо, когда 2 000 фунтов дихромата аммония взорвались, поскольку это сушилось в нагревателе.
Внешние ссылки
ru.knowledgr.com
Окислительные свойства дихроматов - Справочник химика 21
Задания. Составить уравнение окислительно-восстановительной реакции разложения дихромата аммония при нагревании с образованием оксида хрома(П1), азота и воды. Сделать вывод о свойствах оксида хрома (П1) и термической устойчивости дихромата аммония. [c.196]Дихромат К2СГ2О7 и хромат калия К2СГО4 проявляют окислительные свойства обычно в кислой среде, восстанавливаясь до соединений хрома(П1) [c.240]
Опыт 7. Окислительные свойства дихроматов. Двухромовая кислота является сильным окислителем. Так как двухромовая кислота в свободном состоянии не выделена, то применяют смесь ее соли — дихромата с кислотой. Являясь окислителем, ион Сг О восстанавливается до иона Сг + [c.244]Дихромат калия проявляет сильные окислительные свойства в кислой среде [c.516]
Выполнение. В стаканы налить растворы дихромата калия и вольфрамата калия, подкислить серной кислотой. После добавления иодида калия в стакан с дихроматом наблюдается обильное выделение иоДа — хромовая кислота сильный окислитель. Прибавление иодида калия к раствору вольфрама не сопровождается выделением, иода,— для вольфрамовой кислоты окислительные свойства не характерны. [c.185]
III). Гидроксиды железа (II) и (III). Их свойства. Комплексные соединения железа. Химические реакции, лежащие в основе получения чугуна и стали. Роль железа и его сплавов в технике. Хром, электронная формула, степени окисления. Получение, физические и химические свойства хрома. Оксиды хрома (II) и (III). Гидроксиды хрома (II) и (III). Их свойства. Оксид хрома (VI). Хромовая и дихромовая кислоты. Дихромат калия как окислитель. Марганец, злектронная формула, степени окисления. Получение, физические и химические свойства марганца. Кислотно-основные и окислительно-восстановительные свойства соединений марганца. Оксиды марганца (II) и [c.9]
Соединения хрома (VI) как правило, проявляют окислительные свойства. Дихромат-ион СггО — типичный окислитель в кислотной среде [c.240]
Окислительные свойства дихроматов [c.261]
Окислительные свойства дихромата калия [c.144]
Чтобы составить уравнение окислительно-восстановительной реакции, надо знать свойства взаимодействующих веществ и на их основе предугадать образование новых. Окончательно вопрос о продуктах реакции может быть решен экспериментально. Например, при взаимодействии сероводорода с дихроматом калия в кислой среде изменяется цвет раствора из оранжевого в зеленый, характерный для соединений хрома (П1) раствор мутнеет вследствие выпадения в осадок серы. Запись исходных и конечных веществ реакции с указанием изменения степени окисления атомов выглядит так [c.228]
Хроматы и дихроматы — сильные окислители. Особенно сильные окислительные свойства онн проявляют з кислой среде [c.271]
Окислительные свойства дихромата калия. Налить в пробирку 2—3 мл раствора дихромата калия К2СГ2О7, Подкислить серной кислотой (3—5 капель). Добавить 2—3 мл раствора сульфита натрия NajSOs, Наблюдать изменение окраски раствора от оранжевопу (цвет иона СггО ) до зеленого (цвет иона Сг +). В результате реакции ионы 50з окисляются в ионы S04 , Составить уравнение реакции. [c.258]
При избытке в растворе ионов водорода (кислая среда) хромат-ионы переходят в дихромат-ионы, а при избытке гидроксильных ионов (щелочная среда) наблюдается обратное явление. Кислородсодержащие соединения хрома обладают окислительными свойствами, как правило, в кислой среде. Процесс восстановления хрома происходит по таким схемам [c.22]
ОКИСЛИТЕЛЬНЫЕ СВОЙСТВА ДИХРОМАТА КАЛИЯ [c.136]
Почему при взаимодействии солей бария с растворами хромата и дихромата калия выпадают осадки одинакового состава Рассмотрите окислительные свойства К2СГ2О7 при различных pH растворов. [c.136]
Окислительные свойства соединений хрома (VI). 1. В три пробирки внесите по нескольку капель раствора дихромата калия и подкислите их одной-двумя каплями раствора разбавленной серной кислоты. В первую пробирку прибавьте несколько капель раствора иодида калия, во вторую — сульфата железа (II), в третью — нитрита калия или натрия. Последнюю пробирку слегка подогрейте. Напишите уравнения реакций в молекулярной и ионной формах. [c.153]
Хроматы и дихроматы — сильные окислители. Наиболее сильно окислительные свойства проявляются в кислой среде, при этом соединения хрома(VI) восстанавливаются до соединений хрома(III). [c.195]
Хроматы и дихроматы как соли хромовых кислот обладают, особенно в кислой среде, сильными окислительными свойствами. Так, при обыкновенной температуре они легко восстанавливаются в соединения хрома со степенью окисления хрома +3 [c.202]
Примеры (в показателе степени указана высшая степень окисления элемента) Мп+7 — основа высоких окислительных свойств перманганата калия КЛ п04, — азотной кислоты НХОз и ее солей, Сг+ — дихромата калия КоСгоО, и т. д. [c.267]
Активными окислителями являются СгОз, хроматы и дихроматы особенно сильные окислительные свойства проявляет дихромат калия К2СГ2О7 в кислой среде [c.343]
Многие вещества в химических реакциях наиболее часто проявляют восстановительные свойства, другие вещества — окислительные. Так, к типичным восстановителям относятся металлы, водород, бескислородные кислоты — HjS, H l, НВг, HI и их соли, соли железа (И) и некоторых других металлов в низких степенях окисления. Окислительные свойства проявляют галогены, кислород, серная кислота, перманганат калия KMnOi, дихромат калия КгСг О,, хромат калия К СгО и многие другие вещества. [c.70]
Свойства каждого элемента охарактеризованы свойствами веществ, в состав которых входит этот элемент. Многоэлементные вещества отнесены к разделу того элемента, который определяет главные химические свойства всего вещества. Папример, химические свойства веществ К2СГ2О7 и КМГ1О4 представлены в разделах, посвященных соединениям хрома и марганца (а не в разделе соединений калия), поскольку в большинстве реакций этих веществ катионы калия К+ участия не принимают, а просто переходят из реагентов в продукты, тогда как дихромат-ион СггО и перманганат-ион МпО 4 определяют главное для этих веществ — их сильные окислительные свойства. [c.4]
Высший оксид хрома СгОз обладает ярко выраженными окислительными свойствами. Он реагирует со взрывом со многими органическими веществами. Триоксид хрома - это типичный кислотный оксид. Ему соответствуют сильные хромовая Н2СГО4 и дихромовая Н2СГ2О7 кислоты, известные только в растворе. В зависимости от кислотности среды анионы дихромата и хромата Сг04 могут переходить друг в друга. Первый из них устойчив в кислой среде, а второй - в щелочной [c.348]
Мы видим, что меньший по размеру атом хрома относительно легко теряет 8-электроны, отрыв же -электрона, судя по величине третьего потенциала ионизации, требует затраты энергии почти на 4 эВ больше, чем в случае молибдена, и на 7 эВ больше, чем в случае вольфрама. Соответственно, для хрома в твердых соединениях и в растворах наиболее характерна достаточно низкая степень окисления +3, а для молибдена и вольфрама +6. Производные хрома(У1) - хроматы и дихроматы - сильные окислители, а мо-либдаты и вольфраматы совершенно не проявляют окислительных свойств и входят в состав руд этих металлов (например, повеллит СаМо04 и шеелит Са У04). С другой стороны, низкие степени окисления малохарактерны для молибдена и вольфрама, в отличие от хрома, они совсем не образуют аквакатионов в водных растворах. Под действием царской водки и азотной кислоты при нагревании металлический молибден медленно переходит в раствор в виде сложной смеси анионных форм Мо(У1), содержащих от одного до 24 атомов молибдена. Напомним, что полимеризация хрома(У1) ограничена образованием дихроматов СГ2О7. Вольфрам практически не растворяется в кислотах, но косвенными методами могут быть получены многочисленные поливольфраматы (подробнее о них см. в разд. 29.3). [c.368]
Выполнение работы. В первую пробирку с раствором дихромата калия Kj r.jO, и во вторую с раствором сульфида натрия Na S внести по нескольку капель 2 н.-серной кислоты и по 2—3 микрошпателя сульфита натрия NajSO ,. Как изменилась окраска в первой пробирке Почему помутнел раствор во второй пробирке Окислителем или восстановителем может являться в химических реакциях Ka . Oj Na S Окислительные или восстановительные свойства проявляет NajSO , Написать уравнения проведенных реакций. [c.97]
Чистота посуды имеет особое значение. Посуду для анализа тщательно промывают после каждого употребления. Особенно эффективное средство очистки стекла и фарфора — хромовая смесь (дихроматЧ-серная кислота), которую готовят растворением 20—30 г измельченного дихромата калия или натрия в 1 дм h3SO4 (конц.). Очищающая способность этой жидкости заключается в ее окислительном действии. Безводная смесь может реагировать с органическими веществами даже со взрывом, о чем нужно помнить при обработке сосудов с неизвестным содержимым. При разбавлении хромовая смесь теряет свои свойства, ее хранят в толстостенных закрытых сосудах. Если смесь приобретает зеленый цвет (хром восстановлен), она становится непригодной для работы. Для очистки шлифов от смазки лучше использовать органические растворители — бензин, бензол или тетрахлорид углерода. [c.240]
Окислительно-восстановительные свойства нитритов, а. Восстановительные свойства. Налить в пробирку 2—3 мл раствора дихромата калия К2СГ2О7, 2—3 мл разбавленной серной кислоты (для подкисления), 3—4 мл раствора какой-либо соли азотистой кислоты — KN02 или NaN02. Осторожно нагреть. Наблюдать изменение окраски раствора. Написать уравнение окислительновосстановительной реакции, показать схему перемещения электронов. [c.176]
В третьей части гл. 3 Вам следует усвоить элек-тронно-ионный метод составления окислительно-восстановительных реакций. Известный Вам метод электронного баланса для многих реакций оказывается неприменимым, так как в этом методе подсчет числа участвующих в реакции электронов производится по изменению валентности элемента. Во многих же случаях валентность элемента невозможно не только сосчитать, но и определить экспериментально. Научившись составлять окислительно-восстановительные реакции электронно-ионным методом, Вы сможете пользоваться формулой Нернста для нахождения потенциалов и э. д. с. гальванических элементов при любых концентрациях реагирующих веществ в водных растворах. В третьей части много внимания будет уделено свойствам галогенов и реакциям с участием перманганата и дихромата калия. [c.91]
chem21.info
Аммония дихромат, термическое разложение - Справочник химика 21
Опыт 27. Термическое разложение на примере дихромата аммония и роданида ртути [c.78]Опыт 2. Термическое разложение дихромата (VI) аммония [c.37]
Задания. Составить уравнение окислительно-восстановительной реакции разложения дихромата аммония при нагревании с образованием оксида хрома(П1), азота и воды. Сделать вывод о свойствах оксида хрома (П1) и термической устойчивости дихромата аммония. [c.196]
ТЕРМОХИМИЯ Опыт 56. Термическое разложение дихромата аммония [c.38]Реакция термического разложения дихромата аммония идет с выделением большого количества газообразных продуктов по уравнению [c.112]
Оксид хрома (II) представляет собой порошок черно-зеленого цвета, практически нерастворимый в воде, кислотах, щелочах. Лабораторным способом получения СггОз является термическое разложение дихромата аммония (NH,) СГ2О7 СгзОз + N2 + 4Н2О. [c.40]
Составьте уравнения термического разложения следующих солей аммония карбонат, хлорид, сульфат, дихромат, гидросульфид. [c.233]
Рассмотрите реакции термического разложения дихромата и хромата аммония. Какие свойства соединений хрома (V ) проявляются в этих реакциях [c.138]
Опыт 119. Термическое разложение дихромата аммония ( вулкан ). [c.85]
Проводят термическое разложение твердого дихромата аммония. Рассчитайте энтальпийггый фактор (кДж) этой реакции и объясните, почему после инициирования реакции раскаленной стеклянной палочкой она в дальнейшем протекает без внешнего нагревания. Не прибегая к расчету, укажите знак энтропийного фактора этой реакции. Способствует ли такой энтропийный фактор протеканию реакции [c.287]
Напишите уравнение предполагаемых реакций разложения хромата аммония с выделением азота и разложения дихромата аммония с выделением азота и аммиака. Для всех предполагаемых и реально проходящих реакций рассчитайте А 0298. Сформулируйте выводы. Приведите любые соображения по причинам образования различных продуктов при термическом разложении этих солей. [c.292]
Важной аналитической особенностью дихроматов аммония, калия, натрия как наиболее распространенных соединений хрома является их термическое разложение, сопровождающееся восстановлением Сг (VI) до Сг (III). Одновременно выделяются Nj или СО [c.211]
Напишите уравнения реакций, описывающие термическое разложение дихроматов калия и аммония. Что общего и что различного в этих реакциях [c.137]
Для производства искусственных рубинов сплавляют оксид, содержащий 53 % металла А (III), с небольшим количеством оксида металла В (III), который получают термическим разложением дихромата аммония. Назовите металлы А и В, [c.261]
Проведено термическое разложение 54,29 г дихромата аммония, содержащего инертные примеси. После окончания реакции собрано 4,45 л газа при 18° С под давлением 1-10 Па. Определите массовую долю (%) дихромата аммония в техническом продукте. [c.287]
Техника безопасности. При измельчении дихромата аммония в ступке не допускать его пыления — соли хрома ядовиты. Термическое разложение дихромата аммония сопровождается выбросом раскаленных частиц. Во избежание попадания частиц в глаза не наклоняться над реакционным сосудом. Опыт проводить под тягой. [c.196]
При вза и1модействии1 щелочи с хлоридом М еталла (1П) выпадает осадок зеленого цвета, который при нагревании теряет воду, и образуется оксид соответствующего металла — тугоплавкое темно-зеленое вещество, n p им eняeм oe для изготовления масляных красок. Такое же кол1Ичвство окоида металла можно получить при термическом разложении 50,4 г дихромата аммония. Рассчитайте количество исходного хлорида металла (III). [c.15]
Оксид хрома(Ш) СГ2О3 отличается очень высокой устойчивостью на него не действуют вода, кислоты и щелочи в водном растворе. Перевести его в растворимые соединения можно лишь сплавлением со щелочами или дисульфатом натрия КазЗгО . В лаборатории СГ2О3 полз ают термическим разложением дихромата аммония. [c.232]
Составьте уравнения реакций термического разложения нитрата, нитрита, фосфата, хлорида и дихромата аммония. Как доказать, что перечисленные соли являются солями аммония [c.123]
В лаборатории СГ2О3 получают термическим разложением до дихромата аммония [c.380]
Оксид хрома (+3) представляет собой порошок черно-зеленого цвета, нерастворимый в воде, кислотах и щелочах. Удобным лабораторным способом получения СгаОз является термическое разложение дихромата аммония (Nh5)2 r20, по схеме [c.337]
Какие оксиды получают при термическом разложении дихромата аммония и вольфромата аммония Напишите уравнения этих реакций и укажите различие в их характере. [c.321]
Комм. Чем объясняется переход окраски раствора из желтой в оранжевую и обратно (П1) Как меняется кислотно-основный характер соединений хрома с изменением степени окисления от -(-П до -I-VI Используя литературные данные, оцените термическую устойчивость оксидов хрома(П), хрома(П1) и хрома(У1). Чем объясняется различие в химической растворимости оксидов и гидратов оксидов молибдена и вольфрама в степени окисления -1-У1 в кислотах Почему термическое разложение молибдата(У1) и вольфра-мата(У1) аммония ведет к образованию оксидов М0О3 и WO3, в то время как при термическом разложении дихромата аммония полу- [c.236]
По кристаллической структуре СпгОз подобен оксиду алюминия (корунду). Получают оксид хрома (П1) синтезом из простых веществ, а также термическим разложением гидроксида, дихромата аммония или восстановлением дихроматов щелочных элементов углеродом, серой [c.451]
chem21.info










