Способ получения окиси хрома. Способ получения окиси хрома
Способ получения окиси хрома
ОП ИСАНИЕ
ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
Союз Советских
Соцналистнческих
Республик («)668879 (61) Дополнительное к авт. свид-ву(22) Заявлено 030878(2() 2518341/23-26 с присоединением заявки ¹(23) Приоритет(51)М. Кл.
С 01 G 37/02
Государственный комитет
СССР ио делая изобретений и открытий ($3) УДЯ661. 876. 12 . (088.8) Опубликовано 250679. Бюллетень № 23
Дата опубликования описания 28.06,79 (72) АвтО(ВЬ6 изобретен кл
В. А. Пахомов, A. A. Ваулина, Н. П. Пьянкова, В. А. Попов, В. 3. Горяйнов и Н. С. Ягодин (73) Заявитель (54) СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ХРОМА
Изобретение относится к технологии получения окиси хрома реактивной квалификации, используемой в химическом анализе.
Известен способ получения окиси хрома путем восстановления двухромо.вокислого.калия углеводами, например сахаром, при повышенной температуре (11.
Известен также способ получения окиси хрома путем термического разложения хромового ангидрида с последующим выщелачиванием примесей при рН-7 методом многократной декантации,15 отделением промывкой и сушкой осадка (21.
Недостатками этого способа являются повышенное содержание примесей в продукте (Cr+ 0,01%, So, 0,05%), 20 а также длительность процесса иэ-за стадии отмывки, общая продолжительность которых 19 ч.
Целью изобретения является сниже- ние содержания примесей в продукте и ускорение процесса.
Поставленная цель достигается предлагаемым способом-получения окиси хрома путем термического разложения хромового ангидрида, выщелачивания примесей при рН 9-10 с последующим подкислением пульпы до рН 5-6.
При значении рН пульпы ниже 9 снижается степень выщелачивания примесей. При рН более 10 наблюдается плохое отстаивание пульпы вследствие зависания мелкой фракции окиси хрома, для устранения которого требуется дополнительный расход кислоты на уменьшение щелочности пульпы.
При подкислении пульпы до рН 5-6 окись хрома не адсорбирует примеси и может быть легко от них отмыта.
Изобретение иллюстрируется примерами по прототипу (пример 1) и по изобретению (пример 2).
Пример 1. В бак-реактор с мешалкой емкостью 5 м загружают
1035 кг технической окиси хрома, полученной путем термического разложения хромового ангидрида с содержанием не менее 99% Crz О, не более
0,06% ЯО,, не более 0,05% CrOq u
1500 л конденсата.
Полученную пульпу окиси хрома нагревают до кипения и кипятят в течение 10-15 мин. Пульпу после кипячения отстаивают в течение 1 ч. Осветленный раствор сливают, а осадок окиси хрома снова заливаюв горячим конденсатом и
668879
Формула изобретения
Составитель C. Лотхова
Редактор Т. Иванова Техред С. Мигай Корректор С. Иекмар
3акаэ 3579/14 Тираж 590 Подписное
ЦЯИИПИ Гссударственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП Патент, г. Ужгород, ул. Проектная, 4 повторяют вышеуказанный цикл промывки декантацией 8-10 раз. Общая продолжительность промывки 19-21 ч. Пульпу промытой окиси хрома отфильтровывают, например, на нутч-фильтре. Полученный осадок окиси хрома сушат при температуре не более 150 С. 5
Полученный продукт содержит в пересчете на 99% Сг О . 0,01Ъ CrO ;
0,05% SQ т.е. удовлетворяет требованиям норм только для квалификации ч (чистый) . 10
Пример 2. В бак-выщелачиватель загружают 1010 кг технической окиси хрома, полученной путем термического разложения хромового ангидрида с содержанием не менее 99% Ск З,, Ы не более 0,06% SOq не более 0,05%
CrOq и конденсат до соотношения Т:Ж=
1:(2,6-4,0) . Пульпу псдщелачиваюж кальцинированной содой до рН 9,5-0,5, о нагревают до 95 С и интенсивно пере- щ мешивают. Полученную пульпу окиси хрома разбавляют конденсатом до соотношения. Т:Ж 1:(7-10) и одновременно подкисляют серной кислотой до рН
5,5 -0,5 °
Обработанную таким образом пульпу окиси хрома передают на фильтрацию.
Осадок окиси хрома смывают конденсатом в бак, где осуществляют реПульпацию его конденсатом при соотношении
Т:Ж 1:(7-10) и 95 С . После 5-6-раэовой репульпации и фильтрации осадок отмытой окиси хрома передают на сушку в вакуум-сушилку. Сушку проводят при температуре не более 150 С..
Полученный продукт содержит, в пересчете на 99% Cry Og . 0,002-0,003%
CrOу ю 0 005-0 р 010% ЯОф °
Предлагаемый способ дает воэможность гарантированно получить реактив ную окись хрома, соответствующую требованиям норм для реактива кзалификации чда .
Способ получения окиси хрома путем термического разложения хромово-. га ангидрида, выщелачивания примесей из образовавшейся окиси хрома, отделения, промывки и сушки осадка, о тл и ч а ю шийся тем, что, с целью снижения содержания примесей и ускорения процесса, выщелачивание примесей ведут при рН 9-10 с последующим подкислением пульпы до рН 5-6.
Источники информации, принятые во внимание при экспертизе
1. Карякин В. 3., Ангелов И. И. Чистые химические вещества, Химия, 1974, с. 388.
2s Авербух Tе Д Павлов П Ге Технология соединений хрома, Л. Химия, 1967, с. 281-282.


www.findpatent.ru
Способ получения окиси хрома | Банк патентов
Изобретение относится к способам получения окиси хрома, которая может быть использована для производства магнитных носителей, а также для производства грунтовок, эмалей, красок, полировальных паст, производства абразивного материала и металлического хрома.
Известные способы получения окиси хрома основаны, как правило, на термическом разложении CrO3 или восстановлении Na2CrO4 элементарной серой (хроматно-серный метод) - см. Авербух Т.Д., Павлов П.Г. Технология соединений хрома. Л.: Химия, 1973, с.216.
Известно получение пигментной окиси хрома термическим разложением CrO3 при температуре 900-1150°С (см. Авербух Т.Д., Павлов П.Г. Технология соединений хрома. Л.: Химия, 1973, с.217).
Недостатком данного способа получения пигментной окиси хрома является низкое качество готового продукта, обусловленное высокой температурой прокалки и получением частиц окиси хрома большого размера: средний размер частиц составляет около 5 мкм, при этом пигмент имеет темный цвет, причем содержание Cr2О3 в готовом продукте не превышает 99%.
Известно получение абразивной окиси хрома термическим разложением CrO3 (см. авторское свидетельство СССР №1701635, МПК C 01 G 37/02, приоритет от 15.11.89, опубликованное 30.12.1991 г. "Способ получения оксида хрома для полирования").
Недостатком данного способа получения абразивной окиси хрома является низкое качество готового продукта, обусловленное низким содержанием Cr2O3, не превышающим 98%, и наличием примесей, которые не позволяют получить однородные по размеру частицы окиси хрома и обеспечить высокие потребительские свойства окиси хрома для полирования.
Известно получение окиси хрома для магнитных носителей термическим разложением CrO 3 (см. авторское свидетельство СССР №1570996, МПК C 01 G 37/027, приоритет от 20.07.87., опубликованное 15.06.1990 г. "Способ получения порошка двуокиси хрома для носителей магнитной записи").
Получаемая известным способом окись хрома содержит большое количество примесей серы, углерода, кремния SiO2, железа FeO, что не позволяет получить высокоплотную, высокочастотную запись из-за неоднородности зернового состава и величины среднего удельного объема частиц, лежащего в разнодоменной области.
Известен способ получения пигментной окиси хрома восстановлением хромата натрия серой (см. авторское свидетельство СССР №226573, МПК C 01 G 37/02, приоритет от 28.04.1966 г., опубликованное 03.06.1970 г. "Способ получения окиси хрома").
Известен способ получения абразивной окиси хрома восстановлением хромата натрия серой (см. авторское свидетельство СССР №236447, МПК C 01 G 37/02, приоритет от 20.07.1964 г., опубликованное 05.08.1969 г. "Способ получения окиси хрома для полирования").
Известен способ получения пигментной и металлургической окиси хрома путем восстановления соединений шестивалентного хрома Na2CrO4 в щелочном растворе серой (см. авторское свидетельство СССР №343567, МПК C 01 G 37/02, приоритет от 06.04.1970 г., опубликованное 03.11.1972 г. "Способ получения окиси хрома").
Известно также получение металлургической окиси хрома хроматно-серным методом (см. Авербух Т.Д., Павлов П.Г. Технология соединений хрома. Л.: Химия, 1973, с.216-217).
Вышеперечисленные способы получения окиси хрома хроматно-серным методом достаточно сложны, а конечный продукт содержит большое количество примесей, что ухудшает потребительские свойства окиси хрома, например, пигментная окись хрома имеет неудовлетворительные цветовые качества и физико-малярные свойства, а абразивная окись хрома имеет неудовлетворительные полирующие свойства.
Наиболее близким по совокупности существенных признаков к заявляемому изобретению является способ получения окиси хрома путем восстановления бихромата натрия сульфатом аммония, заключающийся в том, что смесь бихромата натрия и сульфата аммония подвергают термическому разложению в течение 6 часов при температуре 700-800°С с дальнейшим вымыванием сульфатов до получения готового продукта - окиси хрома, причем в качестве соли аммония используют сульфат аммония (см. патент Германии №728233, НПК 22 f 7, приоритет от 03.04.1940 г., опубликованный 23.11.1942 г. "Способ получения пигментной окиси хрома").
Известный способ получения окиси хрома является трудоемким, так как требует нескольких стадий выщелачивания (отмывки) готового продукта от сульфата натрия Na2SO4, которого в готовом продукте содержится до 50%.
Кроме того, с помощью известного способа невозможно получить окись хрома иного назначения, кроме пигментной, так как повышение температуры термического разложения свыше заявленной (700-800°С) ведет к плавлению сульфата натрия и образованию намотов в барабанных печах, в которых осуществляют термическое разложение, а также образованию агломератов готового продукта, затрудняющих его термическое разложение и снижающих качество получаемой окиси хрома, содержание которой в готовом продукте не превышает 98%.
Техническим результатом заявляемого изобретения является упрощение способа получения окиси хрома, повышение качества окиси хрома за счет уменьшения примесей и повышения содержания Cr2О3 в готовом продукте, а также возможность получения окиси хрома различного назначения.
Заявляемый технический результат достигается тем, что в способе получения окиси хрома, включающем разложение бихромата натрия и сульфата аммония с последующим вымыванием полученной окиси хрома, согласно изобретению первоначально осуществляют обменное разложение бихромата натрия и сульфата аммония, которое ведут в растворе с концентрацией 400-450 г/л по CrO3 при температуре 100-105°С в течение 45-60 минут при постоянном перемешивании с получением бихромата аммония и сульфата натрия, причем последний затем отделяют от раствора, а раствор, содержащий бихромат аммония, охлаждают до температуры его кристаллизации, после чего осуществляют термическое разложение кристаллов бихромата аммония при температуре 440-1400°С до образования окиси хрома.
Обменное разложение бихромата натрия Na2Cr2O7 и сульфата аммония (Nh5)2SO4 в растворе с концентрацией 400-450 г/л по CrO3 при температуре 100-105°С в течение 45-60 минут при постоянном перемешивании позволяет весь бихромат натрия перевести в бихромат аммония за счет прохождения следующей химической реакции:
Образующийся при этом сульфат натрия Na2SO 4 кристаллизуется и выпадает в осадок.
При концентрации раствора бихромата натрия Na2Cr2O7 и сульфата аммония (Nh5)2SO 4 менее 400 г/л по CrO3 кристаллизация сульфата натрия Na2SO4 не происходит; при концентрации раствора бихромата натрия Na2Cr2O7 и сульфата аммония (Nh5)2SO 4 более 450 г/л по CrO3 обменное разложение бихромата натрия Na2Cr2O7 и сульфата аммония (Nh5)2SO4 затрудняется в связи с преждевременной кристаллизацией сульфата натрия Na 2SO4, в результате чего реакция (1) протекает не в полном объеме.
Химическое разделение продуктов реакции и отделение сульфата натрия Na2SO4 от раствора бихромата аммония исключает необходимость многостадийного вымывания сульфатов и упрощает способ получения окиси хрома.
Охлаждение очищенного от кристаллов сульфата натрия раствора бихромата аммония (Nh5)2Cr2O7 до температуры его кристаллизации позволяет перевести бихромат аммония (NH 4)2Cr2O7 в кристаллическое состояние.
Термическое разложение кристаллического бихромата аммония (Nh5)2Cr2O7 при температуре 440-1400°С до образования окиси хрома обеспечивает возможность получения окиси хрома различного назначения в зависимости от конкретной температуры, лежащей в защищаемых пределах, а именно:
- при термическом разложении бихромата аммония (NH 4)2Cr2O7 при температуре 440-450°С образуется окись хрома, которая используется для магнитных носителей;
- при термическом разложении бихромата аммония (Nh5)2Cr2O7 при температуре 800-900°С образуется мелкокристаллическая пигментная и абразивная окись хрома;
- при термическом разложении бихромата аммония (Nh5)2Cr 2O7 при температуре 1200-1400°С образуется крупнокристаллическая металлургическая окись хрома.
Вымывание полученной окиси хрома Cr2O3 позволяет окончательно отмыть окись хрома Cr2O3 от водорастворимых солей, что способствует уменьшению примесей до минимальных величин.
В результате заявляемый способ позволяет упростить процесс получения окиси хрома за счет исключения многостадийной отмывки готового продукта от сульфата натрия Na2SO 4, повысить качество окиси хрома за счет исключения примеси сульфата натрия и повышения содержание окиси хрома Cr 2O3 в готовом продукте, составляющем более 99%, а также обеспечить возможность получения окиси хрома различного назначения.
Технических решений, совпадающих с совокупностью существенных признаков заявляемого изобретения, не выявлено, что позволяет сделать вывод о соответствии заявляемого изобретения такому условию патентоспособности как "новизна".
Заявляемые существенные признаки, предопределяющие получение указанного технического результата, явным образом не следуют из уровня техники, что позволяет сделать вывод о соответствии заявляемого изобретения такому условию патентоспособности, как "изобретательский уровень".
Условие патентоспособности "промышленная применимость" подтверждается примерами конкретного выполнения, изложенными в разделе "Сведения, подтверждающие возможность осуществления изобретения".
Для получения окиси хрома используют следующее сырье:
1. Раствор бихромата натрия Na2Cr2O 7, концентрации 800-1000±100 г/л по CrO3 ;
2. Сульфат аммония кристаллический (Nh5) 2SO4 с содержанием азота не менее 21%.
Исходный раствор готовят следующим образом.
В раствор бихромата натрия Na2Cr2O7 концентрации 800-1000 г/л по CrO3 добавляют упаренный до концентрации 300-350 г/л по CrO3 маточный раствор бихромата аммония (Nh5)2Cr2O7, возвращаемый в процесс после стадии отделения кристаллов бихромата аммония (Nh5)2Cr2O7. Компоненты смешивают в баке до получения раствора с концентрацией 400-450 г/л по CrO3, после чего в приготовленный раствор добавляют сульфат аммония (Nh5)2SO4, который задают по расчету в стехиометрических количествах к заданному количеству бихромата натрия Na2Cr2O 7.
Концентрация раствора бихромата натрия Na 2Cr2O7 и сульфат аммония (NH 4)2SO4, в котором происходит обменное разложение, составляет 400-450 г/л по CrO3.
Затем осуществляют обменное разложение бихромата натрия Na 2Cr2O7 и сульфата аммония (NH 4)2SO4 при температуре 100-105 в течение 45-60 минут при постоянном перемешивании с образованием бихромата аммония (Nh5)2Cr2O 7 и сульфата натрия Na2SO4, происходящим по химической реакции (1), при этом весь бихромат натрия Na2Cr2O7 переводится в бихромат аммония (Nh5)2Cr2 O7.
Сульфат натрия Na2SO4 в растворах бихроматов обладает ограниченной растворимостью, поэтому значительная его часть сразу же выпадает в осадок.
Далее отделяют сульфата натрия Na2SO4 от раствора, для чего пульпу сульфата натрия Na2SO 4 в растворе бихромата аммония (Nh5) 2Cr2O7 направляют в отстойник, где происходит осаждение основного количества кристаллов сульфата натрия Na2SO4.
Осветленный раствор бихромата аммония (Nh5)2Cr2O 7 после отстойника направляют на контрольную фильтрацию на патронном фильтре, где от него отделяют оставшуюся часть сульфата натрия Na2SO4. Осадок сульфата натрия Na 2SO4 из отстойника и патронного фильтра подают на центрифугу, где происходит его обезвоживание.
Кристаллы сульфата натрия Na2SO4 после центрифуги направляют в производство белого сульфата натрия Na 2SO4. Маточные растворы после центрифуги возвращают в отстойник. Весь процесс отделения сульфата натрия Na2SO4 осуществляют при температуре раствора не ниже 90°С.
Затем раствор, содержащий бихромат аммония (Nh5)2Cr2O7 с концентрацией по CrO3 400-450 г/л и температурой 90°С, охлаждают до температуры 35-40°С, являющейся температурой кристаллизации бихромата аммония (Nh5)2Cr2O 7.
При этом в осадок выпадают кристаллы бихромата аммония (Nh5)2Cr2O7 , которые затем отделяют от маточного раствора на барабанном вакуум-фильтре.
Влажность осадка составляет 10-15%, содержание сульфатов до 1,5%.
Маточный раствор отправляют в голову процесса на упаривание, что способствует более полному вовлечению бихромата аммония (Nh5)2Cr2O 7 в процесс получения окиси хрома Cr2О 3, что, в свою очередь, способствует увеличению содержания окиси хрома Cr2O3 в готовом продукте до 99,5%.
Далее кристаллы бихромата аммония (Nh5 )2Cr2O7 подвергают термическому разложению в барабанной вращающейся печи при температуре 440-1400°С. При этом происходит следующая химическая реакция с образованием окиси хрома Cr2О3:
При термическом разложении бихромата аммония (Nh5 )2Cr2O7 при температуре 440-450°С образуется окись хрома Cr2O3 , которая используется для магнитных носителей;
При термическом разложении бихромата аммония (Nh5)2Cr 2O7 при температуре 800-900°С образуется мелкокристаллическая пигментная и абразивная окись хрома Cr 2О3;
При термическом разложении бихромата аммония (Nh5)2Cr2O7 при температуре 1200-1400°С образуется крупнокристаллическая металлургическая окись хрома Cr2О3.
После получения окиси хрома Cr2О3 осуществляют ее вымывание водой при отношении Т:Ж=1:4-1:6.
Полученную при этом пульпу фильтруют на барабанном вакуум-фильтре, в результате чего осуществляется окончательная отмывка окиси хрома Cr 2О3 от водорастворимых солей, что способствует уменьшению примесей и повышению содержания Cr2О 3 в готовом продукте до 99,5% и выше.
Осадок окиси хрома Cr2O3 с фильтра подают в барабанную вращающуюся сушилку, где он подвергается сушке при температуре 100-150°С.
Пример.
Бихромат натрия Na2 Cr2O7 с концентрацией 1000 г/л по CrO 3 в количестве 1,8 м3 раствора смешивают с 10 м3 упаренного маточного раствора бихромата аммония (Nh5)2Cr2O7 с концентрацией 350 г/л по CrO3 и получают раствор с концентрацией 450 г/л по CrO3 в количестве 11,8 м3.
В 1,8 м3 раствора бихромата натрия Na2 Cr2O7 с концентрацией 1000 г/л по CrO 3, содержится 1,8×1000×1,31=2358 кг сухого бихромата натрия Na2Cr2O7, где 1,31 - пересчетный коэффициент из CrO3 в Na2Cr 2O7. По химической реакции (1) устанавливают, что на 2358 кг бихромата натрия Na2Cr2O 7 необходимо задать 1188 кг сульфата аммония (NH 4)2SO4. Это количество отвешивают на весах и задают в раствор.
Затем согласно химической реакции (1) осуществляют обменное разложение бихромата натрия Na2Cr2O7 и сульфата аммония (Nh5)2SO4.
По окончании обменного разложения от раствора отделяют кристаллы сульфата натрия Na2SO4 в количестве 1278 кг, которые направляют на производство белого сульфата натрия Na2 SO4.
После отделения сульфата натрия Na 2SO4 получают 11 м3 очищенного раствора бихромата аммония (Nh5)2Cr2O 7, который затем охлаждают до температуры его кристаллизации - 35°С.
Полученные таким образом кристаллы бихромата аммония (Nh5)2Cr2O7 отделяют на вакуум-фильтре, при этом концентрация маточного раствора по CrO3 составляет 250 г/л, что обеспечивает получение кристаллов бихромата аммония (Nh5)2 Cr2O7 в количестве (450-250)×11,8×1,26=2973 кг.
Маточный раствор и промывные воды с вакуум-фильтра направляют в голову процесса на упаривание.
Далее кристаллы бихромата аммония (Nh5)2Cr2O 7 загружают в барабанную вращающуюся печь для термического разложения. После термического разложения по химической реакции (2) образуется 1794 кг окиси хрома Cr2O3 .
Для получения окиси хрома Cr2O3 , используемой для магнитных носителей, задают температуру термического разложения 440-450°С.
Для получения мелкокристаллической пигментной и абразивной окиси хрома Cr2О3 задают температуру термического разложения 800-900°С.
Для получения крупнокристаллической металлургической окиси хрома Cr2O3 задают температуру термического разложения 1200-1400°С.
Окись хрома Cr2 O3, полученная заявляемым способом, содержит Cr 2О3 в количестве 99,5% при минимальном количестве примесей: содержание серы S - 0,005%, содержание углерода С - 0,005%, содержание кремния SO2 - 0,07%, содержание железа FeO - 0,1%.
Таким образом, заявляемое изобретение позволяет упростить способ получения окиси хрома Cr2 О3, повысить качество окиси хрома Cr2О 3 за счет уменьшения примесей и повышения содержания Cr 2О3 в готовом продукте, а также получать окись хрома Cr2O3 различного назначения.
bankpatentov.ru
Способ получения окиси хрома
№ 119178
Класс 12m, 8 р Я Яэ1 йб1ВНТИО-Т!ФНЮЧФСЧЗУ
БИУИС7ЕКА
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
А. М, Поляк, Д. Ф. Ризе, Ю. С. Плышевский, А, Н. Торокин, Р. А. Горохова и Г. С. Ганичкина
СПОСОБ ПОЛУЧЕИИЯ ОКИСИ ХРОМА
Заявлено 15 октября 1958 г. за № 609632/23 в Комитет по делам изобретений п открытий прн Совете Министров СССР
Опубликовано в «Бюллетене изобретений» № 8 за 1959 г.
Известны способы получения окиси хрома, например путем обжига бихромата калия с серой, восстановлением хромата натрия сернистым натрием илн серой в щелочном растворе. Однако известные способы имеют недостатки, так как их применение связано с необходимостью создания высоких температур, порядка 800 — 1300, и употреблением оольшого количества щелочи.
Предлагаемый способ получения окиси хрома восстановлением шелочных растворов хромата натрия серой при медленном нагревании суспензии до кипения отличается тем, что в голову процесса на восстановление подают закрепленную промывочную воду и часть основного маточного раствора, содержащего щелочь и гипосульфит, что обеспечивает сокращение расхода щелочи и выход стандартной по содержанию серы окиси хрома.
Способ осуществляют следующим образом.
В стальной реактор, снабженный паровым змеевиком и лопастной мешалкой, загружают раствор хромата натрия, едкий натр (25 — 30 г/л) и тонкоизмельчсш|ую серу (105% от стехиометрии). При интенсивном перемешивании температуру суспензии медленно в течение 20 — 30 мин. доводят до кипения н затем в течение 90 — 120 вин. выдерживают при
95 — 101 .
Пульпу гидратированной окиси хрома с отношением Ж: Т 7: 1 (при содержании 150 г/,г СяОз в щелоке) фильтруют на барабанных фильтрах или фильтрпрессах. Фильтрование и отмывку осадка горячей водой (70 — 80 ) проводят по двухфазной схеме.
Промытый осадок попадает на годсушку и прокалку (при 950—
1050 ) во врап1аюн1уюся или подовую печь. Промывные воды направляют на восстановление в голову процесса.
Затем прокаленный осадок репульпируют, фильтруют и отмывают горячей водой (70 — 80 ) по двухфазной схеме, сушат, размалывают и № 119178 упаковывают в качестве готового продукта — стандартной окиси хрома.
В целях. уменьшения расхода щелочи и повышения выхода окиси хрома до 98 — 99%, промывную воду, закрепленную в процессе четырехфазного фильтрования и промывки и часть маточного раствора (0,75—
1,0 объем на 1 объем хроматного щелока), содержащего щелочь и гипосульфит, заворачивают в голову процесса — на восстановление.
В случае последующей утилизации маточного раствора, для сокращения реакционных объемов, целесообразно на восстановление подавать, упаренный до 350 — 450 г/л С Оз хроматный щелок.
Для восстановления применяют не только природную„но также и газовую серу 2-го и 3-ro сортов, так как содержащийся в ней мышьяк и селен в щелочной среде переходят в раствор и отмываются от окиси хрома.
Предмет изобретения
Комитет по делам изобретений и открытий при Совете Министров СССР
Редактор А. К.Лейкина Гр. 48
Подг к "ен 1 ЧП 59
Тираж 650 Цена 25 коп, Информационно-издательский отдел.
Объем 0,17 и, л. Зак. 4647
Типография Комитета по делам изобретений и открытий при Совете Министров СССР
Москва, Петровка, 14.
Способ получения окиси хрома восстановлением щелочных растворов хромата натрия серой при медленном нагревании суспепзии до кипения, от л и ч а ю шийся тем, что, с целью сокращения расхода щелочи и обеспечения выхода стандартной по содержанию серы окиси хрома в 98% — в голову процесса (на восстановление) подают закрепленную промывную воду и часть основного маточного раствора, содержащего щелочь и гипосульфит.


www.findpatent.ru
Способ получения окиси хрома
ОПИСАНИЕ
ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
Союз Советских
Социалистических
Республик
Зависимое от авт. свидетельства №вЂ”
Заявлено 05.XI.1970 (№ 1490276/23-26) с присоединением заявки №
Приоритет
Опубликовано 21 VI.1973. Бюллетень № 27
Дата опубликования описания 20.Х.1973
М. Кл. С Olg 37/02
Государственный комитет
Совета Министров СССР ло делам изобретений и открытии
УДК 661.876.1(088.8) Авторы изобретения
В. Н. Решетников, В. Н. Брунов и А. Д. Окулов
Новотроицкий завод хромовых соединений
Заявитель
СПОСОБ ПОЛУЧЕНИЯ
ОКИСИ ХРОМА
Изобретение относится к области производства хромовых соединений, в частности к области производства окиси хрома, используемой в качестве неорганического пигментаы
Известен способ получения окиси хрома путем термического .разложения хромового ангидрида с модифнцирующими добавками, повышающими .красящую способностью и укрывистость пигмента. В качестве таких добавок применяют, в частности борную кислоту.
Однако технологический процесс при этом способе осложнен, так:как борная кислота не может быть введена .непосредственно в расплав хромового ангидрида. Хромовый ангидрид необходимо охлаждать, охлажденный плав измельчать и только после этого вводить в него борную кислоту.
В предлагаемом способе для упрощения технологического процесса в качестве модифицирующей добавки используют сернистый на трий, который вводят в хромовый ангидрид в количестве порядка 1 вес. %. Поскольку. сернистый натрий имеет температуру плавления, близкую к температуре плавления хромового ангидрида, их смешение может быть осуществлено не только в твердом, но ыч в расплавленном состоянии, что существенно упрощает технологический процесс. Термическое разложение ведут:при температуре 900—
950 C.
Красящая способность и укрывистость пигмента с добавками сернистого натрия такие же, как и с добавками борной кислоты и значительно превосходят красящую, способность
5 и укрывистость окиси хрома, полученной без модифицирующих добавок.
Пример. 50 г измельченного технического хромового ангидрида прокаливают при 900—
N 950 С в течение 60 мин. Полученную окись хрома тщательно промывают горячей водой, ф ильтруют и сушат при 120 C. Одновременно к 50 г измельченного технического хромового а нгидрида добавляют 0,5 г сернистого
15 натрия; компоненты тщательно смешивают, и затем смесь обрабатывают как описано выше.
Характеристика окиси хрома,,полученной без модифицирующей добавки: содержание
2о Сг.Оа 99,1%, SO4 0,03%; НеО 0,15% водораствор имых солей 0,07%, СгО 0,03%, рН 7,8, красящая:способность — 96, укрывистость
12,7.
25 Характеристика окиси хрома, полученной с модифицирующей добавкой сернистого натрия: содержание CrgOg 99,1%, 504 0,02%, Н20 0,10%, водорастворимых солей 0,05%, Cr0> 0,018%, рН 7,5, красящая способность
30 105, укрывистость 10,3.
386847
П р е д м е т:и з о б р е т е н и я
Составитель И. Магидсон
Текред E. Борисова
Корректоры: С. Сатагулова и Е. Хмелева
Редактор Д. Пинчук Заказ 2812!11 Изд. № 723 Тираж 523 Подписное
ЦНИИПИ Государственного комитета Совета Министров СССР по делам изобретений и открытий
Москва, )К-35, Раушская наб., д. 4j5
Типография, пр. Сапунова, 2
Способ, получения окиси хрома путем термического разложения хромового ангидрида с модифицирующими добавками, отличаюи1ийся тем, что, с целью упрощения технологического процесса, в качестве модифицирующей добавки применяют сернистый натрий, вводимый в количестве поРЯДка 1о1о от веса хРомового ангидрида.


www.findpatent.ru
Способ получения окиси хрома
о и и с А н т)т4
ИЗОБРЕТЕНИЯ
324220
Сок)з Советоких
Социалистических
Республик
К АВТОРСКОМУ СВИДЕТЕПЬСТВУ
Зависимое от авт. свидетельства No—.Л1. Кл. С 01() 37/02
Заявлено 28 1.1969 (Ф 1301358 23-26) с присоединением заявки %в
Приоритет
Комитет по делам изобретений и открытий нри Совете Министрое
СССР
Опубликовано 23.Х11.1971. Вголлетень Х
Дата опубликования n!!!tea«Its! 23.11.1972
УДК 661.876.12 (088.8) Авторы изобретения
Г. Д. Мазалецкий, В. А. Рябин и P. С. Байтакова
Заявитель
СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ХРОМА прогрева ес в течение 1 ((тс при температуре
100 С имс«T кислот)юсть Ilo шкале рН, равIt
30 .I!II÷.
10 Сн«п(посл(. и ронял ки Отмыв(1ют ВОДОЙ От сульфат-i натрия, Полученный продукт имеет следующий сост;)в (в пп): СгОз 99,2; Feo 0,18;
СгО-„водорястворнмы!! и кнслотнорастворимый отсут«твует; с«ря и углерод по 0,02 каж15 ды й.
Способ получения окиси «рома путем обра()o1I(I! сульфатов нли основных coëåkt хрома
20 c(. «äèt «ttlt)IMII щелочных металлов с последующ«й ф:гльтряцнсй пульпы и прокалкой осади
25 раствором монохромятя натрия, полученную схгссь II J)ol(н)Я!От ВОДОЙ и
ИОДВСРI Я!оl фн IBTP
Изобретение относится к области получения окиси хрома.
Известен способ получения окиси хрома путем обработки основного сульфата хром:, кальцинированной содой с последующей фильтрацией и прокалкой полученной пулы!ы.
Предло>кенный способ отличается от известного тем, ITo сульфат или основную соль хрома в нястообрязном состоянии обря()ятывают раствором монохроматя натрия с и;-,",.тедующим прокяливанием, вьнцелачивян! м
ВОДОЙ ll ф ИЛ ЬТР;1 ЦИ ЕЙ. 3TO,((3 «T BOB i),t O)I(II 0 "T!> упростить процесс зя счет исключения cT(tent!;: фи чье рации пульпы трудноф ильтрусмой п1.1роокиси хрома. Фильтр(!ция ol(llctt . .ром;1 ляется высокопроизводительной и эффективной операцией.
Кроме того, с раствором десульфуряторя вносится хром и Т: К в пул! ис получ;)ется В
2 раза больше, что упрощает процесс уll lðêtt и последующей нрокялки продукт(п! д«сульфурации.
Пример. В 50 г пасты основного сульфата хрома, содержащей (в %): 13,б5 СгзО„;
7,27 504, 0,03б FCO; остальное — водя, вводят
21,1 )гл раствора монохромята II ITp IIII (179,8 г/л СТОз). Полученная пульта после
Предмет изобретения

Похожие патенты:











Изобретение относится к химической технологии неорганических веществ, в частности к технологии получения хромового ангидрида - вещества, широко используемого во многих отраслях промышленности: химической, лакокрасочной, текстильной, металлургической и др
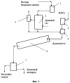
Изобретение относится к получению хромового ангидрида и может быть использовано в химической промышленности



Изобретение относится к способу получения оксида хрома (III), включающему стадии: a) взаимодействия хромата щелочного металла или бихромата щелочного металла с газообразным аммиаком, в частности, при температуре от 200 до 800°C, b) гидролиза реакционного продукта, полученного на стадии а), причем pH-значение воды для гидролиза перед гидролизом или щелочного маточного щелока во время или после гидролиза устанавливают равным от 4 до 11, понижая с помощью кислоты, c) выделения продукта гидролиза, выпавшего в осадок на стадии b), d) сушки продукта, полученного на стадии с), и e) кальцинирования продукта гидролиза, полученного на стадии d) при температуре от 700 до 1400°C. Получаемый оксид хрома (III), который можно применять для металлургических целей, содержит очень малые количества серы и щелочных металлов. 10 з.п. ф-лы, 7 пр.

Изобретение относится к области химии и может быть использовано при получении пигмента для строительных материалов, пластмасс, красок и лаков, стекла и керамики. Осуществляют взаимодействие монохромата натрия с газообразным аммиаком при температуре от 200 до 800°С. Проводят гидролиз реакционного продукта. Понижают рН воды перед гидролизом или рН щелочного маточного щелока во время или после гидролиза до 4-11 путем введения двуокиси углерода. Выделяют выпавший в осадок продукт гидролиза при рН= 4-11. Кальцинируют продукт гидролиза при температуре от 700 до 1400°С. Изобретение позволяет получить оксид хрома (III), содержащий очень малые количества серы, щелочных металлов и побочных продуктов. 11 з.п. ф-лы, 3 пр.
Способ получения окиси хрома
www.findpatent.ru
Хроматно-серный метод получения окиси хрома
Технология минеральных солей (удоБрений, пестицидов, промышленных солей, окислов и кислот)
Этим методом, заключающимся в восстановлении водного раствора хромата натрия серой 200, производят наибольшее количество окиси хрома, главным образом, для переработки на металлический хром. Преимущество метода — использование сравнительно дешевого сырья — раствора монохромата натрия и, вследствие этого, низкая себестоимость продукта (на 13—17% ниже себестоимости окиси хрома, полученной термическим разложением хромового ангидрида 200; см. также 230).
Щелочной раствор монохромата натрия, содержащий 110— 140 г/л СгОз и около 10 г/л щелочи (в пересчете на NaOH), обрабатывается в каскаде реакторов при кипячении (103°) тонкоиз - мельченной (0,2 мм) серой, добавляемой в виде суспензии в части хроматного щелока, приготовленной в шаровой мельнице. По другому варианту восстановление осуществляют в автоклавах расплавленной серой.
Вследствие гидролиза серы в горячем щелочном растворе образуются ионы (S-S„)2~ и другие (ем. гл. XIV), которые восстанавливают шестивалентный хром до трехвалентного, а сера превращается главным образом в S203~- Общее уравнение реакции восстановления:
4Ма2СЮ4 + 6S + (2х + 1)Н20 = 2(Сг2Оэ • *Н20) + 3Na2S203 + 2NaOH
Выделившийся осадок гидроокиси хрома отфильтровывают на барабанных вакуум-фильтрах, промывают и прокаливают для получения окиси хрома в барабанной печи при — 1100° в потоке газов, полученных сжиганием топлива в избытке воздуха для создания окислительной атмосферы. При этом примеси сернистых соединений и щелочи превращаются в водорастворимые соли Na2S04 и Na2Cr04. Для их извлечения выходящий из печи спек окиси хрома выщелачивают, затем несколько раз промывают на фильтрах с промежуточными репульпациями и высушивают в барабанной сушилке с наружным обогревом.
Щелочной раствор тиосульфата натрия, полученный после отделения гидроокиси, перерабатывают с помощью серной кислоты на сульфат натрия и серу по реакции:
3Na2S203 + h3S04 = 3Na2S04 + 4S + h30
Более рациональным является использование этого раствора для восстановления хромата натрия по реакции 240-243: 10Na2Cr04 + 3Na2S203 + 7h3S04 + (2х - 7)Н20 = = 2(2Сг203 • СгОз • *Н20) + 13Na2S04
При этом окись хрома получают по так называемой упрощенной схеме хроматно-серного метода, заключающейся в двухстадий - ном восстановлении монохромата — сначала часть щелочного раствора монохромата восстанавливают жидкой серой в автоклаве, затем к полученной суспензии окиси хрома в щелочном тиосуль - фатном растворе добавляют остальную часть монохроматного раствора и серную кислоту и смесь кипятят. После этого дополнительно обрабатывают раствор в автоклавах при 150°. Отфильтрованный осадок хроми-хроматов прокаливают, при этом он превращается в окись хрома, не содержащую адсорбированной щелочи, так как процесс восстановления завершается в кислой среде. Эта окись хрома не требует дальнейшей обработки и выпускается в качестве готового продукта. Раствор, оставшийся после отделения хроми-хроматов, перерабатывают на товарный сульфат натрия. В упрощенном варианте хроматно-серного метода отсутствует ряд операций, имеющихся в основном варианте — выщелачивание, фильтрование с репульпациями и сушка окиси хрома.
На производство 1 т окиси хрома хроматно-серным методом расходуется 2,02 т монохроматного щелока (67,1% Сг208), 0,85 г серы и 0,06 т кальцинированной соды, а по упрощенному варианту 2,05 т монохроматного щелока, 0,175 т серы, 1 т серной кислоты (100%) и 0,02 т кальцинированной соды. Получаемая окись хрома содержит 98—99% Сг203, меньше 0,01% S, 0,03% С, -0,1% FeO, до 0,08% Н20.
При взаимодействии хлорита натрия с хлором происходит образование хлористого натрия и выделяется двуокись хлора: 2NaC102 + С12 = 2NaCl + 2 СЮ2 Этот способ ранее был основным для получения двуокиси …
На рис. 404 представлена схема производства диаммонитро - фоски (типа TVA). Фосфорная кислота концентрацией 40—42,5% Р2О5 из сборника 1 насосом 2 подается в напорный бак 3, из которого она непрерывно …
Физико-химические свойства Сульфат аммония (Nh5)2S04 — бесцветные кристаллы ромбической формы с плотностью 1,769 г/см3. Технический сульфат аммония имеет серовато-желтоватый оттенок. При нагревании сульфат аммония разлагается с потерей аммиака, превращаясь в …
msd.com.ua
Способ получения окиси хрома
Союз Советских
Социалистических
Республик
Заш(симОС 0Т апr. свидетельства №
Заявлено 26.11.1970 (№ 1406704/23-26) .ЧПК С 01 37/02 с присоединением заявки ¹
Приоритет
Комитет по делам изобретений и открытий при Совете Министров
СССР
Опубликовано 19.Х.1971. Был 1crc«I Л 31
Дата опуo;IIIIIOBaиия описания 1.1.1972
УДК 661.876.1(088.8) Лпторы изобретения
Б. П. Середа, Н. П. Левченко, Г. A. Кравченко, 3. A. Ильюк, Г. Л. Сорокин, В. И. Дейнеженко, Л. К. Чирва, Н. Л. Охотникова, В. Е. Сиванов, П. С. Пилипенко и H. A. Громченко
Заявитель
СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ХРОМА
Изобретение относится к способам получения окиси хрома, применяемой в качестве пигмента, а также продукта для металлургической промышелнности.
Известен способ получения окиси хрома путем взаимодействия щелочного раствора хромата натрия с избытком элементарной серы с последующей обработкой образовавшейся пульпы гидрата окиси хрома соединениями шестивалентного хрома (добавочным количеством раствора хромата натрия), фильтрацией осадка гидрата окиси хрома, прокалкой его, выщелачиванием спека, отмывкой и сушкой полученной окиси хрома.
Недостатком этого способа является наличие в гидрате окиси хрома большого количества неотмываемой водой щелочи (3,9%
1чаОН), а также невысокие скорость фильтрования конечного осадка (0,7 — 1,5 лл/слта . ния) и красящая способность окиси хрома как пигмента (140% от эталона).
С целью устранения этих недостатков предложено в пульпу гидрата окиси хрома «а стадии обработки ее соединениями шестивалеитного хрома (добавочным количеством раствора хромата натрия) вводить гидратированные хромихроматы в количестве предпочтительно 50 — 150% от исходной пульпы гидрата окиси хрома.
Это позволяет повысить скорость фильтрации пульпы гидрата окиси хрома до
3,0 лы, глт-" лтия, снизить содержание щелочи (." IOI-1) в гидроокиси хрома до 1,1%, повысить красящу10 способность Окиси хрома как пш мента до 150% or эталона.
5 Введение гидратированиых хромихроматов
ooBcIIP II1BQQT cIilli. c«llc á0. Icе, iIcliI B QB3 Р333, степе|ш обратного перехода окиси хрома в хромат при прокаливашш гидроокисных соедипешш хрома. По известному способу содер10 жанне «ромата натрия в спеке составляет
11,6",с, а по предложенному — до 3,5%.
Пульпа гидроок1си хрома образуется при тем пера т ре 98 — 100 С, а «poll,I Ii a I liverpool« cll хрома осуществляется при температуре
15 900 — 1250 С.
Пример. 100 лл пульпы гидрата окиси хрома, иолучешюй восстановлением хромата
«атрпя в автоклаве «ри избытке (30", ii) серы и содержащей 86,3 г/л Cr O, нагревают до
20 температуры 98 — 100"С, и затем медленно при температуре кипсш;я рсакцион«ой смеси вводят 39,7 г влаж«ого осадка гпдратированшгх хромихроматов, содержащего 8,2 г
Сг О„- и 2,6 г C;O,--, и 20 лт.г монохроматного раствора с ко«цснтрацпей 180 г/л СгОз.
Полу Ieiil» ю реакционную смесь выдерживают при постоянном иеремешивашш в тече ис 0,5 час при температуре кипения, а затем фп Ii>TPii IÎT. СК01)OCTb фИЛЬТРаЦПП ИСХОДНОЙ
30 пульпы гидрата окиси хрома 1,1 мл/с.н иия, ;; «олучснной — 2,4 лтл/слез лия. Осадок от317()19
Предмет изобретения
С>>е >;>:3. ònët С. Лотхова
Текре:1 Л. Кук.»и>>а
К3>рректор О, Тюр»на
Редактор 3. Горбуиова
3а>таз 3"80!17 Из)ь ¹ 1376 Тира>к 473 Подписное
ЦНИИПИ Ко)и>тета >iî 1!ела>! изобретений и от>трь>тий при Совете Министров СССР ,> оси>)а, Ж-35, 1 «лискаи вая.. д. 4, 5
Тииогр»фи>>, ир. Сапунова, о
М1>П>аlо Г OT Р IСT13() (>fnli>IX Г1)Г!С!1,,1(113>т l i>i, i !30 1стп II lipoK.I>Hill!(> г 0 Г! I> I (>II ИЮ (., другу!о lip!! !" )0:fc I:> л>1И 1.>
C. ИСКЕ CO, tСРж П) С>! 4, ) 1 > !. О,ln() >С! !30(И!. IOTO шестивалентиого Y()омг> (13 пер счете
Cã0;;1. C1iåKfI выще.!Ич 131п>)т, от !.И3>по! От рнст!3оримьл примесеп !I суп>ат I!pi! 15)0 С 11рп тсмпер;!туре прокалкп 900 С:!01!учи>3>т зсг!сный пигмент с содержаниеit 3. г",O-,, 99,0),1, интенсивностью 145.",в, H l(pl! 1250 С вЂ” металлургическую окись хрома с содср)ка)!Ис>м (в %): 99,2 Сг.О-„, 0,0095; 00008.3-". Сt(, В1, Р() отсутствуют.
1. СПОСОО полу>!ения Ок ICI! Kpni!H Ili 1см
T3h2I«iTozvitcT»tttt щс io>ного раствора ipt>itH а
if >1>l I ко» аале 3>сrr I Pi!0É ссРы Г:10" . l i K>I>t>P Г> гкОЙ ООР 8 30 tlHPIlic>fcЯ и » ь
: I l,l и I() О >c,гип ii
3,!г!с пи>оп> xpoilH, фин ьтрац «й ()cHlKH гидрата окиc!t кро»а, прокалкой его, выщелач:.г:!апис) clTI. .а, От ми!ВкОЙ и су1нкОЙ Окиси
: 11E>10 iln-!
>ь!шспия (корости фпл1>Tp1lilltll il Гиижспия
СОДСРЖНИЯ НГС IO×!I В Г:IÄPOOK1IC!I XPOiIH, ПоГгуиа!Огней 1>а;!рокалку, а также !In!3I!Titeil;I>r
itHTiicli иь!и свойс! в целевого продукта, !3 пульпу гпдрата Окиси Kðî»à на стадии oopat)ni !прова!)ные Kport)TKpoitaты.
2. Способ Ilo и. 1, от.)и Пп Ы С X Pnil; IK Pnit HTr>i t) I)OHtlT 13
1f»ã пс)!Одной пульпы ifyрат!! онricir з;ром>).


www.findpatent.ru










