Презентация к уроку "Хром и его соединения". Презентация хром
Презентация по химии "Хром" - химия, презентации

ХРОМ
Элемент № 24
Автор:
Слемзина Т.В.
учитель химии
МБОУ «Гимназия»
г. Ефремов
2013

ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ
- химический элемент VI А группы
- атомный номер 24
- атомная масса 51,996
- обозначается символом Cr
- Электронная формула: 24 Cr )2)8)13)1
1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1
- Степень окисления:
+1; +4; +5; +2; +3; +6; - (наиболее устойчивы в соединениях хрома).

ЭТИМОЛОГИЯ НАЗВАНИЯ
Название элемент
получил от греч. χρῶμα — цвет, краска — из-за разнообразия окраски своих соединений.


ИСТОРИЯ ОТКРЫТИЯ
В 1766 году в окрестностях Екатеринбурга был обнаружен минерал, который получил название «сибирский красный свинец», PbCrO 4 . Современное название — крокоит. В1797 французский химик Л. Н. Воклен выделил из него новый тугоплавкий металл(скорее всего Воклен получил карбид хрома)

НАХОЖДЕНИЕ В ПРИРОДЕ
Хром является довольно распространённым элементом. Основные соединения хрома — хромистый железняк (хромит).
Самые большие месторождения хрома находятся в ЮАР (1 место в мире) , Казахстане, России,
России, Зимбабве, Мадагаскаре.
Главные месторождения хромовых руд в РФ
известны на Урале.
хромит

ФИЗИЧЕСКИЕ СВОЙСТВА
Хром – голубовато-белый металл, с кубичес-
кой объемно-центрированной решеткой с металлическим типом химической связи.
T пл =1890°С, Т кип= 2680 °C, ρ= 7,19 г/см 3 . Чистый хром пластичен при обычных условиях, достаточно хорошо поддаётся механической обработке. Самый твердый из чистых металлов. На воздухе покрыт прочной пленкой оксида.
 600°С 4Cr + 3O 2 = 2Cr 2 O 3 оксид хрома (III) 2. Реагирует c фтором при 350°С, с хлором – при 300°С, с бромом – при температуре красного каления 2Cr + 3Cl 2 = 2CrCl 3 галогениды хрома (III) 3. Реагирует с азотом при t1000°С 2Cr + N 2 = 2CrN или 4Cr + N 2 = 2Cr 2 N нитрид 4. С cерой при t 300°С образует сульфиды от CrS до Cr 5 S 8 , например: 2Cr + 3S = Cr 2 S 3 . 5. Реагирует с бором, углеродом и кремнием с образованием боридов, карбидов и силицидов: Cr + 2B = CrB 2 (возможно образование Cr 2 B, CrB, Cr 3 B 4 , CrB 4 ), 2Cr + 3C = Cr 2 C 3 (возможно образование Cr 23 C 6 , Cr 7 B 3 ), Cr + 2Si = CrSi 2 (возможно образование Cr 3 Si, Cr 5 Si 3 , CrSi). 6. С водородом непосредственно не взаимодействует."
600°С 4Cr + 3O 2 = 2Cr 2 O 3 оксид хрома (III) 2. Реагирует c фтором при 350°С, с хлором – при 300°С, с бромом – при температуре красного каления 2Cr + 3Cl 2 = 2CrCl 3 галогениды хрома (III) 3. Реагирует с азотом при t1000°С 2Cr + N 2 = 2CrN или 4Cr + N 2 = 2Cr 2 N нитрид 4. С cерой при t 300°С образует сульфиды от CrS до Cr 5 S 8 , например: 2Cr + 3S = Cr 2 S 3 . 5. Реагирует с бором, углеродом и кремнием с образованием боридов, карбидов и силицидов: Cr + 2B = CrB 2 (возможно образование Cr 2 B, CrB, Cr 3 B 4 , CrB 4 ), 2Cr + 3C = Cr 2 C 3 (возможно образование Cr 23 C 6 , Cr 7 B 3 ), Cr + 2Si = CrSi 2 (возможно образование Cr 3 Si, Cr 5 Si 3 , CrSi). 6. С водородом непосредственно не взаимодействует."
Cr при обычных условиях – инертный металл, при нагревании становится довольно активным.
- Взаимодействие с неметаллами
- сгорает в кислороде:
t 600°С
4Cr + 3O 2 = 2Cr 2 O 3 оксид хрома (III)
2. Реагирует c фтором при 350°С, с хлором – при 300°С, с бромом – при температуре красного каления
2Cr + 3Cl 2 = 2CrCl 3 галогениды хрома (III)
3. Реагирует с азотом при t1000°С
2Cr + N 2 = 2CrN
или 4Cr + N 2 = 2Cr 2 N нитрид
4. С cерой при t 300°С образует сульфиды от CrS до Cr 5 S 8 , например:
2Cr + 3S = Cr 2 S 3 .
5. Реагирует с бором, углеродом и кремнием с образованием боридов, карбидов и силицидов:
Cr + 2B = CrB 2 (возможно образование Cr 2 B, CrB, Cr 3 B 4 , CrB 4 ),
2Cr + 3C = Cr 2 C 3 (возможно образование Cr 23 C 6 , Cr 7 B 3 ),
Cr + 2Si = CrSi 2 (возможно образование Cr 3 Si, Cr 5 Si 3 , CrSi).
6. С водородом непосредственно не взаимодействует.

ХИМИЧЕСКИЕ СВОЙСТВА
2. Взаимодействие с водой
В тонкоизмельченном раскаленном состоянии хром реагирует с водой
2Cr + 3H 2 O = Cr 2 O 3 + 3H 2
3. Взаимодействие с кислотами
1. В электрохимическом ряду напряжений металлов хром находится до водорода, он вытесняет водород из растворов неокисляющих кислот:
Cr + 2HCl = CrCl 2 + H 2 ;
Cr + H 2 SO 4 = CrSO 4 + H 2 .
2. В присутствии кислорода воздуха образуются соли хрома (III):
4Cr + 12HCl + 3O 2 = 4CrCl 3 + 6H 2 O.
3. Концентрированная азотная и серная кислоты пассивируют хром. Хром может растворяться в них лишь при сильном нагревании, образуются соли хрома (III) и продукты восстановления кислоты:
2Cr + 6H 2 SO 4 = Cr 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O;
Cr + 6HNO 3 = Cr(NO 3 ) 3 + 3NO 2 + 3H 2 O.

ХИМИЧЕСКИЕ СВОЙСТВА
4. Взаимодействие с щелочными реагентами
1. В водных растворах щелочей хром не растворяется, медленно реагирует с расплавами щелочей с образованием хромитов и выделением водорода :
2Cr + 6KOH = 2KCrO 2 + 2K 2 O + 3H 2 .
2. Реагирует с щелочными расплавами окислителей, например хлоратом калия, при этом хром переходит в хромат калия:
Cr + KClO 3 + 2KOH = K 2 CrO 4 + KCl + H 2 O.
5. Восстановление металлов из оксидов и солей
Хром – активный металл, способен вытеснять металлы из растворов их солей:
2Cr + 3CuCl 2 = 2CrCl 3 + 3Cu.
![Химические свойства соединений хрома Степень окисления Оксид +2 +3 Гидроксид CrO (чёрный) Характер Cr(OH) 2 +4 Cr 2 O 3 Cr(OH) 3 (зелёный) CrO 2 Преобладающие формы в растворах Основный (желтый) +6 (серо-зеленый) Амфотерный Примечания не существует Cr 2+ (соли голубого цвета) CrO 3 Очень сильный восстановитель Cr 3+ (зеленые или лиловые соли) [Cr(OH) 4 ] - (зелёный) Несолеобразующий H 2 CrO 4 H 2 Cr 2 O 7 (красный) - Кислотный Встречается редко CrO 4 2- (хроматы, желтые) Cr 2 O 7 2- (дихроматы, оранжевые) Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит. наиболее устойчивая Степень окисления: +2; +3; +6 → основные свойства ↓ ; кислотные свойства → окислительные свойства ; восстановительные свойства ↓](/800/600/http/arhivurokov.ru//kopilka/uploads/user_file_5399b81232cd5/img_user_file_5399b81232cd5_10.jpg)
Химические свойства соединений хрома
Степень окисления
Оксид
+2
+3
Гидроксид
CrO (чёрный)
Характер
Cr(OH) 2
+4
Cr 2 O 3
Cr(OH) 3
(зелёный)
CrO 2
Преобладающие формы в растворах
Основный
(желтый)
+6
(серо-зеленый)
Амфотерный
Примечания
не существует
Cr 2+ (соли голубого цвета)
CrO 3
Очень сильный восстановитель
Cr 3+ (зеленые или лиловые соли) [Cr(OH) 4 ] - (зелёный)
Несолеобразующий
H 2 CrO 4 H 2 Cr 2 O 7
(красный)
-
Кислотный
Встречается редко
CrO 4 2- (хроматы, желтые) Cr 2 O 7 2- (дихроматы, оранжевые)
Переход зависит от рН среды. Сильнейший окислитель, гигроскопичен, очень ядовит.
наиболее
устойчивая
Степень окисления: +2; +3; +6
→ основные свойства ↓ ; кислотные свойства
→ окислительные свойства ; восстановительные свойства ↓

ПОЛУЧЕНИЕ
1)Пирометаллургический способ: FeO * Cr 2 O 3 +4C = 2Cr + Fe + 4CO
2)Алюминотермический способ: Cr 2 O 3 + 2Al = Al 2 O 3 + 2Cr

применение
Использование хрома основано на его жаропрочности, твердости и устойчивости против коррозии.
Больше всего хрома применяют для выплавки хромистых сталей. Значительное количество хрома идет на декоративные коррозионно-стойкие покрытия.
Широкое применение получил порошковый хром в производстве металлокерамических изделий и материалов для сварочных электродов. Хром в виде иона Cr3+ - примесь в рубине, который используется как драгоценный камень и лазерный материал.
Соединениями хрома протравливают ткани при крашении.
Из смеси хромита и магнезита изготовляют хромомагнезитовые огнеупорные изделия

применение
Хром - презентация, доклад, проект
Обратная связь
Если не удалось найти и скачать доклад-презентацию, Вы можете заказать её на нашем сайте. Мы постараемся найти нужный Вам материал и отправим по электронной почте. Не стесняйтесь обращаться к нам, если у вас возникли вопросы или пожелания:
Не стесняйтесь обращаться к нам, если у вас возникли вопросы или пожелания:
Email: [email protected]
Мы в социальных сетях
Социальные сети давно стали неотъемлемой частью нашей жизни. Мы узнаем из них новости, общаемся с друзьями, участвуем в интерактивных клубах по интересам
ВКонтакте >
Что такое Myslide.ru?
Myslide.ru - это сайт презентаций, докладов, проектов в формате PowerPoint. Мы помогаем учителям, школьникам, студентам, преподавателям хранить и обмениваться своими учебными материалами с другими пользователями.
Для правообладателей >
myslide.ru
Презентация по Химии "Хром. Роль хрома в организме человека"
Презентация на тему: Хром. Роль хрома в организме человекаСкачать эту презентацию
Скачать эту презентацию
№ слайда 1 Описание слайда:
Описание слайда: Хром. Роль хрома в организме человека
№ слайда 2 Описание слайда:
Описание слайда: Хром — элемент побочной подгруппы 6-ой группы 4-го периода периодической системы химических элементов Д. И. Менделеева с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром (CAS-номер: 7440-47-3) — твёрдый металл голубовато-белого цвета. Хром иногда относят к чёрным металлам.
№ слайда 3 Описание слайда:
Описание слайда: Люди используют хром в промышленности и медицине – в частности, с помощью его изотопов создаются определённые методы диагностики заболеваний. Хром также может входить в состав лекарственных и витаминных препаратов.
№ слайда 4 Описание слайда:
Описание слайда: Организму человека хром жизненно необходим – он входит в состав всех клеток, и ни один орган или ткань не обходится без этого элемента. В норме в организме постоянно должно быть около 6 мг хрома!
№ слайда 5 Описание слайда:
Описание слайда: Вместе с инсулином хром помогает организму усваивать сахар; участвует в транспортировке белков; приводит в норму углеводный обмен и способствует поддержанию здорового веса; нормализует функцию щитовидной железы и стимулирует процессы регенерации.
№ слайда 6 Описание слайда:
Описание слайда: Синтез нуклеиновых кислот тоже невозможен без хрома – он отвечает за целостность структуры РНК и ДНК, сохраняя неизменной наследственную информацию в генах. Поэтому для правильного роста тканей и их регенерации хром действительно необходим.
№ слайда 7 Описание слайда:
Описание слайда: Для щитовидной железы роль хрома просто спасительна – он может замещать йод, если того не хватает в организме по каким-то причинам.
№ слайда 8 Описание слайда:
Описание слайда: Хром – это элемент, который отвечает за поддержание нормального веса: он нормализует углеводный обмен и помогает организму перерабатывать жир. Благодаря этому жир не накапливается в виде отложений, и вес остаётся в норме. Хром обеспечивает профилактику остеопороза, укрепляя костную ткань; снижает артериальное давление и предупреждает развитие гипертонии; выводит токсины, радионуклиды, соли тяжёлых металлов.
№ слайда 9 Описание слайда:
Описание слайда: В сутки человеку требуется от 50 до 200 мкг хрома, но из неорганических соединений он усваивается плохо. При недостаточном поступлении хрома с пищей может развиться его дефицит, однако избыток хрома тоже опасен. В больших дозах хром становится токсичен для человека: отравления возникают после дозы в 200 мг, а 3 г и более могут стать смертельными.
№ слайда 10 Описание слайда:
Описание слайда: Хром в продуктах
№ слайда 11 Описание слайда:
Описание слайда: Основными источниками хрома считаются пивные дрожжи и печень, поэтому хотя бы один раз в неделю стоит стараться включать их в своё меню. Отварной картофель в кожуре, хлеб из грубой муки и свежие овощи можно есть каждый день, и пару раз в неделю – сыр, курицу, говядину.
№ слайда 12 Описание слайда:
Описание слайда: Другими природными источниками хрома являются проросшие зёрна пшеницы, чёрный перец, зернобобовые, перловка, крабы, устрицы, рыба, креветки, яйца, кукурузное масло; овощи – капуста, редис, свекла, помидоры; фрукты и ягоды – яблоки, виноград, сливы, вишни, черника, голубика, клюква, облепиха, рябина; лекарственные растения – гинкго билоба, сушеница, мелисса и другие.
№ слайда 13 Описание слайда:
Описание слайда: При диабете, беременности и кормлении грудью, а также в возрасте старше 45 лет рекомендуется дополнительно принимать хром – например, порошок пивных дрожжей, запаривая их кипятком и настаивая в течение получаса.
№ слайда 14 Описание слайда:
Описание слайда: Недостаток и дефицит хрома
№ слайда 15 Описание слайда:
Описание слайда: При таких заболеваниях, как атеросклероз, ожирение, диабет, различные инфекции, а также при стрессах, тяжёлых нагрузках, острой нехватке белка, содержание хрома в организме падает. Это можно узнать по волосам – количество хрома в них резко уменьшается.
№ слайда 16 Описание слайда:
Описание слайда: Когда хром расходуется организмом в больших количествах – например, во время беременности; или усиленно выводится, потому что человек питается преимущественно макаронами, белым хлебом и сладостями; или при тяжёлых физических нагрузках – это ведёт к его недостатку, а потом дефициту.
№ слайда 17 Описание слайда:
Описание слайда: При дефиците хрома человек быстро утомляется, плохо спит, его мучает беспокойство и головные боли; снижается чувствительность конечностей, появляется дрожь и нарушается координация мышц; в крови повышается уровень вредного холестерина, ч то ведёт к развитию атеросклероза. У одних людей возникает ожирение, а другие, наоборот, чрезмерно худеют; организм перестаёт нормально усваивать глюкозу, особенно в пожилом возрасте, и в крови постоянно нарушен её уровень – гипогликемия или гипергликемия. В таких условиях резко повышается возможность развития сахарного диабета, ишемической болезни; у мужчин нарушается репродуктивная функция.
№ слайда 18 Описание слайда:
Описание слайда: Избыток хрома
№ слайда 19 Описание слайда:
Описание слайда: Избыток хрома можно получать при его повышенном содержании в воздухе или из-за бесконтрольного приёма биодобавок с этим элементом. Однако при нехватке в питании таких элементов, как железо и цинк, избыток хрома тоже возможен, потому что организм в их отсутствие начинает всасывать хром более активно.
№ слайда 20 Описание слайда:
Описание слайда: Хрома бывает много, если люди работают на производствах, где в воздухе содержится хромовая пыль. На таких производствах случаи заболевания раком лёгких встречаются в несколько десятков раз чаще, чем там, где содержание хрома в норме.
№ слайда 21 Описание слайда:
Описание слайда: Медная пыль и шлаки также содержат хром, поэтому люди, работающие с этими веществами, часто болеют астмой и астматическим бронхитом.
№ слайда 22 Описание слайда:
Описание слайда: При избытке хрома изъязвляются слизистые оболочки и возникают воспалительные заболевания, аллергии, экземы, дерматиты, нервные расстройства, увеличивается риск развития рака.
№ слайда 23 Описание слайда:
Описание слайда: При отравлениях хромом надо срочно изолироваться от источника загрязнения и обратиться к врачу – он назначит лечение. Обычно людям, находящимся на работе в контакте с солями хрома, рекомендуется мыться в душе с особыми растворами.
№ слайда 24 Описание слайда:
Описание слайда: Спасибо за внимание!
ppt4web.ru
Презентация к уроку "Хром и его соединения"

Хром

ХРОМ
- Хром (лат. Cromium), Cr,
химический элемент VI группы периодической системы Менделеева,
- атомная масса 51,996;
- металл голубовато-стального цвета.

Элемент VI группы побочной подгруппы
Элемент под
№ 24 в периодической таблице Д.И.Менделеева
Элемент 4-ого периода
Cr
Массовая доля хрома в земной коре – 0,02%

Хромистый
железняк
FeO* Cr 2 O 3
Нахождение в природе
Хромит
FeCr 2 O 4
Крокоит
PbCrO 4

Месторождения хрома
- В земной коре хрома довольно много – 0,02%.
- Наша страна обладает огромными запасами хромитов. Одно из самых больших месторождений находится в Казахстане, в районе Актюбинска; оно открыто в 1936 г. Значительные запасы хромовых руд есть и на Урале.
- Большими запасами хромитов располагают Куба, Югославия, многие страны Азии и Африки.

История открытия
- В 1797 г. французский химик Л. Вокелен впервые исследовал красноватый, тяжелый минерал крокоизит, попавший в его руки из далекой Сибири.

- Крокоизит, чаще называемый крокоитом (от греческого "крокос" - шафран), -редкий минерал, найденный на Урале в 40-х года XVIII в. и описанный М. В. Ломоносовым .

- Затем он был найден в Сибири петербургским профессором химии И. Леманом в 1762 г. От него попал к Воклену, который открыл в сибирском минерале соединение нового элемента.

- Выделить этот элемент в чистом виде он не смог. Пораженный разнообразием окрасок, образуемых разными соединениями вновь открытого элемента, Воклен назвал его хромом (от греческого слова "хрома" - цвет, краска). В сравнительно чистом виде новый элемент был выделен в 1799 г. Ф. Тассером. Он представлял собой серо-стальной металл с серебристыми блестками в изломе, тугоплавкий (температура плавления 1800° С), не окисляющийся при обычных условиях, с плотностью, почти равной плотности железа.

Металл серебристо-белого цвета
Самый твердый металл
Тем.плавл.
1890 0 C
Физические
свойства
Хрупкий, с плотностью
7,2 г/см 3

Химические свойства хрома
1.Реагирует с неметаллами(при нагревании)
А)4Cr + 3O 2 =2Cr 2 O 3
Б)2Cr + N 2 =2CrN
В)2Cr +3S = Cr 2 S 3
2.Реагирует с парами воды(в раскаленном состоянии)
2Cr + 3H 2 O=Cr 2 O 3 + 3H 2
3.Реагирует с кислотами
Cr + H 2 SO 4 = CrSO 4 + H 2
4.Реагирует с солями менее активных металлов
Cr + CuSO 4 = CrSO 4 + Cu

Соединения хрома
Соединения хрома(II)
Соединения хрома(III)
Соединения хрома(VI)
Cr 2 O 3 -амфотерный оксид
CrO –основный оксид
Cr(OH) 3 -амфотерное соединение
Cr(OH) 2 -
основание
CrO 3 -кислотный оксид
H 2 CrO 4 -хромовая
(H 2 Cr 2 O 7 )-дихромовая кислоты

Соединения хрома(II)
1.Реагирует с кислотами
- При нагревании разлагается
CrO+2HCL=
Cr(OH) 2 =CrO + H 2 O
=CrCL 2 +H 2 O
2.Реагирует с кислотами
2.Окисляется кислородом воздуха
Cr(OH) 2 +H 2 SO 4 =
=CrSO 4 +2H 2 O
4CrO + O 2 =2Cr 2 O 3
SO4

Соединения хрома(III)
Cr 2 O 3 –при обычных условиях не реагирует с растворами кислот и щелочей .
1.Реагирует с кислотами
Cr 2 O 3 –реагирует лишь при сплавлении
Cr(OH) 3 + 3HCL=
Cr 2 O 3 +Ba(OH) 2 =
=CrCL 3 + 3 H 2 O
=Ba(CrO 2 ) 2 +H 2 O
2.Реагирует с щелочами
Cr(OH) 3 +3NaOH=
Реагирует с более активными металлами
Cr 2 O 3 + 2Al= Al 2 O 3 + 2Cr
=Na 3 (Cr(OH) 6 )
3.При нагревании разлагается
2Cr(OH) 3 =Cr 2 O 3 + 3H 2 O

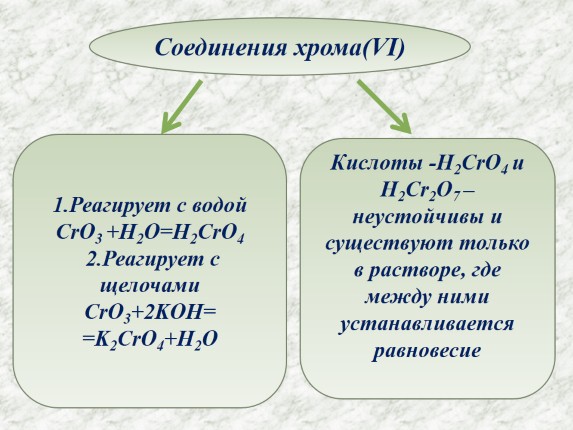
Соединения хрома(VI)
1.Реагирует с водой
Кислоты -H 2 CrO 4 и H 2 Cr 2 O 7 –неустойчивы и существуют только в растворе, где между ними устанавливается равновесие
CrO 3 +H 2 O=H 2 CrO 4
2.Реагирует с щелочами
CrO 3 +2KOH=
=K 2 CrO 4 +H 2 O

В нагревательных элементах электрических печей(сплав железа ,никеля и хрома)
В производстве стали
Применение хрома
Хромирование(создание
защитных и декоративных покрытий)

Применение хрома
Использование хрома основано на его жаропрочности, твердости и устойчивости против коррозии.
Больше всего хрома применяют для выплавки хромистых сталей. Значительное количество хрома идет на декоративные коррозионно-стойкие покрытия.
Широкое применение получил порошковый хром в производстве металлокерамических изделий и материалов для сварочных электродов. Хром в виде иона Cr3+ - примесь в рубине, который используется как драгоценный камень и лазерный материал.
Соединениями хрома протравливают ткани при крашении.
Из смеси хромита и магнезита изготовляют хромомагнезитовые огнеупорные изделия .

Наглядное применение хрома

Сульфат хрома и хромокалиевые квасцы используют для изготовления прочной хромовой кожи
Применение соединений хрома
Соединения хрома применяют в качестве минеральных красок
Хромовую смесь используют для мытья химической посуды в лабораториях

Роль хрома в живых организмах
Важные факты:
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов. Снижение содержания хрома в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
В конце 1950-х гг. два исследователя, Шварц и Мерц, сообщили, что у крыс, которые были на рационе, дефицитном по хрому, развивалась непереносимость сахара; при добавлении же хрома в рацион их состояние нормализовалось. Это было первым подтверждением, что хром необходим животным для нормальной жизни. С тех пор исследователи поняли, что хром играет такую же роль и для здоровья человека.

Пищевые источники хрома
- пшеничные ростки, печень, мясо, сыр, бобы, горох, цельное зерно, черный перец, мелисса, пивные дрожжи.

Проверь себя
С какими из перечисленных ниже веществ
будет реагировать хром
H 2 SO 4
Cu(NO 3 ) 2
Al
KCL
NaNO 3
HCL

Проверь себя
Оксид и гидроксид хрома (II) реагируют
со следующими веществами
H 2 SO 4
HNO 3
HCL
CaCL 2
NaOH
CuO

Ссылки на источники информации и изображения:
Википедия
http://im7-tub-ru.yandex.net/i?id=152996174-45-72&n=21
http://im5-tub-ru.yandex.net/i?id=92218102-28-72&n=21
http://im7-tub-ru.yandex.net/i?id=113413894-55-72&n=21
http://im2-tub-ru.yandex.net/i?id=31291566-60-72&n=21
http://dabi.ru/attachments/7044/6952/images/large.jpg
http://im0-tub-ru.yandex.net/i?id=461512314-61-72&n=21
http://im0-tub-ru.yandex.net/i?id=410341235-12-72&n=21
http://im6-tub-ru.yandex.net/i?id=373203664-10-72&n=21
http://im7-tub-ru.yandex.net/i?id=47417297-37-72&n=21
multiurok.ru
Презентация к уроку "Хром и его соединения"

Хром

ХРОМ
- Хром (лат. Cromium), Cr,
химический элемент VI группы периодической системы Менделеева,
- атомная масса 51,996;
- металл голубовато-стального цвета.

Элемент VI группы побочной подгруппы
Элемент под
№ 24 в периодической таблице Д.И.Менделеева
Элемент 4-ого периода
Cr
Массовая доля хрома в земной коре – 0,02%

Хромистый
железняк
FeO* Cr 2 O 3
Нахождение в природе
Хромит
FeCr 2 O 4
Крокоит
PbCrO 4

Месторождения хрома
- В земной коре хрома довольно много – 0,02%.
- Наша страна обладает огромными запасами хромитов. Одно из самых больших месторождений находится в Казахстане, в районе Актюбинска; оно открыто в 1936 г. Значительные запасы хромовых руд есть и на Урале.
- Большими запасами хромитов располагают Куба, Югославия, многие страны Азии и Африки.

История открытия
- В 1797 г. французский химик Л. Вокелен впервые исследовал красноватый, тяжелый минерал крокоизит, попавший в его руки из далекой Сибири.

- Крокоизит, чаще называемый крокоитом (от греческого "крокос" - шафран), -редкий минерал, найденный на Урале в 40-х года XVIII в. и описанный М. В. Ломоносовым .

- Затем он был найден в Сибири петербургским профессором химии И. Леманом в 1762 г. От него попал к Воклену, который открыл в сибирском минерале соединение нового элемента.

- Выделить этот элемент в чистом виде он не смог. Пораженный разнообразием окрасок, образуемых разными соединениями вновь открытого элемента, Воклен назвал его хромом (от греческого слова "хрома" - цвет, краска). В сравнительно чистом виде новый элемент был выделен в 1799 г. Ф. Тассером. Он представлял собой серо-стальной металл с серебристыми блестками в изломе, тугоплавкий (температура плавления 1800° С), не окисляющийся при обычных условиях, с плотностью, почти равной плотности железа.

Металл серебристо-белого цвета
Самый твердый металл
Тем.плавл.
1890 0 C
Физические
свойства
Хрупкий, с плотностью
7,2 г/см 3

Химические свойства хрома
1.Реагирует с неметаллами(при нагревании)
А)4Cr + 3O 2 =2Cr 2 O 3
Б)2Cr + N 2 =2CrN
В)2Cr +3S = Cr 2 S 3
2.Реагирует с парами воды(в раскаленном состоянии)
2Cr + 3H 2 O=Cr 2 O 3 + 3H 2
3.Реагирует с кислотами
Cr + H 2 SO 4 = CrSO 4 + H 2
4.Реагирует с солями менее активных металлов
Cr + CuSO 4 = CrSO 4 + Cu

Соединения хрома
Соединения хрома(II)
Соединения хрома(III)
Соединения хрома(VI)
Cr 2 O 3 -амфотерный оксид
CrO –основный оксид
Cr(OH) 3 -амфотерное соединение
Cr(OH) 2 -
основание
CrO 3 -кислотный оксид
H 2 CrO 4 -хромовая
(H 2 Cr 2 O 7 )-дихромовая кислоты

Соединения хрома(II)
1.Реагирует с кислотами
- При нагревании разлагается
CrO+2HCL=
Cr(OH) 2 =CrO + H 2 O
=CrCL 2 +H 2 O
2.Реагирует с кислотами
2.Окисляется кислородом воздуха
Cr(OH) 2 +H 2 SO 4 =
=CrSO 4 +2H 2 O
4CrO + O 2 =2Cr 2 O 3
SO4

Соединения хрома(III)
Cr 2 O 3 –при обычных условиях не реагирует с растворами кислот и щелочей .
1.Реагирует с кислотами
Cr 2 O 3 –реагирует лишь при сплавлении
Cr(OH) 3 + 3HCL=
Cr 2 O 3 +Ba(OH) 2 =
=CrCL 3 + 3 H 2 O
=Ba(CrO 2 ) 2 +H 2 O
2.Реагирует с щелочами
Cr(OH) 3 +3NaOH=
Реагирует с более активными металлами
Cr 2 O 3 + 2Al= Al 2 O 3 + 2Cr
=Na 3 (Cr(OH) 6 )
3.При нагревании разлагается
2Cr(OH) 3 =Cr 2 O 3 + 3H 2 O

Соединения хрома(VI)
1.Реагирует с водой
Кислоты -H 2 CrO 4 и H 2 Cr 2 O 7 –неустойчивы и существуют только в растворе, где между ними устанавливается равновесие
CrO 3 +H 2 O=H 2 CrO 4
2.Реагирует с щелочами
CrO 3 +2KOH=
=K 2 CrO 4 +H 2 O

В нагревательных элементах электрических печей(сплав железа ,никеля и хрома)
В производстве стали
Применение хрома
Хромирование(создание
защитных и декоративных покрытий)

Применение хрома
Использование хрома основано на его жаропрочности, твердости и устойчивости против коррозии.
Больше всего хрома применяют для выплавки хромистых сталей. Значительное количество хрома идет на декоративные коррозионно-стойкие покрытия.
Широкое применение получил порошковый хром в производстве металлокерамических изделий и материалов для сварочных электродов. Хром в виде иона Cr3+ - примесь в рубине, который используется как драгоценный камень и лазерный материал.
Соединениями хрома протравливают ткани при крашении.
Из смеси хромита и магнезита изготовляют хромомагнезитовые огнеупорные изделия .

Наглядное применение хрома

Сульфат хрома и хромокалиевые квасцы используют для изготовления прочной хромовой кожи
Применение соединений хрома
Соединения хрома применяют в качестве минеральных красок
Хромовую смесь используют для мытья химической посуды в лабораториях

Роль хрома в живых организмах
Важные факты:
Хром — один из биогенных элементов, постоянно входит в состав тканей растений и животных. У животных хром участвует в обмене липидов, белков (входит в состав фермента трипсина), углеводов. Снижение содержания хрома в пище и крови приводит к уменьшению скорости роста, увеличению холестерина в крови.
В конце 1950-х гг. два исследователя, Шварц и Мерц, сообщили, что у крыс, которые были на рационе, дефицитном по хрому, развивалась непереносимость сахара; при добавлении же хрома в рацион их состояние нормализовалось. Это было первым подтверждением, что хром необходим животным для нормальной жизни. С тех пор исследователи поняли, что хром играет такую же роль и для здоровья человека.

Пищевые источники хрома
- пшеничные ростки, печень, мясо, сыр, бобы, горох, цельное зерно, черный перец, мелисса, пивные дрожжи.

Проверь себя
С какими из перечисленных ниже веществ
будет реагировать хром
H 2 SO 4
Cu(NO 3 ) 2
Al
KCL
NaNO 3
HCL

Проверь себя
Оксид и гидроксид хрома (II) реагируют
со следующими веществами
H 2 SO 4
HNO 3
HCL
CaCL 2
NaOH
CuO

Ссылки на источники информации и изображения:
Википедия
http://im7-tub-ru.yandex.net/i?id=152996174-45-72&n=21
http://im5-tub-ru.yandex.net/i?id=92218102-28-72&n=21
http://im7-tub-ru.yandex.net/i?id=113413894-55-72&n=21
http://im2-tub-ru.yandex.net/i?id=31291566-60-72&n=21
http://dabi.ru/attachments/7044/6952/images/large.jpg
http://im0-tub-ru.yandex.net/i?id=461512314-61-72&n=21
http://im0-tub-ru.yandex.net/i?id=410341235-12-72&n=21
http://im6-tub-ru.yandex.net/i?id=373203664-10-72&n=21
http://im7-tub-ru.yandex.net/i?id=47417297-37-72&n=21
multiurok.ru
Презентация «Хром»
Слайды и текст этой презентации
Слайд 1

ХромРаботу выполнил Учитель химии ГБОУ СОШ № 1465 им. Н.Г. Кузнецова г. Москва Попова Светлана Анатольевна
Слайд 2

CrЭлемент под № 24 в периодической системе Д.И.МенделееваЭлемент VI группы побочной подгруппы Элемент 4-ого периодаМассовая доля хрома в земной коре – 0,02%
Слайд 3
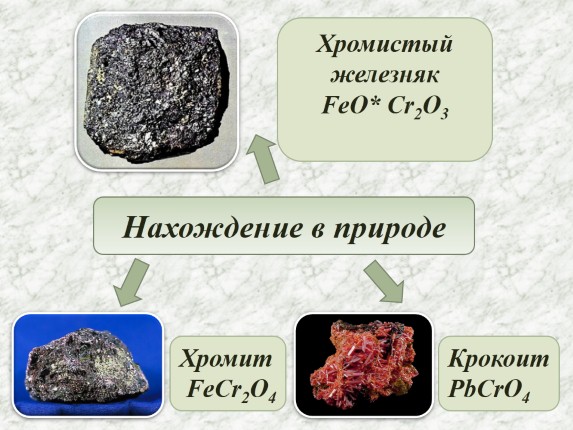
Нахождение в природеХромистый железняк FeO* Cr2O3 Хромит FeCr2O4Крокоит PbCrO4
Слайд 4
Физические свойстваМеталл серебристо-белого цветаСамый твердый металлХрупкий, с плотностью 7,2 г/см3Температура плавления 18900C
Слайд 5

Химические свойства хрома1.Реагирует с неметаллами(при нагревании) А) 4Cr + 3O2 =2Cr2O3 Б) 2Cr + N2 =2CrN В) 2Cr +3S = Cr2S3 2.Реагирует с парами воды (в раскаленном состоянии) 2Cr + 3h3O=Cr2O3 + 3h3 3.Реагирует с кислотами Cr + h3SO4 = CrSO4 + h3 4.Реагирует с солями менее активных металлов Cr + CuSO4 = CrSO4 + Cu
Слайд 6

Применение хромаВ производстве хромированной, т.е. обладающей антикоррозионными свойствами, стали
Слайд 7

В нагревательных элементах электрических печей (сплав железа, никеля и хрома)
Слайд 8

Хромирование (создание защитных от коррозии, а также декоративных покрытий)
Слайд 9

Соединения хромаСоединения хрома(II)CrO –основный оксид Cr(OH)2- основаниеСоединения хрома(III)Cr2O3-амфотерный оксид Cr(OH)3-амфотерный гидроксидСоединения хрома(VI)CrO3-кислотный оксид h3CrO4 - хромовая h3Cr2O7 - дихромовая кислоты
Слайд 10
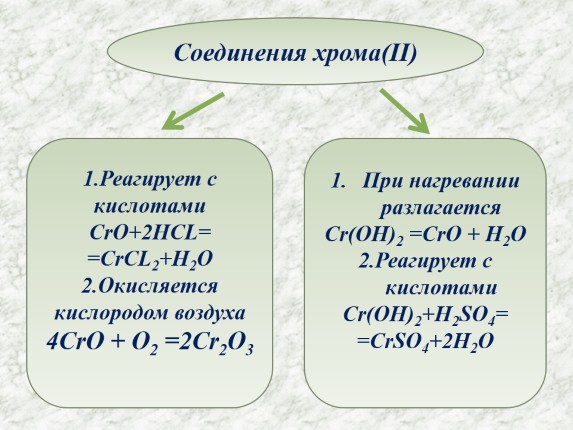
Соединения хрома(II)1.Реагирует с кислотами CrO+2HCL= =CrCL2+h3O 2.Окисляется кислородом воздуха 4CrO + O2 =2Cr2O3 При нагревании разлагается Cr(OH)2 =CrO + h3O 2.Реагирует с кислотами Cr(OH)2+h3SO4= =CrSO4+2h3O
Слайд 11

Соединения хрома(III)Cr2O3 –при обычных условиях не реагирует с растворами кислот и щелочей . Cr2O3 –реагирует лишь при сплавлении Cr2O3+Ba(OH)2= =Ba(CrO2)2+h3O Реагирует с более активными металлами Cr2O3 + 2Al= Al2O3 + 2Cr1.Реагирует с кислотами Cr(OH)3 + 3HCL= =CrCL3 + 3 h3O 2.Реагирует с щелочами Cr(OH)3+3NaOH= =Na3(Cr(OH)6) 3.При нагревании разлагается 2Cr(OH)3=Cr2O3 + 3h3O
Слайд 12
Соединения хрома(VI)1.Реагирует с водой CrO3 +h3O=h3CrO4 2.Реагирует с щелочами CrO3+2KOH= =K2CrO4+h3OКислоты -h3CrO4 и h3Cr2O7 –неустойчивы и существуют только в растворе, где между ними устанавливается равновесие
Слайд 13

СолиХроматы (хромовой кислоты)Дихроматы (дихромовой кислоты)Дихроматы - термически неустойчивые соединения. Реакция разложения дихромата Аммония (опыт «Вулканчик») (Nh5)2Cr2O7=Cr2O3+N2+4h3OХроматы - термически устойчивые соединения
Слайд 14

Сульфат хрома и хромокалиевые квасцы используют для изготовления прочной хромовой кожиСоединения хрома применяют в качестве минеральных красокХромовую смесь используют для мытья химической посуды в лабораторияхПрименение соединений хрома
Слайд 15

Проверь себяС какими из перечисленных ниже веществ будет реагировать хромh3SO4AlKCLHCLNaNO3Cu(NO3)2
Слайд 16
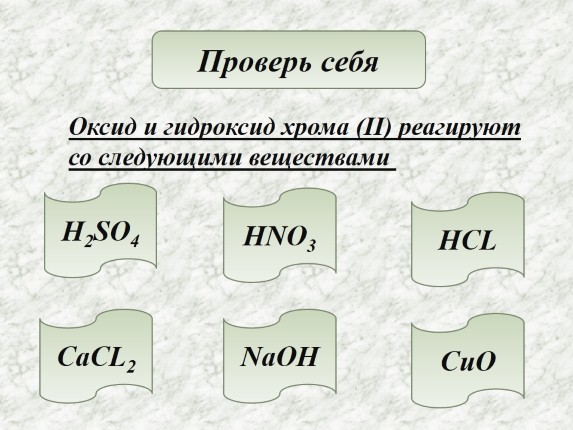
Проверь себяОксид и гидроксид хрома (II) реагируют со следующими веществами h3SO4HNO3HCLCaCL2NaOHCuO
Слайд 17
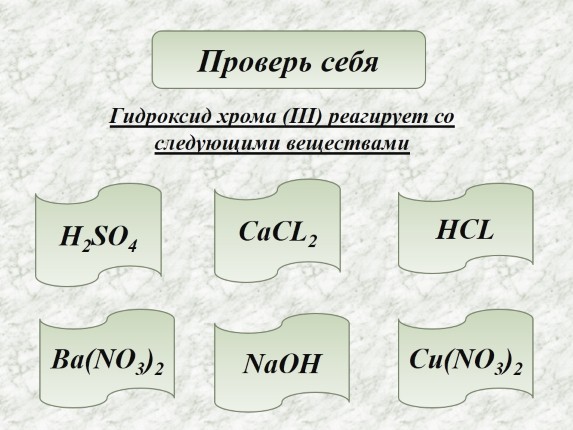
Проверь себяГидроксид хрома (III) реагирует со следующими веществами h3SO4NaOHHCLCaCL2Cu(NO3)2Ba(NO3)2
Слайд 18

http://im5-tub-ru.yandex.net/i?id=92218102-28-72&n=21 http://im7-tub-ru.yandex.net/i?id=152996174-45-72&n=21 http://im7-tub-ru.yandex.net/i?id=113413894-55-72&n=21 http://im2-tub-ru.yandex.net/i?id=31291566-60-72&n=21 http://dabi.ru/attachments/7044/6952/images/large.jpg http://im0-tub-ru.yandex.net/i?id=461512314-61-72&n=21 Ссылки на источники информации и изображения:И.И.Новошинский Н.С.Новошинская Химия 10 класс профильный уровеньhttp://im0-tub-ru.yandex.net/i?id=410341235-12-72&n=21 http://im6-tub-ru.yandex.net/i?id=373203664-10-72&n=21 http://im7-tub-ru.yandex.net/i?id=47417297-37-72&n=21
Слайд 19

http://im4-tub-ru.yandex.net/i?id=265735803-28-72&n=21 http://im0-tub-ru.yandex.net/i?id=133081635-30-72&n=21 http://im1-tub-ru.yandex.net/i?id=135592427-63-72&n=21 http://im0-tub-ru.yandex.net/i?id=91276844-53-72&n=21 http://im6-tub-ru.yandex.net/i?id=23055640-49-72&n=21 http://im1-tub-ru.yandex.net/i?id=201882312-37-72&n=21 http://im6-tub-ru.yandex.net/i?id=18739247-65-72&n=21 http://im2-tub-ru.yandex.net/i?id=264409642-08-72&n=21 http://im5-tub-ru.yandex.net/i?id=278346523-62-72&n=21
lusana.ru
Презентация хром | Образовательный портал EduContest.Net — библиотека учебно-методических материалов
Чтобы посмотреть презентацию с картинками, оформлением и слайдами, скачайте ее файл и откройте в PowerPoint на своем компьютере.Текстовое содержимое слайдов презентации: Элемент № 24Х Р О М Хром — элемент побочной подгруппы шестой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 24 Электронная формулаCr +24 1s2|2s22p6|3s23p63d5|4s1style.fontSize История открытияВ 1797 г. французский химик Л. Вокелен впервые исследовал красноватый, тяжелый минерал крокоизит, попавший в его руки из далекой Сибири. Крокоизит, чаще называемый крокоитом (от греческого "крокос" - шафран), -редкий минерал, найденный на Урале в 40-х года XVIII в. и описанный М. В. Ломоносовым. Затем он был найден в Сибири петербургским профессором химии И. Леманом в 1762 г. От него попал к Вокелену, который открыл в сибирском минерале соединение нового элемента. Выделить этот элемент в чистом виде он не смог. Пораженный разнообразием окрасок, образуемых разными соединениями вновь открытого элемента, Вокелен назвал его хромом (от греческого слова "хрома" - цвет, краска). В сравнительно чистом виде новый элемент был выделен в 1799 г. Ф. Тассером. Он представлял собой серо-стальной металл с серебристыми блестками в изломе, тугоплавкий (температура плавления 1800° С), не окисляющийся при обычных условиях, с плотностью, почти равной плотности железа.Месторождения хромаВ земной коре хрома довольно много – 0,02%. Хромовая руда носит название хромитов или хромистого железняка (потому, что почти всегда содержит и железо). Наша страна обладает огромными запасами хромитов. Одно из самых больших месторождений находится в Казахстане, в районе Актюбинска; оно открыто в 1936 г. Значительные запасы хромовых руд есть и на Урале.Большими запасами хромитов располагают Куба, Югославия, многие страны Азии и Африки.style.rotation
ПолучениеХром получают в промышленности из оксида хрома(III) методом алюминотермии: Cr2O3+2Al=Al2O3+2Cr Физические свойстваХром - серебристо-белый металл. Температура плавления 1890оС, плотность 7,19 г/см3. Чистый хром достаточно пластичен, а технический - самый твёрдый из всех металлов.Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 ,56. Химические свойстваХром химичес
educontest.net