1 Понятие координационного соединения. Координационное число хрома
Координационные соединения хрома - Справочник химика 21
Координационные соединения хрома [c.74]IV. КРИСТАЛЛИЧЕСКИЕ СТРУКТУРЫ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ ХРОМА, МАРГАНЦА, ЖЕЛЕЗА И КОБАЛЬТА [c.3]
Краткие сведения о строении координационных соединений хрома, марганца, железа и кобальта, приведенные на предыдущих страницах, не претендуют, естественно, на роль сколько-нибудь полного обзора стереохимии (и тем более кристаллохимии) этих элементов. В соответствии с характером задач, которые преследуются в публикациях серии Итоги науки , мы ограничились анализом тех результатов, которые были получены за последние годы. Другие структурные материалы привлекались лишь для сопоставления, проведения аналогий и установления различий. Всестороннее освещение стереохимии потребовало бы значительно более полного использования как всех имеющихся структурных данных, так и косвенных сведений о строении комплексов, вытекающих из совокупности химических, спектральных, магнитных и других свойств соединений. [c.63]
Известно очень много устойчивых координационных соединений кобальта(П1), которые проявляют некоторое сходство с координационными соединениями хрома(И1). [c.564]
Кобальт(П1) относится к тем немногим ионам металлов, для которых характерно образование инертных комплексов такими свойствами обладают еще хром(П1), пла-тина(1У) и платина(П). Комплексы этих ионов сохраняются в растворе достаточно долго, чтобы можно было изучить их структуру и свойства. Поэтому они принадлежат к числу тех комплексов, которые были изучены ранее всего и на примере которых химики изучали структуру и изомерию координационных соединений. [c.385]
Объясните характер изменения свойств раствора по мере увеличения числа молекул аммиака в составе соли. Напишите координационные формулы соединений. Каково координационное число хрома [c.227]
Соединения Сг (Ш). У хрома степень окисления +3 является наиболее устойчивой. Координационное число хрома (П1) равно шести, [c.607]
Механизм хромового дубления еще неясен поскольку хромовый комплекс в обычных условиях дубления может иметь заряд, однозначный заряду вещества кожи, то обычное представление о взаимном осаждении не может дать объяснения. Вполне возможно, что дубление заключается в образовании координационного соединения хромового комплекса с коллагеном. Положение далее усложняется тем, что при постоянном значении pH фиксация хрома происходит соответственно адсорбционной изотерме Фрейндлиха (стр. 100), если вести расчет по концентрации хрома в дубильном растворе. Степень начального связывания быстро возрастает с увеличением pH. Поэтому хром вводится при низких значениях pH, чтобы обеспечить полное проникновение и соединение с кожей при тщательно проводимой нейтрализации. [c.392]
Окиснохромовый катализатор относится к однокомпонентным катализаторам полимеризации олефинов, в к-рых образование центров роста не требует обработки соединения металла переменной валентности металлоорганич. соединением. Существует точка зрения, согласно к-рой активный компонент окиснохромового катализатора — поверхностные соединения хрома в степени окисления 6 (предположительно поверхностные хроматы). Образование центров роста связано с восстановлением до соединений, в к-рых степень окисления ионов хрома не превышает 3. При алкилировании мономером координационно ненасыщенных ионов хрома в низкой степени окисления происходит образование активной связи металл — углерод. [c.221]
Комплексы трехвалентного хрома. Существуют тысячи - комплексов хрома (III), которые, за редкими исключениями, все имеют координационное число 6. Основным характеризующим их свойством является кинетическая, устойчивость в водных растворах. Именно поэтому так много этих комплексов удалось выделить и поэтому столько классических исследований основоположников комплексной химии, прежде всего Иергенсена и Вернера, было выполнено на соединениях хрома. Эти комплексы сохраняются в растворах даже в тех случаях, когда они термодинамически должны быть неустойчивы, [c.460]
Среди индуцированных светом изомеризаций координационных соединений известны геометрическая, оптическая и связевая (или структурная). Такие фотохимические изомеризации можно изучать лишь для кинетически инертных комплексных соединений. К ним относятся наряду с октаэдрическими комплексами платины(IV) и квадратно-плоскостными платины(II) преимущественно октаэдрические комплексы хрома(III) и кобальта(III) [21]. [c.288]
После хромирования волокно тщательно промывают, чтобы удалить остатки соединений хрома с поверхности волокна. Трехвалентный хром настолько прочно фиксируется кератином путем образования координационных связей, что не вымывается водой даже при кипячении, и при последующем крашении образует комплекс с красителем, строение которого можно представить схемой [c.93]
Сравнение состава и строения карбонильных соединений Мо и Ш с аналогичными соединениями Сг показывает, что переход от Сг к Мо и У сопровождается увеличением координационного числа металла в соединениях хрома лиганд X отсутствует и фортепианная табуретка , моделирующая структуру комплекса, имеет не четыре, а только три ножки . [c.30]
Соединения Сг([П), Мо(П1), W (III). У хрома степень окисления -ЬЗ является наиболее устойчивой. Координационное число хрома (HI) равно шести, поэтому его комплексы (структурные единицы) имеют форму октаэдра. Валентные электроны в октаэдрических комплексах Сг (HI) располагаются только на связывающих и несвязывающих орбиталях [c.558]
Студенту дали 1,00 г бихромата аммония для получения координационного соединения. Этот образец был сожжен, в результате чего получились оксид хрома(1П), вода и газообразный азот. Оксид хро-ма(П1) заставили прореагировать при 600 С с тетрахлоридом углерода, в результате чего получились хлорид хрома(П1) и фосген (СОСЬ). Обработка хлорида хрома(П1) в избыточном количестве жидкого аммиака привела к образованию хлорида гексамминхрома(П1). Вычислите [c.248]
Для хрома и его аналогов наиболее типичны производные высщей степени окисления, во многом сходные с соответствующими соединениями серы. Соединения хрома (VI) отличаются неустойчивостью в растворах и являются сильными окислителями. При этом они чаще всего восстанавливаются до анионных или катионных комплексов хрома (Ш). Хотя хром располагается в четной группе, наиболее устойчивой его степенью окисления является Ч-З. Это связано с тем, что соединения хрома (III) являются, как правило, комплексными с координационным числом 6 и октаэдрической пространственной конфигурацией расположения лигандов. В этом случае три Зй-электрона иона Сг + равномерно заселяют трижды вырожденные несвязывающие МО комплекса (см. рис. 13,5 д). Возникающая стабилизация системы за счет суммарного спина 3 V2 = V2 (по правилу Хунда) в этом случае больше, чем если бы степень окисления хрома была + 2, -f-4 и т. д. [c.511]
Особую разновидность стереоспецифической полимеризации представляют собой катализаторы — оксиды металлов, нанесенные на поверхность инертных веществ (силикагель, оксид алюминия и др). Наиболее часто используются в качестве катализаторов оксиды хрома. При полимеризации а-олефинов формируются стереорегулярные структуры. Днены образуют обычно гране-1,4-полимеры. Основой каталитического действия этих катализаторов является способность хрома менять свое валентное состояние. При этом считается, что начальный акт полимеризации осуществляется соединениями хрома (VI), а за рост макромолекул ответственны соединения хрома (И) и хрома (И1). Скорость полимеризации этилена, например, растет, если восстановление хрома идет быстрее и глубже. После образования промежуточного соединения мономера с хромом (VI) и его восстановления до низших валентных состояний и десорбции продуктов взаимодействия образуется центр роста цепи за счет координационной ненасыщенности хрома [6. [c.56]
С3Н5 (НН2)з — триаминопропан). Учитывая это, например, формулы комплексных соединений хрома будут записаны так Кз[Сг ( N)в],Kз [Сг(Сг04)з]— в последнем случае каждый ион СаО занимает два координационных места. [c.121]
В структурном отношении исследованы нормальный и протонированный комплексонаты хрома(III) с ЭДТА, гидроксокомплексонат ЭДДА и биядерный комплекс с ТТГА [238] Во всех этих соединениях координационным полиэдром хрома [c.369]
Некоторые химические (комплексопометрическое титрование) и физико-химические (спектрофотометрические, кинетические, полярографические) методы имеют ограниченное применение для определения хрома нли требуют специальных условий для проведения анализа. Это обусловлено кинетической инертностью ак-вокомплекса Сг(1П). В книге детально рассматриваются вопросы состояния и состава комплексных соединений хрома в растворах, кинетики обмена между молекулами и ионами, входящими в состав внутренней координационной сферы комплексных соедине-11ИЙ. Эти процессы определяют не только чувствительность и воспроизводимость многих методов анализа, но и эффективность хроматографических и экстракционных методов отделения хрома от других элементов. [c.6]
Образование лабильного комплекса SOg с металл-ионом катализатора, по мнению ряда исследователей, является важным этапом реакции жидкофазного гомогеннокаталитического окисления SOg водными растворами солей марганца. Сравнительно высокую активность Сг-содержащих контактов в рассматриваемой реакции можно попытаться связать со способностью ионов Сг +, присутствие которых вероятно на поверхности хром-оловянных и железо-хромовых контактов, образовывать координационные соединения с кислыми газами, например SOg. Во всяком случае, именно склонностью ионов Сг + к образованию комплексных соединений с НС1 объясняются каталитические свойства окиси хрома в реакции окисления хлористого водорода. [c.268]
Элементы группы VIII образуют колоссальное количество комплексных ионов и координационных соединений. По вкладу, внесенному в химию при изучении комплексов, платина, вероятно, почти не уступает хрому. Многие комплексы, упоминавшиеся в гл. 37, образованы элементами группы VIII. [c.337]
Интересные результаты о влиянии неводного электролита на электрохимическое поведение координационных соединений были получены при изучении ацетилацетонатов железа (П1), никеля (И), кобальта (П1 и И), меди (П), палладия (П) и хрома (И1) в ацетонитриде на ртутном электроде [29] в присутствии перхлоратов лития и тетраэтиламмония. Это исследование является одним из первых, где показано, что в растворителе с низкой диэлектрической проницаемостью у электрода возможно взаимодействие сопутствующего электролита с деполяризатором или продуктом его электродной реакции, согласно ранее выведенной теории [13] (координационная релаксация), [c.263]
За исключением приведенного примера, все остальные соединения Сг" имеют координационное число 6 и геометрию искаженного октаэдра (см. сл. раздел). В октаэдрической координации возможны два способа распределения электронов и Имеющиеся магнитные данные для соединений хрома(И) .3 6] показывают, что они, как правило, относятся к высокоспиновым комплексам. Обычно для них выполняется закон Кюри — Вейсса, и величина момента составляет 4,95 гв,т. е. близка к чисто спиновому значению. Помимо солей алифатических карбоновых кислот (алканоатов) и бензоата, известен формиат в двух формах красной диамагнитной и голубой парамагнитной. По-види, юму, их структура отличается от структуры ацетата (см. стр. 324). Ион [Сг(С )е1 и.меет магнитный момент 3,2 в и, следовательно, является низкоспиновым комплексом. [c.232]
Все эти соединения окрашены в зеленый цвет, и для них характерно изменение окраски в широких пределах при постоянном химическом составе. Свойство это характерно не только для твердых соединений, у которых изменение цвета может быть обусловлено дисперсностью и кристаллической структурой частиц, но и для растворов. Окраска растворов солей хрома может колебаться от зеленой до фиолетовой в зависимости ог температуры раствора, его концентрации, наличия избытка кислоты и т. д. На холоду растворы соединений хрома обычно окрашены в синефиолетовый цвет, а при нагревании — в зеленый. Согласно координационной теории такое различие окраски зависит от степени гидратации иона хрома фиолетовая окраска растворов обусловлена максимальной гидратацией [Сг бНгО] а зеленая — наличием ряда изомеров с различным числом кислотных радикалов в комплексе, например, [Сг 5НгО С1] , [Сг 4НгО СЬ] и т. д. [c.408]
Растворы солен хрома(111) обычно имеют сине-фиолетовый цвет, но при нагревании становятся зелеными, а спустя некоторое время после охлаждения снова прибретают прежнюю окраску. Это изменение окраски объясняется образованием изомерных гидратов солей, представляющих собой комплексные соединения, в которых все или час- молекул воды координационно связаны во внутренней сфере комплекса, В некоторых случаях такие гидраты удалось выделить в твердом виде. Так, кристаллогидрат хлорида хрома(1П) СгС1з-6Н20 известен в трех изомерных формах в виде сине-фиолетовых, темно-зеленых и светло-зеленых кристаллов одинакового состава. Строение этих изомеров можно установить на основании различного отношения их свежеприготовленных растворов к нитрату серебра. При действии последнего на раствор сине-фиолетового гидрата осаждается весь хлор из раствора темно-зеленого гидрата осаждается 2/3 хлора, а из раствора светло-зеленого гидрата — только 1/3 хлора. Принимая во внимание эти данные, а также координационное число хрома, равное шести, строение рассматриваемых кристаллогидратов можно выразить следующими формулами [c.635]
Для разделения оптических изомеров многих электронейт-ральных координационных соединений в последние годы успешно применялась хроматография на колонках с О-лакто-зой. Так, было достигнуто расщепление октаэдрических грг с-ацетилацетонатов хрома и кобальта [16], иттрия и гадолиния [17], родия [18, 19], но не железа, галлия и индия [16], комплексы которых быстро рацемизуются. Хроматографией на лактозе расщепляется трыс-бензоилацетонат хрома [20]. Адсорбция комплексов некоторых пространственно затрудненных р-кетоиминов с Си(2-Ь) и N (2-1-) на колонке с О-лактозой с последующим элюированием смесью бензол-петро-лейный эфир приводит к их частичному расщеплению [21]. Отрицательные результаты были получены при попытке расщепления плоско-квадратного Си (2- -)-комплекса бис-(4-ими-но-2-пентанона1, тогда как его тетраэдрический N1 (2-Ь)-аналог частично расщепляется. [c.49]
По химической природе аппреты можно разделить на следующие группы [182] силаны (нереакциопноспособные, реакционноспособные и каталитического действия) комплексные соединения (хрома с метакрилатами и т. д.) титанорганические соединения соединения фосфора (диэтилфосфит, соединения со связями Si—О—R и др.) органические кислоты и их соли амины, алкил-фенолы и другие соединения. К аппретам можно отнести [185, 196] моноалкоксиды, моноалкоксипирофосфаты, хелатные и другие координационные соединения. [c.44]
chem21.info
Координационное число - это... Что такое Координационное число?
Координационное число (в химии и кристаллографии) — характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле.
Координационное число в химии
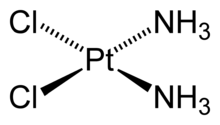
 Строение цис-дихлородиамминплатины (II)
Строение цис-дихлородиамминплатины (II) В химии понятие координационного числа появилось с развитием химии комплексных соединений.
Под ним подразумевается число лигандов (атомов, молекул, ионов), которые образуют первую координационную (внутреннюю) сферу комплексообразователя[1].Например, в комплексной соли гексацианоферрате(III) калия K3[Fe(CN)6] координационное число иона Fe3+ равно 6, а в цис-дихлородиамминплатине (II) (соли Пейроне) Pt(Nh4)2Cl2 центральный атом платины связан с четырьмя лигандами.

 Резонансные структуры HNO3
Резонансные структуры HNO3 Понятие координационного числа применяется и для характеристики центрального атома в молекулах, преимущественно для тех случаев, когда число химических связанных ближайших атомов не равно численному значению валентности. Например, в молекуле азотной кислоты формальная валентность центрального атома азота равна 4, степень окисления - +5, а координационое число - 3.
Понятие координационного числа применяется также при описании структуры жидкостей и аморфных тел. В этом случае координационное число — мера ближнего порядка, среднее число ближайших соседей атома. Оно может быть дробным.
Координационное число в кристаллографии
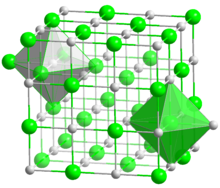
 Кристаллическая решётка NaCl (простая кубическая): показаны элементарные ячейки ионов натрия и хлора
Кристаллическая решётка NaCl (простая кубическая): показаны элементарные ячейки ионов натрия и хлора В кристаллохимии координационное число — характеристика, которая определяет число ближайших равноудаленных одинаковых частиц (ионов или атомов) в кристаллической решётке. Прямые линии, соединяющие центры ближайших атомов или ионов в кристалле, образуют координационный многогранник, в центре которого находится данный атом.
В решётках Браве для всех узлов координационное число одинаково. Число ближайших соседей отражает плотность упаковки вещества. Чем больше координационное число, тем больше плотность и соответственно свойства вещества ближе к металлическим. Данному параметру решетки соответствует первая, вторая (соседи, следующие за ближайшими), третья и т. д. координационные группы частиц.
Для простой кубической решетки координационное число равно шести, для ОЦК — 8, ГЦК и ГП (гексагональной плотноупакованной) — 12.
См. также
Источники
Примечания
biograf.academic.ru
Координационное число — WiKi
 Строение цис-дихлородиамминплатины (II)
Строение цис-дихлородиамминплатины (II) В химии понятие координационного числа появилось с развитием химии комплексных соединений. Под ним подразумевается число лигандов (атомов, молекул, ионов), которые образуют первую координационную (внутреннюю) сферу комплексообразователя[1].
Например, в комплексной соли гексацианоферрате(III) калия K3[Fe(CN)6] координационное число иона Fe3+ равно 6, а в цис-дихлородиамминплатине (II) (соли Пейроне) Pt(Nh4)2Cl2 центральный атом платины связан с четырьмя лигандами.
 Резонансные структуры HNO3
Резонансные структуры HNO3 Понятие координационного числа применяется и для характеристики центрального атома в молекулах, преимущественно для тех случаев, когда число химических связанных ближайших атомов не равно численному значению валентности. Например, в молекуле азотной кислоты формальная валентность центрального атома азота равна 4, степень окисления - +5, а координационое число - 3.
Понятие координационного числа применяется также при описании структуры жидкостей и аморфных тел. В этом случае координационное число — мера ближнего порядка, среднее число ближайших соседей атома. Оно может быть дробным.
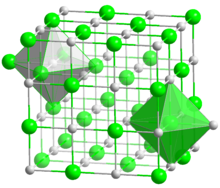 Кристаллическая решётка NaCl (простая кубическая): показаны элементарные ячейки ионов натрия и хлора
Кристаллическая решётка NaCl (простая кубическая): показаны элементарные ячейки ионов натрия и хлора В кристаллохимии координационное число — характеристика, которая определяет число ближайших равноудаленных одинаковых частиц (ионов или атомов) в кристаллической решётке. Прямые линии, соединяющие центры ближайших атомов или ионов в кристалле, образуют координационный многогранник, в центре которого находится данный атом.
В решётках Браве для всех узлов координационное число одинаково. Число ближайших соседей отражает плотность упаковки вещества. Чем больше координационное число, тем больше плотность и соответственно свойства вещества ближе к металлическим. Данному параметру решетки соответствует первая, вторая (соседи, следующие за ближайшими), третья и т. д. координационные группы частиц.
Для простой кубической решетки координационное число равно шести, для ОЦК — 8, ГЦК и ГП (гексагональной плотноупакованной) — 12.
ru-wiki.org
Комплексные соединения хрома. Методика синтеза соли Рейнеке — курсовая работа
Ярко выраженная способность трехвалентного хрома к образованию комплексных соединений особенно отчетливо проявляется в его различных комплексных продуктов присоединения аммиака.
В соответствии со своим КЧ 6 ион хрома (III) может координационно связать шесть молекул аммиака. При этом образуется комплексный ион [Cr(Nh4)6]3+, заряд которого совпадает с зарядом хрома, фигурирующего в качестве центрального атома, поскольку молекулы аммиака не заряжены.
Вследствие прочного связывания молекул аммиака при растворении в воде соединений, содержащих комплекс [Cr(Nh4)6]3+, не происходит моментального распада комплекса – он существует в растворе как ион и лишь постепенно происходит замещение аммиака молекулами воды.
[Cr(Nh4)6]3+ [Cr(h3O)2(Nh4)4]3+ [Cr(h3O)4(Nh4)2]3+ [Cr(h3O)6]3+
Исследования поведения гексаакваиона хрома (III) в растворах соляной кислоты во времени, позволили установить, что равновесие в системе Cr3+-h3O-Cl- 8 устанавливается примерно 3,5 месяца. Комплексообразование в этих растворах протекает последовательно по ступеням во времени:
[Cr(h3O)6]3+
Спектры поглощения растворов показывают, что даже в самом концентрированном относительно соляной кислоты растворе (12 н) комплексообразование заканчивается на третьей ступени.
Таким образом, реакция внедрения ионов хлора в координационную сферу комплекса протекает крайне медленно, инертными являются не только гексааквокомплекс, но и смешанные аквахлориды хрома (III) по отношению к реакции обмена молекул воды на хлорид-ионы, происходящего в процессе образования комплексов; инертность смешанных комплексов уменьшается с увеличением числа ионов хлора в координационной сфере комплекса.
Процессы акватации транс- и цис- дихлородиэтилендиамминхроми-хлорида:
[Cr(en)2Cl2]+ [Cr(en)2Cl(h3O)]2+ ]3++Cl-
Гидроксил может образоваться из молекулы воды, содержащейся во внутренней координационной сфере, в результате отщепления протона. Вероятность образования гидроксила во внутренней координационной сфере растет при повышении рН и уменьшается при понижении рН. Поэтому прибавление кислоты понижает вероятность образования гидроксила во внутренней координационной сфере и, следовательно замедляет процессы акватации именно тех ацидокомплексов, во внутренней координационной сфере которых содержится молекула воды. Если же во внутренней координационной сфере нет молекулы воды, то такого рода влияние величины рН исключается.
Достаточно широко исследовано влияние ионов Cr2+ на процессы акватации ацидохроми-комплексов. Оказалось, что ионы Cr2+ катализируют процессы акватации изученных ацидохроми-комплексов.
Например, каталитический процесс акватации транс-дихлородиаминхроми-хлорида протекает следующим образом. Вероятно, катализатор образует промежуточный комплекс, в котором связь между атомами Cr2+ и Cr3+ осуществляется через ион хлора:
транс-[CrIII(en)2Cl2]+ + [CrII(h3O)6]2+ [Cl(en)2CrIII,II – Cl – CrII,III(h3O)5]3+.
После передачи электрона может произойти распад комплекса. Наиболее вероятен распад по связи CrII – Cl:
[Cl(en)2CrII-Cl-CrIII(h3O)5]3+ → [Cl(en)2CrII(h3O)]+ + [ClCrIII(h3O)5]2+,
освободившееся координационное место у CrII заняла молекула воды.
Замена во внутренней сфере одних лигандов другими часто сопровождается отчетливым изменением окраски комплекса.
Ион [Cr(h3O)6]3+ поглощает свет в красной, голубой частях видимого спектра, а также в ближайшей ультрафиолетовой области, поэтому имеет фиолетовую окраску, вызванную наложением двух дополнительных цветов.
Известно много комплексных анионов состава [CrX6]3-, где Х – монодентатный лиганд типа F-, Cl-, NCS-, CN-, или часть полидентатного аниона типа оксалата (C2O42-). Существует, разумеется, множество смешанных ацидоамино- и и ацидоакво- комплексов.
Проведем некоторую их классификацию9:
1) [Cr(Nh4)6]3+, [Cr(Nh4)5(h3O)]3+, [Cr(Nh4)4(h3O)2]3+, [Cr(Nh4)3(h3O)3]3+, [Cr(Nh4)2(h3O)4]3+, [Cr(h3O)6]3+
2) [Cr(Nh4)5Cl]2+, [Cr(Nh4)4(h3O)Cl]2+, [Cr(Nh4)3(h3O)2Cl]2+, [Cr(Nh4)2(h3O)3Cl]2+, [Cr (h3O)5Cl]2+
3) [Cr(Nh4)4(SCN)2]+, [Cr(Nh4)3(h3O)(SCN)2]+, [Cr(Nh4)2(h3O)2(SCN)2]+, [Cr(h3O)4(SCN)2]+
4) [Cr(Nh4)3(OH)3], [Cr(Nh4)2(h3O)(OH)3], [Cr(h3O)3(OH)3]
5) [Cr(Nh4)2(SCN)4]-, [Cr(h3O)2(SCN)4]-
6) [Cr(h3O)(SCN)5]2-
7) [CrCl6]3-
Важно заметить, что во всех рядах отсутствуют моноамминные соединения, и отсутствуют только они, указывает на существование какой-то закономерности, проявляющейся в неспособности к существованию моноамминных соединений.
Большой интерес представляют соединения типа: [CrAm4R2]+ [CrAm2R4]-. Из соединений первого типа известны главным образом соединения этилендиамина. Они интересны ввиду наблюдающегося у них явления изомерии (стереоизомерии)10.
При октаэдрическом расположении комплексно связанных групп А и В вокруг центрального атома комплекс с общей формулой [ZA4B2] может существовать в двух формах (см. рис. 3)
В случае этилендиаминных соединений различие заключается еще и в том, что в противоположность транс-соединению цис-соединение представляет собой смесь двух оптически активных форм, поскольку, как видно из рис. 4, в этом случае могут существовать две цис-формы, относящиеся друг к другу, как предмет к его зеркальному отражению.
Переходя к рассмотрению второго типа соединений, нужно подчеркнуть, что поскольку в состав комплекса входят четыре отрицательных эквивалента, он представляет собой анион и образует соли с металлами. Хорошо известно соединение, принадлежащее к данному классу, так называемая соль Рейнеке Nh5[Cr(NCS)4(Nh4)2]×h3O, анион которой часто применяют для осаждения больших катионов, как органических, так и неорганических, соль Рейнеке удобно использовать для количественного определения меди, так как можно легко провести осаждение последней в форме Cu[Cr(NCS)4(Nh4)2], не удаляя из раствора другие металлы (кроме Ag, Hg, Tl). Реакция с солью Рейнеке может служить также и как очень чувствительная качественная проба на медь.
3.2 Соль Рейнеке.
3.2.1 Общие сведения.
Из тетрацидодиаминовых комплексов хрома (III) наиболее давно известным является соль эмпирического состава Cr(NCS)3×Nh5SCN×2Nh4×2h3O. Координационная формула этого соединения представляется в виде Nh5[Cr(NCS)4(Nh4)2]×h3O. Соль эта, следовательно, может быть рационально названа тетрароданодиамминхромиат аммония.
Однако как эту соль, так и другие, образующиеся из нее путем замены аммония на другие катионы, часто называют просто солями Рейнеке. Свободную кислоту Н[Cr(NCS)4(Nh4)2], которая может быть получена при взаимодействии Ba[Cr(NCS)4(Nh4)2]2 с разбавленной серной кислотой, также часто называют кислотой Рейнеке. В литературе даже встречается иногда и термин «рейнекат» («рейнекеат»), применяемый для обозначения солей Рейнеке.
Пространственное строение данной соли было выяснено с помощью рентгеноструктурного анализа.
Оказалось, что молекулы аммиака расположены в транс-положении друг к другу11. В этой же работе было также показано, что в анионе соли Рейнеке роданогруппа связана с хромом через атом азота.12
Получены также производные иона тетрароданодиамминхрома (III), содержащие вместо одной роданогруппы остаток ОН-, т.е. соли типа М[Cr(Nh4)2(NCS)3OH]. Также получены диоксалатодиамминхромиаты типа Me[CrPy2(NCS)4] и другие аналогичные соли.
3.2.2 Применение.
Как уже отмечалось, соль Рейнеке довольно широко применяется в аналитической химии, для определения ионов меди, серебра, ртути, кадмия и висмута образуя пучки тонких игл. На серебро, как правило, используют соль Рейнеке в сочетании с тиомочевинной, образуется осадок состава: [Ag(SCN2h5)2]×[Cr(Nh4)2(SCN)4], предел обнаружения 0,4 мкг, предел разбавления 1:2500 (г/г).
Также она применяется и в органическом анализе, например для определения никотина13, атропина14, морфина15:
Сведения о соединениях содержащих анион [Cr(Nh4)2(NCS)4]- достаточно ограничены, не смотря на то, что тетраизотиоцианатодиамминхроматные комплексы могут обладать рядом специфических свойств.
3.3 Многоядерные комплексы хрома (III)
Многоядерные амминные комплексы хрома (III) содержат несколько центральных атомов хрома. В большинстве случаев они связаны между собой ОН-группами.
Важнейшими представителями двухъядерных комплексов являются так называемые родо- и эритрохромовые соли и соли ди-μ-гидроксодихрома (III).
Магнитные моменты биядерных комплексов зависят от температуры, а их значения несколько ниже, чем обычные для октаэдрического CrIII, что указывает на слабое антиферромагнитное взаимодействие через изогнутые мостики Cr-O(H)-Cr. Более сильное антиферромагнитное взаимодействие обнаружено у [(Nh4)5Cr(μ-OH)Cr(Nh4)5]X5:
[(Nh4)5Cr(μ-OH)Cr(Nh4)5]5+ [(Nh4)5Cr-O-Cr(Nh4)5]4+
красный синий
Линейный мостик Cr-O-Cr, очевидно, допускает спаривание d-электронов двух атомов металла посредством dπ-pπ – связей намного легче, чем изогнутый мостик Cr-O(H)-Cr.
Гидролизованные полиядерные комплексы CrIII имеют большое значение в промышленном получении красителей и дубильных веществ. В первом случае они служат протравкой для красителя. В производстве кожи необходимо обрабатывать шкуры животных для предотвращения гниения, чтобы они были мягкими после высушивания. После вымачивания в серной кислоте шкуры насыщают раствором, содержащим CrIII. Раствор постепенно делают щелочным, при этом образуются полиядерные комплексы и связывают мостиками соседние цепочки белков, в основном координируясь к их карбоксильным группам.
3.4 Электронное строение комплексов хрома (III).
Магнитные свойства октаэдрических комплексов хрома (III) можно объяснить довольно просто. Во всех таких комплексах должно быть три неспаренных электрона независимо от силы поля лигандов, что подтверждается на опыте для всех известных одноядерных соединений. Далее, теория предсказывает, что значения магнитных моментов должны приближаться или быть несколько ниже чисто спинового значения. Это также подтверждается данными эксперимента.
turboreferat.ru
Вольфрам, координационные числа - Справочник химика 21
Для положительно четырехвалентных Р1, Рс1, 1г, Т1, РЬ, 5г и 81 наиболее характерно координационное число 6. Молибден и вольфрам могут образовывать комплексы с координационным числом 8. [c.224]Наличие свободных электронов обуславливает хорошую электро- и теплопроводность металлов, их непрозрачность, блеск, ковкость. Металлические свойства проявляют элементы, легко отдающие электроны —в частности, элементы первых двух групп периодической системы. С увеличением числа валентных электронов межатомные взаимодействия приобретают ковалентный характер. Кристаллическая структура металлов часто является плотноупакованной, с координационным числом 12 (гранецентрированная кубическая решетка для Си, Ад, РЬ, гексагональная — для 2п и M.g). Некоторые металлы (щелочноземельные, вольфрам) кристаллизуются в объемноцентрированной кубической структуре. [c.177]
Подобно другим -элементам, хром, молибден и вольфрам склонны образовывать разнообразные комплексные соединения с координационными числами 4 и 6. [c.416]Изо- и гетерополисоединения Ш(У1) и Мо(У1) — комплексные многоосновные кислоты и их соли, в которых вольфрам и молибден входят в комплексный анион. Изополисоединения частично рассмотрены ранее. Они содержат в анионной части кроме вольфрама (молибдена) только кислород и водород. Гетерополисоединения содержат еще один или два элемента, являющихся комплексообразователями (табл. 45). В нормальных вольфраматах и молибдатах Ш и Мо имеют по кислороду координационное число 4 и содержат тетраэдрические группы Я04(Я—Ш, Мо). В полисоединениях координационное их число 6, соответственно этому в них содержатся октаэдрические группировки КО в, Пространственно расположенные вокруг тетраэдра, в центре [c.241]
VI6 группа (Сг, Мо, W). Плавление не изменяет электронного состояния этих металлов, о чем свидетельствуют чрезвычайно высокие седьмые потенциалы ионизации (131—161 эв), поэтому сохраняется заряд ионов (6-Ь), конфигурация их внешних оболочек (р ) и электронная концентрация (6 ЭЛ атом). Вследствие этого жидкий хром, молибден и вольфрам должны иметь ближний порядок, отвечающий их ОЦК структурам, т. е. координационное число, близкое к восьми, сходное расположение атомов и почти такие же межатомные расстояния, как и перед плавлением. Нормальные значения энтропии плавления хрома, молибдена и вольфрама (см. рис. 108) подтверждают сохранение ими ближнего порядка при плавлении. [c.254]
Вольфрам, как и молибден, дает комплексный цианид с координационным числом восемь K4[W( N)g]-21420, переходящий под действием окислителей в K3[W( N)8). [c.650]
Известно до 35 типов гетерополисоединений с различными центральными атомами. Первоначальная точка зрения на структуру этого типа соединений (Розенгейма и, Миолатти) основывалась только на данных химических анализов и умозрительных построениях, согласно которым центральный атом имел координационное число 6, а вольфрам и молибден входили во вторую координационную сферу в виде групп К 2О, или Я04. Кеггин и Полинг на основе данных рентгеноструктурного анализа ввели кристаллохимические представления и построили пространственные структуры гетерополикомплексов. Кеггин построил схему на примере фосфорно-вольфрамовой кислоты, для аниона которой он дал формулу [Р(Ш 3010)4] . Фосфор находится в центральном тетраэдре и имеет координационное число 4. Вольфрам образует октаэдрические лиганды— группировки ШзОю- Наличие групп НзО о, видимо, нельзя считать вполне доказанным. Безусловной является и для вольфрама и для молибдена октаэдрическая координация атомов кислорода вокруг этих элементов с координационным числом 6. Вот не- [c.242]
Аналогично кислородным соединениям ведут себя и галогениды элементов 6-й группы набор галогенидов хрома, приведенный в разд. 28.2, значительно беднее высшими формами, чем семейства галогенидов молибдена и вольфрама, среди которых присутствуют гексагалогениды МоРе, УРе, УС1в и УВГб, не имеющие аналогов у хрома. В то же время молибден и вольфрам, так же как и хром, образуют много низших галогенидов состава МХз и МХд, однако они резко различаются структурно атомы молибдена и вольфрама в них имеют более высокие координационные числа, чем индекс при галогене, и образуют связи металл - металл. Такие соединения, называемые кластерами, более подробно рассматриваются в следующем разделе. [c.368]
Вольфрам — мономорфный металл с о. ц. к. решеткой. Энергия крис таллической решетки 905 мкДж/кмоль. Координационное число 8. Пе риод кристаллической решетки в зависимости от чистоты вольфрама 0,31648- 0,31651 нм при 293 К при 4,2 К составляет 0,3161 нм. Известна метастабильная фаза р, получаемая восстановлением УОз водородом при 500 °С и отвечающая составу Уц 2оО. Температура иеобра тимого превращения р- а составляет 520 °С. [c.399]
У. Вольфрам, повидимому, диморфен. Известны две структуры а и обе кубические. aW ЗВ А2, тип (С с)- отпосится в ЗВ к типу А 15. Он является переходным от кубической 1 ранецептрированной с координационным числом 12 к кубической центрированной с координационным числом 8 + 6 = 14. В решётке имеется два положения атомов . В положении I к. ч. атомов У = 12, причём каждый атом 1 окружён 12 атомами II, на расстоянии е = 2,82 А, образуюш,имп конфигурацию кристаллохимического икосаэдра (см. рис. 441а). [c.295]
Близкое строение имеют кристаллы изоструктурных A i [WU40H], где А = Рг, Nd, Ей и Gd [262, 276]. Здесь тетраэдр WO4 точно так же превращен в искаженную бипирамиду пятой (несколько удлиненной) связью W—ОН, а атомы РЗЭ имеют координационное число 8 [276]. Разница заключается в отсутствии у полиэдров РЗЭ кислородных вершин, не входящих в состав вольфрам-кислиродных полиэдров. [c.56]
Таким образом, выявляется еще один аспект стереохимического различия между молибденом и вольфрамом, с одной стороны, и рением и осмием, с другой. Молибден и вольфрам образуют и октаэдрические моно-, ди- и триоксокомплексы, и тетраэдрические три- и тетраоксокомплексы при одной и той же (высшей) степени окисления. Возможно, что именно в связь с этим фактом следует поставить характерную для этих металлов склонность к промежуточному координационному числу пять и к имитации тетраэдра в рамках пяти- и шестикоординационных комплексов. С другой стороны, рений и осмий образуют тетраэдрические тетраоксо-комнлексы главным образом при конфигурации а октаэдрические диоксокомплексы — при конфигурации без каких-либо признаков тетраэдрического искажения полиэдра. [c.166]
В литературе высказывалось мнение, что истинные карбонилы образуют лишь некоторые элементы (никель, железо, кобальт, рений, хром, молибден, вольфрам, часть платиновых металлов). При этом предполагалось наличие у карбонилов так называемых типич1ных карбонильных овойств. К их числу относили высокую летучесть, растворимость в индиферентных органичеоких растворителях, термическую диссоциацию на металл и окись углерода, комплексное строение. Ряд исследователей считает, что летучие карбонилы могут образовывать только элементы с 5-валентными электронами. Но карбонил углерода обладает всеми типичными карбонильными свойствами. Он летуч, разлагается на углерод и окись углерода, растворяется только в органических растворителях, имеет координационные связи (комплексное строение), и в то же время его центральный атом обладает -5- и р- валентными электронами. [c.12]
chem21.info
1 Понятие координационного соединения
СодержаниеВведение
1.1. Понятие координационного соединения
1.2. Состав комплексных соединений
1.3. Классификация координационных соединений
1.4. Пространственное строение и изомерия комплексных соединений
2. Координационные соединения хрома
3. Заключение
Введение
Обширную группу химических соединений составляют координационные соединения, или комплексы, являющиеся продуктом сочетания отдельных способных к самостоятельному существованию простых соединений. В молекулах координационных соединений всегда можно выделить центральный атом или ион, вокруг которого сгруппированы другие ионы или молекулярные группы.
Координационные соединения имеют исключительно большое значение в живой и неживой природе. Достаточно сказать, что гемоглобин, благодаря которому осуществляется перенос кислорода из легких к клеткам ткани, является комплексом железа, а хлорофилл, ответственный за фотосинтез в растениях, — комплексом магния. Значительную часть природных минералов, в том числе многие силикаты и полиметаллические руды, также составляют координационные соединения. Более того, химические методы извлечения металлов из руд, в частности А1, Си, W, Au, Pt, Fe, связаны с образованием легкорастворимых, легкоплавких или высоколетучих комплексов. Современная химическая промышленность широко использует координационные соединения как катализатор ы (синтез высокополимерных материалов, производство кислот, химическая переработка нефти).
С использованием координационных соединений связана возможность получения многообразных лаков и красок, прочных электрохимических покрытий, фотоматериалов, надежных средств переработки и консервирования пищи.
1.1. Понятие координационного соединения
Координационные соединения это соединения содержащие группу ионов или нейтральных молекул (лигандов), в размещенных определенном порядке (координированных) вокруг атома (иона) – комплексообразователя.
Система комплексообразователь–лиганды образует внутреннюю координационную сферу, которую обычно отделяют квадратными скобками от внешней координационной сферы: K4[Fe(CN)6], [Cr(Nh4)6]Cl3, [PtCl2(Nh4)2], [Cr(CO)6].
Формула координационного иона или молекулы записывается, как правило, слева направо: центральный атом (ион), анионные, затем нейтральные лиганды с указанием их числа в виде правого нижнего индекса: [MLmXn]q.
Координационные соединения бывают катионные [Cr(Nh4)]Cl3, анионные K4[Fe(CN)6], катион-анионные [Cr(Nh4)6] [Fe(CN)6] и нейтральные [PtCl2(Nh4)2].
Координационного соединения называют следующим образом:
- анион, употребляется в именительном падеже,
- далее катион, употребляется в родительном падеже.
Как показывает само название, комплексные соединения — химически сложные и, как правило, состоят из трех или большего числа разнородных элементов. Однако сложность состава не единственная специфическая особенность комплексов. В комплексных соединениях помимо обычных типов связи, действует особая связь, получившая название координационной. В результате проявления этой связи возникает возможность образования прочного соединения из двух других, также устойчивых и, более того, имеющих насыщенную в обычном понимании валентность. Примером может служить образование стабильного продукта CoCl3·6Nh4 при взаимодействии хлорида Со3+ и аммиака. В молекуле аммиака Nh4 атом азота (электронная структура Is2 2s22р1х2р1у 2p1z) имеет максимальную валентность по водороду, соответствующую использованию всех неспаренных электронов 2рх, 2ру и 2рг для образования пар с электронами водородных атомов. Пользуясь диаграммой Льюиса, структуру аммиака выражают формулой [7]

в которой точками изображены электроны, первоначально принадлежавшие атому азота, а крестиками — электроны, принадлежавшие атомам водорода.
Проявление координационной связи является причиной образования комплексных ионов в растворах и расплавах.
Координационная связь, обуславливающая появление комплексных соединений, в ряде случаев весьма прочная, это создает известные трудности при осуществлении химических превращений. Хотя комплексные соединения известны химикам уже более двух столетий, причина их образования долгое время оставалась загадкой. Современное понимание природы комплексов стало возможным благодаря исследованиям швейцарского ученого А. Вернера, который в 1893 г. предложил теорию, вошедшую в химии под названием координационной теории Вернера. Основные положения этой теории таковы:
1. Атомы большинства химических элементов имеют два типа валентности — главную и побочную.
Главная валентность соответствует обычной валентности элемента, проявляемой в результате взаимодействия отдельных атомов или радикалов. Побочная валентность — это дополнительная валентность, обусловливающая взаимное сочетание отдельных, способных к самостоятельному существованию молекул.
- Атомы каждого элемента стремятся насытить как главную, так и побочную валентности.
- Химическое сродство, проявляющееся в виде главной и побочной валентностей, действует по всем направлениям в пространстве, в результате чего каждый атом стремится окружить себя другими атомами или атомными группами. Это явление Вернер назвал координацией, а число атомов или трупп, непосредственно присоединенных к центральному атому, — его координационным числом. При этом несущественно, присоединены ли соответствующие атомы или атомные группы главной или побочной валентностями.

Эффективность координационной теории удобно иллюстрировать на примере комплексных соединений, образуемых треххлористым хромом с аммиаком [7]. Удалось синтезировать только четыре таких соединения, состав которых представлен в таблице. Наиболее примечательно сопоставление их физико-химических свойств. При взаимодействии СгС1з·6NН3 с нитратом серебра происходит немедленное осаждение всех ионов С1- в виде AgCl. Тот же опыт с солью CrCl3·5Nh4 приводит к быстрому осаждению лишь двух ионов С1- из трех, присутствующих в молекуле. Для комплексов, содержащих 4 и 3 молекулы Nh4, способность к осаждению хлора уменьшается, так что у CrCl3·3Nh4 она полностью отсутствует.
На основании этих наблюдений можно заключить, что в различных соединениях треххлористого хрома с аммиаком характер связи С1- в молекуле комплекса неодинаков. Более того, молярная проводимость растворов этих солей резко различна и уменьшается по мере перехода от CrCl3·6Nh4 к CrCl3·3Nh4, так что для последнего комплекса она близка к нулю. Учитывая, что проводимость водных растворов солей обусловлена их электролитической диссоциацией, можно ожидать, что у рассматриваемых аммиакатов способность к диссоциации падает с уменьшением содержания Nh4 и почти отсутствует у CrCl3·3Nh4. Дополнительную полезную информацию о характере связи в молекулах CrCl3·nNh4 удалось получить на основании криоскопических измерений. Например, понижение точки замерзания водного раствора CrCl3·6Nh4 указывает на то, что из 1 моль соли в растворе образуются 4 моль частиц, тогда как из 1 моль соли CrCl3·3Nh4 образуется только 1 моль частиц.
Указанные явления превосходно объясняются в рамках координационной теории Вернера. В соответствии с этой теорией центральное место в молекуле комплексного соединения занимает как правило положительно заряженный ион, его называют комплексообразователем. Рядом с комплексообразователем расположено несколько противоположно заряженных ионов или электронейтральных молекул, которые называются аддендами и образуют у соединения внутреннюю координационную сферу. Остальные ионы, которые не размещаются во внутренней сфере, находятся от центрального иона на более отдаленном расстоянии и составляют внешнюю координационную сферу.
В соответствии с этой теорией ион Сг3+, как и любой другой, проявляет два типа валентности — главную и побочную. Первая из них, судя по степени окисления, равна трем, а вторая, исходя из состава наиболее богатого аммиаком комплекса, равна шести.
Число атомов или групп, непосредственно присоединенных к центральному атому называется координационным числом комплексообразователя. В комплексных соединениях координационное число играет важную роль и является таким же основным его свойством, как и валентность. Величина координационного числа определяется главным образом размерами, зарядом и строением электронной оболочки комплексообразователя. Наиболее часто встречается координационное число шесть, например: у железа, хрома, цинка, никеля, кобальта, четырехвалентной платины; координационное число четыре свойственно двухвалентной меди, трехвалентному золоту, двухвалентной ртути, кадмию. Встречаются иногда и другие координационные числа, но значительно реже (например, два для серебра и одновалентной меди).
Связанные побочной валентностью молекулы аммиака непосредственно группируются вокруг иона Сг3+, образуя вместе с ним внутреннюю координационную сферу, тогда как ионы С1- находятся дальше от металлического иона и не связаны с ним столь прочно. По Вернеру, состав молекулы CrCl3·6Nh4 можно представить формулой

в предположении, что главная связь изображается пунктиром, а побочная — сплошной линией [7]. Все главные связи в молекуле CrCl3·6Nh4 насыщены хлор-ионами, а побочные — молекулами Nh4. Учитывая относительную прочность этих связей, можно ожидать, что при растворении в воде из одной молекулы CrCl3·6Nh4 образуются четыре частицы: [Сг(МН3)6]3+ и 3 иона С1-.
При удалении из CrCl3·6Nh4 одной молекулы Nh4 должна «обнажаться» одна побочная связь, но, учитывая, что, по Вернеру, каждый элемент стремится насытить все свои валентности, резонно допустить, что «обнажившаяся» валентность будет использована на связь с одним из ионов С1-, иначе говоря, этот ион должен одновременно насыщать оба типа валентности. Очевидно, что в этом случае один из ионов С1- переходит в координационную сферу, и теряет способность легко отрываться от иона Сг3+ при растворении аммиакатов в воде. Именно этим объясняется снижение проводимости при переходе от гекса- к пентааммиакату, уменьшающему до трех число частиц, образуемых при диссоциации (два иона С1- и [Cr(Nh4)5Cl]2+ и невозможность осаждения всего хлора при взаимодействии с AgN03.
Свойства CrCl3·4Nh4 и CrCl3·3Nh4 хорошо объясняются формулами [7].


У последней из них все ионы С1-, одновременно насыщающие главную и побочную валентности, теряют способность реагировать с AgNО3 и отщепляться от молекулы CrCl3·3Nh4 при растворении в воде.
Аналогичным образом может быть установлен характер связи между составными частями любого комплексного соединения. Очевидно, что в каждом из них можно выделить атом или ион, являющийся центральным, или комплексообразователем.
1.2. Состав комплексных соединений
Атомы или ионы, расположенные непосредственно вокруг комплексообразователя и связанные с ним за счет проявления дополнительной валентности, называются лигандами. В качестве лигандов могут выступать различные электроположительные, электроотрицательные и нейтральные частицы. Лиганды, подобные оксалат-иону, называются полидентатными (от англ. слова dentate, что означает зубчатый). Заряд комплексного иона легко подсчитать, зная валентность его составных частей. Совершенно аналогичным образом можно подсчитать заряд иона-комплексообразователя, если известен заряд комплексного иона и лигандов.
Ионы или нейтральные части комплекса, не являющиеся лигандами или комплексообразователем, составляют внешнюю сферу комплексов. Состав рассматривавшихся выше аммиачных комплексов треххлористого хрома следует выразить формулами:
гексаамминкобальт (III) хлорид [Cr(Nh4)6]Cl3,
хлоропентаамминкобальт (III) хлорид [Cr(Nh4)5Cl]Cl2,
днхлоротетраамминкобальт (III) хлорид [Cr(Nh4)4Cl2]Cl,
трихлоротриамминкобальт (III) [Cr(Nh4)3C13].
У последнего соединения внешняя сфера комплекса отсутствует.
Важнейшей характеристикой любого комплексного соединения является координационное число, показывающее число лигандов. Октаэдрическое строение комплексов с координационным числом, равным 6, не очевидно и нуждается в доказательствах, которые могут быть получены различными методами. Среди них наибольшую популярность получил метод, основанный на синтезе изомеров, т е. комплексных соединений одинакового состава, обладающих различным строением. Например, для комплексного иона [Сг(Nh4)4Cl2]+ с октаэдрическим расположением лигандов возможно образование двух изомеров. В первом из них (цисизомер) атомы О расположены по одну сторону от атома Сг, а во втором (трансизомер) атомы хлора находятся по обе стороны от центрального атома [6].



Число изомеров может свидетельствовать о геометрической форме комплекса. Симметричное расположение шести лигандов на равном расстоянии от центрального атома можно представить не только в вершинах октаэдра, но также плоского равностороннего шестиугольника и тригональной призмы.
1.3. Классификация координационных соединений
Исключительное многообразие комплексных соединений затрудняет любую попытку их классификации. Как уже отмечалось выше, в роли комплексообразователя может выступать любой химический элемент, однако наиболее распространены металлические комплексы. Последние иногда делят на две группы:
- вернеровские комплексы,
- карбонилы металлов и металлоорганические соединения (например, K[Pt(C2H5)Cl3]).
По составу координационной сферы можно выделить несколько наиболее распространенных классов вернеровских комплексов:
- Аквокомплексы типа [Сг(Н2О)6]С13 (лиганды — нейтральные молекулы воды).
- Аммиакаты типа [Ag(Nh4)2]Cl (лиганды — молекулы аммиака).
- Ацидокомплексы типа K3[A1F6] или K[A1(SО4)2] (лиганды— кислотные остатки кислородных или бескислородных кислот).
- Гидрооксосоли типа Na[Zn(OH)3] (лиганды — гидроксиль-ные группы).
- Полигалогениды типа Те13 или Sb[ICl4].
- Изо- и гетерополикислоты и их производные.
- Формально изополикислоты можно рассматривать как продукт взаимодействия кислоты с ее же ангидридом, например:
- Н2СО4-СгО3 = Н2Сг2О7 = Н2[СrO4(СгО3)] — двухромовая кислота, Н2СгО4
- 2СгО3 = Н2Сг3О10 = Н2[СrO 4(СгО3)2] — трихромовая кислота,
- Н2СгО4 • ЗСгО3 = Н2Сг 4О13 = НСгО4(СгО3)3] — тетрахромовая кислота.
1.4. Пространственное строение и изомерия комплексных соединений
Комплексным соединениям, так же как и в органической химии, характерно явление изомерии. Изомерия - свойство веществ образовывать несколько соединений одинаковых по составу, отличием у которых является взаимное расположение атомов в молекуле, этим объясняется различие свойств.
Изомерия комплексных соединений обусловлена:
- разницей в строении и координации лигандов
- разницей в строении внутренней координационной сферы
- разным распределением частиц между внутренней и внешней сферой.
Изомерия комплексных соединений подразделяется на геометрическую, оптическую, сольватную (или гидратную) и ионную.
Сольватная изомерия это различное распределение молекул растворителя между внутренней и внешней сферами комплексного соединения, а также различный характер химической связи молекул воды с комплексообразователем.
Для комплексных соединений хрома этот тип изомерии представлен существованием трех изомерных гидратов хлорида хрома(III) с общей формулой CrCl3 . 6 h3O.
Первый изомер, [Cr(h3O)6]Cl3 – хлорид гексааквахрома(III) – кристаллическое вещество имеющее серо-сиреневый цвет, раствор их в воде имеет фиолетовый цвет. Окраску раствору придают катионы [Cr(h3O)6]3+. Под действием ионов Ag+ проходит осаждение всех трех хлорид-анионов:
[Cr(h3O)6]Cl3 + 3 AgNO3 = [Cr(h3O)6](NO3)3 + 3 AgCl
Другой изомер – [Cr(h3O)5Cl]Cl2 . h3O, моногидрат хлорида хлоропента-аквахрома(III). Водный раствор его имеет голубовато-зеленое окрашивание, а под действием ионов Ag+ осаждаются только два хлорид-иона:
[Cr(h3O)5Cl]Cl2 + 2 AgNO3 = [Cr(h3O)5Cl](NO3)2 + 2 AgCl
Третий изомер – [Cr(h3O)4Cl2]Cl . 2 h3O, дигидрат хлорида дихлоротетра-аквахрома(III). Водный раствор имеет темно-зеленый цвет, а ионы Ag+ осаждают из раствора только один хлорид-ион:
AgNO3 + [Cr(h3O)4Cl2]Cl = AgCl + [Cr(h3O)4Cl2]NO3
При высушивании двух последних изомеров теряется внешнесферная вода. Возможен постепенный взаимный переход изомеров, при условии изменения pH или температуры раствора. При добавлении избытка кислоты и охлаждении происходит образование первого изомера, а при нагревании – переход ко второму и третьему изомеру.
Ионизационная изомерия обусловлена разным распределением ионов между внешними и внутренними сферами комплексных соединений и, в результате этого, различный характер диссоциации на ионы.
Координационная изомерия – обусловлена различным распределением лигандов во внутренних координационных сферах. А также разница во взаимодействии с AgNO3 . Комплексные соединения хрома имеют два изомера – [Co(Nh4)6]∙[Cr(CN)6] и [Cr(Nh4)6]∙[Co(CN)6]. Первый образует осадок Ag3[Cr(CN)6], а второй – осадок Ag3[Co(CN)6].
Геометрическая изомерия или цис-транс изомерия обусловлена различным пространственным расположением лигандов вокруг центрального атома.
Оптическая изомерия объясняет способность вращать плоскость поляризации плоскополяризованного света. Изомеры отличаются друг от друга направлением вращения плоскости поляризации: один называется правым, второй – левым изомером. Правые и левые изомеры зеркальные изображения друг друга, они не могут быть совмещены в пространстве
2. Координационные соединения хрома
Для хрома, например, известен следующий ряд неорганических комплексных соединений:
[Cr(Nh4)6]CI3: [Cr (Nh4)5h3О] Cl3; [Cr(NH,)4(h3О)2]Cl3;
[Cr(Nh4)3(h3О)3]Cl3; [Cr (NH,)2(h3О)4]Cl3; [Cr (h3О)6]Cl3
Последнее соединение этого ряда является не чем иным, как обыкновенным кристаллогидратом хлорного хрома СгС13 • 6Н2О. Следовательно, кристаллогидрат хлорного хрома по существу есть комплексное соединение, отщепляющее в растворе ионы [Сг (Н20)6]3+. Кристаллогидраты, содержащие шесть молекул воды, встречаются очень часто. К ним относятся, например, кристаллогидраты хлорного железа FeCl3, хлористого никеля NiCl2, хлористого алюминия А1С13 и др. Согласно координационной теории, все они имеют строение, аналогичное строению кристаллогидрата хлорного хрома:
[Fe (Н2О)6] Cl3; [Ni (Н2О)6] С12; [А1 (Н2О)6] С13
Комплексные соединения хрома широко используются в фотографии. При проявлении используется цветная качественная реакция на трехвалентное железо (для позитивного изображения) или на двухвалентное (для негатива). При позитивной печати протекает следующая реакция:
(Nh5)3[Fe(C2O4)3] + K4[Fe(CN)6] → KFe[Fe(CN)6] (или Fe4[Fe(CN)6]3)↓ + 3/2(Nh5)2C2O4 + 3/2K2C2O4.
Осадок образующийся в ходе реакции ферроцианид железа-калия окрашен в синий цвет. При проявлении и закреплении изображения используется фотохимическое восстановление бихромата, которое можно выразить следующей схемой:
Cr2O72- + 14H+ + h3O + 2L + hν → 2[Cr+3(h3O)4(L)2],
где L - это донорная группа (лиганд) различных полимеров. Лигандами в них выступают, например, гидроксильные и карбоксильные группы в природных полисахаридах и полипептидах. Трехвалентный хром восстанавливаясь связывает боковые функциональные группы соседних полимерных молекул, фактически «сшивая» их. В результате происходит ухудшение растворимости полимера. Часто этот процесс называют дублением, подразумевая, что помимо ухудшения растворимости, полимер становится тверже. Бихроматный процесс в технике использует, рельеф, возникающий после проявления. Этот рельеф в сочетании с последующей гальванопластикой может быть использован для офсетной печати, литографии. Шелкография это характерное применение бихроматного процесса. В качестве полимера используют поливиниловый спирт (- CHOH - Ch3-)n.
Cr2O72- + 14H+ + h3O + 2(- CHOH - Ch3-)n + hν → 2[Cr+3(h3O)4((- CHOH - Ch3-)n)2].
Хроморганические соединения это соединения содержащие связь Сr — С. Их можно разделить по типу органического лиганда и характеру соединения его связи с металлом на:
с s-связью Сr — С,
изонитрильные,
карбеновые
карбиновые комплексы,
а также p-комплексы.
Наибольший интерес представляют соединения с 5-, 6- и 7-членными лигандами. Также известны несколько би- и полиядерных комплексов с ареновыми и циклопентадиенильными лигандами.
Хром в хроморганических соединениях может находиться в степенях окисления 0, +1, +2, +3, +4.
Они получаются на основе гексакарбонила хрома [Сr(СО)6] и карбонильных комплексов с лигандами n -и p-типом.
Хроморганические соединения содержащие  связь - гетеролиганды и гомолигандны. Гомолигандные соединения такие как, R3Cr, R4Cr неустойчивы.
связь - гетеролиганды и гомолигандны. Гомолигандные соединения такие как, R3Cr, R4Cr неустойчивы.
Анионные комплексы, типа M3[CrR6], M[CrR3], K3[Cr(CO)3(C2R)3], где M - щелочной металл, R - алкенил, арил. Наиболее важные производные Сг(III) типа [CrR3L3,] (где L, например, ТГФ).
 Арильные комплексы Сr(III) при отсутствии стабилизирующих лигандов претерпевают гомолиз связи Сr — С и
Арильные комплексы Сr(III) при отсутствии стабилизирующих лигандов претерпевают гомолиз связи Сr — С и перегруппировку с образованием бисареновых
перегруппировку с образованием бисареновых комплексов Сг(0). Получают [CrR3(TГФ)3] путем взаимодействия СrСl3 с RMgX в растворе ТГФ. При использовании RM (М -щелочные металлы) образуются анионные комплексы.
комплексов Сг(0). Получают [CrR3(TГФ)3] путем взаимодействия СrСl3 с RMgX в растворе ТГФ. При использовании RM (М -щелочные металлы) образуются анионные комплексы.
Изонитрильные комплексы Сr могут быть гомолигандными [Cr(CNR)6] и гетеролигандными: [Cr(CO)n(CNR)6-n], [Cr(CO)2(CNR)(apeн)]. Получаются они путем замещения СО в карбонилах хрома, а также при восстановлении соединений хрома высшей степени окисления в присутствии избытка изонитрила.
Карбеновые комплексы имеют общие формулы типа - [Сr(СО)5{ = = C(R)(X)}], [Cr(CO)2(C6H6){=C(R)(X)}], гдe X = OR-, SR-, NR-R-2.
Карбеновым комплексам характерна реакция нуклеофильного замещения у карбенового атома углерода. Типична реакция присоединения карбена к активированным олефинам или ацетиленам.

Карбеновые комплексы получаются в результате взаимодействия карбонилов хрома с литийорганическими соединениями.

Карбиновые комплексы хрома:
- нейтральные [Сr(СО)4( CR)X]
CR)X]
- катионные [Сr(СО)5( CR)]X.
CR)]X.
Карбиновые комплексы хрома с нуклеофилами образуют карбеновые комплексы: 
Получение карбиновых комплексов хрома возможно из карбеновых комплексов 
Олефиновые комплексы Сr, в основном, гетеролигандны. Хром также образует комплексы с циклическими полиолефинами: норборнадиеном, циклогептатриеном, циклооктадиеном и циклооктатетраеном. Их получают путем замещения карбонильного лиганда или соконденсацией паров Сr и олефина в глубоком вакууме.
комплексы Сr, в основном, гетеролигандны. Хром также образует комплексы с циклическими полиолефинами: норборнадиеном, циклогептатриеном, циклооктадиеном и циклооктатетраеном. Их получают путем замещения карбонильного лиганда или соконденсацией паров Сr и олефина в глубоком вакууме.
Ацетиленовые комплексы хрома весьма немногочисленны.
комплексы хрома весьма немногочисленны.
Основные типы - [Cr(CO)(NO)(C2h3)( -C5H5)], [Cr(CO)2(C2R2)(C6H6)]. Они получаются в результате реакции обмена лигандов, восстановлением солей хрома в присутствии ацетилена.
-C5H5)], [Cr(CO)2(C2R2)(C6H6)]. Они получаются в результате реакции обмена лигандов, восстановлением солей хрома в присутствии ацетилена.
Из -аллильных комплексов хрома наибольшее распространение имеют соединения с обобщенной формулой [Сr(
-аллильных комплексов хрома наибольшее распространение имеют соединения с обобщенной формулой [Сr( -аллил)3]. При термолизе и ультрофиолетовом облучении они превращаются в [Сr2(
-аллил)3]. При термолизе и ультрофиолетовом облучении они превращаются в [Сr2( -аллил)4].
-аллил)4].
С окисью углерода они образуют соединения типа [Сr(СО)( -аллил)2] или [Сr(СО)6].
-аллил)2] или [Сr(СО)6].
С йодом - [Сr( -аллил)2Х]2.
-аллил)2Х]2.
Получают [Сr( -аллил)3] из аллилмагнийхлорида и СrС13. Из циклопентадиенильных комплексов Сr наиболее тщательно изучены
-аллил)3] из аллилмагнийхлорида и СrС13. Из циклопентадиенильных комплексов Сr наиболее тщательно изучены и
и
Известны также

 и
и (X - галоген, L - Ph4P и др.).
(X - галоген, L - Ph4P и др.).
Димер - диамагнитен. При мягких условиях он претерпевает обратимый гомолиз связи Сr — Сr и образует парамагнетик - мономер
- диамагнитен. При мягких условиях он претерпевает обратимый гомолиз связи Сr — Сr и образует парамагнетик - мономер
при нагревании в толуоле димер декарбонилируется до [Сr2(СО)4( -С5Н5)2].
-С5Н5)2].
С Но образует [Сr(СО)3( -С5Н5)], с амальгамой Na - Na[Cr(CO)3(
-С5Н5)], с амальгамой Na - Na[Cr(CO)3( -C5H5)] (последний с RX дает [Cr(R)(CO)3(
-C5H5)] (последний с RX дает [Cr(R)(CO)3( -C5H5)]).
-C5H5)]).
Получение [Сr(СО)3( -С5Н5)]2 осуществляют из [Сr(СО)6] и дициклопентадиена или циклопентадиенида Na. Кроме того, получают из СО и хромоцена [Cr(CO)2(NO)(
-С5Н5)]2 осуществляют из [Сr(СО)6] и дициклопентадиена или циклопентадиенида Na. Кроме того, получают из СО и хромоцена [Cr(CO)2(NO)( -C5H5)] из [Сr(СО)3(
-C5H5)] из [Сr(СО)3( -С5Н5)]- и NOC1 или фотолизом [Сr(СО)n(
-С5Н5)]- и NOC1 или фотолизом [Сr(СО)n( -С5Н5)]2(п = 2, 3) в присутствии NO.
-С5Н5)]2(п = 2, 3) в присутствии NO.
При взаимодействии галогенидов Сr(2) или Сr(3) с циклопентадиенидом натрия или Сr(СО)6 с циклопентадиеном образуется парамагнетик хромоцен [Сr( -С5Н5)2] , который в свою очередь обратимо окисляется до катиона [Сr(
-С5Н5)2] , который в свою очередь обратимо окисляется до катиона [Сr( -С5Н5)2]+ и обратимо восстанавливается до аниона [Сr(
-С5Н5)2]+ и обратимо восстанавливается до аниона [Сr( -С5Н5)2]- .
-С5Н5)2]- .
С хлористым железом(2) образуется ферроцен, а с СО, НХ, СС13, S - продукты замещения одного С5Н5-лиганда.
Хром также образует комплексы с ароматическими соединениями. Глубоко изучены [Сr(СО)3(арен)]. Для этих соединений характерны реакции обмена лигандов:
комплексы с ароматическими соединениями. Глубоко изучены [Сr(СО)3(арен)]. Для этих соединений характерны реакции обмена лигандов:
- при УФ облучении замещается одна группа СО на RNh3, RNC, RCN, олефин, ацетилен;
- при взаимодействии с аминами, фосфинами замещается ареновый лиганд и образуются комплексы имеющие формулу [Сr(СО)3L3] (L = Nh4, C5H5N, PR3, P(OR)3];
- би- и тридентантные лиганды при 160-220 °С образуют продукты замещения и аренового и карбонильных лигандов, вида [Cr(bipy)3].
Реакции электрофильного замещения атома Н (меркурирование, ацилирование, дейтерирование в кислой среде) в аренкарбонильных комплексах хрома протекают труднее аналогичных реакций бензола. Реакции с бутиллитием и дейтерирование в основной среде протекают в более мягких условиях. Галогенсодержащие комплексы вида [Сr(СО)3(С6Н5Х)] (X = Cl, F) легко замещают галоген на RO-, CN-, карбанионы. Реакция широко используется в органическом синтезе. Получение аренкарбонильных комплексов осуществляют путем обмена лигандов при нагревании аренов с [Cr(CO)6], [Cr(CO)3L3] или [Сr(СО)3( -С10Н8)]. Бисареновые комплексы [Сr(арен)2] - термически устойчивые вещества .
-С10Н8)]. Бисареновые комплексы [Сr(арен)2] - термически устойчивые вещества .
Дибензолхром вступает в реакции металлирования и изотопного обмена водорода в основных средах. В катионных комплексах Сr(I) кислотность связей С — Н на 16-17 порядков выше, чем в бензоле. В хлорзамещенных катионных комплексах [Сr(С6Н5С1)2]+ атом хлора легко замещается на RO-, RNH и др. Дибензолхром получают путем взаимодействия СrС13 с PhMgBr, образующийся [СrРh4] в результате перегруппировки образуется смесь [Сr(С6Н6)2], [Сr(С6Н6)Рh3] и [CrPh3]. Для синтеза алкил- и арилзамещ. дибензолхрома используют метод Фишера-Хафнера:
перегруппировки образуется смесь [Сr(С6Н6)2], [Сr(С6Н6)Рh3] и [CrPh3]. Для синтеза алкил- и арилзамещ. дибензолхрома используют метод Фишера-Хафнера:

Соединения имеющие общую формулу [Сr( -С5Н5)(
-С5Н5)( -С6Н6)] чрезвычайно реакционноспособны. При ацилировании в условиях проведения реакции Фриделя-Крафтса осуществляется расширение 6-членного цикла до 7-членного и образуется[Cr(
-С6Н6)] чрезвычайно реакционноспособны. При ацилировании в условиях проведения реакции Фриделя-Крафтса осуществляется расширение 6-членного цикла до 7-членного и образуется[Cr( -С5Н5)(
-С5Н5)( -C7H6R)]+. Известны комплексы Сr с карборанами в качестве лигандов: [Cr(l,2-C2B9H9R2)2]- и [Сr(1,7-С2В9Н11)2]-. Хромовые комплек-сные соединения широко применяются в качестве катализаторов реакций полимеризации и олигомеризации олефинов, в качестве катализатора используются иод-аллильные комплексы. [Сr(арен)2] используют для получения металлических и оксидных пленок и покрытий.
-C7H6R)]+. Известны комплексы Сr с карборанами в качестве лигандов: [Cr(l,2-C2B9H9R2)2]- и [Сr(1,7-С2В9Н11)2]-. Хромовые комплек-сные соединения широко применяются в качестве катализаторов реакций полимеризации и олигомеризации олефинов, в качестве катализатора используются иод-аллильные комплексы. [Сr(арен)2] используют для получения металлических и оксидных пленок и покрытий.
3.Заключение
Координационная химия или химия комплексных соединений длительное время относились к неорганической химии; это объяснялось тем, что ранее большинство известных комплексных соединений содержало в качестве лигандов, в основном, типичные неорганические молекулы и ионы - аммиак, воду, нитро-, роданогруппу и т.п. Экспериментальные исследования неорганических комплексных соединений задолго до того, как стремительно стала развиваться органическая химия. После создания А. Вернером координационной теории химия комплексных соединений постепенно, в течение десятилетий, стала превращаться в самостоятельный раздел химической науки. Ее успешное развитие связано с именами таких ученных как Трассер, Цейзе, Йергенсен, Грэм, Клаус, Бломстранд, школы А.Вернера, а в двадцатом веке такие ученные как Л.А. Чугаев, И.И. Черняев, А.А. Гринберг, Чата, Найхольм, Фишер, Бьеррум и многих других ученых различных стран. Сейчас координационная химия это наука, которая интенсивно развивавается в разных направлениях, тесно переплетаясь с другими областями химии.
Список литературы
1. Ю.Н. Кукушкин «Химия координационных соединений» Москва: Высшая школа, 1985 г.
2. "Координационая химия" Журнал Российской Академии наук. Основан в 1975 г.
3. А.А. Гринберг «Введение в химию комплексных соединений» Москва: Химия, 1966 г.
4. А.Вернер «Новые воззрения в области неорганической химии» Ленингдарад: ОНТИ, 1936 г.
5. Ф. Коттон, Дж. Уилкинсон «Современная неорганическая химия» Москва: Мир, 1969 г.
6. Н.А. Костромина, В.Н. Кумок, Н.А. Скорик «Химия координационных соединений» Москва: Высшая школа, 1990 г.
7. Общая химия Под ред. Е.М.Соколовской, Г.Д. Вовченко, Л.С. Гузея. Москва: Издательство Московского университета, 1980.
tnu.podelise.ru
Координационное число четыре - Справочник химика 21
| Рис. 1. Пространственная интерпретация координационного числа четыре |  |
Для никеля и палладия наиболее характерна степень окисления +2, а для платины +4. Известны также соединения Р1 (VI). Для никеля и его аналогов наиболее устойчивы координационные числа четыре (тетраэдр или квадрат) и шесть (октаэдр). Степени окисления элементов и отвечающие им пространственные конфигурации комплексов приведены в табл. 54. [c.606]
О механизме замещения в комплексах Аи(1П) и других элементов с плоской квадратной конфигурацией и координационным числом четыре см. обзор [1358]. Изучено замещение в комплексных соединениях золота [420]. [c.25]
| Рис. 23.1. Примеры комплексов с тетраэдрической (а) и плоскоквадратной (б) структурой а -2п(ЫНз)1+ б - Р1(ЫНз) +. Это две наиболее распространенные структуры комплексов, в которых металл имеет координационное число четыре. Штриховые линии на рисунках не обозначают химические связи, они проведены лишь для того, чтобы структура была более наглядной. |  |
Структура комплексов характеризуется координационным числом комплексообразователей, значение которого зависит от природы, радиуса атома, окислительного числа металла. У большинства металлических комплексообразователей координационное число четыре (тетраэдрическая или квадратная форма) или шесть (октаэдрическая форма), хотя встречаются координационные числа и меньше (три и два) и больше (восемь). У одного и того же металла с повышением окислительного числа увеличивается и координационное число [у Pt(II) к. ч.=4, а у Pt (IV) к. ч.=6]. [c.20]
Ионы некоторых металлов характеризуются постоянными координационными числами. Например, координационное число хрома(П1) и кобальта(П1) неизменно равно шести, а координационное число платины(П) всегда равно четырем. Однако координационные числа ионов большинства металлов меняются в зависимости от лигандов. Чаще всего встречаются координационные числа четыре и шесть. [c.372]
Учитывая распределение электронов данного центрального атома и адденда и результаты измерения магнитной восприимчивости, можно решить, какие из электронов и на каких орбитах принимают участие в образовании ковалентных связей. На основании этого можно подтвердить или отвергнуть приписываемую комплексу структуру. Для никеля (II), например, характерно координационное число четыре, которое может осуществляться в тетраэдрической или плоской ковалентной структурах. [c.342]
Координационное число четыре [c.235]
Структуры простых веществ элементов IV группы (углерод, кремний, германий, серое слово, но не свинец) соответствуют правилу Юм-Розери и имеют координационное число четыре. [c.276]
Фосфор в фосфатах образует яр -связи с координационным числом четыре и тетраэдрической симметрией. Основная структурная единица в фосфатах — тетраэдрическая группа РО4 с расстоянием Р—О, равным 0,156 нм (1,56 А). [c.38]
Силикаты с координационными числами четыре и шесть [c.194]
Какие же электронные конфигурации и соответствующие им типы связи могут существовать в комплексах двухвалентной меди с координационным числом четыре Рассмотрим приведенную ниже схему [c.34]
Легче ответить на вопрос, какие электронные конфигурации и соответствующие им типы связей могут быть для комплексных соединений двухвалентного никеля с координационным числом четыре. [c.34]
Для многочисленных комплексов никеля или окисной меди с координационным числом четыре имеются две стереохимические возможности. Одной из них является образование тетраэдрических связей с использованием 5р -гибридных орбит. Однако Полинг указал, что гибридизация должна приводить к четырем более прочным связям, направленным к четырем вершинам квадра- [c.163]
Комплексы иона меди(1) с четырьмя связями обычно построены п виде гетраэдров с участием зр гибридных орбиг (распределение электронов типа А). Однако медно-водородный комплекс(И), имеющий вид Си Х ,И, обладает строением изо-электроиным с комплексами иона меди (И) вида Си Х4, которые обладают координационным числом четыре и, как известно, имеют [c.189]
Для соединений металлов с неметаллами состава 1 1 известны три различные структуры — структура хлористого цезия с координационным числом восемь, структура хлористого натрия с координационным числом шесть и структура сульфида цинка с координационным числом четыре. Представляет интерес вопрос о том, какая из этих структур наиболее вероятна в каждом конкретном случае. Если предполагать, что соединение — ионное, то наиболее существенным фактором, определяющим структуру, является отношение радиуса аниона к радиусу катиона. Естественно предположить, что стабильность максимальна, если анионы соприкасаются с катионами, а не друг с другом. При ином положении отталкивание между анионами может перевесить притяжение между анионами и катионами. Предположим теперь, что соль АХ имеет структуру хлористого цезия, в которой выполняются сформулированные выше условия и размер катионов А постепенно уменьшается. Окружающие анионы X подходят все ближе друг к другу и наконец начинают соприкасаться. Дальнейшее уменьшение размеров катионов приведет к тому, что каждый анион будет соприкасаться со всеми окружающими его анионами, а это вызовет уменьшение стабильности (см. рис. 68). При таком положении весьма вероятно изменение структуры с переходом в структуру с меньшим координационным числом — структуру хлористого натрия. При дальнейшем уменьшении радиуса катиона снова наступит момент, когда анионы начнут соприкасаться друг с другом, и можно ожидать перехода в структуру с еще меньшим координационным числом (структуру сульфида цинка). Простое вычисление показывает, что предельные отношения радиусов гд/гх для трех типов структур равны [c.243]
Р н с. 128. Тетраэдрическая и плоская конфигурации у платины с координационным числом четыре, а—валентности платины расположены по тетраэдру, плоскость чертежа является плоскостью симметрии б—валентности платины расположены в плоскости, симметрии нет. [c.384]
Следствием этой теории является вывод, что комплексы с координационным числом четыре и шесть в основном имеют соответственно тетраэдрическую и октаэдрическую конфигурации. Комплексы переходных металлов иногда отклоняются от этого правила, и это отклонение можно отнести за счет имеющихся в них -электронов. Теория кристаллического поля дает возможно наиболее простое объяснение влиянию -электронов на структуру комплексов. [c.74]
Тенденции образования комплексов с высокими координационными числами противодействуют стерические факторы и электростатическое (или принцип Паули) отталкивание между лигандами. Простой схемы для каких-либо предсказаний с учетом этих критериев не существует. Однако следует отметить, что переходные элементы первого ряда часто имеют координационное число шесть. Координационное число четыре наблюдается главным образом в комплексах, содержащих некоторые большие анионы, такие, как С1 , Вг , Г и О или объемистые нейтральные молекулы. Переходные элементы второго и третьего ряда проявляют такие высокие координационные числа, как восемь. [c.78]
Координационные, или комплексные, соединения содержат ионы металлов, связанные с несколькими окружающими их анионами или молекулами, которые называют лигандами. Ион металла и его лиганды образуют координационную сферу комплекса. Атом лиганда, присоединенный к иону металла, называется донорным атомом. Число донорных атомов, присоединенных к иону металла, называется координационным числом иона металла. Наиболее распространены координационные числа четыре и шесть наиболее распространенные типы структуры координационных комплексов - тетраэдрическая, плоско-ква-дратная и октаэдрическая. [c.400]
По результатам магнитных измерений можно подтвердить или опровергнуть приписываемую веществу структуру. Так, для двухвалентного никеля характерно координационное число четыре, проявляемое в тетраэдрической и плоско-квадратной кристаллической структурах. При координационном числе четыре вокруг комплексообразователя расположены четыре лиганда, которые, будучи донорами, предоставляют четыре пары электронов. При образовании тетраэдрической структуры эти электроны должны находиться в состоянии хр -гибрндизации, а при образовании плоской квадратной — в состоянии с1зр -гиб-ридизации. На рис. 4.21, а представлено распределение электронов по уровням и подуровням в изолированном атоме никеля. При образовании иона N1 + атом теряет два 45-электрона [c.197]
Известно, что теплота растворения соли зависит от концентрации ионов водорода в растворе. Так, теплота растворения Li l и Na l в растворах НС1 зависит от ее концентрации. Самойлов объясняет это обстоятельство тем, что, благодаря наличию положительного заряда, на молекулах воды происходит их некоторое дополнительное отталкивание от положительных ионов и притяжение к отрицательным так как размеры анионов больше, заряды в основном сказываются на взаимодействии воды с катионами. Это дополнительное отталкивание уменьшает положительные тепловые эффекты и увеличивает отрицательные. Основываясь на этом изменении теплового эффекта, Самойлов разработал термохимический метод определения координационных чисел. Эти числа для катионов щелочных металлов оказались равными около 4, а анионов от 4 до 5. Автор считает, что координационное число четыре соответствует наименьшему нарушению структуры воды при образовании раствора ионов. [c.283]
Комплексные соединения содержат в своем составе комплексные группы, или комплексы, отличительные признаки которых указаны выше. Комплексные группы состоят из центрального атома, или ком-плексообразователя, около которого координируются лиганды. Структура комплексов характеризуется координационным числом комплек-сообразователей, значение которого зависит от природы, радиуса и окислительного числа центрального атома. У большинства комплексо-образователей координационное число четыре (тетраэдрическая или квадратная форма) или шесть (октаэдрическая форма), хотя встречаются координационные числа и меньше (три и два) и больше (восемь). У одного и того же комплексообразователя с повышением окислительного числа увеличивается и координационное число. [c.65]
Вернер показал, что для комплексов платины (И) с общей формулой [МааЬа " с координационным числом четыре существует цис — тран -изомерия, причем только в том случае, если четыре лиганда лежат в одной или приблизительно в одной плоскости, как изображено для комплекса [Р1(ЫНд)2С12) [c.235]
В отличие от бора атом алюминия имеет свободные -подуровни на внешнем электронном уровне. Кроме того, ион А1 + отличается небольпгам радиусом при довольно высоком заряде и поэтому является комплексообразователем с координационными числами четыре (как у бора) и шесть. [c.313]
В ионных кристаллах, например солях, энергия определяется в основном электростатическим взаимодействием ионов. Их пространственное расположение определяется в первую очередь особенностями плотной упаковки шаров разного размера. Если один из ионов меньше другого (например, в СзС1), то координационное число 12 не может осуществиться. В решетке СзС ион цезия находится внутри куба, в вершинах которого находятся ионы хлора. Координационное число цезия в нем равняется восьми. Если отношение радиуса катиона к радиусу аниона еще уменьшается, то восемь соседей не могут уместиться вокруг маленького иона и осуществляется решетка типа простой кубической решетки НаС1, в которой в вершинах куба попеременно располагаются ионы хлора и натрия. Координационное число при этом уменьшается до шести. Если рассматриваемое отношение еще меньше, то образуется решетка с координационным числом четыре (например, 2п5 имеет решетку типа алмаза с чередующимися атомами серы и цинка). [c.631]
Соединения серы (VI). Как и у других р-элементов 3-го периода, максимальное координационное число серы при высщей степени окисления равно шести, а ее наиболее устойчивое координационное число четыре. Степень окисления серы +6 проявляется в соединениях с наиболее электроотрицательными элементами в гексафториде SFg, триоксиде SO3, оксо- и диоксодигалогенидах SOF4, S02Hal2 а также в отвечающих им анионных комплексах [c.360]
В некоторых случаях имеет значение то, что лиганд оказывается намного больше катиона по размерам. Эта причина может привести к ограничению координационного числа катиона, поскольку она делает физически невозможным присоединение к нему нескольких лигандов. Например, экспериментальные наблюдения показывают, что если отношение радиусов катиона и лигандов ГкатионаАлиганда меньше 0,155, максимальное координационное число не может превышать двух. Как видно из рис. 23.4, третьему катиону не удается в этом случае подойти достаточно близко к центральному иону, чтобы между ними возникла химическая связь. Однако и в тех случаях, когда отношение указанных радиусов очень мало, более важным фактором остается баланс сил притяжения лигандов к центральному катиону и сил отталкивания между лигандами. Это иллюстрируется сопоставлением комплексов двухвалентной и четырехвалентной платины. Ион двухвалентной платины имеющий радиус 0,93 А, обычно образует комплексные соединения с координационным числом четыре, а ион четырехвалентной платины с радиусом 0,69 А имеет координационное число шесть. Более высокий заряд иона влияет на координационное число гораздо существеннее, чем ограничения, обусловленные его меньшим радиусом. [c.408]
Строго говоря, прямое сопоставление констант равновесия с целью определения относительной термодинамической устойчивости комплексов допустимо лишь для соединений с формулами одного и того же типа. Например, прямое сопоставление значений Снестойк возможно для комплексных ионов u(NHз)J , Си(СН) и Hg( N) , относящихся к одному и тому же типу (с координационным числом четыре). Однако нельзя сопоставлять значения КнестоЯк Для комплексов u(NHз)J+ и Ag(NHз) +. [c.412]
Электронная конфигурация и координационное число центрального атома, а также лигандное окружение определяют геометрию комплексного соединения. Переходным металлам с координационным числом шесть отвечают комплексы с октаэдрической конфигурацией, четыре - с плоско-квадратной и тетраэдрической конфигуратщей. Плоско-квадратная конфигурация наиболее характерна для комплексов Р1(Ц), Р(1(П), Аи(Ш), КЬ(1), 1г(1), тетраэдрическая - для N1(11), Си(П), Со(П), а октаэдрическая - для Сг(П1), Со(Ш), Р1(1У), КЩХП), 1г(Ш). Среди перечисленных комплексов следует отметить комплексы NiiII) с координационным числом четыре, которые могут существовать в рав- [c.505]
В координационной сфере иона металла располагается определенное число лигандов, это число и есть координационное число комплексообразователя. Координационные числа в принципе переменны и определяются природой металла и лиганда, хотя для каждого иона металла имеются характерные для него координационные числа. Очень многие иоиы металлов образуют плоские квадратные или тетраэдрические комплексы с координационным числом четыре или октаэдрические комплексы с координационным числом шесть. Координационные числа 2 и 3, и больше шести — 7, 8, 9 встречаются реже. Комплексы с максимальным числом лнгаидов называют координационно насыщенными. [c.37]
Еще один тип беспорядка наблюдается в некоторых смешанных галогенидах и окислах, которые не содержат комплексных ионов, соответствующих их формулам. Так, например, соединение KLap4 имеет структуру фтористого кальция с ионами калия, замещающими половину ионов кальция, и ионами лантана, замещающими вторую половину ионов кальция. Хотя это соединение отнюдь не является нестехиометрическим, оно не является упорядоченным, поскольку ионы калия и лантана распределены совершенно беспорядочно. Йодистое серебро имеет при низких температурах структуру вурцита с координационным числом четыре, но при 145,8° претерпевает переход, сопровождающийся значительным увеличением электропроводности. Выше 145,8° ионы иодида располагаются более рыхло, так что имеется более чем достаточно мест для серебра. Ионы серебра занимают эти положения беспорядочно и могут свободно передвигаться из одного места в другое. Можно сказать, что при 145,8° в кристалле Agi плавится серебро (но не ионы иода). [c.271]
При более высоких те ушературах могут существовать отдельные молекулы РеС1з. Такие же димерные молекулы содержатся в недонорных растворителях, например в бензоле, тогда как в таких донорных растворителях, как эфир, железо достигает координационного числа четыре путем присоединения молекулы растворителя, причем хлорное железо мономерно. В водном растворе хлорное железо ионизировано и присутствует в виде гидратированных ионов хлора и целого набора катионов, как-то Ре(Н20)б , Ре(Н20)б0Н и т. д. (см. стр. 291). Расплавленное хлорное железо, по-видимому, содержит ряд упомянутых форм в равновесии друг с другой. [c.273]
В противоположность системам с координационным числом четыре шестикоординационные комплексы дают много примеров оптической изомерии очень часто они встречаются среди соединений или ионов типа [М(АА)з], например оптические изомеры триоксалатпого комплекса хрома(1П), XVIII и XIX. Бидентатные лиганды обычно содержат атом углерода, но известны по крайней мере три оптически активных, чисто неорганических комплекса. Один из них был приготовлен Вернером для доказательства того, что оптическая активность этих систем обусловлена не атомом углерода. Чтобы это продемонстрировать, он использовал мостиковый комплекс XX, [c.85]
Для комплексов с координационным числом металла менее шести наиболее вероятным будет механизм замещения Sjv2. Лучше всего изучены комплексы Pt(H) с координационным числом четыре. Для этого случая известно экспериментальное доказательство механизма 5дг2. Скорости реакций с некоторыми комплексами Pt(H), имеющими [c.177]
Ч. Томасу [16], состоит в том, что в них ионы алюминия могут связывать элементы структуры алюмосиликата [Si04] или же слои тетраэдров. Алюминий и кремний занимают тетраэдрические пустоты кислородных тетраэдров и имеют координационное число четыре при валентности три, поэтому прочность связи алюминий — анион равна /4 по сравнению с прочностью связи, равной 1 в окиси алюминия. Таким образом, прочность [c.118]
chem21.info










