Контрольная работа для подготовки к егэ по химии. И для хрома и для железа нехарактерна степень окисления равная
Правильно записано уравнение реакции
⇐ ПредыдущаяСтр 3 из 3l) 2Fe + 3Cl2=FeCl3
2)Fe+S = Fe2S3
3) Fe + Cl2=FeCl2
4) 3Fe + 2O2 = Fe3O4
5. Коэффициент при окислителе в реакции Fe + HNO3 ® Fe(NO3)3+ NO+ h3O:
1) 1
2) 4
3) 8
4) 16
6. При производстве серной кислоты применяют:
1) FeS2
2) Fe2(SO3)3
3) Fe2(SO4)3
4) Fe
7. Fe3O4 -это:
1) магнитный железняк
2) красный железняк
3) бурый железняк
4) железный колчедан, пирит
8.В схеме получения оксида железа (II) Fe ® FeCl2 ®X®FeО X это
1)Fe2О3
2) Fe2(SO3)3
3) Fe(OH)2
4) FeCl3
9.В схеме получения оксида железа (III) Fe ® FeCl3 ®X®Fe2О3 X это
1)FeО
2) Fe2(SO3)3
3) Fe(OH)3
4) Fe(OH)2
10. Для приготовления минеральных красок используют:
1) железный купорос FeSO4.7h3O
2) хлорид железа (III)
3) сульфат железа (III)
4) красную кровяную соль K3(Fe(CN)6)
Тест 10
1. Медь растворяется в разбавленном водном растворе кислоты:
1) серной
2) соляной
3) азотной
4) фтороводородной
2.Какой из металлов не вытесняет водород из разбавленной серной кислоты:
1) железо
2) хром
3)медь
4) цинк
3. Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
| ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ 1) Fе SО4 + Н2 2) Fе2(SО4)3 + Н2 3) Fе2(SО4)3+ SО2+ Н2О 4) FеС12+ Н2 5) FеС13+ Н2 6) FеС13 |
А) Fе+ С12 →
Б) Fе + НС1 →
В) Fе + Н2SО4 (разбавл.) →
Г) Fе + Н2SО4 (конц.)t →
4. И для хрома, и для железа нехарактерна степень окисления, равная
l) +6
2)+2
3) +3
4)+4
5. Для железа нехарактерна степень окисления:
1) +6
2) +2
3) +3
4) +5
6. Верны ли следующие суждения о меди?
А Для меди характерны степени окисления +1 и +2.
Б Медь вытесняет цинк из раствора сульфата цинка
1)верно только А
2) верно только Б
3) верно только Б
4) оба суждения неверны
7. Химическая реакция возможна между:
1) Сu и НСl
2) Fе и Nа3РО4
3) Аg и Мg(NО3)2
4) Zn и FеС12
8. При обычной температуре медь реагирует с:
1)водой
2) азотом
3) хлороводородной кислотой
4) азотной кислотой
9. Гидроксид цинка реагирует реагирует с каждым из веществ:
1) сульфат кальция и оксид серы(VI)
2) гидроксид натрия (р-р) и соляная кислота
3) вода и хлорид натрия
4)сульфат бария и гидроксид железа(III)
10.С водой при комнатной температуре реагирует каждый из двух металлов:
1) барий и медь
2) алюминий и ртуть
3) кальций и литий
4) серебро и натрий
.
Ответы
Тема d- Металлы (Fe, Zn, Cu, Cr, Mn)
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
| № теста | Номер тестового задания | |||||||||
mykonspekts.ru
Переходные металлы. - Химия - Подготовка к ЕГЭ
Металлы побочных подгрупп
Строение атома
Разнообразие форм и свойств соединений металлов побочных подгрупп определяется, в первую очередь, значительным различием в количестве валентных электронов в их атомах. Так, в атоме скандия имеется три валентных электрона; в атоме титана – четыре; ванадия – пять; хрома – шесть: марганца – семь. Напомним, валентными электронами в атомах 3d-элементов являются электроны 3d- и 4s-подуровней. Например, в атоме марганца, как и у его предшественника хрома, 3d-подуровень заполнен ровно наполовину, то есть в основном состоянии атомов Mn и Cr имеется по пять неспаренных валентных d-электронов. В образовании химических связей участвуют также электроны 4s-подуровня атомов хрома и марганца. В атоме хрома один такой электрон, в атоме марганца – два. Таким образом, в основном состоянии у атома хрома имеется шесть неспаренных электронов, высшая степень окисления хрома +6. В возбужденном состоянии атома марганца один из 4s-электронов переходит на 4p-подуровень, образуется электронная конфигурация с семью неспаренными электронами. В итоге, высшая степень окисления марганца равна +7.
В атомах последующих 3d-элементов – железа, кобальта, никеля, меди и цинка – происходит дальнейшее заполнение d-подуровня, при этом высшая степень окисления указанных элементов всегда меньше, чем суммарное число электронов на 4s- и 3d-подуровнях. Поэтому наиболее характерные степени окисления для никеля меди и цинка лишь +2; для железа и кобальта +2 и +3. Это можно объяснить тем, что с увеличением атомного номера увеличивается заряд ядер, уменьшается радиус атомов, электроны удерживаются прочнее. Например, у цинка, десятого d-элемента, проявляющего только степень окисления +2, d-электроны заполненного подуровня уже не являются валентными.
Среди 3d-элементов только первый и последний представители – скандий и цинк – проявляют в соединениях постоянную степень окисления: скандий +3, цинк +2. Все остальные 3d-элементы являются поливалентными. В таблице приведены степени окисления 3d-элементов в образуемых ими соединениях и характер соответствующих гидроксидов.
Получение железа.
Железо восстанавливают из оксидов в доменной печи, в которую слоями засыпают железную руду и кокс. Печь снизу продувают горячим воздухом. При этом углерод кокса, частично окисляясь, образует оксид углерода(II).
Восстановленное расплавленное железо собирается в нижней части печи, где температура достигает 1800 оС. В условиях доменного процесса в присутствии кокса расплав железа растворяет углерод. Образуется сплав, содержащий до 4,3 % углерода. Этот сплав называется чугун. Чугун содержит также кремний (1,25 – 4 %), серу и фосфор (менее 1 %). Чугун используется для получения различных металлоизделий, в основном, методом литья. Но основная масса чугуна используется для передела в сталь – важнейший сплав железа, основной конструкционный материал для машиностроения.
Основная цель процесса передела чугуна в сталь – снижение содержания углерода (до 0,1 – 1,7 %), а также таких примесей, как кремний (до 0,6 %), фосфор и сера (до 0,05 %). Процесс осуществляют в конвертерах и мартеновских печах.
Конвертер для получения стали представляет собой грушевидный сосуд, облицованный изнутри огнеупорным кирпичом. В него загружают жидкий чугун, который затем продувают кислородом. При этом углерод, кремний, фосфор, сера окисляются до CO2, SiO2, P2O5, SO2. Оксиды углерода и серы улетучиваются, оксиды кремния и фосфора взаимодействуют с известняком, входящим в состав облицовки конвертера:
CaСO3 + SiO2 = CaSiO3 + СО2;
3CaСO3 + P2O5 = Ca3(PO4)2 + 3СО2.
Продукты превращений примесей образуют жидкий слой шлака над поверхностью расплавленной стали.
В мартеновскую печь можно загружать твердый чугун и металлический лом. Для связывания примесей в шлак добавляют флюс, в основном, на основе известняка. Печь нагревают газовым пламенем. Существуют также электрические печи для выплавки стали.
Ежегодно в мире производится примерно 700 млн. тонн сплавов на основе железа. Они используются как основные конструкционные материалы в машиностроении.
Производство других металлов осуществляется в гораздо меньших масштабах.
Интересно, что при получении железа основным восстановителем является не углерод, а оксид углерода(II), который образуется в печи за счет частичного окисления кокса, для чего печь продувают воздухом:
2С + О2 2СО;
С + СО2 2СО.
Затем оксид углерода(II) восстанавливает металл:
Fe2O3 + 3CO = 2Fe + 3CO2.
Химические свойства
Железо – металл. Атомы железа легко отдают электроны:
взаимодействие железа с серой:
;
растворение железа в соляной кислоте:
.
В приведенных реакциях степень окисления железа повышается от “0” до “+2”.
Железо при обычных условиях не реагирует с водой. В этом легко убедиться, если опустить в воду железный гвоздь. Однако при действии водяного пара на раскаленное железо образуются оксид железа(II,III) и водород:
Очевидно, что гидроксид железа в таких условиях образоваться не может, поскольку он разлагается при нагревании на оксид железа и воду.
Для многих металлов характерно взаимодействие с кислотами.
С растворами кислот реагируют металлы, расположенные в ряду активности перед водородом. При этом протекают окислительно-восстановительные реакции: ионы водорода выступают в роли окислителя, а металл является восстановителем. В результате образуется соль и водород:
2e
Металлы, расположенные в ряду активности за водородом, с кислотами не реагируют!
Активные металлы вытесняют менее активные металлы из растворов солей:
2e
Как и в случае взаимодействия металлов с кислотами, данная реакция является окислительно-восстановительной. В роли окислителя выступают ионы металла, входящего в состав соли (Cu2+), а простое вещество (Zn) является восстановителем. Так как окислительная способность ионов металлов увеличивается в ряду активности слева направо, то ионы Cu2+ (находятся правее) могут окислять Zn, но не наоборот!
Чаще всего па практике металлами средней активности (Mg, Al, Zn, Fe) восстанавливают из солей малоактивные металлы (Cu, Ag и др.). Однако можно использовать и другие комбинации. Например, восстановить ионы серебра медью, или ионы Fe2+ магнием:
2e
2e
urokidoma.org
Окислители и восстановители — МегаЛекции
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Степень окисления
1. Наибольшую степень окисления марганец имеет в соединении1)MnSO4 2)MnO2 3)K2MnO44) Mn2O3
2.Одинаковую степень окисления хлор имеет в каждом из двух соединений:
1)CrCl3 и Cl2O7 2)KClO4 и Cl2O7 3)KCl и HClO 4)KClO2 и BaCl2
3.Низшую степень окисления азот проявляет в 1)азотной кислоте 2)азотистой кислоте 3)нитрате калия 4)сульфате аммония
4. Минимальную степень окисления хлор проявляет в соединении 1)Nh5Cl 2)Cl2 3)Ca(OCl)2 4)NaClO2
5.В соединениях: Ph4, P2O5, h4PO3 фосфор имеет степени окисления, соответственно равные:
1)+ 3; + 5; – 3 2)– 3; + 5; + 3 3)– 3; + 3; + 5 4)+ 3; – 5; – 3
6. И для хрома, и для железа не характерна степень окисления, равная 1)+ 6 2)+ 2 3)+ 3 4)+ 4
7. Хлор проявляет положительную степень окисления в соединении с 1)серой 2)водородом 3)кислородом 4)железом
8. В ионе аммония NH+4 степень окисления атома азота равна 1)+ 1 2)+ 3 3)– 3 4) – 5
9. Установите соответствие между формулой вещества и степенью окисления азота в нём.
| ФОРМУЛА ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА |
| А) NaNO2 Б) Nh5NO3 В) Nh5NO2 Г)HNO3 | 1)+5 2)+3 3) –3, +5 4)0, +2 5) –3, +3 6) +4, +2 |
10. Установите соответствие между химической формулой соединения и степенью окисления фосфора в нем.
| ФОРМУЛА ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ ФОСФОРА |
| А)h4PO3 Б)h4PO4 В) h4PO2 Г) h5P2O7 | 1)+ 1 2)+ 3 3)+ 5 4)– 1 5) – 3 |
11. Степень окисления +5 фосфор имеет в каждом из двух соединений: 1)Ca3P2 и h4PO4 2)PCl5 и Ph4 3)h5P2O7 и P4 4)Ca(h3PO4)2 и P2O5
12. Наименьшую степень окисления сера проявляет в соединении 1)Na2S 2)Na2SO3 3)Na2SO4 4)SO3
13. Степень окисления серы в NaHSO3 равна 1)+ 6 2)– 2 3)0 4)+ 4
14. Одинаковую степень окисления железо проявляет в соединениях: 1)FeO и FeСO3 2)Fe(OH)3 и FeСl2 3)Fe2O3 и Fe(NO3)2 4)FeO и FePO4
15. В какой молекуле степень окисления элемента равна нулю, а валентность равна единице? 1)O2 2)CaC2 3)Cl2 4)CO
16. Степень окисления +3 азот проявляет в каждом из двух веществ: 1)Nh5Cl и NaNO2 2)NaNO3 и NO2 3)N2O4 и Nh4 4)KNO2 и NF3
17. Высшую степень окисления сера проявляет в соединении 1)SO3 2)Al2S3 3)h3S 4)NaHSO3
18. Степень окисления хлора равна +7 в соединении 1)Ca(ClO2)2 2)HClO3 3)Nh5Cl 4)HClO4
19. В каком соединении степень окисления азота равна –3? 1)KNO2 2)Nh5Cl 3)KNO3 4)N2O3
20. Одинаковую степень окисления фосфор имеет в соединениях 1)Kh3PO4 и KPO3 2)Ca3P2 и h4PO3 3)P4O6 и P4O10 4)h4PO4 и h4PO3
21. Степень окисления + 5 азот имеет в соединении 1)Ca(NO2)2 2)N2O3 3)KNO3 4)Nh5F
22. Степень окисления – 3 азот проявляет в соединении 1)(Nh5)2CO3 2)N2O4 3)HNO2
4) Al(NO3)3
23. Степень окисления, равную + 5, атом хлора проявляет в ионе 1)ClO4- 2)ClO3- 3)ClO2- 4)ClO-
24. Установите соответствие между формулой иона и степенью окисления атома, несущего положительный заряд.
| ФОРМУЛА ИОНА | СТЕПЕНЬ ОКИСЛЕНИЯ |
| А) PF+4 Б) BF−4 В) P2O4−7 Г) SCl2+2 | 1)+7 2)+2 3)+3 4)+4 5)+5 6)+6 |
25.Степень окисления + 3 в соединениях могут проявлять неметаллы 1)фосфор и хлор 2)углерод и кислород 3)азот и фтор 4)кремний и селен
26. Наибóльшую степень окисления сера проявляет в соединении 1)CaS 2)Li2SO3 3)CaSO4 4)h3S
27. Степень окисления + 6 сера проявляет в соединении 1)h3S 2)SO2 3)Na2SO3 4)K2SO4
28.Степень окисления азота в нитриде кальция Ca3N2 равна 1)– 3 2)– 2 3)+ 2 4)+ 5
29. Степень окисления хлора в Са(ClO2)2 равна 1)0 2)– 3 3)+ 3 4)+ 5
30. Установите соответствие между названием вещества и степенью окисления азота в нём.
| НАЗВАНИЕ ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА |
| А)гидросульфид аммония Б) нитрат железа (II) В) нитрит натрия Г) азотистая кислота | 1)– 3 2)– 2 3)+ 1 4) + 2 5) + 3 6)+ 5 |
31. Максимально возможную степень окисления азот проявляет в 1)нитрите калия 2)нитрате алюминия 3)азотистой кислоте 4)хлориде аммония
32 Отрицательная степень окисления у атома серы в соединении 1)NaHS 2)NaHSO3 3)SO2 4)h3SO4
33. Степень окисления хрома в соединении (Nh5)2CrO4 равна 1)+6 2)–6 3)+4 4)–4
34. Установите соответствие между формулой иона и степенью окисления центрального атома в нём.
| ФОРМУЛА ИОНА | СТЕПЕНЬ ОКИСЛЕНИЯ |
| А)PCl4+ Б)PCl4– В) S2O72– Г) SF22+ | 1)+ 7 2)+ 2 3)+ 3 4)+ 4 5) + 5 6)+ 6 |
35. Установите соответствие между химической формулой соединения и значением степени окисления серы в нем.
| ХИМИЧЕСКАЯ ФОРМУЛА | СТЕПЕНЬ ОКИСЛЕНИЯ СЕРЫ |
| А)Mg(HSO4)2 Б)Al2S3 В)S8 Г)(Nh5)2SO3 | 1)0 2)+ 2 3)+ 4 4)+ 6 5)– 2 |
36.Для железа нехарактерна степень окисления 1)+ 6 2)+ 2 3)+ 3 4)+ 5
37.Азот проявляет степень окисления + 3 в каждом из двух соединений: 1)N2O3 и Nh4 2)Nh5Cl и N2O 3)HNO2 и N2h5 4)NaNO2 и N2O3
38. Наименьшую степень окисления сера имеет в соединении 1)Na2S 2)Na2SO4 3)NaHSO3 4)Na2SO3
39. Какой из приведенных неметаллов не проявляет степени окисления, равной номеру группы? 1)N 2)S 3)F 4)Br
40.Одинаковую степень окисления хром проявляет в каждом из двух соединений: 1)СrCl3 и CrO3 2)K2CrO4 и K2Cr2O7 3)K2Cr2O7 и Cr2S3 4)KCrO2 и K2CrO4
41. Установите соответствие между формулой вещества и степенью окисления углерода в нем.
| ФОРМУЛА ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ |
| А)Ch3Cl2 Б)HCHO В)HCOONa Г) CBr4 | 1)– 4 2)– 2 3)0 4)+ 2 5)+ 4 |
42. Среди перечисленных элементов постоянную степень окисления в соединениях проявляет 1)свинец 2)медь 3)стронций 4)сера
43. Степень окисления, равную + 4, атом серы имеет в соединении1)h3SO4 2)FeS2 3)h3SO3 4) NaHSO4
44. В каком соединении степень окисления атома хлора равна + 5? 1)Ca(ClO2)2 2)Cl2O7 3)NaClO4 4)KClO3
45. Степень окисления – 3 фосфор проявляет в соединении1)Ph4 2)P2O3 3)Nah3PO4 4)h4PO4
46. Наибольшую степень окисления марганец проявляет в соединении 1)MnCl2 2)MnO 3)K2MnO4 4)Mn2O7
47. Наибольшую степень окисления азот проявляет в соединении 1)Nh4 2)N2 3)NO2 4N2O5
48. Наименьшую степень окисления атом фосфора имеет в соединении1)h4PO4 2)h4PO3 3)h4PO2 4)h5P2O7
49. Какой элемент во всех соединениях проявляет степень окисления +2? 1)магний 2)железо 3)углерод 4)марганец
50. Одинаковую степень окисления железо проявляет в каждом из двух соединений: 1)FeO и Fe(NO3)3 2)Fe2O3 и FePO4 3)Fe(OH)2 и Fe2(SO4)3 4)Fe2O3 и FeHPO4
51. Степень окисления +4 и 0 соответственно азот проявляет в соединениях:1)NO2 и N2 2)Nh4 и N2 3)NO2 и N2O5 4)Nh4 и N2O5
52. Степень окисления серы в соединении K2S2O7 равна 1)–2 2)0 3)+4 4) +6
53. Установите соответствие между химическим элементом и возможными значениями его степеней окисления.
| ЭЛЕМЕНТ | СТЕПЕНИ ОКИСЛЕНИЯ |
| А)Cl Б)F В)P Г)S | 1)– 2, – 1, 0, + 2 2)– 2, 0, + 4, + 6 3)– 3, 0, + 3, + 5 4)– 1, 0 5)– 1, 0, + 1, + 3, + 5, + 7 6)– 4, – 2, 0, + 2, + 4 |
54. Наименьшую степень окисления хром имеет в соединении 1)K2CrO4 2)CrS 3)CrO3 4)Cr2(SO4)3
55.Установите соответствие между формулой вещества и степенью окисления азота в нем.
| Формула вещества | Степень окисления азота |
| А)NOF Б)(Ch4)2NH В)Nh5Br Г)N2h5 | 1)– 3 2)– 2 3)+ 2 4)+ 3 5)+ 4 6)+ 5 |
56. Степень окисления азота равна – 3 в соединении 1)HNO3 2)NaNO2 3)(Nh5)2SO4 4)N2O5
57 Степень окисления, равную – 3, азот проявляет в каждом из двух соединений: 1)Nh4 и Nh5Cl 2)Nh4 и N2O3 3)HNO3 и Nh4 4) N2O3 и HNO2
58. Степень окисления азота в сульфате аммония равна1)– 3 2)– 1 3)+ 1 4)+ 3
59. Установите соответствие между формулой вещества и степенью окисления углерода в нем.
| ФОРМУЛА ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ |
| А)Ch5 Б)HCHO В)HCOOH Г)CCl4 | 1)– 4 2)– 2 3)0 4)+ 2 5)+ 4 |
60. Степень окисления серы в соединении FeSO3 равна 1)– 1 2)+ 2 3) 0 4)+ 4
61 Максимальная степень окисления фосфора в соединениях равна1)+ 6 2)+ 5 3)+ 3 4)+ 4
62.Степень окисления азота в ионе NН4+ равна1)– 1 2)– 3 3)+ 3 4)+ 5
63. Атом азота проявляет одинаковую степень окисления в каждом из двух соединений:1)Nh4, N2O3 2)HNO2, Li3N 3)Mg3N2, Nh4 4)Nh4, HNO2
64. При взаимодействии фосфора с активными металлами образуются соединения, в которых его степень окисления равна
1)– 3 2)0 3)+ 3 4)+ 5
65.Высшую степень окисления фосфор проявляет в соединении, формула которого1)Ca3P2 2)K3PO4 3)P2O3 4)Ph4
Окислители и восстановители
66. Только окислительными свойствами обладает 1)фтор 2)хлор 3)бром 4)иод
67. В химической реакцииFe + CuSO4 = Cu + FeSO4восстановителем является1)Fe2+ 2)Cu2+ 3)Fe0 4) O2–
68. Оксид серы (IV) является восстановителем в реакции1)SO2 + CaO = CaSO3 2)2SO2 + O2 = 2SO3 3)SO2 + 2h3S = 3S + 2h3O 4)SO2 + NaOH = NaHSO3
69. В реакции меди с концентрированной серной кислотой окислителем является1)Cu2+ 2)H+ 3)Cu0 4) S+6
70.Восстановительные свойства сернистая кислота проявляет в реакции
1)Н2SO3 + 2NaOH = Na2SO3 + 2Н2О 2)Н2SO3 + Br2 + Н2О = Н2SO4 + 2НBr
3)Н2SO3 + 2Н2S = 3S + 3Н2О 4)Н2SO3 + Na2O = Na2SO3 + Н2О
71. Наибольшей восстановительной активностью обладает 1)Li 2)Be 3)B 4)S
72.Углерод выступает в качестве восстановителя в реакции с 1)водородом 2)алюминием 3)кальцием 4)оксидом меди
73. Восстановительные свойства проявляет 1)Н2 2)О2 3)О3 4)F2
74. В реакции оксида железа (III) с оксидом углерода (II) окислителем является1)Fe 0 2)C + 2 3)Fe + 3 4)C + 4
75. Углерод является окислителем в реакции с 1)водой 2)алюминием 3)оксидом меди (II) 4)cерной кислотой
76.Коэффициент перед формулой окислителя в уравнении реакции S + HNO3 → h3SO4 + NO равен 1)1 2)2 3)3 4)4
77. В реакции, схема которой C + HNO3 → NO2 + CO2 + h3O, коэффициент перед формулой восстановителя равен 1)1 2)2 3)3 4)4
78. В реакции оксида хрома (III) с алюминием восстановительные свойства проявляет 1)Cr + 32)Al 0 3)O – 2 4)Cr 0
79. Коэффициент перед формулой окислителя в уравнении реакции, схема которой Nh4 + O2 → N2 + h3O, Равен 1)1 2)2 3)3 4)4
80. Восстановительные свойства железо проявляет в реакции: 1)FeO + h3SO4 = FeSO4 + h3O 2)Fe(OH)2 + 2HCl = FeCl2 + 2h3O 3)2FeCl2 + Cl2 = 2FeCl3 4)FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl
81. Наиболее сильным окислителем является 1)N2 2)O2 3)F2 4)Cl2
82. Хлор является и окислителем, и восстановителем в реакции, уравнение которой 1)2FeCl2 + Cl2 = 2FeCl3 2)Fe + 2 HCl = FeCl2 + h3 3)2KOH + Cl2 = KCl + KClO + h3O 4)MnO2 + 4HCl = Cl2 + MnCl2 + 2h3O
83. В порядке уменьшения восстановительных свойств металлы расположены в ряду: 1)Al, Zn, Fe 2)Al, Na, K 3)Fe, Zn, Mg 4)Fe, Zn, Al
84. В реакции оксида железа (III) с водородом восстановителем является 1)h30 2)Fe + 3 3)Fe 0 4) O – 2
85.Восстановителем в реакцииMnS + 8HNO3(конц) = MnSO4 + 8NO2 + 4h3O является
1)S2- 2)Mn2+ 3)H+ 4)NO3-
86. В реакции оксида вольфрама (VI) с водородом окислителем является 1)W + 6 2)h30 3)O –2 4)W0
87. Кремний является окислителем в реакции с 1)магнием 2)кислородом 3)хлором 4)серой
88. Bодород проявляет свойства окислителя при взаимодействии с 1)кислородом 2)азотом 3)кальцием 4)хлором
89. Оксид серы (IV) является восстановителем в реакции, уравнение которой
1)SO2 + 2NaOH = Na2SO3 + h3O 2)SO2 + 2h3S = 3S + 2h3O
3)SO2 + h3O 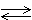 h3SO3 4)2SO2 + O2
h3SO3 4)2SO2 + O2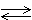 2SO3
2SO3
90. Установите соответствие между схемой реакции и формулой вещества-восстановителя в ней.
| СХЕМА РЕАКЦИИ | ФОРМУЛА ВОССТАНОВИТЕЛЯ |
| А)Cl2+KOH→KCl + KClO + h3O Б)h3O2+Ag2O→h3O + Ag + O2 В)h3O2 + Cl2 → HCl + O2 Г)Cl2 + NO → NOCl | 1)KOH 2)Cl2 3)h3O2 4)Ag2O 5)NO |
91. Оксид углерода (II) проявляет восстановительные свойства при нагревании с 1)N2 2)CO2 3)Fe 4)Fe2O3
92. Бром является восстановителем в реакции, схема которой
1)HBr + O2 → h3O + Br2 2)Br2 + Zn → ZnBr2
3)HBr + Mg → MgBr2 + h3 4)Br2 + KI → I2 + KBr
93. Восстановительные свойства азот проявляет в реакции: 1)N2 + O2 = 2NO 2)N2 + 3h3 = 2Nh4
3)N2 + 6Li = 2Li3N 4)N2 + 3Mg = Mg3N2
94. Только окислительные свойства проявляет 1)сульфид натрия 2)сера 3)серная кислота 4)сульфит калия
95.Только окислительные свойства проявляет 1)сульфид натрия 2)сера 3)серная кислота 4)сульфит калия
96. Окислительные свойства серная кислота проявляет в реакции, схема которой:
1)h3SO4 + Nh4 → Nh5HSO4 2)h3SO4 + KOH → K2SO4 + h3O
3)h3SO4 + P → h4PO4 + SO2 4) h3SO4 + P2O5 → HPO3 + SO3
97. Азот является восстановителем в реакции
1)N2 + O2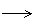 2) N2 + h3
2) N2 + h3 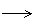 3)N2 + Mg
3)N2 + Mg 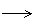 4) N2 + C
4) N2 + C 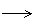
98. Веществом, не проявляющим восстановительные свойства, является
1)NaI 2)Na2S 3)Na2SO3 4)Na2SO4
99. Окислительные свойства в водных растворах проявляет1)карбонат калия 2)сульфат калия 3)сульфид калия 4)дихромат калия
100. Окислительные свойства оксид серы (IV) проявляет в реакции
1)SO2 + NaOH = NaHSO3 2)SO2 + Br2 + 2h3O = h3SO4 + 2HBr
3)SO2 + 2h3S = 3S + 2h3O 4)2SO2 + O2 = 2SO3
101. В реакции магния с концентрированной азотной кислотой окислителем является 1)Mg2+ 2)H+ 3)Mg0 4) NO3–
102.Верны ли следующие суждения об окислительных свойствах азота?
| А. | Азот является более слабым окислителем, чем хлор. |
| Б. | Азот является окислителем в реакции с водородом. |
1)верно только А 2)верно только Б 3)верны оба суждения 4)оба суждения неверны
103. Углерод является восстановителем в реакции с 1)кремнием 2)кальцием 3)водородом 4)водой
104. Восстановительные свойства в водных растворах проявляет 1)сульфид натрия 2)сульфат натрия 3)фосфат натрия 4)карбонат натрия
105. Как окислитель сера выступает в реакции с 1)хлором 2)кислородом 3)бромом 4)железом
106. В окислительно-восстановительной реакции Cu+HNO3(разб) → Cu(NO3)2+NO+h3O коэффициент перед окислителем1)8 2)10 3)6 4)4
107. Углерод является окислителем в реакции1)C+2h3=Ch5 2)C+FeO=Fe+CO
3)C+2Cl2=CCl4 4)C+O2=CO2
108. В уравнении реакции красного фосфора с избытком хлора коэффициент перед формулой окислителя равен1)5 2)2 3)3 4)4
109.Формула вещества, в котором сера может проявлять только восстановительные свойства, – 1)SO2 2)h3SO4 3)h3S 4)K2SO3
110. Наиболее сильным окислителем является 1)О2 2)N2 3)F2 4)I2
111. Установите соответствие между уравнением реакции и формулой вещества, являющегося восстановителем в данной реакции.
| УРАВНЕНИЕ РЕАКЦИИ | ВОССТАНОВИТЕЛЬ |
| А)h3S + I2 = S + 2HI Б)S + 2HI = I2 + h3S В)2SO3 + 2KI = I2 + SO2 + K2SO4 Г) S + 3NO2 = SO3 + 3NO | 1)NO2 2)h3S 3)HI 4)S 5)KI 6)I2 |
112. В уравнении реакции полного сгорания сероводорода в кислороде коэффициент перед формулой окислителя равен1)1 2)2 3)3 4)4
113.В реакции цинка с разбавленной серной кислотой восстановителем является1)Zn0 2)SO2−4 3)H+ 4) Zn2+
114. Свойства восстановителя кремний проявляет в реакции, уравнение которой 1)SiO2+2Mg=2MgO+Si 2)Si+O2=SiO2 3)SiO2+4Mg=Mg2Si+2MgO 4)h3SiО3=SiO2+h3O
115. Установите соответствие между уравнением реакции и формулой вещества, являющегося окислителем в данной реакции.
| УРАВНЕНИЕ РЕАКЦИИ | ОКИСЛИТЕЛЬ |
| А)SO2 + NO2 = SO3 + NO Б)2Nh4 + 2Na = 2NaNh3 + h3 В)4NO2 + O2 + 2h3O = 4HNO3 Г)4Nh4 + 6NO = 5N2 + 6h3O | 1)Nh4 2)O2 3)NO2 4)NO 5)SO2 6)Na |
116. Окислительные свойства фосфор проявляет при взаимодействии с 1)кислородом 2)серой 3)хлором 4) магнием
117. Восстановителем в реакции MnS + 8HNO3(конц) = MnSO4 + 8NO2 + 4h3O является
1)S2- 2)Mn2+ 3)H+ 4)NO3-
megalektsii.ru
Как определить степень окисления атома химического элемента :: SYL.ru
Формальный заряд атома в соединениях — вспомогательная величина, обычно ее используют в описаниях свойств элементов в химии. Этот условный электрический заряд и есть степень окисления. Его значение изменяется в результате многих химических процессов. Хотя заряд является формальным, он ярко характеризует свойства и поведение атомов в окислительно-восстановительных реакциях (ОВР).
Окисление и восстановление
В прошлом химики использовали термин «окисление», чтобы описать взаимодействие кислорода с другими элементами. Название реакций произошло от латинского наименования кислорода - Oxygenium. Позже выяснилось, что другие элементы тоже окисляют. В этом случае они восстанавливаются — присоединяют электроны. Каждый атом при образовании молекулы изменяет строение своей валентной электронной оболочки. В этом случае появляется формальный заряд, величина которого зависит от количества условно отданных или принятых электронов. Для характеристики этой величины ранее применяли английский химический термин "oxidation number", который в переводе означает «окислительное число». При его использовании исходят из допущения, что связывающие электроны в молекулах или ионах принадлежат атому, обладающему более высоким значением электроотрицательности (ЭО). Способность удерживать свои электроны и притягивать их от других атомов хорошо выражена у сильных неметаллов (галогенов, кислорода). Противоположными свойствами обладают сильные металлы (натрий, калий, литий, кальций, другие щелочные и щелочноземельные элементы).
Определение степени окисления
Степенью окисления называют заряд, который атом приобрел бы в том случае, если бы принимающие участие в образовании связи электроны полностью сместились к более электроотрицательному элементу. Есть вещества, не имеющие молекулярного строения (галогениды щелочных металлов и другие соединения). В этих случаях степень окисления совпадает с зарядом иона. Условный или реальный заряд показывает, какой процесс произошел до того, как атомы приобрели свое нынешнее состояние. Положительное значение степени окисления — это общее количество электронов, которые были удалены из атомов. Отрицательное значение степени окисления равно числу приобретенных электронов. По изменению состояния окисления химического элемента судят о том, что происходит с его атомами в ходе реакции (и наоборот). По цвету вещества определяют, какие произошли перемены в состоянии окисления. Соединения хрома, железа и ряда других элементов, в которых они проявляют разную валентность, окрашены неодинаково.
Отрицательное, нулевое и положительное значения степени окисления
Простые вещества образованы химическими элементами с одинаковым значением ЭО. В этом случае связывающие электроны принадлежат всем структурным частицам в равной степени. Следовательно, в простых веществах элементам несвойственно состояние окисления (Н02, О02, С0). Когда атомы принимают электроны или общее облако смещается в их сторону, заряды принято писать со знаком "минус". Например, F–1,О–2, С–4. Отдавая электроны, атомы приобретают реальный или формальный положительный заряд. В оксиде OF2 атом кислорода отдает по одному электрону двум атомам фтора и находится в состоянии окисления О+2. Считают, что в молекуле или многоатомном ионе более электроотрицательные атомы получают все связывающие электроны.
Сера — элемент, проявляющий разные валентность и степени окисления
Химические элементы главных подгрупп зачастую проявляют низшую валентность равную VIII. Например, валентность серы в сероводороде и сульфидах металлов — II. Для элемента характерны промежуточные и высшая валентность в возбужденном состоянии, когда атом отдает один, два, четыре или все шесть электронов и проявляет соответственно валентности I, II, IV, VI. Такие же значения, только со знаком "минус" или "плюс", имеют степени окисления серы:
- в сульфиде фтора отдает один электрон: –1;
- в сероводороде низшее значение: –2;
- в диоксиде промежуточное состояние: +4;
- в триоксиде, серной кислоте и сульфатах: +6.
В своем высшем состоянии окисления сера только принимает электроны, в низшей степени — проявляет сильные восстановительные свойства. Атомы S+4 могут проявлять в соединениях функции восстановителей или окислителей в зависимости от условий.
Переход электронов в химических реакциях
При образовании кристалла поваренной соли натрий отдает электроны более электроотрицательному хлору. Степени окисления элементов совпадают с зарядами ионов: Na+1Cl–1. Для молекул, созданных путем обобществления и смещения электронных пар к более электроотрицательному атому, применимы только представления о формальном заряде. Но можно предположить, что все соединения состоят из ионов. Тогда атомы, притягивая электроны, приобретают условный отрицательный заряд, а отдавая, — положительный. В реакциях указывают, какое число электронов смещается. Например, в молекуле диоксида углерода С+4О-22 указанный в верхнем правом углу индекс при химическом символе углерода отображает количество электронов, удаленных из атома. Для кислорода в этом веществе характерно состояние окисления –2. Соответствующий индекс при химическом знаке О — количество добавленных электронов в атоме.
Как подсчитать степени окисления
Подсчет количества отданных и присоединенных атомами электронов может отнять много времени. Облегчают эту задачу следующие правила:
- В простых веществах степени окисления равны нулю.
- Сумма окисления всех атомов или ионов в нейтральном веществе равна нулю.
- В сложном ионе сумма степеней окисления всех элементов должна соответствовать заряду всей частицы.
- Более электроотрицательный атом приобретает отрицательное состояние окисления, которое записывают со знаком "минус".
- Менее электроотрицательные элементы получают положительные степени окисления, их записывают со знаком "плюс".
- Кислород в основном проявляет степень окисления, равную –2.
- Для водорода характерное значение: +1, в гидридах металлов встречается: Н–1.
- Фтор — наиболее электроотрицательный из всех элементов, его состояние окисления всегда равно –4.
- Для большинства металлов окислительные числа и валентности совпадают.
Степень окисления и валентность
Большинство соединений образуются в результате окислительно-восстановительных процессов. Переход или смещение электронов от одних элементов к другим приводит к изменению их состояния окисления и валентности. Зачастую эти величины совпадают. В качестве синонима к термину «степень окисления» можно использовать словосочетание «электрохимическая валентность». Но есть исключения, например, в ионе аммония азот четырехвалентен. Одновременно атом этого элемента находится в состоянии окисления –3. В органических веществах углерод всегда четырехвалентен, но состояния окисления атома С в метане СН4, муравьином спирте СН3ОН и кислоте НСООН имеют другие значения: –4, –2 и +2.
Окислительно-восстановительные реакции
К окислительно-восстановительным относятся многие важнейшие процессы в промышленности, технике, живой и неживой природе: горение, коррозия, брожение, внутриклеточное дыхание, фотосинтез и другие явления.
При составлении уравнений ОВР подбирают коэффициенты, используя метод электронного баланса, в котором оперируют следующими категориями:
- степени окисления;
- восстановитель отдает электроны и окисляется;
- окислитель принимает электроны и восстанавливается;
- число отданных электронов должно быть равно числу присоединенных.
Приобретение электронов атомом приводит к понижению его степени окисления (восстановлению). Утрата атомом одного или нескольких электронов сопровождается повышением окислительного числа элемента в результате реакций. Для ОВР, протекающих между ионами сильных электролитов в водных растворах, чаще используют не электронный баланс, а метод полуреакций.
www.syl.ru
Другие степени окисления - Справочник химика 21
Иногда для маскирования используют о к и с л ит е л ь и о - восстановительные реакции. Мешающий элемент при этом переводят в другую степень окисления. Примерами могут служить комплексонометрические титрования циркония (IV) или тория (IV) в присутствии ионов железа (III). Титрования проводят при pH 1,5—2, и лоны железа (III) в таких условиях мешают определениям. Мешающее влияние устраняют восстановлением железа аскорбиновой кислотой до железа (II). Количественные расчеты здесь затруднены в связи с отсутствием достоверных данных по константам устойчивости комплексонатов и гидроксокомплексов циркония (IV) и тория (IV). Однако из рис. 45 можно сделать качественную оценку видно, что. при pH 2 логарифм реальной константы устойчивости комплексоната железа (И) меньше единицы. [c.237] Алюминий — основной представитель металлов главной подгруппы III группы периодической системы химических элементов Д. И. Менделеева. Атомный номер 13, относительная атомная масса 26,98154. У алюминия единственный устойчивый изотоп А1. Свойства аналогов алюминия — галлия, индия и таллия — во многом напоминают свойства алюминия. Этому причина — одинаковое строение внешнего электронного слоя элементов — s p, вследствие которого все они проявляют степень окисления +3. Другие степени окисления нехарактерны, за исключением соединений одновалентного таллия, по свойствам близким к соединениям элементов I группы. В связи с этим будут рассмотрены свойства только одного элемента — алюминия и его соединений. [c.150]Внутренние переходные металлы. Лантаноиды и актиноиды образуют ряды переходных металлов иного типа, в которых соседние элементы обладают очень сходными свойствами. Для всех лантаноидов и актиноидов в их соединениях обычно проявляется степень окисления 3. Однако возможны и другие степени окисления, которые иногда являются более характерными для отдельных элементов (например, Еи , Се и и ). [c.419]
У переходных металлов проявляются кроме высших и другие степени окисления, среди которых чаще всего встречаются степени окисления Ь 2 и -Ь 3, [c.450]
Переход в производные других степеней окисления хорощо циден на примере церия. Их окисление до степени окисления +А может происходить как в кислой, так и в щелочной среде. [c.608]
Другие степени окисления. При сплавлении оксидов железа с нитратами щелочных металлов и щелочами железо сравнительно легко окисляется с образованием ферратов — солей железной кислоты [c.271]
Характерная степень окисления +6. Наряду с этим хром дает устойчивые соединения со степенью окисления +3, молибден — иногда +4. В других степенях окисления (+1, +2, +4, +5) хром и его аналоги образуют неустойчивые соединения. Некоторые свойства элементов приведены в табл. 22.1. [c.376]
Пользуясь справочной и учебной литературой, приведите примеры природных неорганических соединений фосфора. Сделайте вывод о наиболее устойчивой степени окисления фосфора. Какими свойствами должны обладать соединения фосфора с другими степенями окисления [c.93]
Характерной для хлора, брома и иода степенью окисления также является —1 однако они могут проявлять и другие степени окисления. В водном растворе НЭ — кислоты с увеличением г,- их сила возрастает от НС1 к Н1. НЭ реагируют как восстановители в ряду НС1—НВг—HI восстановительная способность усиливается. [c.95]
Кроме того, соблюдается правило особой устойчивости незаполненного, наполовину заполненного и полностью заполненного подуровня. Это позволяет объяснить существование у лантаноидов кроме степени окисления 3 других степеней окисления. Особенностью этих элементов является большее сходство их химических свойств по сравнению с элементами других классов. [c.105]
Соединения железа. В I отмечалось, что для железа наиболее характерны соединения, где степень его окисления равна (+2) или (+3). Другие степени окисления для железа малохарактерны. Наиболее устойчивыми являются соединения трехвалентного железа, в которые стремятся переходить соединения двухвалентного железа. [c.353]
Подгруппу азота составляют пять элементов азот, фосфор, мышьяк, сурьма и висмут. Это р-элементы IV группы периодической системы Д. И. Менделеева. На внешнем энергетическом уровне их атомы имеют по пять электронов в состоянии (см. табл. 3.1, п. 2). Поэтому высшая степень окисления этих элементов равна +5, низшая —3, характерна и -f 3. О других степенях окисления см. табл. 3.1. [c.101]
Фосфор — аналог азота, так как имеет валентные электроны, как н у азота (3s 3p ) (см. с. 101). Однако по сравнению с атомом азота атом фосфора характеризуется меньшей энергией ионизации и имеет больший размер (см. табл. 3.1). Это означает, что неметаллические признаки у фосфора выражены слабее, чем у азота. Поэтому для фосфора реже встречается степень окисления —3 и чаше +5. Мало характерны и другие степени окисления (см. табл. 3.1). [c.118]
Другие степени окислення для железа не характерны. [c.209]
Марганец в других степенях окисления похож на соседние с ним по ряду переходные элементы — хром и особенно железо. Технеций по свойствам стоит ближе к рению. [c.532]
За счет четырех неспаренных электронов атом углерода (в возбужденном состоянии) образует четыре химические связи, проявляя степени окисления +4 или —4. Для углерода характерны и другие степени окисления, например +2. [c.94]
Иногда для маскирования используют окислительновосстановительные реакции. Мешающий элемент при этом переводят в другую степень окисления. Примерами могут служить комплексонометрические титрования циркония (IV) или тория (IV) в присутствии ионов железа (III). Титрования проводят при [c.243]
Наличием одного непарного электрона обусловливается сходство фтора с водородом. Однако различие в общем числе валентных электронов и орбиталей предопределяет значительное отличие этих элементов друг от друга. Степень окисления фтора как самого электроотрицательного элемента (4,0) принимается равной -1. [c.310]
Для всех этих элементов перечисленные степени окисления очень важны однако имеются и другие степени окисления. Ион меди Си+ неустойчив, и соединения меди(1), за исключением очень плохо растворимых, легко окисляются. Ион меди(II) Сц2+ [гидратированный до Си(Н20)4 ] входит iB состав многих солей меди, и соединения u(II) — важнейшие соединения меди. Атом меди в ионе u + лишен двух электронов и имеет в 7И-оболочке только семнадцать электронов. Фактически 3d- и 45-электроны удерживаются атомом меди приблизительна с одинаковой силой. Нетрудно заметить, что электронная структура,, приведенная в табл. 19.4 для меди, несколько отличается от структуры, соответствующей диаграмме энергетических уровней, приведенной на рис. 5.6, в том отношении, что на этой диаграмме, медь имеет два 46-электрона и только девять Зс -электронов. [c.558]
Степень окисления +2, отвечающая потере двух электронов, представляется наиболее важной для исех указанных выше элементов, в частности для элементов первого длинного периода, образующих ионы Т1 +, V +, Сг + и Мп2+. Соединения этих элементов отвечают также целому ряду других степеней окисления, связанных с потерей электронов или с совместным владением дополнительными электронами. Максимальная степень окисления соответствует потере или совместному владению всеми электронами -орбиталей следующей (внутренней) оболочки наряду с двумя электронами внешней оболочки. Отсюда следует, что максимальные степени окисления для титана, ванадия, хрома и мар-, ганца равны соответственно +4, +5, +6 и +7. [c.573]
В растворах, содержащих Мп07 и Мп , не удается обнаружить достаточных концентраций ионов марганца других степеней окисления (Мг 1 Мп , Мп 1 образует оксалатные комп- [c.374]
Однако, используя серную кислоту для этих целей необходимо учитывать и другие свойства этой кислоты, ограничивающие ее применение. Концентрированная серная кислота является достаточно сильным окислителем, поэтому ее нельзя использовать для получения таких кислот как НВг, HI, h3S, кислотообразующие элементы которых она может перевести в другие степени окисления, например [c.20]
Если кислотообразующий элемент может находиться в нескольких степенях окисления, то используя подходящий окислитель или восстановитель можно перейти от соли одной кислоты к соли другой кислоты, в которой кислотообразующий элемент находится в другой степени окисления. [c.34]
Перед выполнением задания учитель отмечает, что в главных подгруппах элементы-металлы имели постоянные валентности и степени окисления все щелочные металлы одновалентны (степень окисления +1), щелочноземельные двухвалентны (степень окисления +2), алюминий трехвалентен (степень окисления -fЗ), Иначе обстоит дело с элементами-металлами побочных подгрупп. У них валентные электроны располагаются на двух электронных слоях, атомы этих элементов могут отдавать со своих слоев разное число электронов, проявляя в одном случае одну, а в другом — другую степень окисления. [c.146]
Известны соединения содержащие железо в других степенях окисления [c.22]
Форма кривых амперометрического титрования зависит от выбранного потенциала и от того, какой из участников химической реакции является электрохимически активным. Если на электроде восстанавливается (окисляется) определяемое вещество (R), а титрант (Т) электрохимически неактивен, то ток в процессе титрования будет з еньшаться вследствие связывания определяемого вещества титрантом либо в осадок, либо в прочный комплекс, либо вследствие перехода в другую степень окисления (рис. 14.3, а). Следует заметить, что на практике наблюдается некоторое искривление кривой титрования вблизи точки эквивалентности. Экспериментальная кривая соответствует теоретической, если константа равновесия химической реакции стремится к бесконечности. В противном случае концентрация титруемого вещества и, следовательно, ток при добавлении избытка титранта еще продолжают уменьшаться. Поскольку прямолинейные графики служат наиболее приемлемым типом кривых титрования, конечную точку титрования находят экстраполяцией линейных участков кривой. Примером этого типа кривых титрования является титрование ионов свинца раствором ЭДТА с регистрацией катодного тока РЬ . [c.509]
Общая характеристика. Внешняя электронная конфигурация атомов лантаноидов может быть представлена формулой 4/"5s 5p 5d 6s где п изменяется от О до 14, а т может принимать только два значения О и 1-. Для описания электронной конфигурации лантаноида достаточно указать лишь число 4/- и 5 -электронов, число же остальных электронов остается без изменения. Электронные подуровни 4/ и Ьё, довольно близки гю энергии и при известных условиях может происходить взаимный переход электронов. Основная степень окисления +3 в редкоземельном ряду осуществляется за счет двух электронов б5, одного 5й для 0с1 и Ьи и одного 4/-элект-рона для остальных лантаноидов. Значительно реже некоторые из них могут проявлять степени окисления +2 и +4. При этом наблюдается внутренняя периодичность в изменении степеней окисления (см. 4.4). В целом у атомов лантаноидов с увеличением порядкового номера проявляется общая тенденция, состоящая в замене конфигураций типа 4/ 5d конфигурациями типа 4/ 5й . Для последних членов ряда лантаноидов большая прочность связи 4/- по сравнению с 5й -эл8ктронами проявляется особенно отчетливо. У ионизированных атомов тенденция эта проявляется сильнее, чем у нейтральных атомов. Все лантаноиды образуют устойчивые ионы Э " , однако шесть из них могут проявлять и другие степени окисления +4 (Се, Рг, ТЬ) и +2 (5т, Ей, УЬ). Электронные конфигурации ионов можно представить общей формулой 4/"55 5р . Электроны 5s 5/7 экранируют 4/-электроны от влияния внешних полей, поэтому поведение ионов лантаноидов во многих отношениях напоминает поведение других ионов с внешней оболочкой благородных газов. [c.358]
Элементы подгруппы титана поливалентны. Характерная сте-пень окисления 4-4. Титан наряду с этим имеет многочисленные устойчивые соединения со степенью окисления +3. Для циркония и гафния таких соединений известно мало. В других степенях окисления (+1. +2) соединения титана и его аналогов нругтпйчирм Некоторые свойства элементов приведены в табл. 20.1. [c.364]
Переход электрона из оболочки атома благородного газа на более высокий энергетический уровень требует очень высокой затраты энергии, которая не может бы1Ь компенсирована энергией образования химической связи, поэтому щелочные металлы не проявляют других степеней окисления, кроме +1. [c.320]
Валентными электронами у них, помимо электронов внешнего электронного уровня, являются еще 4—5 электронов соседнего с внешним (незаполненного ) уровня ( -электроны). Поэтому для всех этих элементов высшая степень окисления равна +6, причем для молибдена и вольфрама это состояние является наиболее устойчивым. Вместе с тем каждый из этих элементов образует и соединения, отвечающие другим степеням окисления. Хром проявляет в них степень окисления, равную трем и двум (эти соединения рассматриваются дальше), а молибден и вольфрам — степень окисления, равную четырем (М0О2, WOг). [c.141]
Отсюда делаем заключение, что кислород в противоположность алюминию является сильным окислитед ем. Характерной степенью его окисления является —2, но, как указано выше, он может проявлять и другие степени окисления. Таким образом, в реакции алюминия с кислородом протекает окислительно-восстановительный процесс, благодаря которому степень окисления алюминия повышается от О до +3, а степень окисления кислорода понижается от О до —2 [c.117]
Наиболее характерной степенью окисления для хлора, брома и йода также является (1 ). однако вследствие свободных =орбиталей на внешней орбите они могут проявлять в отличие от фтора и другие степени окисления. Например, электронную конфигурацию хлора см. на етр. 379. Стрелками показаны возможные распаривания электронов в различных возбужденных со- стояниях хлора. Такое распаривание возможно потому,1 что атом хлора имеет свободные квантовые ячейки на Зй- подуровне. При частичном или полном распарива- НИИ электронов хлор может проявлять переменную сте- пень окисления I, 3, 5, 7. Аналогичные степени окисле-j ния могут проявлять в своих соединениях бром и йод., ij [c.264]
Помимо своей максимальной положительной валентности они проявляют и другие степени окисления 1, 2, 3, 4, 5, 6. Наиболее устойГчивымй являются соединения марганца и его аналогов в 2-, 4- и 7-валентных формах. [c.335]
Из производных других степеней окисления рассматриваемых элементов представляют интерес соединения Ре (VI) — фер))а-ты — производные неизвестной железной кислоты НгРе04. Их 1Ю-лучают при сплавлении РегОз с сильными окислителями в присут-.ствии щелочей, например [c.542]
chem21.info
Степень окисления ферум. Железо это
Cтраница 3
На рис. V.8 приведена корреляционная схема, которая дает представление об интервалах изомерных сдвигов 57Fe для соединений железа. Степень окисления железа может меняться от 0 до 6, и охарактеризовать ее по изомерному сдвигу 57Fe не так просто.
Восстановительная атмосфера вызывает понижение степени окисления железа в шлаке, между тем как при окислительной атмосфере под действием больших температур пламени продолжается распад более высоких окислов железа. Повышение степени окисления железа в шлаке воздействием окислительной атмосферы возможно только при температуре пламени ниже 1 200 С и большой поверхности шлака.
Довольно резко в породах изменяется содержание А12Оз, щелочей. Постоянным сохраняется степень окисления железа.
Образец С со степенью окисления 13 % не имеет пластической области, и шлак ведет себя, как стекло. С повышением степени окисления железа до 30 или 56 % в кривых вязкости образцов В и А появляется изгиб, свидетельствующий о том, что шлак в месте изгиба переходит в пластическое состояние.
Но степень окисления серы, входящей в состав этих ионов, различна. В первом случае степень окисления железа совпадает с зарядом простого иона Fe2 и с валентностью железа. Таким образом, валентностью данного элемента в комплексном соединении называют всю сумму связей, которой обладает в данном соединении центральный атом - комплексообразователь.
Тенденция к комплексообразованию подтверждается и существованием типичных двойных солей типа шенитов и квасцов. В этом соединении степень окисления железа 2 стабилизируется, в то время как сульфат FeSO4 в водном растворе склонен к окислению кислородом воздуха. Никель подобных соединений не образует, поскольку степень окисления 3 для этого элемента настолько малохарактерна, что даже не стабилизируется в двойных солях.
Это увеличение степени окисления железа в шлаке продолжается до температуры около 1 200 С. При дальнейшем повышении температуры шлака степень окисления железа значительно падает.
Как указано, центральный атом железа лежит в плоскости 16-членного пор-фирипового кольца, причем он связан с атомами азота пиррольных колец четырьмя из шести имеющихся валентностей, а поэтому для завершения октаэдрического комплекса остаются две валентности; эти валентности находятся выше и ниже плоскости чертежа показанной модели. Кроме того, нужно учитывать также степень окисления железа; когда железо находится в закисном состоянии, как показано на рисунке, то протопорфирин носит название тема или, более четко, феррогема. Если гем находится в свободном состоянии в растворе и не связан с белком, то предполагается, что две молекулы воды находятся в координационной связи с пятым и шестым положениями валентности железа. Джордж обозначает этот феррогем следующим образом: h3O - Fep-H. При окислении он переходит в Н О Fep НаО с одним положительным зарядом. Этот ферригем может координировать хлор-ион с переходом в h3O - Fep-Cl и в этом случае называется гемином; при координированном гидроксилыюм ионе ферригем обозначается как гематин Н2О - Рер-ОН, хотя эти термины иногда употребляются и менее специфически, лишь для обозначения наличия окисного железа. Возможна координация и других молекул, причем в первую очередь играет роль координация с перекисью водорода. Феррогем легко координирует азотистые основания, например пиридин, образуя гемохромогеиы В-Рбр - В. Такое же соединение с ферригемом B-Fep-B называется парагема-тином.
Посредством магнитного метода установлено наличие и дана количественная оценка валентных связей между соседними положительными ионами. Так, в Fe203 на носителе А1203 степень окисления железа равна трем, но одновременно соседние атомы железа образуют между собою ковалентную связь.
Посредством магнитного, метода установлено наличие и дана количественная оценка валентных связей между соседними положительными ионами. Так, в Fe2O3 на носителе А12О3 степень окисления железа равна трем, но одновременно соседние атомы железа образуют между собою ковалентную связь.
Если рассмотреть гидроксиды Fe (OH) 2 и Fe (OH) 3, то с позиции схемы Косселя кислотные свойства второго гидроксида должны быть выражены сильнее, чем первого. Это следует из того, что чем выше степень окисления железа (даже если принять, что радиусы ионов Fe2 и Fe3 одинаковы), тем выше отталкивание протона и тем сильнее выражены кислотные свойства соответствующего гидроксида. Если учесть, что радиус иона Fe3 несколько меньше, чем иона Fe2, то большее отталкивание протона в соединении Fe (OH) 3 по сравнению с Fe (OH) 2 становится еще очевиднее.
Часть окислов железа восстанавливается до металлического железа, другая часть - до [ закись-окиси ]; кроме того, на них выделяется углерод. Количество кислорода, еще содержащегося в руде, характеризует степень окисления железа.
Если после предварительных испытаний остается сомнение, присутствует ли ион железа, можно проделать поверочные реакции. Но следует помнить, что при этом испытании уже нельзя установить первоначальную степень окисления железа в анализируемой пробе.
Лишь в присутствии сильных окислителей удается получить довольно непрочные производные железной кислоты h3FeO4 со степенью окисления железа 6, однако соответствующий оксид выделить не удалось. Если RuO4 - малоустойчивое вещество, которое получают косвенным путем, то OsO4 - соединение вполне устойчивое, образующееся при окислении металла на воздухе.
История
Железо, как инструментальный материал, известно с древнейших времён. Самые древние изделия из железа, найденные при археологических раскопках, датируются 4-м тысячелетием до н. э. и относятся к древнешумерской
overmedic.ru
Контрольная работа для подготовки к егэ по химии
ТЕМА: «Степень окисления, окислительно-восстановительные реакции. Электролиз»I. Используя метод электронного баланса, составьте уравнение реакции.
Определите окислитель и восстановитель.
1. Nh4 + KMnO4 → MnO2 + …………….
- Ph4 + AgNO3 + … → Ag + HNO3 + …
- As2S3 + HNO3(разб.) + … → h4AsO4 + h3SO4 + …
- Al2S3 + HNO3(конц.) →
II. Задачи.
- К 25 мл 34 % соляной кислоты плотностью 1,16 г/мл добавили оксид марганца массой 2,61г. Какая масса карбоната калия может прореагировать без нагревания с выделившемся хлором?
- Сульфат марганца (II) обработали в щелочном растворе пероксидом водорода массой 17 г. Вычислите массу образовавшегося темно-бурого осадка.
- При взаимодействии в сернокислой среде 8,7 г диоксида марганца с бромидом калия выделился бром массой 9,6 г практический выход которого составил 80 %. Какая масса диоксида марганца осталась после реакции?
III. Напишите уравнения четырех возможных реакций между всеми предложенными веществами, не повторяя пары реагентов.
- Даны вещества: перманганат калия, сульфит натрия, вода, гидроксид калия.
- Даны вещества: дихромат калия, концентрированная серная кислота, раствор иодида калия, ртуть.
- Даны растворы хромата калия, сероводородной и азотной кислоты.
- Даны вещества: концентрированная азотная кислота, концентрированная серная кислота, сульфид меди (II), хлор и кислород.
- Даны вещества: концентрированная серная кислота, алюминий, хлор и бромид калия.
А 1. Число электронов, находящихся на электронных орбиталях иона О2-, равно
1) 16 2) 32 3) 8 4) 10
А 2. Возбужденному состоянию атома углерода соответствует электронная конфигурация
1) 1s22s12p3 2) 1s22s22p3 3) 1s22s22p2 4) 1s22s22p5
А 3. Полярность связи Э-Н уменьшается в ряду
1) h3S, HCl 2) HF, h3O 3) Sih5, C2H6 4) h3Se, h3S
А 4. Вещества только с ионной связью указаны в ряду
1) CaF2, Na2S, N2 2) P4, FeCl3, Nh4 3) SiF4, HF, h3S 4) NaCl, LiH, Nh5F
А 5. Степень окисления +3 азот проявляет в соединении
1) N2h5 2) K2NH 3) NF3 4) HNO3
А 6. Вещества с атомной кристаллической решеткой
1) очень твердые и тугоплавкие 2) проводят электрический ток в растворах
3) хрупкие и легкоплавкие 4) проводят электрический ток в расплавах
^ . И для хрома, и для железа нехарактерна степень окисления, равная
1) +6 2) +2 3) +3 4) +4
А 8. Верны ли следующие суждения о галогенах?
А. Окислительные свойства галогенов с увеличением порядкового номера увеличиваются.
Б. Все простые вещества галогены являются только окислителями.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба неверны
^ . Высший гидроксид хлора 1) Cl2O7 2) HCl 3) HClO 4) HClO4
А 10. Летучее водородное соединение углерода проявляет
1) кислотные свойства 2) основные свойства 3) амфотерные свойства
4) не проявляет кислотно-основные свойства
В1. Установите соответствие между формулой вещества и продуктом, который образуетсяна катоде при электролизе его водного раствора.
^
А) Nh5Br 1) водород 2) металл
Б) MgSO4 3) металл и водород
В) HNO3 4) кислород
Г) AgNO3 5) бром
В2. Масса воды, которую надо добавить к 50 г 70% раствора для получения 5% раствора этого же вещества, равна ___________ %. (Число запишите с точностью до целых).
С 1. Используя метод электронного баланса, составьте уравнение реакции:K2Cr2O7 + h3SO4 + h3O2 → Cr2(SO4)3 +…..
Определите окислитель и восстановитель.
lib.znaimo.com.ua










