Энциклопедия по машиностроению XXL. Хром никель железо
Елизаветинский хром-никель-железо рудник — Рудники ⚒ Урала
В 1829 году жителем поселка Горный Щит Матвеем Никитиным на Елизаветинских горах близ Екатеринбурга была обнаружена руда лимонита. Гору ту назвали по рядом расположенному селению Елизавет, названному, в свою очередь, в честь Елизаветы Петровны — дочери императора Петра I. Начиная с 1898 года Елизаветинское месторождение неоднократно привлекало внимание промышленности исключительно как месторождение лимонитовых руд. В 1911-1919 годах добывались только плотные комовые и редниковые руды, для обогащения (промывки от глины) которых рядом была построена мойка.
Начиная с 1898 года Елизаветинское месторождение неоднократно привлекало внимание промышленности исключительно как месторождение лимонитовых руд. В 1911-1919 годах добывались только плотные комовые и редниковые руды, для обогащения (промывки от глины) которых рядом была построена мойка.
Позже были проведены разведочные работы трестом «Уралдразведка» — в 1929-1930 годах на никель, а в 1931-1932 годах — на кобальт. Так, в 1931 году из карьера №5 и №3 было взято несколько тонн кварцита для проведения на Лысьвенском заводе опытов по извлечению кобальта и приготовлению эмали.
В 1932 году «Уралдразведка» провела опробование месторождения с целью установления условий залегания, образования и качества кобальтовых руд. Было пройдено 157 дудок, расположенных в узлах квадратной сетки со сторонами 100 м. Но все 350 проб из-за отсутствия средств полностью на кобальт проанализированы не были, а были использованы для изучения качества железных руд.
Только с 1932-1933 годов Елизаветинские руды стали рассматриваться как комплексные, содержащие кроме железа еще и никель, хром, кобальт и марганец.Руды имели незначительное содержание серы, что позволяло получать без дополнительных присадок специальные (легированные) сорта чугуна и стали.
В 1936-1938 годах месторождение разрабатывалось Первоуральским рудоуправлением, работы велись вручную без проекта в двух карьерах. За этот период было добыто 105 тысяч тонн руды.Добываемая руда отправлялась на Ревдинский завод для выплавки передельного чугуна, а в годы Великой Отечественной Войны по железнодорожной ветке «Рудник-Разъезд №75» на Верхне-Уфалейский никелевый завод.
Железная руда залегала практически у поверхности, на глубине всего 1-5 метров. В верхней части залегали бурые глины, ниже шли «порошковатые» руды и «рудный» кварц.Порошковые руды практически не требовали обогащения, но в плавку напрямую они не шли, поскольку при высыхании выдувались из доменной печи. Они прибавлялись в качестве 30% добавки к плотным рудам при плавке на Ревдинском заводе.
Комовые руды встречались крупными скоплениями и требовали даже взрывных работ.
Средняя мощность залежи составляла 8-9 метров, в отдельных частях она составляла максимум 15-30 метров.
Карта Елизаветинского рудника по состоянию на 1926 год.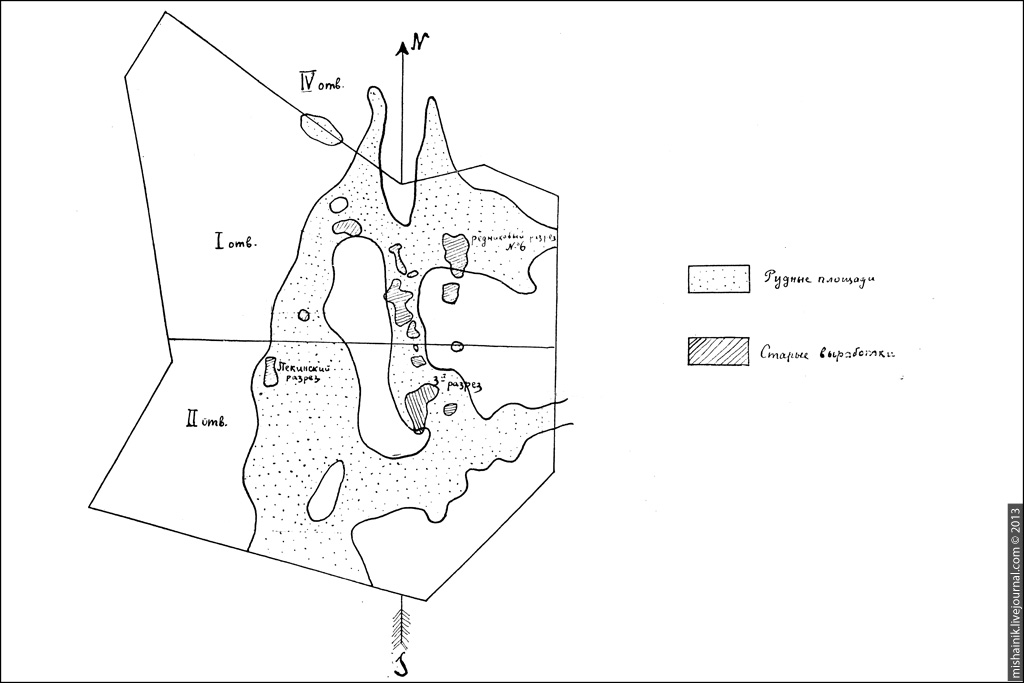
Разработка велась исключительно открытыми работами, достигавшими глубины 25 метров (Карьер №3, Карьер №6 — Редниковый разрез и Карьер №7 — Пекинский разрез), но размер добычи был небольшой, что объяснялось удаленностью заводов-потребителей.
Запасы железных руд месторождения подсчитывались неоднократно и окончательный подсчет запасов выявил цифру более 10 млн. тонн.За годы Великой Отечественной войны месторождение было выработано и после войны рудник был закрыт.
Использованная литература и источники:
Токарев И. Дунито-пироксенитовый массив Уктусских гор (к петрографии окрестностей г. Екатеринбурга). Записки УОЛЕ. Том XXXVIII, Вып.1, 1922.Учебная геологическая практика. / Под ред. В.Н. Огородникова. 2011.
Елизаветинский рудник на карте:
codepeople-post-map require JavaScripturalmines.ru
Нержавеющая сталь
Основу всех сталей составляет железо, они также содержат хром, никель и небольшое количество углерода. Для улучшения литейных, прочностных и других свойств сталей к ним делают добавки. Сталь для зубных протезов содержит 1% титана.Нержавеющая сталь, применяемая в ортопедической стоматологии — многокомпонентный сплав. В него входят железо, хром, никель, углерод, титан и ряд других добавок. Главным компонентом, обеспечивающим коррозионную устойчивость сплава, является хром. Его содержится в сплаве 17—19%. Минимальное содержание хрома, обеспечивающее коррозионную стойкость сплава, должно быть не меньше 12—13%.Для повышения пластичности сплава в него добавляют 8—11% никеля. Присутствие никеля делает сплав ковким, что облегчает обработку давлением. В промышленности виды стали принято обозначать марками. Компоненты, входящие в состав сплава, обозначают буквами: кремний —С, хром—X, никель—Н, титан —T и т. д. Цифрами обозначают процент содержания компонента в сплаве. Первая цифра марки обозначает содержание углерода в десятых долях процента.Наиболее распространенной в зубопротезной практике-является нержавеющая сталь марки 1Х18Н9Т. Этот сплав состоит из 72% железа, 18% хрома, 9% никеля, 0,1% углерода и до 1% титана. В небольшом количестве всегда присутствуют посторонние примеси, среди которых наиболее . нежелательными являются сера и фосфор. Железо с углеродом в сплавах может находиться в различных сочетаниях: в виде химического соединения — карбида железа Fe3C или в виде твердого расплава, когда атомы углерода располагаются в кристаллической решетке между атомами железа. Углерод в сплаве может находиться в свободном состоянии в виде графита. Различные виды связи железа с углеродом наблюдаются при термической обработке стали, ее кристаллизации из расплава.
Встречаются следующие структурные виды связи железа и углерода:
1. Аустенит — твердый раствор углерода в железе, характеризующийся пластичностью, ковкостью сплава при твердости около 200 кгс/см2 по Бринеллю.
2. Феррит — твердый раствор углерода, очень мягкий и пластичный. Его твердость около 80 кгс/мм2 по Бринеллю.
3. Цементит — карбид железа (Fe3C), очень твердый и хрупкий.
4. Перлит — смесь кристаллов цементита и феррита. Получается из аустенита в результате его распада при температуре 723°С.
5. Ледебурит — смесь перлита и цементита, очень , твердый и хрупкий.
Аустенитная структура нержавеющей стали отвечает всем основным требованиям, предъявляемым к зубопротезным материалам, поэтому при термической и механической обработке стали ее стараются в конечном итоге фиксировать в аустенитной структуре.Хром с углеродом также может давать ряд химических соединений — карбидов хрома: Cr4C, Cr3C2, O5C2. Они образуются при термической обработке сплава в температурном интервале 450—850°С.Карбиды образуются по границам кристаллических зерен, что ттриводит к уменьшению количества гнободного хрома в этих зонах, и в связи с этим увеличивается возможность возникновения межкристалмической коррозии.Чтобы уменьшить возможность образования карбидов хрома, в состав нержавеющей стали вводят титан, активнее вступающий в связь с углеродом и образующий карбиды титана. При этом образование корбидов хрома прекращается, и таким образом типі н предотвращает межкристаллическую коррозию стали. Для улучшения жидкотекучести и жаростойкости стали, используемой для литья, в нее вводят 2,5% кремния (сплав ЭИ-95).Нержавеющая сталь нашла широкое применение при изготовлении зубных протезов. Из нее делают различные виды несъемных зубных протезов, металлические части съемных протезов (кламмеры, дуги и т. п.). Нержавеющая сталь аустенитной структуры благодаря пластичности и ковкости хорошо обрабатывается методом давления.
Для изготовления штампованных коронок промышленность выпускает стандартные гильзы. Их получают из листа стали марки 1Х18Н9Т толщиной 0,25—0,3 мм методом холодной штамповки. Следует иметь в виду, что стандартные гильзы из нержавеющей стали имеют разную толщину. Наиболее истонченной частью оказывается область перехода боковых стенок ко дну. Вследствие возникающего при штамповке наклепа структура стали в гильзах оказывается деформированной. Показателем этого является повышенная твердость боковых частей гильзы. Если микротвердость (по Виккерсу) в середине дна составляет 130—150 кгс/мм2, то у боковых стенок она достигает 290 кгс/мм2. Для придания гильзам хорошей ковкости в зуботехнических лабораториях их подвергают отжигу при температуре 1000—1050°С. В настоящее время Ленинградский завод «Медполимер» выпускает 22 размера гильз диаметром 6—16 мм через каждые 0,5 и 18 мм.Из этой же стали выпускают проволоку диаметром 0,6; 0,8; 1,0; 1,2; 1,5 и 2,0 мм для изготовления различных ортодонтических аппаратов, кламмеров, штифтов. Кроме этого, выпускают 2 вида стандартных кламмеров диаметром 1,0 и 1,2 мм.Сталь марок ЭИ-95 и ЭЯ1Т имеет хорошие литейные свойства и применяется для отливки различных деталей зубных протезов. Недостатком ее является относительно большая усадка приглитье (доЗ%), низкий предел прочности (около 30 кгс/мм2), показывающий величину нагрузки, необходимую, чтобы вызвать остаточную деформацию материала.Эту сталь используют и для промышленного изготовления стандартных защиток для фасеток и зубов, которые комплектуют гарнитурами (передние и боковые зубы). Стандартные зубы применяют крайне редко, главным образом в районах, где нет условий для организации индивидуального литья.
| Следующая > |
Следующие статьи:
Предыдущие статьи:
111article-factory.ru
Железо-хром, система - Диаграмма состояни
Системы железо—никель и железо—хром—никель подробно рассмотрены в работе [56]. Сплавы железа с никелем образуют в основном у-твердые растворы. Никель сильно снижает критические точки, фиксирующие превращение у- в а-железо, причем точки на диаграмме состояния, соответствующие превращению а- в у-железо, с увеличением содержания никеля смещаются вверх, а точки, соответствующие превращению у- в а-железо, смещаются вниз. Превращения у —> а при охлаждении и а у при нагреве никелевых и хромоникелевых сталей происходят с большим гистерезисом. [c.158] На сечении диаграммы состояния тройной системы Fe—Сг—Ni при 1100 "С (рис 304) этим сплавам соответствуют двухфазные области a -fv (основа никель или железо-f никель) и a-fv (основа железо), где а -фаза с о. ц. к. решеткой обогащена хромом. При более высоких температурах эти сплавы являются однофазными а (о, ц. к.) в сплавах на основе железа и у (г. ц. к.) в сплавах с высоким содержанием никеля. [c.577]| Рис. 15. Изотермические разрезы диаграмм состояния системы железо—хром— никель а — при [100°С б — при 800° С в — при 400° С | 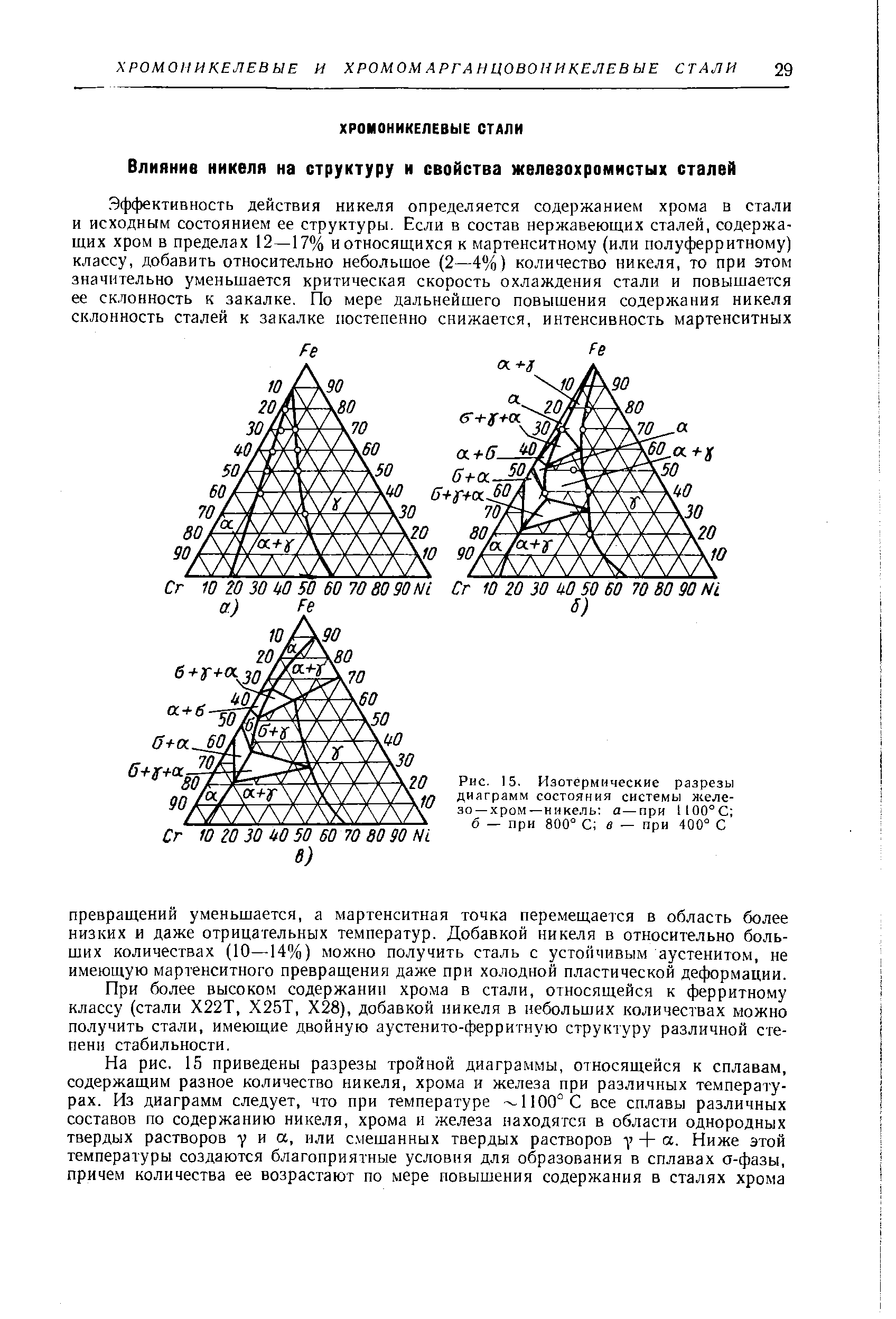 |
Диаграмма состояния системы хром — железо, по данным работы 36], приведена на рис. 9. Хром и железо обладают неограниченной взаимной растворимостью как в твердом, так и в жидком состоянии. Линии ликвидуса и солидуса в системе пересекаются, образуя при 20% Сг температурный минимум, равный 1783°К. [c.24]
Наконец, системы элементов, не образующих между собой ни твердых, ИИ жидких растворов, отнесены к четвертому типу диаграмм состояния (рис. 77, г). В таких сплавах трещины не образуются, как бы ни была низка температура затвердевания более легкоплавкой примеси. При любой разности температур затвердевания обоих элементов в такого рода системах эффективный интервал кристаллизации в идеальном случае равен нулю, а в реальных сплавах определяется концентрацией других элементов. В сварочной ванне, кристаллизующейся в соответствии с диаграммой этого рода (рис. 77, г), образуются дендриты более тугоплавкого элемента, а не смешивающаяся с ним жидкость вытесняется фронтом растущих кристаллов на поверхность сварного шва. Нерастворимы в железе в твердом и жидком состоянии висмут, свинец и серебро. Висмут не растворим также в хроме. [c.196]
| Рис. 1. Диаграмма состояния системы железо—хром | 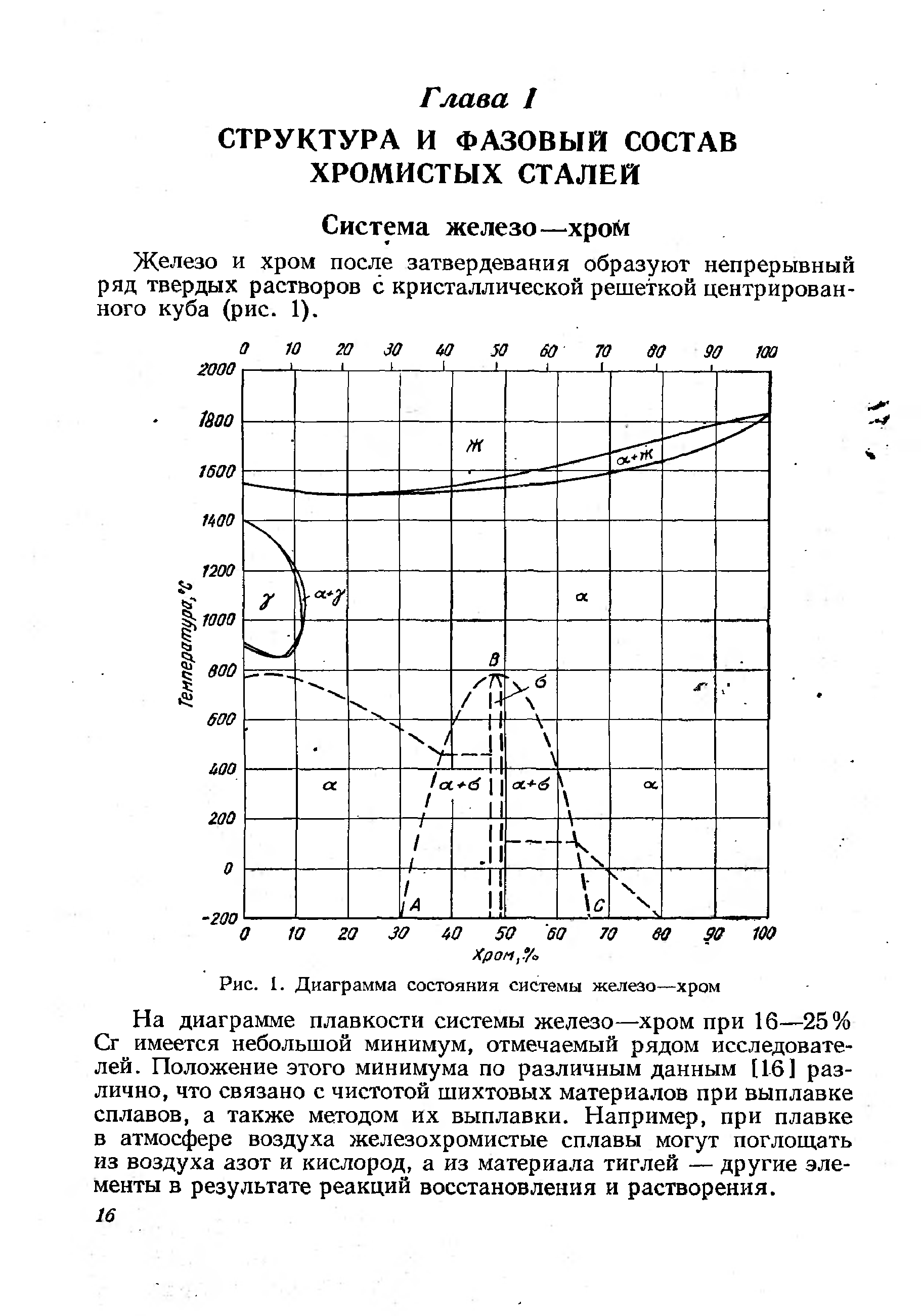 |
| Рис. 123. Диаграмма состояния системы железо — хром—никель при 0,10% С с указанием положения структурных составляющих при быстром охлаждении из области наибольшего распространения аустенита |  |
| Рис. 124. Горизонтальные сечения тройной диаграммы состояния системы железо — хром — никель при 800 и 650°С [190] | ![Рис. 124. Горизонтальные сечения тройной диаграммы состояния системы железо — хром — никель при 800 и 650°С [190]](/800/600/http/mash-xxl.info/pic1/168159000241192136007029069217228183053180254031.png) |
Критические точки технических сортов стали (даже углеродистой), содержащих примеси, не совпадают обычно по температуре с точками диаграммы состояний системы железо — углерод. Повышенное содержание марганца или никеля позволяет снизить температуру нагрева для закалки стали, а кремний, хром и вольфрам, наоборот, требуют ее повышения. [c.182]
Диаграммы состояния типа железо — цементит (с эвтектикой и эвтектоидом) системы циркония с серебром, бериллием, кобальтом, хромом, медью, железом, марганцем, молибденом, никелем, ванадием, вольфрамом, водородом. [c.443]
На рис. 2 приведена диаграмма состояния системы Ре—Сг (без углерода). Хром стабилизирует -железо и сужает область существования у-железа. При содержании хрома 12—13 7о у-область замыкается, образуя петлю. [c.13]
| Рис. 91. Диаграмма состояний сплавов системы железо — хром — углерод при содержании хрома а-12%. б-т | 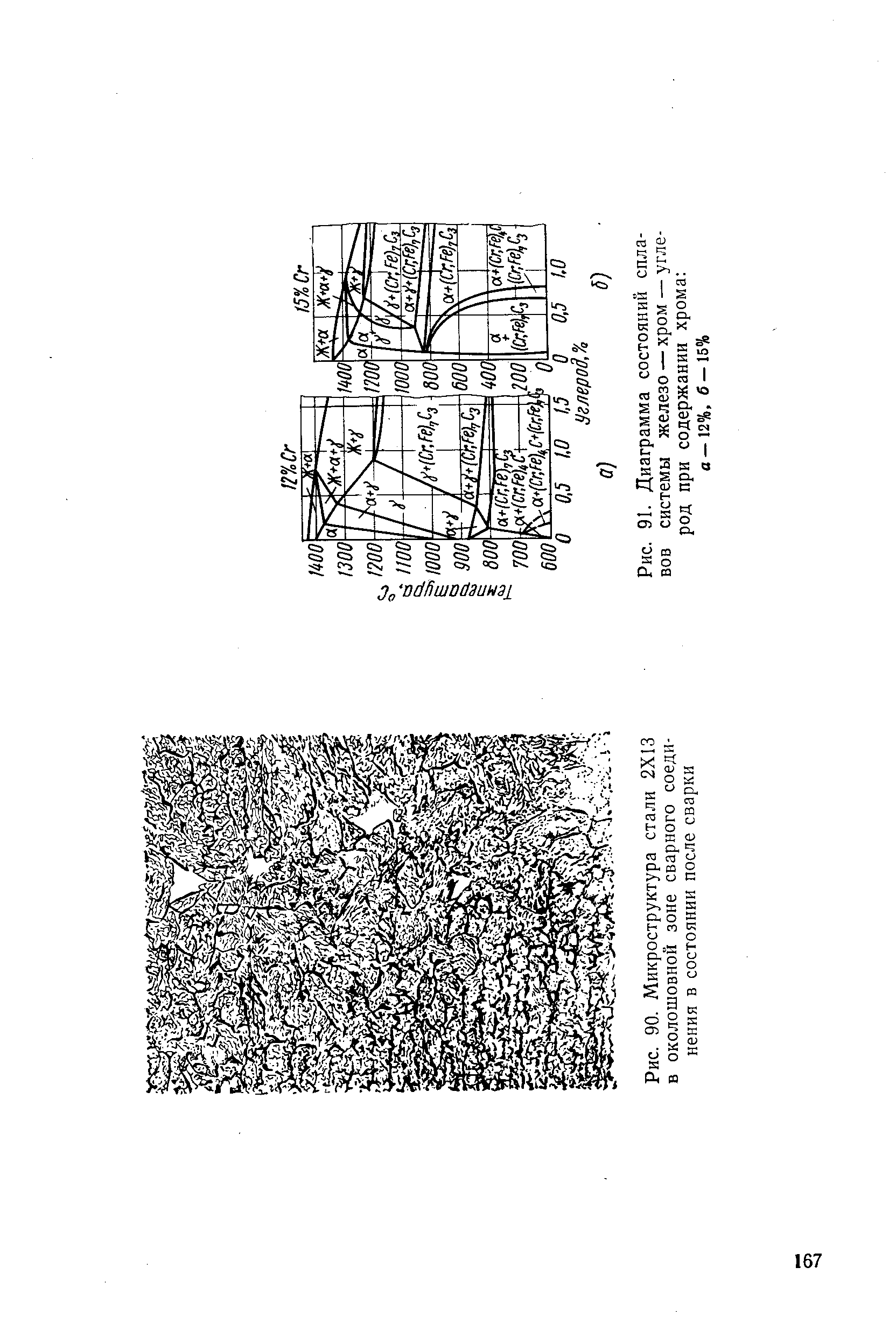 |
Это же относится и к исследованиям, планируемым для контроля однородности конечного продукта. Учет физико-химических и физико-механических особенностей исходного материала часто позволяет уменьшить объем эксперимента, обеспечивая вместе с тем контроль наиболее слабых звеньев цепи. Во многих случаях оказывается возможным отказаться от измерения неоднородности всех аттестуемых компонентов и сосредоточить усилия на доказательном подтверждении качества материала на основе контроля распределения компонентов — индикаторов однородности [1, 59, 60]. Ими могут служить наи- более ликвирующие или летучие компоненты, сравнительно труднее растворяющиеся, хуже прочих дробящиеся, образующие обособленные составляющие и т. д. Иногда наблюдалась существенная неоднородность распределения компонента, отнесенного к числу благополучных , исходя из физико-химических особенностей (в работе [6] — исходя из диаграммы состояния системы хром — железо ). Это связано, по-видимому, с неполным учетом всех обстоятельств в приведенном примере — возможности неравномерного распределения хрома, вводимого в металлический расплав в виде тугоплавкого ферросплава, карбидной ликвации вследствие наличия углерода в системе и др. Подобные случаи свидетельствуют не против уче- та закономерностей образования неоднородности, а о том, что он должен быть максимально полным и всесторонним. [c.132]
Анализируя диаграмму состояния железо—хром, Н. Т. Гудцов считал, что ось кривой, ограничивающей у-область, не совпадает с направлением оси температур и пересекает ось концентраций при 50% (ат.) хрома. Делается предположение, что на поле диаграммы, по другую сторону оси кривой, должна быть другая, встречная ветвь гиперболы, ограничивающая область сплавов, отличающихся по своему кристаллическому строению от а-области. Таким образом, Н. Т. Гудцов считает, что области а-фаз закономерно должны встречаться во всех системах сплавов с суженной у-об- [c.582]
На диаграмме состояния системы железо— хром (рис. 48), построенной по результатам термических, микроскопических, дилатометрических и рентгеноструктурных [c.334]
| Рис. 49. Участок диаграммы состояния системы железо — хром [31 | 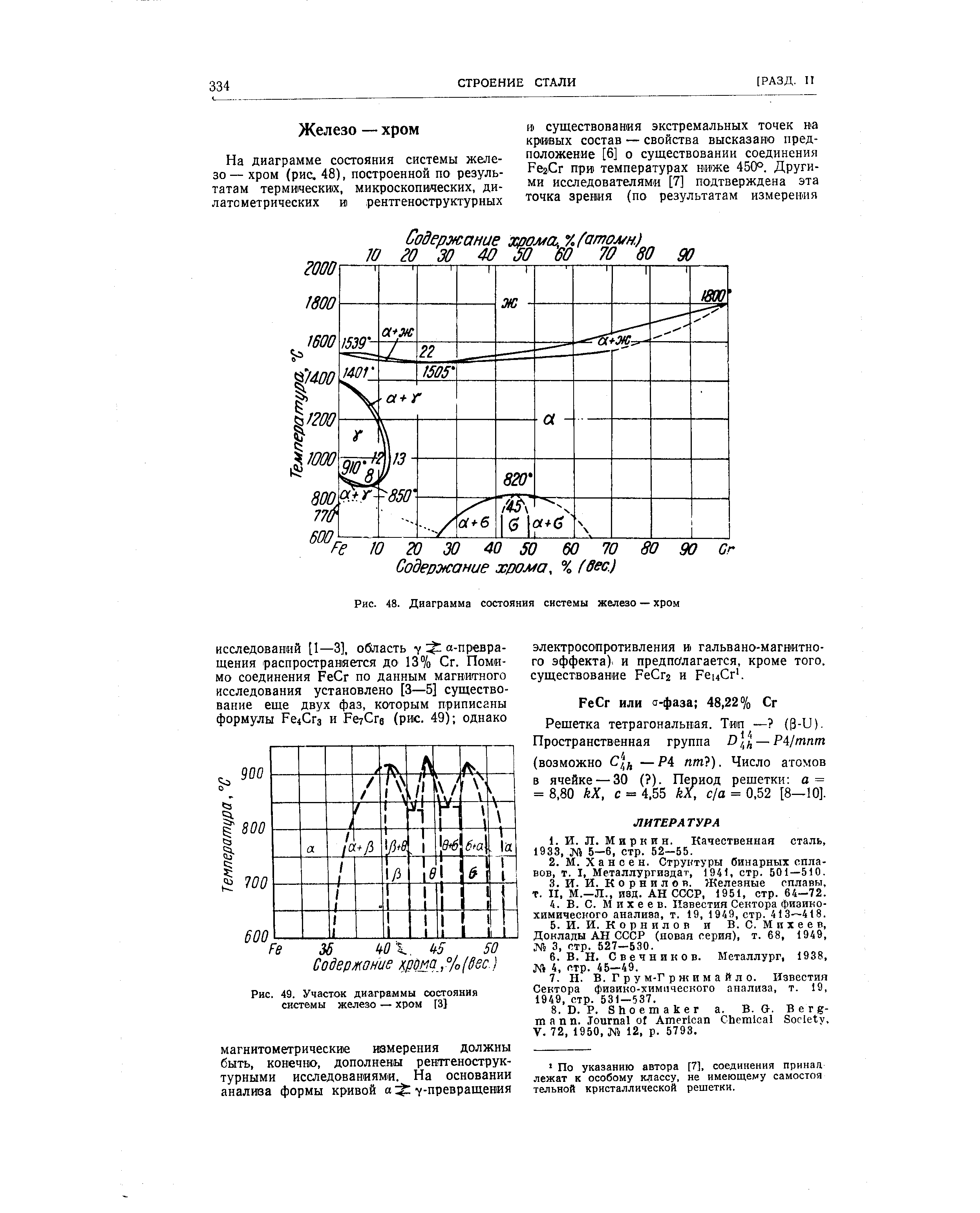 |
Как следует из диаграммы состояния системы железо — хром (рис. 1.3), безуглеродистые железохромистые сплавы имеют замкнутую [c.26]
| Рис. 1.3. Диаграмма состояния системы железо — хром, иллюстрирующая влияние углерода на смещение у-области. | 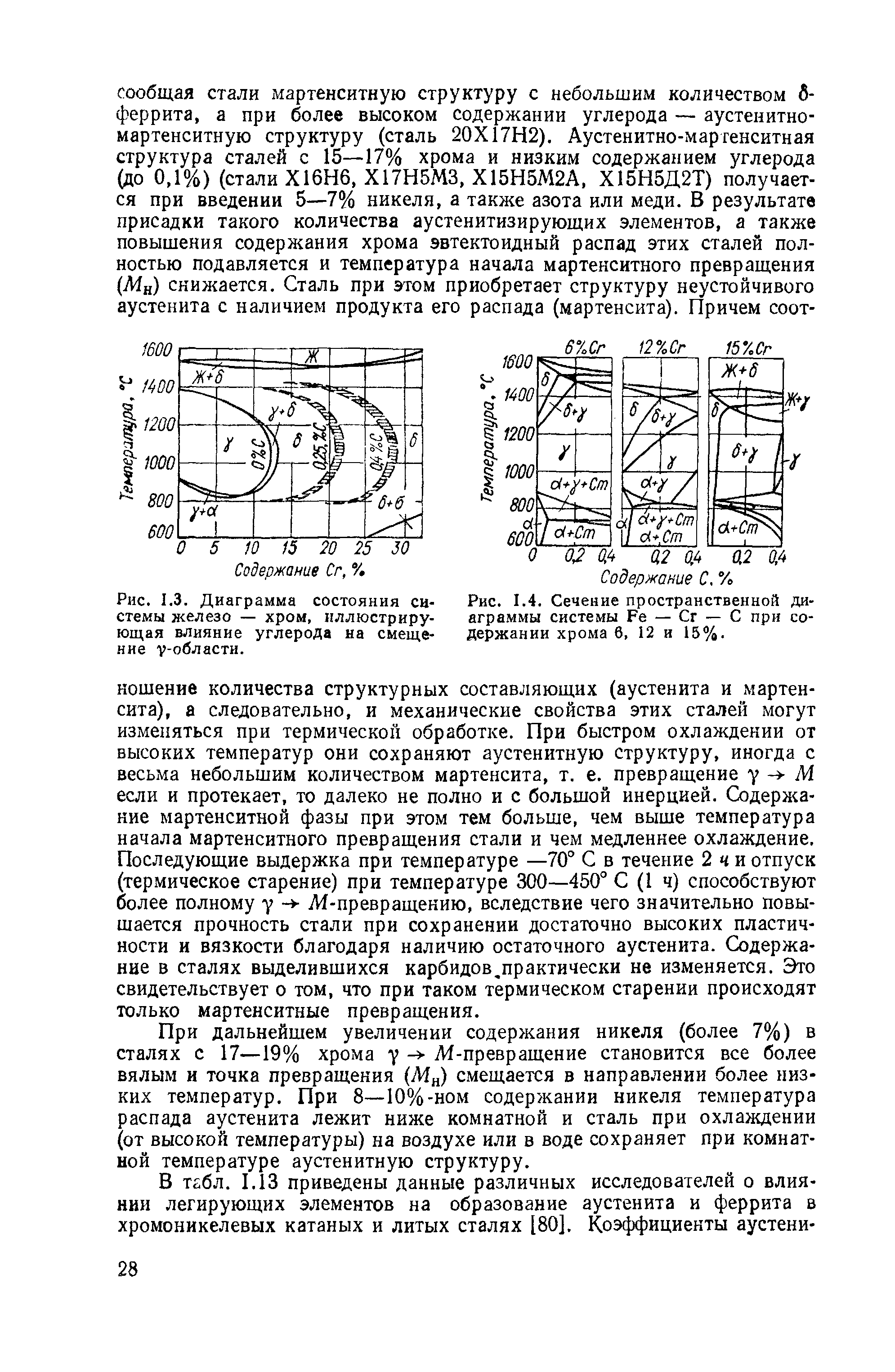 |
Железо и хром имеют одинаковый тип кристаллической решетки объемноцентрированного куба (а-решетка) с близкими параметрами и дают непрерывный ряд твердых растворов. Диаграмма состояния для системы Ре—Сг приведена на рис. 224. [c.474]
Железо-углерод, система — Диаграмма состояния 3 — 320, 360 Железоуглеродистые сплавы — см. Сплааы железоуглеродистые Железо-хром, система — Диаграмма состояния [c.77]
В системе тройных сплавов железо — углерод — хром, как показывают диаграммы состояния (фиг. 181), присутствуют следующие сложные карбиды 1)(РеСг)зС 2) (РеСг), 3) (РеСг) и затем а-фаза и а-твердый раствор хрома в железе Стедовательно, в стали хром [c.286]
Легирующие элементы оказывают большое влияние на точку Л,, соответствующую температуре перехода перлита в аустенит (рис. 93, а). Никель и марганец снижают температуру А , а Т1, Мо, 31, У и другие элементы повышают температуру Л1 (см. рис, 93, а). Легирующие элементы уменьшают эвтектондную концентрацию углерода (рис. 93, б) к предельную растворимость углерода в аустените, сдвигая точки 5 к на диаграмме состояния Ре—С влево. Как видно из рис. 94, где приведены вертикальные разрезы тройной диаграммы состояния Ре—Мп—С и Ре—Сг—С, перитектическое, эвтектическое и эвтектоидное превращения протекают не при постоянной температуре, как в двойных системах, а в некотором интервале температур. В системе р е—Мп.—С у-фаза с увеличением содержания марганца существует и в области более низких температур. В системе Ре—Сг—С с возрастанием концентрации хрома область существования у-ф>ззь( сужается. Состав карбидной фазы (К) в марганцовистых сталях соответствует соединению (РеМп)8С, в котором часть атомов железа. замещена атомами марганца. В хромистых сталях образуются (Ре, Сг)зС и специальные хромистые карбиды, состав и структура которых зависят от содержания углерода и хро.ма. При низком содержании углерода и высоком содержании хрома образуются ферритные стали, не претерпевающие полиморфного превращения (рис. 94, б). [c.137]
Установлено, что по структуре и фазовому составу электроосажденных сплавов железо—никель—хромовые сплавы, полученные из сульфамидного электролита, отличаются от нержавеющих сталей. Электроосажденные сплавы имеют мелкодисперсное строение и представляют собой преимущественно а-фа-зу. Термообработка при температуре 800—850° С в защитной атмосфере вызывает укрупнение зерен и изменение фазового состава сплава в соответствии с диаграммой состояния системы железо—никель—хром. Табл. 1, рис. 4, библ. 8. [c.124]
Фазовые превращения расс.чатриваемых сплавов имеют много общего с присущими системе железо — хром. На рис. 4-1 приведена диаграмма состояния Ре-Сг [4-7] с учетом данных [4-8] по исследованию ее низкотемпературной части. В высокотемпературной области имеется непрерывный ряд а (ОЦК)-твердых растворов с пределами значений параметров решетки, определяемыми л4елезо. 1 и хро-мо.м (0,260 и 0,278 нм). На диаграмме состояния приведена концентрационная зависимость точки Кюри а-твердого раствора. В этой системе наблюдается область ГЦК. При те.мпературе ниже 820°С при молярном содержании Сг 16—71% (массовом 11,5—69,5%) в струк-гуре появляется промежуточная а-фаза — хрупкая немагнитная составляющая. Это интерметаллическое соединение РеСг почти эквиатом ного состава, растворяющееся в а-фазе. Элементарная ячейка а-фазы имеет тетрагональную симметрию периоды решетки а= = 0,879 нм, с=0,455 нм. Выпадение [c.196]
ТИХ]), т.е. в районе неравновесного солидуса (см. рис. 10.11). Склонность к трещинам возрастает при увеличении ТИХ], снижении пластичности в ТИХ], а та1сже при росте темпа растягивающих деформаций в ТИХ), совместно приводящих к исчерпанию пластичности (8 > бщт) и образованию трещин. Эти фаеторы структурно-чувствительны. Структура металла шва и ЗТВ зависит от химического состава и теплофизических условий кристаллизации. Роль химического состава в первом приближении оценивают по псевдобинарным диаграммам состояния системы Ре - Сг - № при постоянном содержании железа (рис. 10.12). Согласно этой диаграмме в стабильно аустенитных сталях с соотношением СГэкв/Н экв [c.53]
Как видно из диаграммы состояния системы железо — хром (рис. 192), при содержании хрома около 12,8% область твердых растЕоров 7-железа замыкается, а при большем содержании хрома образуется а-железо. Под влиянием углерода в железохромистых сталях область 7-железа расширяется и замыкается при более высоком содержании хрома (рис. 193). Однако, в то же время, хром снижает концентрацию углерода в перлите и в насыщенном аустените. [c.339]
| Фиг. 162. Диаграмма состояния системы железо — хром (Вайн и Эборн). | 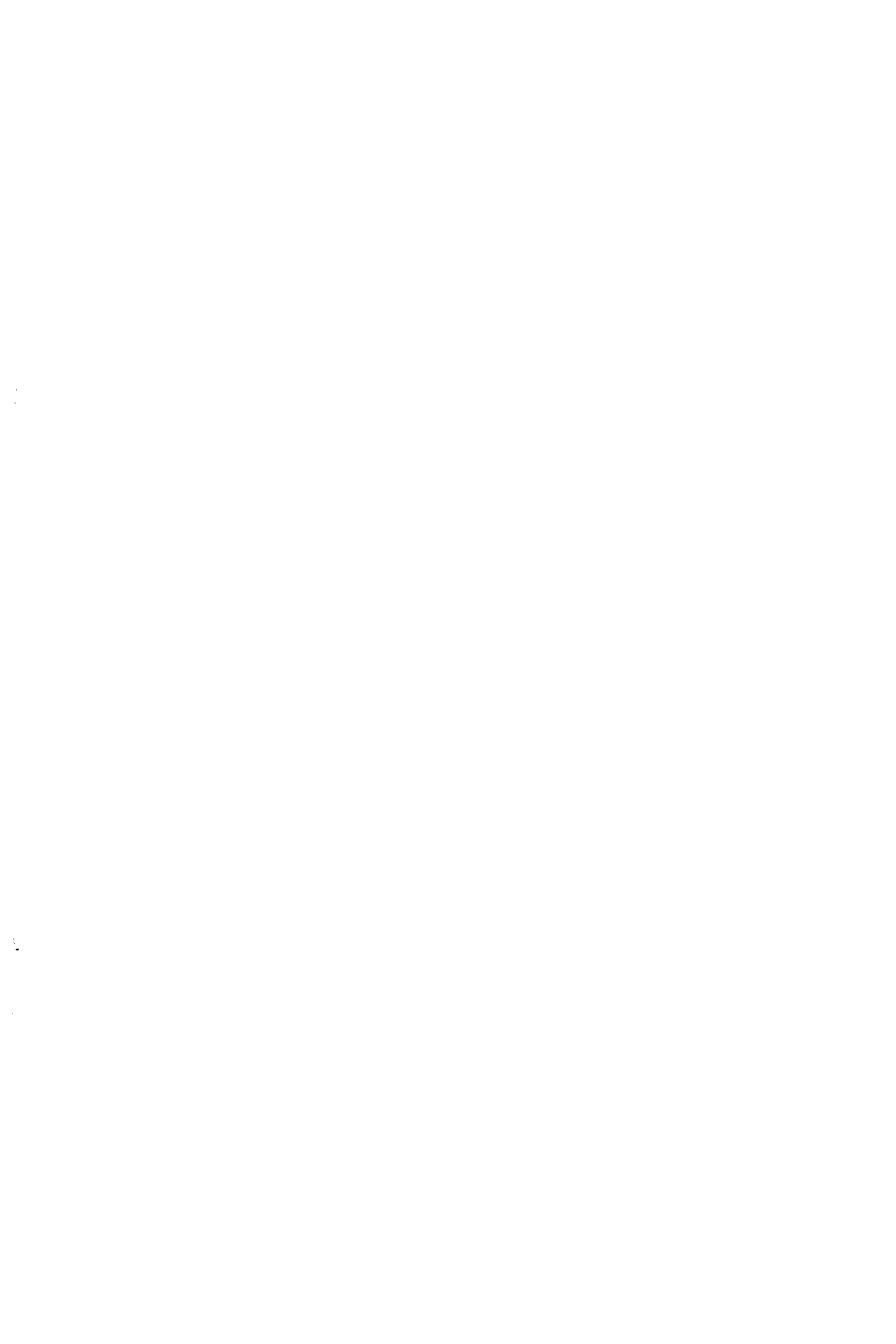 |
Это главным образом элементы VIII группы, у которых быстро заполняется (лс ) -электронная. цодоболочка. Поскольку атомы этих элементов близки к модели твердых шаров, мы можем дать вероятное объяснение того, как они способствуют образованию плотноупакованной структуры у-ж леза. Равновесные диаграммы состояния с замкнутой у-областью характеризуют фазовое равновесие в системах железа с ванадием, ниобием, танталом, хромом, молибденом и вольфрамом. Эти элементы имеют кубическую объемноцентрированную структуру, которая весьма стабильна и характеризуется высокой температурой плавления. Это, естественно, наводить на мысль о том, что электронное строение атомов этих элементов благоприятствует образованию кубической объемноцентрированной структуры также и в сплавах с железом. Это довольно наглядный пример, однако для полного объяснения наблюдаемого в сплавах на основе железа вида диаграмм состояния его совершенно недостаточно, поскольку равновесные диаграммы состояния с у-областью петлеобразного типа наблюдаются также в системах железо—алюминий и железо—кремний несмотря на то, что алюминий имеет структуру гранецентрированного куба, а кремний— структуру алмаза. [c.188]
На рис. 69—71 схематически представлена изометрическая проекция тройной диаграммы состояния железо—хром—углерод, а также некоторые ее плоские сечения. Эта диаграмма ограничена тремя двойными диаграммами (Ре—Сг, Ре—С и Сг—С). Система железо—хром характеризуется наличием при низких температурах а-фазы, образование которой идет довольно быстро только после деформации, а-хром имеет объемноцентрированную кубическую решетку н при высоких температурах образует саб-железом непрерывный ряд твердых растворов. На диаграмме хром—углерод имеется три карбида СгздСв, СГ27С3 и Сг Са. В простых сплавах последний, по-видимому, не образуется. Первые два карбида могут содержать в твердом растворе большое количество других элементов. [c.73]
mash-xxl.info
Система железо — хром — никель
Расчеты температур процесса алюминотермического восстановления окислов железа, хрома, ванадия, никеля и некоторых других металлов позволяют установить в интервале температур 2300—3300 К следующую зависимость. максимальной температуры процесса от величины теплового эффекта реакции восстановления (>И, отнесенной I г-атому шихтовых материалов (в системе СИ) [c.68]Положение фазовых областей в системе железо — хром — марганец —никель для медленно охлажденных сплавов приведено на рис. 10 [17]. [c.31]
Были сделаны попытки изыскания жаропрочных сплавов на основе системы железо—никель (без хрома), но они не увенчались успехом. [c.222]
| Рис. 247. Влияние марганца и никеля, а также небольших количеств углерода и азота на положение границы, отделяющей 7-область, в системе железо—хром—никель—марганец [199] | ![Рис. 247. Влияние марганца и никеля, а также небольших количеств углерода и азота на положение границы, отделяющей 7-область, в системе железо—хром—никель—марганец [199]](/800/600/http/mash-xxl.info/pic1/122070048148180063050187016002252200003101030020.png) |
Системы железо—никель и железо—хром—никель подробно рассмотрены в работе [56]. Сплавы железа с никелем образуют в основном у-твердые растворы. Никель сильно снижает критические точки, фиксирующие превращение у- в а-железо, причем точки на диаграмме состояния, соответствующие превращению а- в у-железо, с увеличением содержания никеля смещаются вверх, а точки, соответствующие превращению у- в а-железо, смещаются вниз. Превращения у —> а при охлаждении и а у при нагреве никелевых и хромоникелевых сталей происходят с большим гистерезисом. [c.158]
Система железо — никель — хром. Из этой группы только два типа могут обладать хорошей устойчивостью к окислению [c.56]
Критические точки технических сортов стали (даже углеродистой), содержащих примеси, не совпадают обычно по температуре с точками диаграммы состояний системы железо — углерод. Повышенное содержание марганца или никеля позволяет снизить температуру нагрева для закалки стали, а кремний, хром и вольфрам, наоборот, требуют ее повышения. [c.182]
Металлы широко распространены в природе из более чем 100 известных в настоящее время химических элементов периодической системы элементов Менделеева 71 являются металлами. Наиболее распространенными в технике металлами являются железо, медь, алюминий, цинк, никель, хром, марганец, вольфрам, магний, свинец, олово и др. В последнее время все большее распространение получают титан, бериллий, ниобий, цирконий, германий, тантал и др. Металлы обладают определенным сочетанием химических, физико-механических и технологических свойств, отличающих их от других твердых тел — неметаллов или металлоидов. [c.95]
Металлы, занимающие в периодической системе- элементов места, смежные с железом и имеющие близкие к железу свойства (в частности — атомные радиусы), склонны к образованию в железе растворов почти идеального типа. Такими металлами являются хром и марганец, имеющие 24-й и 25-й порядковые номера системы элементов, и кобальт и никель, стоящие по другую сторону от железа и. занимающие 27-е и 28-е й еста в ней. Относительно близкие к железу свойства имеют также молибден, вольфрам и ванадий. [c.190]
Вещества, оседающие в системе парогенератора, образуют плотные и трудно удаляемые отложения, в составе которых обычно преобладают окислы железа, соединения меди, цинка и незначительные количества хрома, марганца, никеля, кальция и магния. Все эти вещества, за исключением кальция и магния, являются продуктами коррозии конструкционных материалов, т. е. котельной стали и латуни. [c.170]
Система железо — никель — хром была предметом многих исследований (см. основные работы [1—8] обзор работ при 1955 г дан в работе [9]). Здесь приведены политермические разрезы системы при постоянном содержании никеля [7, 8] и при постоянном содержании железа [4], изотермические разрезы [6] и проекции поверхностей ликвидуса и солидуса [3] (рис. 127—137). [c.559]
Большое распространение нашли нержавеющие стали тройной системы Железо — хром — никель без присадок и с добавками титана, ниобия, мо- [c.25]Из указанных на рис. 12 и 13 диаграмм следует, что в системе железо— хром — никель содержание 18—19% хрома и 8—10% никеля при небольшом содержании углерода является оптимальным составом для получения практически пригодного сплава. Однако хромоникелевая сталь указанного состава при определенных условиях проявляет неустойчивость, которая в значительной степени вызывается влиянием углерода и режимом термической обработки. [c.27]
Хром применяется в жаростойких сплавах в количестве 2—35 /о- Из диаграммы состояния системы железо — хром ясно, что мартенситные стали содержат 2—14 /о Сг, а ферритные 14—35 /о Сг. Однако эти границы могут сдвигаться из-за присутствия других элементов. Например, элементы, способствую-ш,ие устойчивости аустенита (углерод, азот, марганец и никель), расширяют область мартенситных сталей в сторону большего содержания хрома, в то время как кремний, вольфрам, молибден, титан, ниобий и алюминий сужают ее, снижая верхний предел содержания хрома. [c.669]
Растворно-осадительный механизм роста, приводящий к необратимому увеличению объема вследствие развития диффузионной пористости, изучен применительно к графи-тизированным сплавам железа, никеля и кобальта. С углеродом указанные металлы образуют растворы внедрения и сильно различаются от него коэффициентами диффузии. Большое различие в диффузионной подвижности имеет место и в сплавах других металлов и неметаллов. Но при гермоциклировании этих сплавов, когда многократно повторяются процессы растворения и выделения избыточных фаз, накопление пор не обнаруживается. Число изученных систем невелико, но по крайней мере в микроструктуре термоциклиронанных твердых растворов на основе хрома и никеля, меди и титана, алюминия и меди, алюминия и кремния и некоторых других поры не выявлены. В указанных системах. компоненты образуют растворы замещения ч в них реализуется вакансионный механизм диффузии. [c.98]
Отрицательное влияние ниобия на горячеломкость аустенитных швов тесно связано с характером его растворимости в никеле и железе. Ниобий, как и титан, способен давать легкоплавкую эвтектику с каждым из указанных элементов [22, 33]. В табл. 34 приведены данные о предельной растворимости и температуре эвтектики для бинарных сплавов никеля и железа с ниобием и титаном. Согласно нашим представлениям о природе кристаллизационных трещин, можно ожидать, что в тех случаях, когда шов содержит относительно мало никеля, т. е. представляет собой аустенитную сталь, наибольшую опасность должен представлять ниобий, а не титан. В пользу такого утверждения говорит относительно более низкая растворимость ниобия в лнизкая температура эвтектики в системе Fe—Ni по сравнению с эвтектикой Fe—Ti. Наоборот, при сварке высоконикелевых аустенитных сталей и сплавов на никелевой основе следует ожидать отрицательного действия скорее титана, а не ниобия. В пользу этого утверждения говорит относительно более низкая температура эвтектики в системе N1—Ti по сравнению с эвтектикой Ni—Nb. Практика сварки аустенитных сталей, в общем, подтверждает эти предположения. При сварке сталей типа 18-8 ниобий опаснее титана. При сварке сталей с соотношением содержаний хрома и никеля, равным или меньшим единицы, например при сварке стали ЭИ696 (Х10Н20Т2), большую опасность представляет титан, а не ниобий. [c.209]
В тройной - системе железо—хром—марганец действие марганца на изменение положения критических точек аналогично никелю, что видно из данных, приведенных на рис. 245. Однако эффективность влияния марганца на расширение 7-области значительно меньше никеля и зависит от содержания хрома [354— 356]. В низкоуглеродистых хромомарганцевистых сплавах при содержании более 15% Сг получить однофазную аустенитную сталь не представляется возможным, так как граница, отделяющая 7-область, идет выше 15% Мп параллельно оси марганца. [c.417]
Сложнолегирсванные сплавы железа на основе системы железо—хром обладают высокой жаропрочностью и жаростойкостью. Они служат основой коррозионно-стойких сталей. Главный легирующий компонент — никель. [c.419]
Установлено, что по структуре и фазовому составу электроосажденных сплавов железо—никель—хромовые сплавы, полученные из сульфамидного электролита, отличаются от нержавеющих сталей. Электроосажденные сплавы имеют мелкодисперсное строение и представляют собой преимущественно а-фа-зу. Термообработка при температуре 800—850° С в защитной атмосфере вызывает укрупнение зерен и изменение фазового состава сплава в соответствии с диаграммой состояния системы железо—никель—хром. Табл. 1, рис. 4, библ. 8. [c.124]
Анодная защита в отличие от катодной применяется только в тех случаях, когда металл или сплав изделия легко переходит в пассивное состояние, которое должно сохраняться в окислительных средах. К легко пассивирующим металлам относятся хром, никель, титан, цирконий и другие и сплавы системы железо — цементит, содержащие эти металлы. Анодная защита осуществляется присоединением к конструкции положительного полюса источника постоянного тока (анода), а катоды помещаются около поверхности изделия. При анодной защите резко снижается скорость коррозии при минимальном расходе энергии, так как сила тока очень мала. Анодную защиту применяют для предохранения изделий, соприкасающихся с сильно агрессивной средой. Очень часто защищают изделия, изготовленные из титана, циркония, легированных сталей, например 10Х18Н9Т (рис. 31), углеродистых сталей. При таком методе увеличивается срок службы аппаратуры. Анодную защиту также часто используют с целью снижения загрязнений агрессивной среды продуктами коррозии. [c.130]
ТИХ]), т.е. в районе неравновесного солидуса (см. рис. 10.11). Склонность к трещинам возрастает при увеличении ТИХ], снижении пластичности в ТИХ], а та1сже при росте темпа растягивающих деформаций в ТИХ), совместно приводящих к исчерпанию пластичности (8 > бщт) и образованию трещин. Эти фаеторы структурно-чувствительны. Структура металла шва и ЗТВ зависит от химического состава и теплофизических условий кристаллизации. Роль химического состава в первом приближении оценивают по псевдобинарным диаграммам состояния системы Ре - Сг - № при постоянном содержании железа (рис. 10.12). Согласно этой диаграмме в стабильно аустенитных сталях с соотношением СГэкв/Н экв твердого раствора до полного исчезновения жидкой фазы. При большем соотношении Сгэкв/Н1экв твердые фазы аустенит и междендритный эвтектический феррит, который образуется из последних порций жидкой фазы, обогащенной хромом и никелем по ликвационному механизму. [c.53]
Большое практическое значение имеет тройная система железо — хром — никель, так как хромоникелевые стали с малым содержанием углерода ширс/ко применяются на практике. На рис. 68 показана модель системы железо — хром — никель. [c.342]
Сравнивая распределение фаз при комнатной температуре, изображенное на соответствующих треугольниках концентраций моделей Fe — В — С и Fe — Сг — Ni, легко заметить, как в двухфазную область (а + у) в системе железо — хром — никель вклинивается область (а+7). Так как эти области не могут соприкасаться (см. общую теорию фазовога равновесия), то с двух сторон между ними располагаются трехфазные области (а + у-Ьа)- Чтобы проверить правильность построения такой модели, следует сделать вертикальные и горизонтальные сечения изучаемой части диаграммы. [c.342]
Применение прецизионных сплавов системы железо—никель обусловлено их особыми физическими свойствами. При легировании железа никелем коррозионная стойкость возрастает с увеличением содержания в них никеля. Сплавы Fe—Ni будут более устойчивы, чем обычные углеродистые стали, в атмосферных условиях, в морской воде, а также в слабых растворах солей, кислот и щелочей. В то же время нельзя не отметить, что в этих сплавах наличие железа >20 % способствует появлению на поверхности металла точечной коррозии, например в растворах, содержащих иоиы I-, Вг , 1 и 10J". Аналогичные сплавы подвержены коррозионному растрескиванию в растворах NaOH и КОН, особенно в присутствии хлористых солей. Легирование железа, например хромом, заметно повышает коррозионную стойкость сплава вследствие перевода его в пассивное состояние. Резкое повышение коррозионной стойкости наблюдают при содержании в сплавах 12—13 % Сг. Такое количество хрома является минимальным для сплавов, которые будут коррозиоиностойкими в окислительных средах и в атмосферных условиях. Увеличение содержания хрома >13% приводит к дальнейшему повышению коррозионной стойкости сплава. [c.160]Применительно к многослойным металлическим покрытиям можно следующим образом пользоваться теорией многоэлектродного элемента Ч Пусть основной металл (железо) последовательно покрыт цинком, никелем и хромом, причем в интересующей нас среде цинк является наиболе электроотрицательным из этих металлов, а хром наименее отрицательным. Тогда полюсность основного металла в данной системе определяется следующим выражением [c.331]
mash-xxl.info