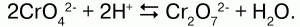Доклад: Хром 2. Хром доклад
Доклад - Хром - Химия
/>/>/>/>
Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил:Гуляева Т.А.
КАРАГАНДА2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
/> /> Введение.К металлам побочных подгрупппериодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома,марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общиехарактеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы —хром Cr, молибден Мо и вольфрам W. Хром возглавляет побочную подгруппу 4группы. Его электронная формула +24Cr 1s2|2s22p6|3s23p63d5|4s1
На внешнем энергетическомуровне атомов хрома и молибдена содержится по одному электрону, вольфрама — дваэлектрона, что обусловливает металлический характер этих элементов и отлично отэлементов главной подгруппы. В соответствии с числом валентных электронов онипроявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общейформулы h3RO4.Сила кислот закономерноснижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо,хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хромапроявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединениявысшей степени окисления, которые во многом весьма похожи на соответствующиесоединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера вподгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390°С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитейв электрических лампочках накаливания.
Металлы подгруппы хрома вобычных условиях весьма устойчивы к воздействию воздуха и воды. При нагреваниивзаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием идр. Известны их многочисленные сплавы с другими металлами. Сплавы и самиметаллы — весьма ценные материалы современной техники.
По физическим и химическимсвойствам молибден и вольфрам сходны между собой и несколько отличаются отхрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметнопонижается.
/>/>Нахождение в природе.Хром встречается ввидесоединений в различных минералах. Наиболее распространен минерал хромит, илихромистый железняк FeCr204,богатые месторождениякоторого имеются на Урале и в Казахстане. Массовая доля хрома в земной коресоставляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г.Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень солянойкислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся беломосадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудникиописал академик П. С. Паллас. «Березовские копи, — писал он, — состоят изчетырех рудников, которые разрабатываются с 1752 года. В них наряду с золотомдобываются серебро и свинцовые руды, а также находят замечательный красныйсвинцовый минерал, который не был обнаружен больше ни в одном другом рудникеРоссии. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари),тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минералабывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошокона дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, былинайдены огромные залежи хромита — основного промышленного сырья дляпроизводства феррохрома. В годы войны на базе этого месторождения был построенАктюбинский ферросплавный завод, который впоследствии стал крупнейшимпредприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположенобольшое число месторождений этого металла: Сарановское, Верблюжьегорское,Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистыхруд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии,на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такиепромышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия,совершенно лишены хромового сырья, а США и Канада располагают лишь оченьбедными рудами, практически не пригодными для производства феррохрома. Всего жена долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским краснымсвинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этогоминерала был в конце XVIII века привезен Палласом в Париж. Крокоитомзаинтересовался известный французский химик Луи Никола Воклен. В 1796 году онподверг минерал химическому анализу. «Все образцы этого вещества, которыеимеются в нескольких минералогических кабинетах Европы, — писал Воклен в своемотчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника.Раньше рудник был очень богат этим минералом, однако говорят, что несколько летназад запасы минерала в руднике истощились и теперь этот минерал покупают навес золота, в особенности, если он желтый. Образцы минерала, не имеющиеправильных очертаний или расколотые на кусочки, годятся для использования их вживописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся навоздухе… Красивый красный цвет, прозрачность и кристаллическая формасибирского красного минерала заставила минералогов заинтересоваться егоприродой и местом, где он был найден; большой удельный вес и сопутствующая емусвинцовая руда, естественно, заставляли предполагать о наличии свинца в этомминерале...».
Один из друзей Воклена предложил емуназвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразногоцвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входитво многие термины, не связанные с элементом хромом: слово «хромосома»,например, в переводе с греческого означает «тело, которое окрашивается»; дляполучения цветного, изображения пользуются прибором хромоскопом; фотолюбителямхорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования ватмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилосьпредложенное название, поскольку открытый им металл имел скромную серую окраскуи как будто не оправдывал своего имени. Но друзья все же сумели уговоритьВоклена и, после того как французская Академия наук по всей формезарегистрировала его открытие, химики всего мира внесли слово «хром» в спискиизвестных науке элементов.
Свое название хром получил от греческогослова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
/>/>Получение.Сr2О3+ 2Аl = Аl2О3 +2Сr
Металлический хром получаюттакже электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ.Растертый в порошок крокоит он поместил в раствор углекислого калия ипрокипятил. В результате опыта ученый получил углекислый свинец и желтыйраствор, в котором содержалась калиевая соль неизвестной тогда кислоты. Придобавлении к раствору ртутной соли образовывался красный осадок, после реакциисо свинцовой солью появлялся желтый осадок, а введение хлористого оловаокрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинцаВоклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовыйангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокойтемпературы. Когда опыт был закончен, ученый обнаружил в тигле множество серыхсросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество.Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой рудыпоступает сегодня на ферросплавные заводы, где выплавляются различные сортаферрохрома и металлического хрома.
Впервые феррохром был получен в 1820 годувосстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854году удалось получить чистый металлический хром электролизом водных растворовхлорида хрома. К этому же времени относятся и первые попытки выплавитьуглеродистый феррохром в доменной печи. В 1865 году был выдан первый патент нахромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыгралэлектрический ток, точнее электротермический способ получения металлов исплавов. В 1893 году французский ученый Муассан выплавил в электропечиуглеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производстворазвивалось черепашьими темпами. Мизерные количества ферросилиция иферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегуреки Сатки (Южный Урал) был построен маленький электрометаллургический завод«Пороги», который стал производить феррохром, а затем и ферросилиций. Но обудовлетворении нужд своей промышленности не могло быть и речи: потребностьРоссии в ферросплавах приходилось почти полностью покрывать ввозом их из другихстран.
/>/>Физические свойства.Хром обладает всеми характерными свойствами металлов —хорошо проводит тепло, почти не оказывает сопротивления электрическому току,имеет присущий большинству металлов блеск. Любопытна одна особенность хрома:при температуре около 37°С он ведет себя явно «вызывающе» — многие его физическиесвойства резко, скачкообразно меняются. В этой температурной точке внутреннеетрение хрома достигает максимума, а модуль упругости падает до минимальныхзначений. Так же внезапно изменяются электропроводность, коэффициент линейногорасширения, термоэлектродвижущая сила. Пока ученые не могут объяснить этуаномалию.
Даже незначительные примеси делают хром очень хрупким,поэтому в качестве конструкционного материала его практически не применяют,зато как легирующий элемент он издавна пользуется у металлургов почетом.Небольшие добавки его придают стали твердость и износостойкость. Такие свойстваприсущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%),входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаютсяисключительной твердостью — они-то и позволяют металлу уверенно сопротивлятьсяодному из опаснейших врагов — износу.
В качестве представителяметаллов, относящихся к побочным подгруппам периодической системы, рассмотримхром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранеерассмотренных металлов он, как и все металлы с достраивающимся предпоследнимэлектронным слоем атома, отличается тугоплавкостью и твердостью. По твердостихром превосходит все металлы, он царапает стекло.
/>/>Химические свойства./> /> Расположение электронов на 3d- и4s-орбиталях атома хрома можно представитьсхемой:Отсюда видно, что хром можетпроявлять в соединениях различные степени окисления — от +1 до +6; из нихнаиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Такимобразом, в образовании химических связей участвует не только электрон внешнегоуровня, но и пять электронов d-подуровнявторого снаружи уровня.
Как и у алюминия, наповерхности хрома образуется оксидная пленка Сr2О3.Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться несразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированнойсерной кислотах хром не растворяется, так как его оксидная пленка упрочняется,т. е. хром переходит в пассивное состояние. По этой же причине невзаимодействуют с хромом разбавленные серная и соляная кислоты, содержащиерастворенный кислород. Пассивацию хрома можно устранить очисткой поверхностиметалла.
При высокой температуре хромгорит в кислороде, образуя оксид Cr2О3. Раскаленный хромреагирует с парами воды:
2Cr + ЗН2О= Cr2О3 + ЗН2
Металлический хром принагревании реагирует также с галогенами, галогеноводородами, серой, азотом,фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3; 2Cr + N2 = 2CrN
2Cr +3S = Cr2S3; Cr + Si = CrSi
На воздухе хром совершенно неизменяется. Поэтому хромом с помощью электролиза его соединений покрывают —хромируют — стальные изделия для предохранения их от ржавления и механическогоизноса. Эти же качества хром придает своим сплавам с железом — хромистымсталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошлав виде вилок, ножей и других предметов домашнего обихода. Блестящие,серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская»Московского метрополитена.
При химических реакциях атомхрома может отдавать, кроме единственного электрона наружного слоя, до 5электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6).Но, как и все элементы с достраивающимся предпоследним слоем атома, хромпроявляет несколько значений степеней окисления, т. е. кроме высшего и низшиезначения, а именно + 2 и + 3. У металлов с переменной валентностью, как и уэлементов одного и того же периода, например III, с возрастанием степениокисления уменьшается радиус иона. Так, у хрома:
/>
Радиус иона
При этом соблюдается та жесамая закономерность в изменении химических свойств соединений металла свозрастанием его степени окисления, как у элементов одного и того же периода, аименно:
1. С возрастанием степениокисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значенияхстепени окисления и близких значениях ионного радиуса химические свойствагидроксидов элементов оказываются сходными.
Это мы и наблюдаем нагидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2и Mg2; Сг3 и А13; С г6и S6*:
/>
Гидроксиды хрома
Гидроксидыэлементов III периода
Хром образует три рядасоединений:
/>
Познакомимся с важнейшими изэтих соединений. При растворении хрома в кислотах получаются соли, в которыххром двухвалентен, например:
/>
Соединения двухвалентногохрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, вкоторых содержится хром в степени окисления +6: оксид
/>/>Применение.Хром широко используется, как добавочный материал кметаллам, для получения высококачественной стали, подшипников и др. данныйпроцесс называется хромированием.
Молодое Советское государство не могло зависеть откапиталистических стран в такой важнейшей отрасли промышленности, какпроизводство качественных сталей, являющейся основным потребителем ферросплавов.Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны,требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая,автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование истроительство ферросплавных заводов. В 1931 году вошел в строй Челябинскийзавод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Одиниз создателей советской качественной металлургии член-корреспондент Академиинаук СССР В. С. Емельянов в эти годы находился в Германии, куда он былнаправлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась нетолько в Германию, но и в Швецию, Италию, США. И у них же нам приходилосьпокупать феррохром.
Но когда вслед заЧелябинским в 1933 году были построены еще два ферросплавных завода—в Запорожьеи Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, втом числе и феррохром, но и получила возможность экспортировать их за границу.Качественная металлургия страны была практически полностью обеспеченанеобходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии иокислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углеродвреден: карбидообразующие «наклонности» хрома приводят к тому, что большиеколичества этого элемента связываются в карбиды, выделяющиеся на границах зеренстали, а сами зерна оказываются бедны хромом и не могут стойко оборонятьсяпротив натиска кислот и кислорода. Поэтому содержание углерода в нержавеющейстали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться«чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов.Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием,в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служатсплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта имолибдена придает металлу способность переносить большие нагрузки при t = 650—900°С. Из этих сплавов делают, например, лопатки газовых турбин.<sup/>Сплав кобальта,молибдена и хрома («комохром») безвреден для человеческого организма и поэтомуиспользуется в восстановительной хирургии.
Одна из американских фирм недавно создала новыематериалы, магнитные свойства которых изменяются под влиянием температуры. Этиматериалы, основу которых составляют соединения марганца, хрома исурьмы,по мнению ученых, найдут применение в различных автоматических устройствах,чувствительных к колебаниям температуры, и смогут заменить более дорогиетермоэлементы.
Хромиты широко используют и в огнеупорнойпромышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал дляфутеровки мартеновских печей и других металлургических агрегатов. Этот материалобладает высокой термостойкостью, ему не страшны многократные резкие изменениятемпературы.
Химики используют хромиты для получения бихроматовкалия и натрия, а также хромовых квасцов, которые применяются для дублениякожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», асапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимаетдеятельное участие в производстве красителей для стекольной, керамической,текстильной промышленности.
Окись хрома позволила тракторостроителям значительносократить сроки обкатки двигателей. Обычно эта операция, во время которой всетрущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго иэто, конечно, не очень устраивало работников тракторных заводов. Выход изположения был найден, когда удалось разработать новую топливную присадку, в составкоторой вошла окись хрома. Секрет действия присадки прост: при сгорании топливаобразуются мельчайшие абразивные частицы окиси хрома, которые, оседая навнутренних стенках цилиндров и других подвергающихся трению поверхностях,быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Этаприсадка в сочетании с новым сортом масла позволила в 30 раз сократитьпродолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную«специальность»: в США изготовлена экспериментальная магнитофонная пленка,рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицыокиси хрома. Замена оказалась удачной — качество звучания резко улучшилось,пленка стала надежнее в работе. Новинкой в первую очередь предполагаетсяобеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемойхромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причинанеудач заключалась в том, что используемый при этом электролит содержалтрехвалентный хром, который не мог создать нужное покрытие. А вот егошестивалентному «собрату» такая задача оказалась по плечу. С этого времени вкачестве электролита начали применять хромовую кислоту — в ней валентностьхрома равна 6. Толщина защитных покрытий (например, на некоторыхнаружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1миллиметра. Но иногда хромовое покрытие используют в декоративных целях — дляотделки часов, дверных ручек и других предметов, не подвергающихся серьезнойопасности. В таких случаях на изделие наносят тончайший слой хрома(0,0002—0,0005 миллиметра).
Существует и другой способ хромирования —диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначальностальную деталь помещали в порошок хрома и нагревали в восстановительнойатмосфере до высоких температур. При этом на поверхности детали появлялсяобогащенный хромом слой, по твердости и коррозионной стойкости значительнопревосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но»)при температуре примерно 1000°С хромовый порошок спекается и, кроме того, наповерхности покрываемого металла образуются карбиды, препятствующие диффузиихрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка дляэтой цели начали использовать летучие галоидные соли хрома — хлорид или иодид,что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно вустановке для хромирования, пропуская пары соответствующей галоидоводороднойкислоты через порошкообразный хром или феррохром. Образующийся газообразныйхлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом.Такое покрытие гораздо прочнее связано с основным материалом, чемгальваническое.
До последнего времени хромировали только металлическиедетали. А недавно советские ученые научились наносить хромовую «броню» наизделия из пластмасс. Подвергнутый испытаниям широко известныйполимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менеестрашными такие известные «враги» конструкционных материалов, как истирание,изгиб, удар. Само собой разумеется, возрос срок службы деталей.
/>/>Резюме.… Прежде чем закончить рассказ о хроме, мы вновь обратимсяк воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, —я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! —незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда быладля нас символом технического прогресса. И вот теперь Англия покупает нашферрохром! Англичане понимают толк в том, что покупают».
/>/>Список Литературы:1. «Химия за 11 класс».Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химияза 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия дляподготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Доклад - Хром - Химия

Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил: Гуляева Т.А.
КАРАГАНДА 2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
 |
К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W.Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24 Cr 1s2 |2s2 2p6 |3s2 3p6 3d5 |4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3 RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современнойтехники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается.
Хром встречается ввиде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr2 04, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе… Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2 О3 + 2Аl = Аl2 О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
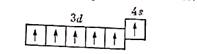 |
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2 О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2 О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2 О = Cr2 О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3 ; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2 S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
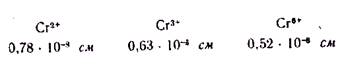
Радиусиона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2; Сг3 и А13; С г6 и S6 *:

Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:
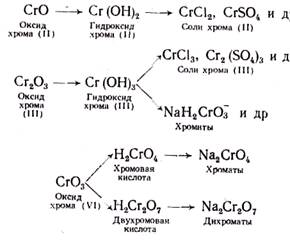
Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:
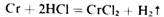
Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид
Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием .
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома исурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
… Прежде чем закончить рассказ о хроме, мы вновь обратимся к воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, — я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! — незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда была для нас символом технического прогресса. И вот теперь Англия покупает наш феррохром! Англичане понимают толк в том, что покупают».
1. «Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия для подготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Реферат: Хром

Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил: Гуляева Т.А.
КАРАГАНДА 2001г.
Оглавление:
Введение............................................................................................ 3
Нахождение в природе..................................................................... 3
Происхождение................................................................................. 4
Получение.......................................................................................... 5
Физические свойства......................................................................... 5
Химические свойства......................................................................... 6
Применение....................................................................................... 8
Резюме............................................................................................. 10
Список Литературы:....................................................................... 11
 |
К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W. Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24Cr 1s2|2s22p6|3s23p63d5|4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современной техники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается.
Хром встречается в виде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr204, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
...Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная... Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры.
Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе... Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2О3 + 2Аl = Аl2О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
 |
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2О = Cr2О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:

Радиус иона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2; Сг3 и А13; С г6 и S6*:

Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:

Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:

Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид
Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием.
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома и сурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
...Прежде чем закончить рассказ о хроме, мы вновь обратимся к воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, — я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! — незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда была для нас символом технического прогресса. И вот теперь Англия покупает наш феррохром! Англичане понимают толк в том, что покупают».
1. «Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия для подготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.referatmix.ru
Доклад - Хром 2 - Химия
Оглавление: В/> ведение. К металлам побочных подгрупп периодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома, марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общие характеристики подгрупп хрома и семейства железа.Побочную подгруппу VI группы составляют следующие элементы — хром Cr, молибден Мо и вольфрам W. Хром возглавляет побочную подгруппу 4 группы. Его электронная формула +24Cr 1s2|2s22p6|3s23p63d5|4s1
На внешнем энергетическом уровне атомов хрома и молибдена содержится по одному электрону, вольфрама — два электрона, что обусловливает металлический характер этих элементов и отлично от элементов главной подгруппы. В соответствии с числом валентных электронов они проявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общей формулы h3RO4. Сила кислот закономерно снижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо, хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хрома проявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединения высшей степени окисления, которые во многом весьма похожи на соответствующие соединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера в подгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390 °С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитей в электрических лампочках накаливания.
Металлы подгруппы хрома в обычных условиях весьма устойчивы к воздействию воздуха и воды. При нагревании взаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием и др. Известны их многочисленные сплавы с другими металлами. Сплавы и сами металлы — весьма ценные материалы современной техники.
По физическим и химическим свойствам молибден и вольфрам сходны между собой и несколько отличаются от хрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметно понижается. Нахождение в природе. Хром встречается ввиде соединений в различных минералах. Наиболее распространен минерал хромит, или хромистый железняк FeCr204, богатые месторождения которого имеются на Урале и в Казахстане. Массовая доля хрома в земной коре составляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г. Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П. С. Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, были найдены огромные залежи хромита — основного промышленного сырья для производства феррохрома. В годы войны на базе этого месторождения был построен Актюбинский ферросплавный завод, который впоследствии стал крупнейшим предприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположено большое число месторождений этого металла: Сарановское, Верблюжьегорское, Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистых руд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии, на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами, практически не пригодными для производства феррохрома. Всего же на долю хрома приходится 0,02% земной коры. Происхождение. Найденный минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе… Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...».
Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входит во многие термины, не связанные с элементом хромом: слово «хромосома», например, в переводе с греческого означает «тело, которое окрашивается»; для получения цветного, изображения пользуются прибором хромоскопом; фотолюбителям хорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования в атмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
Свое название хром получил от греческого слова «хрома» — краска за то, что все соединения хрома имеют яркие окраски. Получение. Металлический хром получают восстановлением оксида хрома (III) при нагревании с алюминием:
Сr2О3 + 2Аl = Аl2О3 +2Сr
Металлический хром получают также электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовый ангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Впервые феррохром был получен в 1820 году восстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. К этому же времени относятся и первые попытки выплавить углеродистый феррохром в доменной печи. В 1865 году был выдан первый патент на хромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыграл электрический ток, точнее электротермический способ получения металлов и сплавов. В 1893 году французский ученый Муассан выплавил в электропечи углеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производство развивалось черепашьими темпами. Мизерные количества ферросилиция и ферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегу реки Сатки (Южный Урал) был построен маленький электрометаллургический завод «Пороги», который стал производить феррохром, а затем и ферросилиций. Но об удовлетворении нужд своей промышленности не могло быть и речи: потребность России в ферросплавах приходилось почти полностью покрывать ввозом их из других стран. Физические свойства и Химические свойства. Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло. Химические свойства. Р/> асположение электронов на 3d- и 4s-орбиталях атома хрома можно представить схемой:
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2О = Cr2О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2+ h3; 2Cr + N2= 2CrN
2Cr + 3S = Cr2S3; Cr + Si = CrSi На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
/> Радиус иона При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными. Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2; Сг3 и А13; С г6 и S6*:
/> Гидроксиды хрома Гидроксиды элементов III периода Хром образует три ряда соединений:
/> Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:
/> Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид Опыт №1. Получение оксида хрома (III) Приборы и реактивы: асбестированная сетка; спички; бихромат аммония (Nh5)2Cr2O7 (измельченный). Выполнение опыта. Расстилаю большой лист бумаги, на который кладу асбестированную сетку. Тонко измельченный бихромат аммония насыпаю в виде горки. До бихромата аммония дотрагиваюсь зажженной спичкой. Начинается разложение бихромата, которое протекает с выделением тепла и постепенно захватывает все большие и большие количества соли. В конце реакция идет все более бурно — появляются искры, пламя, летит рыхлый и легкий пепел — типичное извержение вулкана в миниатюре. Образовалось большое количество рыхлого темно-зеленого вещества. Вывод: оксид хрома (III) Cr2O3 получается путем нагревания бихромата аммония: (Nh5)2Cr2O7[pic]Cr2O3+N2+4h3O Опыт №2. Исследование свойств оксида хрома (III) Приборы и реактивы: колба; вода h3O; оксид хрома (III) Cr2O3; серная кислота Выполнение опыта. Добавляю полученный зеленый порошок оксида хрома (III) сначала в колбу с водой Cr2O3 + 3h3O = 2Cr(OH)3 затем в колбу с серной кислотой Cr2O3 + 3h3SO4 = Cr2(SO4)3 + 3h3O Наблюдаю растворение оксида в обоих колбах. Вывод: Оксид хрома растворяется в воде и в кислотах. Опыт №3.Окислительные свойства солей хрома (VI) Приборы и реактивы: раствор бихромата калия K2Cr2O7; раствор сульфита натрия Na2SO3; серная кислота h3SO4. Выполнение опыта. К раствору K2Cr2O7, подкисленному серной кислотой, добавляю раствор Na2SO4. Наблюдаю изменения окраски. Оранжевый раствор стал зелено- фиолетовым. Вывод: В кислой среде хром восстанавливается сульфитом натрия от хрома (VI) дохрома(III): K2Cr2O7 + 3Na2SO3 + 4h3SO4 = K2SO4 + Cr2(SO4)3 + 3Na2SO4 + 4h3O Опыт №4. Исследование свойств солей хрома (VI) Приборы и реактивы: концентрированный раствор бихромата калия K2Cr2O7; концентрированная соляная кислота HCl Выполнение опыта. К концентрированному раствору бихромата калия K2Cr2O7 добавляю концентрированную соляную кислоту HCl. При нагревании наблюдается выделение резкого хлорного запаха, от которого жжет нос и горло. Вывод: Так как все соединения хрома (VI) являются сильными окислителями, то при реакции с соляной кислотой: K2Cr2O7 + 14HCl [pic] 3Cl2( + 2CrCl3 + 2KCl + 7h3O происходит восстановление хлора: 2Cl- -2[pic]Cl20 Опыт №5. Переход хромата в бихромат и обратно Приборы и реактивы: раствор хромата калия K2CrO4, раствор бихромата калия K2Cr2O7, серная кислота, гидроксид натрия. Выполнение опыта. К раствору хромата калия добавляю серную кислоту, в результате происходит изменение окраски раствора из желтого в оранжевый. 2K2CrO4 + h3SO4 = K2Cr2O7 + K2SO4 + h3O К раствору бихромата калия добавляю щелочь, в результате происходит изменение окраски раствора из оранжевого в желтый. K2Cr2O7 + 4NaOH = 2Na2CrO4 + 2KOH + h3O Вывод: В кислой среде хроматы неустойчивы, ион CrO42- желтого цвета превращается в ион Cr2O72- оранжевого цвета, а в щелочной среде эта реакция протекает в обратном направлении 2CrO42- + 2H+ кислая среда((щелочная среда Cr2O72- + h3O. Опыт №6. Получение малорастворимых солей хромовых кислот Приборы и реактивы: раствор хромата калия K2CrO4, раствор бихромата калия K2Cr2O7, раствор нитрата серебра AgNO3. Выполнение опыта. Наливаю в одну пробирку раствор хромата калия, в другую — раствор бихромата калия, и добавляю в обе пробирки раствор нитрата серебра, в обоих случаях наблюдаю образование красно-бурого осадка. K2CrO4 + 2AgNO3= Ag2CrO4( + 2KNO3 K2Cr2O7 + AgNO3 ( Ag2CrO4(+ KNO3 Вывод: Растворимые соли хрома при взаимодействии с нитратом серебра образуют нерастворимый осадок Опыт №7. Получение гидроксида хрома Приборы и реактивы: раствор соли хрома (III) CrCl3, едкий натр (гидроксид натрия) NaOH. Выполнение опыта. В пробирку с раствором хлорида хрома (III) по каплям добавляю раствор едкого натра до образования серо-зеленого осадка. Вывод: Гидроксид хрома Cr(OH)3 получается при действии на соль трехвалентного хрома щелочью: CrCl3 + 3NaOH = Cr(OH)3( + 3NaCl Сплавы.Применение. Хром широко используется, как добавочный материал к металлам, для получения высококачественной стали, подшипников и др. данный процесс называется хромированием.
Молодое Советское государство не могло зависеть от капиталистических стран в такой важнейшей отрасли промышленности, как производство качественных сталей, являющейся основным потребителем ферросплавов. Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны, требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая, автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование и строительство ферросплавных заводов. В 1931 году вошел в строй Челябинский завод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Один из создателей советской качественной металлургии член-корреспондент Академии наук СССР В. С. Емельянов в эти годы находился в Германии, куда он был направлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась не только в Германию, но и в Швецию, Италию, США. И у них же нам приходилось покупать феррохром.
Но когда вслед за Челябинским в 1933 году были построены еще два ферросплавных завода—в Запорожье и Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, в том числе и феррохром, но и получила возможность экспортировать их за границу. Качественная металлургия страны была практически полностью обеспечена необходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии и окислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служат сплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при t = 650—900° С. Из этих сплавов делают, например, лопатки газовых турбин.Сплав кобальта, молибдена и хрома («комохром») безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Одна из американских фирм недавно создала новые материалы, магнитные свойства которых изменяются под влиянием температуры. Эти материалы, основу которых составляют соединения марганца, хрома исурьмы, по мнению ученых, найдут применение в различных автоматических устройствах, чувствительных к колебаниям температуры, и смогут заменить более дорогие термоэлементы.
Хромиты широко используют и в огнеупорной промышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал для футеровки мартеновских печей и других металлургических агрегатов. Этот материал обладает высокой термостойкостью, ему не страшны многократные резкие изменения температуры.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности.
Окись хрома позволила тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошла окись хрома. Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы окиси хрома, которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную «специальность»: в США изготовлена экспериментальная магнитофонная пленка, рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицы окиси хрома. Замена оказалась удачной — качество звучания резко улучшилось, пленка стала надежнее в работе. Новинкой в первую очередь предполагается обеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002—0,0005 миллиметра).
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но») при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
До последнего времени хромировали только металлические детали. А недавно советские ученые научились наносить хромовую «броню» на изделия из пластмасс. Подвергнутый испытаниям широко известный полимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.Сплавы Семейство хромовых сплавов весьма многочисленно.
Таблица 3- Основные хромовые сплавы
|Названи|Хром |Железо|Никель|Алюминий|Кобаль|Вольфрам|
|е |Cr | | | |т | |
| | |Fe |Ni |Al |Co |W |
|Феррохр|65% |35 % | | | | |
|ом | | | | | | |
|Нихром |15-30%| |70-85%| | | |
|Хромаль|17-30%|64-79%| |4-6% | | |
|Стеллит|20-25%|1-3% | | |45-60%|5-29% | Феррохром — сплав хрома с железом, вводимый в жидкую сталь для ее
легирования. Вводить хром в чистом виде в сталь очень затруднительно — он
медленно растворяются в жидком металле, так как температуры его плавления
выше, чем у стали. У феррохрома же температура плавления такая же, как у
стали, или ниже.
Нихромы и хромали, устойчивы в интервале 1000-13000C, обладают высоким
электросопротивлением, используются для изготовления нагревателей в
электрических печах сопротивления.
Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу
способность переносить большие нагрузки при 650-900° С. Из этих сплавов
делают, например, лопатки газовых турбин.
Стеллит очень твердый сплав, стоек против износа и коррозии;
применяется в металлообрабатывающей промышленности, для изготовления
режущих инструментов.
Комохром — сплав хрома, кобальта и молибдена безвреден для
человеческого организма и поэтому используется в восстановительной
хирургии.
Хром входит в состав очень многих марок сталей.
«Нержавейка» — сталь, отлично противостоящая коррозии и окислению,
содержит примерно 17-19% хрома и 8-13% никеля. Но этой стали углерод
вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие
количества этого элемента связываются в карбиды, выделяющиеся на границах
зерен стали, а сами зерна оказываются бедны хромом и не могут стойко
обороняться против натиска кислот и кислорода. Поэтому содержание углерода
в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В
некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из
которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят
25-30% хрома. Такая сталь выдерживает температуры до 1000°С.
Хромолибденовые стали используются для создания фюзеляжей самолетов. Список Литературы: «Химия за 11 класс». Г.Е. Рудзитис, Ф.Г. Фельдман
«Неорганическая химия за 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
«Химия для подготовительных отделений». Г.П. Хомченко.
Интернет.
www.ronl.ru
Доклад - Исследование свойств хрома и его соединений
Министерство образования Российской Федерации
ГИМНАЗИЯ №1
Кафедра Химии
ТВОРЧЕСКАЯ РАБОТА
ИССЛЕДОВАНИЕ СВОЙСТВ ХРОМА И ЕГО СОЕДИНЕНИЙ
Пояснительная записка
Руководитель Г.И. Астахова
Выполнил ученик 9 «В» класса Б.А.Кулаев
Красноярск, 2001 г.
Содержание
Содержание… 2
Введение… 3
1.Исторические сведения… 4
2. Хром в природе… 6
3. Свойства хрома. Теоретическая часть… 7
3.1 Общие сведения… 7
3.2 Физические свойства… 8
3.4 Соединения хрома… 12
3.4.1 Оксиды… 12
3.4.2 Гидроксиды… 13
3.4.3 Кислоты… 13
3.4.4 Соли… 14
4. Свойства хрома. Экспериментальная часть… 14
4.1 Опыт №1. Получение оксида хрома (III)… 14
4.2 Опыт №2. Исследование свойств оксида хрома (III)… 15
4.3 Опыт №3.Окислительные свойства солей хрома (VI)… 16
4.4 Опыт №4. Исследование свойств солей хрома (VI)… 16
4.5 Опыт №5. Переход хромата в бихромат и обратно… 17
4.6 Опыт №6. Получение малорастворимых солей хромовых кислот… 17
4.7 Опыт №7. Получение гидроксида хрома… 18
5. Применение хрома… 18
5.1 Хромирование… 20
5.2 Сплавы… 22
6. Экологические проблемы… 24
Заключение… 26
Литература… 27
Приложение А… 28
Введение
Хром и его соединения активно используются в промышленном производстве, особенно в металлургии, химической, огнеупорной промышленности. Область его применения достаточно широка, поэтому углубленное изучение свойств хрома является необходимым дополнением к соответствующим разделам школьной программе по химии, тем более, что в учебнике этот материал, по-моему, незаслуженно отсутствует.
Данная работа посвящена изучению основных физических и химических свойств хрома и его соединений, позволяет оценить важность этого химического элемента.
1.Исторические сведения
В 1766 году петербургский профессор химии И.Г.Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15 километрах от Екатеринбурга. Обрабатывая камень соляной кислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся белом осадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудники описал академик П.С.Паллас. «Березовские копи, — писал он, — состоят из четырех рудников, которые разрабатываются с 1752 года. В них наряду с золотом добываются серебро и свинцовые руды, а также находят замечательный красный свинцовый минерал, который не был обнаружен больше ни в одном другом руднике России. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари), тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минерала бывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошок она дает красивую желтую краску...». Минерал был назван «сибирским красным свинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этого минерала был в конце XVIII века привезен Палласом в Париж. Крокоитом заинтересовался известный французский химик Луи Никола Воклен. В 1796 году он подверг минерал химическому анализу. «Все образцы этого вещества, которые имеются в нескольких минералогических кабинетах Европы, — писал Воклен в своем отчете, — были получены из этого (Березовского) золотого рудника. Раньше рудник был очень богат этим минералом, однако говорят, что несколько лет назад запасы минерала в руднике истощились и теперь этот минерал покупают на вес золота, в особенности, если он желтый. Образцы минерала, не имеющие правильных очертаний или расколотые на кусочки, годятся для использования их в живописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся на воздухе… Красивый красный цвет, прозрачность и кристаллическая форма сибирского красного минерала заставила минералогов заинтересоваться его природой и местом, где он был найден; большой удельный вес и сопутствующая ему свинцовая руда, естественно, заставляли предполагать о наличии свинца в этом минерале...»
В 1797 году Воклен повторил анализ. Растертый в порошок крокоит он поместил в раствор углекислого калия и прокипятил. В результате опыта ученый получил углекислый свинец и желтый раствор, в котором содержалась калиевая соль неизвестной тогда кислоты. При добавлении к раствору ртутной соли образовывался красный осадок, после реакции со свинцовой солью появлялся желтый осадок, а введение хлористого олова окрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинца Воклен выпарил фильтрат, а выделившиеся красные кристаллы (это был оксид шестивалентного хрома) смешал с углем, поместил в графитовый тигель и нагрел до высокой температуры. Когда опыт был закончен, ученый обнаружил в тигле множество серых сросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество. Так впервые был выделен новый элемент. Один из друзей Воклена предложил ему назвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразного цвета его соединений. Сначала Воклену не понравилось предложенное название, поскольку открытый им металл имел скромную серую окраску и как будто не оправдывал своего имени. Но друзья все же сумели уговорить Воклена и, после того как французская Академия наук по всей форме зарегистрировала его открытие, химики всего мира внесли слово «хром» в списки известных науке элементов.
В 1854 году удалось получить чистый металлический хром электролизом водных растворов хлорида хрома. В металлургии, где расход хрома для легирования сталей очень велик, используют не сам хром, а его сплав с железом — феррохром. Впервые феррохром был получен в 1820 году восстановлением смеси оксидов железа и хрома древесным углем в тигле. В 1865 году был выдан первый патент на хромистую сталь.
2. Хром в природе
Среднее содержание хрома в земной коре 83 г/т, по массе содержаниехрома в земной коре составляет 0,035%, в воде морей и океанов 2´10-5 мг/л. Мировые подтвержденные запасы хромовых руд составляют 1,8 млрд. т. Более 60% сосредоточено в ЮАР. Крупными запасами обладают Зимбабве, Казахстан Турция, Индия, Бразилия. Руды хрома имеются в Новой Каледонии, на Кубе, в Греции, Югославии. В то же время такие промышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, совершенно лишены хромового сырья, а США и Канада располагают лишь очень бедными рудами [1]. Запасы хромовых руд России сосредоточены главным образом в группе Сарановских месторождений (Верблюжьегорское, Алапаевское, Халиловское и др.) на Урале (Пермская область) и составляют 6,4 млн. т. (0,36% от мировых запасов).
Добыча хромовых руд в мире составляет около 12 млн. т. в год, в том числе 108 тыс. т. в России. Главные производители товарной хромовой руды — ЮАР, Казахстан, на долю которых приходится более 60% добычи сырья ежегодно.
В Красноярском крае месторождения хрома отсутствуют. Но на правом берегу р.Енисей, в устье р.Березовой (к югу от устья р. Подкаменная Тунгуска) есть рудопроявление с выходом пород 1,5´4 м, возраст пород оценивается в 500 млн. лет. Содержание чистого хрома в руде порядка 42% .
По содержанию Cr2 O3 хромовые руды подразделяются на очень богатые (более 65%), богатые (65-52%), средние (52-45%), бедные (45-30%), убогие (30-10%). Руды, содержащие более 45% Cr2 O3 не требуют обогащения.
| Показатель | Донской ГОК (Казахстан) | Сарановская шахта (Россия, Пермская обл.) | Рудопроявление в Красноярском крае |
| Содержание Cr2 O3 в исходной руде, % | 46,6 | 39,1 | 62 |
3. Свойства хрома. Теоретическая часть
3.1 Общие сведения
 |
Рисунок 1- Структура атома хрома
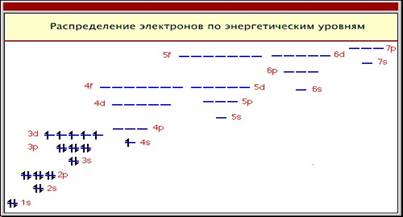
Рисунок 2-Распределение электронов по энергетическим уровням
3.2Физические свойства
Хром — твердый, довольно тяжелый, пластичный, ковкий металл серо-стального цвета, плавится при 1878±220С, кипит при 24690С [2]. Ничтожные примеси кислорода, азота, углерода резко изменяют физические свойства хрома, в частности он становится хрупким. Получить хром без этих примесей очень трудно. Устойчив к коррозии на воздухе и в воде.
Структура кристаллической решетки объемноцентрированная кубическая.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут достоверно объяснить эту аномалию.
Таблица 1- Физические свойства хрома
| Параметр | Значение |
| Плотность при 200C | 7,19 г/см3 |
| Температура плавления | 1878±220С |
| Температура кипения | 2469-2480 0C |
| Теплота парообразования | 344,4 кДж/Моль |
| Теплопроводность | 93,7 Вт/(м´К) |
| Температурный коэффициент линейного расширения | 6,2´10-6 |
| Удельное электрическое сопротивление | 12,7´10-8 Ом´м |
| Твердость по Бринеллю | 687 МПа |
| Удельная магнитная восприимчивость | +4,45´10-8 м/кг3 |
3.3Химические свойства
При небольших температурах хром химически мало активен (взаимодействует только с фтором). Выше 6000C взаимодействует с галогенами, серой, азотом, кремнием, бором, углеродом, кислородом. Взаимодействие с кислородом протекает сначала довольно активно, затем, однако, резко замедляется, так как поверхность покрывается тонкой чрезвычайно устойчивой пленкой, препятствующему дальнейшему окислению. Это явление называется пассивированием. При 12000C пленка начинает разрушаться, окисление снова идет быстро. При 20000C хром воспламеняется в кислороде с образованием темно-зеленого оксида Cr2 O3 .
Хром пассивируется холодными концентрированными h3 SO4 и HNO3, однако при сильном нагревании он растворяется в этих кислотах [3]:
2Cr + 6h3 SO4(конц.) = Cr2 (SO4 )3 + 3SO2 + 6h3 O
Cr + 6HNO3(конц.) = Cr(NO3 )3 + 3NO2 + 3h3 O
Хром растворяется в разбавленных сильных кислотах (HCl и h3 SO4 ). В этих случаях в отсутствии воздуха образуются соли Cr2+, а на воздухе — соли Cr3+ :
Cr + 2HCl = CrCl2 + h3
4Cr + 12HCl +3O2 = 4CrCl3 + 6h3 O
Нерастворим в h4 PO4, HClO4 благодаря образованию защитной пленки.
Таблица 2- Основные химические реакции чистого хрома
| Хром реагирует | ||
| 0…600 0С | 600…1200 0С | 1200…2000 0С |
1. со фтором 2Cr0+ 3F20= 2Cr+3 F3- | 1. с галогенами: 2Cr0+ 3Cl20 | 1. с кислородом: 4Cr + 3O2 |
2. ссерой: 2Cr0+ 3S0 | ||
3. с азотом: 2Cr0+ N20 | ||
4. с кремнием: 4Cr0+ 3Si0 | ||
5. с бором Cr0+ B0 | ||
6. с углеродом 4Cr0+ 3С0 | ||
7. с кислородом: 4Cr0+ 3O20= 2Cr2+3 O3-2 | ||
8. с серной кислотой: 2Cr0+ 6h3+ SO4-2 = Cr2+3 (SO4 )3-2 + 3S-2 O2 +6h3 O |
3.4 Соединения хрома
3.4.1 Оксиды
Оксид хрома (II) CrO (основной) — сильный восстановитель, чрезвычайно неустойчив в присутствии влаги и кислорода. Практического значения не имеет.
Оксид хрома (III) Cr2 O3 (амфотерный) устойчив на воздухе и в растворах.
Cr2 O3 + h3 SO4 = Cr2 (SO4 )3 + h3 O
Cr2 O3 + 2NaOH = Na2 CrO4 + h3 O
Образуется при нагревании некоторых соединений хрома (VI), например:
4CrO3 2Cr2 O3 + 3О2
2Cr2 O3 + 3О2
(Nh5 )2 Cr2 O7 Cr2 O3 + N2 + 4h3 O
Cr2 O3 + N2 + 4h3 O
4Cr + 3O2 2Cr2 O3
2Cr2 O3
Оксид хрома (III) используется для восстановления металлического хрома невысокой чистоты с помощью алюминия (алюминотермия) или кремния (силикотермия):
Cr2 O3 +2Al = Al2 O3 +2Cr
2Cr2 O3 + 3Si = 3SiO3 + 4Cr
Оксид хрома (VI) CrO3 (кислотный) — темно малиновые игольчатые кристаллы. Получают действием избытка концентрированной h3 SO4 на насыщенный водный раствор бихромата калия:
K2 Cr2 O7 + 2h3 SO4 = 2CrO3 + 2KHSO4 + h3 O
Оксид хрома (VI) — сильный окислитель, одно из самых токсичных соединений хрома.
При растворении CrO3 в воде образуется хромовая кислота h3 CrO4
CrO3 + h3 O = h3 CrO4
Кислотный оксид хрома, реагируя со щелочами, образует желтые хроматы CrO42- .
CrO3 + 2KOH = K2 CrO4 + h3 O
3.4.2 Гидроксиды
Гидроксид хрома (III) обладает амфотерными свойствами, растворяясь как в кислотах (ведет себя как основание):
2Cr(OH)3 + 3h3 SO4 = Cr2 (SO4 )3 + 6h3 O
так и в щелочах (ведет себя как кислота):
Cr(OH)3 + KOH = K[Cr(OH)4 ]
Cr(OH)3 + NaOH = NaCrO2 + 2h3 O
При прокаливании гидроксида хрома (III) образуется оксид хрома (III) Cr2 O3 .
2Cr(OH)3 Cr2 O3 + 3h3 O
Cr2 O3 + 3h3 O
Нерастворим в воде.
3.4.3 Кислоты
Кислоты хрома, отвечающие его степени окисления +6 и различающиеся соотношением числа молекул CrO3 и h3 O, существуют только в виде растворов. При растворении кислотного оксида CrO3, образуется монохромовая кислота (просто хромовая) h3 CrO4 .
CrO3 + h3 O = h3 CrO4
Подкисление раствора или увеличение в нем CrO3 приводит к кислотам общей формулы nCrO3 h3 O при n=2, 3,4 это, соответственно, ди, три, тетрохромовые кислоты. Самая сильная из них — дихромовая, то есть h3 Cr2 O7. Хромовые кислоты и их соли- сильные окислители и ядовиты.
3.4.4 Соли
Различают два вида солей: хромиты и хроматы
Хромитами с общей формулой RCrO2 называются соли хромистой кислоты HCrO2.
Cr(OH)3 + NaOH = NaCrO2 + 2h3 O
Хромиты обладают различной окраской — от темно коричневой до совершенно черной и обычно встречаются в виде сплошных массивов. Хромит мягче многих других минералов, температура плавления хромита зависит от его состава 1545-17300С. Хромит имеет металлический блеск и почти нерастворим в кислотах.
Хроматы — соли хромовых кислот. Соли монохромовой кислоты h3 CrO4 называют монохроматами (хроматы) R2 CrO4, соли дихромовой кислоты h3 Cr2 O7 дихроматы (бихроматы) — R2 Cr2 O7. Монохроматы обычно окрашены в желтый цвет. Они устойчивы только в щелочной среде, а при подкислении превращаются в оранжево-красные бихроматы:
2Na2 CrO4+ h3 SO4 = Na2 Cr2 O7 + Na2 SO4 + h3 O
4. Свойства хрома. Экспериментальная часть
4.1 Опыт №1. Получение оксида хрома (III)
Приборы и реактивы: асбестированная сетка; спички; бихромат аммония (Nh5 )2 Cr2 O7 (измельченный).
Выполнение опыта. Расстилаю большой лист бумаги, на который кладу асбестированную сетку. Тонко измельченный бихромат аммония насыпаю в виде горки. До бихромата аммония дотрагиваюсь зажженной спичкой.
Начинается разложение бихромата, которое протекает с выделением тепла и постепенно захватывает все большие и большие количества соли. В конце реакция идет все более бурно — появляются искры, пламя, летит рыхлый и легкий пепел — типичное извержение вулкана в миниатюре. Образовалось большое количество рыхлого темно-зеленого вещества.
Вывод: оксид хрома (III) Cr2 O3 получается путем нагревания бихромата аммония:
(Nh5 )2 Cr2 O7  Cr2 O3 +N2 +4h3 O
Cr2 O3 +N2 +4h3 O
4.2 Опыт №2. Исследование свойств оксида хрома ( III)
Приборы и реактивы: колба; вода h3 O; оксид хрома (III) Cr2 O3; серная кислота
Выполнение опыта. Добавляю полученный зеленый порошок оксида хрома (III) сначала в колбу с водой
Cr2 O3 + 3h3 O = 2Cr(OH)3
затем в колбу с серной кислотой
Cr2 O3 + 3h3 SO4 = Cr2 (SO4 )3 + 3h3 O
Наблюдаю растворение оксида в обоих колбах.
Вывод: Оксид хрома растворяется в воде и в кислотах.
4.3 Опыт №3.Окислительные свойства солей хрома ( VI)
Приборы и реактивы: раствор бихромата калия K2 Cr2 O7; раствор сульфита натрия Na2 SO3; серная кислота h3 SO4 .
Выполнение опыта. К раствору K2 Cr2 O7, подкисленному серной кислотой, добавляю раствор Na2 SO4. Наблюдаю изменения окраски.
Оранжевый раствор стал зелено- фиолетовым.
Вывод: В кислой среде хром восстанавливается сульфитом натрия от хрома (VI) до хрома (III):
K2 Cr2 O7 + 3Na2 SO3 + 4h3 SO4 = K2 SO4 + Cr2 (SO4 )3 + 3Na2 SO4 + 4h3 O
4.4 Опыт №4. Исследование свойств солей хрома ( VI)
Приборы и реактивы: концентрированный раствор бихромата калия K2 Cr2 O7; концентрированная соляная кислота HCl
Выполнение опыта. К концентрированному раствору бихромата калия K2 Cr2 O7 добавляю концентрированную соляную кислоту HCl. При нагревании наблюдается выделение резкого хлорного запаха, от которого жжет нос и горло.
Вывод: Так как все соединения хрома (VI) являются сильными окислителями, то при реакции с соляной кислотой:
K2 Cr2 O7 + 14HCl  3Cl2 + 2CrCl3 + 2KCl + 7h3 O
3Cl2 + 2CrCl3 + 2KCl + 7h3 O
происходит восстановление хлора:
2Cl- -2 Cl20
Cl20
4.5 Опыт №5. Переход хромата в бихромат и обратно
Приборы и реактивы: раствор хромата калия K2 CrO4, раствор бихромата калия K2 Cr2 O7, серная кислота, гидроксид натрия.
Выполнение опыта. К раствору хромата калия добавляю серную кислоту, в результате происходит изменение окраски раствора из желтого в оранжевый.
2K2 CrO4 + h3 SO4 = K2 Cr2 O7 + K2 SO4 + h3 O
К раствору бихромата калия добавляю щелочь, в результате происходит изменение окраски раствора из оранжевого в желтый.
K2 Cr2 O7 + 4NaOH = 2Na2 CrO4 + 2KOH + h3 O
Вывод: В кислой среде хроматы неустойчивы, ион CrO42- желтого цвета превращается в ион Cr2 O72- оранжевого цвета, а в щелочной среде эта реакция протекает в обратном направлении
2CrO42- + 2H+кислая сред஬щелочная среда Cr2 O72- + h3 O.
4.6 Опыт №6. Получение малорастворимых солей хромовых кислот
Приборы и реактивы: раствор хромата калия K2 CrO4, раствор бихромата калия K2 Cr2 O7, раствор нитрата серебра AgNO3 .
Выполнение опыта. Наливаю в одну пробирку раствор хромата калия, в другую — раствор бихромата калия, и добавляю в обе пробирки раствор нитрата серебра, в обоих случаях наблюдаю образование красно-бурого осадка.
K2 CrO4 + 2AgNO3 = Ag2 CrO4 ¯ + 2KNO3
K2 Cr2 O7 + AgNO3 ® Ag2 CrO4 ¯+ KNO3
Вывод: Растворимые соли хрома при взаимодействии с нитратом серебра образуют нерастворимый осадок
4.7 Опыт №7. Получение гидроксида хрома
Приборы и реактивы: раствор солихрома (III) CrCl3, едкий натр (гидроксид натрия) NaOH.
Выполнение опыта. В пробирку с раствором хлорида хрома (III) по каплям добавляю раствор едкого натра до образования серо-зеленого осадка.
Вывод: Гидроксид хрома Cr(OH)3 получается при действии на соль трехвалентного хрома щелочью:
CrCl3 + 3NaOH = Cr(OH)3 ¯ + 3NaCl
5. Применение хрома
Основная часть добываемой в мире хромистой руды поступает сегодня на ферросплавные заводы, где выплавляются различные сорта феррохрома и металлического хрома.
Хромиты широко используют в огнеупорной промышленности для изготовления огнеупорного хромитового и хромомагнезитового кирпича. Такой кирпич химически пассивен, устойчив при температурах выше 22000С, хорошо выдерживает резкие колебания температур. Магнезитохромитовый кирпич — отличный огнеупорный материал для футеровки (защитной внутренней облицовки) мартеновских печей и других металлургических агрегатов. Своды из хромомагнезитового кирпича выдерживают вдвое больше плавок, чем своды из упорного кварцевого материала.
Химики используют хромиты для получения бихроматов калия и натрия, а также хромовых квасцов, которые применяются для дубления кожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», а сапоги из нее «хромовыми». Растворимые в воде хроматы натрия и калия применяются в текстильном и кожевенном производстве, как консерванты древесины (они уничтожают древесные грибки).
Хромовая смесь — сернокислый раствор бихромата калия или натрия используется для мытья химической посуды в лабораториях. Наиболее часто применяется раствор содержащей по массе приблизительно 12 частей K2 Cr2 O7, 70 частей воды и 22 части h3 SO4 .
Как бы оправдывая свое название, хром принимает деятельное участие в производстве красителей для стекольной, керамической, текстильной промышленности. Нерастворимые хроматы некоторых металлов (PbCrO4, ZnCrO4, SrCrO4 ) — прекрасные художественные краски. Богатством оттенков — от розово-красного до фиолетового славится SnCrO4, используемый в живописи по фарфору.
В мире драгоценных камней рубину принадлежит второе место после алмаза. Технология получения искусственного рубина заключается в следующем: в оксид алюминия Al2 O3 вводят дозированную добавку оксида хрома (III), — ему-то и обязаны рубиновые кристаллы своим чарующим цветом. Но искусственные рубины ценятся не только за свои «внешние данные»: рожденный с их помощью лазерный луч способен буквально творить чудеса.
Оксид хрома (III) позволил тракторостроителям значительно сократить сроки обкатки двигателей. Обычно эта операция, во время которой все трущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго и это, конечно, не очень устраивало работников тракторных заводов. Выход из положения был найден, когда удалось разработать новую топливную присадку, в состав которой вошел оксид хрома (III). Секрет действия присадки прост: при сгорании топлива образуются мельчайшие абразивные частицы оксида хрома (III), которые, оседая на внутренних стенках цилиндров и других подвергающихся трению поверхностях, быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Эта присадка в сочетании с новым сортом масла позволила в 30 раз сократить продолжительность обкатки.
Замена в рабочем слое магнитофонной пленки оксида железа на частицы оксида хрома (III) позволила резко улучшить качество звучания, пленка стала надежнее в работе.
Фотоматериалы и лекарства, катализаторы для химических процессов и металлические покрытия — всюду хром оказывается «при деле». О хромовых покрытиях следует рассказать подробнее.
5.1 Хромирование
Давно было замечено, что хром не только отличается большой твердостью (в этом отношении у него нет конкурентов среди металлов), но и хорошо сопротивляется окислению на воздухе, не взаимодействует с кислотами. Тонкий слой этого металла попробовали электролитически осаждать на поверхность изделий из других материалов, чтобы предохранить их от коррозии, царапин и прочих «травм». Однако хромовые покрытия оказались пористыми, легко отслаивались и не оправдывали возлагаемых на них надежд.
Почти три четверти века бились ученые над проблемой хромирования, и лишь в 20-х годах прошлого столетия проблема была решена. Причина неудач заключалась в том, что используемый при этом электролит содержал трехвалентный хром, который не мог создать нужное покрытие. А вот его шестивалентному «собрату» такая задача оказалась по плечу. С этого времени в качестве электролита начали применять хромовую кислоту — в ней валентность хрома равна 6. Толщина защитных покрытий (например, на некоторых наружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1 миллиметра. Но иногда хромовое покрытие используют в декоративных целях — для отделки часов, дверных ручек и других предметов, не подвергающихся серьезной опасности. В таких случаях на изделие наносят тончайший слой хрома (0,0002-0,0005 миллиметра).
Литовские химики разработали способ создания многослойной «кольчуги» для особо ответственных деталей. Тончайший верхний слой этого покрытия (под микроскопом его поверхность и в самом деле напоминает кольчугу) состоит из хрома: в процессе службы он первым «принимает огонь на себя», но пока хром окисляется, проходят многие годы. Тем временем деталь спокойно несет свою ответственную службу.
Хромированию подвергаются не только металлические детали, но и изделия из пластмасс. Подвергнутый испытаниям широко известный полимер — полистирол, «одетый» в хром, стал прочнее, для него оказались менее страшными такие известные «враги» конструкционных материалов, как истирание, изгиб, удар. Само собой разумеется, возрос срок службы деталей.
Существует и другой способ хромирования — диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначально стальную деталь помещали в порошок хрома и нагревали в восстановительной атмосфере до высоких температур. При этом на поверхности детали появлялся обогащенный хромом слой, по твердости и коррозионной стойкости значительно превосходящий сталь, из которой сделана деталь. Но при температуре примерно 1000°С хромовый порошок спекается и, кроме того, на поверхности покрываемого металла образуются карбиды, препятствующие диффузии хрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка для этой цели начали использовать летучие галоидные соли хрома — хлорид или иодид, что позволило снизить температуру процесса. Хлорид (или иодид) хрома получают непосредственно в установке для хромирования, пропуская пары соответствующей галоидоводородной кислоты через порошкообразный хром или феррохром. Образующийся газообразный хлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом. Такое покрытие гораздо прочнее связано с основным материалом, чем гальваническое.
5.2 Сплавы
Семейство хромовых сплавов весьма многочисленно.
Таблица 3- Основные хромовые сплавы
| Название | Хром Cr | Железо Fe | Никель Ni | Алюминий Al | Кобальт Co | Вольфрам W |
| Феррохром | 65% | 35 % | ||||
| Нихром | 15-30% | 70-85% | ||||
| Хромаль | 17-30% | 64-79% | 4-6% | |||
| Стеллит | 20-25% | 1-3% | 45-60% | 5-29% |
Феррохром — сплав хрома с железом, вводимый в жидкую сталь для ее легирования. Вводить хром в чистом виде в сталь очень затруднительно — он медленно растворяются в жидком металле, так как температуры его плавления выше, чем у стали. У феррохрома же температура плавления такая же, как у стали, или ниже.
Нихромы и хромали, устойчивы в интервале 1000-13000C, обладают высоким электросопротивлением, используются для изготовления нагревателей в электрических печах сопротивления.
Добавка к хромоникелевым сплавам кобальта и молибдена придает металлу способность переносить большие нагрузки при 650-900° С. Из этих сплавов делают, например, лопатки газовых турбин.
Стеллит очень твердый сплав, стоек против износа и коррозии; применяется в металлообрабатывающей промышленности, для изготовления режущих инструментов.
Комохром — сплав хрома, кобальта и молибдена безвреден для человеческого организма и поэтому используется в восстановительной хирургии.
Хром входит в состав очень многих марок сталей.
«Нержавейка» — сталь, отлично противостоящая коррозии и окислению, содержит примерно 17-19% хрома и 8-13% никеля. Но этой стали углерод вреден: карбидообразующие «наклонности» хрома приводят к тому, что большие количества этого элемента связываются в карбиды, выделяющиеся на границах зерен стали, а сами зерна оказываются бедны хромом и не могут стойко обороняться против натиска кислот и кислорода. Поэтому содержание углерода в нержавеющей стали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться «чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов. Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием, в нее вводят 25-30% хрома. Такая сталь выдерживает температуры до 1000°С.
Хромолибденовые стали используются для создания фюзеляжей самолетов.
6. Экологические проблемы
(Влияние геологоразведочных работ, добычи и переработки сырья на окружающую среду)
Хром относится к высоко токсичным веществам. Действие на живой организм солей хрома сопровождается раздражением кожи или слизистой оболочки, иногда с образованием язв. Поражают они главным образом верхние дыхательные пути, легкие и глаза. Оксиды хрома менее токсичны, чем чистый металл.
Таблица 4-Предельно допустимые концентрации оксидов хрома
| CrO3 | Cr2 O3 | |
| Разовая в воздухе населенных мест, мг/м3 | 0,01 | 1,0 |
| Суточная в воздухе населенных мест мг/м3 | 0,0015 | - |
| В воде для хозяйственно-питьевого и культурно-бытового водоснабжения, мг/л | 0,1 | 1,0 |
| В воде для рыбохозяйственных целей, мг/л | 0,1 | 0,5 |
При проведении геологоразведочных работ на хромовые руды не требуются специальные меры по защите окружающей среды. При добыче хромовых руд для исключения попадания рудной пыли в воздух населенных пунктов следует выполнять ряд условий: соблюдение определенного расстояния от населенных пунктов, орошение дорог в карьерах и в складах добытой руды.
Наиболее значительное нарушение окружающей среды связано с переработкой хромового сырья, при котором в воздух попадает значительное количество пыли при сухом долблении и сортировке. При мокром обогащении сточные воды нуждаются в отчистке от хрома, его оксидов, что исключает сброс сточных вод в водоемы и требует строительства экранированных шламохранилищ.
Заключение
В данной работе рассмотрены основные вопросы изучения свойств хрома- химического элемента VI группы периодической системы Менделеева.
В первых двух разделах реферата кратко изложены факты открытия и дальнейшего использования хрома, указана особенность распространения хрома в природных месторождениях: хром никогда не встречается в несвязанном состоянии.
Далее рассмотрены физические свойства хрома. Отмеченыаномальные изменения физических свойств хрома при температуре 370С.
Основные разделы реферата посвящены изучению химических свойств хрома и его соединений. Отмечены малая химическая активность хрома, сильные окислительные свойства и высокая токсичность его соединений.
Отдельный раздел посвящен экспериментальному исследованию свойств основных практически значимых соединений хрома — оксидов, гидроксидов и солей. Все опыты подтверждены соответствующими химическими реакциями. Результаты экспериментов могут быть использованы при формировании лабораторного практикума по разделу «Металлы» курса химии школьной программы.
Также в реферате рассмотрены вопросы промышленного применения хрома и экологические проблемы его добычи и переработки.
Литература
1. Лисицын А.Е., Остапенко П.Е. Минеральное сырье. Хром // Справочник. — М.: ЗАО Геоинформмарк, 1999. — 25 с.
2. Салли А., Брендз Э. Хром.- Изд. 2-е переработ. и доп. Перев. с англ. М.: Металлургия, 1971.- 360 с.
3. Химия. Решение задач: учеб. пособие для уч. сред. и ст. шк. возраста/ Авт.- сост. А.Е.Хасанов. — Мн.: Современный литератор, 1999. -448 с.
4. Неорганическая химия. Энциклопедия школьника/ Гл. ред. И.П.Алимарин.- М.: Советская Энциклопедия, 1975.- 384 с.
5. Энциклопедический словарь юного химика/ Сост. В.А.Крицман, В.В.Станцо.- М.: Педагогика, 1982.- 368 с.
Приложение А
(справочное)
Таблица А.1-Важнейшие природные соединения хрома
| Название минерала | Химическая формула |
| Хромистый железняк | FeO*Cr2 O3 или FeCr2 O4 |
| Магнезиохромит | MgO*Cr2 O3 или MgCr2 O4 |
| Алюмохромит | FеО*(Аl, Сr)2 O3 или Fe(Al,Cr)2 O4 |
| Пикотит | (Mg,Fe)(Al, Сr,Fе)2 O3, или (Mg,Fe)O*(AI, Сr,Fе)2 О3 |
| Хромитит | (Fe*Al)2 O3 *2Cr2 O3 |
| Добреслит | FeS*Cr2 S3 |
| Крокоит | PbCrO4 |
| Вокеленит | 2(Pb*Cu)CrO4 (Pb*Cu)3 (PO4 )2 |
| Феницит | 3PbO*2Cr2 O3 |
| Березовит | (PbO)2 *(PbCrO4 )PbCrO3 |
Таблица А.2-Свойства оксидов хрома
| валентность | обозначение | свойства | |
| II | CrO | основной | восстановитель |
| III | Cr2 O3 | амфотерный | |
| VI | CrO3 | кислотный | окислитель |
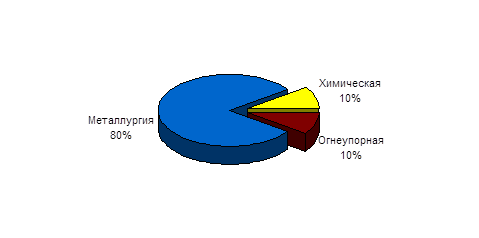
Рисунок А.1- Структура применения хрома по отраслям промышленности
www.ronl.ru
Реферат - Хром - Химия
/>/>/>/>
Реферат
ТЕМА:
Хром
Выполнил: Фединяк С.
Проверил:Гуляева Т.А.
КАРАГАНДА2001г.
Оглавление:
Введение… 3
Нахождение в природе… 3
Происхождение… 4
Получение… 5
Физические свойства… 5
Химические свойства… 6
Применение… 8
Резюме… 10
Список Литературы:… 11
/> /> Введение.К металлам побочных подгрупппериодической системы Д. И. Менделеева относятся все d-элементы. Таких подгрупп 10: скандия, титана, ванадия, хрома,марганца, железа, кобальта, никеля, меди и цинка. Здесь рассматриваются общиехарактеристики подгрупп хрома и семейства железа.
Побочную подгруппу VI группы составляют следующие элементы —хром Cr, молибден Мо и вольфрам W. Хром возглавляет побочную подгруппу 4группы. Его электронная формула +24Cr 1s2|2s22p6|3s23p63d5|4s1
На внешнем энергетическомуровне атомов хрома и молибдена содержится по одному электрону, вольфрама — дваэлектрона, что обусловливает металлический характер этих элементов и отлично отэлементов главной подгруппы. В соответствии с числом валентных электронов онипроявляют максимальную степень окисления +6 и образуют оксиды типа RO3, которым соответствуют кислоты общейформулы h3RO4.Сила кислот закономерноснижается от хрома к вольфраму. Большинство солей этих кислот в воде малорастворимо,хорошо растворяются только соли щелочных металлов и аммония.
Элементы подгруппы хромапроявляют также степени окисления +5, +4, +3, +2. Но наиболее типичны соединениявысшей степени окисления, которые во многом весьма похожи на соответствующиесоединения серы. С водородом элементы подгруппы хрома соединений не образуют.
С ростом порядкового номера вподгруппе возрастает температура плавления металлов. Вольфрам плавится при 3390°С. Это самый тугоплавкий металл. Поэтому его используют для изготовления нитейв электрических лампочках накаливания.
Металлы подгруппы хрома вобычных условиях весьма устойчивы к воздействию воздуха и воды. При нагреваниивзаимодействуют с кислородом, галогенами, азотом, фосфором, углем, кремнием идр. Известны их многочисленные сплавы с другими металлами. Сплавы и самиметаллы — весьма ценные материалы современной техники.
По физическим и химическимсвойствам молибден и вольфрам сходны между собой и несколько отличаются отхрома. Химическая активность металлов в ряду хром — молибден — вольфрам заметнопонижается.
/>/>Нахождение в природе.Хром встречается ввидесоединений в различных минералах. Наиболее распространен минерал хромит, илихромистый железняк FeCr204,богатые месторождениякоторого имеются на Урале и в Казахстане. Массовая доля хрома в земной коресоставляет 0,03%. Хром обнаружен на Солнце, звездах и в метеоритах.
… Еще в 1766 году петербургский профессор химии И. Г.Леман описал новый минерал, найденный на Урале на Березовском руднике, в 15километрах от Екатеринбурга (ныне Свердловск). Обрабатывая камень солянойкислотой, Леман получил изумрудно-зеленый раствор, а в образовавшемся беломосадке обнаружил свинец. Спустя несколько лет, в 1770 году, Березовские рудникиописал академик П. С. Паллас. «Березовские копи, — писал он, — состоят изчетырех рудников, которые разрабатываются с 1752 года. В них наряду с золотомдобываются серебро и свинцовые руды, а также находят замечательный красныйсвинцовый минерал, который не был обнаружен больше ни в одном другом рудникеРоссии. Эта свинцовая руда бывает разного цвета (иногда похожего на цвет киновари),тяжелая и полупрозрачная… Иногда маленькие неправильные пирамидки этого минералабывают вкраплены в кварц подобно маленьким рубинам. При размельчении в порошокона дает красивую желтую краску...».
В 1936 году в Казахстане, в районе Актюбинска, былинайдены огромные залежи хромита — основного промышленного сырья дляпроизводства феррохрома. В годы войны на базе этого месторождения был построенАктюбинский ферросплавный завод, который впоследствии стал крупнейшимпредприятием по выпуску феррохрома и хрома всех марок.
Богат хромистой рудой и Урал. Здесь расположенобольшое число месторождений этого металла: Сарановское, Верблюжьегорское,Алапаевское, Монетная дача, Халиловское и др. По разведанным запасам хромистыхруд Россия занимает ведущее место в мире.
Руды хрома имеются в Турции, Индии, Новой Каледонии,на Кубе, в Греции, Югославии, некоторых странах Африки. В то же время такиепромышленные страны, как Англия, Франция, ФРГ, Италия, Швеция, Норвегия,совершенно лишены хромового сырья, а США и Канада располагают лишь оченьбедными рудами, практически не пригодными для производства феррохрома. Всего жена долю хрома приходится 0,02% земной коры.
/>/>Происхождение.Найденный минерал был назван «сибирским краснымсвинцом». Впоследствии за ним закрепилось название «крокоит».
Образец этогоминерала был в конце XVIII века привезен Палласом в Париж. Крокоитомзаинтересовался известный французский химик Луи Никола Воклен. В 1796 году онподверг минерал химическому анализу. «Все образцы этого вещества, которыеимеются в нескольких минералогических кабинетах Европы, — писал Воклен в своемотчете, — были получены из этого (т. е. Березовского.—С. В.) золотого рудника.Раньше рудник был очень богат этим минералом, однако говорят, что несколько летназад запасы минерала в руднике истощились и теперь этот минерал покупают навес золота, в особенности, если он желтый. Образцы минерала, не имеющиеправильных очертаний или расколотые на кусочки, годятся для использования их вживописи, где они ценятся за свою желто-оранжевую окраску, не изменяющуюся навоздухе… Красивый красный цвет, прозрачность и кристаллическая формасибирского красного минерала заставила минералогов заинтересоваться егоприродой и местом, где он был найден; большой удельный вес и сопутствующая емусвинцовая руда, естественно, заставляли предполагать о наличии свинца в этомминерале...».
Один из друзей Воклена предложил емуназвать элемент хромом (по-гречески «хрома» — окраска) из-за яркого разнообразногоцвета его соединений. Между прочим, слог «хром» в значении «окрашенный» входитво многие термины, не связанные с элементом хромом: слово «хромосома»,например, в переводе с греческого означает «тело, которое окрашивается»; дляполучения цветного, изображения пользуются прибором хромоскопом; фотолюбителямхорошо известны пленки «изопанхром», «панхром», «ортохром»; яркие образования ватмосфере Солнца астрофизики называют хромосферными вспышками и т. д.
Сначала Воклену не понравилосьпредложенное название, поскольку открытый им металл имел скромную серую окраскуи как будто не оправдывал своего имени. Но друзья все же сумели уговоритьВоклена и, после того как французская Академия наук по всей формезарегистрировала его открытие, химики всего мира внесли слово «хром» в спискиизвестных науке элементов.
Свое название хром получил от греческогослова «хрома» — краска за то, что все соединения хрома имеют яркие окраски.
/>/>Получение.Металлический хром получаютвосстановлением оксида хрома (III) принагревании с алюминием:
Сr2О3+ 2Аl = Аl2О3 +2Сr
Металлический хром получаюттакже электролизом водных растворов соединений хрома.
В 1797 году Воклен повторил анализ.Растертый в порошок крокоит он поместил в раствор углекислого калия ипрокипятил. В результате опыта ученый получил углекислый свинец и желтыйраствор, в котором содержалась калиевая соль неизвестной тогда кислоты. Придобавлении к раствору ртутной соли образовывался красный осадок, после реакциисо свинцовой солью появлялся желтый осадок, а введение хлористого оловаокрашивало раствор в зеленый цвет. После осаждения соляной кислотой свинцаВоклен выпарил фильтрат, а выделившиеся красные кристаллы (это был хромовыйангидрид) смешал с углем, поместил в графитовый тигель и нагрел до высокойтемпературы. Когда опыт был закончен, ученый обнаружил в тигле множество серыхсросшихся металлических иголок, весивших в 3 раза меньше, чем исходное вещество.Так впервые был выделен новый элемент.
Основная часть добываемой в мире хромистой рудыпоступает сегодня на ферросплавные заводы, где выплавляются различные сортаферрохрома и металлического хрома.
Впервые феррохром был получен в 1820 годувосстановлением смеси окислов железа и хрома древесным углем в тигле. В 1854году удалось получить чистый металлический хром электролизом водных растворовхлорида хрома. К этому же времени относятся и первые попытки выплавитьуглеродистый феррохром в доменной печи. В 1865 году был выдан первый патент нахромистую сталь. Потребность в феррохроме начала резко расти.
Важную роль в развитии производства феррохрома сыгралэлектрический ток, точнее электротермический способ получения металлов исплавов. В 1893 году французский ученый Муассан выплавил в электропечиуглеродистый феррохром, содержащий 60% хрома и 6% углерода.
В дореволюционной России ферросплавное производстворазвивалось черепашьими темпами. Мизерные количества ферросилиция иферромарганца выплавляли доменные печи южных заводов. В 1910 году на берегуреки Сатки (Южный Урал) был построен маленький электрометаллургический завод«Пороги», который стал производить феррохром, а затем и ферросилиций. Но обудовлетворении нужд своей промышленности не могло быть и речи: потребностьРоссии в ферросплавах приходилось почти полностью покрывать ввозом их из другихстран.
/>/>Физические свойства.Хром — серовато-белыйблестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый,его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит изсмеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56.Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов —хорошо проводит тепло, почти не оказывает сопротивления электрическому току,имеет присущий большинству металлов блеск. Любопытна одна особенность хрома:при температуре около 37°С он ведет себя явно «вызывающе» — многие его физическиесвойства резко, скачкообразно меняются. В этой температурной точке внутреннеетрение хрома достигает максимума, а модуль упругости падает до минимальныхзначений. Так же внезапно изменяются электропроводность, коэффициент линейногорасширения, термоэлектродвижущая сила. Пока ученые не могут объяснить этуаномалию.
Даже незначительные примеси делают хром очень хрупким,поэтому в качестве конструкционного материала его практически не применяют,зато как легирующий элемент он издавна пользуется у металлургов почетом.Небольшие добавки его придают стали твердость и износостойкость. Такие свойстваприсущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%),входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаютсяисключительной твердостью — они-то и позволяют металлу уверенно сопротивлятьсяодному из опаснейших врагов — износу.
В качестве представителяметаллов, относящихся к побочным подгруппам периодической системы, рассмотримхром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранеерассмотренных металлов он, как и все металлы с достраивающимся предпоследнимэлектронным слоем атома, отличается тугоплавкостью и твердостью. По твердостихром превосходит все металлы, он царапает стекло.
/>/>Химические свойства./> /> Расположение электронов на 3d- и4s-орбиталях атома хрома можно представитьсхемой:Отсюда видно, что хром можетпроявлять в соединениях различные степени окисления — от +1 до +6; из нихнаиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Такимобразом, в образовании химических связей участвует не только электрон внешнегоуровня, но и пять электронов d-подуровнявторого снаружи уровня.
Как и у алюминия, наповерхности хрома образуется оксидная пленка Сr2О3.Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться несразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + h3
В азотной и концентрированнойсерной кислотах хром не растворяется, так как его оксидная пленка упрочняется,т. е. хром переходит в пассивное состояние. По этой же причине невзаимодействуют с хромом разбавленные серная и соляная кислоты, содержащиерастворенный кислород. Пассивацию хрома можно устранить очисткой поверхностиметалла.
При высокой температуре хромгорит в кислороде, образуя оксид Cr2О3. Раскаленный хромреагирует с парами воды:
2Cr + ЗН2О= Cr2О3 + ЗН2
Металлический хром принагревании реагирует также с галогенами, галогеноводородами, серой, азотом,фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + h3; 2Cr + N2 = 2CrN
2Cr +3S = Cr2S3; Cr + Si = CrSi
На воздухе хром совершенно неизменяется. Поэтому хромом с помощью электролиза его соединений покрывают —хромируют — стальные изделия для предохранения их от ржавления и механическогоизноса. Эти же качества хром придает своим сплавам с железом — хромистымсталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошлав виде вилок, ножей и других предметов домашнего обихода. Блестящие,серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская»Московского метрополитена.
При химических реакциях атомхрома может отдавать, кроме единственного электрона наружного слоя, до 5электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6).Но, как и все элементы с достраивающимся предпоследним слоем атома, хромпроявляет несколько значений степеней окисления, т. е. кроме высшего и низшиезначения, а именно + 2 и + 3. У металлов с переменной валентностью, как и уэлементов одного и того же периода, например III, с возрастанием степениокисления уменьшается радиус иона. Так, у хрома:
/>
Радиус иона
При этом соблюдается та жесамая закономерность в изменении химических свойств соединений металла свозрастанием его степени окисления, как у элементов одного и того же периода, аименно:
1. С возрастанием степениокисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значенияхстепени окисления и близких значениях ионного радиуса химические свойствагидроксидов элементов оказываются сходными.
Это мы и наблюдаем нагидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2и Mg2; Сг3 и А13; С г6и S6*:
/>
Гидроксиды хрома
Гидроксидыэлементов III периода
Хром образует три рядасоединений:
/>
Познакомимся с важнейшими изэтих соединений. При растворении хрома в кислотах получаются соли, в которыххром двухвалентен, например:
/>
Соединения двухвалентногохрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, вкоторых содержится хром в степени окисления +6: оксид
/>/>Применение.Хром широко используется, как добавочный материал кметаллам, для получения высококачественной стали, подшипников и др. данныйпроцесс называется хромированием.
Молодое Советское государство не могло зависеть откапиталистических стран в такой важнейшей отрасли промышленности, какпроизводство качественных сталей, являющейся основным потребителем ферросплавов.Чтобы воплотить в жизнь грандиозные планы индустриализации нашей страны,требовалась сталь—конструкционная, инструментальная, нержавеющая, шарикоподшипниковая,автотракторная. Один из важнейших компонентов этих сталей — хром.
Уже в 1927—1928 годах началось проектирование истроительство ферросплавных заводов. В 1931 году вошел в строй Челябинскийзавод ферросплавов, ставший первенцем нашей ферросплавной промышленности. Одиниз создателей советской качественной металлургии член-корреспондент Академиинаук СССР В. С. Емельянов в эти годы находился в Германии, куда он былнаправлен для изучения опыта зарубежных специалистов.
Да, в то время наша хромистая руда вывозилась нетолько в Германию, но и в Швецию, Италию, США. И у них же нам приходилосьпокупать феррохром.
Но когда вслед заЧелябинским в 1933 году были построены еще два ферросплавных завода—в Запорожьеи Зестафони, наша страна не только прекратила ввозить важнейшие ферросплавы, втом числе и феррохром, но и получила возможность экспортировать их за границу.Качественная металлургия страны была практически полностью обеспеченанеобходимыми материалами отечественного производства.
«Нержавейка»—сталь, отлично противостоящая коррозии иокислению, содержит примерно 17—19% хрома и 8—13% никеля. Но этой стали углеродвреден: карбидообразующие «наклонности» хрома приводят к тому, что большиеколичества этого элемента связываются в карбиды, выделяющиеся на границах зеренстали, а сами зерна оказываются бедны хромом и не могут стойко оборонятьсяпротив натиска кислот и кислорода. Поэтому содержание углерода в нержавеющейстали должно быть минимальным (не более 0,1%).
При высоких температурах сталь может покрываться«чешуей» окалины. В некоторых машинах детали нагреваются до сотен градусов.Чтобы сталь, из которой сделаны эти детали, не «страдала» окалинообразованием,в нее вводят 25—30% хрома. Такая сталь выдерживает температуры до 1000°С!
В качестве нагревательных элементов успешно служатсплавы хрома с никелем — нихромы. Добавка к хромоникелевым сплавам кобальта имолибдена придает металлу способность переносить большие нагрузки при t = 650—900°С. Из этих сплавов делают, например, лопатки газовых турбин.<sup/>Сплав кобальта,молибдена и хрома («комохром») безвреден для человеческого организма и поэтомуиспользуется в восстановительной хирургии.
Одна из американских фирм недавно создала новыематериалы, магнитные свойства которых изменяются под влиянием температуры. Этиматериалы, основу которых составляют соединения марганца, хрома исурьмы,по мнению ученых, найдут применение в различных автоматических устройствах,чувствительных к колебаниям температуры, и смогут заменить более дорогиетермоэлементы.
Хромиты широко используют и в огнеупорнойпромышленности. Магнезитохромитовый кирпич—отличный огнеупорный материал дляфутеровки мартеновских печей и других металлургических агрегатов. Этот материалобладает высокой термостойкостью, ему не страшны многократные резкие изменениятемпературы.
Химики используют хромиты для получения бихроматовкалия и натрия, а также хромовых квасцов, которые применяются для дублениякожи, придающего ей красивый блеск и прочность. Такую кожу называют «хромом», асапоги из нее «хромовыми».
Как бы оправдывая свое название, хром принимаетдеятельное участие в производстве красителей для стекольной, керамической,текстильной промышленности.
Окись хрома позволила тракторостроителям значительносократить сроки обкатки двигателей. Обычно эта операция, во время которой всетрущиеся детали должны «привыкнуть» друг к другу, продолжалась довольно долго иэто, конечно, не очень устраивало работников тракторных заводов. Выход изположения был найден, когда удалось разработать новую топливную присадку, в составкоторой вошла окись хрома. Секрет действия присадки прост: при сгорании топливаобразуются мельчайшие абразивные частицы окиси хрома, которые, оседая навнутренних стенках цилиндров и других подвергающихся трению поверхностях,быстро ликвидируют шероховатости, полируют и плотно подгоняют детали. Этаприсадка в сочетании с новым сортом масла позволила в 30 раз сократитьпродолжительность обкатки.
Недавно окись хрома приобрела еще одну интересную«специальность»: в США изготовлена экспериментальная магнитофонная пленка,рабочий слой которой содержит не частицы окиси железа, как обычно, а Частицыокиси хрома. Замена оказалась удачной — качество звучания резко улучшилось,пленка стала надежнее в работе. Новинкой в первую очередь предполагаетсяобеспечить блоки магнитной памяти электронно-вычислительных машин.
Почти три четверти века бились ученые над проблемойхромирования, и лишь в 20-х годах нашего столетия проблема была решена. Причинанеудач заключалась в том, что используемый при этом электролит содержалтрехвалентный хром, который не мог создать нужное покрытие. А вот егошестивалентному «собрату» такая задача оказалась по плечу. С этого времени вкачестве электролита начали применять хромовую кислоту — в ней валентностьхрома равна 6. Толщина защитных покрытий (например, на некоторыхнаружных деталях автомобилей, мотоциклов, велосипедов) составляет до 0,1миллиметра. Но иногда хромовое покрытие используют в декоративных целях — дляотделки часов, дверных ручек и других предметов, не подвергающихся серьезнойопасности. В таких случаях на изделие наносят тончайший слой хрома(0,0002—0,0005 миллиметра).
Существует и другой способ хромирования —диффузионный, протекающий не в гальванических ваннах, а в печах. Первоначальностальную деталь помещали в порошок хрома и нагревали в восстановительнойатмосфере до высоких температур. При этом на поверхности детали появлялсяобогащенный хромом слой, по твердости и коррозионной стойкости значительнопревосходящий сталь, из которой сделана деталь. Но (и здесь нашлись свои «но»)при температуре примерно 1000°С хромовый порошок спекается и, кроме того, наповерхности покрываемого металла образуются карбиды, препятствующие диффузиихрома в сталь. Пришлось подыскивать другой носитель хрома; вместо порошка дляэтой цели начали использовать летучие галоидные соли хрома — хлорид или иодид,что позволило снизить температуру процесса.
Хлорид (или иодид) хрома получают непосредственно вустановке для хромирования, пропуская пары соответствующей галоидоводороднойкислоты через порошкообразный хром или феррохром. Образующийся газообразныйхлорид обволакивает хромируемое изделие, и поверхностный слой насыщается хромом.Такое покрытие гораздо прочнее связано с основным материалом, чемгальваническое.
До последнего времени хромировали только металлическиедетали. А недавно советские ученые научились наносить хромовую «броню» наизделия из пластмасс. Подвергнутый испытаниям широко известныйполимер—полистирол, «одетый» в хром, стал прочнее, для него оказались менеестрашными такие известные «враги» конструкционных материалов, как истирание,изгиб, удар. Само собой разумеется, возрос срок службы деталей.
/>/>Резюме.… Прежде чем закончить рассказ о хроме, мы вновь обратимсяк воспоминаниям В. С. Емельянова. «Года два назад,—писал ученый в 1967 году, —я узнал глубоко взволновавшую меня новость, оставшуюся в нашей стране — увы! —незамеченной. Мы продали партию феррохрома Англии — стране, которая всегда быладля нас символом технического прогресса. И вот теперь Англия покупает нашферрохром! Англичане понимают толк в том, что покупают».
/>/>Список Литературы:1. «Химия за 11 класс».Г.Е. Рудзитис, Ф.Г. Фельдман
2. «Неорганическая химияза 9 класс». Ю.В. Ходаков, Д.А. Эпштейн, П.А. Глоризов.
3. «Химия дляподготовительных отделений». Г.П. Хомченко.
4. Интернет.
www.ronl.ru
Реферат google chrome
скачатьРеферат на тему:
План:
- Введение
- 1 История
- 1.1 Анонсирование
- 1.2 Выпуск
- 1.3 Развитие
- 1.4 История версий
- 2 Особенности
- 2.1 Безопасность
- 2.2 Скорость
- 2.3 Стабильность
- 2.4 Интерфейс
- 2.5 Темы
- 2.6 Расширения
- 2.7 Автоматический перевод веб-страниц
- 2.8 Каналы и процесс обновления
- 2.9 Инструменты для веб-мастеров
- 2.10 Служебные страницы браузера
- 2.11 Статистика использования
- 2.12 Лицензии
- 3 Реакция
- 4 Критика Примечания
- 6 Обзоры в прессе
Введение
Эта статья о браузере; об операционной системе см.: Google Chrome OS.
Для термина «Chrome» см. другие значения.
Google Chrome (МФА [ɡuːɡl krəum][5][6][7], MWCD /ˈgü-gəl ˈkrōm/[8][9][10], англ. chrome — хром) — браузер, разрабатываемый компанией Google на основе свободного браузера Chromium и использующий для отображения веб-страниц движок WebKit. Первая публичная бета-версия для Microsoft Windows вышла 2 сентября 2008 года, а первая стабильная — 11 декабря 2008 года. По данным StatCounter браузер находится на третьем месте по популярности, а его рыночная доля в июне 2011 года составила ▲21,80%[11].
1. История
На протяжении шести лет главный исполнительный директор Google Эрик Шмидт не поддерживал идею о создании отдельного браузера. Он указывал на то, что «Google являлась небольшой компанией», и что он не хотел участвовать в «болезненных войнах браузеров». После того, как основатели компании Сергей Брин и Ларри Пейдж наняли нескольких разработчиков Mozilla Firefox и создали демонстрацию Chrome, Шмидт сказал: «она была настолько хорошей, что заставила меня изменить свое мнение».[12]
Первоначально Chrome выпущен только под Microsoft Windows, позднее (9 декабря 2009 года) появились dev- и beta-версии[13][14] для операционных систем Linux и Mac OS X. Первоначально сборки для этих ОС не обладали полной функциональностью аналогичных бета-версий для Windows (например, синхронизацией закладок), но с появлением ветви 5.0.* функциональность сборок для всех ОС стала равной[15].
В 2011 году в Google Chrome 11 был представлен новый логотип, заменивший прежний объёмный[16][17], приблизивший его к логотипу Chromium, но в цветном варианте.
1.1. Анонсирование
2 сентября 2008 года компания Google объявила о выпуске собственного браузера Chrome.
1.2. Выпуск
Первая бета версия браузера была опубликована для Microsoft Windows (начиная с XP и для более поздних версий) 2 сентября 2008 года, была доступна на 43 языках[18]. За первые несколько часов после выпуска в Google было отправлено несколько сотен различных сообщений об ошибках[19].
Chrome быстро приобрел около 1 % рынка[20][21][22][23]. После первоначального всплеска пользователей доля упала до низкого уровня в 0,73 % в октябре 2008 года. Затем начала расти снова, пока в декабре 2008, Chrome снова не преодолел порог в 1 %.
1.3. Развитие
Команда разработчиков Chrome решила использовать в своем браузере движок WebKit, как им посоветовала команда Android. Как и большинство других браузеров Chrome был протестирован внутри компании перед выпуском.
Первая версия Google Chrome полностью прошла Acid1 и Acid2 тесты, но не Acid3 (только 79/100 тестов). Начиная с версии 4.0 Chrome проходит все тесты.
1.4. История версий
| 0.2.149 | 2008-09-02 | 522 | 0.3 | Windows | Первый выпуск[26]. |
| 0.3.154 | 2008-10-29 | Улучшенная производительность и надежность плагинов. Проверка орфографии в полях ввода. Улучшенная поддержка прокси. Обновлено управление окнами и вкладками. | |||
| 0.4.154 | 2008-11-24 | 525 | Менеджер закладок с поддержкой импорта и экспорта. В настройки добавлена секция Безопасность. Новые оповещения о блокировке всплывающих окон. Другие улучшения безопасности. | ||
| 1.0.154 | 2008-12-11 | 528 | Первый стабильный выпуск | ||
| 2.0.172 | 2009-05-24 | 530 | 0.4 | JavaScript работает быстрее на 35 % по тестам SunSpider. Поддержка колеса мыши. Полноэкранный режим. Полностраничное масштабирование. Автозаполнение форм. Сортировка закладок по имени. Прилипание вкладок к браузеру и сторонам экрана. Базовая поддержка Greasemonkey[27]. | |
| 3.0.195 | 2009-10-12 | 532 | 1.2 | Новая страница «новая вкладка» с расширенными настройками. JavaScript на 25 % быстрее. Поддержка HTML5 тегов video и audio. Облегчённые стили | |
| 4.0.249 | 2010-01-25 | 532.5 | 1.3 | Расширения, синхронизация закладок, расширенные средства разработчика, улучшена поддержка HTML5, улучшения производительности, полное прохождение тестов ACID3, поддержка «HTTP byte range», улучшена безопасность, новая экспериментальная возможность anti-reflected-XSS, названная «XSS Auditor»[28]. | |
| 4.1.249 | 2010-03-17 | Всплывающая панель перевода, новые настройки приватности, отключён «XSS Auditor»[29]. | |||
| 5.0.375 | 2010-05-21 | 533 | 2.1 | WindowsMacLinux | Улучшена производительность JavaScript, синхронизация настроек браузера, расширение поддержки HTML5 (Geolocation APIs, App Cache, web sockets, и file drag-and-drop), обновленный менеджер закладок, интегрированный Adobe Flash Player[30][31]. |
| 6.0.472 | 2010-09-02 | 534.3 | 2.2 | Изменения интерфейса тулбаров (напр. перемещены кнопки меню), omnibox и обновление страницы новой вкладки. Автозаполнение форм. Расширены возможности по синхронизации расширений[32] Поддержка WebM видео и PDF (по умолчанию выключена).[33]. | |
| 7.0.517 | 2010-10-21 | 534.7 | 2.3.11.22 | Содержит больше количество исправлений, направленных на стабилизацию браузера. Отложенное назначение SSL-сокетов: SSL запросы с высоким приоритетом теперь всегда отправляются на сервер в первую очередь. Новые опции по управлению cookies. Обновлена страница новой вкладки для возможности добавления веб-приложений. | |
| 8.0.552 | 2010-12-02 | 534.10 | 2.4.9.19 | Chrome Web Store, новый встроенный просмотрщик PDF-файлов с повышенной безопасностью, возможность синхронизации веб-приложений и улучшенная обработка плагинов[34]. Также добавлена страница «about:flags» для представления новых экспериментальных функций, таких как Chrome Instant, отображение вкладок сбоку экрана, меню настроек во вкладках, отключение устаревших плагинов и «облачная» печать. | |
| 9.0.597 | 2011-02-03 | 534.13 | 2.5.9.6 | Поддержка WebGL включена по умолчанию, Adobe Flash «в песочнице», возможность включить Chrome Instant через меню настроек[35], поддержка WebP[36], а также различные экспериментальные функции, такие как предпросмотр печати, GPU ускорение, Google Native Client, CRX-less Web Apps, Web Page Prerendering, Experimental Extension APIs, Disable hyperlink auditing. | |
| 10.0.648 | 2011-03-08 | 534.16 | 3.0.12.18 | Раздел для подключения к Google Cloud Print доступен по умолчанию[37]. Ускорено выполнение JavaScript в связи с использованием Crankshaft, улучшенного компилятора для V8[38]. Поддержка webNavigation API. GPU-ускорение видео в песочнице. Окна настроек отображаются в новой вкладке. Предупреждения о вредоносных программах и отключение устаревших плагинов. Поддержка фоновых расширений. Добавлена синхронизация паролей и включена по умолчанию[39][40]. | |
| 11.0.696 | 2011-04-27 | 534.23 | 3.1.8.12 | HTML5 API для речевого ввода. Новый логотип. | |
| 12.0.742 | 2011-06-07 | 534.30 | 3.2.10.15 | Аппаратное ускорение 3D CSS. Улучшенная защита от загрузки вредоносных файлов. Возможность удалять cookies, оставляемые Adobe Flash, прямо из браузера. Запуск приложений через адресную строку. Улучшена поддержка чтения с экрана. Новая страница настроек синхронизации. Удалена поддержка Gears[41]. Добавлены кнопки печати и сохранения в PDF документах. | |
| 13.0.782 | 2011-06-13 | 535.1 | 3.3.10.10 | Группировка вкладок. Фокусировка на уже открытой вкладке при переходе на идентичную страницу. Ускорение 2D Canvas включено по умолчанию. Instant теперь применяется только к поиску. Добавление Google Instant Pages. Улучшения предпросмотра печати. Экспериментальная страница для новой вкладки[42]. | |
| 14.0.797 | 2011-06-20 | 535.1 | 3.4.4.0 |
| Красный | Устаревшая версия |
| Зелёный | Текущая стабильная версия |
| Голубой | Текущая бета-версия |
| Фиолетовый | Текущая dev-версия |
2. Особенности
Google Chrome направлен на повышение безопасности, скорости и стабильности. 9 июня 2009 года разработчики Google Chrome в своём интервью для неофициального сообщества пользователей обозначили стратегию дальнейшего развития своего продукта, которая заключается в том, что браузер будет иметь максимально высокую скорость работы и минимально допустимый функционал, а все дополнительные функции планируется внедрять при помощи расширений[43].
2.1. Безопасность
Chrome периодически загружает обновления из двух чёрных списков (один для фишинг сайтов и один для сайтов содержащих вредоносное ПО) и предупреждает пользователя, когда тот пытается посетить вредоносный сайт.
Chrome, как правило, создаёт для каждой вкладки отдельный процесс, чтобы не допустить ситуации при которой содержимое одной вкладки имеет возможность влиять на содержимое другой (также, в случае, если процесс обработки содержимого вкладки зависнет, его можно будет завершить без риска потери данных других вкладок)[44]. Процессу вкладки даётся наименьшее число привилегий, процесс может совершать вычисления, но не может производить чтение или запись. Образно выражаясь, вкладка находится в песочнице.
Как правило, плагины (наиболее популярный Adobe Flash Player), не являются частью браузера и не могут быть встроены в песочницу. 30 марта 2010 года Google объявил, что вскоре Adobe Flash будет встроен в браузер, что избавляет пользователя от необходимости загружать и устанавливать его. Обновляться Flash Player будет также автоматически[45]. Начиная с версии 5.0.375.86 Adobe Flash Player был интегрирован[46].
При загрузке исполняемого файла (например, с расширением EXE, DLL или BAT) сначала необходимо подтвердить загрузку, нажав кнопку Сохранить, которая появляется на панели загрузок. Это позволяет предотвратить автоматическую загрузку вредоносного программного обеспечения на компьютер.
Браузер поддерживает режим инкогнито. Страницы, которые просматриваются в окне в режиме инкогнито, не появятся в истории браузера или истории поиска, а также не оставят на компьютере других следов, таких как файлы cookie, они автоматически удаляются когда пользователь закроет это окно. Тем не менее, все файлы, которые будут загружены, или закладки, которые будут созданы, останутся в целости и сохранности.
Как предупреждает сам браузер, переход в режим инкогнито не влияет на поведение других пользователей, серверов или программ и не позволяет защититься от:
- Веб-сайтов, которые собирают информацию о вас или передают её другим
- Поставщиков услуг Интернета или их сотрудников, которые отслеживают, какие страницы вы посещаете
- Вредоносного ПО, которое отслеживает нажатие клавиш клавиатуры
- Слежки тайными агентами
- Людей, которые стоят у вас за спиной
2.2. Скорость
Google Chrome использует высокопроизводительный[47][48][49] движок обработки JavaScript V8. Также для ускорения загрузки страниц Google Chrome может использовать упреждающее чтение DNS[50].
2.3. Стабильность
В Chrome используется многопроцессная архитектура, и каждой вкладке или плагину, в большинстве случаев, соответствует отдельный процесс. Эта процедура, называемая изоляцией процессов, исключает вероятность того, что вкладки будут мешать друг другу[51]. Также, злоумышленник, используя одну вкладку, не сможет подсмотреть, что происходит в другой, и, если на одной вкладке произойдет сбой, это не помешает работе всего браузера — нужно будет просто закрыть данную вкладку.
Chrome включает в себя диспетчер задач, который позволяет посмотреть, как сайты и плагины используют оперативную память, процессор и интернет-канал пользователя, а также — завершить их работу в случае необходимости.
2.4. Интерфейс
По умолчанию интерфейс Google Chrome включает кнопки: назад, вперед, обновить/остановить загрузку, добавить текущую страницу в закладки, перейти на главную страницу (домой). Кнопка перехода на главную страницу может быть отключена.
Панель вкладок является основным компонентом интерфейса и находится в верхней части окна, а не под строкой адреса. Это изменение выглядит достаточно контрастно по сравнению со многими другими браузерами. Вкладка легким перетаскиванием на свободное место может быть перенесена в отдельное окно (возможен также и обратный вариант). Каждая вкладка имеет свой собственный набор элементов, в том числе Omnibox.
Omnibox — это адресная строка, которая находится наверху каждой вкладки, она совмещает в себе адресную строку и строку поиска. Omnibox перенаправляет запрос в поисковую систему в том случае, если адрес не соответствует правилам написания URL — к примеру, не содержит точек, косых черт, содержит пробелы в начале адреса и т. д. При вводе поискового запроса Google, используя функцию поиска в Интернете «Мне повезет», предлагает первый по списку URL-адрес (например, при вводе в адресную строку слова «яндекс» браузер автоматически предложит вариант «www.yandex.ru»). Также автодополнение предлагается поиском по закладкам и истории ранее посещенных страниц. В браузере возможен вызов различных поисковых машин прямо из адресной строки. Для этого надо ввести сокращение для данной поисковой машины (например, букву 'g' для google), затем нажать клавишу «Пробел» и ввести поисковый запрос. Сокращения для поисковых машин можно задавать самостоятельно. При посещении сайтов браузер автоматически копирует оттуда строку поисковых запросов и в следующий раз при вводе этого сайта автоматически будет предложен поиск с использование его поисковой системы.
Одной из отличительных черт Chrome является страница быстрого доступа, которая может заменять домашнюю страницу и открывается при создании новой вкладки. На странице быстрого доступа содержится 8 наиболее посещаемых веб-сайтов (отображаются в виде маленьких снимков веб-страниц), недавно закрытые вкладки, советы по использованию Chrome и синхронизация закладок[52]. По желанию пользователь может изменить внешний вид страницы, добавив или удалив одну из опций.
Chrome имеет менеджер закладок, доступный из меню. Слева от Omnibox имеется кнопка (на ней изображена звёздочка), при нажатии на которую текущая страница добавляется в закладки[53]. На данный момент эта функция не доступна в версиях Chrome на платформах Linux и Mac[54]. В 6-ой версии эта кнопка была убрана вместе с опцией в параметрах, а звёздочка переместилась в правую часть Omnibox, как у браузера Mozilla Firefox.
Окно «Параметры Google Chrome» содержит три вкладки: «Основные», «Личные материалы» и «Расширенные». Вкладка «Основные» содержит настройки: домашней страницы, поисковых систем и браузера по умолчанию. Вкладка «Личные материалы» содержит настройки: синхронизации закладок, сохранение паролей, автозаполнение форм, возможность импорта данных о работе из другого браузера и настройку тем. Вкладка «Расширенные» содержит настройки: конфиденциальности, сети, переводчика, загрузок и безопасности.
Chrome позволяет пользователю создавать локальные ярлыки на приложения (а именно — их страницы). При запуске такого ярлыка страница, на которую он ведет, открывается в Chrome, но без элементов интерфейса (за исключением заголовка окна).
При загрузке файла с веб-сайта в нижней части вкладки появляется панель загрузок, на которой отображается ход загрузки. Список всех загруженных файлов находится на странице загрузок.
2.5. Темы
Начиная с версии 3.0, пользователи могут установить темы изменяющие внешний вид браузера. Была создана галерея, которая включала в себя как темы от Google, так и темы от третьих лиц.
2.6. Расширения
Расширения Google Chrome позволяют расширить возможности и функции браузера. Та или иная функция может быть полезна для некоторых людей, но не для всех. Расширения позволяют добавлять в Google Chrome только нужные возможности, избегая накопления функций, которые не используются. Google создал специальную галерею расширений от третьих лиц.
Впервые расширения появились в стабильной версии Chrome 4.0, а галерея была официально открыта 25 января 2010 года. На момент открытия в ней было уже 1500 расширений.
2.7. Автоматический перевод веб-страниц
Функция перевода страниц стала доступна начиная с версии 4.1.249.1036 (от 17 марта 2010 года).
При посещении страниц, язык которых отличен от используемого в интерфейсе Google Chrome, в верхней части страницы автоматически появляется панель с предложением перевести веб-страницу.
Данная функция использует сервис Google Translate. Пользователь может выбрать язык и сайт, содержание которых в будущем переводить не требуется. Также пользователь может полностью отключить функцию перевода в настройках.
2.8. Каналы и процесс обновления
8 января 2009 года Google представил три канала обновления: Stable (стабильный), Beta (бета), Developer (для разработчиков). До внесения этого изменения было только два канала: Beta и Developer. Это было сделано с целью того, чтобы пользователи быстрее получали более стабильные версии.
22 июля 2010 года Google объявил о повышении скорости обновления стабильных версий браузера — цикл их выхода сокращается до шести недель (вместо прежних трёх месяцев)[55]. В связи с этим запускается дополнительный, четвёртый, канал обновления — «Canary» («Канарейка», по аналогии с канарейками, используемыми шахтёрами для контроля опасных концентраций газов в угольных шахтах), на котором будут тестироваться изменения, связанные с риском. Данный канал будет схож с каналом Developer, однако в случае необходимости он будет получать дополнительные обновления, поэтому номера его версий будут превышать номера версий последнего. Отдельной особенностью Chrome Canary является его параллельная (независимая от какой-либо другой, уже установленной версии) установка в систему и, соответственно, независимые обновления[56]. Первоначально доступен только для Windows-платформы[57].
Google Chrome автоматически обновляется при обнаружении новой версии браузера. Процесс обновления происходит в фоновом режиме и не требует от пользователя никаких действий. Если Google Chrome был открыт во время обновления, достаточно закрыть и открыть браузер для запуска новой версии[58].
2.9. Инструменты для веб-мастеров
Веб-инспектор: Для запуска необходимо, нажать правой кнопкой мыши на любом компоненте веб-страницы и выбрать «Просмотр кода элемента». Появится диалоговое окно, в котором указываются элементы и ресурсы, связанные с этим компонентом. Также имеется возможность, просмотреть иерархическое представление модели DOM и консоль JavaScript. (Чтобы открыть консоль JavaScript, нужно нажать среднюю кнопку в нижней части. В ОС Windows, также можно открыть меню Страница > Разработчикам > Консоль JavaScript.)
Диспетчер задач: Для запуска необходимо: открыть меню «Страница» и выбрать «Разработчикам» (в ОС Windows). Выбрать «Диспетчер задач». Также можно воспользоваться быстрыми клавишами Shift + Escape. В диспетчере задач показываются все процессы, запущенные в Google Chrome, и используемые этими процессами ресурсы (память, процессор и сеть).
Отладчик JavaScript: Для запуска необходимо: открыть меню «Страница» и выбрать «Разработчикам» (в ОС Windows). Выбрать «Отладка JavaScript». Откроется командная строка отладчика JavaScript, который можно использовать для отладки запущенных процессов.
2.10. Служебные страницы браузера
Для запуска необходимо: ввести любую из перечисленных ниже команд в адресной строке для просмотра дополнительной информации.
| about:about | Список Служебных страниц |
| about:cache | Показать содержимое кеша. |
| about:crash (устаревшая, не используется)about:kill | Отображет страницу с сообщением о неполадке. В русской версии Chrome сообщение начинается с текста «Опаньки…». |
| about:credits | Разработки применяемые в Chrome. |
| about:dns | Показывает записи DNS |
| about:flags | Разблокировать скрытые (экспериментальные) возможности. |
| about:histograms | Графики различных статистических параметров |
| about:inducebrowsercrashforrealz | Вызвать сбой Google Chrome. Для просмотра разработчиками процессов, происходящих в системе при сбое. |
| about:memory | Показывает информацию об используемой приложением и вкладками памяти |
| about:plugins | Показать установленные плагины. |
| about:shorthang | Вызвать «зависание» вкладки. Для тестирования разработчиками защиты от зависания. |
| chrome://net-internals/ | Информация о соединениях. |
| about:terms | Условия предоставления услуг Google Chrome. |
| about:versionabout: | Номер версии и сборки. Аналог — about:. |
| view-source:[URL] | Просмотр исходного кода страницы |
2.11. Статистика использования
Chrome автоматически отправляет информацию об использовании браузера в Google. Часть механизмов сбора подобной информации может быть отключена пользователем, а часть — нет[59].
| Установка | Случайно сгенерированный знак, включенный в установочную программу. Используется для измерения процента удачных установок Google Chrome[60] | При установке | Нет |
| RLZ-идентификатор[61] | Зашифрованная строка, по данным Google, содержащая не идентифицирующую пользователя информацию о том, как браузер был скачан и о первой неделе его использования. Используется для определения эффективности рекламных кампаний[60] Google предоставляет исходный код для расшифровки этой строки.[62]. |
| Частично[60][63] |
| ID клиента[64] | Уникальный идентификатор, а также данные об использовании и сбоях программы. | Неизвестно | Да[65] |
| Подсказка[64] | Текст, введенный в адресной строке | Во время набора | Да |
| Страница не найдена | Текст, введенный в адресной строке | При сообщении «Сервер не найден» | Да |
| Сборщик ошибок | Подробности о сбоях | Неизвестно | Да[65] |
В марте 2010 года Google ввела новый способ сбора статистики об установках. Уникальный идентификатор, включенный в Chrome, теперь используется лишь при первом подключении Google Update к серверу компании. После получения ответа от сервера идентификатор удаляется[66].
2.12. Лицензии
Браузер распространяется на условиях специальной собственнической лицензии EULA.
Часть кода браузера[67][68], или весь код[69] открыт под названием Chromium под лицензией типа BSD и другими.
Примерно до 9 сентября 2008 года EULA содержало абзац, дававший Google безотзывную неисключительную лицензию на безвозмездное использование, создание производных работ, распространение и публикацию в рекламных целях всей передаваемой через браузер информации. Подобные абзацы также были, например, в соглашениях ICQ и Facebook, а в данном случае оно взято из «Условий оказания Услуг Google»[70]. После критики в блогах и на Slashdot данный абзац был убран из соглашения браузера[71][72].
3. Реакция
Во время запуска бета-версии браузера осенью 2008 года пресса положительно восприняла браузер от Google, при этом реакция многих изданий была исключительно восторженной, отмечая то, что Google создала превосходный браузер[73].
4. Критика
- Microsoft Windows 7 поддерживает технологию мультитач, поддержка которой до сих пор не реализована в браузере Google Chrome (по данным на 23.02.2011).
- Браузер Google Chrome не поддерживает формат APNG.
Примечания
- Google Chrome Releases — только стабильные - googlechromereleases.blogspot.com/search/label/Stable updates (англ.) блог с анонсами стабильных версий Google Chrome
- Google Chrome Releases — только beta версии - googlechromereleases.blogspot.com/search/label/Beta updates (англ.) блог с анонсами бета версий Google Chrome
- Google Chrome Releases — только Dev update - googlechromereleases.blogspot.com/ (англ.) — блог с анонсами тестовых версий Google Chrome
- Google Chrome Terms of Service - www.google.com/chrome/intl/en/eula_text.html
- «google» перевод английский-русский - lingvo.abbyyonline.com/ru/en-ru/google. Lingvo.abbyyonline.com.
- «chrome» перевод английский-русский - lingvo.abbyyonline.com/ru/en-ru/chrome. Lingvo.abbyyonline.com.
- How to pronounce Google - inogolo.com/query.php?desc=786&key=1 (англ.). inogolo.com.
- Google - Definition and More from the Free Merriam-Webster Dictionary - www.merriam-webster.com/dictionary/google (англ.). Merriam-Webster, Incorporated.
- Chrome - Definition and More from the Free Merriam-Webster Dictionary - www.merriam-webster.com/dictionary/chrome (англ.). Merriam-Webster, Incorporated.
- Чаще - news.yandex.ru/yandsearch?text="гугл хром"&rpt=nnews2&grhow=clutop по-русски называется фактически переводным вариантом Гугл Хром, в то время как транскрипционным вариантом является Гугл Кроум.
- Top 5 browsers on July 11 - gs.statcounter.com/#browser-ww-monthly-201107-201107-bar (англ.). StatCounter (Июль 2011).
- Julia Angwin Sun Valley: Schmidt Didn’t Want to Build Chrome Initially, He Says - blogs.wsj.com/digits/2009/07/09/sun-valley-schmidt-didnt-want-to-build-chrome-initially-he-says/. WSJ Digits Blog (9 июля 2009).
- Выпущена бета-версия Google Chrome для Linux - www.google.com/chrome/intl/ru/w00t.html . Google (???).
- Страница загрузки - www.google.com/chrome?platform=linux .
- Новая бета-версия Google Chrome для Mac и Linux - chrome.blogspot.com/2010/02/new-beta-of-google-chrome-for-mac-with.html (англ.)
- Steve Rura A fresh take on an icon - chrome.blogspot.com/2011/03/fresh-take-on-icon.html (англ.). Google Inc. (21 марта 2011 года).
- Adam Ostrow Google Chrome Gets a New Icon [PIC - mashable.com/2011/03/21/google-chrome-icon/] (англ.). Mashable (21 марта 2011 года).
- It was when not if... Google Chrome - www.doeswhat.com/2008/09/02/it-was-when-not-if-google-chrome/ (September 2008).
- Issues — chromium — Google Code - code.google.com/p/chromium/issues/list
- Pichai, Sundar; Upson, Linus A fresh take on the browser - googleblog.blogspot.com/2008/09/fresh-take-on-browser.html. Google Blog (2008-09-01).
- Google Chrome update: First screenshot, and live-blog alert - news.cnet.com/8301-17939_109-10030025-2.html. CNet (2008-09-01).
- Google launches Chrome web browser - www.cbc.ca/technology/story/2008/09/01/google-browser.html. The Canadian Press (September 2, 2008).
- Come on Google... Chrome for Mac? - www.doeswhat.com/2008/11/22/come-on-google-chrome-for-mac/ (November 2008).
- Chromium.org - dev.chromium.org/getting-involved/dev-channel/release-notes/
- ChangeLog - v8 - code.google.com/p/v8/source/browse/trunk/ChangeLog.
- Official Google Blog: A fresh take on the browser - googleblog.blogspot.com/2008/09/fresh-take-on-browser.html
- Google Chrome Releases: Stable Update: Google Chrome 2.0.172.28 - googlechromereleases.blogspot.com/2009/05/stable-update-google-chrome-2017228.html
- Google Chrome Releases: Stable Channel Update - googlechromereleases.blogspot.com/2010/01/stable-channel-update_25.html
- Google Chrome Releases: Stable Channel Update - googlechromereleases.blogspot.com/2010/03/stable-channel-update.html 2010-03-17
- Brian Rakowski Evolving from beta to stable with a faster version of Chrome - googleblog.blogspot.com/2010/05/evolving-from-beta-to-stable-with.html. Google (2010-05-25).
- Adobe Flash Player support now enabled in Google Chrome’s stable channel - chrome.blogspot.com/2010/06/adobe-flash-player-support-now-enabled.html (2010-06-30).
- Dev Channel Update - googlechromereleases.blogspot.com/2010/06/dev-channel-update_17.html. Google Chrome Releases (2010-06-17).
- Dev Channel Update - googlechromereleases.blogspot.com/2010/07/dev-channel-update.html. Google Chrome Releases (2010-07-02).
- Stable, Beta Channel Updates - googlechromereleases.blogspot.com/2010/12/stable-beta-channel-updates.html. Google.
- Safer plug-ins, faster search, and richer graphics - chrome.blogspot.com/2010/12/safer-plug-ins-faster-search-and-richer.html. Google.
- WebP Home - code.google.com/speed/webp/. Google.
- Dev Channel Update - googlechromereleases.blogspot.com/2010/12/dev-channel-update_16.html. Google.
- A New Crankshaft for V8 - blog.chromium.org/2010/12/new-crankshaft-for-v8.html. Google.
- Stephen Shankland Faster JavaScript gets Google Chrome 10 spotlight - news.cnet.com/8301-30685_3-20040627-264.html (англ.). CNET (8 марта 2011).
- Sebastian Anthony Chrome updated with faster JavaScript engine, tabbed settings and password sync - downloadsquad.switched.com/2011/03/08/chrome-updated-with-faster-javascript-engine-tabbed-settings-an/ (англ.). Switched DownloadSquad (8 марта 2011).
- Chrome Stable Release - googlechromereleases.blogspot.com/2011/06/chrome-stable-release.html (June 7, 2011).
- Google Chrome Releases: Dev Channel Update - googlechromereleases.blogspot.com/2011/06/dev-channel-update_08.html.
- John Migman. Интервью с разработчиками - my-chrome.ru/2009/06/intervyu-s-razrabotchikami-google-chrome/ . My-Chrome Blog (???).
- Chung, Marc chromes-process model explained - blog.marcchung.com/2008/09/chromes-process-model-explained.html (2008-09-05).
- Paul, Ryan Google bakes Flash into Chrome, hopes to improve plug-in API - arstechnica.com/web/news/2010/03/google-bakes-flash-into-chrome-hopes-to-improve-plugin-api.ars (March 2010).
- Мой Google Chrome > Google Chrome 5.0.375.86 Stable - my-chrome.ru/2010/06/google-chrome-5-0-375-86-stable/
- Design Elements - code.google.com/apis/v8/design.html (англ.)
- Speed test: Google Chrome beats Firefox, IE, Safari - news.cnet.com/8301-17939_109-10030888-2.html (англ.)
- Быстрый запуск веб-приложений - www.google.ru/chrome/intl/ru/more/speed.html
- Работа с данными - www.google.com/support/chrome/bin/answer.py?hl=ru&answer=114836
- Chromium Developer Documentation Process Models - dev.chromium.org/developers/design-documents/process-models (2008-09-03).
- Google Chrome after a year: Sporting a new stable release — Official Google Blog - googleblog.blogspot.com/2009/09/google-chrome-after-year-sporting-new.html
- Add a Bookmark Button to Google Chrome’s Toolbar — Google Chrome — Lifehacker - lifehacker.com/5350737/add-a-bookmark-button-to-google-chromes-toolbar
- Google Issue 21152: Expose UI for bookmark menu on all platforms - code.google.com/p/chromium/issues/detail?id=21152 (September 2009).
- Anthony Laforge Release Early, Release Often - blog.chromium.org/2010/07/release-early-release-often.html (2010-07-22).
- Huan Ren Install/run two Google Chrome builds side by side - groups.google.com/a/chromium.org/group/chromium-dev/browse_thread/thread/bf71d02dae94eb88?pli=1 (2010-07-22).
- Google Chrome Google Chrome Canary Build - tools.google.com/dlpage/chromesxs (2008-09-03).
- [1] - www.google.com/support/chrome/bin/answer.py?answer=95414 Справка Google Chrome об обновлении
- Communications between Chromium/Google Chrome and service providers - blog.chromium.org/2008/10/google-chrome-chromium-and-google.html
- ↑ 1234 Google Chrome Privacy Whitepaper - www.google.com/intl/en/landing/chrome/google-chrome-privacy-whitepaper.pdf
- &rlz= in Google referrer: Organic traffic or AdWords? - foliovision.com/2008/12/09/adwords-ppc-organic-rlz/.
- In The Open, For RLZ - google-opensource.blogspot.com/2010/06/google-chromes-rlz-library-is-now-open.html (2010-06-02).
- Браузер должен быть скачан с официального сайта Google Chrome - www.google.com/chrome для отключения RLZ-идентификатора
- ↑ 12Google Reacts to Some Chrome Privacy Concerns - blogoscoped.com/archive/2008-09-09-n68.html.
- ↑ 12 Управляется настройкой «Помочь улучшить Google Chrome, автоматически отправляя в Google статистику использования и отчеты о сбоях». По умолчанию отключено.
- Google Chrome Unique Identifier Change - www.theregister.co.uk/2010/03/16/google_chrome_unique_identifier_change/ (2010-03-16).
- Google Code — Chromium - code.google.com/chromium/: «Chromium is the open-source project behind Google Chrome.»
- Chromium Developer Documentation - dev.chromium.org/: «Google Chrome is built with open source code from Chromium»
- Google Chrome Terms of Service - www.google.com/chrome/intl/en/eula_text.html (англ.). Google (15 августа 2008).
- Google Terms of Service - www.google.com/accounts/TOS
- Google Amends Chrome License Agreement After Objections - www.pcworld.com/businesscenter/article/150637/google_amends_chrome_license_agreement_after_objections.html (англ.). PC World (3 сентября 2008).
- Пользовательское соглашение на браузер Google Chrome подверглось резкой критике - net.compulenta.ru/368880/ . Компьюлента (4 сентября 2008).
- Don Reisinger Giving Google Chrome A Spin. This Thing Moves Fast. - www.webcitation.org/5yOICYoOp (англ.). TechCrunch (2008-09-02). — «All in all, Google Chrome, after just a little time using it, is superb. It’s not only fast, but it’s useful. It’s not only elegant, but it understands what you really want to do with a browser. And although it suffers from some setbacks that shouldn’t be overlooked, it’s still a highly-capable browser. Download Chrome. You won’t regret it.» Архивировано из первоисточника - techcrunch.com/2008/09/02/giving-google-chrome-a-spin-this-thing-moves-fast/ 2 мая 2011.
6. Обзоры в прессе
- Ionut Ilascu Google Chrome Inside Out - www.softpedia.com/reviews/windows/Google-Chrome-Inside-Out-Review-92938.shtml (англ.). Softpedia (3 сентября 2008).
- Lucian Parfeni Google Chrome 5 Beta Review - www.softpedia.com/reviews/linux/Google-Chrome-Review-137377.shtml (англ.). Softpedia (13 марта 2010).
- Craig Grannell Google Chrome for Mac review - www.techradar.com/reviews/pc-mac/software/home-and-reference-software/google-chrome-for-mac-702605/review (англ.). TechRadar (14 июля 2010). — Can Chrome beat Safari to claim the title of best browser on the Mac?.
- Nick Mediati Google Chrome 5 - www.pcworld.com/article/150579/google_chrome_web_browser.html (англ.). PCWorld. — «Google's streamlined and speedy browser offers strong integrated search and an intriguing alternative to Firefox and Internet Explorer.»
- Seth Rosenblatt Google Chrome — CNET Editor's Review - download.cnet.com/Google-Chrome/3000-2356_4-10881381.html?tag=rb_content;main (англ.). CNET (8 марта 2011).
wreferat.baza-referat.ru

 2Cr+3 Cl3-
2Cr+3 Cl3- 2Cr2 O3
2Cr2 O3  Cr2+2 S3-2
Cr2+2 S3-2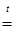 2Cr+3 N-3
2Cr+3 N-3 Cr4+3 Si3-4
Cr4+3 Si3-4 Cr+3 B-3
Cr+3 B-3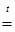 Cr4+3 C3-4
Cr4+3 C3-4