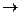Большая Энциклопедия Нефти и Газа. Железо алюминий хром
Железо-хромо-алюминиевый сплав - Большая Энциклопедия Нефти и Газа, статья, страница 1
Железо-хромо-алюминиевый сплав
Cтраница 1
Железо-хромо-алюминиевый сплав № 2 ( Х25Ю5 по ГОСТу № 5632 - 51 является тройным ферритовым твердым раствором; сплав содержит 23 - 26 % Сг, 4 5 - 5 5 % А1, 0 5 % Ti и примеси С, Si, Mn, Ni, S, Р, вошедшие в состав сплава с шихтой в процессе его плавки. Основными составляющими сплава являются железо, хром и алюминий. [1]
Железо-хромо-алюминиевый сплав № 2 ( Х25Ю5 по ГОСТу № 5632 - 51) является тройным ферритовым твердым раствором; сплав содержит 23 - 26 % Сг, 4 5 - 5 5 % А1, 0 5 % Ti и примеси С, Si, Mn, Ni, S, Р, вошедшие в состав сплава с шихтой в процессе его плавки. Основными составляющими сплава являются железо, хром и алюминий. [2]
Железо-хромо-алюминиевый сплав № 2 является более устойчивым в азотной кислоте, чем нержавеющая сталь 18 / 8; потери на растворение сплава № 2 в азотной кислоте за 100 час. [4]
Железо-хромо-алюминиевый сплав № 2 является весьма устойчивым при высоких температурах в газовых средах, содержащих серу и ее соединения с кислородом и водородом. [6]
Железо-хромо-алюминиевый сплав № 2 является более устойчивым в азотной кислоте, чем нержавеющая сталь 18 / 8; потери на растворение сплава № 2 в азотной кислоте за 100 час. [8]
Железо-хромо-алюминиевый сплав № 2 является весьма устойчивым при высоких температурах в газовых средах, содержащих серу и ее соединения с кислородом и водородом. [10]
Таким образом железо-хромо-алюминиевый сплав № 2 по высокой химической устойчивости при высоких температурах в газовых средах, содержащих углерод, серу и их соединения с кислородом, водород и сероводород, азот и другие химически активные соединения, не имеет себе равных среди металлических сплавов на основе железа, никеля с ферритовой и аустени-товой ( для железных и никелевых сплавов) структурами. [12]
Знание механических свойств железо-хромо-алюминиевых сплавов необходимо для расчета конструкций реакторов пиролизных установок, разработки технологии изготовления сплавов и определения условий их эксплуатации, как прочных и жаропрочных материалов при комнатной и высоких температурах. [14]
С увеличением содержания хрома сопротивление окислению железо-хромо-алюминиевых сплавов, - как следует из хода кривых / и / /, резко возрастает; сплавы с 25 % Сг имеют наименьшие потери на окисление, при содержании 5 - 6 % А1 они составляют 0 10 г лг2 час, а при содержании 8 - 10 % А1 - 0 064 г-м 2-час. [15]
Страницы: 1 2 3
www.ngpedia.ru
Лекция 21. Конструкционные металлы. Алюминий. Хром. Железо
Химия  Лекция 21. Конструкционные металлы. Алюминий. Хром. Железо
Лекция 21. Конструкционные металлы. Алюминий. Хром. Железо
просмотров - 17
Ключевые слова: физические и химические свойства металлов, оксиды, гидроксиды, соли металлов.
Алюминий– основной представитель металлов главной подгруппы III группы периодической системы. Внешняя электронная конфигурация - 3s23p1, в соединениях проявляет степень окисления +3.
Нахождение в природе. По распространенности занимает третье место среди всех элементов (после О и Si) и первое среди металлов. Важнейшие минералы: бокситы – смесь гидроксидов Al(OH)3 и AlOOH; алюмосиликаты – (Na,K)2O∙Al2O3∙2SiO2; корунд (глинозем) – Al2O3; криолит – 3NaF∙AlF3.
Физические свойства.Серебристо-белый металл, плотность (при 20°С) 2698,9 кг/м3; tпл 660,24°С; tкип около 2500°С;
Химические свойства. Алюминий является активным металлом, сильным восстановителем. Но наличие защитной оксидной пленки на его поверхности затрудняет его взаимодействие со многими окислителями при обычных условиях. При 25ºС алюминий образует с хлором, бромом и иодом соответственно AlCl3, AlВr3, AlI3. Реакции с фтором, кислородом, азотом, серой происходят при достаточно высоких температурах.
В отличие от щелочных и щелочноземельных металлов, алюминий при обычных условиях не реагирует с водой, так как защищен пленкой нерастворимого в воде оксида. При этом эта пленка легко растворяется в растворах кислот и щелочей, в связи с этим не защищает алюминий от взаимодействия с ними:
2Al + 6HCl → 2AlCl3 + 3h3↑
Al + 4HNO3 → Al(NO3)3 + NO↑ + 2h3O
2Al + 2NaOH + 6h3O → 2Na[Al(OH)4] + 3h3↑
Исключением являются концентрированные серная и азотная кислоты, в которых алюминий пассивируется.
Важным свойством алюминия является его способность восстанавливать некоторые металлы из их оксидов при высокой температуре. Этот способ получения металлов принято называть алюмотермией: 4Al + 3MnO2 → 3Mn + 2Al2O3
Хром. Внешняя электронная конфигурация атома хрома 3d54s1. В соединениях обычно проявляет степени окисления +2, +3, +6, среди них наиболее устойчивы Сr3+.
Нахождение в природе.Хром – довольно распространенный элемент на Земле. Его кларк (среднее содержание в земной коре) составляет 8,3·10–3%. Хром никогда не встречается в свободном состоянии. В хромовых рудах практическое значение имеет только хромит FeCr2O4.
Физические свойства. Хром - твердый, тяжелый, тугоплавкий металл. Плотность 7190 кг/м3; tпл 1890 °С; tкип 2480 °С.
Химические свойства. Хром химически малоактивен. При обычных условиях устойчив к кислороду и влаге, но соединяется с фтором, образуя CrF3. Выше 600°С взаимодействует с парами воды, давая Сr2О3; с азотом - Cr2N, CrN; с углеродом - Сr3С2; с серой - Cr2S3. Со многими металлами хром дает сплавы. Хром загорается в кислороде при 2000°С с образованием темно-зеленого оксида хрома (III) Сr2О3. Помимо оксида (III), известны других соединения с кислородом, к примеру CrO, СrО3, получаемые косвенным путем. Хром легко реагирует с разбавленными растворами соляной и серной кислот с образованием хлорида и сульфата хрома и выделением водорода; «царская водка» и азотная кислота пассивируют хром. С увеличением степени окисления возрастают кислотные и окислительные свойства хрома.
Железо. Конфигурация внешней электронной оболочки атома 3d64s2. Железо проявляет переменную валентность (наиболее устойчивые степени окисления +2 и +3).
Нахождение в природе. По распространенности в земной коре занимает второе место среди металлов. Для извлечения железа используются в основном такие руды, как гематит (Fe2O3), магнитные железняки (Fe3О4), бурые железняки (НFeO2· nh3O), а также шпатовые железняки (FeСО3).
Физические свойства. Плотность (20°C) 7874 кг/м3, tпл 1539°С, tкип 3200°С.
Химические свойства. С кислородом железо образует оксид (II) FeO, оксид (III) Fe2O3 и оксид (II,III) Fe3O4 (соединение FeO c Fe2O3, имеющее структуру шпинели). Во влажном воздухе при обычной температуре железо покрывается рыхлой ржавчиной (Fe2O3·nh3O). Вследствие своей пористости ржавчина не препятствует доступу кислорода и влаги к металлу и в связи с этим не предохраняет его от дальнейшего окисления. При нагревании в водяном паре железо окисляется с образованием Fe3O4 (ниже 570 °С) или FeO (выше 570 °С) и выделением водорода.
Железо легко реагирует с галогенами и галогеноводородами, давая соли, к примеру хлориды FeCl2 и FeCl3. При нагревании железа с серой образуются сульфиды FeS и FeS2. Карбиды железа - Fe3C (цементит) и Fe2C (е-карбид) - выпадают из твердых растворов углерода в железе при охлаждении. Fe3C выделяется также из растворов углерода в жидком железе при высоких концентрациях С. При нагревании железо энергично реагирует с кремнием и фосфором, образуя силициды (к примеру, Fe3Si и фосфиды (к примеру, Fe3P).
Контрольные вопросы:
1. Общая характеристика алюминия.
2. Общая характеристика хрома.
3. Общая характеристика железа.
Список рекомендуемой литературы:
1. Глинка Н.Л. Общая химия: учеб. пособие для вузов / Н.Л. Глинка. - М.: КНОРУС, 2009. - С. 651 – 656, 672 – 677, 690 - 712.
2. Коровин Н.В. Общая химия: учебник для технических направл. и спец. вузов - 7-е изд., испр. - М.: Высшая школа, 2006. - С. 362 - 377.
Е.А. Буйлова, Д.Р. Галиева
oplib.ru
Отделение железа, алюминия и хрома от марганца, кобальта и никеля
Методом радиоактивных индикаторов было установлено [175], что наиболее полное отделение ванадия от ряда сопутствующих элементов (железо, алюминий, хром, марганец, кобальт и никель) осуществляется экстракцией его из водного раствора фторида натрия 0,3% раствором 8-оксихинолина в изобутиловом эфире при рН = 3,5- 4,5. [c.95]Пиридин, являясь слабым основанием, образует с сильными минеральными и органическими кислотами соли, в водном растворе сильно гидролизованные. С уксусной кислотой и угл. -кислотой пиридин прочных солей не образует это представляет большое удобство при пользовании им для отделения полуторных окислов от кальция, стронция и бария. Действие пиридина аналогично действию аммиака. Если к слабо кислому (азотно- или солянокислому) раствору, содержащему железо, алюминий, хром, марганец, кобальт и никель, прибавить пиридин, то железо, алюминий и хром выделяются в осадок в виде гидроокисей Ре (ОН),,, А1(0Н)з и Сг(ОН)з. С марганцем е, кобальтом и никелем пиридин образует комплексные растворимые соединения. При прибавлении пиридина к слабо кислому раствору устанавливается определенная концентрация водородных ионов, по нашим наблюдениям, примерно соответствующая pH = 6,5. [c.21]
Купферон реагирует со многими катионами, образуя труднорастворимые комплексы. Растворимость купферона-тов металлов зависит от кислотности растворов регулируя кислотность, можно провести разделение катионов. Например, в сильнокислом растворе (5—10 %-ной соляной или серной) купфероном осаждаются железо, галлий, гафний, ниобий, палладий, полоний, олово, тантал и титан частично осаждаются висмут, молибден, сурьма, вольфрам. В слабокислом растворе осаждаются висмут, медь, ртуть, молибден, олово, торий, вольфрам. В нейтральной среде осаждаются (в присутствии ацетатного буфера) серебро, алюминий, бериллий, кобальт, хром, марганец, никель, свинец, РЗЭ, таллий и цинк. Купферон дает возможность отделить железо, титан, ванадий и цирконий от алюминия, кобальта, меди, арсенита и фосфата. Его часто используют для отделения мешающих катионов, например железа при определении алюминия, а также железа и ванадия при определении фосфора в феррованадии. [c.165]
Определению марганца персульфатным методом мешает высокое содержание хрома (выше 1,5—2%) и кобальта, вызывающих окраску раствора, на фоне которой трудно установить конец титрования. В этом случае для отделения марганца от хрома, железа, алюминия, вольфрама и других металлов применяют окись цинка, которая осаждает указанные металлы, а в растворе остаются марганец, кобальт и никель. [c.324]
Преимуществами этого метода являются получение осадков, легко отделяемых фильтрованием, и малое соосаждение. Осаждаются алюминий, хром (П1), железо (HI), титан (IV), цирконий (IV), торий (IV), церий (IV), висмут, олово (IV) в растворе остаются ванадий (V), кобальт, никель, марганец, цинк, кадмий, ртуть (II) и щелочноземельные металлы. Это один из лучших методов отделения алюминия от цинка. При pH 3,5—4,0 можно осадить алюминий, отделяя его от бериллия, а затем при pH больше осадить бериллий. [c.87]
Очень полезный метод отделения многих металлов в один прием заключается в электролизе со ртутным катодом в разбавленной серной кислоте. Таким путем можно отделить от алюминия большие количества следующих элементов железа, меди, никеля, кобальта, цинка, галлия, германия, серебра, кадмия, индия, олова, сурьмы, хрома, молибдена, свинца, висмута, мышьяка, селена, теллура, ртути, таллия, рения, золота и платиновых металлов (кроме рутения). Марганец удаляется лишь-частично, но остающиеся количества его обычно не мешают, если алюминий определяют алюминоном. Вместе с алюминием в растворе после электролиза остаются бериллий, ванадий, фосфор, магний, щелочноземельные и редкоземельные металлы. Ход анализа описан на стр. 147. [c.137]
Как правило, колориметрическому определению бора мешают присутствие окислителей (нитраты, хроматы, перекись водорода), разрушающих красители, фтор-ион, образующий комплексное соединение с бором [91], а также некоторые элементы, такие, как железо, никель, марганец, мель, хром, кобальт, алюминий, ванадий, титан, молибден, цирконий, олово, мышьяк. Влияние окислителей устраняют восстановлением их гидразином, фтор-ион связывают добавлением двуокиси кремния. В литературе имеется обзор методов определения бора с применением дистилляции, ионного обмена, электролиза с ртутным катодом и определения в видимой и УФ-обла-сти спектра с применением флуорометрии, спектроскопии, полярографии и амперометрического титрования в урановых материалах, полупроводниках, сталях и цвет ных сплавах [107, 108]. Подробно методы отделения ме- тающих примесей изложены в п. 2 гл. I. [c.49]
Изучено [338] отделение цинка от ряда элементов при помощи анионного обмена. 5—50 мг цинка в 2 н. НС1 полностью адсорбируются на 15-сантиметровой колонке, содержащей 3 з сильноосиовного анионита амберлит IPiA-400 (в С1-форме). При последующем пропускании 50 мл 2 н. НС1 практически весь алюминий, магний, медь, кобальт, никель, марганец, хром, трехвалентное железо, торий, цирконий, четырехвалентный титан,шестивалентный уран, бериллий и кальций находятся в элюате. Кадмий, четырехвалентное олово, трехвалентная сурьма и висмут ведут себя подобно цинку. Удерживается некоторое количество свинца и индия. Цинк, кадмий и индий элюируются водой и 0,25 н. азотной кислотой, которая также удаляет 20% олова и некоторое количество сурьмы, висмута и свинца. Если применять только воду, то на колонке упорно удерживается небольшое количество цинка. Описаны методы выделения цинка из растворов, свободных от индия и кадмия. [c.86]
Кобальт и никель можно разделить при анализе руд и сплавов на ЭДЭ-Юп и дауэксе-1. Алюминий, железо и медь в бронзах можно определять на СБС в Н-форме. Можно на СБС отделить бериллий от алюминия и меди. На КУ-2 в Н- и Na-форме можно разделять магний, алюминий, хром, марганец, железо, никель, медь. Цинк из медных сплавов можно выделять на СБС в Nh5-фopмe, разделять железо и молибден в сталях, ферромолибдене и рудах. Молибден и рений разделяют на СБС, КУ-1, СБСР, МСФ, ЭДЭ-Юп, сульфоугле, вофатите П, амберлите ИРА-400, дауэксе-50, вофатите Ц. Ниобий и титан можно разделить на КУ-2 в Н-форме. Отделение кадмия от свинца и висмута проводят на сульфоугле, КУ-1, СБС, СДВ-3. [c.146]
Перекись водорода и перекись натрия препятствуют полному осаждению циркония на холоду при кипячении в их присутствии цирконий полностью осаждается. При осаждении гидроокиси циркония щелочами отделяются следующие элементы мюминий, галлий, цинк, молибден, вольфрам, ванадий, бериллий, мышьяк и Сурьма. В присутствии карбонатов отделяется уран. Для этой цели к щелочи прибавляют I—2 г Na Og. Прибавление перекиси водорода улучшает отделение. В осадке с цирконием находятся железо, титан, марганец, хром, кобальт, никель, медь, кадмий, серебро, индий, таллий, торий и редкоземельные элементы. Магний и щелочноземельные металлы при достаточном содержании карбонатов также полностью осаждаются. Этот метод может иметь некоторое значение для отделения циркония от молибдена, вольфрама, ванадия, алюминия и бериллия. По данным Руффа [700], бериллий не отделяется щелочью количественно, так же как и алюминий, особенно в присутствии больших количеств аммонийных солей. Осаждение гидроокиси циркония аммиаком может применяться при гравиметрическом определении циркония. Но этот метод используется лишь в случае отсутствия примесей, осаждаемых аммиаком. [c.53]
При восстановлении малых количеств мышьяка гипофосфитом натрия образуются окрашенные коллоидные растворы — б Большинство элементов, как, например, медь, железо, олово, висмут, алюминий, марганец, цинк, свинец, щелочные и щелочноземельные металлы, не мешают колориметрическому определению мышьяка гипофосфитным методом. Однако ряд элементов в этих же условиях или восстанавливаются до металла (серебро, ртуть и др.) или цр низших степеней окисления (молибден), или образуют окрашенные растворы (кобальт, никель, хром), в результате чего непосредственное колориметрическое определение мышьяка в присутствии таких элементов невозможно. В этом случае для отделения мышьяка от примесей применяют метод отгонки в виде А5С1д. [c.270]
Затем к раствору прибавляют раствор хлорида железа-3 в количестве, достаточном для осаждения фосфата железа, и раствор с осадком выпаривают на водяной бане досуха. Остаток смачивают несколькими каплями 6 н. раствора уксусной кислоты и смывают раствор струей воды в пробирку. Добавляют несколько мг ацетата аммония, доводят водой объем до 2 мл и нагревают до кипения. В осадке остаются фосфат железа и основные ацетаты железа, алюминия и хрома. Отделив его центрифугированием, смачивают водой, добавляют перекись натрия и кипятят. Образовавшийся раствор отделяют и обнаруживают в нем хром и алюминий. Раствор после отделения фосфат-иона, железа, хрома и алюминия делают аммиачным и, слегка нагрев, насыщают сероводородом после непродолжительного стояния центрифугируют. В раствор переходят щелочные и щелочноземельные элементы, в осадке остаются никель, кобальт, марганец и цинк. Осадок обрабатывают при по-мешнванпн 2 н. раствором соляной кислоты. В растворе присутствуют хлориды марганца и цинка, в осадке сульфиды кобальта и никеля. Далее анализ ведут, как описано выше. [c.181]
Помимо никеля и алюминия, в водном слое остаются также железо (II), кобальт, марганец, хром, титан и уран. Небольшие количества меди и ванадия переходят совместно с железом в эфирный слой, но для большинства целей разделение достаточно удовлетворительно. То же может быть сказано об отделении железа от серной и фосфорной кислот. Изучая поведение следов (различных элементов при извлечении хлорида железа из разбавленного солянокислого раствора изопропиловым эфиром, Р. Е. Eighty и J. D. Moulton нашли, что значительная часть As, Mo, Se и Те переходит совместно с железом в эфирный слой, потери В и V и умеренны (около 20%), а А1, Sb, Ва, Bi, d, Са, Сг, Со, Си, РЬ, Mg, Мп, Ni, Si, Ag, Sn, Ti, W и Zn полностью остаются в водном слое. Опыты проводились следующим образом. Солянокислый раствор (с несколько более высокой концентрацией соляной кислоты, чем 1 1), содержащий около 3 мг примесей и 30 е железа (III) в ви де хлорида, экстрагировался шестью порциями эфира (в общей сложности 900 мл) и затем, после переведения хлоридов в сульфаты, исследовался спектроскопически. [c.149]
Осаждение гидроокиси бериллия в присутствии ЭДТА. Это один из лучших методов отделения бериллия. Бериллий—один из очень немногих элементов, осаждаемых аммиаком в присутствии ЭДТА. В растворе остаются алюминий, хром (П1), ванадий (V), если его немного, свинец, железо (1П), висмут, медь, кадмий, никель, кобальт, марганец, цинк. Фосфорная кислота мешает разделению, ее надо предварительно отделить. Титан осаждается. Если алюминий присутствует в количестве, значительно превышающем содержание бериллия, этот метод разделения следует предпочесть методу с оксихинолином. [c.570]
Суспензия окиси цинка не должна показывать щелочной реакции по фенолфталеину. В присутствии большого количества железа (III), что имеет место, например, при анализе стали, после окЕСЛения раствора пробы, осадок от окиси цинка будет содержать все железо, вольфрам, ванадий, хром, уран, цирконий, титан, алюминий, фосфор, мышьяк, олово и почти полностью медь, молибден и кремний. Железо (II), вольфрам (если они не полностью окислены) и малые количества кремния, меди, молибдена, сурьмы и свинца могут оказаться в фильтрате, если они присутствовали в первоначальном растворе в значительных количествах. Фильтрат содержит марганец и кобальт почти полностью если осадок переосадить и соединить фильтраты, то отделение марганца и кобальта можно считать полным. Отделение никеля не так удовлетвори- [c.108]
Наиболее часто применямый метод отделения хрома основан на окислении последнего в щелочной среде до хромата, который остается в растворе, в то время как многие металлы — железо, титан, марганец, никель, кобальт и т. п., выпадают при этом в осадок. Элементы, остающиеся вместе с хромом в рас-, творе, частью не мешают дальнейшему колориметрическому определению (алюминий, мышьяк, фосфор), частью же najiy-шают ход определения (уран в хроматном методе, ванадий и большое количество молибдена в дифенилкарбазидном методе). Окисление можно вести в горячем растворе перекисью натрия или перекисью водорода с едким натром. Окислять можно также сплавлением с перекисью натрия или со смесью карбоната натрия (10 ч.) и нитрата калия (1 ч.), а некоторые образцы, например, силикаты анализируют, сплавляя даже с одним карбонатом натрия. При сплавлении марганец окисляется до манганата, но последний можно восстановить до гидрата двуокиси марганца, добавляя спирт к горячему раствору сплава. Хром обычно не остается в нерастворимом остатке после выщелачивания содового сплава, и поэтому повторное сплавление не требуется. Следует избегать плавня, содержащего слишком много нитрата, а также слишком высокой температуры при сплавлении, так как это может привести к разъеданию платинового тигля и ввести в раствор немного платины. [c.496]
При определении цинка мещают многие элементы, включая алюминий, бериллий, висмут, кадмий, кобальт, хром(III), медь, железо(III), марганец, ртуть, молибден(VI), никель и титан, которые реагируют с цинконом и должны быть отделены до комплексообразования с цинком. Для этой цели рекомендуется отделение на анионообменнике [9, 11]. [c.447]
chem21.info
Железо-хром-алюминиевый сплав для электронагрева сопротивлением | Производителя
Железо-хром-никелевый сплав для электронагрева сопротивлением имеет более высокую рабочую температуру, чем хромоникелевый сплав. Максимальная рабочая температура составляет 1440℃. Чем больше содержание хрома и алюминия в сплаве, тем выше его термостойкость.
Благодаря своей превосходной стойкости к окислению, сульфидированию и науглероживанию данный сплав отличается более долгим сроком службы и более высокой эффективностью затрат. Все эти характеристики делают этот сплав идеальным материалом для производства нагревательных элементов для электронагревателей.
Особое внимание следует уделить и недостаткам железо-хром-алюминиевого сплава, таким как низкая прочность при высоких температурах и увеличение пластичности при росте эксплуатационной температуры. Таким образом, Вы должны учитывать коэффициент деформации при выборе сплава для нагревательных элементов. Для получения более детальной информации Вы можете связаться с нами напрямую.
Технические характеристики
| Модель | 1Cr13A14 | 0Cr25A15 | 0Cr21A16 | 0Cr23A15 | 0Cr21A14 | 0Cr21A16Nb | 0Cr27A17Mo2 | |
| Свойства | ||||||||
| Химический состав | Cr | 12.0-15.0 | 23.0-26.0 | 19.0-22.0 | 22.5-24.5 | 18.0-21.0 | 21.0-23.0 | 26.5-27.8 |
| Al | 4.0-6.0 | 4.5-6.5 | 5.0-7.0 | 4.2-5.0 | 3.0-4.2 | 5.0-7.0 | 6.0-7.0 | |
| Re | Баланс | Баланс | Баланс | Баланс | Баланс | Баланс | Баланс | |
| Fe | — | — | — | — | — | — | — | |
| Nb0.5 | Mo1.8-2.2 | |||||||
| Максимальная рабочая температура (℃) | 950 | 1250 | 1250 | 1250 | 1100 | 1350 | 1400 | |
| Удельное сопротивление (μΩ.м,20℃) | 1.25 | 1.42 | 1.42 | 1.35 | 1.23 | 1.45 | 1.53 | |
| Плотность (г/см3) | 7.4 | 7.10 | 7.16 | 7.25 | 7.35 | 7.10 | 7.10 | |
| Коэффициент теплопроводности (кДж/м.ч.℃) | 52.7 | 46.1 | 63.2 | 60.2 | 46.9 | 46.1 | 45.2 | |
| Коэффициент линейного удлинения (α×10-6/℃) | 15.4 | 16.0 | 14.7 | 15.0 | 13.5 | 16.0 | 16.0 | |
| Средняя температура плавления (℃) | 1450 | 1500 | 1500 | 1500 | 1500 | 1510 | 1520 | |
| Прочность на разрыв (МПа) | 580-680 | 630-780 | 630-780 | 630-780 | 600-700 | 650-800 | 680-830 | |
| Удлинение (%) | >16 | >12 | >12 | >12 | >12 | >12 | >10 | |
| Относительное сужение (%) | 65-75 | 60-75 | 65-75 | 65-75 | 65-75 | 65-75 | 65-75 | |
| Число переменного изгиба | >5 | >5 | >5 | >5 | >5 | >5 | >5 | |
| Жесткость (H.B.) | 200-260 | 200-260 | 200-260 | 200-260 | 200-260 | 200-260 | 200-260 | |
| Микроструктура | Феррит | Феррит | Феррит | Феррит | Феррит | Феррит | Феррит | |
| Магнетизм | Да | Да | Да | Да | Да | Да | Да | |
www.etwinternational.ru
Железа хрома - Справочник химика 21
Навеску стали (или чугуна) растворяют в кислотах, после чего раствор подвергают электролизу со ртутным катодом в слабокислой среде. В результате железо, хром, марганец и другие металлы осаждаются на ртутном катоде, образуя амальгамы, а титан, алюминий и ванадий в виде соответствующих ионов остаются 8 растворе. [c.446]Ионы галогенов в меньшей степени влияют на аНодное поведение титана, тантала, молибдена, вольфрама и циркония, и их пассивное состояние может сохраняться в среде с высокой концентрацией хлоридов, в отличие от железа, хрома и Ре—Сг-спла-вов, теряющих пассивность. Иногда это объясняют образованием на перечисленных металлах (Т1, Та, Мо и др.) нерастворимых защитных основных хлоридных пленок. Однако в действительности подобная ситуация возникает благодаря относительно высокому сродству этих металлов к кислороду, что затрудняет замещение ионами С1 кислорода из пассивных пленок, вследствие более высоких критических потенциалов металлов, выше которых начинается питтингообразование. [c.85]
Эффективность этих методов в значительной степени зависит от типа применяемого катализатора. В качестве катализаторов используют в основном оксиды различных металлов ванадия, железа, хрома, меди, а также их композиции. [c.62]Окяокись алюминия Промотированная окись железа Ионообменные смолы Окись железа — окись кобальта — окись тория Промотированная окись железа Хромит цинка Хромит меди Никель [c.203]
Для превращения СО в СО2 процесс проводят при более низких (450—500 °С) температурах в присутствии катализатора, состоящего из смеси окислов железа, хрома и алюминия. Из 1 СН4 получают около 3,18 ж газа следующего состава (в объемн. %) 60,5 Н2 20,2 N3 4 СО 14,8 СО2 0,5 СН4. После удаления других компонентов получают смесь На и N3 с объемным соотношением компонентов, равным 3 1, которое и необходимо для синтеза аммиака. [c.214]
На первых производствах бутадиена дегидрированием бутенов использовались преимущественно железоокисные катализаторы [2, 4]. В зарубежной практике это были катализаторы, известные, под шифрами 1707, Шелл-105, Шелл-205 и др. [2, 4], в отечественной промышленности использовали железо-хром-цин-ковый катализатор К-16 [4]. В 1950-х годах на ряде заводов был применен фосфатный катализатор [2, 4], выходы бутадиена при этом повысились более чем вдвое, а избирательность — до 80— 85%. Последующие работы позволили создать катализаторы, отличающиеся высокой активностью, избирательностью и продолжительным сроком службы [37, 38]. [c.658]
Устойчивыми к коррозии являются нержавеющие стали, содержащие, кроме железа, хром, никель, марганец и малые добавки титана и ниобия. На изделиях из таких сплавов под действием воздуха и воды возникает химически и механически арочная окисная пленка, которая полностью пассивирует металл. [c.640]
Блочный катализатор сотовой структуры, используемый во второй каталитической ступени, представляет собой монолитный блок, собранный из отдельных пористых элементов со сквозными каналами. В качестве активного компонента используются окислы железа, хрома, кобальта, марганца, меди, ванадия и сурьмы, нанесенные методом пропитки на высокотемпературную керамику сотовой структуры. [c.181]
В отличие от щелочных металлов, никель, ванадий, железо, хром и другие тяжелые металлы не изменяют кислотности катализатора. Не происходит существенных изменений и в пористой структуре. Исследователи [45, 54, 132] пришли к выводу, что при отложении тяжелых металлов физические свойства алюмосиликата не меняются, а образуется поверхностный слой, обладающий совершенно иными каталитическими свойствами. В результате металлы оказывают существенное влияние на активность катализа- [c.139]
Эта реакция может идти как на гетерогенных, так и на гомогенных катализаторах. Наиболее четко она наблюдается в присутствии серной кислоты, а также солей алюминия, никеля, железа, хрома и кобальта. [c.69]
Катализаторы конверсии окиси углерода могут быть приготовлены на основе окислов железа, хрома, никеля, кобальта, меди, цинка, магния и других металлов. Наиболее распространены катализаторы на основе окиси железа, активные при 400—450 С. Состав их следующий (в вес. %) РегОз 51—90 СггОз 5—10 MgO до 16 остаточное содержание 50з 0,5—5,2 (227]. [c.89]
Потенциал металла покрытия измеряют на цельном электроде, считая, что диффузионные и кинетические ограничения, а также площадь электрода из-за пор практически не меняются. Затем строят поляризационную кривую для иокрытия, на нее наносят потенциал системы основа — металлическое покрытие и по нему определяют плотность тока коррозионного элемента. На рис. П.10 приведены коррозионные диаграммы двухэлектродных систем. Из приведенных графиков следует, что в электрохимическом отношении при одинаковых толщинах покрытий наиболее активна система железо-медь, а наименее активна железо—хром, чем объясняются высокие во многих случаях защитные свойства хромовых покрытий. Таким образом, возможность определения коррозионного тока, возникающего между основой и покрытием, позволяет оценить защитную способность покрытия и является объективным показателем пористости покрытия. [c.75]
С0 + Нз0 = С02 + Н2 промотируют введением добавок хрома и тория. Для этого в раствор нитрата железа (II) вводят соответствующее количество бихромата аммония и нитрата тория. В результате их совместной кристаллизации при выпаривании раствора, разложения прокаливанием и восстановления водородом получается промотированный железный катализатор, содержащий в поверхностном слое все три металла железо, хром и торий. [c.429]
Металл Медь Железо Хром Алюминий [c.159]
Ионы хлора и, в меньшей степени, других галогенов нарушают пассивность или препятствуют ее возникновению на железе, хроме, никеле, кобальте и нержавеющих сталях. С точки зрения теории оксидной пленки, ионы С1 проникают в оксидную пленку через поры или дефекты легче, чем другие ионы (например 504 ). Возможно также, что они могут коллоидально диспергировать оксидную пленку и увеличить ее проницаемость. [c.84]
График зависимости от t имеет вид прямой линии (рис. 10.2). Это уравнение справедливо для пленок с хорошими защитными свойствами, т. е. при Мрм/л рок > 1- Оно применимо для описания высокотемпературного окисления многих металлов, таких как медь, никель, железо, хром и кобальт. [c.193]
Легирование является эффективным средством повышения стойкости металлов к воздействию агрессивных сред как при обычных, так и при повышенных температурах. Уже отмечалось, что легирование железа хромом или алюминием способствует повышению стойкости к окислению (разд. 10.9), а введение небольшого количества легирующих добавок меди, хрома или никеля улучшают стойкость в атмосфере (см. разд. 8.4). [c.292]
В качестве адсорбентов были проверены силикаты магния, железа, хрома, алюминия, молибдена. При сочетании исследованных адсорбентов с различными десорбентами существенно повысить степень концентрирования сернистых соединений в хроматографических фракциях не удалось. [c.104]
Доступность для добычи определяется главным образом географическим расположением месторождений, концентрацией полезного вещества в его месторождениях и глубиной залегания сырья. Например, титан рассеян в земной коре и поэтому отнесен к редким элементам, хотя его содержание в коре (0,617о) чуть не в два раза боль(не, чем углерода. В отличие от титана углерод сконцентрирован в доступных растительных, животных материалах и особенно в мощных залежах топлива и карбонатов. Неравномерно распределено сырье по поверхности земного шара, поэтому многие государства не обеспечены важнейшими видами сырья. Так, крупнейшие страны Европы ФРГ, Италия и Франция— располагают весьма ограниченными ресурсами нефти, природного газа, дсбеста и руд, железа, хрома, никеля, меди и др. [c.7]
Реактор состоял из цилиндрической реакционной камеры (1), с нанесенным на ее внутреннюю поверхность железо-хромо-калиевым катализатором (3), винтового закручивающего устройства (2) с углом наклона винтовых каналов, (3 = 45. Пиролизу подвергалась углеводородная фракция нефти с температурой кипения (80-1б0) С при температуре (620-780) С. Объемная скорость подачи сырья составляла (2,0— 2,5) г/г час, разбавление водяным паром - 200% весовых. [c.248]
Для металлов переходных групп характерна сильно пониженная способность к растворению в кислотах и к анодному растворению после обработки поверхности этих металлов окислителями. Такое состояние металлов называется пассивностью. Для хрома, золота и платины достаточно воздейстиия кислорода воздуха для того, чтобы эти металлы перешли в пассивное состояние. Если железо погрузить в концентрированную азотную кислоту, то оно становится пассивным и не растворяется в разбавленной азотной кислоте. Можно перевести в пассивное состояние железо, хром, никель и другие металлы, обработав их окислителями, например опустив в раствор бихроматов, нитратов и др. [c.635]
Вместо алюминия в состав квасцов могут входить другие трех-валент)1ые металлы — железо, хром, а вместо калия — натрий или аммоний. Например, хромокалиевые квасцы имеют состав К25О4-Ср2(5О4)з-24Н0О. [c.390]
Восстанавливаемые из оксидов кре.мний, железо, хром и другие элeмeнtьr переходят в расплав. [c.88]
По оценкам группы Union arbide orporation в резервуаре оставалось 5 - 10 т вещества. Таким образом, из 41 т первоначального содержимого 30 - 35 т МИЦ, продуктов разложения МИЦ (газов) и, возможно, некоторых жидкостей и твердых веществ было выброшено в атмосферу через предохранительный клапан. Члены группы отобрали две пробы из оставшегося в резервуаре твердого содержимого. Результаты анализа этих проб дали следующую картину крайне малые количества МИЦ и воды, около 5% гидролизуемого хлора (т. е. хлора, не связанного с углеродом, входящего в основном в хлорзамещенные амины), следы железа, хрома и никеля (отношение этих элементов примерно совпадало с отношением, в котором они находятся в металле резервуара). Не было обнаружено натрия. [c.433]
При нанесении металлов на алюмосиликатный катализатор в газах крекинга возрастает количество водорода, сухого газа и уменьшается количество тяжелой его части. Абсолютные значения этих величин зависят от природы металла и его содержания на катализаторе. Наиболее резко состав газов в указанном направлении изменяется при содержании на катализаторах никеля, кобальта, меди, менее всего — при содержании железа, хрома свинца. С увеличением концентрации металла на катализаторе указанные тенденции усиливаются. Так, при содержании на катализаторе 0,16 вес. % никеля концентрация водорода в газе 10,5 вес. %, а сухого газа 42,0 вес. %, что соответственно в 35 и 14 раз больше, чем в газе крекинга, полученном на исходном ката.дизаторе. В то же время количество пропан-пропиленовой и бутан-бутиленовой фракции уменьшается в 1,2 раза. При содержании на катализаторе 0,5 вес. % никеля концентрация водорода в газе увеличивается в 50 раз, сухого газа — в 16 раз, а концентрация пропан-пропиленовой и бутан-бутиленовой фракций уменьшается соответственно в 1,2 и 1,4 раза. [c.159]
Сильно дегидрирующие металлы (никель, медь, кобальт) даже при ничтожном их содержании в катализаторе приводят к резкому увеличению коксоотложения вследствие повышенного образования непредельных углеводородов. Слабодегидрирующие металлы (ванадий, хром, молибден, железо) при небольшом их содержании в катализаторе (до 0,01 вес. %) образуют меньше кокса, чем исходный катализатор. При большем содержании металла в катализаторе коксообразование увеличивается. При содержании тяжелых металлов в катализаторе более 0,03—0,05 вес. % характер их влияния на изменение времени, необходимого для отложения 2% кокса, одинаков. По уменьшению количества образующегося кокса исследованные металлы располагаются в следующем порядке никель, медь>кобальт> молибден, ванадий > железо, хром>сви-нец>бериллий, магний, кальций, стронций>литий>натрий>ка-лий>цезий. Тормозящее влияние щелочных металлов возрастает в соответствии с увеличением их основности [257]. [c.176]
Малая стоимость катализатора также является определяющим фактором как для неподвижного, так и для взвешенного слоя, несмотря на то, что стоимость израсходованного катализатора (потери его) составляет, как правило, лишь незначительную часть себестоимости продукта. Снижение себестоимости достигается в основном заменой дорогостоящих платины, серебра и других катализаторов, хотя и менее активными, но более дешевыми окислами железа, хрома, молибдена, ванадия и др. Применение дешевых сильнопористых носителей позволяет наносить на них высокодиснерсное каталитическое вещество, создавая достаточную поверхность. Так, применяются платиновые контактные массы на силикагелевом носителе, содержащие лишь доли процента (весовые) платины. Замена пемзы синтетическими пористыми носителями позволила уменьшить содержание серебра в контактной массе в 2—3 раза без снижения активности. [c.127]
Катализаторы, используемые в окислительных процессах, весьма разнообразны. ПрИлМеняются металлические катализаторы — платина и другие металлы группы платины па соответствующих носителях, окислы металлов — окислы ванадия, железа, хрома, молибдена, никеля и других металлов, промотировапные различными соединениями и сформованные в виде таблеток, гранул, сфероидальных зерен и т. н. В настоящее время стремятся металлические катализаторы заменить окиспыми. [c.138]
Диапазон температур и давлений, применяемых при гидрогенизации топлива, составляет 380—550"С и 20—70 МПа. Катализаторами служат контактные массы на основе вольфрама, молибдена, железа, хрома и других металлов с различными активаторами. Для получения наибольшего выхода жидкого моторного топлива гидрогенизацию ведут двухстадийно. Первую стадию проводят при 380—400°С, подавая в реактор высокого давления водород и пульпу исходного топлива с катализаторами, распределенными в жидком продукте гидрирования. В результате жидкофазного гидрирования получают широкую фракцию среднего масла , которую после удаления фенолов снова гидрируют уже в паровой фазе (вторая стадия) в реакторе с потоком взвеси катализатора (см. ч. I, рис. 115) при 400—550°С и 30—60 МПа. Конечными продуктами гидрогенизации и последуюших операций гидроочистки, гидрокрекинга и каталитического риформипга (см. с. 69) служат искусственные бензин, котельное и дизельное топливо, а также газ, содержащий легкие предельные углеводороды газообразные продукты путем конверсии могут быть переработаны на водород, выход которого достаточен, чтобы обеспечить все предыдущие стадии производства. [c.54]
Малая стоимость катализатора— определяющий фактор как для неподвижного, так и для взвешенного слоя, несмотря на то, что стоимость израсходованного катализатора (потери его) составляют, как правило, лишь незначительную часть себестоимости продукта. Снижение себестоимости катализатора достигается, в основном, заменой дорогостоящих пЛаТинБГ, серебра и других металлов, входящих тг сисгав "ксжтятшШЗГмасс, менее активными, но и более дешевыми окислами железа, хрома, ванадия и т. д. Тонкое диспергирование катализатора носителе также позволяет снизить стоимость. Большое значение в стоимости катализаторов имеет рационализация технологии, полное использование всех видов сырья, применение современной, интенсивной, непрерывно работающей аппаратуры [I]. [c.61]
Из таких катализаторов наиболее изученным и до сих пор приковывающим к себе внимание является никелевый катализатор на кизельгуре. Первые обобщенные работы по гидрированию и гид-рогенолизу углеводов проводились именно на этом катализаторе [2], так как используемый носитель является наиболее доступным, дешевым и распространенным. После признания этого катализатора в разных странах стали появляться работы, посвященные его усовершенствованию, в частности промотированию железом, хромом, марганцем и др. [3]. В дальнейшем большое внимание уделялось и уделяется сейчас теоретическим аспектам действия этого катализатора как в процессе гидрирования, так и в процессе гид-рогенолиза углеводов [4, 5]. Работы, выполненные в последние годы, показывают, что наряду с природой катализатора важное значение имеет аппаратурное оформление и оптимальные условия проведения процесса. Так, при гидрировании глюкозы и ксилозы [6, 7] влияние давления водорода описывается экстремальной за- [c.22]
Железо — хром Сернокислое железо Ре50[c.950]
Пайка твердым припоем нержавеющих сталей или других подобных сплавов обычно производится при температурах в пределах от 1090° до 1200° С с применением одного из при-1юев, содержащих никель, железо, хром, кремний и бор в среде сухого водорода. Этот припой, диффундируя в основной металл, дает прочность соединения, равную по существу прочности основного металла. Как видно из рис. 2.6, пайка твердым припоем позволяет получить высококачественное соединение, но сами припои отличаются хрупкостью. В местах соединений твердым припоем недопустимы никакие сварные операции, так как возникающие при сварке напряжения могут привести к образованию трещин в твердом припое. [c.28]
Производство мономеров для получения синтетического каучука (бутадиена, изопрена, стирола) в значительной мере базируется на процессах каталитического дегидрирования различных углеводородов. Выбор катализатора эависит от типа применяемого сырья [46, 52]. Наиболее распространенными для дегидрирования алканов в алкены являются алюмо-хромовые катализаторы. Для дегидрирования олефинов в диеновые углеводороды кроме алюм о-хромовых применяют железосодержащие и кальций-никель-фосфатные катализаторы, стабилизированные окисью хрома. В процессах дегидрирования алкилароматических углеводородов применяют железо-хромо-калиевые катализаторы. [c.409]
Наплавку выполняют по установленной технологии, чтобы избежать коробления деталей с подогревом детали до 400— 500 °С, со ступенчатым и разбросным наложением наплавленных валиков. Присадочным материалом могут служить стальная напла1В0Чная проволока (ГОСТ 110543— 82), смеси порошков для наплавки (ГОСТ 4 1546—75) марок С-2М, ФБХ6-2, БХ, КБХ, состоящих из железа, хрома, марганца, кремния и бора. Порошки применяют для дуговой наплавки износостойкого [c.266]
КавтарадзеН, Н., О природе адсорбции водорода на никеле, железе, хроме и платине, ЖФХ, 32, № 4, 909—913 (1956). [c.195]
Новым направлением в фиксации атмосферного азота является так называемый ферментативный метод с использованием комплексных соединений переходных металлов (железа, хрома, молибдена), в котором используется принцип естественной фиксации азота растениями в прирбдных условиях [c.186]
Технология изготовления. Конструкция теплообменника зависит от требований технологии производства, в частности от технологии соединения труб с трубными досками. Наиболее перспективными, по-видимому, являются гелиеводуговая сварка и высокотемпературная пайка тугоплавким припоем — сплавом железа, хрома, никеля, кремния и бора с точкой плавления около 1100° С. Для осуществления пайки твердым припоем необходима атмосфера водорода при отсутствии влаги (см. гл. 2). В некоторых теплообменниках применена сварка, в других используется пайка, некоторые теплообменники были сначала сварены, а затем пропаяны. Для выявления лучшей технологии были проведены испытания на длительную прочность соединений. Обнаружилось, что повреждения были одинаковыми как в случае сварки, так и в случае пайки — в обоих вариантах имели место случайные свищи. Одной из наиболее существенных конструктивных проблем является вопрос концентрации напряжений в основании сварного шва в трубной доске. На рис. 2.5 показана фотография микрошлифа такого шва, на которой ясно видны места сильной концентрации напряжений на конце трещины, упирающейся в сварочный шов. Хотя влияние такой концентрации напряжений можно уменьшить путем развальцовки трубы в трубной доске, последнюю операцию не всегда легко осуществить при малом диаметре труб. Возникающие в стенке трубы при вальцовке остаточные напряжетшя сжатия имеют тенденцию к релаксации при высоких температурах, особенно в условиях переменных температурных режимов, связанных с резкими изменениями температуры жидкости, текущей в трубах. Следовательно, имеются весьма веские доводы в пользу припаивания труб к трубной доске твердым припоем. При последнем способе получается хорошее со всех точек зрения металлическое сцепление трубы с трубной доской. Было выявлено, что если трубы свариваются, а затем еще и пропаиваются, то при этом достигается высокая монолитность конструкции. Действительно, более 7000 сваренных, а затем пропаянных соединений труб с трубной доской были подвергнуты длительным испытаниям, при этом не обнаружилось ни одного свища [14]. [c.271]
chem21.info
свинец серебро сплав железа с хромом и алюминием
МЕДИ СПЛАВЫ — сплавы на основе меди, содержащие олово, цинк, алюминий, никель, железо, марганец, кремний, бериллий, хром, свинец, золото, серебро, фосфор и другие легирующие элементы. Добавки повышают прочность и твердость, стойкость против коррозии, улучшают антифрикционные свойства. М. с. делят на латуни, бронзы и медно-никелевые сплавы. Латуни — М. с., в которых главным легирующим элементом является цинк. Самыми распространенными латунями являются томпак (80 [c.156] Классификация металлов . Металлы составляют большую часть всех элементов в периодической системе Д. И. Менделеева, но в технике они классифицируются по иным признакам. До настоящего времени не разработана научно обоснованная классификация металлов. В практике получили применение исторически сложившиеся классификации, базиру.ющиеся на таких признаках металлов, как их распространенность в природе, применимость, физические и частично химические свойства. Металлы делятся на черные и цветные. К черным металлам относятся железо, марганец, хром и сплавы на их основе, к цветным — все остальные. Цветные металлы делятся на 4 группы 1) тяжелые медь, свинец, олово, цинк и никель 2) легкие алюминий, магний, кальций, калий и натрий часто к этой группе относят также барий, бериллий, литий и другие щелочные и щелочноземельные металлы 3) драгоценные, или благородные платина, иридий, осмий, палладий, рутений, родий, золото и серебро 4) редкие а) тугоплавкие [c.115]МЕДИ СПЛАВЫ — сплавы на ото ве меди. В виде бронзы применялись за 3000 лет до н. э. В жидком состоянии медь сплавляется со многими элементами, с большинством из них — в любом соотношении. Лишь вольфрам, молибден, осмий, рутений и тантал практически не сплавляются с нер. В твердом состоянии макс. растворимость элементов (в альфа-твердом растворе меди) изменяется в очень широких пределах от сотых и десятых долей процента (хром, ниобий, свинец, ванадий, цирконий) до процентов (серебро, алюминий, мышьяк, бериллий, кадмий, кобальт, железо, магний, кремний, титан и др.) и десятков процентов (индий, олово, цинк). Неограниченно растворяются никель, золото, марганец, палладий и платина. Однако с золотом, марганцем, палладием и платиной М. с. в твердом состоянии претерпевают превращения. С увеличением концентрации легирующего элемента в альфа-твердом растворе меди повышается мех. прочность сплавов их теплопроводность и электропроводность уменьшаются (менее всего при легировании серебром). К вредным примесям относятся висмут, сурьма, свинец и углерод (в медноникелевых сплавах), к-рые приводят к хрупкости. Стойкость против коррозии М. с. зависит от природы легирующего элемента и окружающей среды. Повышают стойкость никель, олово и алюминий. С понижением т-ры раст [c.780]
При затруднениях в определении скорости коррозии рекомендуется пользоваться распределением металлов по группам, в пределах которых контакт может считаться допустимым. Для атмосферных условий эксплуатации можно выделить пять таких групп I — магний П — алюминий, цинк, кадмий П1 — железо, углеродистые стали, свинец, олово IV — никель, хром, коррозионностойкие стали (в пассивном состоянии) типа Х17 и 18—8 V — медно-никелевые и медноцинковые сплавы, медь, серебро, золото. [c.74]
Обычно на практике классифицируют металлы, исходя из общих сырьевых, технологических и потребительских признаков. Принято разделение металлов на черные и цветные. К черным металлам относятся железо и его сплавы, а также металлы, применяемые главным образом в сплавах с железом—хром, марганец. К ц в е т н ы м—относятся все остальные металлы, которые, в свою очередь, подразделяются на тяжелы е—медь, никель, свинец, олово, цинк л е г к ие—алюминий, магний, калий, натрий малы е—сурьма, ртуть, висмут, кадмий редкие—вольфрам, молибден, ванадий, кобальт, ниобий, тантал, титан, бериллий, литий и др. рассеянны е—германий, рений, индий, галлий и др. благородные—платина, палладий, иридий, осмий, рутений, золото и серебро. [c.113]
Приводимый ниже ход анализа в частности, предназначен для анализа сплавов на магниевой основе, но он также годен и для сплавов на основе алюминия и цинка. Меркаптоуксусную кислоту используют как реагент, предпочитая ее о-фенантролину, который не совсем пригоден в присутствии цинка. Марганец, индий, таллий, кадмий, медь и олово (IV) не оказывают вредного влияния (на некоторые из них расходуется реагент и требуется его достаточный избыток). Хром мешает по той причине, что придает зеленую окраску раствору. Следующие металлы дают окрашенные соединения или осадки с реагентом свинец (в больших количествах), серебро, висмут, никель (1/44 интенсивности окраски, придаваемой железом), кобальт (ср. со стр. 484). Можно использовать цитраты для предотвращения осаждения различных элементов в щелочном растворе. В том случае, когда взято 4 г анализируемого образца, воспроизводимость составляет + 0,0002 %. Для очень низких концентраций железа используется кювета необычной длины — 20 см, при этом для измерения требуется 500 мл раствора. [c.487]
До настоящего времени в простом сосуде удавалось глянцевать или полировать следующие металлы алюминий и его сплавы, сурьму, серебро, висмут, кадмий, хром, кобальт, медь ч ее сплавы, олово, железо, нормальные и специальные стали, германий, бериллий, индий, магний, марганец, молибден, никель и его сплавы, ниобий, золото, свинец, тантал, торий, титан, вольфрам, уран, цинк и цирконий. [c.251]
В первой части книги весьма полно приведены линии спектров 32 элементов, необходимые для анализа важнейших металлов и сплавов. К таким элементам мы отнесли алюминий, ванадий, висмут, вольфрам, железо, золото, индий, кадмий, кальций, кобальт, кремний, магний, марганец, медь, молибден, мышьяк, натрий, никель, ниобий, олово, платину, свинец, серу, серебро, сурьму, титан, углерод, фосфор, хром, церий, цинк, цирконий. [c.11]
Сероводород разрушающе действует на металлы. Растворяясь в воде, он образует слабую кислоту, которая может вызывать точечную коррозию в присутствии кислорода или диоксида углерода. Сероводород реагирует почти со всеми металлами, образуя сульфиды. Наибольшую активность среди тяжелых металлов проявляют те, которые характеризуются электронной конфигурацией ( 8 или Наиболее сильно сероводородной коррозии подвергается серебро и медь или их сплавы - латунь и бронза. Известно, что этому виду коррозии подвержены также железо, сталь, алюминий, никель, хром, кобальт, палладий, титан, но в меньшей степени, чем серебро, ртуть, медь, кадмий, таллий, висмут и свинец. [c.23]
Хотя развитие производства сплавов в порошке имеет интересные перспективы, основные находящиеся уже теперь в употреблении металлические порошки представляют собой чистые металлы медь, никель, кобальт, хром, алюминий, магний, кремний, свинец, цинк, железо, вольфрам, молибден, тантал, серебро, золото, платину и иридий. [c.157]
Металлические покрытия делят на две группы коррозионностойкие и протекторные. Например, для покрытия сплавов на основе железа в первую группу входят никель, серебро, медь, свинец, хром. Они более электроположительны по отношению к железу, т. е. в электрохимическом ряду напряжений металлов стоят правее железа. Во вторую группу входят цинк, кадмий, алюминий. По отношению к железу они более электроотрицательны, т. е. в ряду напряжений находятся левее железа. [c.144]
В технике и в быту наибольшее применение из металлов имеют железо, алюминий, цинк, свинец, медь, олово, серебро, золото, ртуть и др. Очень большое техническое значение имеет ряд сплавов этих металлов с более редкими металлами (вольфрамом, никелем, ванадием, молибденом, хромом и др.). [c.310]
Металлы и окислы металлов. Алюминий, бериллий, железо, свинец, никель, хром, марганец, молибден, серебро, кремний, тантал, титан, цинк, вольфрам, нержавеющие стали, ферромагнитные сплавы и ферриты. [c.10]
В ряде обзоров, касающихся катализаторов для окисления и дегидрогенизации спиртов, указаны кроме меди другие катализаторы, проверенные в различных исследованиях или рекомендуемые патентами. В качестве катализаторов указаны никель, кобальт, платина, серебро, железо, латунь, сплавы меди с серебром, с цинком, с висмутом, с кадмием, с палладием, а также окислы цинка, олова, хрома, кобальта, ванадия, кадмия, магния, бериллия, циркония, бария, марганца. Затем идут ванадиевокислые соли щелочных металлов, сернистые, фосфористые и т. п. соединения цинка, кадмия, никеля, кобальта, железа, алюминия, кальция и магния, а также расплавленные свинец, смеси солей (хлористый барий с хлористым кальцием, хлористый калий с хлористым натрием и т. п.). [c.148]
При решении вопроса о допустимости контакта между металлами можно также рукоиодствоваться следующими данными. Все металлы разделены на пять групп первая группа магний вторая — п,и1гк, алюминий, кадмий третья — железо, углеродистые стали, свинец, олово четвертая — никель, хром, хромистые стали (Х17), хромоиикелевые стали (Х18Н9) пятая — медноникелевые сплавы, медь, серебро. [c.182]
Большинство химических элементов являются металлами (см. рис. 53). Многие из них в силу своей химической активности находятся в природе в связанном состоянии, и поэтому до XVIII в. были известны лишь металлы, встречающиеся в самородном состоянии или легко выплавляемые из руд, такие, как золото, серебро, медь, ртуть, свинец, олово, железо и висмут (причем висмут долгое время принимали за разновидность свинца, олова или сурьмы). Использование сплава меди с оловом сыграло важную роль в развитии производительных сил общества и открыло бронзовый век . Совершенствование плавильных печей позволило производить чугун и другие сплавы железа, появление которых явилось новой вехой в создании человеком материальных ценностей. Алюминий, никель, хром, марганец, магний и другие хорошо известные теперь металлы стали получать лишь в конце XIX — начале XX в., а титан — только в середине XX в. [c.390]
КИСЛОТОСТОЙКИЕ МАТЕРИАЛЫ — материалы, отличающиеся повышенной кислотостойкостью, вид химически стойких материалов. В пром. масштабах используются с середины 18 в. Различают К. м. металлические и неметаллические. К металлическим К. м. относятся сплавы на основе железа, а также цветные металлы и их сплавы (см. также Кислотостойкие сплавы). Кислотостойкие сплавы на основе железа углеродистые стам (нелегированные, низколегированные), содержащие до 1% С высоколегированные стали, имеющие в своем составе хром, никель, медь, марганец, титан и др. хим. элементы чугуны (нелегированные, высоколегированные), содержащие более 2,5—2,8% С. Кислотостойкие цветные металлы никель, медь, алюминий, титан, цирконий, олово, свинец, серебро, ниобий, тантал, золото, платина и др. Углеродистые стали стойки в растворах холодной азотной к-ты (концентрация 80—95%), серной к-ты (выше 65%) до т-ры 80° С, в плавиковой к-те (выше 65%), а также в смесях азотной и серной к-т. На углеродистые стали сильно действуют органические к-ты (адипиновая, муравьиная, карболовая, уксусная, щавелевая), особенно с повышением их т-ры. Высоколегированные стали, отличаясь повышенной стойкостью к коррозии металлов (см. также Коррозионностойкие материалы), являются в то же время кислотостойкими. Большинство легирующих добавок значительно повышают кислотостойкость сталей. Так, медь придает хромоникелевым сталям повышенную стойкость к серной к-те. Сталь с 17—19% Сг, 8-10% Мп, 0,75-1% Си, 0,1% С и 0,2—0,5% Si стойка в азотной к-те (любой концентрации и т-ры вплоть до т-ры кипения) и многих др. хим. соединениях (см. Кислотостойкая сталь). Кислотостойки высоколегированные чугуны никелевые, хромистые (см. Хромистый чугун), алюминиевые (см. Чугалъ), высококремнистые (ферросилиды), хромоникель-медистые (см. Нирезист), хромони-келькремнистые (никросилал). Наиболее распространены ферросилиды [c.586]
Металлургическое производство возникло в глубокой древности. Еще на заре развития человеческого общества (до и. э.) были известны и применялись железо, медь, серебро, золото, ртуть, олово, свинец. Прежде других металлов были получены олово и свинец как сравнительно легко восстанавливаемые из окислов. Но они не были пригодны для изготовления орудий труда и оружия. Освоение производства сплава меди, с оловом явилось началом новой эпохи в истории материальной культуры, называемой бронзовым веком. Совершенствование плавильных печей создало возможность выплавлять из руд железо, которое вытеснило бронзу, и в виде чугуна и различных сплавов железа стало основой развития промышленности, транспорта и сельского хозяйства До начала XVIII в. человечеству были известны лишь такие металлы, как золото, серебро, медь, ртуть, железо, свинец, олово, сурьма и висмут.. Алюминий, никель, магний, хром, марганец и ряд других стали получать только в конце XIX и в начале XX вв. [c.115]
chem21.info
Хромо-алюминиевые сплавы - Справочник химика 21
В Советском Союзе термический метод получения ацетилена разрабатывается как высокотемпературный пиролиз до 1100—1200° в трубчатых печах, оборудованных трубами из жаростойкого силава № 2. Примеиение такого технологического оформления стало возможным благодаря созданию железо-хромо-алюминиевого сплава JV 2, разработанного в Институте металлургии АН СССР [2, 3]. [c.180] Железо-хром-алюминиевые сплавы, к которым относятся фехраль и хромаль, обладают тем недостатком, что после нагревания они становятся хрупкими. Однако во многих случаях нагревающие элементы из этого материала находят успешное применение. [c.15]В печах с рабочей температурой до 1000—1200° С применяют нагревательные элементы из нихрома или железо-хромо-алюминиевых сплавов, от 1200 до 1350° С — карборундовые нагревательные элементы или расплавленные соли, при более высоких температурах — в вакууме или соответствующей защитной среде применяют уголь, графит, вольфрам, молибден. В зависимости от профиля сечения материала выбирают конструкцию нагревательного элемента и способ его крепления в камере печи. На рис. 18 показаны некоторые конструкции нагревательных элементов и способы их крепления на стенках печи. Нагревательные элементы из проволоки изготовляют в виде спиралей, которые укрепляют на крючках или керамических опорах. Ленточные нагревательные элементы имеют форму петель и подвешиваются или укладываются на опорах на стенках печи. [c.45]
Для плавки в небольших количествах алюминия, магния, цинка, свинца, олова и их сплавов, при температуре до 800—850° С, применяют также электрические печи сопротивления тигельного типа или, как их называют, печи-ванны с литым тиглем из жароупорной стали или чугуна. Тигель помещается в шахте печи, на внутренней стенке которой располагают нагревательные элементы из нихрома или железо-хромо-алюминиевых сплавов. Рабочая температура печи до 1000—1100° С. Схема устройства такой печи показана на рис. 88. [c.271]
НЕКОТОРЫЕ СВОЙСТВА И ОПЫТ ПРИМЕНЕНИЯ ЖАРОУПОРНОГО ЖЕЛЕЗО-ХРОМО-АЛЮМИНИЕВОГО СПЛАВА № 2 В ВЫСОКОТЕМПЕРАТУРНОМ ПИРОЛИЗНОМ ПРОЦЕССЕ [c.316]
ЖАРОУПОРНОСТЬ ЖЕЛЕЗО-ХРОМО-АЛЮМИНИЕВЫХ СПЛАВОВ [c.317]
Теория окисления железо-хромо-алюминиевых сплавов разработана И. И. Корниловым [1]. Содержанием теории окисления являются следующие процессы. Тройной твердый раствор аз хрома и алюминия в железе взаимодействует с кислородом воздуха при нагреве при этом на поверхности металла образуется тонкая прочная окисная пленка с желто-зеленоватым оттенком, она состоит из окислов железа, хрома и алюминия. При температурах выше 700° алюминий, входящий в состав сплава, начинает взаимодействовать с окислами железа и хрома в результате этих реакций, протекающих в твердом состоянии, на поверхности металла образуются шпинели слож- [c.318]
Железо-хромо-алюминиевый сплав № 2 является более устойчивым в азотной кислоте, чем нержавеющая сталь 18/8 потери на растворение сплава №2 в азотной кислоте за 100 час. испытания составляют 0,02 г-м 1тс, тогда как потери на коррозию нержавеющей стали за то же время испытания составляют 0,15—0,17 г-м /час. [c.321]Железо-хромо-алюминиевый сплав № 2 является весьма устойчивым при высоких температурах в газовых средах, содержащих серу и ее соединения с кислородом и водородом. [c.321]
Знание механических свойств железо-хромо-алюминиевых сплавов необходимо для расчета конструкций реакторов пиролизных установок, разработки технологии изготовления сплавов и определения условий их эксплуатации, как прочных и жаропрочных материалов при комнатной и высоких температурах. [c.322]
Плавка сплава, ковка слитков, прокатка заготовок достаточно полно описаны и технология каждого вида металлургического процесса обоснована на основе данных механических свойств железо-хромо-алюминиевых сплавов, изменения их в зависимости от состава и температуры в работах [c.324]Без разработанной совершенной технологии сварки труб из железо-хромо-алюминиевого сплава № 2 невозможно было бы их применить для высокотемпературного пиролиза углеводородов. Сплав № 2, как нами отмечалось ранее в работах [1 —3], подвергается сварке электродуговым способом. Технология сварки труб из сплава разработана и освоена Гипрокаучуком, одним из предприятий Министерства химической промышленности, и Институтом металлургии им. А. А. Байкова АН СССР. [c.325]
ПРИМЕНЕНИЕ ТРУБ ИЗ ЖЕЛЕЗО-ХРОМО-АЛЮМИНИЕВОГО СПЛАВА № 2 ДЛЯ ВЫСОКОТЕМПЕРАТУРНОГО ПИРОЛИЗА УГЛЕВОДОРОДОВ [c.327]
| Рис. 10. Змеевик в Р/г витка из сверленых труб размером БХ Омм железо-хромо-алюминиевого сплава № 2 после 6000 час. работы при 900—1350° |  |
Железо-хромо-алюминиевый сплав № 2 обладает высокой жароупорностью до 1300°, он может работать и при температуре более высокой, до т. пл. 1500°, без значительных потерь на окисление. [c.333]
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ЖЕЛЕЗО-ХРОМО АЛЮМИНИЕВОГО СПЛАВА № 2 [c.169]
В нашей стране на опытно-промышленных установках в течение ряда лет ведутся опыты с целью создания отечественного метода получения ацетилена в многопоточной трубчатой печи - Основным аппаратом является печь с беспламенными панельными горелками. Трубы изготовлены из железо-хромо-алюминиевого сплава, пригодного для работы в условиях температур порядка 1200° С и обладающего удовлетворительными механическими свойствами. Закалка газов пиролиза осуществляется в специальном аппарате коллекторного типа, куда через восемь форсунок подается вода. Аппарат установлен на двух катковых опорах, которые вместе с П-образным компенсатором воспринимают изменения длины труб при перепаде температуры в печи. [c.100]
Печи. Для нагревания закрытых кювет необходимы печи, обеспечивающие достаточный изотермический объем и возможность перегрева окон кюветы. Такие трубчатые печи с рабочей температурой до 1600 °С делают обычно из тугоплавкой фарфоровой, шамотной или алундовой трубки, на которую наматывают проволочный нагреватель. До 1100 °С можно использовать нихром марки ХН80/20, более высокие температуры (до 1200 °С) выдерживают нагреватели из железо-хромо-алюминиевых сплавов № 2 (1150 °С), № 3 (1300 °С), № 4 и ЭИ-695 (1400 °С). [c.352]
Железо-хромо-алюминиевый сплав № 2 (Х25Ю5 по ГОСТу № 5632—51) является тройным ферритовым твердым раствором сплав содержит 23— 26% Сг, 4,5—5,5% А1, 0,5% Т1 и примеси С, 51, Мп, N1, 8, Р, вошедшие в состав сплава с шихтой в процессе его плавки. Основными составляющими сплава являются железо, хром и алюминий. В свободном, т. е. несплавлен-ном состоянии, они представляют собой поликристаллические тела. Основные физические и механические свойства этих металлов и сплава приведены в работах [1—3]. [c.316]
На основе исследования химического взаимодействия железа с хромом и алюминием построена частичная фазовая диаграмма системы железо—хром—алюминий (рис. 1). Тройные сплавы на основе железа с хромом и алюминием и на основе хрома с железом и алюминием кристаллизуются с образованием ограниченных а-твердых растворов, со стороны диаграммы фазового равновесия Ре—Сг до 100% каждого компонента, со стороны железо—алюминий —до с 33% А1, со стороны хром—алюминий— до с 17,5% А1. В концентрационном треугольнике железо—хром—алюминий область тройных твердых растворов ограничена кривой линией авс. Выше этой линии сплавы имеют гетерогенную микроструктуру,- Железохромовые твердые растворы при охлаждении, начиная с температуры с 920°, претерпевают превращение с образованием в интервале 40—55% Сг хрупкой а-фазы в концентрационном треугольнике железо—хром—алюминий область а-фазы имеет незначительное распространение, до с 5% А1, а двухфазная область аз+ распространяется в интервале со26—70% Сг и до 10% А1 (при 50% Сг). Установлена область существования металлического соединения РезА1, обозначенная бгд. Линия пт — граница распространения магнитных железо-хромо-алюминиевых сплавов. Область, обозна- [c.316]
Окисление железо-хромо-алюминиевых сплавов изучено в атмосфере воздуха при 1000—1400° результаты исследования опубликованы в работах [1,2]. Построены диаграммы состав—жароупорность, характеризующие окисление сплавов в зависимости от содержания хрома и алюминия. При этом установлено, что чем концентрированнее твердые растворы, т. е. чем больще растворено в железе алюминия и хрома (до 50%), тем они большее сопротивление оказывают действию кислорода воздуха. Это хорошо иллюстрирует диаграмма (рис. 2), характеризующая изменение потери веса (в г > час) за 240 час. испытания при 1200—1220° на окисление железо-хромо-алюминиевых сплавов с содержанием 5—6% А1 (кривая /) и 8—10% Л1 (кривая II) в зависимости от содержания хрома (дог537%). Эта диаграмма показывает, что жароупорные до 500° хромистые стали с содержанием со12% Сг при сплавлении с алюминием в заданных количествах являются жароупорными уже при температурах, более высоких 1200—1220° потери на [c.317]
Таким образом кривые потерь на окисление железо-хромо-алюминиевых сплавов с содержанием 5—6 и 8—10% А1 и до 37% Сг изменяются в зависимости от содержания хрома прерывно, с образованием минимума при 25% Сг. Эта диаграмма (рис. 2) имеет практическое значение, она позволила определить составы сплавов с высокой сопротивляемостью окислению кисло родом воздуха и установить оптимальное содержание хрома в сплаве (рав ное 25%), который имеет из группы высокожароупорных сплавов мини мальные потери на окисление, т. е. является наиболее жароупорным сплавом [c.318]
Таким образом железо-хромо-алюминиевый сплав № 2 по высокой химической устойчивости при высоких температурах в газовых средах, содержащих углерод, серу и их соединения с кислородом, водород и сероводород, азот и другие химически активные соединения, не имеет себе равных среди металлических сплавов на основе железа, никеля с ферритовой и аустени-товой (для железных и никелевых сплавов) структурами. [c.322]
Изменение механических свойств — сопротивления разрыву и процента удлинения — железо-хромо-алюминиевых сплавов с 5 % А1 и разным содержанием хрома (максимум до 30%) изображено на рис. 6, а, б. Диаграмма состав — механические свойства (рис. 6, а) показывает резкое возрастание прочности с с ОО кг1мм для сплава с 10% Сг до оо80 кг/мм а я сплава с 30% Сг. Пластичность сплавов при этом, как видно из хода кривой процента удлинения, резко уменьшается, если сплав с 10% Сг имел удлинение при разрыве с/о28%, а сплав с 30% Сг — всего лишь 8%. [c.322]
| Рис. 8. Труба из железо-хромо-алюминиевого сплава № 2 (ЭИ292) для обработки легкоокисляющихся металлов при высоких температурах в вакууме |  |
Предъявляемым требованиям для осуществления пиролизных процессов при разных температурах удовлетворяют металлические материалы. Они являются компактными, плотными, теплопроводными, термически устойчивыми с удовлетворительными данными по механическим свойствам. Металургическим путем из них можно получать трубы и использовать их в качестве реакторов для пиролиза углеводородов при температурах, при которых эти реакторы обеспечивают ведение процесса пиролиза, не разрушаясь сами от действия газовой коррозии. Металлические материалы удовлетворяют многим техническим требованиям и условиям эксплуатации их в пирогенных установках. Однако в высокотемпературных пиролизных процессах могут быть применимы только высокохимически стойкие металлические материалы. Нержавеющие стали с содержанием 8, 10—12, 14% N1 и 18% Сг, с 25% N1 и 20% Сг, остальное железо, применяемые для пиролиза углеводородов при температурах 750° и выше, легко окисляются, они взаимодействуют с серой и разрушаются, науглероживаются и охрупчива-ются сталь содержит в своем составе дорогостоящий никель, более нужный в других отраслях техники. По стоимости нержавеющая сталь дороже в Р/г—2 раза железо-хромо-алюминиевого сплава № 2. [c.327]
| Рис. 11. Пирозмеевик из железо-хромо-алюминиевого сплава № 2 для промышленной пирогенной установки. Размеры змеевика трубы — 114X8 мм, диаметр змеевика (внутренний) 1500 мм, высота 4300 мм |  |
| Рис. 14. Повышение производительности установки с трубами из железо-хромо-алюминиевого сплава № 2 конверсии этана и выход этилена в процентах по сравнению с трубами из нержавеющей стали ОХ 18Н12 (/) | 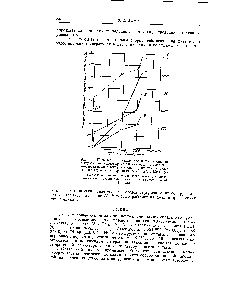 |
chem21.info