Химические свойства хрома. Получение хрома алюмотермией
1.1.2 Алюмотермия
К пирометаллургическим способам относится металлотермия. Металлотермия (от металлы и греч . therme - жар, тепло), металлургические процессы, основанные на восстановлении металлов из их соединений (оксидов, галогенидов и др.) более активными металлами, и протекающие с выделением теплоты (напр., алюминотермия, магниетермия). Впервые металлотермические реакции изучил и подробно описал Н. Н. Бекетов (1865г.). В настоящее время применяется восстановление алюминием – алюминотермия и восстановление кремнием - силикотермия. Эти процессы используются главным образом при получении безуглеродистых ферросплавов хрома, ванадия, титана, вольфрама и др [2]. Различают внепечные, электропечные и вакуумные металлотермические процессы.
Алюминотермия, алюминотермический процесс - получение металлов и сплавов восстановлением окислов металлов алюминием. Шихта (из порошкообразных материалов) засыпается в плавильную шахту или тигель и поджигается с помощью запальной смеси. Если при восстановлении выделяется много теплоты, осуществляется внепечная алюминотермия, без подвода тепла извне, развивается высокая температура (1900-2400о С). Процесс протекает с большой скоростью, образующиеся металл и шлак хорошо разделяются. Если теплоты выделяется недостаточно, в шихту вводят подогревающую добавку или проводят плавку в дуговых печах.
Соединение алюминия с кислородом сопровождается громадным выделением тепла, значительно большим, чем у многих других металлов. В виду этого при накаливании смеси оксида соответствующего металла с порошком алюминия происходит бурная реакция, ведущая к выделению из взятого оксида свободного металла. Метод восстановления при помощи Al (алюминотермия) часто применяют для получения ряда элементов (Cr, Mn, V, W и др.) в свободном состоянии.
Алюмотермией иногда пользуются для сварки отдельных стальных частей, в частности стыков трамвайных рельсов. Применяемая смесь (“термит”) состоит обычно из тонких порошков Аl (75%) и Fе3O4 (25%), которая поджигается при помощи запала из смеси Al и BaO2(зажигательная смесь готовится из порошка Аl и Na2O2 или ВаO2 в соотношении 1:1). Основная реакция идет по уравнению:
8Al+3Fe3O4=4Al2O3+9Fe+3350кДж. Для успешного течения алюмотермического процесса без внешнего подогрева необходимо, чтобы реакция восстановления выделила достаточное количество тепла. По правилу Жемчужного приход тепла на 1г шихты (теплопроизводительность шихты q) ориентировочно должен составлять не менее (550кал·4,1868) Дж. Если теплопроизводительность ниже этой нормы, то без подогрева извне процесс не получает развития.
Согласно второму закону термодинамики, самопроизвольно протекают процессы, идущие с уменьшением свободной энергии (G298 0). В первом приближении величину G298 изучаемой реакции восстановления можно рассчитать, пользуясь уравнением:
G298=Н298 - ТS298. (1.6)
Поскольку процессы металлотермического восстановления осуществляются в области весьма высоких температур, при ориентировочном расчете можно принять Т=2000К.
Допустив независимость тепловых эффектов от температуры, теплопроизводительность шихты (q) можно определить из уравнения:
q = - Н298/ΣМi, (1.7)
где ΣМi – сумма молекулярных (атомных) масс реагирующих веществ, взятых в стехиометрическом состоянии.
В случае присутствия в шихте нескольких окислов теплопроизводительность смеси находится на основании величины q для отдельных окислов:
q = (q1m1+q2m2+…+qnmn)/(m1+m2+…mn), (1.8)
где q1,q2,…qn – теплопроизводительность реакции восстановления определенного оксида, кал/г; m1,m2,…mn – сумма масс восстанавливаемого оксида и восстановителя (алюминия), г.
По значению q оценивается тепловая сторона процесса.
Расчет шихты для получения определенного количества сплава (металла) заданного состава представляет собой решение задач на базе стехиометрических уравнений и соотношений.
Пример. Рассчитать шихту для получения 20г ферромарганца, содержащего 30% Mn. Железо восстанавливается из Fe2O3, а марганец из MnO2. В качестве восстановителя использовать алюминий.
Расчет шихты:
кол-во железа: mFe = 20·70/100 = 14г,
кол-во марганца: mMn = 20·30/100 = 6г.
Расчет количества MnO2 (mMnO2) и Fe2O3 (mFe2O3), необходимых для получения 20г ферромарганца:
mMnO2 = mMn·М MnO2 /АMn = 6·87/54,93 = 9,5г
mFe2O3 = mFe·М Fe2O3 /2АFe = 14·160/55,85 = 20г,
где m – масса оксида или элемента; М – молекулярная масса; А – атомная масса.
Расчет количества восстановителя-алюминия, используя стехиометрические данные реакции восстановления.
Расчет количества Al, необходимого для получения 14г Fe:
2/3Fe2O3 + 4/3Al = 2/3Al2O3 + 4/3 Fe,
(4/3АAl )/ (4/3АFe) = mAl / mFe,
mAl = (4/3·26,97·14) / (4/3·55,85) = 6,76г.
Расчет кол-ва Al, необходимого для получения 6г Mn:
MnO2 + 4/3Al = 2/3Al2O3 + Mn,
4/3·АAl / АMn = mAl / mMn,
mAl = (4/3·26,97·6)/ 54,93 = 3,93г.
Следовательно, для получения 20г 30%-го сплава FeMn необходима следующая шихта:
mMnO2 = 9,5г; mFe2O3 = 20г;
mAl = 6,76 + 3,93 = 10,69г.
studfiles.net
Алюмотермия Википедия
Алюминотермия (алюмотермия; от лат. Aluminium и греч. therme — тепло, жар) — способ получения металлов, неметаллов (а также сплавов) восстановлением их оксидов металлическим алюминием:
2Al + Cr2О3 = Al2О3 + 2Cr; Fe2O3 + 2Al = 2Fe + Al2O3При этой реакции выделяется большое количество теплоты, смесь нагревается до 1900—2400 °C.
История
Алюминотермия (от алюминий и греч. thérme — теплота), алюминотермический процесс, получение металлов и сплавов восстановлением оксидов металлов алюминием (см. Металлотермия). Шихта (из порошкообразных материалов) засыпается в плавильную шахту или тигель и поджигается с помощью запальной смеси. Если при восстановлении выделяется много теплоты, осуществляется внепечная алюминотермия, без подвода тепла извне, развивается высокая температура (1900—2400°С), процесс протекает с большой скоростью, образующиеся металл и шлак хорошо разделяются. Если теплоты выделяется недостаточно, в шихту вводят подогревающую добавку или проводят плавку в дуговых печах (электропечная алюминотермия). В Советском Союзе электропечная алюминотермия была широко распространена. Алюминотермию применяют для получения низкоуглеродистых легирующих сплавов трудновосстановимых металлов — титана, ниобия, циркония, бора, хрома и др., для сварки рельсов и деталей стального литья; для получения огнеупора — термиткорунда. Алюминотермия открыта русским учёным Н. Н. Бекетовым (1859), в промышленности внепечной процесс освоен немецким химиком Г. Гольдшмидтом (1898).
Применение
Алюминотермия применяется для получения хрома, ванадия, марганца, вольфрама и других металлов и сплавов. Термит (смесь порошка алюминия с железной окалиной) используют при сварке рельсов, стальных труб, металлических конструкций.
См. также
Литература
- Плинер Ю. Л., Сучильников С. И., Рубинштейн Е. А. Алюминотермическое производство ферросплавов и лигатур, М., 1963.
Ссылки
wikiredia.ru
7.8. Алюминотермический способ получения металлического хрома и феррохрома
7.8. Алюминотермический способ получения металлического хрома и феррохрома |
Содержание > ГЛАВА 7. Электрометаллургия хромовых ферросплавов > 7.8. Алюминотермический способ получения металлического хрома и феррохрома
Металлический хром, соответствующий химическому составу по ГОСТ 5905-80, получают алюминотермическим методом (табл. 7.20) на Ключевском заводе ферросплавов. Восстановление хрома алюминием происходит с образованием промежуточного оксида CrO; процесс характеризуется следующими реакциями (298–2700 K):
Для выплавки металлического хрома используется оксид хрома с общим содержанием хрома в пересчете на Cr2O3>99 (марка ОХМ-0) и 98% (марка ОХМ-1). В качестве восстановителя применяется порошок первичного алюминия. При внепечной плавке для получения недостающего количества тепла в шихту вводят натриевую селитру, содержащую >99% NaNO3. В качестве флюса используют известь. Оксид кальция образует с Al2O3 соединения с пониженной температурой плавления (рис. 7.20).
Таблица 7.20. Химический состав, %, металлического хрома (ГОСТ 5905-80) различных марок
Примечание. Содержание Cr – не менее, для остальных – не более.
Введение СаО в шихту снижает температуру плавления шлака. В окислительных условиях возможно образование хромитохромата кальция 9СаО∙4CrO3∙Cr2O3 (tпл = 1218оС). Это облегчает получение хромоизвестковых расплавов перед восстановлением хрома из его оксида алюминием в период предварительного расплавления части оксидов в электропечи при выплавке металлического хрома и низкоуглеродистого феррохрома. На рис. 7.21 приведена технологическая схема получения металлического хрома, которая включает переработку конечных шлаков на полупродукт для синтетических шлаков или клинкер. Плавку металлического хрома на блок ведут в разъемном чугунном горне с футеровкой в нижней части стен магнезитовым кирпичом и подиной из магнезитового порошка. Горн устанавливается в специальной камере. Плавку проводят с использованием шихты, состоящей из оксида хрома (марки ОХМ-0 и ОХМ-1), алюминиевого порошка и натриевой селитры.
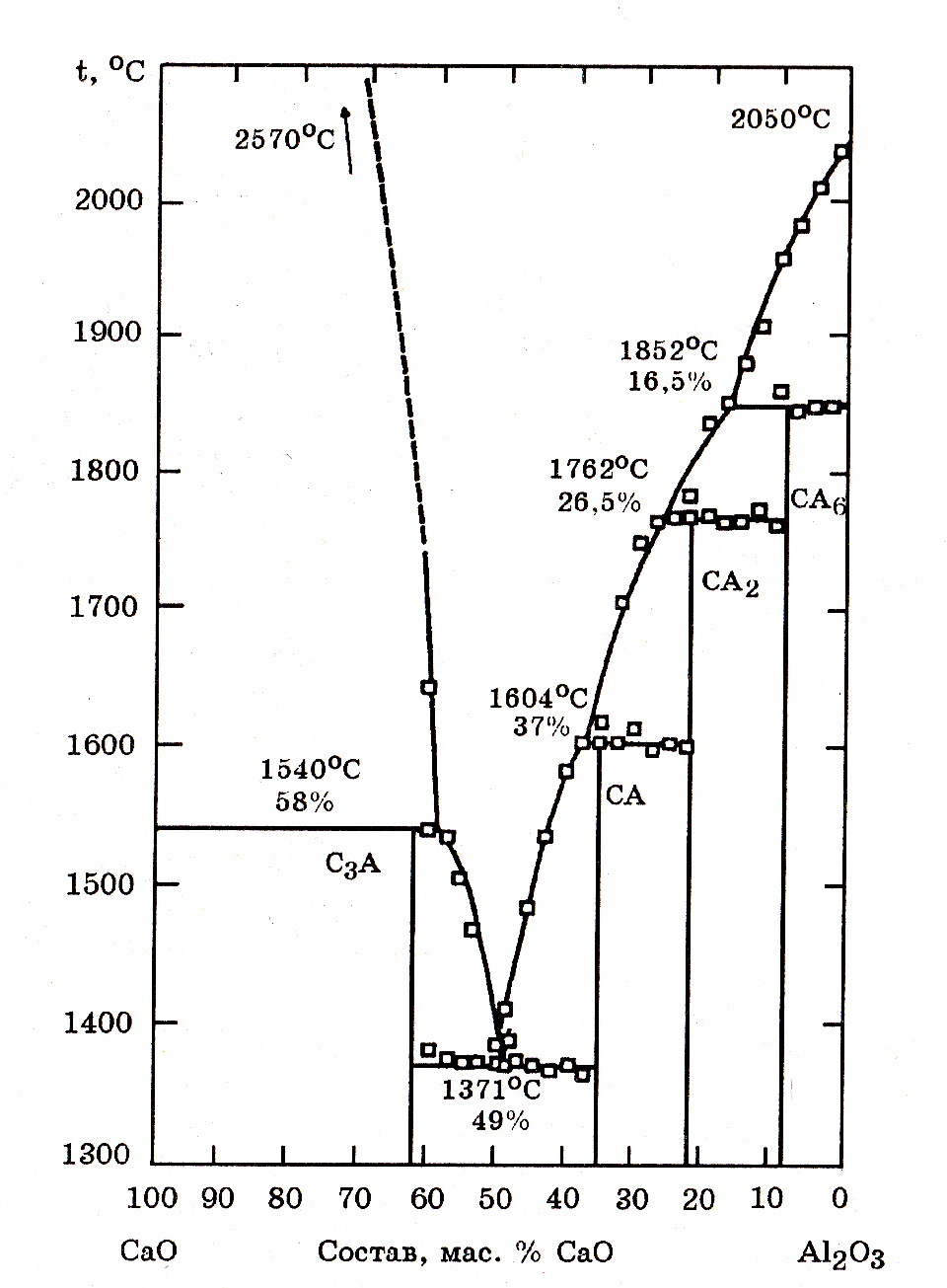
Рис.7.20. Диаграмма равновесного состояния системы СаО–Al2O3*
Плавку ведут с нижним запалом, задавая вначале в горн 10–15% всей шихты. Поджигают запальную смесь, состоящую из магниевого порошка или стружки магния и селитры, а затем, после начала восстановления, загружают остальную шихту, равномерно распределяя ее по поверхности расплава, и закрывают горн для уменьшения тепловых потерь. Полученный слиток охлаждают в воде, а затем подвергают дроблению. Для получения 1 т металлического хрома с 97% Cr расходуется 1650 кг Cr2O3, 620 кг алюминиевого порошка и 140 кг натриевой селитры. Извлечение хрома составляет 88%. Металл обычно содержит 98-99,3% Cr; 1,1–0,1% Al; 0,3–0,1% Si; 0,3–0,6% Fe; 0,01-0,02% C; 0,04–0,006% P; <0,02% S;0,03–0,2% N.
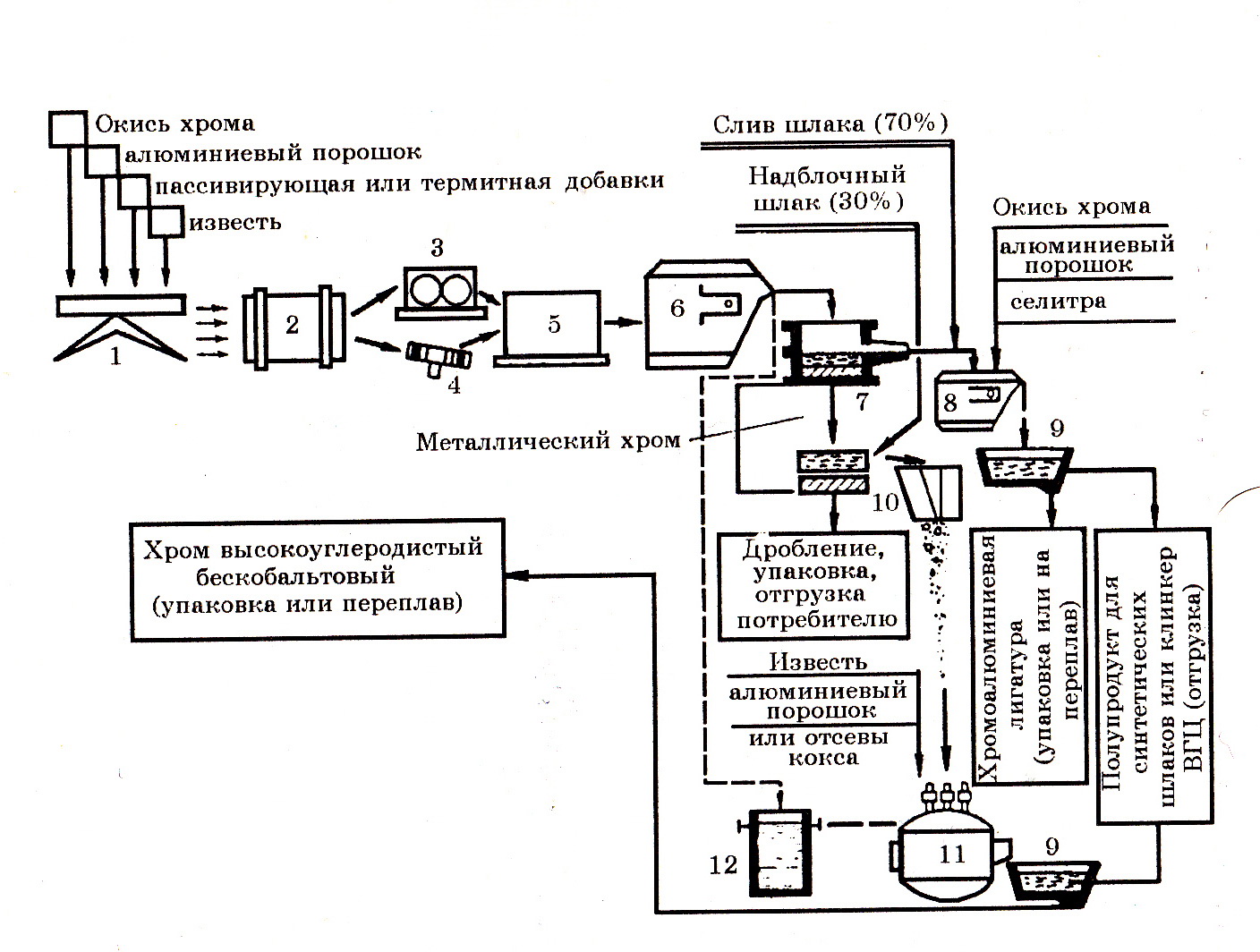
Рис. 7.21. Технологическая схема производства металлического хрома с довосстановлением шлаков и получением полупродукта или клинкера высокоглиноземистого цемента: 1 – весы; 2 – смеситель; 3 – пресс брикетировочный; 4 - гранулятор тарельчатый; 5 – печь сушильная; 6 – горн плавильный для выплавки металлического хрома; 7 – изложница для металла и шлака; 8 – горн для восстановления шлака; 9 – шлаковня; 10 – дробилка для шлака; 11 – электропечь для довосстановления шлака; 12 – ковш разливочный
При получении алюминотермического хрома особой чистоты внепечную плавку и разливку хрома ведут в герметичных камерах с созданием в них пониженного давления* (рис. 7.22). Шихту, состоящую из оксида хрома повышенной чистоты по примесным элементам, хромата кальция, хромового ангидрида и алюминиевого порошка (марки А99, ГОСТ 11069-79), окатывают. Затем окатыши прокаливают при 400–500оС для удаления влаги и окисления примесного углерода. Проплавление шихты ведут в реакционном горне. Хром и шлак выпускают из горна в изложницы, установленные в разливочной камере. Получаемый хром содержит от 0,001 до 0,01% азота и углерода каждого и водорода 1–2 см3/100 г. С использованием приведенных выше компонентов содержание примесных элементов существенно снижается: железа от 0,3 до 0,08%, кремния от 0,16 до 0,03%, при этом уменьшается содержание примесей цветных металлов.
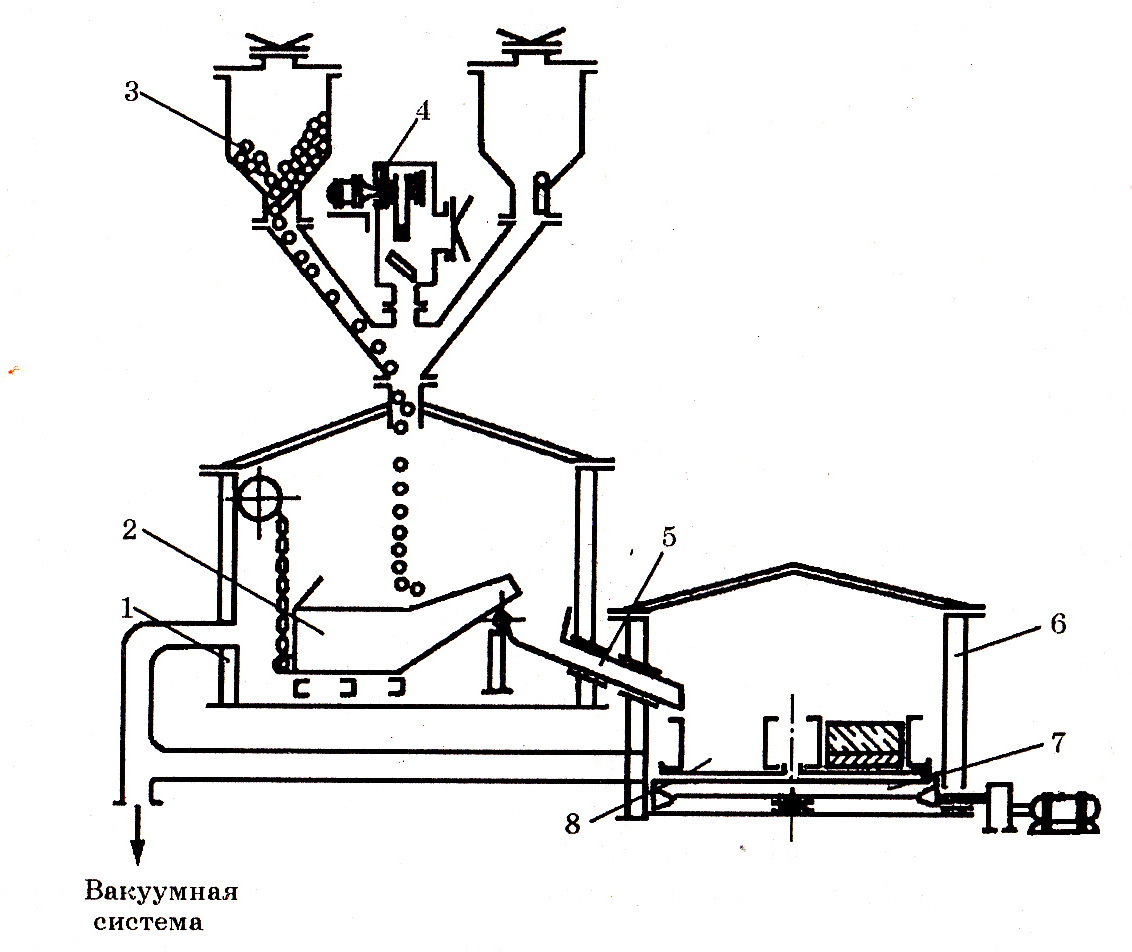
Рис. 7.22. Двухкамерная установка для внепечной выплавки сплавов под разрежением и в нейтральной атмосфере: 1 – плавильная камера; 2 – наклоняющийся плавильный горн; 3 – бункеры для окатышей; 4 - устройство для зажигания шихты; 5 – желоб для выпуска продуктов плавки; 6 – разливочная камера; 7 – поворотный стол; 8 - изложницы
Технология алюминотермического феррохрома. Алюминотермический низкоуглеродистый имеет следующий химсостав, %:
В качестве исходных шихтовых материалов используют хромитовый концентрат (58,5% Cr2O3; 1,6% SiO2; 10% Al2O3; 14% MgO), порошок первичного алюминия, известь и небольшое количество селитры. Плавку ведут в наклоняющемся плавильном агрегате. Удельная теплота процесса составляет 3100–3180 кДж/кг, что обеспечивает температуру процесса 2360оС. Извлечение хрома при плавке составляет 89%, а сквозное извлечение хрома с учетом потерь при обогащении ~58%. В табл. 7.21 приведены технико-экономические показатели получения алюминотермического феррохрома.
Таблица 7.21. Расходные коэффициенты и производительность электропечного агрегата при выплавке феррохрома алюминотермическим методом по различным вариантам плавки
Шлак содержит 60% Al2O3, 2–4% Cr2O3, 10–13% CaO, 20–24% MgO, 0,8–1% FeO и 0,8–1,5% SiO2, его направляют на переработку для получения высокоглиноземистого полупродукта или клинкера высокоглиноземистого цемента по приведенной выше схеме.
ttvsif.at.ua
Алюмотермия Википедия
Алюминотермия (алюмотермия; от лат. Aluminium и греч. therme — тепло, жар) — способ получения металлов, неметаллов (а также сплавов) восстановлением их оксидов металлическим алюминием:
2Al + Cr2О3 = Al2О3 + 2Cr; Fe2O3 + 2Al = 2Fe + Al2O3При этой реакции выделяется большое количество теплоты, смесь нагревается до 1900—2400 °C.
История[ | код]
Алюминотермия (от алюминий и греч. thérme — теплота), алюминотермический процесс, получение металлов и сплавов восстановлением оксидов металлов алюминием (см. Металлотермия). Шихта (из порошкообразных материалов) засыпается в плавильную шахту или тигель и поджигается с помощью запальной смеси. Если при восстановлении выделяется много теплоты, осуществляется внепечная алюминотермия, без подвода тепла извне, развивается высокая температура (1900—2400°С), процесс протекает с большой скоростью, образующиеся металл и шлак хорошо разделяются. Если теплоты выделяется недостаточно, в шихту вводят подогревающую добавку или проводят плавку в дуговых печах (электропечная алюминотермия). В Советском Союзе электропечная алюминотермия была широко распространена. Алюминотермию применяют для получения низкоуглеродистых легирующих сплавов трудновосстановимых металлов — титана, ниобия, циркония, бора, хрома и др., для сварки рельсов и деталей стального литья; для получения огнеупора — термиткорунда. Алюминотермия открыта русским учёным Н. Н. Бекетовым (1859), в промышленности внепечной процесс освоен немецким химиком Г. Гольдшмидтом (1898).
Применение[ | код]
Алюминотермия применяется для получения хрома, ванадия, марганца, вольфрама и других металлов и сплавов. Термит (смесь порошка алюминия с железной окалиной) используют при сварке рельсов, стальных труб, металлических конструкций.
См. также[ | код]
Литература[ | код]
- Плинер Ю. Л., Сучильников С. И., Рубинштейн Е. А. Алюминотермическое производство ферросплавов и лигатур, М., 1963.
Ссылки[ | код]
ru-wiki.ru
Алюмотермия Вики
Алюминотермия (алюмотермия; от лат. Aluminium и греч. therme — тепло, жар) — способ получения металлов, неметаллов (а также сплавов) восстановлением их оксидов металлическим алюминием:
2Al + Cr2О3 = Al2О3 + 2Cr; Fe2O3 + 2Al = 2Fe + Al2O3При этой реакции выделяется большое количество теплоты, смесь нагревается до 1900—2400 °C.
История[ | код]
Алюминотермия (от алюминий и греч. thérme — теплота), алюминотермический процесс, получение металлов и сплавов восстановлением оксидов металлов алюминием (см. Металлотермия). Шихта (из порошкообразных материалов) засыпается в плавильную шахту или тигель и поджигается с помощью запальной смеси. Если при восстановлении выделяется много теплоты, осуществляется внепечная алюминотермия, без подвода тепла извне, развивается высокая температура (1900—2400°С), процесс протекает с большой скоростью, образующиеся металл и шлак хорошо разделяются. Если теплоты выделяется недостаточно, в шихту вводят подогревающую добавку или проводят плавку в дуговых печах (электропечная алюминотермия). В Советском Союзе электропечная алюминотермия была широко распространена. Алюминотермию применяют для получения низкоуглеродистых легирующих сплавов трудновосстановимых металлов — титана, ниобия, циркония, бора, хрома и др., для сварки рельсов и деталей стального литья; для получения огнеупора — термиткорунда. Алюминотермия открыта русским учёным Н. Н. Бекетовым (1859), в промышленности внепечной процесс освоен немецким химиком Г. Гольдшмидтом (1898).
Применение[ | код]
Алюминотермия применяется для получения хрома, ванадия, марганца, вольфрама и других металлов и сплавов. Термит (смесь порошка алюминия с железной окалиной) используют при сварке рельсов, стальных труб, металлических конструкций.
См. также[ | код]
Литература[ | код]
- Плинер Ю. Л., Сучильников С. И., Рубинштейн Е. А. Алюминотермическое производство ферросплавов и лигатур, М., 1963.
Ссылки[ | код]
ru.wikibedia.ru
Алюмотермия - Справочник химика 21
АЛЮМИНОТЕРМИЯ (алюмотермия)— способ получения металлов и их сплавов, а также неметаллов восстановлением их оксидов металлическим алюминием. А, основана на том, что соединение кислорода с алюминием сопро- [c.18]Для сварки рельсов по методу алюмотермии используют порошок алюминия и оксид железа РедО . Составьте термохимическое уравнение, если при образопании 1 кг железа выдадилось 6340 кДж теплоты. [c.35]
Алюмотермией получают феррованадий, феррониобий и ферротантал. Чистый металлический ванадий может быть попучен методом восстановления У Об кальцием в стальной бомбе. Образующиеся частицы металлического ванадия после промывки сплавляются в слиток в вакуумной печи. Полученный таким образом металл содержит до 99,9% ванадия и обладает хорошей пластичностью. Ниобий и тантал можно получить термическим разложением пентаиодидов или пентахлоридов при 2000 С или восстановлением металлическим натрием или калием. [c.371]На этом свойстве А1 основан метод восстановления металлов (Сг, Мп, W, V и др.) из их оксидов — метод алюмотермии, открытый Н. Н. Бекетовым (1859). [c.277]
Относительно чистый хром получают методом алюмотермии [c.373]
Металлический алюминий служит в основном для производства сплавов. Сплавы алюминия менее устойчивы к коррозии из-за возникновения гальванических микроэлементов в местах включений примесей. Алюминий идет на производство кабелей, фольги, зеркал, серебристой краски. Способность алюминия восстанавливать металлы из оксидов при высоких температурах послужила основой метода алюмотермии, т. е. восстановления тугоплавких металлов, например хрома или марганца, из их оксидов [c.152]
По содержанию в земной коре хром относится к довольно распространенным элементам. Основной рудой хрома является Хромистый железняк РеО-СггОз. Элементарный хром можно получить методом алюмотермии из оксида хрома (III) [c.273]
Эксперимент 9.3. Проведение алюмотермии [c.145]
Алюмотермией называют реакции, протекающие между окислами металлов и алюминием, с образованием соответствующего свободного металла п окиси алюминия. Алюмотермией можно получить только те металлы, теплота образования окислов которых меньше теплоты образования окиси алюминия. Этим способом получают в промышленности такие металлы, как Сг, Мп, Т], [c.334]
В некоторых случаях (при низких температурах) исходным указателем возможного направления реакции является значение тепловых эффектов реакций образования сложных веществ из простых. Хорошо известный пример — реакция алюмотермии [c.55]
Получение марганца алюмотермией. В фарфоровый тигель возьмите 10 г пиролюзита и прокалите его при температуре 800 С в течение 1 ч. Полученный продукт охладите и перемешайте в ступке с 3 частями порошкообразного алюминия. Смесь поместите в фарфоровый тигель, уплотните ее, вставьте посредине магниевую ленту, зачищенную наждачной бумагой, и сверху насыпьте 10 частей зажигательной смеси. Зажигательную смесь приготовьте, осторожно свешивая в стакане 10 частей пероксида бария с 1 частью магния (или алюминия). Тигель закройте асбестовой крышкой с отверстием для магниевой ленты, поставьте на песочную баню (опыт проводите в вытяжном шкафу), погрузив стенки тигля в песок на /з глубины. Затем длинной лучинкой подожгите магниевую ленту (опыт проводите в присутствии преподавателя). Наблюдайте бурную реакцию восстановления марганца алюминием. После охлаждения тигель разбейте и выньте королек металла. [c.120]
Эта особенность алюминия широко используется для получения различных металлов из окислов путем восстановления их алюминием. Впервые метод восстановления металлов из их окислов алюминием был применен русским ученым Н. Н. Бекетовым и получил название алюмотермии. [c.334]
Последняя из приведенных здесь реакций лежит в основе процесса алюмотермии. [c.119]
Хром может быть получен с помощью реакции алюмотермии [c.113]
Высокий электроотрицательный потенциал алюминия и значительное сродство к кислороду обусловили его применение в качестве раскислителя сталей, восстановителя при получении ряда материалов методом алюмотермии. [c.477]
Проведите реакцию алюмотермии (разд. 50.1,1.3). [c.587]
В промышленности иногда применяется и неорганическое топливо. Так. при обжиге некоторых руд и в алюмотермии используется тепло, полученное в результате сжигания серы и алюминия, но все эти вещества не являются топливом в общетехническом смысле этою понятия. [c.4]
I) А1+р з04— АЬОз+Ре — реакция алюмотермии. В качестве окислителя выступают ионы железа Ре + и РеЗ+, а атомы алюминия являются сильнейшим восстановителем. [c.411]
Хром легко пассивируется, поэтому широко используется в ка- естве гальванических защитных покрытий и для получения корро- ионностойких сталей. Молибден применяется для изготовления химической аппаратуры, вольфрам — в электротехнической промышленности (в частности, для производства ламп накаливания). 4олибден и вольфрам применяются в качестве катализаторов. Относительно чистый хром получают методом алюмотермии [c.550]
Вычислите термодинамические характеристики АЯ°298, AS°298, ЛС°298 процссса алюмотермии при стандартной температуре и 1000°С [c.113]
Вследствие высокого сродства к кислороду (ДС /== —1582кДж/моль А12О3) алюминий активно восстанавливает многие металлы из оксидов алюмотермия). При этом реакция обычно сопровождается выделением большого количества тепла и повышением температуры до 1200— 3000 С. Алюмотермия применяется в производстве марганца, хрома, ванадия, вольфрама, ферросплавов. [c.452]
В промышленности используют два типа скелетных никелевых катализаторов — катализатор Бага [193] и никель Ренея [194]. Оба получают из сплава N1 с А1, однако, если никель Ренея представляет собой мелкодисперсный порошок, состоящий из чистого никеля, то катализатор Бага — кусочки никель-алюминиевого сплава (65—75% N1 и 35—25% А1). Исходные сплавы получают чаще всего пирометаллургическими способами — сплавлением компонентов или алюмотермией. В последнее время используют методы порошкообразной металлургии — спекание предварительно спрессованных смесей никелевых и алюминиевых порошков в восстановительной или инертной атмосфере при 660—700 °С. Реакции между двумя твердыми телами с образованием новой твердой фазы включают процесс диффузии, поскольку реагирующие вещества разделяются образующимся продуктом реакции [174]. Реагирующие вещества сохраняют постоянную активность с обеих сторон реакционной поверхности раздела фаз, в связи с чем скорость переноса материала определяется скоростью нарастания толщины диффузионного слоя продукта и выражается формулой [c.166]
При восстановлении 80 г оксида жепеза (1Л) алюминием (реакция алюмотермии) выделяется 42 6,3 кДж. При сгорании 5,4 г металлического алюминия выделяется 167,3 кДж. На основании этих данных вычислить теплоту образования оксида железа (111). [c.46]
Кобальт обычно получают переработкой полиметаллических руд. Рядом последовательных пйрометаллургических операций выделяют С03О4, который затем восстанавливают углем, водородом, иногда методом алюмотермии. Особо чистый кобальт получают электролитическим рафинированием, а также термическим разложением некоторых его соединений. Основная масса производимого кобальта используется для получения сплавов его применяют для электролитического покрытия металлических деталей. [c.596]
Благодаря большому отрицательному значению ДО (АЬОз) возможна алюмотермия — выделение металлов из их оксидов при действии алюминия. Этот весьма общий метод получения металлов был предложен Н. Н. Бекетовым в 1859 г. Алюмотермию используют для лабораторного получения многих металлов (Мп, Сг, У, V и др.) и в ряде случаев в промышленности (получение Са, 5г, Ваидр.). [c.343]
Кобальт обычно получают переработкой полиметаллических руд. Рядом последовательных пирометаллургических операций выделяют С03О4, который затем восстанавливают углем, водородом, иногда методом алюмотермии. Особо чистый кобальт получают электролитическим рафинированием, а также термическим разложением некоторых его соединений. [c.634]
Наряду с сродством к фтору бор обладает также очень сильным сродством к кислороду (см. получение элементов из их оксидов алюмотермией в разд. 36.2). Соединения бора с кислородом обычно можно получить путем окисления бора кислородом воздуха. Гидролиз галогенидов бора (ВС1з и др.), в которых [c.573]
Применение основа легких сплавов, применяемых в авто- и самолетостроении, судо- и вагоностроении, моторо- и машиностроении и т. д., раскислитель стали, в алюмотермии (с. 152). [c.183]
Опыт 15. Алюмотермия (ТЯГА ). Термит — сухую смесь порошков Рсз04 (257о) и А1 (75%) — внесите в тигель из термостойкого материала, насыпьте в середину зажигательную смесь и укрепите в ней магниевую ленту. (Зажигательная смесь готовится из порошка А1 и ЫагОг или ВаОг в соотношении 1 1.) Установите тигель за защитным экраном на асбестовом листе и подожгите ленту магния. Объясните наблюдаемое. Какое практическое значение находит термит [c.94]
Опыт 2. Получение марганца методом алюмотермии. Приготовьте МП3О4. Для этого 40 г тонкоизмельченного МпОг поместите в тигель и нагревайте при 800° С в муфельной печи в течение часа. После охлаждения полученный МП3О4 разотрите в порошок и тщательно перемешайте с 10 г порошка алюминия. Смесь поместите в шамотный тигель, покройте слоем 10 г зажигательной смеси. В смесь вставьте магниевую ленту. Тигель поставьте а вытяжной шкаф, магниевую ленту подожгите горящей лучинкой, закрепленной в длинную стеклянную трубку. Объясните энергичное течение реакции. По охлаждении металлический порошок отделите от шлака и сдайте лаборанту. [c.139]
Значительное количество алюминия расходуется для получения металлов методом алюмотермии. Соединение алюминия с кислородом, как указывалось, сопровождается очень большим выделением теплоты, намного превышающим таковое для других металлов. В связи с этим при накаливании смеси оксида с порошком алюминия происходит бурная реакция, сопровождающаяся выделением свободного металла. Например, при поджигании особым запалом термита (смеси А1 и Рез04) [c.282]
Наибольшие количества металлического хрома получают из хромита. Для этого предварительной обработкой получают окись хрома СггОз, а затем алюмотерми-ческим способом восстанавливают металлический хром (см. 3, гл. XVni). Отметим, что металлический хром можно получить не только алюмотермией, но также восстанавливая СггОз при нагревании с кремнием, кальцием, водородом, а также электролитическим восстановлением расплавов солей хрома. [c.339]
Теплота образования V2O5 равна 1050 1 Цж/моль, а АЬОз— 1652 кДж/моль. Определите тепловой эффект реакции получения ванадия методом алюмотермии. [c.26]
Неорганическая химия (1989) -- [ c.44 , c.45 , c.131 ]Общая химия (1987) -- [ c.193 , c.226 ]
Общая и неорганическая химия Изд.3 (1998) -- [ c.489 ]
Справочник Химия изд.2 (2000) -- [ c.307 ]
Современная общая химия Том 3 (1975) -- [ c.182 ]
Курс неорганической химии (1963) -- [ c.385 ]
Курс общей химии (1964) -- [ c.195 , c.245 , c.380 ]
Неорганическая химия (1979) -- [ c.252 ]
Общая и неорганическая химия (1981) -- [ c.343 ]
Современная общая химия (1975) -- [ c.182 ]
Общая и неорганическая химия (1994) -- [ c.355 ]
Общая и неорганическая химия (1981) -- [ c.242 ]
Основы общей химической технологии (1963) -- [ c.194 ]
Теоретические основы общей химии (1978) -- [ c.262 ]
Общая химическая технология Том 2 (1959) -- [ c.126 , c.174 , c.189 ]
Курс неорганической химии (1972) -- [ c.345 ]
Химия Справочник (2000) -- [ c.230 ]
chem21.info
Свойства хрома| Задания 412 - 415
Задание 411Хромит калия окисляется бромом в щелочной среде. Зеленая окраска раствора переходит в желтую. Составьте электронные и молекулярные уравнения реакции. Какие ионы обусловливают начальную и конечную окраску раствора?Решение:Уравнения электронного баланса:
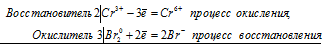
Ионно-молекулярное уравнение:
2Cr3+ + 3Br20 = 2Cr6+ + 6Br-
Молекулярное уравнение реакции:
2KCrO2 + 3Br2 + 8NaOH = 2K2CrO4 + 6KBr + 4h3O
Начальная, зелёная окраска обусловливается хромит-ионами CrO2-, а конечная, жёлтая – хромат-ионами CrO42-.
Задание 412Составьте электронные и молекулярные уравнения реакций растворения: а) молибдена в азотной кислоте; б) вольфрама в щелочи в присутствии кислорода. Учтите, что молибден и вольфрам приобретают высшую степень окисления.Решение:а) Растворение молибдена в азотной кислоте:
Уравнения электронного баланса:
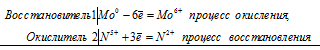
Ионно-молекулярное уравнение:
Mo0 + 2N5+ = Mo6+ + 2N2+
Молекулярное уравнение реакции:
Mo + 2HNО3 = h3MoO4 + 2NO
б) Растворение вольфрама в щелочи в присутствии кислорода:
Уравнения электронного баланса:
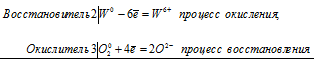
Ионно-молекулярное уравнение:
2W0 + 3O20 = 2W6+ + 6O2-
Молекулярное уравнение реакции:
2W + 3O2 + 4NaOH = 2Na2WO4 + 2h3O
Задание 413При сплавлении хромита железа Fe(CrO2)2 с карбонатом натрия в присутствии кислорода хром (III) и железо (II) окисляются и приобретают соответственно степени окисления +6 и +3. Составьте электронные и молекулярное уравнения реакции.Решение:Уравнения электронного баланса:

Ионно-молекулярное уравнение:
4Fe(CrO2)2 + O20 = 8CrO42- + 4Fe3+ + 2O2-
Молекулярное уравнение реакции:
4Fe(CrO2)2 + O2 + 8Na2CO3 8Na2CrO4 + 2Fe2O3&darr + 8CO2 ↑
Задание 414К подкисленному серной кислотой раствору дихромата калия прибавили порошок алюминия. Через некоторое время оранжевая окраска раствора перешла в зеленую. Составьте электронные и молекулярное уравнения реакции.Решение:Уравнения электронного баланса:
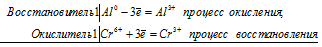
Ионно-молекулярное уравнение:
Al0 + Cr6+ = Al3+ + Cr3+
Молекулярное уравнение реакции:
2Al + K2Cr2O7 + 3h3SO4 = Al2(SO4)3 + 2KCrO2 + 3h3O
Задание 415Хром получают методом алюминотермии из его оксида (III), а вольфрам - восстановлением оксида вольфрама (VI) водородом. Составьте электронные и молекулярные уравнения соответствующих реакций.Решение:а) Получение хрома методом алюминотермии:
Уравнения электронного баланса:
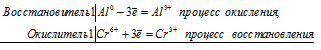
Ионно-молекулярное уравнение:
Al0 + Cr6+ = Al3+ + Cr3+
Молекулярное уравнение реакции:
2Al + Cr2O3 = Al2О3 + 2Cr
б) Получение вольфрама методом алюминотермии:
Уравнения электронного баланса:
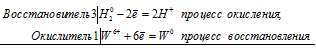
Ионно-молекулярное уравнение:
3Н20 + W6+ = 6H+ + W0
Молекулярное уравнение реакции:
3Н2 + WO3 = 3h3O + W
buzani.ru





