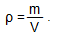Железо в периодической таблице менделеева. Хром в таблице менделеева обозначение
Железо положение в таблице менделеева
Железо, его положение в периодической системе химических элементов Д. И. Менделеева, взаимодействие с серой, хлороводородной кислотой, растворами солей.
ПЛАН ОТВЕТА:
положение в п. с. и строение атома физические свойства химические свойства Химический элемент железо находится в 4-ом периоде 8-ой группе побочной подгруппе. В атоме железа четыре электронных слоя. Электронами заполняется d–подуровень третьего слоя, на нём находится 6 электронов, а на четвёртом слое s–подуровне находится 2 электрона. В соединениях железо проявляет степени окисления +2 и +3.
| IV период VIII группа побочная подгруппа | Fe)))) | +2 | +3 | ||
| +26 2 8 8+6 2 | 4s | ?? | |||
| 3d | ?? | ? | ? | ? | ? |
Простое вещество железо – серебристо-белый металл с температурой плавления 15390С, плотностью 7,87 г/см3, обладает магнитными свойствами. Железо – химически активный металл. При нагревании оно взаимодействует с серой с образованием сульфида железа(II): Fe0 + S0 = Fe+2S-2. Железо вытесняет водород из растворов кислот, при этом образуются соли железа(II), например, при действии на железо соляной кислоты образуется хлорид железа(II): Fe0 + 2H+1Cl-1 = Fe+2Cl2-1 + h30. Железо может вытеснять менее активные металлы из растворов их солей, например, при действии железа на раствор сульфата меди(II) образуются металлическая медь и сульфат железа(II): Fe0 + Cu+2SO4 = Cu0 + Fe+2SO4.
Во всех реакциях железо проявляет свойства восстановителя. Более сильные окислители – хлор, кислород, концентрированные кислоты – окисляют железо до степени окисления +3.
Если домашнее задание на тему: » Железо, его положение в периодической системе химических элементов Д И Менделеева, взаимодействие оказалось вам полезным, то мы будем вам признательны, если вы разместите ссылку на эту сообщение у себя на страничке в вашей социальной сети.  Свежие новости
Сочинения по теме
- Гимназия №12, г. Липецк Знаменщикова Надежда Александровна Тема урока: Железо и его соединения(9 класс) Цель: сформировать понятие о зависимости направления реакций окисления от Тест «Химический элемент» Названия химических элементов имеют в основном ……. Происхождение Знаки химических элементов обозначаются Латинскими буквами Английским и буквами Русскими буквами Заполните пропуски в таблице Химический Урок химии в 9 классе на тему «Мир металлов». Разработку составила учитель химии муниципального автономного общеобразовательного учреждения «Базарно-Матакская средняя общеобразовательная Контрольная работа по химии по теме «Кислород и сера» Вариант 1 1.Составить уравнения электролитической диссоциации серной кислоты. 2. Составить полное и сокращенное уравнения
- Тест ЕГЭ по химии Обратимые и необратимые химические реакции Химическое равновесие Ответы
Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов 1. Химическое равновесие в системе 2NO(г)
Ниобий в компактном состоянии представляет собой блестящий серебристо-белый (или серый в порошкообразном виде) парамагнитный металл с объёмноцентрированной кубической кристаллической решеткой.
Имя существительное. Насыщение текста существительными может стать средством языковой изобразительности. Текст стихотворения А. А. Фета «Шепот, робкое дыханье...», в свое
1. Железо: положение в периодической системе химических элементов Д. И. Менделеева, строение атома, во
overmedic.ru
Железо в периодической таблице менделеева
МЕТАЛЛЫ ПОБОЧНЫХ ПОДГРУПП
Характеристика переходных элементов – меди, хрома, железа по их положению в периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов.
Понятие переходный элемент обычно используется для обозначения любого из d- или f-элементов. Эти элементы занимают переходное положение между электроположительными s-элементами и электроотрицательными p-элементами. d-Элементы образуют три переходных ряда - в 4-м, 5-м и 6-м периодах соответственно. Первый переходный ряд включает 10 элементов, от скандия до цинка. Он характеризуется внутренней застройкой 3d-орбиталей. Хром и медь имеют на 4s-орбиталях всего по одному электрону. Дело в том, что полузаполненные или заполненные d-подоболочки обладают большей устойчивостью, чем частично заполненные. В атоме хрома на каждой из пяти 3d-орбиталей, образующих 3d-подоболочку, имеется по одному электрону. Такая подоболочка является полузаполненной. В атоме меди на каждой из пяти 3d-орбиталей находится по паре электронов (аналогичным образом объясняется аномалия серебра). Все d-элементы являются металлами. Большинство из них имеет характерный металлический блеск. По сравнению с s-металлами их прочность в целом значительно выше. В частности, для них характерны свойства: высокий предел прочности на разрыв; тягучесть; ковкость (их можно расплющить ударами в листы). d-элементы и их соединения обладают рядом характерных свойств: переменные состояния окисления; способность к обра зованию комплексных ионов; образование окрашенных соединений. d-Элементы характеризуются также более высокой плотностью по сравнению с другими металлами. Это объясняется сравнительно малыми радиусами их атомов. Атомные радиусы этих металлов мало изменяются в этом ряду. d-Элементы - хорошие проводники электрического тока, особенно те из них, в атомах которых имеется только один внешний s-электрон сверх полузаполненной или заполненной d-оболочки. Например, медь.
Химические свойства .
Электроотрицательность металлов первого переходного ряда возрастают в направлении от хрома к цинку. Это означает, что металлические свойства элементов первого переходного ряда постепенно ослабевают в указанном направлении. Такое изменение их свойств проявляется и в последовательном возрастании окислительно-восстановительных потенциалов с переходом от отрицательных к положительным значениям.
Характеристика хрома и его соединений
Хром - твердый, голубовато-белый металл.ρ = 7,2г/см 3 , t плавл = 1857 0 С СО: +1,+2,+3,+4,+5,+6Химические свойства.
- При обычных условиях хром реагирует только со фтором. При высоких температурах (выше 600 0 C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором.
4Cr + 3O 2 2Cr 2 O 3
2Cr + 3Cl 2 2CrCl 3
2Cr + 3S Cr 2 S 3
- В раскалённом состоянии реагирует с парами воды:
2Cr + 3H 2 O Cr 2 O 3 + 3H 2
- Хром растворяется в разбавленных сильных кислотах (HCl, H 2 SO 4). В отсутствии воздуха образуются соли Cr 2+ , а на воздухе – соли Cr 3+ .
Cr + 2HCl → CrCl 2 + H 2 -
2Cr + 6HCl + O 2 → 2CrCl 3 + 2H 2 O + H 2 -
- Наличие защитной окисной плёнки на поверхности металла объясняет его пассивность по отношению к холодным концентрированным кислотам – окислителям. Однако при сильном нагревании эти кислоты растворяют хром:
2 Сr + 6 Н 2 SО 4 (конц) Сr 2 (SО 4) 3 + 3 SО 2 + 6 Н 2 О
Сr + 6 НNО 3 (конц) Сr(NО 3) 3 + 3 NO 2 + 3 Н 2 О
Получение.Соединения хрома
Соединения двухвалентного хрома
Оксид хрома (II ) CrO
Физические свойства: твердое нерастворимое в воде вещество ярко-красного или коричнево- красного цвета. Химические свойства. CrO – основной оксид.Получение.
Cr 2 O 3 + 3Н 2 2Cr + 3H 2 O Гидроксид хрома (II ) Сr(ОН) 2 Физические свойства: твердое нерастворимое в воде вещество желтого цвета. Химические свойства. Сr(ОН) 2 – слабое основание.- Взаимодействует с кислотами: Cr(OH) 2 + 2HCl → CrCl 2 + 2H 2 O Легко окисляется в присутствии влаги кислородом воздуха в Сr(ОН) 3:
4Cr(OH) 2 + O 2 + 2H 2 O → 4Cr(OH) 3
- При прокаливании разлагается:
Соединения трёхвалентного хрома
Оксид хрома (III ) Cr 2 O 3 Физические свойства: темно-зеленое тугоплавкое вещество, нерастворимое в воде. Химические свойства. Cr 2 O 3 - амфотерный оксид.Хромит натрия
- При высокой температуре восстанавливается водородом, кальцием, углеродом до хрома:
Cr 2 O 3 + 3Н 2 2Cr + 3H 2 O
Получение.
Гидроксид хрома (III ) Cr (OH ) 3 Физические свойства: нерастворимое в воде вещество зелёного цвета. Химические свойства. Сr(ОН) 3 – амфотерный гидроксид2Cr(OH) 3 + 3H 2 SO 4 →Cr 2 (SO 4) 3 + 6H 2 O
Cr(OH) 3 + KOH → KCrO 2 + 2H 2 O
(хромит калия) Получение.
- При действии щелочей на соли Сr 3+ выпадает студнеобразный осадок гидроксида хрома (III) зеленого цвета:
Сr 2 (SО 4) 3 + 6NaОН → 2 Сr(ОН) 3 ↓ + 3 Na 2 SО 4 ,
Соединения шестивалентного хрома
Оксид хрома (VI ) CrO 3 Физические свойства: твердое вещество темно-красного цвета, хорошо растворимое в воде. Ядовит! Химические свойства. CrO 3 – кислотный оксид.- Взаимодействует со щелочами, образуя соли желтого цвета-хроматы:
CrO 3 + 2KOH → K 2 CrO 4 + H 2 O
- Взаимодействует с водой, образуя кислоты: CrO 3 + H 2 O → H 2 CrO 4 хромовая кислота
- Термически неустойчив: 4 CrO 3 → 2Cr 2 O 3 + 3O 2
- Получают из хромата (или дихромата) калия действием H 2 SO 4 (конц.).
K 2 CrO 4 + H 2 SO 4 → CrO 3 + K 2 SO 4 + H 2 O
K 2 Cr 2 O 7 + H 2 SO 4 → 2CrO 3 + K 2 SO 4 + H 2 O
Гидроксиды хрома (VI) H 2 CrO 4 - хромовая кислота , H 2 Cr 2 O 7 - дихромовая кислота Обе кислоты неустойчивы, при попытке их выделения в чистом виде распадаются на воду и оксид хрома (VI). Однако соли их вполне устойчивы. Соли хромовой кислоты называют хроматами, они окрашены в желтый цвет, а соли дихромовой кислоты – дихроматами, они окрашены в оранжевый цвет.Железо и его соединения
Железо – сравнительно мягкий ковкий металл серебристого цвета, пластичный, намагничивается. T плавл =1539 0 С. ρ = 7,87г/см 3 . СО: +2 – со слабыми окислителями – растворы кислот, солей, неметаллы, кроме кислорода и галогенов +3 – с сильными окислителями – концентрированные кислоты, кислород, галогены.Химические свойства.
- Взаимодействие с простыми веществами.
- Горит в кислороде, образуя окалину - оксид железа (II,III): 3Fe + 2O 2 → Fe 3 O 4 Железо реагирует с неметаллами при нагревании:
- Взаимодействие со сложными веществами.
- При высокой температуре (700–900C) железо реагирует с парами воды:
3Fe
pbmc.ru
Монетные металлы - Современные монетные металлы
Химия - Монетные металлы - Современные монетные металлы
01 марта 2011Оглавление:1. Монетные металлы2. Современные монетные металлы3. «Монетные неметаллы»4. Монетные металлы и типы денежных систем
В настоящее время помимо сплавов золота, серебра и меди денежные знаки изготавливают из алюминия, цинка, никеля, палладия, платины или их сплавов. Их обозначают в соответствии с Периодической системой химических элементов или локальными национальными стандартами, например:
| Алюминий | Al | A |
| Алюминиевая бронза | CuAl | МА |
Список монетных металлов
| Акмонитал | (сплав железа с хромом, кремнием,углеродом, магнием, серой и фосфором) |  | 1 итальянская лира |
| Алюминиевая бронза | CuAl | 10 французских сантимов | |
| Алюминий | Al |  | 1 польский злотый |
| Биллон | CuAg | 10 австрийских крейцеров | |
| Бронза | CuSn |  | Древнеримский бронзовый асс |
| Железо | Fe | ||
| Сталь |   | Американский стальной цент | |
| Чугун | |||
| Золото | Au |  | Златник Владимира |
| Колыванская медь | CuAuAg |  | Сибирская монета достоинством 10 копеек |
| Латунь | CuZn |  | 10 копеек |
| Медно-никелевый сплав | CuNi |  | 10 копеек |
| Медно-цинковый сплав | CuZn |  | 5 копеек |
| Медь | Cu | Полновесная медная копейка | |
| Мельхиор | CuNiFeMn |  | 10 польских грошей |
| Нейзильбер | CuZnNi |  | 2 украинских гривны |
| Нержавеющая сталь | FeCrNi |  | 1 французский сантим |
| Никелевая бронза | CuSnNi | ||
| Никелево-железный сплав | NiFe | ||
| Никелево-цинковый сплав | NiZn | ||
| Никель | Ni |  | 5 французских франков |
| Олово | Sn | Как правило, используетсядля изготовления фальшивых или пробных монет | |
| Палладий | Pd |   | 25 рублей |
| Платина | Pt |  | 50 канадских долларов |
| Потин | (сплав меди с большим содержанием олова,свинца и других металлов) |  | Монета древних кельтов |
| Северное золото | CuAlZnSn |  | Монеты достоинством 10, 20 и 50 евроцентов |
| Серебро | Ag |  | Сребреник Ярослава Мудрого |
| Свинец | Pb | Как правило, используетсядля изготовления фальшивых или пробных монет | |
| Стерлинг | AgCu |  | Пенни Эдуарда I |
| Хром | Cr | ||
| Хромированная сталь | FeCr |  | 3 румынских лея |
| Цинк | Zn |  | 10 пфеннигов |
| Электр, электрон, электрум | AuAg |  | Лидийская монета |
Просмотров: 3210
4108.ru
Периодическая система химических элементов Д.И.Менделеева. Таблица Менделеева.
| |||||||||||||||||||||||||||||||||||||||||
tehtab.ru