7.9 Виды веществ и их агрегатное состояние. Агрегатное состояние хрома
Физические свойства оксидов — урок. Химия, 8–9 класс.
Агрегатное состояние
Оксиды металлов, например, оксид меди(\(II\)) CuO, оксид железа(\(III\)) Fe2O3, оксид кальция CaO, являются твёрдыми кристаллическими веществами.
Некоторые оксиды неметаллов при обычных условиях также находятся в твёрдом агрегатном состоянии. Например, твёрдыми веществами являются оксид кремния SiO2, оксид фосфора(\(V\)) P2O5 и оксид серы(\(VI\)) SO3.
Жидким веществом является оксид водорода, то есть вода h3O.
Среди оксидов неметаллов при нормальных условиях некоторые являются газообразными веществами. Например, SO2, N2O, NO, NO2, CO и CO2.
Цвет оксидов может быть самым разнообразным.
Отметим, что бесцветным, например, является оксид кремния в виде кварца или горного хрусталя. Из жидких оксидов цвета не имеет вода. Большинство газообразных оксидов также не имеет окраски.
Оксид меди(\(I\)) Cu2O — вещество красного цвета:

Оксид меди(\(II\)) CuO чёрного цвета:

Оксид магния MgO белого цвета:

Оксид хрома(\(III\)) Cr2O3 тёмно-зелёного цвета:

Оксид азота(\(IV\)) NO2 — газообразное вещество бурого цвета. Такой же цвет у твёрдого оксида железа(\(III\)) Fe2O3:

Риски, связанные с воздействием оксидов на организм
Самый ядовитый из оксидов — оксид углерода(\(II\)), или угарный газ CO. Его молекулы связываются гемоглобином крови намного прочнее, чем молекулы кислорода. Поэтому при наличии даже незначительной примеси этого вещества в воздухе человек может погибнуть от удушья.
Ядовитыми также являются диоксид серы SO2 и диоксид азота NO2.
www.yaklass.ru
Оксиды
Несолеобразующие (безразличные, индифферентные) оксиды СО, SiO, N20, NO.
Солеобразующие оксиды:
Основные. Оксиды, гидраты которых являются основаниями. Оксиды металлов со степенями окисления +1 и +2 (реже +3). Примеры: Na2O - оксид натрия, СаО - оксид кальция, CuO - оксид меди (II), СоО - оксид кобальта (II), Bi2O3 - оксид висмута (III), Mn2O3 - оксид марганца (III).
Амфотерные. Оксиды, гидраты которых являются амфотерными гидроксидами. Оксиды металлов со степенями окисления +3 и +4 (реже +2). Примеры: Аl2O3 - оксид алюминия, Cr2O3 - оксид хрома (III), SnO2 - оксид олова (IV), МnO2 - оксид марганца (IV), ZnO - оксид цинка, ВеО - оксид бериллия.
Кислотные. Оксиды, гидраты которых являются кислородсодержащими кислотами. Оксиды неметаллов. Примеры: Р2О3 - оксид фосфора (III), СO2 - оксид углерода (IV), N2O5 - оксид азота (V), SO3 - оксид серы (VI), Cl2O7 - оксид хлора (VII). Оксиды металлов со степенями окисления +5, +6 и +7. Примеры: Sb2O5 - оксид сурьмы (V). СrОз - оксид хрома (VI), МnОз - оксид марганца (VI), Мn2O7 - оксид марганца (VII).

Изменение характера оксидов при увеличении с. о. металла | Cr+2O (осн.) | Cr+32O 3(амф.) | Cr+6O 3(кисл.) |
Mn+2O (осн.) | Mn+4O2 (амф.) | Mn+6O3 (кисл.) | |
Mn+32O3 (осн.) | Mn+72O 7 (кисл.) |
Оксиды бывают твердые, жидкие и газообразные, различного цвета. Например: оксид меди (II) CuO черного цвета, оксид кальция СаО белого цвета - твердые вещества. Оксид серы (VI) SO3 - бесцветная летучая жидкость, а оксид углерода (IV) СО2 - бесцветный газ при обычных условиях.
Твердые:
CaO, СuО, Li2O и др. основные оксиды; ZnO, Аl2O3, Сr2O3 и др. амфотерные оксиды; SiO2, Р2O5, СrO3 и др. кислотные оксиды.
Жидкие:
SO3, Cl2O7, Мn2O7 и др..
Газообразные:
CO2, SO2, N2O, NO, NO2 и др..
Растворимые:
а) основные оксиды щелочных и щелочноземельных металлов;
б) практически все кислотные оксиды (исключение: SiO2).
Нерастворимые:
а) все остальные основные оксиды;
б) все амфотерные оксиды
в) SiO2
1. Кислотно-основные свойства
Общими свойствами основных, кислотных и амфотерных оксидов являются кислотно-основные взаимодействия, которые иллюстрируются следующей схемой:

Пример:

(только для оксидов щелочных и щелочно-земельных металлов) (кроме SiO2).

Амфотерные оксиды, обладая свойствами и основных и кислотных оксидов, взаимодействуют с сильными кислотами и щелочами:

2. Окислительно - восстановительные свойства
Если элемент имеет переменную степень окисления (с. о.), то его оксиды с низкими с. о. могут проявлять восстановительные свойства, а оксиды с высокими с. о. - окислительные.
Примеры реакций, в которых оксиды выступают в роли восстановителей:
Окисление оксидов с низкими с. о. до оксидов с высокими с. о. элементов.
2C+2O + O2 = 2C+4O2
2S+4O2 + O2 = 2S+6O3
2N+2O + O2 = 2N+4O2
Оксид углерода (II) восстанавливает металлы из их оксидов и водород из воды.
C+2O + FeO = Fe + 2C+4O2
C+2O + h3O = h3 + 2C+4O2
Примеры реакций, в которых оксиды выступают в роли окислителей:
Восстановление оксидов с высокими с о. элементов до оксидов с низкими с. о. или до простых веществ.
C+4O2 + C = 2C+2O
2S+6O3 + h3S = 4S+4O2 + h3O
C+4O2 + Mg = C0 + 2MgO
Cr+32O3 + 2Al = 2Cr0 + 2Al2O3
Cu+2O + h3 = Cu0 + h3O
Использование оксидов малоактивных металлов дпя окисления органических веществ.

Некоторые оксиды, в которых элемент имеет промежуточную с. о., способны к диспропорционированию;
например:
2NO2 + 2NaOH = NaNO2 + NaNO3 + h3O
1. Взаимодействие простых веществ - металлов и неметаллов - с кислородом:
4Li + O2 = 2Li2O;
2Cu + O2 = 2CuO;
S + O2 = SO2
4P + 5O2 = 2P2O5
2. Дегидратация нерастворимых оснований, амфотерных гидроксидов и некоторых кислот:
Cu(OH)2 = CuO + h3O
2Al(OH)3 = Al2O3 + 3h3O
h3SO3 = SO2↑ + h3O
h3SiO3 = SiO2 + h3O
3. Разложение некоторых солей:
2Cu(NO3)2 = 2CuO + 4NO2↑ + O2↑
CaCO3 = CaO + CO2↑
(CuOH)2CO3 = 2CuO + CO2↑ + h3O
4. Окисление сложных веществ кислородом:
Ch5 + 2O2 = CO2 + h3O
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
4Nh4 + 5O2 = 4NO + 6h3O
5.Восстановление кислот-окислителей металлами и неметаллами:
Cu + h3SO4 (конц) = CuSO4 + SO2↑ + 2h3O
10HNO3 (конц) + 4Ca = 4Ca(NO3)2 + N2O↑ + 5h3O
2HNO3 (разб) + S = h3SO4 + 2NO↑
6. Взаимопревращения оксидов в ходе окислительно-восстановительных реакций (см. окислительно-восстановительные свойства оксидов).
examchemistry.com
| Гальванических цехов
Если в состав ванны входит несколько растворов различных веществ, то количество выделяющихся веществ рассчитывается как сумма веществ для всех растворов, согласно табл. 3.23. Например, при электрохимическом полировании используется ванна, содержащая растворы ортофосфорной кислоты концентрацией 500 – 1100 г/л, ангидрида хромового концентрацией 30 – 80 г/л и серной кислоты концентрацией 250 – 550 г/л. Процесс происходит при 60 – 80оС; плотность тока 15 – 80 А/дм2. В этом случае с поверхности ванны происходит выделение хромового ангидрида 7,2 г/(ч м2), ортофосфорной кислоты 18 г/(ч м2) и серной кислоты 25 г/(ч м2).
Таблица 3.23 Удельное количество загрязняющих веществ, выделяющихся с поверхности гальванических ванн при различных технологических процессах.
Таблица 3.24 Удельное выделение загрязняющих веществ при производстве Изделий из стеклопластиков
1,0
0,8
0,6
0,4
Рис. 3.1. Изменение относительного 0,2 содержания аэрозоля загрязняющего вещества в удаляемом воздухе при дви- жения по воздуховоду. 0 Борто-0 2 4 6 8 ф м вой от- Воздуховод сос 3.7. Производство изделий на стеклопластиках. Загрязняющие вещества, содержащиеся в используемом смолах и связующих веществах, при производстве изделий из стеклопластиков выделяются в основном в виде паров или пыли. Данные о выбросах загрязняющих веществ представлены в табл. 3.24.
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте: |
zdamsam.ru
Агрегатное состояние — Википедия РУ

Агрега́тное состоя́ние вещества (от лат. aggrego «присоединяю») — физическое состояние вещества, зависящее от соответствующего сочетания температуры и давления. Изменение агрегатного состояния может сопровождаться скачкообразным изменением свободной энергии, энтропии, плотности и других физических величин.[1]
Традиционно выделяют три агрегатных состояния: твёрдое тело, жидкость и газ. К агрегатным состояниям принято причислять также плазму[2], в которую переходят газы при повышении температуры и фиксированном давлении. Отличительной особенностью является отсутствие резкой границы перехода к плазменному состоянию. Существуют и другие агрегатные состояния.
Определения агрегатных состояний не всегда являются строгими. Так, существуют аморфные тела, сохраняющие структуру жидкости и обладающие небольшой текучестью и способностью сохранять форму; жидкие кристаллы текучи, но при этом обладают некоторыми свойствами твёрдых тел, в частности, могут поляризовать проходящее через них электромагнитное излучение.
Для описания различных состояний в физике используется более широкое понятие термодинамической фазы. Явления, описывающие переходы от одной фазы к другой, называют критическими явлениями.
Основным термодинамическим (феноменологическим) признаком различия видов агрегатного состояния вещества является наличие энергетической границы между фазами: теплота испарения как граница между жидкостью и её паром и теплота плавления как граница между твёрдым веществом и жидкостью[3].
Четыре основных состояния
Твёрдое тело
 Кристаллические вещества: атомное разрешение изображения титаната стронция. Яркие атомы — Sr, темнее их Ti.
Кристаллические вещества: атомное разрешение изображения титаната стронция. Яркие атомы — Sr, темнее их Ti. В твёрдом состоянии вещество сохраняет как форму, так и объём. При низких температурах все вещества замерзают — превращаются в твёрдые тела. Температура затвердевания может быть несколько повышена при увеличении давления. Твёрдые тела делятся на кристаллические и аморфные. С микроскопической точки зрения твёрдые тела характерны тем, что молекулы или атомы в них в течение длительного времени сохраняют своё среднее положение неизменным, только совершая колебания с небольшой амплитудой вокруг них. В кристаллах средние положения атомов или молекул строго упорядочены. Кристаллы характеризуются пространственной периодичностью в расположении равновесных положений атомов, которая достигается наличием дальнего порядка и носит название кристаллической решётки. Естественная форма кристаллов — правильные многогранники.
В аморфных телах атомы колеблются вокруг хаотически расположенных точек, у них отсутствует дальний порядок, но сохраняется ближний, при котором молекулы расположены согласованно на расстоянии, сравнимом с их размерами. Согласно классическим представлениям, устойчивым состоянием (с минимумом потенциальной энергии) твёрдого тела является кристаллическое. Частным случаем аморфного состояния является стеклообразное состояние. Аморфное тело находится в метастабильном состоянии и с течением времени должно перейти в кристаллическое состояние, однако время кристаллизации часто столь велико, что метастабильность вовсе не проявляется. Аморфное тело можно рассматривать как жидкость с очень большой (часто бесконечно большой) вязкостью. Кристаллические твёрдые тела имеют анизотропные свойства, то есть их отклик на приложенные внешние силы зависит от ориентации сил относительно кристаллографических осей. В твердотельном состоянии вещества могут иметь много фаз, которые отличаются составлением атомов или другими характеристиками, такими как упорядочение спинов в ферромагнетиках.
Жидкость
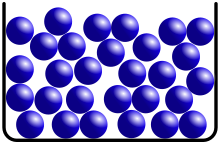 Структура классической одноатомной жидкости.
Структура классической одноатомной жидкости. В жидком состоянии вещество сохраняет объём, но не сохраняет форму. Это означает, что жидкость может занимать только часть объёма сосуда, но также может свободно перетекать по всей поверхности сосуда. Жидкое состояние обычно считают промежуточным между твёрдым телом и газом. Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана. Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает изменение формы (внутренних частей жидкого тела). Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии. Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твёрдое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления. Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза). Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей. Как и газ, жидкости тоже в основном изотропные. Однако, существуют жидкости с анизотропными свойствами — жидкие кристаллы. Кроме изотропной, так называемой нормальной фазы, эти вещества, мезогены, имеют одну или несколько упорядоченных термодинамических фаз, которые называют мезофазы. Составление в мезофазы происходит благодаря особой форме молекул жидких кристаллов. Обычно это длинные узкие молекулы, которым выгодно укладываться так, чтобы их оси совпадали.
Газ
Основная статья: Газ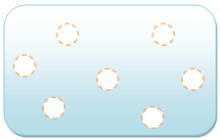 Промежутки между молекулами газа очень большие. Молекулы газа обладают очень слабыми связями. Молекулы в газе могут перемещаться свободно и быстро.
Промежутки между молекулами газа очень большие. Молекулы газа обладают очень слабыми связями. Молекулы в газе могут перемещаться свободно и быстро. Газообразное состояние характерно тем, что оно не сохраняет ни форму, ни объём. Газ заполняет всё доступное пространство и проникает в любые его закоулки. Это состояние, свойственное веществам с малой плотностью. Переход из жидкого в газообразное состояние называют испарением, а противоположный ему переход из газообразного состояния в жидкое — конденсацией. Переход из твёрдого состояния в газообразное, минуя жидкое, называют сублимацией или возгонкой. С микроскопической точки зрения газ — это состояние вещества, в котором его отдельные молекулы взаимодействуют слабо и движутся хаотически. Взаимодействие между ними сводится к спорадическим столкновениям. Кинетическая энергия молекул превышает потенциальную. Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма и не образуют свободной поверхности, а стремятся заполнить весь доступный объём (например, сосуда). По химическим свойствам газы и их смеси весьма разнообразны — от малоактивных инертных газов до взрывчатых газовых смесей. Понятие «газ» иногда распространяют не только на совокупности атомов и молекул, но и на совокупности других частиц — фотонов, электронов, броуновских частиц, а также плазму. Некоторые вещества не имеют газообразного состояния. Это вещества со сложным химическим строением, которые при повышении температуры распадаются вследствие химических реакций раньше, чем становятся газом. Не существует различных газообразных термодинамических фаз одного вещества. Газам свойственна изотропия, то есть независимость характеристик от направления. В привычных для человека земных условиях, газ имеет одинаковую плотность в любой точке, однако это не является универсальным законом, во внешних полях, например в поле тяготения Земли, или в условиях различных температур плотность газа может меняться от точки к точке. Газообразное состояние вещества в условиях, когда возможно существование устойчивой жидкой или твёрдой фазы этого же вещества, обычно называется паром.
Плазма
 Плазменная декоративная лампа.
Плазменная декоративная лампа. Четвёртым агрегатным состоянием вещества часто называют плазму. Плазма является частично или полностью ионизированным газом и в равновесном состоянии обычно возникает при высокой температуре, от нескольких тысяч К[1] и выше. В земных условиях плазма образуется в газовых разрядах. В общем, её свойства напоминают свойства газообразного состояния вещества, за исключением того факта, что для плазмы принципиальную роль играет электродинамика, то есть равноправной с ионами и электронами составляющей плазмы является электромагнитное поле.
Плазма — самое распространённое во Вселенной агрегатное состояние вещества. В этом состоянии находится вещество звёзд и вещество, наполняющее межпланетное, межзвёздное и межгалактическое пространство. Бо́льшая часть барионного вещества (по массе около 99,9 %) во Вселенной находится в состоянии плазмы.[4].
Фазовый переход
Низкотемпературные состояния
Сверхтекучесть
Способность вещества в особом состоянии (квантовой жидкости), возникающем при понижении температуры к абсолютному нулю (термодинамическая фаза), протекать через узкие щели и капилляры без трения. До недавнего времени сверхтекучесть была известна только у жидкого гелия, однако в последние годы сверхтекучесть была обнаружена и в других системах: в разреженных атомных бозе-конденсатах, твёрдом гелии.
Сверхтекучесть объясняется следующим образом. Поскольку атомы гелия являются бозонами, квантовая механика допускает нахождение в одном состоянии произвольного числа частиц. Вблизи абсолютного нуля температур все атомы гелия оказываются в основном энергетическом состоянии. Поскольку энергия состояний дискретна, атом может получить не любую энергию, а только такую, которая равна энергетическому зазору между соседними уровнями энергии. Но при низкой температуре энергия столкновений может оказаться меньше этой величины, в результате чего рассеяния энергии попросту не будет происходить. Жидкость будет течь без трения.
Конденсат Бозе — Эйнштейна
Получается в результате охлаждения бозе-газа до температур, близких к абсолютному нулю. В таком сильно охлаждённом состоянии достаточно большое число атомов оказывается в своих минимально возможных квантовых состояниях и квантовые эффекты начинают проявляться на макроскопическом уровне. Конденсат Бозе — Эйнштейна проявляет ряд квантовых свойств, таких как сверхтекучесть и резонанс Фешбаха[en].
Фермионный конденсат
Представляет собой Бозе-конденсацию в режиме БКШ «атомных куперовских пар» в газах состоящих из атомов-фермионов. (В отличие от традиционного режима бозе-эйнштейновской конденсации составных бозонов).
Такие фермионные атомные конденсаты являются «родственниками» сверхпроводников, но с критической температурой порядка комнатной и выше. [5]
Вырожденный газ
Газ, на свойства которого существенно влияют квантовомеханические эффекты, возникающие вследствие тождественности его частиц. Вырождение наступает в условиях, когда расстояния между частицами газа становятся соизмеримыми с длиной волны де Бройля; в зависимости от спина частиц выделяются два типа вырожденных газов — ферми-газ, образованный фермионами (частицами с полуцелым спином) и бозе-газ, образованный бозонами (частицами с целым спином).
Сверхтекучее твёрдое тело
Термодинамическая фаза квантовой жидкости, представляющей собой твёрдое тело со свойствами сверхтекучей жидкости.
Высокоэнергетические состояния
Глазма
Состояние адронного поля[6], предшествующее при столкновениях кварк-глюонной плазме. Состоит из цветных токовых трубок.[7] Глазма является особенностью теоретической модели «конденсата цветового стекла» (англ. color glass condensate) — подхода к описанию сильного взаимодействия в условиях высоких плотностей[8].
Глазма образуется при столкновении адронов друг с другом (например, протонов с протонами, ионов с ионами, ионов с протонами). Считается также, что в эволюции Вселенной состояние глазмы предшествовало кварк-глюонной плазме, которая существовала в первые миллионные доли секунды сразу после Большого взрыва. Время существования глазмы — несколько иоктосекунд[9].
Кварк-глюонная плазма
Состояние вещества в физике высоких энергий и физике элементарных частиц, при котором адронное вещество переходит в состояние, аналогичное состоянию, в котором находятся электроны и ионы в обычной плазме. Ему предшествует состояние глазмы[10] (глазма термализуется, то есть разрушается, порождая множество хаотично движущихся кварков, антикварков и глюонов: кварк-глюонную плазму[11]).
Состояния при большом давлении
Нейтронное состояние
Принципиально отличное от других состояние вещества, состоящее только из нейтронов. В нейтронное состояние вещество переходит при сверхвысоком давлении, недоступном пока в лаборатории, но которое существует внутри нейтронных звезд. При переходе в нейтронное состояние, электроны вещества объединяются с протонами и превращаются в нейтроны. Для этого необходимо, чтобы силы гравитации сжали вещество настолько, чтобы преодолеть отталкивание электронов, обусловленное принципом Паули. В результате, в нейтронном состоянии, вещество полностью состоит из нейтронов и имеет плотность порядка ядерной. Температура вещества при этом не должна быть очень высокой (в энергетическом эквиваленте, в пределах от сотни МэВ).
Другие состояния
Тёмная материя
Форма материи, которая не испускает электромагнитного излучения и не взаимодействует с ним. Это свойство данной формы вещества делает невозможным её прямое наблюдение. Однако возможно обнаружить присутствие тёмной материи по создаваемым ею гравитационным эффектам.
Обнаружение природы тёмной материи поможет решить проблему скрытой массы, которая, в частности, заключается в аномально высокой скорости вращения внешних областей галактик.
Сверхкритический флюид
Состояние вещества, при котором исчезает различие между жидкой и газовой фазой. Любое вещество, находящееся при температуре и давлении выше критической точки, является сверхкритической жидкостью. Свойства вещества в сверхкритическом состоянии промежуточные между его свойствами в газовой и жидкой фазе. Так, СКФ обладает высокой плотностью, близкой к жидкости, низкой вязкостью и при отсутствии межфазных границ поверхностное натяжение также исчезает. Коэффициент диффузии при этом имеет промежуточное между жидкостью и газом значение. Вещества в сверхкритическом состоянии могут применяться в качестве заменителей органических растворителей в лабораторных и промышленных процессах. Наибольший интерес и распространение в связи с определёнными свойствами получили сверхкритическая вода и сверхкритический диоксид углерода.
Вырожденная материя
- Ферми-газ 1-я стадия Электронно-вырожденный газ, наблюдается в белых карликах, играет важную роль в эволюции звёзд.
- 2-я стадия нейтронное состояние в него вещество переходит при сверхвысоком давлении, недостижимом пока в лаборатории, но существующем внутри нейтронных звёзд. При переходе в нейтронное состояние электроны вещества взаимодействуют с протонами и превращаются в нейтроны. В результате вещество в нейтронном состоянии полностью состоит из нейтронов и обладает плотностью порядка ядерной. Температура вещества при этом не должна быть слишком высока (в энергетическом эквиваленте не более сотни МэВ).
- при сильном повышении температуры (сотни МэВ и выше) в нейтронном состоянии начинают рождаться и аннигилировать разнообразные мезоны. При дальнейшем повышении температуры происходит деконфайнмент, и вещество переходит в состояние кварк-глюонной плазмы. Оно состоит уже не из адронов, а из постоянно рождающихся и исчезающих кварков и глюонов. Возможно[12], деконфайнмент происходит в два этапа.
- При дальнейшем неограниченном повышении давления без повышения температуры вещество коллапсирует в чёрную дыру.
- При одновременном повышении и давления, и температуры к кваркам и глюонам добавляются иные частицы. Что происходит с веществом, пространством и временем при температурах, близких к планковской, пока неизвестно.
См. также
Примечания
Литература
- Шульц М. М., Мазурин О. В. Современное представление о строении стёкол и их свойствах. — Л.: Наука. 1988 ISBN 5-02-024564-X
http-wikipediya.ru
Алюминий, Вступление | |
| Символ | Al |
| Латинское название | Aluminum |
| Тип вещества | простой химический элемент |
| Первооткрыватель | Х.К. Эрстед |
| Год открытия | 1825 |
Основные параметры алюминия по таблице Менделеева | |
| Атомный номер Z | 13 |
| Атомная масса | 26.981538 |
| Группа | 13 |
| Период | 3 |
| Принадлежность к группе | другие металлы |
Механические свойства алюминия | |
| Плотность твердых веществ | 2.710 · 103 (Килограмм / Метр3) |
| Модуль упругости твердого тела | 7.1 · 1010 (Ньютон / Метр2) |
| Модуль сдвига | 2.6 · 1010 (Ньютон / Метр2) |
| Скорость звука | 5100 (Метр / Секунда) |
Термодинамические свойства алюминия | |
| Агрегатное состояние при нормальных условиях | твердое тело |
| Точка плавления по Кельвину | 933.47 (Кельвин) |
| Точка плавления по Цельсию | 660.32 (°C) |
| Точка кипения по Кельвину | 2792.15 (Кельвин) |
| Точка кипения по Цельсию | 2519 (°C) |
| Коэффициент линейного теплового расширения твердых тел в интервале температур (0..100°C) | 23.8 · 10 − 6 (1 / Кельвин) |
Электрические свойства алюминия | |
| Тип электрической проводимости | проводник |
| Удельное электрическое сопротивление проводников (при 20°C) | 2.700 · 10 − 8 (Ом · Метр) |
| Температурный коэффициент сопротивления (при 20°C) | 4.30 · 10 − 3 (1 / Кельвин) |
Магнитные свойства алюминия | |
| Тип магнитной проницаемости | парамагнетик |
Свойства атома алюминия | |
| Конфигурация электронного облака | 1s2 | 2s22p63s23p1 |
| Радиус атома | 118 · 10 − 12 (Метр) |
| Число протонов p | 13 |
| Число нейтронов n | 14 |
| Число электронов e | 13 |
| Массовое число A | 27 |
| Атомная структура алюминия | 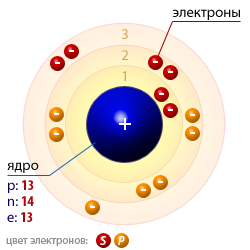 |
Химические свойства алюминия | |
| Валентность | 3 |
Распространенность алюминия | |
| Вселенная состоит из алюминия на | 0.005% |
| Солнце состоит из алюминия на | 0.006% |
| Мировой океан состоит из алюминия на | 5×10-7% |
| Человеческое тело состоит из алюминия на | 0.00009% |
Вселенная | |
| Вселенная состоит из алюминия на | 0.005% |
www.fxyz.ru
7.9 Виды веществ и их агрегатное состояние
С точки зрения физики различные системы, состоящие из огромного количества частиц, образуют макроскопические тела (или макротела).Макротела могут перемещаться относительно друг друга по законам динамики. С другой стороны – макротела обладают свойствами, обусловленными их микроскопическим строением, хаотическим движением микрочастиц.
Свойства макрочастиц характеризуются: плотностью вещества, давлением, температурой, химической структурой, радиоактивностью.
Плотность вещества – это количество вещества, приходящееся в среднем на единицу объема тела, т.е.
= m/v, [кг/м3], где m – масса, кг; v – объем, м3
Плотности известных в настоящее время веществ находятся в очень широком диапазоне – от 1017кг/м3(плотности атомных ядер) до
10 –26 кг/м3(плотности газов межгалактического пространства). Вместе с тем, плотности жидкостей и твердых тел независимо от степени сжатия лежат в достаточно узком диапазоне. Это объясняется плотной “упаковкой” частиц жидкостей и твердых тел в отличие от газов. Самый ковкий металл – золото (из 1 г – проволока 2,4 км), самый тугоплавкий – вольфрам (3420оС), самый твердый – хром, самый тепло-и электропроводный – серебро.
Давление – это сила, действующая со стороны газа или жидкости на единицу поверхности: т.е.

где F – сила, H ; S – площадь поверхности, м2
Силы, действующие внутри твердых тел, характеризуются механическим напряжением (?). Давление и механическое напряжение в системе СИ измеряется в Паскалях (1Па = 1Н/м2)
Температура – это степень нагретости тела.
Она характеризует интенсивность теплового движения частиц тела.
Чем больше скорость движения частиц тела, тем больше скорость движения тела, тем выше его температура. Абсолютная температура пропорциональна средней кинетической энергии поступательного движения частиц, т.е.
3/2kТ = mv2/2 ,
где v – скорость движения частиц:
k = 1,38 10-23Дж/К – постоянная Больцмана.
При изменении температуры изменяются некоторые физические свойства тел: объём, электрическое сопротивление, интенсивность излучения, вязкость и др. Например, при температуре жидкого гелия многие металлы и сплавы становятся сверхпроводниками, т.е. у них исчезает электрическое сопротивление. Изменяются и другие физические характеристики: свинец становится твердым, как сталь, а резина – хрупкой как стекло.
За единицу измерения температуры принят градус. Наряду со стоградусной шкалой (шкала Цельсия) применяется также шкалаабсолютных температур,ноль которой лежит на 273о(округленно) ниже температуры точки плавления льда.
Величина абсолютной температуры Т = t +273, где t – температура в оС.
Понятие химической структуры было рассмотрено в п.6.8, а радиоактивность - в п.6.5.
С позиций физики, вещество - это вид материи, обладающий массой покоя. Физика различает: аморфное вещество- твердое вещество, не обладающее упорядоченным строением;
кристаллическое вещество- твердое вещество, имеющее периодическое расположение составляющих его частиц;
оптически активное вещество- вещество способное вызывать поворот плоскости поляризации проходящего через него света;
поверхностно-активное вещество- вещество, способное адсорбироваться на поверхности раздела фаз и понижать их поверхностную энергию;
радиоактивное вещество - вещество, в котором осуществляется радиоактивный распад, т.е. когда вещество самопроизвольно испускает частицы.
Таким образом, физика рассматривает неорганические вещества в четырех агрегатных состояниях: газообразном, жидком, твердом и плазменном.
Химия рассматривает вещество через понятия химического элемента и соединения. Взаимосвязь, закономерности и свойства элементов отражает периодическая система химических элементов Д.И. Менделеева.
Биология имеет дело с живыми веществами, т.е. с совокупностью тел живых организмов, населяющих землю.
При изучении живых организмов биология рассматривает биогенные, биокостные, межклеточные, физиологически активные вещества.
Биогены (от греч. биос-жизнь, генос-рождающийся) - вещества, в том числе химические элементы, абсолютно необходимые для существования живых организмов и обязательно входящие в их состав.
Биокостные вещества- вещества, создающиеся одновременно живыми организмами и костными процессами и являющиеся по формулировке акад. В.И. Вернадского "закономерной структурой из живого и костного вещества". Вещество биокостное особенно характерно для почвы; фактически все поверхностные слои Земли (осадочные породы) - результат преобразования вещества биокостного.
Межклеточное вещество- бесструктурная аморфная масса, состоящая из тончайших нитевидных структур (фибрилл), особенно хорошо развитое в соединительных тканях и определяющее их структуру.
Вещество физиологически активное - любое вещество, вырабатываемое организмом и получаемое извне и оказывающее либо стимулирующее, либо подавляющее воздействие на происходящие в организме процессы (биогены, гормоны, ингибиторы, ферменты и др.)
Например, если бы железо, подобно золоту и серебру не ржавело, т.е. не окислялось, то мы бы не существовали, и ни одно растение на Земле не зеленело. Та же "ржавчина" снабжает железом нашу кровь и придает ей красный цвет. Самый "живой" металл - кальций. В организме взрослого человека его около 1,5 кГ. Зубная эмаль - это соединение фосфора.
Щитовидная железа содержит поразительно много йода и вырабатывает йодосодержащие гормоны. Много йода содержит лук, яйца, молоко, морская рыба, морская капуста.
Итак, все окружающее пространство заполнено физическими телами, которые образованы различными веществами. Вещества могут находиться в твердом, жидком, газообразном и плазменном состоянии в зависимости от температуры и давления. Вещества образуются из химических элементов.
studfiles.net
Агрегатное состояние — WiKi

Агрега́тное состоя́ние вещества (от лат. aggrego «присоединяю») — физическое состояние вещества, зависящее от соответствующего сочетания температуры и давления. Изменение агрегатного состояния может сопровождаться скачкообразным изменением свободной энергии, энтропии, плотности и других физических величин.[1]
Традиционно выделяют три агрегатных состояния: твёрдое тело, жидкость и газ. К агрегатным состояниям принято причислять также плазму[2], в которую переходят газы при повышении температуры и фиксированном давлении. Отличительной особенностью является отсутствие резкой границы перехода к плазменному состоянию. Существуют и другие агрегатные состояния.
Определения агрегатных состояний не всегда являются строгими. Так, существуют аморфные тела, сохраняющие структуру жидкости и обладающие небольшой текучестью и способностью сохранять форму; жидкие кристаллы текучи, но при этом обладают некоторыми свойствами твёрдых тел, в частности, могут поляризовать проходящее через них электромагнитное излучение.
Для описания различных состояний в физике используется более широкое понятие термодинамической фазы. Явления, описывающие переходы от одной фазы к другой, называют критическими явлениями.
Основным термодинамическим (феноменологическим) признаком различия видов агрегатного состояния вещества является наличие энергетической границы между фазами: теплота испарения как граница между жидкостью и её паром и теплота плавления как граница между твёрдым веществом и жидкостью[3].
Четыре основных состояния
Твёрдое тело
 Кристаллические вещества: атомное разрешение изображения титаната стронция. Яркие атомы — Sr, темнее их Ti.
Кристаллические вещества: атомное разрешение изображения титаната стронция. Яркие атомы — Sr, темнее их Ti. В твёрдом состоянии вещество сохраняет как форму, так и объём. При низких температурах все вещества замерзают — превращаются в твёрдые тела. Температура затвердевания может быть несколько повышена при увеличении давления. Твёрдые тела делятся на кристаллические и аморфные. С микроскопической точки зрения твёрдые тела характерны тем, что молекулы или атомы в них в течение длительного времени сохраняют своё среднее положение неизменным, только совершая колебания с небольшой амплитудой вокруг них. В кристаллах средние положения атомов или молекул строго упорядочены. Кристаллы характеризуются пространственной периодичностью в расположении равновесных положений атомов, которая достигается наличием дальнего порядка и носит название кристаллической решётки. Естественная форма кристаллов — правильные многогранники.
В аморфных телах атомы колеблются вокруг хаотически расположенных точек, у них отсутствует дальний порядок, но сохраняется ближний, при котором молекулы расположены согласованно на расстоянии, сравнимом с их размерами. Согласно классическим представлениям, устойчивым состоянием (с минимумом потенциальной энергии) твёрдого тела является кристаллическое. Частным случаем аморфного состояния является стеклообразное состояние. Аморфное тело находится в метастабильном состоянии и с течением времени должно перейти в кристаллическое состояние, однако время кристаллизации часто столь велико, что метастабильность вовсе не проявляется. Аморфное тело можно рассматривать как жидкость с очень большой (часто бесконечно большой) вязкостью. Кристаллические твёрдые тела имеют анизотропные свойства, то есть их отклик на приложенные внешние силы зависит от ориентации сил относительно кристаллографических осей. В твердотельном состоянии вещества могут иметь много фаз, которые отличаются составлением атомов или другими характеристиками, такими как упорядочение спинов в ферромагнетиках.
Жидкость
 Структура классической одноатомной жидкости.
Структура классической одноатомной жидкости. В жидком состоянии вещество сохраняет объём, но не сохраняет форму. Это означает, что жидкость может занимать только часть объёма сосуда, но также может свободно перетекать по всей поверхности сосуда. Жидкое состояние обычно считают промежуточным между твёрдым телом и газом. Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана. Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает изменение формы (внутренних частей жидкого тела). Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии. Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твёрдое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления. Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза). Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей. Как и газ, жидкости тоже в основном изотропные. Однако, существуют жидкости с анизотропными свойствами — жидкие кристаллы. Кроме изотропной, так называемой нормальной фазы, эти вещества, мезогены, имеют одну или несколько упорядоченных термодинамических фаз, которые называют мезофазы. Составление в мезофазы происходит благодаря особой форме молекул жидких кристаллов. Обычно это длинные узкие молекулы, которым выгодно укладываться так, чтобы их оси совпадали.
Газ
Основная статья: Газ Промежутки между молекулами газа очень большие. Молекулы газа обладают очень слабыми связями. Молекулы в газе могут перемещаться свободно и быстро.
Промежутки между молекулами газа очень большие. Молекулы газа обладают очень слабыми связями. Молекулы в газе могут перемещаться свободно и быстро. Газообразное состояние характерно тем, что оно не сохраняет ни форму, ни объём. Газ заполняет всё доступное пространство и проникает в любые его закоулки. Это состояние, свойственное веществам с малой плотностью. Переход из жидкого в газообразное состояние называют испарением, а противоположный ему переход из газообразного состояния в жидкое — конденсацией. Переход из твёрдого состояния в газообразное, минуя жидкое, называют сублимацией или возгонкой. С микроскопической точки зрения газ — это состояние вещества, в котором его отдельные молекулы взаимодействуют слабо и движутся хаотически. Взаимодействие между ними сводится к спорадическим столкновениям. Кинетическая энергия молекул превышает потенциальную. Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма и не образуют свободной поверхности, а стремятся заполнить весь доступный объём (например, сосуда). По химическим свойствам газы и их смеси весьма разнообразны — от малоактивных инертных газов до взрывчатых газовых смесей. Понятие «газ» иногда распространяют не только на совокупности атомов и молекул, но и на совокупности других частиц — фотонов, электронов, броуновских частиц, а также плазму. Некоторые вещества не имеют газообразного состояния. Это вещества со сложным химическим строением, которые при повышении температуры распадаются вследствие химических реакций раньше, чем становятся газом. Не существует различных газообразных термодинамических фаз одного вещества. Газам свойственна изотропия, то есть независимость характеристик от направления. В привычных для человека земных условиях, газ имеет одинаковую плотность в любой точке, однако это не является универсальным законом, во внешних полях, например в поле тяготения Земли, или в условиях различных температур плотность газа может меняться от точки к точке. Газообразное состояние вещества в условиях, когда возможно существование устойчивой жидкой или твёрдой фазы этого же вещества, обычно называется паром.
Плазма
 Плазменная декоративная лампа.
Плазменная декоративная лампа. Четвёртым агрегатным состоянием вещества часто называют плазму. Плазма является частично или полностью ионизированным газом и в равновесном состоянии обычно возникает при высокой температуре, от нескольких тысяч К[1] и выше. В земных условиях плазма образуется в газовых разрядах. В общем, её свойства напоминают свойства газообразного состояния вещества, за исключением того факта, что для плазмы принципиальную роль играет электродинамика, то есть равноправной с ионами и электронами составляющей плазмы является электромагнитное поле.
Плазма — самое распространённое во Вселенной агрегатное состояние вещества. В этом состоянии находится вещество звёзд и вещество, наполняющее межпланетное, межзвёздное и межгалактическое пространство. Бо́льшая часть барионного вещества (по массе около 99,9 %) во Вселенной находится в состоянии плазмы.[4].
Фазовый переход
Низкотемпературные состояния
Сверхтекучесть
Способность вещества в особом состоянии (квантовой жидкости), возникающем при понижении температуры к абсолютному нулю (термодинамическая фаза), протекать через узкие щели и капилляры без трения. До недавнего времени сверхтекучесть была известна только у жидкого гелия, однако в последние годы сверхтекучесть была обнаружена и в других системах: в разреженных атомных бозе-конденсатах, твёрдом гелии.
Сверхтекучесть объясняется следующим образом. Поскольку атомы гелия являются бозонами, квантовая механика допускает нахождение в одном состоянии произвольного числа частиц. Вблизи абсолютного нуля температур все атомы гелия оказываются в основном энергетическом состоянии. Поскольку энергия состояний дискретна, атом может получить не любую энергию, а только такую, которая равна энергетическому зазору между соседними уровнями энергии. Но при низкой температуре энергия столкновений может оказаться меньше этой величины, в результате чего рассеяния энергии попросту не будет происходить. Жидкость будет течь без трения.
Конденсат Бозе — Эйнштейна
Получается в результате охлаждения бозе-газа до температур, близких к абсолютному нулю. В таком сильно охлаждённом состоянии достаточно большое число атомов оказывается в своих минимально возможных квантовых состояниях и квантовые эффекты начинают проявляться на макроскопическом уровне. Конденсат Бозе — Эйнштейна проявляет ряд квантовых свойств, таких как сверхтекучесть и резонанс Фешбаха[en].
Фермионный конденсат
Представляет собой Бозе-конденсацию в режиме БКШ «атомных куперовских пар» в газах состоящих из атомов-фермионов. (В отличие от традиционного режима бозе-эйнштейновской конденсации составных бозонов).
Такие фермионные атомные конденсаты являются «родственниками» сверхпроводников, но с критической температурой порядка комнатной и выше. [5]
Вырожденный газ
Газ, на свойства которого существенно влияют квантовомеханические эффекты, возникающие вследствие тождественности его частиц. Вырождение наступает в условиях, когда расстояния между частицами газа становятся соизмеримыми с длиной волны де Бройля; в зависимости от спина частиц выделяются два типа вырожденных газов — ферми-газ, образованный фермионами (частицами с полуцелым спином) и бозе-газ, образованный бозонами (частицами с целым спином).
Сверхтекучее твёрдое тело
Термодинамическая фаза квантовой жидкости, представляющей собой твёрдое тело со свойствами сверхтекучей жидкости.
Высокоэнергетические состояния
Глазма
Состояние адронного поля[6], предшествующее при столкновениях кварк-глюонной плазме. Состоит из цветных токовых трубок.[7] Глазма является особенностью теоретической модели «конденсата цветового стекла» (англ. color glass condensate) — подхода к описанию сильного взаимодействия в условиях высоких плотностей[8].
Глазма образуется при столкновении адронов друг с другом (например, протонов с протонами, ионов с ионами, ионов с протонами). Считается также, что в эволюции Вселенной состояние глазмы предшествовало кварк-глюонной плазме, которая существовала в первые миллионные доли секунды сразу после Большого взрыва. Время существования глазмы — несколько иоктосекунд[9].
Кварк-глюонная плазма
Состояние вещества в физике высоких энергий и физике элементарных частиц, при котором адронное вещество переходит в состояние, аналогичное состоянию, в котором находятся электроны и ионы в обычной плазме. Ему предшествует состояние глазмы[10] (глазма термализуется, то есть разрушается, порождая множество хаотично движущихся кварков, антикварков и глюонов: кварк-глюонную плазму[11]).
Состояния при большом давлении
Нейтронное состояние
Принципиально отличное от других состояние вещества, состоящее только из нейтронов. В нейтронное состояние вещество переходит при сверхвысоком давлении, недоступном пока в лаборатории, но которое существует внутри нейтронных звезд. При переходе в нейтронное состояние, электроны вещества объединяются с протонами и превращаются в нейтроны. Для этого необходимо, чтобы силы гравитации сжали вещество настолько, чтобы преодолеть отталкивание электронов, обусловленное принципом Паули. В результате, в нейтронном состоянии, вещество полностью состоит из нейтронов и имеет плотность порядка ядерной. Температура вещества при этом не должна быть очень высокой (в энергетическом эквиваленте, в пределах от сотни МэВ).
Другие состояния
Тёмная материя
Форма материи, которая не испускает электромагнитного излучения и не взаимодействует с ним. Это свойство данной формы вещества делает невозможным её прямое наблюдение. Однако возможно обнаружить присутствие тёмной материи по создаваемым ею гравитационным эффектам.
Обнаружение природы тёмной материи поможет решить проблему скрытой массы, которая, в частности, заключается в аномально высокой скорости вращения внешних областей галактик.
Сверхкритический флюид
Состояние вещества, при котором исчезает различие между жидкой и газовой фазой. Любое вещество, находящееся при температуре и давлении выше критической точки, является сверхкритической жидкостью. Свойства вещества в сверхкритическом состоянии промежуточные между его свойствами в газовой и жидкой фазе. Так, СКФ обладает высокой плотностью, близкой к жидкости, низкой вязкостью и при отсутствии межфазных границ поверхностное натяжение также исчезает. Коэффициент диффузии при этом имеет промежуточное между жидкостью и газом значение. Вещества в сверхкритическом состоянии могут применяться в качестве заменителей органических растворителей в лабораторных и промышленных процессах. Наибольший интерес и распространение в связи с определёнными свойствами получили сверхкритическая вода и сверхкритический диоксид углерода.
Вырожденная материя
- Ферми-газ 1-я стадия Электронно-вырожденный газ, наблюдается в белых карликах, играет важную роль в эволюции звёзд.
- 2-я стадия нейтронное состояние в него вещество переходит при сверхвысоком давлении, недостижимом пока в лаборатории, но существующем внутри нейтронных звёзд. При переходе в нейтронное состояние электроны вещества взаимодействуют с протонами и превращаются в нейтроны. В результате вещество в нейтронном состоянии полностью состоит из нейтронов и обладает плотностью порядка ядерной. Температура вещества при этом не должна быть слишком высока (в энергетическом эквиваленте не более сотни МэВ).
- при сильном повышении температуры (сотни МэВ и выше) в нейтронном состоянии начинают рождаться и аннигилировать разнообразные мезоны. При дальнейшем повышении температуры происходит деконфайнмент, и вещество переходит в состояние кварк-глюонной плазмы. Оно состоит уже не из адронов, а из постоянно рождающихся и исчезающих кварков и глюонов. Возможно[12], деконфайнмент происходит в два этапа.
- При дальнейшем неограниченном повышении давления без повышения температуры вещество коллапсирует в чёрную дыру.
- При одновременном повышении и давления, и температуры к кваркам и глюонам добавляются иные частицы. Что происходит с веществом, пространством и временем при температурах, близких к планковской, пока неизвестно.
См. также
Примечания
Литература
- Шульц М. М., Мазурин О. В. Современное представление о строении стёкол и их свойствах. — Л.: Наука. 1988 ISBN 5-02-024564-X
ru-wiki.org





 Кв
Кв