Никель - это что такое? Свойства никеля. Никель медь никель хром
Никель, хим. состав и применение никелевых и медно-никелевых сплавов
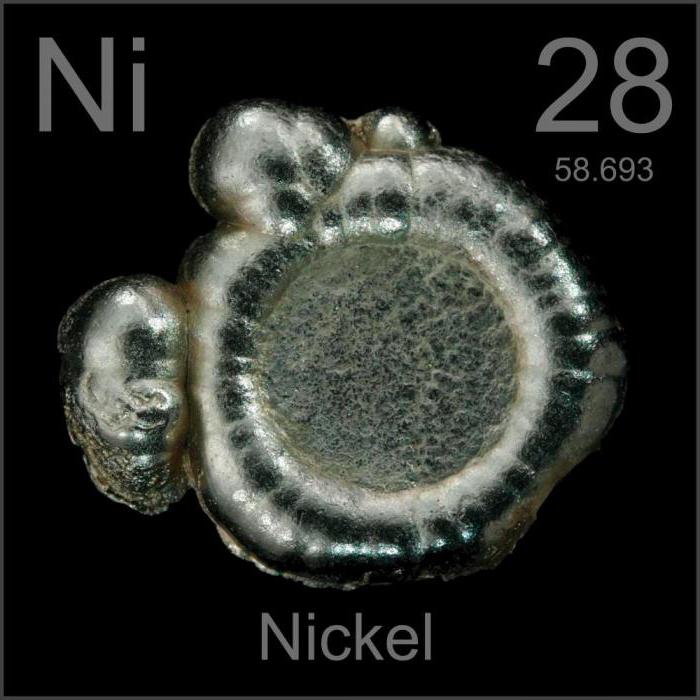
Никель — высокопрочный пластичный металл серебристо-белого цвета. Был открыт в 1751 году шведским химиком Акселем Кронстедтом. В периодической системе Д. И. Менделеева имеет номер 28 и символ Ni, атомная масса равна 58,71.
Никель — твердый и вязкий металл с ферромагнитными свойствами. Он хорошо поддается сварке, ковке, штамповке и прокатке. Отличается устойчивостью в химически активных средах, в том числе в щелочах. В атмосферных условиях покрывается защитной оксидной пленкой и не окисляется даже при температуре 800 ⁰С.
Физические свойства никеля:
- Температура плавления — 1455 ⁰С.
- Скрытая теплота плавления — 73 кал/г.
- Температура кипения — 2913 ⁰С.
- Скрытая теплота испарения — 1450 кал/г.
- Плотность — 8800 кг/м3.
- Предел прочности при растяжении отожженного никеля — 4000−5000 МПа.
- Предел прочности при растяжении деформированного никеля — 7500−9000 МПа.
- Предел текучести отожженного никеля — кГ/мм2.
- Предел текучести деформированного никеля — 70 кГ/мм2.
- Теплопроводность — 90,9 Вт/(м*К).
- Удельное электросопротивление — 0,0684 мкОм*м.
- Модуль упругости — 196−210 ГПа.
- Модуль нормальной упругости — 20000 кГ/мм2.
- Модуль сдвига — 7300 кГ/мм2.
- Твердость литого никеля — 60−70 кГ/мм2.
- Твердость отожженного никеля 70−90 кГ/мм2.
- Твердость деформированного никеля — 200 кГ/мм2.
Благодаря своим свойствам никель в чистом виде и особенно в сплавах широко применяется в различных областях промышленности. Металл образует твердые растворы со многими элементами.
Марки и химический состав никеля
Согласно ГОСТ 849-2008, выпускается 7 марок никеля — Н0, Н1Ау, Н1у, Н1, Н2, Н3 и Н4. В их составе содержится от 97,6 до 99,99 % никеля в сумме с небольшим процентом кобальта (Co) — от 0,005 до 0,7 %. Остальную массу занимают примеси:
- Углерод (C) — есть во всех марках никеля.
- Магний (Mg).
- Алюминий (Al).
- Кремний (Si).
- Фосфор (P).
- Сера (S) — есть во всех марках.
- Марганец (Mn).
- Железо (Fe).
- Медь (Cu) — есть во всех марках.
- Цинк (Zn).
- Мышьяк (As)
- Кадмий Cd).
- Олово (Sn).
- Сурьма (Sb).
- Свинец (Pb).
- Висмут (Bi).

Подробный химический состав никеля разных марок представлен в таблице ниже.
| Марка | Химический состав, % | |||||||||||||||||
| Ni и co, не менее | В том числе Co, не более | Примеси, не более | ||||||||||||||||
| C | Mg | Al | Si | P | S | Mn | Fe | Cu | As | Cd | Sn | Sb | Pb | Bi | ||||
| H0 | 99,99 | 0,005 | 0,005 | 0,001 | 0,001 | 0,001 | 0,001 | 0,001 | 0,001 | 0,002 | 0,001 | 0,0005 | 0,0005 | 0,0003 | 0,0003 | 0,0003 | 0,0003 | 0,0001 |
| h2Ay | 99,95 | 0,1 | 0,001 | 0,001 | — | 0,002 | 0,001 | 0,001 | — | 0,01 | 0,1 | 0,001 | 0,001 | 0,0006 | 0,0005 | 0,0005 | 0,0005 | 0,0001 |
| h2y | 99,95 | 0,1 | 0,01 | 0,001 | — | 0,002 | 0,001 | 0,001 | — | 0,01 | 0,015 | 0,001 | 0,001 | 0,0005 | 0,0005 | 0,0005 | 0,0005 | 0,0003 |
| h2 | 99,93 | 0,1 | 0,01 | 0,001 | — | 0,002 | 0,001 | 0,001 | — | 0,02 | 0,02 | 0,001 | 0,001 | 0,001 | 0,001 | 0,0001 | 0,001 | 0,0006 |
| h3 | 99,8 | 0,15 | 0,02 | — | — | 0,002 | — | 0,003 | — | 0,04 | 0,04 | 0,005 | — | — | — | 0,1 | — | |
| h4 | 98,6 | 0,7 | 0,1 | — | — | — | — | 0,03 | — | — | 0,6 | — | — | — | — | — | — | |
| h5 | 97,6 | 0,7 | 0,15 | — | — | — | — | 0,04 | — | — | 1,0 | — | — | — | — | — | — | |
Влияние примесей на свойства металла
Сера является одной из наиболее вредных примесей. Она придает никелю краcноломкость, из-за которой ухудшаются свойства металла при обработке давлением. Чтобы нейтрализовать действие серы, добавляют марганец и/или магний.
Углерод в количестве до 0,1 % никак не влияет на свойства металла, однако при большем содержании этого элемента он выпадает из твердого раствора при отжиге и снижает пластичность холодного никеля.
При содержании висмута и свинца в количестве от 0,002 % становится невозможной горячая обработка металла: так как эти элементы почти не растворяютися в твердом состоянии, из-за них разрушается слиток. Поэтому во всех марках никеля количество свинца и висмута ограничено 0,001 и 0,0006 % соответственно.
Алюминий увеличивает электросопротивление никеля. Данный элемент содержится в самой чистой марке — Н0. Кроме того, широко применяются сплавы никеля и алюминия: у них высокая жаропрочность и устойчивость к коррозии.
Железо не оказывает ощутимого влияния на свойства никеля. Кремний раскисляет основной металл, благодаря чему благоприятно влияет на его литейные свойства, химическую стойкость и прочность.
Кобальт повышает жаростойкость, жаропрочность и прочность никеля, а марганец оказывает положительные влияние на технологические и механические свойства металла, улучшает его электросопротивление.
Применение никеля в чистом виде
Для защиты металлов от коррозии
Для этого используются покрытия, которые наносятся гальванопластикой или плакированием. Первый способ применяют для алюминия, чугуна, магния и цинка, второй — для нелегированных сталей и железа.
Для производства металлических изделий, которые имеют постоянные формы и высокую коррозионную устойчивость
Никель в чистом виде стоит дороже, чем железо и сталь, поэтому используется в тех случаях, когда невозможно обойтись другим металлом с никелевым покрытием. Из никеля производят тигли и котлы, цистерны для перевозки и плавления щелочей, хранения реагентов, пищевых продуктов и др. В никелевых трубах изготавливают конденсаты. Инструменты их этого металла устойчивы при взаимодействии с агрессивными элементами, поэтому они практически незаменимы в химических лабораториях и медицинских центрах. Различные приборы из никеля применяются для телевидения, радиолокации и атомной техники.

В качестве катализаторов и фильтров в химической промышленности
Никель обладает такими же каталитическими свойствами, что и палладий, но стоит значительно меньше, поэтому широко используется в виде порошка в реакциях гидрирования спиртов, непредельных и ароматических углеводородов, циклических альдегидов.
Порошок чистого никеля также подходит для создания пористых фильтров, которые используются для фильтрования различных продуктов: топлива, газов и др.
Для механических прерывателей нейтронного пучка.
Свойства никеля позволяют получать нейтронные импульсы с большой энергией, в результате чего пластины из этого металла применяются в ядерной физике.
Также никель используют при изготовлении электродов в щелочных аккумуляторах.
Никелевые сплавы
В сплавах никель (вместе с кобальтом) соединяется с алюминием, кремнием, марганцем, железом и хромом. Согласно ГОСТ 492-73, в них допускается не более 1,4 % примесей. В составе примесей содержится незначительная доля магния, свинца, серы, углерода, висмута, мышьяка, сурьмы, кадмия, олова. Отдельной группой выступают медно-никелевые сплавы.
Все сплавы никеля разделяются на четыре большие группы:
- Конструкционные. Особенность этих сплавов — высокие механические свойства и повышенная устойчивость к коррозии. К этой группе относятся прежде всего сплавы на медно-никелевой основе, такие как мельхиор, монель, нейзильбер. Они хорошо свариваются и поддаются обработке в холодном и горячем виде.
- Жаростойкие. Основными элементами этих сплавов являются никель и железо. Они отличаются высокой жаростойкостью и жаропрочностью, применяются преимущественно для производства электронагревательных приборов. Их также используют для изготовления малогабаритных тензорезисторов и потенциометрических обмоток.
- Термоэлектродные. Это сплавы с высоким удельным сопротивлением и большой электродвижущей силой. Их используют для производства компенсационных проводов, термопар, прецизионных приборов. К данной группе относятся некоторые никелевые (хромель, алюмель) и медно-никелевые (константан, копель, манганин) сплавы.
- Сплавы с особыми свойствами. В эту группу входят сплавы, которые находят особое применение благодаря своим уникальным свойствам. Инвар — сплав никеля и железа, который отличается повышенной упругостью. Он применяется для изготовления эталонов длины, мерных геодезических проволок, несущих конструкций лазеров, деталей часовых механизмов и др. Пермаллой — также сплав никеля и железа, обладающий высокой проницаемостью в магнитных полях. Его используют для производства магнитопроводов, деталей реле, сердечников трансформаторов и др.
Сплав с кремнием
Кремнистый никель НК 0,2 содержит 99,4 % никеля (с кобальтом), 0,15 - 0,25 % кремния и до 0,45 % примесей. Из этого сплава изготавливаются ленты и полосы, которые находят применения в электротехнике: из них делают детали приборов и устройств.
Сплавы никеля и марганца
Марганцевый никель выпускается четырех марок — НМц1, НМц2, НМц2,5 и НМц5. Из сплава НМц1 производят сетки управления ртутных выпрямителей. НМц2 находит применение в электронных лампах повышенной прочности, используется для держателей сеток и др. Проволока из сплавов НМц2,5 и НМц5 используется в свечах двигателей — автомобильных, авиационных и тракторных. НМц5 также применяется для радиоламп.
Алюмель
Алюмель (НМцАК 2-2-1) — сплав никеля, алюминия, марганца и кремния. Он содержит 1,60−2,40 % алюминия, 1,80−2,70 % марганца, 0,85−1,50 кремния, до 0,7 % примесей, остальная часть — никель с кобальтом (кобальта — до 1,2 %). Алюмель применяется для изготовления термопар, которые используются для измерения температуры в различных областях промышленности, системах автоматики, а также в медицине и научных исследованиях.
Хромели
Хромель Т (НХ 9,5) — сплав никеля и 9-10 % хрома с содержанием примесей в количестве не более 1,4 %. Из этого сплава изготавливают проволоку для термопар.
Хромель К (НХ 9) содержит 8,5−10 % хрома и до 1,4 % примесей. Проволока из данного сплава используется для компенсационных проводов.
В состав хромеля ТМ (НХМ 9,5) входит 9−10 % хрома, 0,1−0,6 % кремния и до 0,15 % примесей. Сплав используется для изготовления термопар.
Хромель КМ (НХМ 9) — это сплав никеля, 8,5−10 % хрома, 0,1−0,6 % кремния с содержанием не более 0,15 % примесей. Применяется для изготовления проволоки компенсационных проводов.
Медно-никелевые сплавы
Это сплавы на медной основе, при этом никель является в них основным легирующим элементом. Смешение никеля и меди гарантирует высокую прочность, электросопротивление и устойчивость к коррозии.
В качестве элементов медно-никелевых сплавов могут также выступать алюминий, железо, марганец, цинк, титан, свинец, кремний. Согласно ГОСТ 492-73, допускается не более 2 % примесей, для некоторых сплавов — не более 0,15 %. Наиболее распространенные медно-никелевые сплавы — это копель, константан, мельхиор, нейзильбер, куниаль, манганин, монель.
Копель
Копель (МНМц43-0,5) содержит 0,1−1 % марганца, 42,5−44 % никеля, до 0,6 % примесей, остальная масса приходится на медь. Сплав имеет большую термоэлектродвижущую силу, выпускается в виде проволоки, которая применяется для компенсационных проводов, а также для изготовления термопар.
Константан
Константан (МНМц40-1,5) — термостабильный сплав с высоким удельным электросопротивлением. Он состоит из 1-2 % марганца, 39-41 % никеля, примерно 59 % меди и не более 0,9 % примесей. Константан выпускается в виде проволоки, полос и лент. Используется для изготовления приборов высокого класса точности, реостатов и электронагревательных элементов, компенсационных проводов и термопар.
Мельхиор
Мельхиор (МНЖМц30-1-1) — конструкционный медно-никелевый сплав с содержанием 18-22 % никеля, примерно 80 % меди и не боле 0,6 % примесей. Некоторые разновидности мельхиора содержат железо и марганец. Он обладает высокой пластичностью и коррозионной стойкостью. Хорошо поддается обработке давлением в холодном и горячем виде — штампуется, режется, чеканится. Его легко паять и полировать. Мельхиор имеет серебристый оттенок, выпускается в виде труб, полос и ленты. Применяется для изготовления монет, недорогих ювелирных украшений и посуды. Из него делают трубные доски кондиционеров, конденсаторные трубы. Сплав также используется в приборостроении.
Нейзильбер
Название нейзильбер (МНЦ15-20) переводится с немецкого как «новое серебро». Такое название он получил из-за того, что напоминает драгоценный металл, но при этом он стоит намного дешевле. Из него делают столовые приборы, которые серебрятся после отливки. В промышленности нейзильбер применяется для производства паровой и водяной арматуры, медицинских инструментов и деталей точных приборов. Из него производят ордены и медали, ювелирные изделия, гитарные лады. Нейзильбер также используется для изготовления финифти и филиграни. Сплав содержит 18-22 % цинка, 13,5-16,5 % никеля, около 38 % меди и не более 0,9 % примесей. Выпускается в виде ленты, труб, полос, проволоки и прутков.
Куниаль
Куниаль — дисперсионно-твердеющий сплав меди, никеля и алюминия. Куниаль А (МНА13-3) содержит 2,3-3 % алюминия, 12-15 % никеля, около 80 % меди и не более 1,9% примесей. Куниаль Б (МНА6-1,5) — 1,2-1,8 % алюминия, 5,5-6,5 % никеля, около 90 % меди и не более 1,1 % примесей.
Куниаль А выпускается в виде прутков, применяется в машиностроении для изделий повышенной прочности. Из куниаля Б изготавливают полосы, которые используются в электротехнике для пружин и других изделий.
Манганин
Манганин (МНМц3-12) — термостабильный сплав, содержащий 11,5-13,5 % марганца, 2,5-3,5 % никеля, около 85 % меди и не более 0,9 % примесей. Он выпускается в виде листов и проволоки, находит применение в измерительной технике: из манганина делают шунты, катушки, добавочные сопротивления, магазины сопротивлений и др.
Монель
Монель (НМЖМц28-2,5-1,5) — сплав на основе никеля, который содержит 2-3 % железа, 1,2-1,8 % марганца, 27-29 % меди и не более 0,6 % примесей. Выпускается в виде лент, полос, листов и проволоки. Применяется в различных сферах промышленности: медицинской, химической, нефтяной, судо- и авиастроительной. Из него делают дрели, музыкальные инструменты, оправы для очков, различные антикоррозионные детали.
ferrolabs.ru
это что такое? Свойства никеля
Шел 1751 год. В маленькой Швеции благодаря ученому Акселю Фредерику Крондстедту появился элемент под номером 17. На тот момент было всего 12 известных металлов, плюс сера, фосфор, углерод и мышьяк. Они и приняли к себе в компанию новенького, название ему - никель.
Немного истории
За много лет до этого чудесного открытия горняки из Саксонии были знакомы с рудой, которую можно было принять за медную руду. Попытки извлечь из этого материала медь были тщетными. Почувствовав себя обманутыми, руду стали называть "купферникель" (по-русски - "медный дьявол").
Этой рудой заинтересовался эксперт по минералам Крондстедт. После долгих трудов получился новый металл, который и назвали никелем. Эстафету по исследованию перехватил Бергман. Он еще больше очистил металл и пришел к заключению, что данный элемент напоминает железо.

Физические свойства никеля
Никель входит в десятую группу элементов и находится в четвертом периоде таблицы Менделеева под атомным номером 28. Если в таблице вы уведете символ Ni, это и есть никель. Он имеет оттенок желтый, на серебристой основе. Даже на воздухе металл не становится блеклым. Твердый и достаточно вязкий. Хорошо поддается ковке, благодаря чему можно изготовить очень тонкие изделия. Прекрасно полируется. Никель можно притянуть с помощью магнита. Даже при температуре 340 градусов со знаком минус просматриваются магнитные особенности никеля. Никель - это металл, стойкий к коррозии. Он проявляет слабую химическую активность. Что можно сказать про химические свойства никеля?
Химические свойства
Что необходимо для определения качественного состава никеля? Здесь следует перечислить из каких атомов (а именно их количества) состоит наш металл. Молярная масса (ее еще называют атомной массой) равна 58,6934 (г/моль). С измерениями продвинулись дальше. Радиус атома нашего металла 124 пм. При измерении радиуса иона, результат показал (+2е) 69 пм, а число 115 пм – это ковалентный радиус. По шкале известного кристаллографа и великого химика Полинга, электроотрицательность равна 1,91, а потенциал электронный - 0,25 В.
Действия воздуха и воды на никель практически ничтожны. То же можно сказать и о щелочи. Почему этот металл так реагирует? На его поверхности создается NiO. Это покрытие в виде пленки, которая не дает окисляться. Если никель раскалить до очень высокой температуры, тогда он начинает проявлять реакцию с кислородом, а также воздействует с галогенами, причем со всеми.
Если никель попадет в азотную кислоту, то реакция не заставит себя ждать. Также он охотно активизируется в растворах с содержанием аммиака.
Но не вся кислота действует на никель. Такие кислоты, как соляная и серная, растворяют его очень медленно, но верно. А попытки проделать то же самое с никелем в фосфорной кислоте вообще не увенчались успехом.

Никель в природе
Домыслы ученых заключаются в том, что ядро нашей планеты — это сплав, в котором железа содержится 90 %, а никеля в 10 раз меньше. Есть наличие кобальта - 0,6 %. В процессе вращения в слой земного покрытия выбрались атомы никеля. Они-то и являются основателями сульфидно медно-никелевых руд, вместе с медью, серой. Некоторые более смелые атомы никеля на этом не остановились и пробивали дорогу дальше. На поверхность атомы стремились в компании с хромом, магнием, железом. Далее попутчики нашего металла окислялись и отсоединялись.
На поверхности земного шара имеют место кислые породы и ультраосновные. По наблюдению ученых, содержание никеля в кислых породах гораздо ниже, чем в ультраосновных. Поэтому почва и растительность там достаточно хорошо обогащены никелем. А вот путешествие обсуждаемого героя в биосфере и воде оказалось не так заметно.
Никелевые руды
Промышленно-никелевые руды делятся на два типа.
- Сульфидные медно-никелевые. Минералы: магний, пирротин, кубанит, милерит, петландит, сперрилит - вот что содержится в этих рудах. Спасибо магме, которая их образовала. Из сульфидных руд можно также получить палладий, золото и многое другое.
- Силикатные никелевые руды. Они неплотные, похожие на глину. Руды этого типа бывают железистые, кремнистые, магнезиальные.

Где применяется никель
Обширно никель применяется в такой мощной отрасли, как металлургия. А именно в изготовлении самых разнообразных сплавов. В основном в сплав входит железо, никель и кобальт. Существует много сплавов, в основу которых входит именно никель. Соединяется наш металл в сплав, например, с титаном, хромом, молибденом. Никель также используется, чтобы защитить продукцию, которая быстро подвергается коррозии. Эту продукцию никелируют, то есть создают специальное никелевое покрытие, которое не дает коррозии сделать свое противное дело.
Никель - это очень хороший катализатор. Поэтому он активно используется в химической промышленности. Это приборы, химпосуда, аппараты для различного применения. Для химреагентов, продовольствия, доставки щелочей, хранения эфирных масел используют цистерны и резервуары из никелевых материалов. Без этого металла не обходятся в атомной технике, телевидении, в самых разных приборах, список которых очень длинный.
Если заглянуть в такую сферу, как приборостроение, а следом в сферу машиностроения, то можно заметить, что аноды и катоды – это никелевые листы. И это далеко не весь перечень применения такого просто чудесного металла. Не стоит преуменьшать значение никеля и в медицине.

Никель в медицине
Никель в медицине используется очень широко. Для начала возьмем инструменты, необходимые для проведения операции. Результат операции зависит не только от самого врача, но и от качества инструмента, которым он работает. Инструменты подвергаются многочисленным стерилизациям, и если они изготовлены из сплава, в который не входит никель, то коррозия не заставит себя долго ждать. А инструменты, сделанные из стали, которая содержит никель, гораздо дольше служат.
Если говорить об имплантатах, для их изготовления пускают в ход никелевые сплавы. Никельсодержащая сталь обладает высокой степенью прочности. Приспособления для фиксации костей, протезы, винты - все сделано из этой стали. В стоматологии имплантаты тоже заняли свои крепкие позиции. Бюгели, брекеты из нержавеющей стали используют ортодонты.
Никель в живых организмах
Если смотреть на мир снизу-вверх, то картина вырисовывается примерно такая. Под ногами у нас почва. Содержание никеля в ней больше чем в растительности. Но если рассмотреть эту растительность под той призмой, которая нас интересует, то большое содержание никеля находится в бобовых. А в злаковых культурах процент никеля возрастает.
Рассмотрим коротко среднее содержание никеля в растениях, морских и наземных животных. И конечно же, в человеке. Измерение идет в весовых процентах. Итак, масса никеля в растениях 5*10-5. Наземные животные 1*10-6, морские животные 1,6*10-4. И у человека содержание никеля 1-2*10-6.
Роль никеля в организме человека
Здоровым и красивым человеком хочется быть всегда. Никель - это один из важных микроэлементов в организме человека. Никель обычно накапливается в легких, почках и печени. Скопления никеля у человека встречается в волосах, щитовидной и поджелудочной железе. И это далеко не все. Чем же занимается металл в организме? Тут можно смело сказать, что он и швец, и жнец, и на дуде игрец. А именно:
- не без успеха старается помогать обеспечивать клетки кислородом;
- окислительно-восстановительные работы в тканях тоже ложатся на плечи никеля;
- не стесняется поучаствовать в регулировании гормонального фона организма;
- благополучно окисляет витамин С;
- можно отметить его причастность в обмене жиров;
- отлично никель влияет на кроветворение.
Хотелось бы отметить огромное значение никеля в клетке. Этот микроэлемент оберегает мембрану клетки и нуклеиновые кислоты, а именно их конструкцию.
Хотя перечень достойных трудов никеля можно продолжить. Из вышеперечисленного заметим, что никель организму необходим. Этот микроэлемент в наше тело поступает через пищу. Обычно никеля в организме хватает, ведь его нужно совсем немного. Тревожные звоночки недостатка нашего металла – это появление дерматита. Вот такое значение никеля в организме человека.

Сплавы из никеля
Существует много разных сплавов из никеля. Отметим основные три группы.
К первой группе относятся сплавы никеля и меди. Они так и называются никель-медные сплавы. В каких бы соотношениях ни сплавляли эти два элемента, результат потрясающий и главное – без неожиданностей. Однородный сплав гарантирован. Если в нем присутствует больше меди, чем никеля, то более ярко выражаются свойства меди, а если преобладает никель, сплав проявляет характер никеля.
Никель-медные сплавы популярны в производстве монет, машинных деталей. Сплав Константин, в котором почти 60 % меди, а остальное никель, используется для того, чтобы создать аппаратуру более высокой точности.
Рассмотрим сплав с никелем и хромом. Нихромы. Устойчивы к коррозии, кислотам, жаропрочные. Такие сплавы применяют для реактивных двигателей, атомных реакторов, но только в том случае, если в них присутствует до 80 % никеля.
Перейдем к третьей группе сплавов. Это сплавы с железом. Делят их на 4 вида.
- Жаропрочный – стойкий к высоким температурам. Такой сплав почти на 50 % содержит никель. Здесь сочетание может быть с молибденом, титаном, алюминием.
- Магнитные - увеличивают магнитную проницаемость, часто используют в электротехнике.
- Антикоррозийные – без этого сплава не обойтись при производстве химического оборудования, а также при работе в агрессивной среде. В сплав входит молибден.
- Сплав, сохраняющий свои размеры и упругость. Термопара в печи. Именно сюда идет такой сплав. При нагревании сохраняются размеры габаритов, и упругость не теряется. Сколько никеля нужно, чтобы сплав был с такими свойствами? Металла в сплаве должно быть приблизительно 40 %.
Никель в быту
Если оглядеться вокруг, то можно понять, что никелевые сплавы окружают человека везде. Начнем с мебели. Сплав защищает основу мебели от повреждений, вредных воздействий. Обратим внимание на фурнитуру. Хоть на оконную, хоть на мебельную. Она может долго эксплуатироваться и очень симпатично смотрится. Продолжим нашу экскурсию в ванную. Здесь без никеля никак. Лейки для душа, кран, смеситель - все это никелированное. Благодаря этому можно забыть, что такое коррозия. И не стыдно посмотреть на изделие, потому что выглядит мило и поддерживает декор. Детали с никелированным покрытием встречаются в декоративных строениях.

Никель никак нельзя назвать второстепенным металлом. Разные минералы и руды могут похвастаться наличием никеля. Радует, что такой элемент присутствует на нашей планете и даже в теле человека. Здесь он играет не последнюю скрипку в кроветворных процессах и даже в ДНК. Обширно используется в технике. Свое главенство никель одержал благодаря химической стойкости при защите покрытий.
Никель – это металл, у которого большое будущее. Ведь в некоторых сферах он незаменим.
fb.ru
Никель — что это за металл?

Никель — металл с атомным номером 28. Обозначается символом Ni. Он имеет серебристо-белый оттенок, в нормальных условиях покрывается оксидной пленкой. Благодаря своей пластичности, никель легко поддается ковке.
Физические свойства
Никель — ферромагнетик, то есть при температуре ниже точки Кюри он обладает намагниченностью при отсутствии внешнего магнитного поля. Для никеля точка Кюри составляет 358 ⁰С. Металл не тускнеет на открытом воздухе.
Основные физические свойства никеля:
- Структура решетки — кубическая гранецентрированая.
- Плотность при нормальных условиях — 8,902 г/см3.
- Температура плавления — 1453 ⁰С.
- Удельная теплота плавления — 17,61 кДж/моль.
- Температура кипения – 3000 ⁰С.
- Удельная теплота испарения — 378,6 кДж/моль.
- Молярная теплоемкость — 26,1 Дж/(K*моль)
- Удельная теплоемкость — 0,440 кдж/(кг*К).
- Теплопроводность — 90,9 Вт/(м*К).
- Удельное электрическое сопротивление — 0,0684 мкОм*м.
История
Никель был официально открыт в 1751 году химиком Акселем Кронстедтом, который нашел его в кобальтовой земле. Однако еще раньше его раскапывали в горах Саксонии. Горняки использовали руду, содержащую никель, для изготовления стекла. По внешним признакам саксонцы сначала принимали эту руду за серебряную и пытались переплавить ее в драгоценный металл, но этого не получалось. Кроме того, при плавлении из руды выделялся ядовитый газ, который наносил вред горнякам. Неудачу потерпели и попытки добыть из этой руды медь.
В итоге в конце XVII в. саксонцы назвали руду «купферникель», что в переводе означает «медный дьявол». Это связано с тем, что горняки считали выделение ядовитого газа происками злых духов, обитавших в горах. Именно купферникель исследовал Аксель Кронстедт в 1751 году. Он получил из него окисел зеленого цвета и восстановил его до металла, который до этого не был известен науке. Химик назвал этот металл никелем.
В 1775 году Торберн Улаф Бергман получил никель в более чистом виде и подробнее описал его свойства. Он выяснил, что по своему составу этот металл больше похож на железо, чем на медь. В конце XVIII – начале XIX вв. многие химики, начиная с Жозефа Луи Пруста, детально изучали никель. В 1804 году немецкий химик Иеремия Вениамин Рихтер получил наконец чистый металл, и никель окончательно утвердился как химический элемент.
Биологическая роль
Никель — микроэлемент, который необходим всем живым организмам. Его среднее содержание в растениях — 0,00005 %, в наземных животных — 0,000001 %, в морских — 0,00016 % массы тела.
Роль никеля в организме изучена не до конца. Известно, что он участвует в ферментативных реакциях и влияет на окислительные процессы. Он содержится в легких, печени, мышцах, поджелудочной и щитовидной железах, некоторых отделах головного мозга. Микроэлемент также накапливается в ороговевших тканях человека, животных и птиц, в том числе в волосах и перьях.
Избыточное содержание никеля в растениях приводит к уродливым формам, в организме животных — к различным глазным заболеваниям (кератоконъюнктивитам, кератитам).
Пары и пыль никеля токсичны и могут вызывать поражения кожи, легких и носоглотки, а частое вдыхание паров металла опасно появлением злокачественных новообразований.
Нахождение в природе и производство

Больше всего никеля содержится в глубоких слоях. В земной коре — его 0,0058%, в ультраосновных породах — 0,2 %. Если верить гипотезе, что земное ядро состоит из никелистого железа, общее содержание никеля в земле составляет примерно 3%. Никель также обнаружен в некоторых метеоритах.
В земной коре этот металл соседствует с железом и магнием, с которыми он имеет сходную валентность. В минералах магния и железа никель содержится в виде изоморфной примеси. Также существует 53 известных науке минерала никеля. Большая часть из них была образована под воздействием давления и высоких температур, например, при застывании магмы. Сульфидные руды, содержащие данный металл, имеют в своем составе медь. Некоторые руды никеля включают железо, серу, мышьяк, кобальт, магний.
Больше всего этого металла добывается на территории России. Крупные никелевые рудники также находятся в Канаде, Австралии, Новой Каледонии, Индонезии и на Кубе.
Больше всего никеля (около 80%) получают из сульфидных медно-никелевых руд, значительно меньше — из силикатных (окисленных) руд.
Химические свойства
Никель химически малоактивен. Он образует поверхностную оксидную пленку, из-за чего устойчив в атмосфере, щелочи, многих кислотах и воде. Металл не подвергается коррозии. Образует два оксида (NiO и Ni2O3) и два гидроксида (Ni(OH)2 и Ni(OH)3).
Хлорид, нитрат, сульфат и нитрат никеля — четыре растворимые соли. Они имеют желтый или желто-коричневый оттенок и окрашивают растворы в зеленый цвет. Фосфат, оксалат и сульфиды никеля (черный, зеленый и бронзовый) — нерастворимые соли.
Металл поглощает газы (углерод, водород и многие другие), которые ухудшают его механические свойства. С кислородом взаимодействует при температуре выше 500 ⁰С.
В мелкодисперсном состоянии никель самовоспламеняется на воздухе. При нагревании соединяется с галогенами. Образует сульфид при горении в сере, а при нагревании оксида NiO с серой получается моносульфид. Металл также вступает в реакцию с азотной кислотой: образуются нитрат никеля и оксид азота.
По химическим свойствам больше всего похож на железо и кобальт, в меньшей степени — на благородные металлы и медь. Он горит только в виде порошка, проявляет переменную валентность в соединениях (чаще всего двухвалентен). Образует комплексные и координационные соединения.
Применение
Наиболее широкая область применения никеля — изготовление сплавов различных металлов. Его сплавляют:
- Со сталью. Это повышает химическую стойкость сплава: все нержавеющие стали содержат в своем составе никель.
- С железом. Этот сплав имеет низкий коэффициент термического расширения, благодаря чему он успешно используется для изготовления различных деталей для электроприборов.
- С кобальтом и магнием. Образуется жаростойкий сплав, который выдерживает высокие температуры до 500 ⁰С и отличается устойчивостью к коррозии.
- С золотом и серебром. Это так называемое «белое золото» — прочный ювелирный сплав.
- С хромом. В результате образуется нихром — жаропрочный, крипоустойчивый, пластичный сплав, который хорошо держит форму.
- С железом, медью и хромом. Этот сплав характеризуется высокой магнитной восприимчивостью.
Сплавы никеля отличаются высокой степенью вязкости, благодаря чему находят применение при изготовлении брони. Многие сплавы используются в газотурбинных установках, конструкциях атомных реакторов. Из них также делают нагревательные элементы и монеты. Сплавы получили широкое применение в производстве аккумуляторов.
Никель используется и в чистом виде: из него изготавливают трубы, листы и др., а в химических лабораториях он служит катализатором многих реакций. Из металла также производят специализированную химическую аппаратуру. Оксид никеля применяется в производстве стекла, керамики и глазурей. Для многих металлов используется никелирование — создание никелевого покрытия с целью защитить от коррозии.
Из никеля делают спирали электронных сигарет, им обматывают струны музыкальных инструментов. В медицине этот элемент используется для протезирования и изготовления брекет-систем.
ferrolabs.ru
Медные сплавы с никелем - Справочник химика 21
Для медных сплавов, никеля, углеродистых сталей [c.31]Для предупреждения коррозии стали, чугуна, меди и медных сплавов, никеля, олова, алюминия и его сплавов находит применение хромат циклогексиламина, используемый также в виде порошка. [c.171]
Этим объясняется, почему на практике редко создается потребность в полном исследовании какого-нибудь вещества. Обычно ограничиваются открытием некоторых элементов, например железа, марганца, свинца в медном сплаве никеля, хрома, ванадия в стали меди, железа в алюминии. [c.210]
Черные металлы Медь и медные сплавы Никель и никелевые сплавы Свинец и свинцовые сплавы Алюминий и алюминиевые сплавы Магний и магниевые сплавы [c.7]Особенно усиливает коррозию магниевых сплавов контакт со следующими металлами медью, медными сплавами, никелем, никелевыми сплавами, свинцом, всеми марками стали, в том числе и нержавеющей, серебром и его сплавами, молибденом. В жестких условиях эксплуатации, например в морской атмосфере или тропических условиях, не допускается контакт магниевых сплавов с цинком, цинковыми покрытиями. [c.243]
Медь и медные сплавы Никель 6 12 18 — [c.64]
Кальцинированная сода — 15— 20, жидкое стекло — 8—10, не-. ионогенное ПАВ — 3 55—80 Сталь, медные сплавы, никель. Полировочные пасты, консервирующие и волочильные смазки, минеральные масла и жировые плевки То же [c.693]
Реактив пригоден для выявления микроструктуры меди и медных сплавов, никеля, молибдена и их сплавов [88, 130]. [c.69]
Никель- медный сплав (монель) НМЖ.Мц 28—2,5-1,5 27—29 1 67—70 1.2-1,8 2,0—3,0 Плакирующий слой верха корпуса атмосферных колонн [c.25]
При переработке сильно засоленных нефтей облицовку и внутренние детали аппаратуры изготовляют из никель-медного сплава — монеля (см. табл. 10). [c.26]
При наличии в воздухе частиц хлористых солей (в частности, в морской атмосфере) большинство технических металлов и сплавов подвергается усиленной коррозии. Некоторые примеси в воздухе могут усиливать коррозию одних металлов и не оказывать влияния на другие. Так, медь и медные сплавы подвергаются усиленной коррозии при наличии в атмосфере даже небольших количеств паров аммиака, никель же в этих условиях не разрушается. Во влажном воздухе, даже загрязненном 502, НаЗ и некоторыми другими газами, свинец не подвержен коррозии, так как на его поверхности образуется защитная пленка. [c.180]
Электролитическое разделение компонентов медных сплавов с оловом, цинком, никелем раньше применялось при ликвидации запасов артиллерийской бронзы в 1906—1908 гг., при переработке латунных и медноникелевых ломов, оставшихся после войны 1914—1918 гг. Ныне объем электролитической [c.213]
Элементы-металлы входят в состав всех групп периодической системы, кроме нулевой. Химические и физические свойства простых веществ, образованных элементами-металлами, — собственно металлов — имеют ряд особенностей. Металлический блеск, высокая тепло- и электропроводность определяются особенностями электронной структуры атомов металлов. Интересно, что электропроводность различных металлов сильно различается. Это можно легко показать, включив в электрическую цепь с гальванометром поочередно медную, железную и, например, нихромовую проволоку (сплав никеля и хрома). Проволока из меди обладает столь высокой электропроводностью, что гальванометр зашкаливает . Включение в тех же условиях в цепь проволоки из железа дает лишь слабое отклонение стрелки гальванометра. В случае нихромовой проволоки отклонение стрелки гальванометра незаметно — так велико электрическое сопротивление сплава нихром (на этом основано его использование в электронагревательных приборах). [c.252]
Хром, молибден и вольфрам широко применяются для легирования сталей, никелевых и медных сплавов. При содержании хрома более 12% сталь становится коррозионно стойкой. Нержавеющие стали с добавками молибдена более жаропрочны и лучше свариваются. Хром в большом количестве идет для гальванических покрытий на стальных изделиях. Лучшие покрытия хромом получаются при нанесении их на подслой никеля или меди. [c.340]
Принадлежность данного сплава к определенному типу дает возможность с большой степенью достоверности предвидеть примерный его состав. Так, например, алюминиевые сплавы содержат магний, железо, кремний, титан, медь, цинк, марганец, никель и др. медные сплавы — олово, цинк, СБ1 н ц, сурьму, висмут, железо, никель, кремний, фосфор и др. [c.453]
Стальные детали подвергаются коррозии при контактировании нх с медью и медными сплавами, нержавеющими сталями, никелем и никелевыми сплавами. Детали из этих сплавов, контактирующих со сталью, необходимо оцинковывать или кадмировать. Могут быть также использованы прокладки из оцинкованного железа или оцинковка стальных деталей. [c.7]
Как указывалось, дуговые печи косвенного действия выполняются качающимися однофазными с двумя горизонтально расположенными электродами и цилиндрическим кожухом (рис. 2-27). Печи используются в основном для переплава медных сплавов, идущих на фасонное литье иногда печи применяются для выплавки некоторых сортов чугуна и никеля. Основное их преимущество— сравнительно небольшой угар металла, так как зона высоких температур (дуга) не соприкасается непосредственно с расплавляемым металлом. [c.74]
Лужение медных сплавов погружением в растворы солей, содержащих двухвалентное олово, применяется при пайке. Цинк осаждается на алюминии погружением в горячие, щелочные, цинкатные растворы в целях получения тонкого покрытия как основы для последующего электроосаждения других металлов, в основном меди, никеля и хрома. В результате химического осаждения можно получить чисто декоративные оловянные и серебряные покрытия. [c.83]
Перед нанесением покрытия необходимо проводить тщательную обработку поверхности. Сталь очищают электролитически и подвергают кислотному травлению для получения микрошероховатости поверхности. Медные сплавы тщательно очищают и протравливают. Так как никель непосредственно не восстанавливается на медной поверхности, поверхность этих сплавов должна катализироваться с хлористым палладием до нанесения покрытия. Перед погружением в ванну избыток хлористого палладия необходимо тщательно смыть. На алюминиевые сплавы никелевые покрытия можно наносить только после декапирования и травления. Более эффективные результаты достигаются, если перед нанесением никелевого покрытия производится дальнейшая предварительная обработка путем осаждения цинкового покрытия погружением в цинковый раствор. [c.84]
Электроосаждение медных сплавов возможно при использовании сложных щелочных цианистых растворов в температурных пределах 30—90° С (в зависимости от используемого раствора). Латунные и бронзовые изделия могут получать покрытие при использовании анодов соответствующего состава сплавов, причем катодная производительность и состав электролитических осадков зависят от плотности тока, применяемого в процессе осаждения. Большинство осадков обладает довольно хорошим блеском, но выравнивание в основном плохое или отсутствует. Для декоративного использования стали применяют обычно тонкослойные осадки, без грунта или в сочетании с никелем в целях улучшения выравнивания. При этом обычно наносят лак, чтобы избежать потускнения под влиянием атмосферных воздействий. В некоторых случаях можно использовать декоративное хромовое покрытие, но осадки сплавов меди часто имеют высокие внутренние напряжения, что может привести к серьезному растрескиванию хрома. Электролитические осадки бронзы могут служить в качестве защитных грунтовых покры- [c.95]
Никелевые покрытия имеют толщину от 5 до 40 мкм. Для декоративных покрытий используют никель или сочетание никель- -хром в зависимости от состава основного металла (стали, цинкового сплава, меди или медных сплавов, алюминия или алюминиевых сплавов, пластмассы) и условий окружающей среды. С более толстослойным покрытием изготовляют химическое оборудование или изделия, применяемые в гальванопластике. [c.97]
Железо и железные сплавы Медь и медные сплавы Никель и никелевые сплавы Свипец и свини,о 5ые сплавы Алюминий и алюминиевые сплавы Балл корро- зионной стойкости [c.155]
При конструировании химических машин необходимо выбирать материалы с таким расчетом, чтобы были предотвращены условия возникновения элект[)о-химической коррозии, поэтому в деталях и узлах, где сопрягаются два металла, необходимо избегать контакта металлов, электрохимические потенциалы которых значительно отличаются друг от друга. Недопустимо создавать контакт со сталью меди и медных сплавов, никеля и никелевых сплавов, благородных металлов и их сплавов. Для предотвращения коррозионного разрушения в таких случаях целесообразно применение оцинкования и кадлшрования стальных деталей, применение прокладок и шайб из оцинкованного железа. Для нержавеющих сталей недопустимым является контакт с алюминием и его сплавами, медью и медными сплавами и т. д. Для алюминиевых сплавов недопустим контакт со сталями, медными и никелевым сплавами и допустим контакт с. юбы.ми материалами, покрытыми цинком, кадмием и алюминием. Необходилю также учитывать коррозию свинца при контакте его с портланд-цементом, так как он обладает щелочными свойства.ми. [c.81]
Тринатрийфосфат — 20—35, веиоиогенное ПАВ—3, сульфонол — 0,5—1,5 55—80 Сталь, медные сплавы, никель. Полировочные пасты, консервирующие и воло ильные смазки, минеральные масла и жировые пленки Анионоактивные ПАВ добавляются с повышением температуры раствора [c.693]
Аналитический разновес для взвешивания на обычных аналитических весах имеет следующий набор гирь 100 г, 50 г, 20 г, 10 г, 10 г, 5 г, 2 г, 2 г, 1 г, 500 мг, 200 мг, 200 мг, 100 мг, 50 мг, 20 мг, 20 мг, 10 жг и 2 рейтера, каждый весом по 10 мг. Аналитические граммовые гири изготовляются из медных сплавов или нержавеющей стали, их поверхность отполирована и покрыта золотом, никелем или хромом. Миллиграммовые гири изготовляются из алюминия, никеля, нейзильбера. Рейтеры (рис. 65) делают из алюминиевой или стальной проволоки в форме двухзубчатой вилки с петлей наверху. [c.44]
Гибкий элемент изготовляют гидравлической формовкой из высоколегированных сталей 08Х18Н10Т, 10Х17Н13М2Т, никелевых ц никель-медных сплавов. Применяют элементьГс й-образ-ным и и-образным профилем волны. [c.318]
Каталитическое гидрирование в паровой фазе при атмосферном давлении над восстановленным никелем было открыто Сабатье Вскоре В. Н. Ипатьев впервые применил гидрирование в жидкой фазе под давлением водорода. За почти семидесятилетний период развития и изучеааия реакций гидрирования было открыто много весьма активных катализаторов позволявших работать при очень мягких условиях никелевые катализаторы на носителях, хромит-медные катализаторы, окись платины, платиновая чернь и др. Большое значение, в том числе и промышленное, получили так называемые скелетные никелевые катализаторы ( никель Ренея ) . К настоящему времени ряд катализаторов значительно пополнен, а известные катализаторы усовершенствованы. Так, например, очень активными катализаторами являются сплавы никеля и родия, платины и рутения, модифицированные катионами палладиевые катализаторы и др. Скелетные катализаторы значительно улучшены промотированием , а приготовление катализаторов усовершенствовано так, что платиновая чернь, например, может быть получена с хГоверхностью до 200 м /г, в то время как в прошлом лучшие образцы имели поверхность не более 50—60 м г. [c.130]
Из медных сплавов бронзы менее склонны к растрескнвагшю, чем латущ], Никель и его сплавы меньше подвержены этому виду разрушения, чем медные сплавы. [c.116]
Имеются доказательства, что при пластической деформации атомы цинка концентрируются преимущественно у границ зерен Различия в составе приводят к электрохимическому взаимодей ствию таких участков с зернами. По этой причине в ряде агрес сивных сред небольшая межкристаллитная коррозия может про исходить и без приложенного напряжения. Однако участки пла стической деформации при определенных значениях потенциала могут способствовать адсорбции комплексных ионов аммония, что в свою очередь приводит к быстрому образованию трещин. Аналогичный эффект может наблюдаться и вдоль линий скольжения (транскристаллитное растрескивание). По-видимому, выделение цинка на границах зерен является существенной причиной наблюдаемой межкристаллитной коррозии латуней в то же время наличие структурных дефектов в области границ зерен или линий скольжения играет большую роль в протекании КРН. Следовательно, разрушение медных сплавов в результате растрескивания наблюдается не только в сплавах меди с цинком, но также и со множеством других элементов, например кремнием, никелем, сурьмой, мышьяком, алюминием, фосфором [21 и бериллием [31]. [c.338]
Легирование никеля медью несколько повышает стойкость металла в восстановительных средах (например, в неокислительных кислотах). Ввиду повышенной стойкости меди к питтингу, склонность сплавов никель—медь к питтингообразованию в морской воде ниже, чем у никеля, а сами питтинги в большинстве случаев неглубокие. При содержании более 60—70 ат. % Си (62—72 % по массе) сплав теряет характерную для никеля способность пассивироваться и по своему поведению приближается к меди (см. разд. 5.6.1), сохраняя, однако, заметно более высокую стойкость к ударной коррозии. Медно-никелевые сплавы с 10—30 % N1 (купроникель) не подвергаются питтингу в неподвижной морской воде и обладают высокой стойкостью в быстро движущейся морской воде. Такие сплавы, содержащие кроме того от нескольких десятых до 1,75 % Ре, что еще более повышает стойкость к ударной коррозии, нашли применение для труб конденсаторов, работающих на морской воде. Сплав с 70 % N1 монель) подвержен питтингу в стоячей морской воде, и его лучше всего применять только в быстро движущейся аэрированной морской воде, где он равномерно пассивируется. Питтинг не образуется в условиях, когда обеспечивается катодная защита, например при контакте сплава с более активным металлом, таким как железо. [c.361]
Медь применяется в виде металла, многочисленных сплавов и соединений. Около 40% всей добываемой меди идет на изготовление электрических проводов и кабелей. Из меди изготовляют нагревательные аппараты. Сплавы меди с другими металлами широко применяются в машиностроительной промышленности, в электротехнике, в судостроении, энергетической промышленности. К важнейшим сплавам меди относятся бронза (90% Си, 10% Sn), латунь (60% Си, 40% Zn), мельхиор (80% Си, 20% N1), манганин (85% Си, 12% Мп, 3% N1), нейзильбер (65% Си, 20% Zn, 15% Ni), кон-стантан (59% Си, 40% N1, 1% Мп). Все медные сплавы обладают высокой стойкостью против атмосферной коррозии. Современные серебряные монеты сделаны из сплава меди с никелем ( u+Ni). [c.418]
Как видно из приведенных данных, при малых скоростях движения воды влияние различных положительных контактов мало сказьшается на коррозии стали, а при больших скоростях движения воды проявляется индивидуальная природа катода и в наибольшей степени усиливают коррозию стали медь и никель. Поэтому детали из меди и медных сплавов, нержавеющих сталей, никеля или никелевых сплавов, контактирующих со сталью, необходимо оцинковьшать или кадмировать. Могут быть также П1жменены прокладки из оцинкованного железа или оцинкованных стальных деталей. [c.201]
Предлагается следующий состав химического палладирования (моль/л) палладий хлористый 0,05 пирофосфат натрия 0,11 фторид аммония 0,3 аммиак 8, гипофосфнт иатрия 0,05, pH 10, температура 45—55 °С скорость осаждения 3—4 мкм/ч Из указанного раствора были получены светлые, гладкие палладиевые аокрытия толщиной до 10 мкм на меди и медных сплавах, на никеле, кобальте и их сплавах, серебре и платине. [c.88]
ПСр 72 ПСр 71 ПСр 62 ПСр 50Кд ПСр 50 ПСр 45 ПСр 40 ПСр 37,5 ПСр 25 ПСр 15 ПСр 10 ПСр 2,5 ПСр 72 ПСр 62 ПСр 40 ПСр 25 ПСр 12М Лужение и пайка меди, медных и медно-никелевых сплавов, никеля, ковара, нейзильбера, латуней и бронз. Пайка стали с медью, никелем, медными и медноникелевыми сплавами. [c.362]
Вообще говоря, в морской воде в качестве окислителя могут выступать ионы НзО или молекулы воды и растворенный кислород. Исследованию катодных процессов в хлоридсодержащих средах были посвящены работы Г. В. Акимова, Н. Д. Томашева, Г. Б. Кларк, И. Л. Розенфельда. Как показали исследования, коррозия магния и его сплавов протекает в основном за счет водородной деполяризации алюминий и его сплавы, коррозионностойкие и конструкционные стали, никель и никелевые сплавы, медь, медные сплавы подвергаются коррозии с кислородной деполяризацией. Растворимость кислорода в морской воде ограничена. При протекании коррозии с кислородной деполяризацией очень часто скорость катодного процесса определяется диффузией кислорода и поверхноети металла. В таких условиях перемешивание среды или перемещение поверхности металла относительно среды является важным фактором, который может оказать существенное влияние на характер коррозии. При перемешивании скорость катодного процесса будет уве-личиваться и металл из пассивного состояния может переходить в пробойное состояние (см. рис. 18). [c.43]
chem21.info