Качественные-реакции-неорганической-химии. Качественные реакции неорганической химии. Качественная реакция на хром 3
Качественные реакции на катионы
⇐ ПредыдущаяСтр 4 из 8Следующая ⇒NH 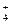 ; Na+; K+; Mg2+; Ba2+; Ca2+; Fe2+; Fe3+; Mn2+; Co2+; Ni2+; Zn2+;
; Na+; K+; Mg2+; Ba2+; Ca2+; Fe2+; Fe3+; Mn2+; Co2+; Ni2+; Zn2+;
Al3+; Cr3+; Ag+; Pb2+; Cu2+; Cd2+ .
Реакция на ион Na+
Ионы натрия образуют с дигидроантимонатом калия в нейтральной или слабощелочной среде белый кристаллический осадок дигидроантимоната натрия:
2NaCl + K2h3SbO4 = Na2h3SbO4↓ + 2KCl
2Na+ + h3SbO 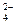 = Na2h3SbO4↓
= Na2h3SbO4↓
Потирание изнутри стенок пробирки стеклянной палочкой и охлаждение пробирки под холодной струей воды ускоряет осаждение.
Реакция на ион K+
1. Гидротартрат натрия образует с раствором солей калия белый кристаллический осадок гидротартрата калия:
KCl + NaHC4h5O6 = KHC4h5O6↓ +NaCl
K+ +HC4h5O6 - = KHC4h5O6↓
Осадок выпадает при потирании стеклянной палочкой внутренней стенки пробирки и охлаждение пробирки под струей холодной воды.
2. Кобальтинитрит натрия образует с растворами солей калия желтый осадок - кобальтинитрит калия:
2KCl + Na3 [Co(NO2)6] = K2 Na[Co(NO2)6]↓ + 2 NaCl
2K+ + Na+ + [Co(NO2)6]3- = K2 Na[Co (NO2)6]↓
Реакция на ион NH 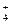
1. Едкие щелочи KOH и NaOH при нагревании вытесняют из растворов солей аммония аммиак:
Nh5Cl +KOH = KCl + Nh4 + h3O
NH 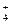 + OH- = Nh4 + h3O
+ OH- = Nh4 + h3O
Выделяющийся аммиак можно обнаружить по запаху или по влажной индикаторной ленте (щелочная реакция).
2. Реактив Неслера (щелочной раствор комплексной соли K2[HgJ4]) образует с раствором соли аммония осадок оранжево-бурого цвета:
Nh5Cl + 2K2 [HgJ4] +2KOH = [2J-2Hg-Nh3]J↓ +5KJ +KCl 2h3O
NH 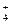 +2[HgJ4]2- + 2OH- = Nh3Hg2J3 ¯+ 5J- + 2h3O
+2[HgJ4]2- + 2OH- = Nh3Hg2J3 ¯+ 5J- + 2h3O
В присутствии очень малых количеств раствор окрашивается или в желтый или в бурый цвет.
Реакция на ион Mg2+
Гидрофосфат натрия образует с солями магния в присутствие Nh5OH и Nh5Cl белый кристаллический осадок.
Поместите в пробирку по 2-3 капли растворов MgCl2 и Nh5Cl, прибавьте к полученной смеси 2-3 капли раствора Na2HPO4. Тщательно перемешайте содержимое пробирки стеклянной палочкой и затем добавьте к раствору Nh5OH:
MgCl2 + Nh5Cl + Nh5OH + Na2HPO4 = MgNh5PO4↓ + 2NaCl + Nh5Cl + h3O
Mg2+ + HPO 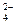 +Nh5OH = MgNh5PO4↓ + h3O
+Nh5OH = MgNh5PO4↓ + h3O
Реакция на ион Ba2+
1. Дихромат–ион образует с ионами бария осадок желтого цвета (хромат бария):
2BaCl2 + K2Cr2O7 + h3O = 2BaCrO4↓ + 2KCl + 2HCl
2Ba2+ + Cr2O 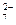 + h3O = 2BaCrO4↓+ 2H+.
+ h3O = 2BaCrO4↓+ 2H+.
2. Сульфат – ион образует с ионами бария осадок белого цвета (сульфат бария), не растворимый в кислотах:
BaCl2 + h3SO4 = BaSO4↓ + 2HCl
Ba2+ + SO 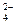 = BaSO4↓
= BaSO4↓
3. Оксалат – ион образует с ионами бария осадок белого цвета (оксалат бария):
BaCl2 + (Nh5)C2O4 = Nh5Cl + BaC2O4↓
Ba2+ + C2O 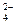 = BaC2O4↓
= BaC2O4↓
Реакция на ион Ca2+
Оксалат-ион образует с ионами кальция белый кристаллический осадок:
CaCl2 + (Nh5)2C2O4 = CaC2O4↓ + 2Nh5Cl
Ca2+ + C2O 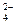 = CaC2O4¯
= CaC2O4¯
Проведению реакции могут мешать ионы бария.
Реакция на ион Fe2+
Растворы двухвалентного железа окрашены в бледно-зеленный цвет.
Гексацианоферрат (III) калия с двухвалентным железом образует синий осадок, называемый турнбулевой синью:
3FeCl2 + 2K 3 [Fe (CN) 6] = Fe 3 [Fe (CN) 6]2↓ + 6KCl
3Fe2+ + 2[Fe (CN) 6]3- = Fe 3 [Fe (CN) 6]2↓
Реакция на ион Fe3+
Растворы трехвалентного железа имеют желтую или красно-бурую окраску.
1. Ионы трехвалентного железа с роданид-ионом образуют соединение, окрашивающее раствор в кроваво-красный цвет:
FeCl3 + 3Nh5CNS = Fe (CNS) 3 + 3Nh5Cl
Fe3+ + 3CNS- = Fe (CNS)3
или
Fe3+ + 6CNS- = [Fe (CNS)6 ]3-
2. Гексацианоферрат (II) калия с трехвалентным железом образует темно-синий осадок, называемый берлинской лазурью:
4FeCl3 + 3K 4 [Fe (CN)6 ] = Fe 4 [Fe (CN) 6 ]3↓ + 12KCl
4Fe3+ + 3[Fe (CN)6 ]4- = Fe4[Fe (CN)6 ]3↓
3. Ионы трехвалентного железа со фторидом натрия в растворе образуют бесцветное комплексное соединение:
FeCl3 + 6NaF =Na3 [Fe F6] + 3NaCl
Fe3+ + 6NaF = [Fe F6]3- + 6Na+
Реакция на ион Mn2+
Концентрированные растворы солей марганца имеют бледно-розовый цвет, разбавленные растворы – бесцветны.
Ионы двухвалентного марганца в кислой среде окисляются (в данном случае висмутатом натрия) до перманганат–ионов красно-фиолетового цвета:
2Mn(NO3)2 + 5NaBiO3 + 14HNO3 = 2NaMnO4 + 5Bi(NO3)3 + 3NaNO3 +7h3O
2Mn2+ +5BiO  + 14H+ = 2MnO
+ 14H+ = 2MnO  + 5Bi3+ +7h3O
+ 5Bi3+ +7h3O
Реакция на ион Cr3+
Растворы солей хрома имеют зеленую или фиолетовую окраску.
Ионы трехвалентного хрома окисляются перекисью водорода в щелочной среде до хромат – ионов.
Поместить в пробирку 2-3 капли соли хрома (III), прилить раствор щелочи до растворения осадка. К полученному раствору хромита (изумрудно – зеленого цвета) прилить 2-3 капли перекиси водорода и осторожно нагреть пробирку. Зеленая окраска раствора перейдет в желтую:
CrCl3 + 4NaOH = NaCrO2 + 3NaCl + 2h3O
Cr3+ + 4OH- = CrO 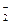 +2h3O
+2h3O
2NaCrO2 + 3h3O2 + 2NaOH = 2Na2CrO4 + 4h3O
2CrO 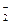 + 3h3O2 + 2OH- = 2CrO
+ 3h3O2 + 2OH- = 2CrO 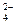
Реакция на ион Co2+
Разбавленные растворы солей кобальта имеют розовую окраску. Роданид-ион с ионами кобальта образуют комплексную соль синего цвета.
Поместите в пробирку 2-3 капли раствора кобальта (II), насыпьте немного сухой соли роданида аммония и прилейте 5-6 капель амилового или изоамилового спирта. Смесь перемешайте. Наблюдайте расслоение жидкостей и окрашивание верхнего слоя в голубой или синий цвет.
CoCl2 + 4Nh5CNS = (Nh5)2[Co (CNS) 4] + 2Nh5Cl
Co2+ + 4CNS- = [Co(CNS)4]2-
Этой реакции мешают ионы железы (III), которые образуют с роданидом соединение кроваво – красного цвета. Поэтому ионы железа (III) предварительно связывают в бесцветный комплекс фторидом натрия или фторидом аммония.
Реакция на ион Ni2+
Растворы солей никеля имеют зеленую окраску.
Ионы никеля в аммиачной среде образуют с диметилглиоксимом осадок комплексной соли ало-красного цвета.

Этой реакции мешают ионы трехвалентного и двухвалентного железа:
Реакция на ион Zn2+
Растворы солей цинка бесцветны.
С гексацианоферратом (II) калия ионы цинка образуют аморфный осадок салатного цвета:
3ZnCl2 +2K 4 [Fe (CN) 6] 2 = K 2 Zn 3 [Fe (CN) 6]2↓ + 6KCl
2K+ + 3Zn2+ + 2[Fe(CN)6]4- = K2Zn 3[Fe(CN)6]2↓
Реакция на ион Al3+
Растворы солей алюминия бесцветны.
При осторожном добавлении щелочей (по каплям) образуется осадок белого цвета в виде белых студенистых хлопьев, часто всплывающих на поверхность раствора:
AlCl3 + 3NaOH = Al (OH)3↓ + 3NaCl
Al3+ + 3OH- = Al(OH)3↓
Гидроксид алюминия обладает амфотерными свойствами: при действии на Al (OH)3 раствором кислоты или щелочи происходит растворение осадка:
Al(OH)3 + 3HCl = AlCl3 + 3h3O
Al(OH)3 + 3H+ = Al3+ + 3h3O
Al(OH)3 + 3NaOH = Na3[Al(OH)6]
Al(OH)3 + 3OH- = [Al(OH)6]3-
Реакция на ион Ag+
1. Хлорид – ион осаждает ионы серебра из раствора в виде белого творожистого осадка:
AgNO3 + HCl = AgCl↓ + HNO3
Ag+ + Cl- = AgCl↓
Хлорид серебра нерастворим в азотной кислоте, но растворим в гидроксиде аммония:
AgCl + 2Nh5OH = [Ag (Nh4)2]Cl + 2h3O
Если на полученный раствор [Ag(Nh4)2]Cl подействовать раствором азотной кислоты, то AgCl снова выпадает в виде творожистого белого осадка:
[Ag(Nh4)2]Cl + 2HNO3 = AgCl↓ + 2Nh5NO3
2. Иодид – ион с ионами серебра образует осадок желтого цвета:
AgNO3 + KJ = AgJ↓ + KNO3
Ag+ + J- = AgJ↓
Реакция на ион Pb2+
1. Хлорид – ион осаждает ионы свинца в виде белого творожистого осадка:
Pb(NO3)2 + 2HCl = PbCl2↓ + 2HNO3
Pb2+ + 2Cl- = PbCl2↓
Хлорид свинца нерастворим в гидроксиде аммония:
PbCl2 + Nh5OH = реакция не идет.
2. Иодид – ион осаждает ионы свинца в виде осадка желтого цвета:
Pb (NO3)2 + 2KJ = PbJ2↓ + 2KNO3
Pb2+ + 2J- = PbJ2↓
Часть осадка растворите в 5-6 каплях уксусной кислоты при нагревании, а затем осторожно охладите под струей холодной воды. Хлорид свинца из раствора выпадает в виде золотистых хлопьев.
Реакция на ион Cu2+
1. Гидроксид аммония, добавленный в избытке к солям меди, образует растворимое комплексное соединение василькового цвета:
CuSO4 + 4Nh5OH = [Cu (Nh4)4]SO4 + 4h3O
Cu2+ + 4Nh5OH = [Cu (Nh4)4]2+ + 4h3O
2. Гексацианоферрат калия осаждает ион меди (II) из раствора в виде осадка красно-коричневого цвета:
2CuSO4 + K4[Fe(CN)6] = Cu2[Fe(CN)6]↓ + 2K2SO4
2Cu2+ + [Fe(CN)6]4- = Cu2[Fe(CN)6]↓
Реакция на ион Cd2+
Сульфид – ион в слабокислой среде осаждает ионы кадмия из раствора в виде осадка желтого цвета:
CdCl2 + Na2S = CdS↓ + 2NaCl
Cd2+ + S2- = CdS↓
Контрольные вопросы
1. Приведите примеры катионов и анионов, которые могут быть обнаружены с помощью окислительно-восстановительных реакций.
2. Какие ионы образуют окрашенные комплексные соединения: Cu2+; Cu+; Fe2+; Fe3+; Co3+; Zn2+; Ag+?
3. Присутствие каких ионов может быть обнаружено по образованию летучих веществ: SO 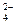
 ; CO
; CO  ; PO
; PO  ; Na+ ; NH
; Na+ ; NH 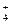 ?
?
4. Как доказать наличие ионов Сu2+ и Ag+ в одном растворе?
Лабораторная работа № 3 (4 ч.)
Тема: Карбонаты. Жесткость воды (постоянная и временная).
Цель: ознакомиться со способами устранения временной и постоянной жесткости воды.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Присутствие в воде ионов Са2+ и Мg2+ обуславливает так называемую жёсткость воды. Жёсткая вода вызывает повышенный расход мыла, поскольку при взаимодействии солей кальция и магния с мылом образуются нерастворимые осадки:
2С17Нз5СООNа+ Са(НСО3)2 = 2NаНСОз + (С17Н35СОО)2Са¯
На стенках паровых котлов жёсткая вода образует накипь, обладающую плохой теплопроводностью. Кроме того, накипь способствует коррозии стенок котлов. В жёсткой воде плохо разваривается мясо, овощи, плохо заваривается чай. Очень жёсткая вода не пригодна для питья. Условная классификация воды по уровню жёсткости приведена в табл. 3.
Таблица 3
Читайте также:
lektsia.com
Качественное обнаружение хрома - Справочник химика 21
Исходя из свойств некоторых органических соединений, применяемых в анализе, перспективными для качественного обнаружения ионов металлов метод адсорбционно-комплексообразовательной хроматографии являются (в скобках указаны определяемые элементы) ализарин С (алюминий, циоконий, торий) алюминон (алюминий, бериллий) арсеназо III (цирконий, гафний, торий, уран, редкоземельные элементы) диметилглиоксим [никель, кобальт, железо (II), палладий (И)] 2,2 -дипиридил [железо (И)] дитизон (серебро, висмут, ртуть, свинец, цинк) дифенил-карбазид [хром (VI)] 2-нитрозо-1-нафтол (кобальт) нитро-зо-Н-соль (кобальт) рубеановая кислота [железо (III), [c.248] Качественное обнаружение. Основано на окислении СгЗ+ персульфатом аммония до и обнаружении последнего реакциями с дифенилкарбазидом и образования над.хромата хрома (надхромовых кислот). [c.314]Качественное обнаружение хрома [c.182]
Качественное обнаружение хрома [c.155]
Описанная методика качественного анализа использована для определения примесей в образцах олова, серебра, германия, железа, ванадия, кремния, алюминия, углерода и пленок хрома, кремния и лантана. Все обнаруженные на масс-спектрограмме пики соответствуют одно-, двух- и трехзарядным положительным атомарным ионам. Более сложных ионов на масс-спектрограмме обнаружено не было. [c.174]
Одной из известных качественных реакций для открытия рения является проба на перл буры. При нагревании в восстановительном пламени перл буры окрашивается рением в черный цвет, который исчезает в окислительном пламени вследствие окисления рения до Re(VII). Используют также перл соды, который в окислительном пламени в присутствии рения окрашивается в желтый цвет. Этим методом можно определять до 0,015 мг Re [1266]. Метод пригоден для обнаружения рения в сплавах при его содержании >5% вольфрам и молибден не мешают, а хром, рубидий и осмий мешают обнаружению рения- [c.69]
МЕТОДЫ КАЧЕСТВЕННОГО ОБНАРУЖЕНИЯ ХРОМА [c.26]
На чем основано качественное обнаружение хрома, цинка и марганца [c.162]
Можно ли ограничиться фактом качественного обнаружения хрома, цинка и марганца [c.162]
Рассмотренная реакция окнсления иона Сг + в анион СгО особенно важна, так как она служит характерной качественной реакцией для обнаружения хрома. г [c.260]
Соединения хрома при сплавлении с бурой образуют изумруднозеленые стекла. Этими процессами пользуются для качественного обнаружения Со, Сг и других элементов в соединениях. [c.282]
Окисление Сг до СггО в кислой среде в отсутствие хлоридов. Персульфат аммония является весьма важным и широко используемым окислителем не толь ко для качественного обнаружения, но и для количественного определения хрома. В кислых растворах нитра [c.162]
Для проверки этого положения нами был поставлен на двух дизелях следующий простой опыт в дизельное топливо было введено 0,1% никелевой соли нафтеновых кислот, а в дизельное масло такое же количество (0,1%) хромовой соли нафтеновых кислот. Нафтенаты никеля и хрома были получены реакцией двойного обмена между нафтенатом натрия и соответствующей азотнокислой солью. Никель и хром были выбраны вследствие легкости их качественного обнаружения даже при совершенно ничтожном содержании, малой летучести их солей и возможности точного количественного определения. [c.340]
К- М. Ольшановой был использован принцип осадочной хроматографии в систематическом хроматографическом качественном анализе неорганических веществ [5]. Ею совместно с Н. М. Морозовой был разработан осадочно-хрома-тографический метод для обнаружения церия, индия, таллия и других редких элементов с использованием различных неорганических и органических осадителей [44]. [c.66]
Расплавы Nh5h3PO2 использованы для качественного обнаружения кобальта, титана, молибдена, вольфрама, хрома, ванадия и урана 16.198]. [c.290]
Статья Ловица посвящена хрому вернее — установлению присутствия хрома в минералах, найденных на Урале 2. В первый раз (в 179 8 г.) Ловиц открыл хром в хромистом железняке и в свинцовой красной руде. В данной же статье он указывал на наличие хрома и в других минералах, содержащих соединение хромиевой кислоты сверх железа, также и с марганцем . Вероятно, это были хромистые железняки с примесями пиролюзита, поскольку они не разнились особенно по внещним признакам от обычного хромистого железняка. Ловица, таким образом, прежде всего интересовало изучение минералов с точки зрения содержания в них хрома, а не химия хрома. Впрочем, это был интерес всеобщий. И А. А. Мусин-Пушкин, и В. М. Севергин также интересовались хромовыми рудами и методами их испытаний. В частности, А. А. Мусину-Пушкину принадлежит метод химического испытания хромистых руд описываемый Ловицем в его статье. В усовершенствованном Ловицем виде метод этот состоял в сплавлении измельченной в порошок руды с селитрой и выщелачиванием образовавшегося хромата натрия. Ловиц дал в статье важнейшие качественные реакции на хром действие на соли хромовой кислоты уксуснокислого свинца и азотнокислого серебра. Помимо этого он привел ряд указаний относительно открытия хрома в рудах химическим путем в присутствии других элементов, в частности железа и марганца, а также описал меры предосторожности при обнаружении хрома в случае, если он присутствует лишь в малых количествах. [c.470]
Для определения хрома масс-спектральным методом используют главным образом приборы, в которых ионы получаются путем электронного удара и искрового разряда. Первые обычно используют в сочетании с предварительным концентрированием хрома в виде летучих соединений. Так, при анализе нержавеющей стали с использованием прибора с двойной фокусировкой типа МС-9 из анализируемой пробы выделяют хром в виде гексафторацетила-цетоната хрома(1П) [629]. Предел обнаружения 0,05 нг Сг. 8-Окси-хинолинат хрома(П1) применяют для определения нанограммовых количеств хрома [923] качественно этим методом можно определить 5-10" 3 хрома. Метод определения хрома в лунных образцах и геологических материалах включает процесс превращения. Сг (III) в летучий хелат по реакции с 1,1,1-трифторпентандио-ном-2,4 в запаянной трубке, экстракцию его гексаном и последующий анализ паров экстракта методом изотопного разбавления на масс-спектрометре [736]. Погрешность метода — 1 отн.%. [c.98]
В тех случаях-, когда в качестве главных компонентов анализируемого образца определяют мало распространенные элементы, такие, как серебро, золото, никель, кобальт, хром, которые обычно находятся в используемых чистых реактивах в пренебрежимо малых концентрациях, проведение холостой пробы не обязательно. Однако, если цель качественного анализа —обнаружение следов некоторых компонентов в анализируемом объекте, и для этого используют особенно чувствительные реакции и методы, то холостай проба обязательна. [c.183]
При анализе раствора, содержащего смесь ионов AF, Сг , Zv , обнаружению катионов алюминия дробным методом мешают ионы цинка и хрома (П1). Поэтому на первом этапе дробного анализа необходимо удалить мешающие ионы, в данном случае, связать в комплекс ионы цинка, добавив в раствор гексацианоферрат (П) калия KJFe( N)g], а катионы Сг окислить до СгО " действием пероксида водорода HjOj в щелочной среде. Затем, на втором этапе, уже можно обнаружить ионы алюминия качественной реакцией с ализарином. [c.157]
Согласно литературным данным [4—6], хромоникелевая шпинель не может быть стабильной в сплавах с высоким содержанием хрома, и диффундирующий через окалину хром восстанавливает окись никеля до металлического никеля, что термодинамически вполне возможно, так как свободная энергия образования окиси никеля равна 51,3 ккал1г-ат, а окиси хрома 83,5 ккал1г-ат [7]. В результате окалина состоит из окиси хрома, легированной никелем, присутствие которого в окалине обнаружено качественным спектральным анализом для всех сплавов. При исследовании окалины мнкрорентгеноспектральным методом установлено присутствие в ней титана и ниобия. Вольфрам в окалине не обнаружен. [c.47]
chem21.info
Качественные реакции неорганической химии. Качественные реакции на катионы
 С этим файлом связано 7 файл(ов). Среди них: Povrezhdenia_glaz__khimicheskiy_ozhog.pdf, Biokhimia_v_skhemakh_i_tablitsakh.pdf, Качественные реакции неорганической химии.doc, БИОХИМИЧЕСКИЙ АНАЛИЗ КРОВИ норма.docx, voprosy_k_ekzamenu_po_neorganicheskoy_khimii.pdf.
С этим файлом связано 7 файл(ов). Среди них: Povrezhdenia_glaz__khimicheskiy_ozhog.pdf, Biokhimia_v_skhemakh_i_tablitsakh.pdf, Качественные реакции неорганической химии.doc, БИОХИМИЧЕСКИЙ АНАЛИЗ КРОВИ норма.docx, voprosy_k_ekzamenu_po_neorganicheskoy_khimii.pdf. Показать все связанные файлы
Показать все связанные файлы Качественные реакции неорганической химии.
1. Качественные реакции на катионы.
1.1.1 Качественные реакции на катионы щелочных металлов (Li+, Na+, K+, Rb+, Cs+). На катионы щелочных металлов возможно провести только с сухими солями, т.к. практически все соли щелочных металлов растворимы (исключением являются Li3PO4, LiF, Li2SiO3, KClO4, RbClO4, CsClO4). Обнаружить их можно, внеся небольшое количество соли в пламя горелки. Тот или иной катион окрашивает пламя в соответствующий цвет:Li+ - темно-розовый.Na+ - желтый.K+ - фиолетовый.Rb+ - красный.Cs+ - голубой.
Как уже отмечалось ранее, катион лития Li+ можно выявить и другим путем. При сливании раствора соли лития с фосфатами, фторидами или силикатами образуются соответствующие осадки:3Li+ + PO43- -----> Li3PO4↓ Li+ + F- ----> LiF↓2Li+ + SiO32- ------> Li2SiO3↓ Осадить ионы K+, Rb+, Cs+ можно перхлорат-анионом ClO4-.Me+ + ClO4- -----> MeClO4↓ (Me = K, Rb, Cs) Но я бы не советовал ее использовать при написании самостоятельных, контрольных и т.п. работ, более эффективен метод, изложенный выше.
1.1.2 Качественные реакции на катионы щелочно-земельных металлов (Ca2+, Sr2+, Ba2+. Ra2+ рассматривать не будем.). Катионы щелочно-земельных металлов, в отличии от катионов щелочных, можно выявить двумя способами: в растворе и по окраске пламени. Кстати, к щелочно-земельным относятся кальций, стронций, барий и радий. Бериллий и магний нельзя отнести к этой группе, как это любят делать на просторах Интернета.Окраска пламени:Ca2+ - кирпично-красный.Sr2+ - карминово-красный.Ba2+ - желтовато-зеленый.
Реакции в растворах. Катионы рассматриваемых металлов имеют общую особенность: их карбонаты и сульфаты нерастворимы. Катионы кальция обычно выявляют карбонат-анионом:Ca2+ + CO32- ------> CaCO3↓Который легко растворяется в азотной кислоте с выделением углекислого газа:2H+ + CO32- -------> h3O + CO2↑Катионы бария и стронция предпочитают выявлять сульфат-анионом с образованием сульфатов, нерастворимых в конц. азотной кислоте:Sr2+ + SO42- ------> SrSO4↓Ba2+ + SO42- ------> BaSO4↓
1.1.3. Качественные реакции на катионы свинца Pb2+, серебра Ag+, ртути (I) Hg2+, ртути (II) Hg2+. Рассмотрим их на примере свинца и серебра.Эта группу катионов объединяет одна общая особенность: они образуют нерастворимые хлориды. Но катионы свинца и серебра можно выявить и другими галогенидами.
Качественная реакция на катион свинца - образование хлорида свинца (осадок белого цвета), либо образование иодида свинца (осадок ярко желтого цвета):Pb2+ + 2I- -------> PbI2↓
Качественная реакция на катион серебра - образование белого творожистого осадка хлорида серебра, желтовато-белого осадка бромида серебра, образование желтого осадка иодида серебра:Ag+ + Cl- ------> AgCl↓ Ag+ + Br- ------> AgBr↓ Ag+ + I- ------> AgI↓ Как видно из выше изложенных реакций, галогениды серебра (кроме фторида) нерастворимы, а бромид и иодид даже имеют окраску. Но отличительная черта их не в этом. Данные соединения разлагаются на свету на серебро и соответствующий галоген, что также помогает их идентифицировать. Также при добавлении к данным осадкам тиосульфата натрия они растворяются:AgHal + 2Na2S2O3 -------> Na3[Ag(S2O3)2] + NaHal, (Hal = Cl, Br, I).То же самое произойдет при добавлении аммиака:AgHal + 2Nh4 -----> [Ag(Nh4)2]Hal
Существует также еще одна качественная реакция на катион серебра - образование оксида серебра черного цвета при добавлении щелочи:2Ag+ + 2OH- -----> Ag2O↓ + h3OЭто связано с тем, что гидроксид серебра при нормальных условиях не существует и сразу же распадается на оксид и воду.
1.1.4. Качественная реакция на катионы алюминия Al3+, хрома (III) Cr3+, цинка Zn2+, олова (II) Sn2+.Данные катионы объединены образованием нерастворимых оснований, легко переводимых в комплексные соединения. Групповой реагент - щелочь.Al3+ + 3OH- -------> Al(OH)3 + 3OH- -------->[Al(OH)6]3-Cr3+ + 3OH- ------> Cr(OH)3 + 3OH- ------->[Cr(OH)6]3-Zn2+ + 2OH- ------> Zn(OH)2 + 2OH- ------>[Zn(OH)4]2-Sn2+ + 2OH- -------> Sn(OH)2 + 2OH- ------->[Sn(OH)4]2-
Раствор, содержащий [Cr(OH)6]3-, при добавлении бромной воды в щелочной среде становится желтым из-за образования хромат-аниона CrO42-:2[Cr(OH)6]3- + 3Br2 + 4OH- -----> 2CrO42- + 6Br- + 8h3O
1.1.5. Качественная реакция на катионы железа Fe2+, Fe3+.
Данные катионы также образуют нерастворимые основания. Иону Fe2+ отвечает нерастворимый осадок белого (на воздухе зеленого) цвета - гидроксида железа (II) Fe(OH)2, катиону Fe3+ отвечает метагидроксид железа (III) FeO(OH) бурого цвета. Но для избежания недорозумений советую писать гидроксид Fe(OH)3.Качественная реакция на Fe2+:
Fe2+ + 2OH- -----> Fe(OH)2↓Fe(OH)2 будучи соединением двухвалентного железа на воздухе неустойчиво и постепенно переходит в метагидроксид железа (III).4Fe(OH)2 + O2 -----> 4FeO(OH)↓ + 2h3O
Качественная реакция на Fe3+:Fe3+ + 3OH- -----> FeO(OH)↓ + h3O
Еще одной качественной реакцией на Fe3+ является взаимодействие с роданид-анионом, образуя роданид железа темно-красного цвета (III) (эффект "крови"):Fe3+ + 3SCN- ------> Fe(SCN)3Полученный роданид легко разрушается фторидами:Fe(SCN)3 + 6NaF -----> Na3[FeF6] + 3NaSCNОчень чувствительная реакция на Fe3+, помогает обнаружить даже очень незначительные следы данного катиона.
1.1.6. Качественная реакция на катион марганца (II) Mn2+. Данная реакция основана на жестком окислении марганца в кислой среде с изменением степени окисления с +2 до +7. При этом раствор окрашивается в темно-фиолетовый цвет из-за появления перманганат-аниона. Рассмотрим на примере нитрата марганца (II):2Mn(NO3)2 + 5PbO2 + 6HNO3 ------> 2HMnO4 + 5Pb(NO3)2 + 2h3O
1.1.7. Качественная реакция на катионы меди Cu2+, кобальта Co2+ и никеля Ni2+.Особенность этих катионов в том, что их соли растворяются в аммиаке с образованием комплексных солей - аммиакатов:Cu2+ + 4Nh4 -------> [Cu(Nh4)4]2+Аммиакаты окрашивают растворы в яркие цвета, к примеру аммиакат меди окрашивает раствор в ярко-синий цвет.
1.1.8. Качественные реакции на катион аммония Nh5+.Взаимодействие солей аммония с щелочами при небольшой температуре:Nh5+ + OH- ---t---> Nh4↑ + h3OВлажная лакмусовая бумажка, поднесенная к току аммиака, окрасится в синий цвет.На этом я закончу описание выявления катионов. Теперь рассмотрим качественные реакции на некоторые анионы.
2. Качественные реакции на анионы.2.1.1. Качественные реакции на сульфид-анион S2-. Из сульфидов растворимы сульфиды только щелочных металлов. Нерастворимые сульфиды имеют специфическую окраску, по которым можно определить тот или иной сульфид.Осаждаются сульфиды марганца Mn2+, Pb2+, Zn2+, Ag+, Cd2+, Sn2+ и некоторых других.Окраска:MnS - телесный (розовый).ZnS - белый.PbS - черный.AgS - черный.CdS - лимонно-желтый.SnS - шоколадный.Сульфиды переводятся в раствор сильными кислотами (HNO3).Также сульфид-анион можно выявить, приливая раствор сульфида к бромной воде:S2- + Br2 ------> S↓ + 2Br-Образующаяся сера выпадает в осадок.
2.1.2. Качественная реакция на сульфат-анион SO42-.Сульфат-анион обычно осаждают катионом свинца, либо бария:Pb2+ + SO42- ------> PbSO4↓Осадок сульфата свинца белого цвета.
2.1.3.Качественная реакция на силикат-анион SiO32-. Силикат-анион легко осаждается из раствора в виде стекловидной массы при добавлении сильных кислот.SiO32- + 2H+ -----> h3SiO3↓ (SiO2 * nh3O)
2.1.4. Качественные реакции на хлорид-анион Cl-, бромид-анион Br-, иодид-анион I- смотрите в пункте "качественные реакции на катион серебра Ag+".
2.1.5. Качественная реакция на сульфит-анион SO32-. При добавлении к раствору сильных кислот образуется диоксид серы SO2 с резким запахом (запах подожженной спички):SO32- + 2H+ -----> SO2↑ + h3O
2.1.6. Качественная реакция на карбонат-анион CO32-.При добавлении к раствору карбоната сильных кислот образуется углекислый газ CO2, гасящий горящую лучинку:CO32- + 2H+ -----> CO2↑ + h3O
2.1.7. Качественная реакция на тиосульфат-анион S2O32-. При добавлении конц. серной или соляной кислоты к раствору тиосульфата образуется диоксид серы SO2 и выпадает в осадок сера S:S2O32- + 2H+ -----> S↓ + SO2↑ + h3O
2.1.8. Качественная реакция на хромат-анион CrO42-. При добавлении к раствору хромата раствор солей бария выпадает желтый осадок хромата бария BaCrO4, разлагающегося в сильнокислой среде:Ba2+ + CrO42- ----> BaCrO4↓ Растворы хроматов окрашены в желтый цвет. При подкислении раствора цвет изменится на оранжевый, отвечающий дихромат-аниону Cr2O72-:2CrO42- + 2H+ -----> Cr2O72- + h3O
2.1.9. Качественная реакция на дихромат-анион Cr2O72-.При добавлении к раствору дихромата раствор соли серебра образуется осадок оранжевого цвета Ag2Cr2O7:2Ag+ + Cr2O72- -----> Ag2Cr2O7↓ Растворы дихроматов окрашены в оранжевый цвет. При подщелачивании раствора окраска изменяется на желтую, отвечающая хромат-аниону CrO42-:Cr2O72- + 2OH- -----> 2CrO42- + h3OКроме того, дихроматы - сильные окислители в кислой среде. При внесении в раствор дихромата какой-либо восстановитель окраска раствора изменится с оранжевого на зеленый, отвечающей катиону хрома (III) Сr3+(На примере иодидов):6I- + Cr2O72- + 14H+ ------> 3I2 + 2Cr3+ + 7h3OЭффектной качественной реакцией на шестивалентный хром - темно-синее окрашивание раствора при добавлении конц. перекиси водорода в эфире. Образуется пероксид хрома состава CrO5.
2.2.0. Качественная реакция на перманганат-анион MnO4-. Перманганат-анион "выдает" темно-фиолетовая окраска раствора. Кроме того, перманганаты - сильнейшие окислители, в кислой среде восстанавливаются до Mn2+ (фиолетовая окраска исчезает), в нейтральной до Mn+4 (окраска исчезает, выпадает бурый осадок диоксида марганца MnO2) и в щелочной до MnO42- (окраска раствора изменяется на темно-зеленый).
2.2.1. Качественная реакция на манганат-анион MnO42-. При подкислении раствора манганата темно-зеленая окраска изменяется на темно-фиолетовую, отвечающую перманганат-аниону MnO4-:3K2MnO4 + 4HCl(разб.) -----> MnO2↓ + 2KMnO4 + 4KCl + 2h3O
2.2.2.Качественная реакция на фосфат-анион PO43-. При добавлении к раствору фосфата раствор соли серебра выпадает желтый осадок фосфата серебра (I) Ag3PO4:3Ag+ + PO43- -----> Ag3PO4↓ Аналогична реакция и к дигидрофосфат-аниону h3PO4-.
2.2.3. Качественная реакция на феррат-анион FeO42-.Осаждение из раствора феррата бария красного цвета:Ba2+ + FeO42- ----> BaFeO4↓
2.2.4. Качественная реакция на нитрат-анион NO3-. Подкисленный раствор нитратов обладает окислительными свойствами подобно азотной кислоте. К примеру, смесь растворов нитрата калия и серной кислоты реагирует с медью:3Cu + 2KNO3 + 4h3SO4 -----> 3CuSO4 + K2SO4 + 2NO↑ + 4h3OОксид азота (II) NO буреет на воздухе.
Вот основные качественные реакции на анионы. Далее мы рассмотрим качественные реакции на простые и сложные вещества.
3.Качественные реакции на простые и сложные вещества. Некоторые сложные вещества, как и ионы, обнаруживаются качественными реакциями. Ниже я опишу качественные реакции некоторых веществ.3.1.0.Качественная реакция на водород h3. "Лающий" хлопок при поднесении горящей лучинки к источнику водорода.
3.1.1. Качественная реакция на кислород O2. Яркое загорание тлеющей лучинки в атмосфере кислорода.
3.1.2. Качественная реакция на озон O3. Взаимодействие озона с раствором иодидов с выпадением кристаллического I2иода в осадок:2KI + O3 + h3O -----> 2KOH + I2↓ + O2↑ В отличии от озона кислород в данную реакцию не вступает.
3.1.3. Качественная реакция на хлор Cl2. Взаимодействие недостатка хлора с растворами иодидов:2KI + Cl2 ----> 2KCl + I2↓ В результате реакции в осадок выпадает иод I2.При избытке хлора реакций пойдет дальше - иод растворится с образованием иодноватой кислоты HIO3:I2 + 5Cl2 + 6h3O ------> 2HIO3 + 10HCl
3.1.4. Качественные реакции на аммиак Nh4.Взаимодействие аммиака с газообразным хлороводородом с образованием белых кристалликов хлорида аммония ("дым" без огня):Nh4 + HCl ----> Nh5Cl Примечание: следующие реакции не дают в школьном курсе. Однако, это самые надежные качественные реакции на аммиак.Почернение бумажки, смоченной в растворе соли ртути (I) Hg2+. Подробно рассмотрим реакцию:Hg2Cl2 + 2Nh4 -----> Hg(Nh3)Cl↓ + Hg↓ + Nh5ClБумажка чернеет из-за выделения мелкодисперсной ртути.
Взаимодействие аммиака с щелочным раствором тетраиодомеркурата (II) калия (реактив Несслера):2K2[HgI4] + Nh4 + 3KOH ------> [O(Hg)2Nh3]I↓ + 7KI + 2h3OКомплекс [O(Hg)2Nh3]I коричневого цвета (цвет ржавчины) выпадает в осадок.Две последние реакции являются самыми надежными на аммиак.
3.1.5. Качественная реакция на фосген COCl2. Испускание белого "дыма" от бумажки, смоченного в растворе аммиака:COCl2 + 4Nh4 -----> (Nh3)2CO + 2Nh5Cl
3.1.6. Качественная реакция на угарный газ CO. Помутнение раствора при пропускании угарного газа в раствор хлорида палладия (II):PdCl2 + CO + h3O -----> CO2↑ + 2HCl + Pd↓
3.1.7. Качественная реакция на углекислый газ CO2.Тушение тлеющей лучинки в атмосфере углекислого газа.При пропускании через раствор известкового молока Ca(OH)2 образуется осадок, растворяющийся при дальнейшем пропускании газа:Ca(OH)2 + CO2 --------> CaCO3↓ + h3OCaCO3 + CO2 + h3O -------> Ca(HCO3)2
3.1.8. Качественная реакция на оксид азота (II) NO.Оксид азота (II) очень чувствителен к кислороду воздуха, потому на воздухе буреет, окисляясь до оксида азота (IV):2NO + O2 ----> 2NO2
Качественные реакции органической химии.
18.01.2012 19:16 | Обновлено 22.05.2012 12:14 | Автор: Avetik | | |
В этой статье я опишу некоторые качественные реакции органических соединений. Их огромное количество, ведь органических соединений гораздо больше: свыше 27 000 000 органических на 500 000 неорганических. Разница очевидна.
В органической химии качественные реакции определяют преимущественно вещества, а если быть точнее, то представителей класса веществ (алканы, алкены и т.д.).
1. Качественная реакция на алканы. Определить, что какое-то вещество в смеси или в чистом виде алкан, несложно. Для этого газ либо поджигают - горение алканов сопровождается синим пламенем, либо пропускают через раствор перманганата калия. Алканы не окисляются перманганатом калия на холоду, вследствие этого раствор не будет изменять окраску.
2. Качественная реакция на алкены. Чтобы убедиться в наличии алкена, нужно пропустить его в раствор перманганата калия (реакция Вагнера). В ходе реакции раствор обесцветится, выпадает бурый диоксид марганца MnO2 (реакция на примере этилена):3C2h5 + 2KMnO4 + 4h3O ------> 3Ch3OH-Ch3OH + 2KOH + 2MnO2↓
Так же, алкены обесцвечивают бромную воду:C2h5 + Br2 -----> C2h5Br2Бромная вода обесцвечивается, образуется дибромпроизводное.
3. Качественная реакция на алкины. Алкины можно выявить и по реакции Вагнера или с помощью бромной воды:
3C2h3 + 8KMnO4 -----> 3KOOC-COOK + 8MnO2↓ + 2KOH + 2h3OC2h3 + 2Br2 ----> C2h3Br4
Алкины с "наружной" тройной связью реагируют с аммиачным раствором оксида серебра (гидроксид диаминсеребра (I))(реактив Толленса):C2h3 + 2[Ag(Nh4)2]OH -------> Ag2C2↓ + 4Nh4↑ + 2h3O
Получившийся ацетиленид серебра (I) выпадает в осадок.Данная качественная реакция действует только на алкины с "наружной" тройной связью. Алкины, у которых тройная связь в середине (R-C-=C-R) в эту реакцию не вступают.
Такая способность алкинов замещать протон на атом металла, подобно кислотам, обусловлено тем, что атом углерода находится в состоянии sp-гибридизации и электроотрицательность атома углерода в таком состоянии такая же, как у азота. В следствии этого, атом углерода сильнее обогощается электронной плотностью и протон становится подвижным.
4. Качественная реакция на альдегиды. Одна из самых интересных качественных реакций в органической химии - на альдегиды, предназначена исключительно для выявления соединений, содержащих альдегидную группу. К альдегиду приливают аммиачный раствор оксида серебра, реакция идет при нагревании:Ch4-CHO + 2[Ag(Nh4)2]OH ---t--> Ch4-COOH + 2Ag↓ + 4Nh4↑ + h3O Если опыт проведен грамотно, то выделяющееся серебро покрывает колбу ровным слоем, создавая эффект зеркала. Именно поэтому реакция называется реакцией серебряного зеркала.Примечание: реакцией серебряного зеркала также можно выявить метановую (муравьиную) кислоту HCOOH. При чем тут кислота, если мы говорим про альдегиды? Все просто: муравьиная кислота - единственная из карбоновых кислот, содержащая одновременно альдегидную и карбоксильную группы:
В ходе реакции метановая кислота окисляется до угольной, которая разлагается на углекислый газ и воду:HCOOH + 2[Ag(Nh4)2]OH ---t--> CO2↑ + 2h3O + 4Nh4↑ + 2Ag↓
Помимо реакции серебряного зеркала существует также реакция с гидроксидом меди (II) Cu(OH)2. Для этого свежеприготовленному гидроксиду меди (II) добавляют альдегид и нагревают смесь:CuSO4 + 2NaOH -----> Na2SO4 + Cu(OH)2↓ Ch4-CHO + 2Cu(OH)2 ---t---> Ch4-COOH + Cu2O↓ + 2h3OВыпадает оксид меди (I) Cu2O - осадок красного цвета.
Еще один метод определения альдегидов - реакция с щелочным раствором тетраиодомеркурата (II) калия, известный нам из предыдущей статьи как реактив Несслера:Ch4-CHO + K2[HgI4] + 3KOH ------> Ch4-COOK + Hg↓ + 4KI + 2h3O
При добавлении альдегида к раствору фуксинсернистой кислоты раствор окрашивается в светло-фиолетовый цвет.
5. Качественные реакции на спирты. Спирты по количеству гидроксильных групп бывают одно-, двух-, многоатомными. Для одно- и многоатомных реакции различны.Качественные реакции на одноатомные спирты:Простейшая качественная реакция на спирты - окисление спирта оксидом меди. Для этого пары спирта пропускают над раскаленным оксидом меди. Затем полученный альдегид улавливают фуксинсернистой кислотой, раствор становится фиолетовым:Ch4-Ch3-OH + CuO --t--> Ch4-CHO + Cu + h3O
Спирты идентифицируются пробой Лукаса - конц. раствор соляной кислоты и хлорида цинка. При пропускании вторичного или третичного спирта в такой раствор образуется маслянистый осадок соответствующего алкилхлорида:Ch4-CHOH-Ch4 + HCl --ZnCl2--> Ch4-CHCl-Ch4 + h3OПервичные спирты в реакцию не вступают.
Еще одним известным методом является иодоформная проба:Ch4-Ch3-OH + 4I2 + 6NaOH ------> CHI3↓ + 5NaI + HCOONa + 5h3O
Качественные реакции на многоатомные спирты.Наиболее известная качественная реакция на многоатомные спирты - взаимодействие их с гидроксидом меди (II). Гидроксид растворяется, образуется хелатный комплекс темно-синего цвета. Обратите внимание на то, что в отличии от альдегидов многоатомные спирты реагируют с гидроксидом меди (II) без нагревания.
2Ch3OH-Ch3OH + Cu(OH)2 ------>Ch3OH--- −Oh3C______Cu_____ Ch3O− ---HOh3C
6. Качественные реакции на карбоновые кислоты. На карбоновые кислоты обычно подчеркивают образование цветных осадков с тяжелыми металлами. Но наиболее осуществимая качественная реакция на метановую кислоту HCOOH. При добавлении концентрированной серной кислоты h3SO4 к раствору муравьиной кислоты образуется угарный газ и вода:HCOOH --h3SO4---> CO↑ + h3OУгарный газ можно поджечь. Горит синем пламенем:
2CO + O2 --t--> 2CO2
Из многоосновных кислот рассмотрим качественную реакцию на щавелевую. При добавлении к раствору щавелевой кислоты раствор соли меди (II) выпадет осадок оксалата меди (II):Cu2+ + C2O42- -----> CuC2O4↓
Щавелевая кислота также, как и муравьиная, разлагается концентрированной серной кислотой:h3C2O4 ----h3SO4---> CO↑ + CO2↑ + h3O
7. Качественные реакции на амины. На амины качественных реакций нет (за исключением анилина). Можно доказать наличие амина окрашиванием лакмуса в синий цвет. Если же амины нельзя выявить, то можно различить первичный амин от вторичного путем взаимодействия с азотистой кислотой HNO2. Для начала нужно ее приготовить, а затем добавить амин:NaNO2 + HCl -----> NaCl + HNO2Первичные дают азот N2:Ch4-Nh3 + HNO2 ------> Ch4-OH + N2↑ + h3O
Вторичные - алкилнитрозоамины - вещества с резким запахом (на примере диметилнитрозоамина):Ch4-NH-Ch4 + HNO2 -----> Ch4-N(NO)-Ch4 + h3O
Анилин образует осадок при добавлении бромной воды:C6H5Nh3 + 3Br2 ------> C6h3Nh3(Br)3↓ + 3HBr
Анилин C6H5Nh3 можно обнаружить по сиреневой окраске при добавлении хлорной извести.
8. Качественные реакции на фенол. Фенол лучше всегообнаруживает хлорид железа (III) - образуется фиолетовое окрашивание раствора. Этот лучший метод обнаружения фенола, т.к. реакция очень чувствительна.
Также фенол наряду с анилином дает осадок желтоватого цвета при пропускании в водный раствор брома - 2,4,6 - трибромфенол:C6H5OH + 3Br2 ------> C6h3OH(Br)3↓ + 3HBr
Фенолы дают фенол-альдегидные смолы при реакции фенола с альдегидом в кислой среде. При этом образуется мягкие пористые массы фенол-альдегидных смол (реакция поликонденсации).
9. Качественная реакция на алкилхлориды. Вещества, содержащие хлор, могут окрашивать пламя в зеленый цвет. Для этого нужно обмакнуть медную проволоку в алкилхлориде и поднести к пламени (проба Бельштейна).
10. Качественная реакция на углеводы. Большинство углеводов имеют альдегидные и гидроксильные группы, поэтому для них характерны все реакции альдегидов и многоатомных спиртов. Существует способ, который помогает различить глюкозу от фруктозы. Этот способ носит название проба Селиванова. Для того, чтобы различить эти углеводы, к ним приливают смесь резорцина и соляной кислоты. Реагирует со смесью фруктоза, при этом раствор окрашивается в малиновый цвет.
Крахмал в присутствии иода окрашивается в темно-синий цвет. При нагревании окраска исчезает, при охлаждении появляется вновь.
11. Качественная реакция на белки. Белки выявляются в основном на реакциях, основанные на окрасках.Ксантопротеиновая реакция. Данная реакция обнаруживает ароматические аминокислоты, входящие в белки (на примере тирозина):(OH)C6h5CH(Nh3)COOH + HNO3 ----h3SO4-----> (OH)C6h4(NO2)CH(Nh3)COOH↓ + h3O - выпал осадок желтого цвета.(OH)C6h4(NO2)CH(Nh3)COOH + 2NaOH -------> (ONa)C6h4(NO2)CH(Nh3)COONa + h3O - раствор становится оранжевым.
Обнаружение серосодержащих аминокислот:Белок + (Ch4COO)2Pb ---NaOH---> PbS↓ (осадок черного цвета).
Биуретовая реакция для обнаружения пептидной связи (CO-NH):Белок + CuSO4 + NaOH -----> красно-фиолетовое окрашивание.
Спецефический запах при горении:Белок ----обжиг----> запах паленой шерсти перейти в каталог файлов
перейти в каталог файлов
uhimik.ru
Открытие - хром - Большая Энциклопедия Нефти и Газа, статья, страница 3
Открытие - хром
Cтраница 3
Можно проделать более чувствительную реакцию на хром. К сухому остатку прибавляют несколько кристаллов KNO3 и безводного Na2CO3 - Прокаливают до полного сплавления смеси и, не прекращая нагревания, выдерживают ее в жидком состоянии 3 - 5 мин. Желтый цвет сплава не служит еще достаточным признаком для открытия хрома. Поэтому испытывают сплав на содержание в нем хромата, растворяя его в горячей воде. В присутствии хрома выпадает кирпично-красный осадок хромата серебра. [31]
Присутствие Pb, Pt, Se, Те, Fe, U, Th, Co увеличивает предел обнаружения хрома. Ионы Sn ( II), Ce ( IV) мешают открытию хрома. [32]
Из всех исчисленных элементов наиболее распространен в природе и часто применяется в практике хром. В соединениях того и другого рода хром встречается в природе, хотя довольно редко. Уральская красная хромовая руда или хро-мовосвинцовая соль ( крокоизит) РЬСгО1 была для Вокелена источником для открытия хрома, которому он ридал его название ( от греческого слова - крашу) по причине ярких цветов, свойственных соединениям этого элемента; соли СЮа желтого и красного, СгЮ3 зеленого и фиолетового цветов. Малые ее количества составляют красящее начало многих минералов и горных пород, пр. [33]
Обнаружение рассматриваемых ионов редких элементов в предварительных испытаниях не всегда возможно, что заставляет их открывать из смеси, главным образом дробным путем. Сами ионы редких элементов несколько влияют на открытие других катионов 3 - й группы. Fe действием K4 [ Fe ( CN) e ]; в присутствии больших количеств Се видоизменяется внешний эффект при открытии Мп действием РЬО2, для открытия хрома трилоном Б необходим очень большой избыток реактива; перед открытием алюминия из раствора алюмината следует проверять полноту отделения циркония. [34]
Обнаружение рассматриваемых ионов редких элементов в предварительных испытаниях не всегда возможно, что заставляет их открывать из смеси, главным образом дробным путем. Сами ионы редких элементов несколько влияют на открытие других катионов 3 - й группы. Так, например, ион UO2 мешает открытию Fe действием K4fFe ( CN) e ]; в присутствии больших количеств Се видоизменяется внешний эффект при открытии Мп действием РЬО2, для открытия хрома трилоном Б необходим очень большой избыток реактива; перед открытием алюминия из раствора алюмината следует проверять полноту отделения циркония. [35]
Техника реакций растирания весьма проста: крупинка испытуемого вещества и 1 - 2 кристаллика реактива кладутся рядом в кюветку и слабо растираются пестиком в течение 1 - 3 секунд, после чего наблюдают цвет смеси. Только для небольшого числа реакций ( никель с диаметилглиоксимом, железо с форроцианидом калия и некоторые другие) требуется более сильное растирание. Иногда, для усиления яркости окраски, смесь полезно увлажнить дыханием. Изредка, например, при открытии хрома в виде его фосфата растертая смесь слабо подогревается. [36]
Можно проделать более чувствительную реакцию на хром. К сухому остатку прибавляют несколько кристаллов КЖ) 3 и безводного Na. Прокаливают до полного сплавления смеси и, не прекращая нагревания, выдерживают ее в жидком состоянии 3 - 5 мин. Желтый цвет сплава не служит еще достаточным признаком для открытия хрома. Поэтому испытывают сплав на содержание в нем хромата, растворяя его в горячей воде. В присутствии хрома выпадает кирпично-красный осадок хромата серебра. [37]
Вокелен, изучая эту руду, обнаружил в ней наличие неизвестного металла, названного им хромом в связи с тем, что этот металл дает окрашенные соли, и выделил сам металл. Сообщение Вокелена об открытии хрома было опубликовано только в 1798 г. ( Ann. Петербурге не ранее 1799 г. Между тем из вышеприведенных данных следует, что Ловиц в 1798 г. уже изучил полученный от А. А. Мусина-Пушкина образец красной свинцовой руды, в коем открыл... Ловицу, таким образом, принадлежит несомненное соавторство в открытии хрома. [38]
Из истории открытия хрома, обычно описываемой в литературе, мы знаем, что Вокален в 1797 г. при исследовании красной сибирской свинцовой руды, полученной из России, открыл в ней новый металл - хром. Ловиц мог узнать об открытии Вокелена не ранее как в середине 1798 г. Таким образом, слова Ловица в коем открыл я в первый раз неизвестный до тех пор металл хромий свидетельствуют о том, что он произвел это открытие независимо от Вокелена. Ловиц был весьма осторожен при публикации своих сообщений и никогда не высказывал необоснованных и малодоказательных утверждений. С другой стороны, необычайная скромность Ловица3, очевидно, явилась причиной того, что он не выступил в защиту своего соавторства в открытии хрома. Невидимому, этим и объясняется, что Ловиц своевременно не сообщил в печати о своем открытии. [39]
Реакция применяется для дробного открытия иона Zn в присутствии других катионов и, в частности, всех катионов III группы. Не отнимайте от нее кончик капилляра до тех пор, пока вокруг осадка не появится водянистая зона шириной в несколько миллиметров. Если ион Zn отсутствует, образуется кольцо оранжевого цвета, свойственного дитизону в щелочной среде. Реакцию удобно комбинировать с открытием хрома капельной реакцией с бензидином, описанной на стр. [40]
Реакция применяется для дробного открытия иона Zn в присутствии других катионов, и в частности, всех катионов III группы. Не отнимайте от нее кончик капилляра до тех пор, пока вокруг осадка не появится водянистая зона шириной в несколько миллиметров. Если ион 2п отсутствует, образуется кольцо оранжевого цвета, свойственного дитизону в щелочной среде. Реакцию удобно комбинировать с открытием хрома капельной реакцией с бензи-дином, описанной на стр. [41]
В первый раз ( в 179 8 г.) Ловиц открыл хром в хромистом железняке и в свинцовой красной руде. Вероятно, это были хромистые железняки с примесями пиролюзита, поскольку они не разнились особенно по внешним признакам от обычного хромистого железняка. Ловица, таким образом, прежде всего интересовало изучение минералов с точки зрения содержания в них хрома, а не химия хрома. Впрочем, это был интерес всеобщий. Мусин-Пушкин, и В. М. Севергин также интересовались хромовыми рудами и методами их испытаний. В частности, А. А. Мусину-Пушкину принадлежит метод химического испытания хромистых руд 3, описываемый Ловицем в его статье. Ловиц дал в статье важнейшие качественные реакции на хром: действие на соли хромовой кислоты уксуснокислого свинца и азотнокислого серебра. Помимо этого он привел ряд указаний относительно открытия хрома в рудах химическим путем в присутствии других элементов, в частности железа и марганца, а также описал меры предосторожности при обнаружении хрома в случае, если он присутствует лишь в малых количествах. [42]
Страницы: 1 2 3
www.ngpedia.ru
Реакции катиона хрома Сг - Справочник химика 21
АНАЛИТИЧЕСКИЕ РЕАКЦИИ КАТИОНОВ ТРЕТЬЕЙ ГРУППЫ (ионы алюминия, хрома, железа, марганца и цинка) [c.94]Предварнтельные испытания. Открытие катионов алюминия А1 . Катионы алюминия открывают капельным методом реакцией с ализарином. Открытию катионов алюминия с помощью этой реакции мешают катионы хрома, цинка, олова. Поэтому капельную реакцию с ализарином обычно проводят на фильтровальной бумаге, щюпитанной раствором гексацианоферрата(И) калия K4[Fe( N)6]. Мешающие катионы связываются в соответствующие малорастворимые гексацианоферраты(П) и образуют на бумаге темное пятно, а катионы алюминия перемещаются с водным раствором к периферии пятна, где при последующей реакции с 328 [c.328]
Реакции катионов хрома [c.90]Реакции катиона хрома [c.123]
Реакции катиона хрома Сг + [c.293]
РЕАКЦИИ КАТИОНОВ /Я ГРУППЫ. АЛЮМИНИИ. ХРОМ 171 [c.171]
Величина IgPpfi меняется в пределах 2,28—2,43. В эту подгруппу сульфидов включаются MnS, FeS, oS, NiS, ZnS. К ним относится и сульфид ванадила VOS. Все сульфиды подгруппы сернистого аммония окрашены, кроме сульфида цинка (белый). Так как катион хрома (II) обладает сильным восстановительным действием и неустойчив (хотя и образуют черный очень малорастворимый сульфид rS), то здесь рассматриваются катионы хрома (III), хромат- и бихромат-ионы кроме марганца (II), рассматриваются также манганат- и перманганат-ионы. Аналитические свойства хрома (III) объясняются структурой электронейтрального атома (ЗiiЧs ). То же самое наблюдается у меди (И) (3d "4si). Трисульфид хрома черно-коричневый, подвергается гидролизу вследствие меньшей растворимости гидроокиси хрома (III). В табл. 38 сопоставлены основные характеристики катионов этой подгруппы. Все катионы данной подгруппы легко переходят из одной степени окисления в другую, используются при редоксметодах анализа и как катализаторы в кинетических методах. В химико-аналитических реакциях этих ионов сказывается сходство их электронной структуры по горизонтальному направлению. Катионы ярко окрашены и образуют разнообразные комплексные соединения. 8-оксихинолин, который называют органическим сероводородом , дает характерные, ярко окрашенные внутрикомплексные соединения с этими катионами, начиная от титана и до цинка (табл. 38). [c.205]
Аналитические реакции катиона хрома(Ш) Сг . Реакции с щелочами и с аммиаком. Катионы с растворами щелочей или аммиака образуют осадок гидроксида хрома(П1) Сг(ОН)з серо-зеленого или синефиолетового цвета [c.380]
Окислительно-восстановительные реакции применяются также для разделения ионов и перевода в раствор малорастворимых соединений. Например, при анализе катионов, для того чтобы отделить катионы хрома от катионов железа, марганца и некоторых других, их окисляют в щелочной среде перекисью водорода до анионов СгО ", переходящих в раствор, в котором и открываются ионы хрома. [c.176]
Другие реакции катионов хрома Ш). Катион Сг с гидрофосфатом натрия НагНРОд образует осадок фосфата хрома СГРО4 зеленого цвета, растворимый в кислотах и щелочах с арсенитами и арсенатами дает малорастворимые осадки арсенита СгАзОз и арсената СгАз04 соответственно. [c.382]
Соли типа КСгОг — хромиты — можно рассматривать как производные метахромистой кислоты НСгОг. Соли этой кислоты и соли, в состав которых входит катион хрома(III), как соли, соответственно, слабой кислоты и слабого основания, подвержены сильному гидролизу. Поэтому водные растворы хромитов имеют сильно щелочную реакцию, а солей, содержащих катион хрома(III)—кислую. При нагревании раствора гидролиз усиливается. Соли хрома(III) и слабых кислот нацело гидролизуются. Например [c.258]
В растворе открывают катионы aлюvIиния А1 " (катионы хрома Сг " были открыты ранее на стадии предварительных испытаний). К испытуемому раствору прибавляют концентрированный раствор хлорида a i-мония КН4С1 и нафевают до кипения. Выпадает белый осадок гидроксида алюминия А1(0Н)з, который отде.тяют центрифугированием, растворяют в небольшом количестве хлороводородной кислоты и в полученном растворе открывают катионьг алюминия реакцией с ализарином по образованию комплекса алюминия с ализарином красного цвета. [c.309]
Реакции окисления катионов хрома(Ш) до хромат-ионов и днхро-мат-ионов. Катионы при взаимодействии с окислителями (nepoK ii-дом водорода, перманганатом калия и др.) окисляются до хромат- [c.381]
Растворимость 2п(ОП)2 в избытке раствора ЫН40Н объясняется образованием комплексных ионов [2п(ЫНз)4Р+ или [2п(ЫНз)бР+. Этой реакцией катион 2п + отличается от катионов алюминия, хрома, железа н марганца. [c.295]
Растворимость Zn(0H)2 в избытке раствора Nh5OH объ ясняется образованием комплексных ионов [2п(ЫНз)41" или IZn (ЫНз)й]+ +. Этой реакцией катион Zn++ отличается от катионов алюминия, хрома, железа и марганца. [c.266]
Окисление катионов хрома (III) перекисью водорода или перекисью натрия до Сг04 -. Рассмотрим реакцию окисления СгЗ+ перекисью натрия в щелочной среде [c.101]
Исследования, проведенные в ряде стран, показали, что металлы, широко применяемые в промышленности и распространенные в окружающей среде, могут оказывать на организм человека не только токсикологическое, но и канцерогенное воздействие [935, 987]. К химическим канцерогенам относят такие металлы, как бериллий, хром, никель потенциальными канцерогенами являются кобальт, кадмий, свинец и некоторые другие металлы [931]. Понятие канцерогенность металла относится не к элементу как таковому, а к его определенному физико-химическому состоянию. Например, канцерогенность хрома может быть объяснена следующим образом. Этот элемент в виде хромат-аниона с помощью сульфатной транспортной системы проникает через клеточную мембрану, тогда как катион хром(П1) сквозь нее не проходит. Клеточная метаболическая система восстанавливает хромат до хрома(П1), который в отличие от оксоаниона хрома(VI) образует прочные комплексы внутри клетки с нуклеиновыми кислотами, протеинами и нуклеозидами, вызывая повреждения ДНК, которые в свою очередь ведут к мутации, а следовательно, и к развитию рака [931]. Согласно концепции Мартелла канцерогенность металла связана со степенью его электроположительности. Ионы электроположительных металлов образуют лабильные комплексы и большей частью не канцерогенны. Ионы же металлов с низкой электроположительностью образуют высококовалентные связи с донорными группами биолигандов и способны подвергаться только очень медленным обменным реакциям с другими лигандами, находящимися в биологических системах, что в конечном счете обусловливает канцерогенное действие этих катионов [931]. [c.500]
Комм. В чем причины протекания реакций с гидроксид-иона-ми, приводящих к выпадению, а затем — к растворению осадка в П1 Соблюдается ли критерий протекания ОВР при взаимодействии гексагидроксохромат(Ш)-иона с бромом (ПО При ответе используйте справочные данные. Почему из водных растворов невозможно вьщелить сульфид и карбонат хрома(П1) (Пг и Пз) В чем причина выделения осадка ортофосфата хрома(П1) при действии гидроортофосфат-иона на катион хрома(П1) в П4 Приведите условия его осаждения с учетом ПР. [c.237]
Механизм окисления НС1 на окиси хрома рассмотрен в [5781. В этой работе Гельбштейн с сотрудниками обращают внимание на то, что окись хрома хорошо сорбирует кислород благодаря способности ионов Сг +легко отдавать d-электроны (стадия I). Появление вакантных d-орбиталей у увеличивает возможность координации этих ионов с НС1 (стадия П), в результате которой образуется промежуточное соединение типа хлорокиси хрома ( rO l) и выделяется вода (стадия П1). При взаимодействии хлорокиси с НС1 возможно возникновение промежуточного комплекса состава ( rjOn+ida- 2НС1) (стадия IV), в котором степень ионности катионов хрома понижена. Благодаря этому облегчается взаимодействие промежуточного комплекса с кислородом, приводящее к получению продуктов реакции — хлора и воды — и регенерации катионов Сг + (стадия V). Лимитирующими процесс стадиями по [578] являются стадии III и V. Определяющая роль скорости хемосорбции кислорода следует из данных [5791. [c.278]
Глина также может быть превращена в гидрофобную реакцией с органонесрганическим катионным соединением — стеаратохло-ридом хрома [127], который делает ее предпочтительно смачиваемой маслом в присутствии воды. В этом соединении стеариновая кислота устанавливает правильное соотношение с катионами хрома, образуя катионный поверхностно-активный комплекс, который прочно удерживается поверхностью глины. [c.216]
Двойная оксосоль. Красный (гидрат темно-фиолетовый). При нагревании разлагается без плавления. Хорошо растворим в воде (серо-синяя окраска раствора отвечает аквакомплексу [Сг(Н20)б] "), гидролизуется по катиону хрома(П1). Реагирует со щелочами, гидратом аммиака. Слабый окислитель и восстановитель. Вступает в реакции двойного обмена. Качественные реакции на ион Сг + — восстановление до Сг + или окисление до СГО4 и СГ2О7 . Применяется как дубитель кож, протрава при крашении тканей, реактив в фотографии. Образуется при совместной кристаллизации сульфатов хрома (П1) и калия. [c.122]
Общие реакции катионов II аналитической группы. Г. Действие гидрофосфатов щелочных металлов и аммония (см. табл. 7). N32HP04, К2НРО4 или (Nh5)2HP04 образуют с катионами второй аналитической группы белые осадки гидрофосфатов или фосфатов магния, марганца, бария, стронция, кальция, железа (II), алюминия и висмута желтые осадки железа (III) и зеленые — хрома [c.49]
С целью выяснения группировок молекулы, обусловливающих каталитическую реакцию с Сг"+, были синтезированы аналоги I и И, содержащие в качестве С-заместителеи метилглициновые (III), аминоэнантовые (IV), две глициновые и две оксигруппы (V). Обследование III—V, а также известных ранее VI и VII, содержащих оксиэтильные группы, показало, что ни одно из них не дает подобной реакции с хромом. Представляло интерес выяснить, имеется ли связь между реакцией гашения флуоресценции в присутствии Сг и наличием комплексообразования с этим катионом. [c.138]
Очень ценный метод фотометрического определения хрома с дифенилкарбазидом легко выполняется в экстракционном варианте. Образующийся при реакции содержащий хром малиновый продукт является катионом и после введения, например, трихлорацетатов, антрацен-а-сульфокатов, нафталин- 3-сульфона-тов или других подходящих для этого анионов экстрагируется легче, чем в присутствии только хлоридов или сульфатов [41], Экстрагировать можно бутиловым или амиловым спиртом. [c.38]
Для ознакомления с характерными реакциями катионов III группы берут 0,1 н. растворы хлорного железа Fe lj, сернокислого марганца MnS04, хлористого хрома r l j, сернокислого цин- [c.56]
chem21.info
Опыты по химии. Хром | Подготовка к ЦТ и ЕГЭ по химии
Взаимопревращение хроматов и дихроматов
Оксиду хрома (VI) соответствуют сразу две кислоты – хромовая Н2CrO4 и дихромовая Н2Cr2O7, Хромат калия K2CrO4 и дихромат калия K2Cr2O7 – соли этих кислот. Хроматы – желтого цвета, дихроматы – оранжевого. В кислой среде хромат-ион превращается в дихромат-ион. В присутствии щелочи дихроматы снова становятся хроматами. Хромат калия превращаем в дихромат, добавляя кислоту. Желтый раствор становится оранжевым.
2K2CrO4 + h3SO4 = K2Cr2O7 + K2SO4 + h3O
В стакан с дихроматом калия добавляем щелочь, оранжевый раствор становится желтым – дихроматы превращаются в хроматы.
K2Cr2O7 + 2KOH = 2K2CrO4 + h3O
Мы убедились в том, хроматы превращаются в дихроматы и наоборот при изменении кислотности среды.
Оборудование: пробирки, штатив для пробирок.
Техника безопасности.
Остерегаться попадания на кожу вводных растворов хроматов и дихроматов – эти вещества вызывают аллергию и являются канцерогенными.
Соблюдать правила работы с кислотами и щелочами. При попадании раствора щелочи на кожу, промыть водой и 2% раствором уксусной кислоты. При попадании раствора кислоты на кожу, промыть водой и 2% раствором питьевой соды.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Окисление ацетона хромовым ангидридом
Хромовый ангидрид – это оксид хрома (IV), представляет собой кристаллы темно-красного цвета. Как и все соединения хрома (IV), хромовый ангидрид – сильный окислитель. Поместим оксид хрома на фарфоровую пластинку и капнем на него несколько капель ацетона. Через несколько секунд ацетон загорается. При этом оксид хрома (IV) восстанавливается до оксида хрома (III), а ацетон окисляется до углекислого газа и воды.
Оборудование: фарфоровая пластинка, пипетка.
Техника безопасности. Соблюдать правила работы с легковоспламеняющимися жидкостями, правила работы с окислителями.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Окислительные свойства дихроматов
Дихроматы, например дихромат калия K2Cr2O7 – сильные окислители. Под действием восстановителей дихроматы в кислой среде переходят в соли хрома (III). Примером такой реакции может служить окисление сульфита натрия раствором дихромата калия в кислой среде. К раствору дихромата калия добавляем серную кислоту и раствор сульфита натрия.
K2Cr2O7 + 3Na2SO3 + 4h3SO4 = Cr2(SO4)3 + 3Na2SO4+ K2SO4 + 4h3O
Оранжевая окраска, характерная для дихроматов, переходит в зеленую. Образовался раствор сульфата хрома (III) зеленого цвета. Соли хрома — ярко окрашены, именно поэтому элемент получил такое название: «хром», что в переводе с греческого означает «цвет, краска».
Оборудование: химический стакан, стеклянная палочка.
Техника безопасности.
Остерегаться попадания на кожу вводных растворов хроматов и дихроматов – эти вещества вызывают аллергию и являются канцерогенными.
Соблюдать правила работы с кислотами. При попадании раствора кислоты на кожу, промыть водой и 2% раствором питьевой соды.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Разложение дихромата аммония («вулкан»)
Перед нами – оранжевые кристаллы дихромата аммония. Горящая лучинка вызывает бурную реакцию. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция.
(Nh5)2 Cr2O7 = Cr2O3 + N2 + 4h3O
Окислитель — хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду: мы наблюдаем реакцию разложения соли. Реакция началась от горящей лучинки, но не прекратилась, когда лучинку убрали, а стала еще интенсивней. Дело в том, что в процессе реакции выделяется теплота, и начавшись от лучинки, процесс лавинообразно развивается до тех пор, пока вся масса дихромата не превратится в оксид хрома (III), азот и воду. Оксид хрома – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Оборудование: шпатель, металлическая пластинка, лучинка из дерева.
Техника безопасности.
Остерегаться попадания на кожу дихроматов – эти вещества вызывают аллергию и являются канцерогенными.
Оксид хрома III является опасным веществом, опыт проводить под тягой, соблюдать правила пожарной безопасности.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Внешний вид хрома
Взаимодействие хрома с соляной кислотой
Амфотерность гидроксида хрома (III)
Хлорид хрома (III)
Разрушение гидроксокомплекса хрома
Окисление соединений хрома (III)
Качественная реакция на хромат анион
Качественная реакция на дихромат анион
Взаимодействие дихромата с сульфитом
Взаимодействие хромовой смеси со спиртом
Образование пероксида хрома
Хромирование деталей
www.yoursystemeducation.com
Качественные-реакции-неорганической-химии
 С этим файлом связано 8 файл(ов). Среди них: himiya-reshenie-kachestvennyh-zadach.pdf, himiya-neorganic-v-reaktsiyah.pdf, himiya-svyazi-mejdu-klassami-veshestv.pdf, himiya-organic-reaktsii.pdf, Неорганическая химия.docx, A10_kharakternye_khimicheskie_svoystva.docx, Kachestvennye-reaktsii-neorganicheskoy-khimii.pdf, Khimia__Otlichnik_EGE.pdf, Khimia_Skhemy_tablitsy.pdf.
С этим файлом связано 8 файл(ов). Среди них: himiya-reshenie-kachestvennyh-zadach.pdf, himiya-neorganic-v-reaktsiyah.pdf, himiya-svyazi-mejdu-klassami-veshestv.pdf, himiya-organic-reaktsii.pdf, Неорганическая химия.docx, A10_kharakternye_khimicheskie_svoystva.docx, Kachestvennye-reaktsii-neorganicheskoy-khimii.pdf, Khimia__Otlichnik_EGE.pdf, Khimia_Skhemy_tablitsy.pdf. Показать все связанные файлы Качественные реакции неорганической химии. Всем химикам, как опытным, так и начинающим, хоть раз, но доводилось слышать этот термин. В химии качественные реакции очень важны, с ними тесно связан один из разделов химии — аналитическая химия. Итак, в этой статье я изложу качественные реакции, как школьного курса, так и немного «нестандартные». Ну что ж, начнем! Качественные реакции определяют катионы, анионы, порой и целые соединения. 1. Качественные реакции на катионы. 1.1.1 Качественные реакции на катионы щелочных металлов (Li+, Na+, K+, Rb+, Cs+). Катионы щелочных металлов возможно провести только с сухими солями, т.к. практически все соли щелочных металлов растворимы. Обнаружить их можно при внесении небольшого количества соли в пламя горелки. Тот или иной катион окрашивает пламя в соответствующий цвет: Li+ — темно-розовый. Na+ — желтый. K+ — фиолетовый. Rb+ — красный. Cs+ — голубой. Катионы так же можно обнаружить и с помощью химических реакций. При сливании раствора соли лития с фосфатами образуется нерастворимый в воде, но растворимый в конц. азотной кислоте, фосфат лития: 3Li+ + PO4 3- = Li3PO4↓ Li3PO4 + 3HNO3 = 3LiNO3 + h4PO4Катион K+ можно вывести гидротартрат-анионом HC4h5O6- — анионом винной кислоты: K+ + HC4h5O6- = KHC4h5O6↓ Катионы K+ и Rb+ можно выявить добавлением к растворам их солей кремнефтористой кислоты h3[SiF6] или ее солей — гексафторсиликатов: 2Me+ + [SiF6]2- = Me2[SiF6]↓ (Me = K, Rb) Они же и Cs+ осаждаются из растворов при добавлении перхлорат-анионов: Me+ + ClO4- = MeClO4↓ (Me = K, Rb, Cs). 1.1.2 Качественные реакции на катионы щелочно-земельных металлов (Ca2+, Sr2+, Ba2+, Ra2+). Катионы щелочно-земельных металлов можно выявить двумя способами: в растворе и по окраске пламени. Кстати, к щелочно-земельным относятся кальций, стронций, барий и радий. Бериллий и магний нельзя отнести к этой группе, как это любят делать на просторах Интернета. Окраска пламени: Ca2+ — кирпично-красный. Sr2+ — карминово-красный. Ba2+ — желтовато-зеленый. Ra2+ — темно-красный. Реакции в растворах. Катионы рассматриваемых металлов имеют общую особенность: их карбонаты и сульфаты нерастворимы. Катион Ca2+ предпочитают выявлять карбонат-анионом CO3 2-: Ca2+ + CO3 2- = CaCO3↓ Который легко растворяется в азотной кислоте с выделением углекислого газа: 2H+ + CO3 2- = h3O + CO2↑ Катионы Ba2+, Sr2+ и Ra2+ предпочитают выявлять сульфат-анионом с образованием сульфатов, нерастворимых в кислотах: Sr2+ + SO4 2- = SrSO4↓ Ba2+ + SO4 2- = BaSO4↓ Ra2+ + SO4 2- = RaSO4↓ 1.1.3. Качественные реакции на катионы свинца (II) Pb2+, серебра (I) Ag+, ртути (I) Hg2+, ртути (II) Hg2+. Рассмотрим их на примере свинца и серебра. Эта группу катионов объединяет одна общая особенность: они образуют нерастворимые хлориды. Но катионы свинца и серебра можно выявить и другими галогенидами. Качественная реакция на катион свинца — образование хлорида свинца (осадок белого цвета), либо образование иодида свинца (осадок ярко желтого цвета): Pb2+ + 2I- = PbI2↓ Качественная реакция на катион серебра — образование белого творожистого осадка хлорида серебра, желтовато-белого осадка бромида серебра, образование желтого осадка иодида серебра: Ag+ + Cl- = AgCl↓ Ag+ + Br- = AgBr↓ Ag+ + I- = AgI↓ Как видно из выше изложенных реакций, галогениды серебра (кроме фторида) нерастворимы, а бромид и иодид даже имеют окраску. Но отличительная черта их не в этом. Данные соединения разлагаются под действием света на серебро и соответствующий галоген, что также помогает их идентифицировать. Поэтому часто емкости с этими солями испускают запахи. Также при добавлении к данным осадкам тиосульфата натрия происходит растворение: AgHal + 2Na2S2O3 = Na3[Ag(S2O3)2] + NaHal, (Hal = Cl, Br, I). То же самое произойдет при добавлении жидкого аммиака или его конц. раствора. Растворяется только AgCl. AgBr и AgI в аммиаке практически нерастворимы: AgCl + 2Nh4 = [Ag(Nh4)2]Cl Существует также еще одна качественная реакция на катион серебра — образование оксида серебра черного цвета при добавлении щелочи: 2Ag+ + 2OH- = Ag2O↓ + h3O Это связано с тем, что гидроксид серебра при нормальных условиях не существует и сразу же распадается на оксид и воду. 1.1.4. Качественная реакция на катионы алюминия Al3+, хрома (III) Cr3+, цинка Zn2+, олова (II) Sn2+. Данные катионы объединены образованием нерастворимых оснований, легко переводимых в комплексные соединения. Групповой реагент — щелочь. Al3+ + 3OH- = Al(OH)3↓ + 3OH- = [Al(OH)6]3-Cr3+ + 3OH- = Cr(OH)3↓ + 3OH- = [Cr(OH)6]3-Zn2+ + 2OH- = Zn(OH)2↓ + 2OH- = [Zn(OH)4]2-Sn2+ + 2OH- = Sn(OH)2↓ + 2OH- = [Sn(OH)4]2-Не стоит забывать, что основания катионов Al3+, Cr3+ и Sn2+ не переводятся в комплексное соединение гидратом аммиака. Этим пользуются, чтобы полностью осадить катионы. Zn2+ при добавлении конц. раствора аммиака сначала образует Zn(OH)2, а при избытке аммиак способствует растворению осадка: Zn(OH)2 + 4Nh4 = [Zn(Nh4)4](OH)2Раствор, содержащий [Cr(OH)6]3-, при добавлении хлорной или бромной воды в щелочной среде становится желтым из-за образования хромат-аниона CrO4 2-: 2[Cr(OH)6]3- + 3Br2 + 4OH- = 2CrO4 2- + 6Br- + 8h3O 1.1.5. Качественная реакция на катионы железа (II) и (III) Fe2+, Fe3+. Данные катионы также образуют нерастворимые основания. Иону Fe2+ отвечает гидроксид железа (II) Fe(OH)2 — осадок белого цвета. На воздухе сразу покрывается зеленым налетом, поэтому чистый Fe(OH)2 получают в атмосфере инертых газов либо азота N2Катиону Fe3+ отвечает метагидроксид железа (III) FeO(OH) бурого цвета. Примечание: соединения состава Fe(OH)3 неизвестно (не получено). Но все же большинство придерживаются записи Fe(OH)3Качественная реакция на Fe2+: Fe2+ + 2OH- = Fe(OH)2↓ Fe(OH)2 будучи соединением двухвалентного железа на воздухе неустойчиво и постепенно переходит в гидроксид железа (III): 4Fe(OH)2 + O2 + 2h3O = 4Fe(OH)3Качественная реакция на Fe3+: Fe3+ + 3OH- = Fe(OH)3↓ Еще одной качественной реакцией на Fe3+ является взаимодействие с роданид-анионом SCN-, при этом образуется роданид железа (III) Fe(SCN)3, окрашивающий раствор в темно-красный цвет (эффект «крови»): Fe3+ + 3SCN- = Fe(SCN)3Роданид железа (III) легко «разрушается» при добавлении фторидов щелочных металлов: 6NaF + Fe(SCN)3 = Na3[FeF6] + 3NaSCN Раствор становится бесцветным. Очень чувствительная реакция на Fe3+, помогает обнаружить даже очень незначительные следы данного катиона. 1.1.6. Качественная реакция на катион марганца (II) Mn2+. Данная реакция основана на жестком окислении марганца в кислой среде с изменением степени окисления с +2 до +7. При этом раствор окрашивается в темно-фиолетовый цвет из-за появления перманганат-аниона. Рассмотрим на примере нитрата марганца: 2Mn(NO3)2 + 5PbO2 + 6HNO3 = 2HMnO4 + 5Pb(NO3)2 + 2h3O 1.1.7. Качественная реакция на катионы меди (II) Cu2+, кобальта (II) Co2+ и никеля (II) Ni2+. Особенность этих катионов в образовании с молекулами аммиака комплексных солей — аммиакатов: Cu2+ + 4Nh4 = [Cu(Nh4)4]2+Аммиакаты окрашивают растворы в яркие цвета. К примеру, аммиакат меди окрашивает раствор в ярко- синий цвет. 1.1.8. Качественные реакции на катион аммония Nh5+. Взаимодействие солей аммония со щелочами при кипячении: Nh5+ + OH- =t= Nh4↑ + h3O При поднесении влажная лакмусовая бумажка окрасится в синий цвет. 1.1.9. Качественная реакция на катион церия (III) Ce3+. Взаимодействие солей церия (III) с щелочным раствором пероксида водорода: Ce3+ + 3OH- = Ce(OH)3↓ 2Ce(OH)3 + 3h3O2 = 2Ce(OH)3(OOH)↓ + 2h3O Пероксогидроксид церия (IV) имеет красно-бурый цвет. 1.2.1. Качественная реакция на катион висмута (III) Bi3+. Образование ярко-желтого раствора тетраиодовисмутата (III) калия K[BiI4] при действии на раствор, содержащий Bi3+, избытком KI: Bi(NO3)3 + 4KI = K[BiI4] + 3KNO3Связано это с тем, что сначала образуется нерастворимый BiI3, который затем связывается с помощью I- в комплекс. На этом я закончу описание выявления катионов. Теперь рассмотрим качественные реакции на некоторые анионы. 2. Качественные реакции на анионы. 2.1.1. Качественные реакции на сульфид-анион S2-. Из сульфидов растворимы сульфиды только щелочных металлов и аммония. Нерастворимые сульфиды имеют специфическую окраску, по которым можно определить тот или иной сульфид. Окраска: MnS — телесный (розовый). ZnS — белый. PbS — черный. Ag2S — черный. CdS — лимонно-желтый. SnS — шоколадный. HgS (метакиноварь) — черный. HgS (киноварь) — красный. Sb2S3 — оранжевый. Bi2S3 — черный. Некоторые сульфиды при взаимодействии с кислотами-неокислителями образуют токсичный газ сероводород h3S с неприятным запахом (тухлых яиц): Na2S + 2HBr = 2NaBr + h3S↑ S2- + 2H+ = h3S↑ А некоторые устойчивы к разбавленным растворам HCl, HBr, HI, h3SO4, HCOOH, Ch4COOH — к примеру CuS, Cu2S, Ag2S, HgS, PbS, CdS, Sb2S3, SnS и некоторые другие. Но они переводятся в раствор конц. азотной кислотой при кипячении (Sb2S3 и HgS растворяются тяжелее всего, причем последний гораздо быстрее растворится в царской водке): CuS + 8HNO3 =t= CuSO4 + 8NO2↑ + 4h3O Также сульфид-анион можно выявить, приливая раствор сульфида к бромной воде: S2- + Br2 = S↓ + 2Br-Образующаяся сера выпадает в осадок. 2.1.2. Качественная реакция на сульфат-анион SO42-. Сульфат-анион обычно осаждают катионом свинца, либо бария: Pb2+ + SO4 2- = PbSO4↓ Осадок сульфата свинца белого цвета. 2.1.3. Качественная реакция на силикат-анион SiO32-. Силикат-анион легко осаждается из раствора в виде стекловидной массы при добавлении сильных кислот: SiO3 2- + 2H+ = h3SiO3↓ (SiO2 * nh3O) 2.1.4. Качественные реакции на хлорид-анион Cl-, бромид-анион Br-, иодид-анион I- смотрите в пункте «качественные реакции на катион серебра Ag+«. 2.1.5. Качественная реакция на сульфит-анион SO32-. При добавлении к раствору сильных кислот образуется диоксид серы SO2 — газ с резким запахом (запах зажженной спички): SO3 2- + 2H+ = SO2↑ + h3O 2.1.6. Качественная реакция на карбонат-анион CO32-. При добавлении к раствору карбоната сильных кислот образуется углекислый газ CO2, гасящий горящую лучинку: CO3 2- + 2H+ = CO2↑ + h3O 2.1.7. Качественная реакция на тиосульфат-анион S2O32-. При добавлении раствора серной или соляной кислоты к раствору тиосульфата образуется диоксид серы SO2 и выпадает в осадок элементарная сера S: S2O3 2- + 2H+ = S↓ + SO2↑ + h3O 2.1.8. Качественная реакция на хромат-анион CrO42-. При добавлении к раствору хромата раствора солей бария выпадает желтый осадок хромата бария BaCrO4, разлагающегося в сильнокислой среде: Ba2+ + CrO4 2- = BaCrO4↓ Растворы хроматов окрашены в желтый цвет. При подкислении раствора цвет изменится на оранжевый, отвечающий дихромат-аниону Cr2O7 2-: 2CrO4 2- + 2H+ = Cr2O7 2- + h3O Кроме того хроматы являются окислителями в щелочной и нейтральной средах (окислительные способности хуже, чем у дихроматов): S2- + CrO4 2- + h3O = S + Cr(OH)3 + OH-2.1.9. Качественная реакция на дихромат-анион Cr2O72-. При добавлении к раствору дихромата раствора соли серебра образуется осадок оранжевого цвета Ag2Cr2O7: 2Ag+ + Cr2O7 2- = Ag2Cr2O7↓ Растворы дихроматов окрашены в оранжевый цвет. При подщелачивании раствора окраска изменяется на желтую, отвечающую хромат-аниону CrO4 2-: Cr2O7 2- + 2OH- = 2CrO4 2- + h3O Кроме того, дихроматы — сильные окислители в кислой среде. При внесении в подкисленный раствор дихромата какого-либо восстановителя окраска раствора изменится с оранжевого на зеленый, отвечающей катиону хрома (III) Сr3+ (в качестве восстановителя бромид-анион): 6Br- + Cr2O7 2- + 14H+ = 3Br2 + 2Cr3+ + 7h3O Эффектная качественная реакция на шестивалентный хром — темно-синее окрашивание раствора при добавлении конц. перекиси водорода в эфире. Образуется пероксид хрома состава CrO52.2.0. Качественная реакция на перманганат-анион MnO4-. Перманганат-анион «выдает» темно- фиолетовая окраска раствора. Кроме того, перманганаты — сильнейшие окислители, в кислой среде восстанавливаются до Mn2+ (фиолетовая окраска исчезает), в нейтральной — до Mn+4 (окраска исчезает, выпадает бурый осадок диоксида марганца MnO2) и в щелочной — до MnO4 2- (окраска раствора изменяется на темно-зеленый): 5SO3 2- + 2MnO4- + 6H+ = 5SO4 2- + 2Mn2+ + 3h3O 3SO3 2- + 2MnO4- + h3O = 3SO4 2- + 2MnO2↓ + 2OH-SO3 2- + 2MnO4- + 2OH- = SO4 2- + 2MnO4 2- + h3O 2.2.1. Качественная реакция на манганат-анион MnO42-. При подкислении раствора манганата темно- зеленая окраска изменяется на темно-фиолетовую, отвечающую перманганат-аниону MnO4-: 3K2MnO4(р.) + 4HCl(разб.) = MnO2↓ + 2KMnO4 + 4KCl + 2h3O 2.2.2. Качественная реакция на фосфат-анион PO43-. При добавлении к раствору фосфата раствора соли серебра выпадает желтоватый осадок фосфата серебра (I) Ag3PO4: 3Ag+ + PO4 3- = Ag3PO4↓ Аналогична реакция и к дигидрофосфат-аниону h3PO4-2.2.3. Качественная реакция на феррат-анион FeO42-. Осаждение из раствора феррата бария красного цвета (реакция проводится в среде щелочи): Ba2+ + FeO4 2- =OH-= BaFeO4↓ Ферраты — сильнейшие окислители (сильнее перманганатов). Устойчивы в щелочной среде, неустойчивы в кислой: 4FeO4 2- + 20H+ = 4Fe3+ + 3O2↑ + 10h3O 2.2.4. Качественная реакция на нитрат-анион NO3-. Нитраты в растворе не проявляют окислительных способностей. Но при подкислении раствора способны окислить, к примеру, медь (раствор подкисляют обычно разб. h3SO4): 3Cu + 2NO3- + 8H+ = 3Cu2+ + 2NO↑ + 4h3O 2.2.5. Качественная реакция на гексацианноферрат (II) и (III) ионы [Fe(CN)6]4- и [Fe(CN)6]3-. При приливании растворов, содержащих Fe2+, образуется осадок темно-синего цвета (турнбулева синь, берлинская лазурь): K3[Fe(CN)6] + FeCl2 = KFe[Fe(CN)6] + 2KCl (при этом осадок состоит из смеси KFe(II)[Fe(III)(CN)6], KFe(III)[Fe(II)(CN)6], Fe3[Fe(CN)6]2, Fe4[Fe(CN)6]3). 2.2.6. Качественная реакция на арсенат-анион AsO43-. Образование нерастворимого в воде арсената серебра (I) Ag3AsO4, имеющего цвет «кофе с молоком»: 3Ag+ + AsO4 3- = Ag3AsO4↓ Вот основные качественные реакции на анионы. Далее мы рассмотрим качественные реакции на простые и сложные вещества. 3. Качественные реакции на простые и сложные вещества. Некоторые простые и сложные вещества, как и ионы, обнаруживаются качественными реакциями. Ниже я опишу качественные реакции на некоторые вещества. 3.1.1. Качественная реакция на водород h3. Лающий хлопок при поднесении горящей лучинки к источнику водорода. 3.1.2. Качественная реакция на азот N2. Тушение горящей лучинки в атмосфере азота. При пропускании в раствор Ca(OH)2 осадок не выпадает. 3.1.3. Качественная реакция на кислород O2. Яркое загорание тлеющей лучинки в атмосфере кислорода. 3.1.4. Качественная реакция на озон O3. Взаимодействие озона с раствором иодидов с выпадением кристаллического иода I2 в осадок: 2KI + O3 + h3O = 2KOH + I2↓ + O2↑ В отличии от озона кислород в данную реакцию не вступает. Полагается 3.1.5. Качественная реакция на хлор Cl2. Хлор – газ желто-зеленого цвета с очень неприятным запахом.При взаимодействии недостатка хлора с растворами иодидов в осадок выпадает элементарный иод I2: 2KI + Cl2 = 2KCl + I2↓ Избыток хлора приведет к окислению образовавшегося иода: I2 + 5Cl2 + 6h3O = 2HIO3 + 10HCl 3.1.6. Качественные реакции на аммиак Nh4. Примечание: данные реакции не дают в школьном курсе. Однако, это самые надежные качественные реакции на аммиак. Почернение бумажки, смоченной в растворе соли ртути (I) Hg2+: Hg2Cl2 + 2Nh4 = Hg(Nh3)Cl + Hg + Nh5Cl Бумажка чернеет из-за выделения мелкодисперсной ртути. Взаимодействие аммиака с щелочным раствором тетраиодомеркурата (II) калия K2[HgI4] (реактив Несслера): 2K2[HgI4] + Nh4 + 3KOH = [Hg2N]I · h3O↓ + 7KI + 2h3O Комплекс [Hg2N]I · h3O бурого цвета (цвет ржавчины) выпадает в осадок. Две последние реакции являются самыми надежными на аммиак. Реакция аммиака с хлороводородом («дым» без огня): Nh4 + HCl = Nh5Cl 3.1.7. Качественная реакция на фосген (хлорокись углерода, карбонил хлорид) COCl2. Испускание белого «дыма» от бумажки, смоченной в растворе аммиака: COCl2 + 4Nh4 = (Nh3)2CO + 2Nh5Cl 3.1.8. Качественная реакция на угарный газ (моноксид углерода) CO. Помутнение раствора при пропускании угарного газа в раствор хлорида палладия (II): PdCl2 + CO + h3O = CO2↑ + 2HCl + Pd↓ 3.1.9. Качественная реакция на углекислый газ (диоксид углерода) CO2. Тушение тлеющей лучинки в атмосфере углекислого газа. Пропускание углекислого газа в раствор гашеной извести Ca(OH)2: Ca(OH)2 + CO2 = CaCO3↓ + h3O Дальнейшее пропускание приведет к растворению осадка: CaCO3 + CO2 + h3O = Ca(HCO3)23.2.1. Качественная реакция на оксид азота (II) NO. Оксид азота (II) очень чувствителен к кислороду воздуха, потому на воздухе буреет, окисляясь до оксида азота (IV) NO2: 2NO + O2 = 2NO2
Показать все связанные файлы Качественные реакции неорганической химии. Всем химикам, как опытным, так и начинающим, хоть раз, но доводилось слышать этот термин. В химии качественные реакции очень важны, с ними тесно связан один из разделов химии — аналитическая химия. Итак, в этой статье я изложу качественные реакции, как школьного курса, так и немного «нестандартные». Ну что ж, начнем! Качественные реакции определяют катионы, анионы, порой и целые соединения. 1. Качественные реакции на катионы. 1.1.1 Качественные реакции на катионы щелочных металлов (Li+, Na+, K+, Rb+, Cs+). Катионы щелочных металлов возможно провести только с сухими солями, т.к. практически все соли щелочных металлов растворимы. Обнаружить их можно при внесении небольшого количества соли в пламя горелки. Тот или иной катион окрашивает пламя в соответствующий цвет: Li+ — темно-розовый. Na+ — желтый. K+ — фиолетовый. Rb+ — красный. Cs+ — голубой. Катионы так же можно обнаружить и с помощью химических реакций. При сливании раствора соли лития с фосфатами образуется нерастворимый в воде, но растворимый в конц. азотной кислоте, фосфат лития: 3Li+ + PO4 3- = Li3PO4↓ Li3PO4 + 3HNO3 = 3LiNO3 + h4PO4Катион K+ можно вывести гидротартрат-анионом HC4h5O6- — анионом винной кислоты: K+ + HC4h5O6- = KHC4h5O6↓ Катионы K+ и Rb+ можно выявить добавлением к растворам их солей кремнефтористой кислоты h3[SiF6] или ее солей — гексафторсиликатов: 2Me+ + [SiF6]2- = Me2[SiF6]↓ (Me = K, Rb) Они же и Cs+ осаждаются из растворов при добавлении перхлорат-анионов: Me+ + ClO4- = MeClO4↓ (Me = K, Rb, Cs). 1.1.2 Качественные реакции на катионы щелочно-земельных металлов (Ca2+, Sr2+, Ba2+, Ra2+). Катионы щелочно-земельных металлов можно выявить двумя способами: в растворе и по окраске пламени. Кстати, к щелочно-земельным относятся кальций, стронций, барий и радий. Бериллий и магний нельзя отнести к этой группе, как это любят делать на просторах Интернета. Окраска пламени: Ca2+ — кирпично-красный. Sr2+ — карминово-красный. Ba2+ — желтовато-зеленый. Ra2+ — темно-красный. Реакции в растворах. Катионы рассматриваемых металлов имеют общую особенность: их карбонаты и сульфаты нерастворимы. Катион Ca2+ предпочитают выявлять карбонат-анионом CO3 2-: Ca2+ + CO3 2- = CaCO3↓ Который легко растворяется в азотной кислоте с выделением углекислого газа: 2H+ + CO3 2- = h3O + CO2↑ Катионы Ba2+, Sr2+ и Ra2+ предпочитают выявлять сульфат-анионом с образованием сульфатов, нерастворимых в кислотах: Sr2+ + SO4 2- = SrSO4↓ Ba2+ + SO4 2- = BaSO4↓ Ra2+ + SO4 2- = RaSO4↓ 1.1.3. Качественные реакции на катионы свинца (II) Pb2+, серебра (I) Ag+, ртути (I) Hg2+, ртути (II) Hg2+. Рассмотрим их на примере свинца и серебра. Эта группу катионов объединяет одна общая особенность: они образуют нерастворимые хлориды. Но катионы свинца и серебра можно выявить и другими галогенидами. Качественная реакция на катион свинца — образование хлорида свинца (осадок белого цвета), либо образование иодида свинца (осадок ярко желтого цвета): Pb2+ + 2I- = PbI2↓ Качественная реакция на катион серебра — образование белого творожистого осадка хлорида серебра, желтовато-белого осадка бромида серебра, образование желтого осадка иодида серебра: Ag+ + Cl- = AgCl↓ Ag+ + Br- = AgBr↓ Ag+ + I- = AgI↓ Как видно из выше изложенных реакций, галогениды серебра (кроме фторида) нерастворимы, а бромид и иодид даже имеют окраску. Но отличительная черта их не в этом. Данные соединения разлагаются под действием света на серебро и соответствующий галоген, что также помогает их идентифицировать. Поэтому часто емкости с этими солями испускают запахи. Также при добавлении к данным осадкам тиосульфата натрия происходит растворение: AgHal + 2Na2S2O3 = Na3[Ag(S2O3)2] + NaHal, (Hal = Cl, Br, I). То же самое произойдет при добавлении жидкого аммиака или его конц. раствора. Растворяется только AgCl. AgBr и AgI в аммиаке практически нерастворимы: AgCl + 2Nh4 = [Ag(Nh4)2]Cl Существует также еще одна качественная реакция на катион серебра — образование оксида серебра черного цвета при добавлении щелочи: 2Ag+ + 2OH- = Ag2O↓ + h3O Это связано с тем, что гидроксид серебра при нормальных условиях не существует и сразу же распадается на оксид и воду. 1.1.4. Качественная реакция на катионы алюминия Al3+, хрома (III) Cr3+, цинка Zn2+, олова (II) Sn2+. Данные катионы объединены образованием нерастворимых оснований, легко переводимых в комплексные соединения. Групповой реагент — щелочь. Al3+ + 3OH- = Al(OH)3↓ + 3OH- = [Al(OH)6]3-Cr3+ + 3OH- = Cr(OH)3↓ + 3OH- = [Cr(OH)6]3-Zn2+ + 2OH- = Zn(OH)2↓ + 2OH- = [Zn(OH)4]2-Sn2+ + 2OH- = Sn(OH)2↓ + 2OH- = [Sn(OH)4]2-Не стоит забывать, что основания катионов Al3+, Cr3+ и Sn2+ не переводятся в комплексное соединение гидратом аммиака. Этим пользуются, чтобы полностью осадить катионы. Zn2+ при добавлении конц. раствора аммиака сначала образует Zn(OH)2, а при избытке аммиак способствует растворению осадка: Zn(OH)2 + 4Nh4 = [Zn(Nh4)4](OH)2Раствор, содержащий [Cr(OH)6]3-, при добавлении хлорной или бромной воды в щелочной среде становится желтым из-за образования хромат-аниона CrO4 2-: 2[Cr(OH)6]3- + 3Br2 + 4OH- = 2CrO4 2- + 6Br- + 8h3O 1.1.5. Качественная реакция на катионы железа (II) и (III) Fe2+, Fe3+. Данные катионы также образуют нерастворимые основания. Иону Fe2+ отвечает гидроксид железа (II) Fe(OH)2 — осадок белого цвета. На воздухе сразу покрывается зеленым налетом, поэтому чистый Fe(OH)2 получают в атмосфере инертых газов либо азота N2Катиону Fe3+ отвечает метагидроксид железа (III) FeO(OH) бурого цвета. Примечание: соединения состава Fe(OH)3 неизвестно (не получено). Но все же большинство придерживаются записи Fe(OH)3Качественная реакция на Fe2+: Fe2+ + 2OH- = Fe(OH)2↓ Fe(OH)2 будучи соединением двухвалентного железа на воздухе неустойчиво и постепенно переходит в гидроксид железа (III): 4Fe(OH)2 + O2 + 2h3O = 4Fe(OH)3Качественная реакция на Fe3+: Fe3+ + 3OH- = Fe(OH)3↓ Еще одной качественной реакцией на Fe3+ является взаимодействие с роданид-анионом SCN-, при этом образуется роданид железа (III) Fe(SCN)3, окрашивающий раствор в темно-красный цвет (эффект «крови»): Fe3+ + 3SCN- = Fe(SCN)3Роданид железа (III) легко «разрушается» при добавлении фторидов щелочных металлов: 6NaF + Fe(SCN)3 = Na3[FeF6] + 3NaSCN Раствор становится бесцветным. Очень чувствительная реакция на Fe3+, помогает обнаружить даже очень незначительные следы данного катиона. 1.1.6. Качественная реакция на катион марганца (II) Mn2+. Данная реакция основана на жестком окислении марганца в кислой среде с изменением степени окисления с +2 до +7. При этом раствор окрашивается в темно-фиолетовый цвет из-за появления перманганат-аниона. Рассмотрим на примере нитрата марганца: 2Mn(NO3)2 + 5PbO2 + 6HNO3 = 2HMnO4 + 5Pb(NO3)2 + 2h3O 1.1.7. Качественная реакция на катионы меди (II) Cu2+, кобальта (II) Co2+ и никеля (II) Ni2+. Особенность этих катионов в образовании с молекулами аммиака комплексных солей — аммиакатов: Cu2+ + 4Nh4 = [Cu(Nh4)4]2+Аммиакаты окрашивают растворы в яркие цвета. К примеру, аммиакат меди окрашивает раствор в ярко- синий цвет. 1.1.8. Качественные реакции на катион аммония Nh5+. Взаимодействие солей аммония со щелочами при кипячении: Nh5+ + OH- =t= Nh4↑ + h3O При поднесении влажная лакмусовая бумажка окрасится в синий цвет. 1.1.9. Качественная реакция на катион церия (III) Ce3+. Взаимодействие солей церия (III) с щелочным раствором пероксида водорода: Ce3+ + 3OH- = Ce(OH)3↓ 2Ce(OH)3 + 3h3O2 = 2Ce(OH)3(OOH)↓ + 2h3O Пероксогидроксид церия (IV) имеет красно-бурый цвет. 1.2.1. Качественная реакция на катион висмута (III) Bi3+. Образование ярко-желтого раствора тетраиодовисмутата (III) калия K[BiI4] при действии на раствор, содержащий Bi3+, избытком KI: Bi(NO3)3 + 4KI = K[BiI4] + 3KNO3Связано это с тем, что сначала образуется нерастворимый BiI3, который затем связывается с помощью I- в комплекс. На этом я закончу описание выявления катионов. Теперь рассмотрим качественные реакции на некоторые анионы. 2. Качественные реакции на анионы. 2.1.1. Качественные реакции на сульфид-анион S2-. Из сульфидов растворимы сульфиды только щелочных металлов и аммония. Нерастворимые сульфиды имеют специфическую окраску, по которым можно определить тот или иной сульфид. Окраска: MnS — телесный (розовый). ZnS — белый. PbS — черный. Ag2S — черный. CdS — лимонно-желтый. SnS — шоколадный. HgS (метакиноварь) — черный. HgS (киноварь) — красный. Sb2S3 — оранжевый. Bi2S3 — черный. Некоторые сульфиды при взаимодействии с кислотами-неокислителями образуют токсичный газ сероводород h3S с неприятным запахом (тухлых яиц): Na2S + 2HBr = 2NaBr + h3S↑ S2- + 2H+ = h3S↑ А некоторые устойчивы к разбавленным растворам HCl, HBr, HI, h3SO4, HCOOH, Ch4COOH — к примеру CuS, Cu2S, Ag2S, HgS, PbS, CdS, Sb2S3, SnS и некоторые другие. Но они переводятся в раствор конц. азотной кислотой при кипячении (Sb2S3 и HgS растворяются тяжелее всего, причем последний гораздо быстрее растворится в царской водке): CuS + 8HNO3 =t= CuSO4 + 8NO2↑ + 4h3O Также сульфид-анион можно выявить, приливая раствор сульфида к бромной воде: S2- + Br2 = S↓ + 2Br-Образующаяся сера выпадает в осадок. 2.1.2. Качественная реакция на сульфат-анион SO42-. Сульфат-анион обычно осаждают катионом свинца, либо бария: Pb2+ + SO4 2- = PbSO4↓ Осадок сульфата свинца белого цвета. 2.1.3. Качественная реакция на силикат-анион SiO32-. Силикат-анион легко осаждается из раствора в виде стекловидной массы при добавлении сильных кислот: SiO3 2- + 2H+ = h3SiO3↓ (SiO2 * nh3O) 2.1.4. Качественные реакции на хлорид-анион Cl-, бромид-анион Br-, иодид-анион I- смотрите в пункте «качественные реакции на катион серебра Ag+«. 2.1.5. Качественная реакция на сульфит-анион SO32-. При добавлении к раствору сильных кислот образуется диоксид серы SO2 — газ с резким запахом (запах зажженной спички): SO3 2- + 2H+ = SO2↑ + h3O 2.1.6. Качественная реакция на карбонат-анион CO32-. При добавлении к раствору карбоната сильных кислот образуется углекислый газ CO2, гасящий горящую лучинку: CO3 2- + 2H+ = CO2↑ + h3O 2.1.7. Качественная реакция на тиосульфат-анион S2O32-. При добавлении раствора серной или соляной кислоты к раствору тиосульфата образуется диоксид серы SO2 и выпадает в осадок элементарная сера S: S2O3 2- + 2H+ = S↓ + SO2↑ + h3O 2.1.8. Качественная реакция на хромат-анион CrO42-. При добавлении к раствору хромата раствора солей бария выпадает желтый осадок хромата бария BaCrO4, разлагающегося в сильнокислой среде: Ba2+ + CrO4 2- = BaCrO4↓ Растворы хроматов окрашены в желтый цвет. При подкислении раствора цвет изменится на оранжевый, отвечающий дихромат-аниону Cr2O7 2-: 2CrO4 2- + 2H+ = Cr2O7 2- + h3O Кроме того хроматы являются окислителями в щелочной и нейтральной средах (окислительные способности хуже, чем у дихроматов): S2- + CrO4 2- + h3O = S + Cr(OH)3 + OH-2.1.9. Качественная реакция на дихромат-анион Cr2O72-. При добавлении к раствору дихромата раствора соли серебра образуется осадок оранжевого цвета Ag2Cr2O7: 2Ag+ + Cr2O7 2- = Ag2Cr2O7↓ Растворы дихроматов окрашены в оранжевый цвет. При подщелачивании раствора окраска изменяется на желтую, отвечающую хромат-аниону CrO4 2-: Cr2O7 2- + 2OH- = 2CrO4 2- + h3O Кроме того, дихроматы — сильные окислители в кислой среде. При внесении в подкисленный раствор дихромата какого-либо восстановителя окраска раствора изменится с оранжевого на зеленый, отвечающей катиону хрома (III) Сr3+ (в качестве восстановителя бромид-анион): 6Br- + Cr2O7 2- + 14H+ = 3Br2 + 2Cr3+ + 7h3O Эффектная качественная реакция на шестивалентный хром — темно-синее окрашивание раствора при добавлении конц. перекиси водорода в эфире. Образуется пероксид хрома состава CrO52.2.0. Качественная реакция на перманганат-анион MnO4-. Перманганат-анион «выдает» темно- фиолетовая окраска раствора. Кроме того, перманганаты — сильнейшие окислители, в кислой среде восстанавливаются до Mn2+ (фиолетовая окраска исчезает), в нейтральной — до Mn+4 (окраска исчезает, выпадает бурый осадок диоксида марганца MnO2) и в щелочной — до MnO4 2- (окраска раствора изменяется на темно-зеленый): 5SO3 2- + 2MnO4- + 6H+ = 5SO4 2- + 2Mn2+ + 3h3O 3SO3 2- + 2MnO4- + h3O = 3SO4 2- + 2MnO2↓ + 2OH-SO3 2- + 2MnO4- + 2OH- = SO4 2- + 2MnO4 2- + h3O 2.2.1. Качественная реакция на манганат-анион MnO42-. При подкислении раствора манганата темно- зеленая окраска изменяется на темно-фиолетовую, отвечающую перманганат-аниону MnO4-: 3K2MnO4(р.) + 4HCl(разб.) = MnO2↓ + 2KMnO4 + 4KCl + 2h3O 2.2.2. Качественная реакция на фосфат-анион PO43-. При добавлении к раствору фосфата раствора соли серебра выпадает желтоватый осадок фосфата серебра (I) Ag3PO4: 3Ag+ + PO4 3- = Ag3PO4↓ Аналогична реакция и к дигидрофосфат-аниону h3PO4-2.2.3. Качественная реакция на феррат-анион FeO42-. Осаждение из раствора феррата бария красного цвета (реакция проводится в среде щелочи): Ba2+ + FeO4 2- =OH-= BaFeO4↓ Ферраты — сильнейшие окислители (сильнее перманганатов). Устойчивы в щелочной среде, неустойчивы в кислой: 4FeO4 2- + 20H+ = 4Fe3+ + 3O2↑ + 10h3O 2.2.4. Качественная реакция на нитрат-анион NO3-. Нитраты в растворе не проявляют окислительных способностей. Но при подкислении раствора способны окислить, к примеру, медь (раствор подкисляют обычно разб. h3SO4): 3Cu + 2NO3- + 8H+ = 3Cu2+ + 2NO↑ + 4h3O 2.2.5. Качественная реакция на гексацианноферрат (II) и (III) ионы [Fe(CN)6]4- и [Fe(CN)6]3-. При приливании растворов, содержащих Fe2+, образуется осадок темно-синего цвета (турнбулева синь, берлинская лазурь): K3[Fe(CN)6] + FeCl2 = KFe[Fe(CN)6] + 2KCl (при этом осадок состоит из смеси KFe(II)[Fe(III)(CN)6], KFe(III)[Fe(II)(CN)6], Fe3[Fe(CN)6]2, Fe4[Fe(CN)6]3). 2.2.6. Качественная реакция на арсенат-анион AsO43-. Образование нерастворимого в воде арсената серебра (I) Ag3AsO4, имеющего цвет «кофе с молоком»: 3Ag+ + AsO4 3- = Ag3AsO4↓ Вот основные качественные реакции на анионы. Далее мы рассмотрим качественные реакции на простые и сложные вещества. 3. Качественные реакции на простые и сложные вещества. Некоторые простые и сложные вещества, как и ионы, обнаруживаются качественными реакциями. Ниже я опишу качественные реакции на некоторые вещества. 3.1.1. Качественная реакция на водород h3. Лающий хлопок при поднесении горящей лучинки к источнику водорода. 3.1.2. Качественная реакция на азот N2. Тушение горящей лучинки в атмосфере азота. При пропускании в раствор Ca(OH)2 осадок не выпадает. 3.1.3. Качественная реакция на кислород O2. Яркое загорание тлеющей лучинки в атмосфере кислорода. 3.1.4. Качественная реакция на озон O3. Взаимодействие озона с раствором иодидов с выпадением кристаллического иода I2 в осадок: 2KI + O3 + h3O = 2KOH + I2↓ + O2↑ В отличии от озона кислород в данную реакцию не вступает. Полагается 3.1.5. Качественная реакция на хлор Cl2. Хлор – газ желто-зеленого цвета с очень неприятным запахом.При взаимодействии недостатка хлора с растворами иодидов в осадок выпадает элементарный иод I2: 2KI + Cl2 = 2KCl + I2↓ Избыток хлора приведет к окислению образовавшегося иода: I2 + 5Cl2 + 6h3O = 2HIO3 + 10HCl 3.1.6. Качественные реакции на аммиак Nh4. Примечание: данные реакции не дают в школьном курсе. Однако, это самые надежные качественные реакции на аммиак. Почернение бумажки, смоченной в растворе соли ртути (I) Hg2+: Hg2Cl2 + 2Nh4 = Hg(Nh3)Cl + Hg + Nh5Cl Бумажка чернеет из-за выделения мелкодисперсной ртути. Взаимодействие аммиака с щелочным раствором тетраиодомеркурата (II) калия K2[HgI4] (реактив Несслера): 2K2[HgI4] + Nh4 + 3KOH = [Hg2N]I · h3O↓ + 7KI + 2h3O Комплекс [Hg2N]I · h3O бурого цвета (цвет ржавчины) выпадает в осадок. Две последние реакции являются самыми надежными на аммиак. Реакция аммиака с хлороводородом («дым» без огня): Nh4 + HCl = Nh5Cl 3.1.7. Качественная реакция на фосген (хлорокись углерода, карбонил хлорид) COCl2. Испускание белого «дыма» от бумажки, смоченной в растворе аммиака: COCl2 + 4Nh4 = (Nh3)2CO + 2Nh5Cl 3.1.8. Качественная реакция на угарный газ (моноксид углерода) CO. Помутнение раствора при пропускании угарного газа в раствор хлорида палладия (II): PdCl2 + CO + h3O = CO2↑ + 2HCl + Pd↓ 3.1.9. Качественная реакция на углекислый газ (диоксид углерода) CO2. Тушение тлеющей лучинки в атмосфере углекислого газа. Пропускание углекислого газа в раствор гашеной извести Ca(OH)2: Ca(OH)2 + CO2 = CaCO3↓ + h3O Дальнейшее пропускание приведет к растворению осадка: CaCO3 + CO2 + h3O = Ca(HCO3)23.2.1. Качественная реакция на оксид азота (II) NO. Оксид азота (II) очень чувствителен к кислороду воздуха, потому на воздухе буреет, окисляясь до оксида азота (IV) NO2: 2NO + O2 = 2NO2  перейти в каталог файлов
перейти в каталог файловuhimik.ru