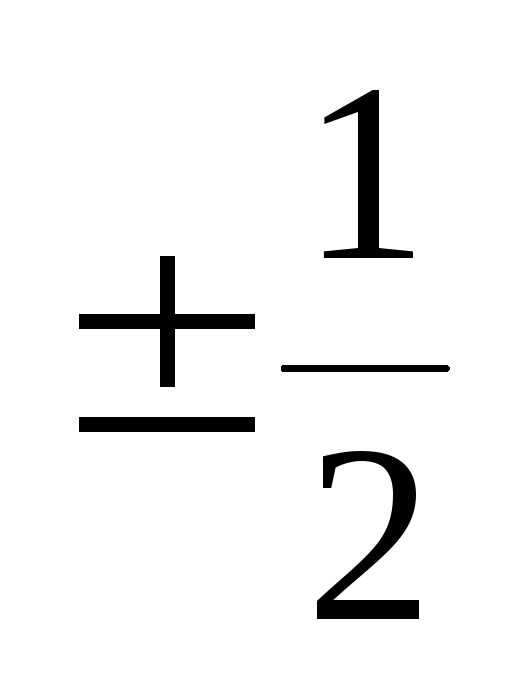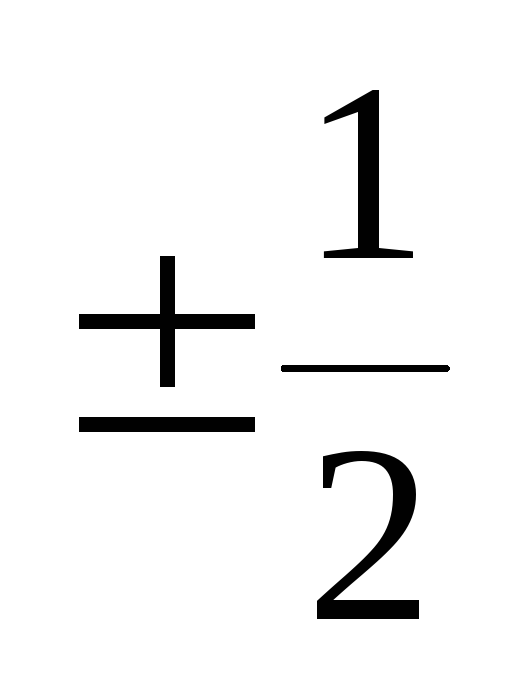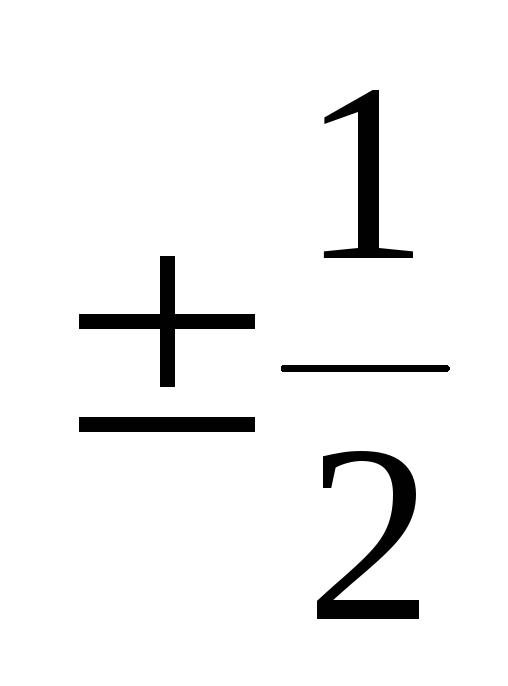Правила заполнения электронов по орбиталям Уровни. Хром по орбиталям
Распределение электронов по уровням, подуровням и орбиталям во многоэлектронном атоме
Распределение характеризуется следующими правилами:
принципом Паули;
правилом Гунда;
принципом наименьшей энергии и правилом Клечковского.
По принципу Паули в атоме не может быть двух и более электронов с одинаковым значением всех четырех квантовых чисел. Основываясь на принципе Паули можно установить максимальную емкость каждого энергетического уровня и подуровня.
| № уровня | Подуровень, ℓ | Обозначение подуровня | Магнитное квантовое число, m | Спиновое квантовое число,s |
| n=1 | 0 | 1s | 0 |
|
| n=2 | 0 1 | 2s 2p | 0 -1, 0, 1 |
|
| n=3 | 0 1 2 | 3s 3p 3d | 0 -1, 0, 1 -2,-1, 0, 1, 2 |
|
| n=4 | 0 1 2 3 | 4s 4p 4d 4f | 0 -1, 0, 1 -2,-1, 0, 1, 2 -3, -2, -1, 0, 1, 2, 3 |
|
Таким образом, максимальное количество электронов на:
s-подуровне – 2,
p- подуровне – 6,
d-подуровне – 10,
f-подуровне – 14.
В пределах квантового уровня n электрон может принимать значения 2n2 различных состояний, что было установлено опытным путем с помощью спектрального анализа.
Правило Гунда: в каждом подуровне электроны стремятся занять максимальное число свободных энергетических ячеек, чтобы суммарный спин имел наибольшее значение.
Например:
правильно неправильно неправильно
3р3:s = +1/2+1/2+1/2=1,5 s =-1/2+1/2+1/2=0,5 s = -1/2+1/2-1/2=-0,5
Принцип наименьшей энергии и правило Клечковского: электроны в первую очередь заселяют квантовые орбитали с минимальной энергией. Так как запас энергии в атоме определяется значением суммы главного и орбитального квантовых чисел (n + ℓ), то сначала электроны заселяют орбитали, для которых сумма (n + ℓ) наименьшая.
Например: сумма (n + ℓ) для 3d - подуровня равна n = 3, l = 2, следовательно, (n + ℓ) = 5; для 4s-подуровня: n = 4, ℓ = 0, следовательно, (n + ℓ) = 4. В этом случае в первую очередь заполняется 4s-подуровень и только потом 3d-подуровень.
Если суммарные значения энергии равны, то заселяется тот уровень, который находится ближе к ядру.
Например: для 3d: n = 3, ℓ = 2, (n + ℓ) = 5;
для 4p: n = 4, ℓ = 1, (n + ℓ) = 5.
Так как n = 3 < n = 4, 3d заселится электронами раньше, чем 4 p.
Таким образом, последовательность заполнения уровней и подуровней электронами в атомах:
1s2<2s2<2p6<3s2<3p6<4s2<3d10<4p6<5s2<4d10<5p6<6s2<5d10≈4f14<6p6<7s2…..
Электронные формулы
Электронная формула - это графическое изображение распределения электронов по уровням и подуровням в атоме. Существует два вида формул:
при написании используются только два квантовых числа: n и ℓ. Главное квантовое число указывается цифрой перед буквенным обозначением подуровня. Орбитальное квантовое число указывается буквой s, p, d или f. Количество электронов указывается цифрой как показатель степени.
+2He: 1s2; +10Ne: 1s2 2s2 2p6;
+3Li: 1s2 2s1; +14Si: 1s2 2s2 2p6 3s2 3p6.
То есть соблюдается последовательность
1s2<2s2<2p6<3s2<3p6<4s2<3d10<4p6<5s2<4d10<5p6<6s2<5d10≈4f14<6p6<7s2…..
графическая электронная формула - используются все 4 квантовых числа - это распределение электронов по квантовым ячейкам. Главное квантовое число изображается слева, орбитальное – внизу буквой, магнитное – количество клеток, спиновое – направление стрелок.
Н
m=0,00,0
-1,-1 0 +1
апример: 8O:…2s2 2p4
Графическая формула используется для записи только валентных электронов.
Рассмотрим составление электронных формул элементов по периодам.
I период содержит 2 элемента, у которых полностью заселен электронами I квантовый уровень и s-подуровень (максимальное количество электронов на подуровне - 2):
1H: n=1 1s1
2He: n=1 1s2
Элементы, у которых последним заполняется s-подуровень, относят к s-семейству и называют s-элементами.
У элементов II периода идет заполнение II квантового уровня, s- и p-подуровня (максимальное количество электронов на р-подуровне - 8).
3Li: 1s2 2s1; 4 Be: 1s2 2s2;
5B: 1s2 2s2 2p1; 10Ne: 1s2 2s2 2p6
Элементы, у которых последним заполняется р-подуровень, относят к р-семейству и называют р-элементами.
У элементов III периода начинается формирование III квантового уровня. У Na и Mg идет заселение электронами 3s-подуровня. У элементов от 13Al до 18Ar заселяется 3p-подуровень; 3d-подуровень остается незаполненным, так как обладает более высоким уровнем энергии, чем 4s-подуровень и не заполняется у элементов III периода.
3d-подуровень начинает заполняться у элементов IV периода, а 4d - у элементов V периода (в соответствии с последовательностью):
19K: 1s2 2s2 2p6 3s2 3p6 4s1;20Ca: 1s2 2s2 2p6 3s2 3p6 4s2;
21Sс: 1s2 2s2 2p6 3s2 3p6 4s2 3d1; 25Mn: 1s2 2s2 2p6 3s2 3p6 4s2 3d5;
33As: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3; 43Tc: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p65s2 4d5
Элементы, у которых последним заполняется d-подуровень, относят к d-семейству и называют d-элементами.
4f заполняется только после 57 элемента VI периода:
57La:1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 5s2 4d105p6 6s25d1;
58Сe: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 5s2 4d105p6 6s25d14f1;
Заселение электронами V квантового уровня идет аналогично IV периоду. Таким образом, соблюдается показанная ранее последовательность заселения электронами уровней и подуровней:
1s2
2s22p6
3s23p6
4s23d104p6
5s24d105p6
6s25d104f146p6
7s2…..
Вывод:
заселение электронами нового квантового уровня всегда начинается с s-подуровня. У элементов данного периода заселяются электронами только s и p подуровни внешнего квантового уровня;
заселение d-подуровня запаздывает на I период; 3d-подуровень заполняется у элементов IV периода, 4d – подуровень у элементов V периода и т.д.;
заселение электронами f подуровня запаздывает на 2 периода; 4f-подуровень заселяется у элементов VI периода, 5f – подуровень у элементов VII периода и т.д.
studfiles.net
Строение атома - материалы для подготовки к ЕГЭ по Химии
Автор статьи — профессиональный репетитор И. Давыдова (Юдина).Атом - в переводе с древнегреческого – неделимый - это наименьшая частица химического элемента, являющаяся носителем его свойств. Современные представления о строении атома требуют для понимания знаний основ квантовой механики, поэтому мы ограничимся упрощенной моделью.
Атом состоит из ядра (в составе которого протоны и нейтроны) и электронов. Несмотря на то, что ядро составляет большую часть массы атома, оно очень мало.
| Заряд z | Масса m | |
| Протон p+ | +1 | 1 |
| Нейтрон n0 | 0 | 1 |
| Электрон e- | -1 | 0 |
Количество протонов равно количеству электронов и равно номеру атома в периодической таблице. Число нейтронов равно разности атомной массы и номера элемента.

Бор – пятый элемент периодической таблицы, в его атоме 5 протонов и 5 электронов. Атомная масса ≈ 11, количество нейтронов равно 11 – 5 = 6.
Элементы, имеющие одинаковое количество протонов в ядре, но различающиеся числом нейтронов, называются изотопами.
Например, 35Cl и 37Cl – изотопы, различающиеся атомной массой и количеством нейтронов.
| Число протонов | Число нейтронов | Число электронов | |
| 35Cl | 17 | 18 | 17 |
| 37Cl | 17 | 17 |
Вокруг ядра по различным траекториям - орбиталям движутся электроны. Каждой орбитали соответствует определенный уровень энергии, чем ближе орбиталь к ядру, тем меньшей энергией должен обладать электрон, чтобы находиться на ней.

Порядок заполнения орбиталей:
Электроны располагаются на орбиталях в соответствии со следующими правилами:
- Принцип наименьшей энергии: в первую очередь электроны заполняют наиболее низкие по энергии уровни (ближайшие к ядру).
Энергия орбиталей на уровнях и подуровнях изменяется следующим образом: 1s < 2s < 2р < Зs < Зр < 4s < 3d < 4р < 5s <4d < 5р < 6s < 4f ≈ 5d < 6p < 7s < 5f ≈6d < 7p . (●)
| Тип орбитали | Число орбиталей на энергетическом уровне | Максимальное количество электронов на этих орбиталях |
| s | 1 | 2 |
| 3 | 6 | |
| d | 5 | 10 |
| f | 7 | 14 |
Перед оставшимися двумя принципами введем понятие спина электрона. Спин – характеристика самого электрона, представить его (это упрощенная модель, а ненастоящий физический смысл понятия спин!) можно как направление движения электрона вокруг своей оси: по или против часовой стрелки. Возможных значений всего два: +1/2 и -1/2.
- Принцип Паули: на каждой орбитали может быть не более двух электронов, причем их спины должны быть различными.
- Правило Хунда: суммарный спин системы должен быть максимально возможным.
Рассмотрим заполнение орбиталей электронами на нескольких примерах. У каждого следующего элемента таблицы Менделеева на один протон и один электрон больше, чем у предыдущего. У элементов n-го периода заполнены предыдущие n-1 электронные уровни.

В атоме магния в основном состоянии нет неспаренных электронов.
Если атому сообщили дополнительную энергию (например, нагрели), то электронная пара может распарится и один из электронов переходит на свободную орбиталь того же энергетического уровня. В возбужденном состоянии атом магния имеет два неспаренных электрона и может образовать две связи (валентность II).

- фосфор – пятнадцатый элемент, распределяем 15 электронов: Фосфор - элемент третьего периода, следовательно, первый и второй энергетические уровни полностью заполнены - 1s22s22p6.Фосфор находится в пятой группе, значит, на третьем уровне у него пять электронов - 3s23p3. Итого получаем1s22s22p63s23p3.

В атоме фосфора в основном состоянии 3 неспаренных электрона. В возбужденном состоянии атом фосфора имеет пять неспаренных электронов и может образовать пять связей (валентность V).

- цирконий – сороковой элемент, распределяем 40 электронов. Цирконий - элемент пятого периода, следовательно, первые четыре энергетических уровня полностью заполнены - 1s22s22p63s23p64s23d104p6.Заполнение пятого уровня начинается с 5s2. Цирконий – второй d – элемент в пятом периоде, значит, он содержит 2 электрона на 4d – подуровне. Итого получаем: 1s22s22p63s23p64s23d104p65s24d2.

В атоме циркония в основном состоянии 2 неспаренных электрона.В возбужденном состоянии цирконий имеет четыре неспаренных электрона.

Исключениями из общего порядка заполнения электронных подуровней являются хром, марганец, медь, серебро и золото – у них наблюдается «провал» электрона с внешного s – подуровня на предвнешний d. Например, электронные конфигурации хрома и меди вместо 4s23d4 и 4s23d9 имеют вид 4s13d5 и 4s13d10.


Задания для тренировки:
- Сколько протонов и электронов содержит ион NO2-1) 46p, 46e 2) 23p, 24e3) 23р, 23e 4) 46p, 47e
- Чем отличаются изотопы одного и того же химического элемента?1) Числом протонов 2) Числом электронов3) Зарядом ядра 4) Массовым числом
- Укажите атом, в котором больше всего электронов:1) 2Н 2) 40Аr 3) 41Ar 4) 39К
- Изобразить электронно-графическую схему атома хлора в основном и всех возможных возбужденных состояниях. Какие валентности способен проявлять хлор?
- Объяснить, почему сера проявляет валентность VI, а кислород – не проявляет, хотя оба эти элемента содержат по 6 электронов на внешнем слое.
Звоните нам: 8 (800) 775-06-82 (бесплатный звонок по России) +7 (495) 984-09-27 (бесплатный звонок по Москве)
Или нажмите на кнопку «Узнать больше», чтобы заполнить контактную форму. Мы обязательно Вам перезвоним.
ege-study.ru
Правила заполнения электронов по орбиталям Уровни
СТРОЕНИЕ АТОМАА том – электронейтральная частица, состоящая из (+) заряженного ядра и (-) заряженных электронов, находящихся вне ядра.
том – электронейтральная частица, состоящая из (+) заряженного ядра и (-) заряженных электронов, находящихся вне ядра.
Атом – мельчайшая, химически неделимая частица вещества.
В ядро входят протоны, которые вносят массу и (+) заряд и нейтроны,
которые вносят массу. Количество протонов (+р) = заряду ядра (Z) = порядковому номеру элемента в периодической системе. Количество нейтронов (0n) = массе атома – порядковый номер элемента. Вне ядра располагаются электроны, которые вносят (-) заряд. Количество электронов (e-)= количеству протонов (+р ), следовательно в атоме количество (+) зарядов = количеству (-), а значит атом электронейтрален, т.е. заряд атома равен 0.
РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОНОВ В АТОМЕ ПО ОРБИТАЛЯМ
Электроны располагаются вне ядра на различных уровнях, а на каждом уровне есть определенные орбитали.
Орбиталь – пространство вокруг ядра, где наиболее вероятно расположение электрона. Существуют орбитали 4-х типов: s – орбиталь вмещает 2e- и имеет форму шара (O).
p – орбиталь вмещает 6e- и имеет форму гантели (∞). d - орбиталь вмещает 10e-
и f – орбиталь вмещает 14e-.
Правила заполнения электронов по орбиталям
| Уровни | Подуровни | Число орбиталей | Число e- на подуровнях | Общее число e- на уровне |
| 1 | s | 1 | 2 | 2 |
| 2 | s p | 1 3 | 2 6 | 8 |
| 3 | s p d | 1 3 5 | 2 6 10 | 18 |
| 4,5,6,7 | s p d f | 1 3 5 7 | 2 6 10 14 | 32 |
1) Количество электронов (e-)= порядковому номеру элемента.
2) Количество электронных уровней = № периода.
3) На последнем уровне количество e- = № группы (Только в главных подгруппах).
4) В побочных подгруппах количество e- на последнем уровне = 2 (или 1)
5) Порядок заполнения орбиталей: 1s
6) На каждом подуровне заполняется сначала по одному электрону в ячейку, затем по второму.
П ример №1
ример №1
1) Заряд ядра(Z) = +16 т. к. порядковый номер элемента-16, следовательно количество +р = 16 и e- =16. А 0n = 32 – 16 = 16.
e- располагаются на 3-х уровнях, т. к. № периода-3. На 1-ом уровне количество e- = 2 (максимум), на 3-м (последнем) e- = 6, т. к. № группы-6, а на 2-ом уровне остается 8 e- (16 – 2 – 6=8).
2) Поскольку 3 электронных уровня, то рисуем пустые орбитали: 1s, 2s, 2p, 3s, 3p, 3d, которые заполняем согласно определенной последовательности. На 1-ом слое только 2e-, которые располагаются на 1s-орбитали. На 2-ом слое 8e-, которые располагаются на 2s и 2p орбиталях. На 3-м слое 6e-, поэтому 3s орбиталь заполнена, на 3p остается 4e-, а 3d свободна.
Распределение e- по орбиталям можно записать в строчку: 1s22s22p63s23p4 (последний уровень подчеркнут).
koledj.ru
Магнитные хрома - Справочник химика 21
Ход электронного пучка в электронном микроскопе изображен на рие. 11,8. В общем он сходен с ходом световых лучей в обычном микроскопе. Однако поскольку электроны легко рассеиваются и поглощаются, для фокусировки пучка электронов применяют электромагнитное катушки, создающие электростатические или магнитные поля. Для уменьшения рассеяния электронов внутри электронного микроскопа поддерживают высокий вакуум. Наконец, с той же целью для исследования применяют объекты очень малой толщины, нанесенные обычно на тончайшую нитроцеллюлозную, кварцевую, углеродную или другие пленки, прозрачные для пучка электронов. Если последнее условие не будет соблюдено, то под воздействием электронов может происходить нагревание и разрушение объекта. Очень часто вместо самих объектов в электронном микроскопе наблюдают их отпечатки на различных пленках. Такие пленки —отпечатки (реплики) для придания им большей контрастности обычно оттеняют с помощью напыления каким-нибудь молекулярно-раздробленным металлом (например, хромом). [c.49] Например, линия испускания изотопа Ге расщеплена на шесть компонент благодаря наличию у ядра железа собственного магнитного момента (см. гл. XI. 3). Однако диффузия распадающегося с переходом в Ге в матрицу из меди, платины, палладия, хрома или нержавеющей стали, позволяет получить источник мессбауэровского излучения, обладающий синглетной линией испускания с большим значением величины вероятности испускания -квантов. [c.190]Составьте диаграмму распределения электронов в атоме хрома и в ионе Сг +. К иону Сг + присоединяются шесть ионов СЫ , так что пары электронов заполняют полностью пустые 45- и 4р-орбитали и оставшиеся Зс -орбитали иона хрома. Укажите тип гибридизации валентных орбиталей иона хрома. Сколько неспаренных электронов имеет ион Сг(СЫ)в и каковы его магнитные свойства [c.58]
В связи с наличием в их структуре заполненных электронных орбиталей атомы и ионы парамагнетиков проявляют и диамагнитные свойства. Поскольку оба эффекта противоположны по знаку, суммарная магнитная восприимчивость вещества будет определяться наибольшим из них. Примерами веществ с ярко выраженными парамагнитными свойствами служат пары щелочных металлов, кислород и оксид азота N0 как в газообразном, так и в жидком состоянии, твердые литий, хром, палладий, а также ряд других металлов. [c.301]
Электронное состояние переходных металлов определяет ряд их физических свойств (температуры плавления и кипения, межатомные расстояния, прочность или твердость кристаллической решетки и т. п.). Для металлов 4-го периода прочность решетки возрастает от К, Са и Ti, V, достигает максимума у хрома, затем падает у Мп и вновь несколько растет в ряду Fe -)- o- Ni. При учете распределения с1- и 5-электронов в переходных металлах помимо указанных физических свойств большое значение придается магнитным свойствам. С современной точки зрения магнитные свойства металлов определяются -электронами с неспаренными спинами. Соответствующие магнитные моменты насыщения )J, для металлов 4-го периода имеют значения Сг 0,22 Мп 1,22 Ре 2,22 Со 1,71 N1 0,6(0,66). [c.147]
По магнитным свойствам различают диамагнитные металлы (выталкиваемые из магнитного поля) и парамагнитные (втягиваемые магнитным полем). Диамагнитны медь, серебро, золото, цинк, кадмий, ртуть, цирконий. Парамагнитными считают скандий, иттрий, лантан, титан, ванадий, ниобий, тантал, хром, молибден, вольфрам, марганец, рений, рутений, радий, палладий, осмий, иридий, платину. Железо, кобальт и никель обладают ферромагнетизмом, т. е. особенно высокой магнитной восприимчивостью. [c.257]
К числу ферромагнетиков относятся железо, никель, кобальт, редкоземельные металлы от гадолиния до тулия, их соединения, сплавы, а также сплавы хрома и марганца и др. Особенностью ферромагнитных веществ является большое значение [х, а также то, что они сохраняют намагничивание и после того, как намагничивающее поле прекратило свое действие магнитная проницаемость (X и коэффициент % для них не являются постоянными [c.288]
Хромсодержащие осадки перерабатывают с получением смешанных оксидов ферромагнитного диоксида хрома, основного сульфата хрома, фосфата хрома, хроматов, ферритов [80]. На основе ферритов и связующих добавок (например, эпоксидной смолы) получают материал, способный поглощать электромагнитные волны, защищать от магнитного воздействия. [c.120]
Стали с особыми свойствами. К этой группе относятся нержавеющие, жаростойкие, жаропрочные, магнитные и иекото[)ые другие стали. Нержавеющие стали устойчивт, против коррозии в атмосфере, влаге и в растворах кислот, жаростойкие — в коррозионно-активных средах при высоких температурах. Жаропрочные стали сохраняют высокие механические свойства при нагревании до значительных температур, что важно при изготовлении лопаток газовых турбин, деталей реактивных двигателей и ракетных установок. Важнейшие легирующие элементы жаропрочных стале это хром (15—20%), никель (8—15%), вольфрам. Жаропрочные ста.ли принадлежат к аустеннтиым сплавам. [c.686]
Главная масса никеля идет на производство различных сплавов с железом, медью, цинком и другими металлами. Присадка никеля к стали повышает ее вязкость и стойкость против коррозии. Сплавы на основе никеля можно разделить на жаропрочные, магнитные и сплавы с особыми свойствами. Жаропрочные сплавы никеля используются в современных турбинах и реактивных двигателях, где температура достигает 850—900 °С таких температур сплавы на основе железа не выдерживают. К важнейшим жаропрочным сплавам никеля относятся нимоник, инконель, хастеллой. В состав этнх сплавов входит свыше 60% никеля, 15—20% хрома и другие металлы. Производятся также металлоксрамические жаропрочные сплавы, содержащие никель в качестве связующего металла. Эти снлавы выдерживают нагревание до 1100 °С. Широко применяются для изготовления элементов электронагревательных устройств сплавы типа нихром а, простейший из которых содержит 80% никеля и 20% хрома. [c.694]
У диамагнетиков (водород, инертные газы и др.) ц оксид азота, соли редкоземельных металлов, соли железа, кобальта и никеля и др.) ц > 1. Ферромагнетики (Ре, N1, Со и их сплавы, сплавы хрома и марганца, Сс1) имеют магнитную проницаемость ц 1. Магнитная проницаемость ферромагнетиков нелинейно зависит от напряженности внешнего поля. Кривая намагничивания В (я) ферромагнетиков имеет вид характерной петли гистерезиса, по ширийе которой различают материалы магнитомягкие (электротехнические стали) и магнитожесткие (постоянные магниты). При определенных значениях напряженности поля индукция достигает насыщения. [c.38]
Использование кобальта в технике. Кобальт используется как легирующий металл в сталях, придавая им особые свойства (стали нержавеющие, инструментальные, с особыми магнитными свой-стками). Кобальт также является основой жаропрочных сплавов, леп ,юваниь х титаном, хромом, молибденом и другими металлами, Большое количество кобальта иснользуется в производстве сверхтвердых материалов на основе карбидов титана и вольфрама. [c.315]
Аустенитные стали получили свое название по аустенитной фазе или 7-фазе, которая существует в чистом железе в виде стабильной структуры в температурном интервале от 910 до 1400 °С. Эта фаза имеет гранецентрированную кубическую решетку, немагнитна и легко деформируется. Она является основной или единственной фазой аустенитных нержавеющих сталей при комнатной температуре и в зависимости от состава имеет стабильную или метастабильную структуру. Присутствие никеля в значительной степени способствует сохранению аустенитной фазы при закалке промышленных сплавов Сг—Ре—N1 от высоких температур. Увеличение содержания никеля сопровождается повышением стабильности аустенита. Легирование марганцем, кобальтом, углеродом и азотом также способствует сохранению при закалке и стабилизации аустенита. Аустенитные нержавеющие стали могут упрочняться холодной обработкой, но не термообработкой. При холодной обработке аустенит в метастабиль-ных сплавах (например, 201, 202, 301, 302, 302В, 303, ЗЗОЗе, 304, 304Ь, 316, 316Ь, 321, 347, 348 см. табл. 18.2) частично переходит в феррит. По этой причине указанные стали и являются метастабильными. Они магнитны и имеют объемно-центрирован-ную кубическую решетку. Этим превращением объясняется значительная степень упрочнения при механической обработке. В то же время стали 305, 308, 309, 3098 при холодной обработке слабо упрочняются, и если и становятся магнитными, то в очень малой степени. Сплавы с повышенным содержанием хрома и никеля (например, 310, 3108, 314) имеют практически стабильную аустенитную структуру и при холодной обработке не превращаются в феррит и Не становятся магнитными. Аустенитные нержавеющие стали очень широко применяют в различных областях, включая строительство и автомобильное производство, а также в качестве конструкционного материала в пищевой и химической промышленности. [c.297]
Основная часть никеля (85—87%) расходуется для- производства сплавов с железом, хромом, медью и другими металлами. Эти сплавы отличаются высокими механическими, антикоррозионными, магнитными и электрическими свойствами. Сплавы никеля с алюминием (а также с магнием и кремнием) используются в качестве исходного вещества для получения никеля Ренея — никелевого катализатора скелетного типа, образующегося при действии щелочи на эти сплавы. [c.286]
Магнитные стали используют для изготовления постоянных магнитов и сердечников магнитных устройств, работающих в переменных полях. Для постоянных магнитов применяют высокоуглеродистые стали, легированные хромом или вольфрамом. Они хорошо намагничиваются и длительное время сохраняют остаточную индукцию. Сердечники магнитных устройств изготовляют из низко-углеродистых (менее 0,005% С) сплавов железа с кремнием. Эти стали легко пе-ремагничиваются и характеризуются малым значением электрических потерь. [c.629]
Конструкционные стали могут быть и углеродистыми и легированными. Основные легирующие элементы конструкционных сталей Сг, N1, Мп. Эти стали хорошо поддаются обработке давлением, резанием они хорошо свариваются. Конструкционные стали применяются для изготовления деталей машин, конструкций и сооружений. Инструментальные стали тоже могут быть и углеродистыми и легированными. Основной легирующий элемент — хром. Эти стали характеризуются высокой твердостью, прочностью, износостойкостью. Их применяют для изготовления режущих и измерительных инструментов, штампов и т. п. К сталям с особыми свойствами относятся нержавеющие, жаростойкие, жаропрочные, магнитные и некоторые другие стали. Нержавеющие стали устойчивы против коррозии в агрессивных средах, жаростойкие — против коррозии при высоких температурах. В энергетике важны жаропрочные стали, сохраняющие высокие механические свойства при нагревании до значительных температур, что важно при изготовлении лопаток газовых турбин. В электротехнике важны магнитные стали, которые используются для постоянных магнитов и сердечников магнитных устройств, работающих в переменных полях. Постоянные магниты делают из высокоуглеродистых сталей, легированных хромом или вольфрамом. Они хорошо намагничиваются и долго сохраняют остаточную индукцию. Сердечники, наоборот, делают из низкоуглеродистых сталей, легированных кремнием. Они легко перемагничиаются и характеризуются малыми электрическими потерями. [c.296]
Задача 3.15. Вычислить расщепление /)-терма атома хрома в магнитном поле напряженностью 1000 Гс, [c.90]
Полинг предполагает, что образование связей в переходных металлах обусловлено электронами в с1-, з- и ]0-состояниях, а не только электронами в -состоянии. Одни лишь -орбитали недостаточны для образования связи, и только гибридизация между й-, 5- и р-ор-биталями может привести к очень стабильным гибридным орбиталям. С этой точки зрения в IV периоде для образования связи пригодны одна 45-, три 4р- и пять 3 /-орбиталей и при полном их использовании связь может осуществляться девятью орбиталями. Если бы для связи использовались все девять возможных орбита-лей, то при переходе от К к Си следовало бы ожидать непрерывного увеличения прочности связи. Однако максимум прочности решетки достигается у хрома, а далее прочность уменьшается по направлению к никелю. Это привело Полинга к предположению, что только некоторые -орбитали пригодны для образования металлической связи, С учеюм магнитных свойств принимается, что для образования металлической связи из пяти -орбиталей пригодны только 2,56. Остальные 2,44 -орбитали являются атомными орбиталями. Электроны на атомных -орбиталях связаны с ядром атома и не участвуют в образовании металлической связи. Электроны связывающих -орбиталей полностью отделены от атома и коллективизированы в системе электронов кристалла. В свою очередь, атомные -орбитали, содержащие электроны с неспаренными спинами, обусловливают магнитные свойства металлов. Таким образом, Полинг различает связывающие -электроны, которые участвуют в ковалентных связях между соседними атомами кристалла и обеспечивают силы сцепления в металле и атомные -электроны, ответственные за парамагнетизм. Связывающие электроны описываются гибридными 5р-функциями, атомные же — просто -функциями. [c.148]
Весьма ценными свойствами металлов являются их пластичность, упругость, прочность. Онн способны под давлением изменять свою форму, не разрушаясь. Это свойство металлов позволяет п.рокатывать их в листы или вытягивать в проволоку. Прочность и пластичность металлов зависят от температуры с повышением температуры прочность понижается, а пластичность возрастает. По степени твердости металлы значительно отличаются друг от друга. Так, калий, натрий — металлы мягкие (их можно резать ножом) хром по твердости близок к алмазу — царапает стекло. Температура плавления и плотность металлов также изменяются в ши- роких интервалах. Самый легкоплавкий металл — ртуть (температура плавления —38,87 °С) самый тугоплавкий— вольфрам (температура плавления 3370 °С). Плотность лития — 590 кг/м , а осмия — 22 480 кг/м Металлы отличаются также своим отношением к магнитным полям. По этому свойству они делятся на три группы ферромагнитные металлы — способные намагничиваться при действии слабых магнитных полей (например, железо, кобальт, никель и гадолиний) [c.389]
Основная часть никеля (85—87%) расходуется на производство сплавов с железом, хромом, медью и другими металлами. Эти сплавы отличаются высокими механическими, антикоррозионными, магнитными и электрическими свойствами. Сплавы никеля с алюминием (а также с магнием и кремнием) используют в качестве исходного вещества для получения никеля Ренея — никелевого катализатора скелетного типа, образующегося при действии щелочи на эти сплавы. Никель применяется в производстве щелочных аккумуляторов и в гальванотехнике. В 1980 г. производство никеля составило в капиталистических и слаборазвитых странах около 1 млн. т, в ближайшие 7—10 лет оно возрастет еще на 7% в год. [c.403]
Рабочее покрытие на магнитных лентах обычно представляет собой патентованную смесь многочисленных компонентов (до 20 и более), однако в данном случае этот материал можно считать, по-видимому, смесью магнитных окисных частиц и полимерного связующего. Такая смесь в затвердевшем виде доллсна быть химически инертной по отношению к морской воде. Частицы окислов (таких металлов, как железо, хром и т. д.) также не должны подвергаться дальнейшему окислению и разрушению. [c.478]
Наконец, мы сами можем частично управлять величинами Т , контролируя доступность подходящих путей релаксации. Простейшей причиной ускорения релаксации служит присутствие в образце парамагнитных веществ, которые с помощью своих неспаренных электронов эффективно инициируют ЯМР-переходы. Их можно специально добавлять в образец, если нужно сократить время релаксации для ускорения эксперимента или для повышения точности количественных измерений. Для этой цели обычно используется ацетилацетонат хрома(Ш). В то же время приготовленные в обычных условиях образцы неизбежно содержат примеси пара.магнитного вещества - растворенного кислорода, которые нужно удалить обезгаживанием, если мы хотим получить самые узкие из возможных лиш1и или собираемся проводить измерения ядерного эффекта Оверхаузера или других параметров релаксационных процессов. [c.133]
Возможность ироведепия сварки старого металла с новым оценивается ио изменению его состава. Для этого используется метод неразрушающего контроля, основанный на измерении магнитной ироницаемости металла труб с помощью магнетоскопа [367]. Используемые для изготовления труб радиантной камеры змеевика хромоникелевые трубы в нормальных условиях не магнитны. Однако при проникании в них заметного количества углерода происходит образование карбида, матрица сплава настолько обедняется хромом, что остается магнитный железоникелевый сплав. [c.176]
Основное применение карбонилы находят при приготовлении чистых металлов. Процесс Монда для рафинирования никеля и приготовления чистого железа для специальных целей, например магнитных сердечников, основан на образовании летучего карбонила, очищении паров от примесей, содержащихся в исходных металлах, и последующем разложении для получения чистого металла. Карбонилы хрома, молибдена и вольфрама были применены в масспектроскопии для определения устойчивых изотопов соответствующих металлов [9]. Карбонил никеля был использован для приготовления металлических зеркал и для покрытия различных предметов тонкими металлическими пленками. Карбонил железа находит применение в качестве антидетонатора в горючем для двигателей внутреннего сгорания. [c.226]
chem21.info